 Хром та його властивості
Хром та його властивості
 Відкриття Хрому n Мінерал, що містить хром, був відкритий біля Єкатеринбурга в 1766 р. І. Г. Леманном і названий «сибірським червоним свинцем» . Зараз цей мінерал називається Крокоітом. Відомий і його склад - Рb. Cr. О 4. А свого часу «сибірський червоний свинець» викликав чимало розбіжностей серед вчених. Тридцять років сперечалися про його склад, поки, нарешті, в 1797 р. французький хімік Луї Нікола Воклен не виділив з нього метал, який (теж, до речі, після деяких суперечок) назвали хромом. Воклен обробив крокоит поташем До 2 CO 3: хромат свинцю перетворився на хромат калію. Потім за допомогою соляної кислоти хромат калію був перетворений на окис хрому і воду (хромова кислота існує лише в розбавлених розчинах). Нагрівання зелений порошок окису хрому в графітовому тиглі з вугіллям, Воклен отримав новий тугоплавкий метал. Паризька академія наук за всією формою засвідчила відкриття. Але, швидше за все, Воклен виділив не елементарний хром, а його карбіди. Про цесвідчить голкоподібних форма отриманих Вокленом світлосірих кристалів. Назва «хром» запропонували друзі Воклена, але воно йому не сподобалося - метал не відрізнявся особливим кольором. Однак друзям вдалося вмовити хіміка, посилаючись на те, що з яскраво забарвлених сполук хрому можна отримувати гарні фарби. (До речі, саме в роботах Воклена вперше поясненасмарагдова забарвлення деяких природних силікатів берилію та алюмінію; їх, як з'ясував Воклен, фарбували домішки сполук хрому. ) Так і закріпилася за новим елементом цю назву.
Відкриття Хрому n Мінерал, що містить хром, був відкритий біля Єкатеринбурга в 1766 р. І. Г. Леманном і названий «сибірським червоним свинцем» . Зараз цей мінерал називається Крокоітом. Відомий і його склад - Рb. Cr. О 4. А свого часу «сибірський червоний свинець» викликав чимало розбіжностей серед вчених. Тридцять років сперечалися про його склад, поки, нарешті, в 1797 р. французький хімік Луї Нікола Воклен не виділив з нього метал, який (теж, до речі, після деяких суперечок) назвали хромом. Воклен обробив крокоит поташем До 2 CO 3: хромат свинцю перетворився на хромат калію. Потім за допомогою соляної кислоти хромат калію був перетворений на окис хрому і воду (хромова кислота існує лише в розбавлених розчинах). Нагрівання зелений порошок окису хрому в графітовому тиглі з вугіллям, Воклен отримав новий тугоплавкий метал. Паризька академія наук за всією формою засвідчила відкриття. Але, швидше за все, Воклен виділив не елементарний хром, а його карбіди. Про цесвідчить голкоподібних форма отриманих Вокленом світлосірих кристалів. Назва «хром» запропонували друзі Воклена, але воно йому не сподобалося - метал не відрізнявся особливим кольором. Однак друзям вдалося вмовити хіміка, посилаючись на те, що з яскраво забарвлених сполук хрому можна отримувати гарні фарби. (До речі, саме в роботах Воклена вперше поясненасмарагдова забарвлення деяких природних силікатів берилію та алюмінію; їх, як з'ясував Воклен, фарбували домішки сполук хрому. ) Так і закріпилася за новим елементом цю назву.
 Фізичні властивості Хрому n n n У вільному вигляді хром — сірий метал з кубічною об'ємноцентрованою ґраткою, а = 0, 28845 нм. Це єдина елементарна тверда сполука, яке виявляє антиферомагнітні властивості при кімнатній температурі (і нижче). При температурі вище 38 °C він перетворюється в парамагнетик. Хром має твердість за шкалою Мооса 5, найтвердіший із чистих металів. Дуже чистий хром достатньо добре піддається механічній обробці. Металічний хром на повітрі пасивує під дією кисню, утворюючи тонкий захисний шар поверхневого оксиду. Шар, що складається лише з кількох атомів завтовшки, є дуже щільним і, на відміну від заліза або нелегованої сталі, запобігає дифузії кисню в матеріал та виникненню іржі. Пасивація може бути підвищена шляхом короткочасного контакту з такою кислотою-окисником як азотна. Протилежний ефект досягається при обробці сильним відновником, який руйнує захисний оксидний шар на металі. Хром, оброблений таким способом, легко розчиняється в навіть в слабких кислотах.
Фізичні властивості Хрому n n n У вільному вигляді хром — сірий метал з кубічною об'ємноцентрованою ґраткою, а = 0, 28845 нм. Це єдина елементарна тверда сполука, яке виявляє антиферомагнітні властивості при кімнатній температурі (і нижче). При температурі вище 38 °C він перетворюється в парамагнетик. Хром має твердість за шкалою Мооса 5, найтвердіший із чистих металів. Дуже чистий хром достатньо добре піддається механічній обробці. Металічний хром на повітрі пасивує під дією кисню, утворюючи тонкий захисний шар поверхневого оксиду. Шар, що складається лише з кількох атомів завтовшки, є дуже щільним і, на відміну від заліза або нелегованої сталі, запобігає дифузії кисню в матеріал та виникненню іржі. Пасивація може бути підвищена шляхом короткочасного контакту з такою кислотою-окисником як азотна. Протилежний ефект досягається при обробці сильним відновником, який руйнує захисний оксидний шар на металі. Хром, оброблений таким способом, легко розчиняється в навіть в слабких кислотах.
 Хімічні властивості Хрому n Хром є елементом перехідних металів, перший елемент шостої групи. Хром (0) має електронну конфігурацію 4 s 13 d 5. Метал володіє широким спектром можливих процесів окиснення, де +3 є найбільш енергетично стабільним, тому сполуки Хрому +3 і +6 більш характерні, у той час як +1, +4 і +5 — рідкісні. n n
Хімічні властивості Хрому n Хром є елементом перехідних металів, перший елемент шостої групи. Хром (0) має електронну конфігурацію 4 s 13 d 5. Метал володіє широким спектром можливих процесів окиснення, де +3 є найбільш енергетично стабільним, тому сполуки Хрому +3 і +6 більш характерні, у той час як +1, +4 і +5 — рідкісні. n n
 Історія добування Хрому n Мінерал, що містить хром, був відкритий біля Єкатеринбурга в 1766 р. І. Г. Леманном і названий «сибірським червоним свинцем» . Зараз цей мінерал називається Крокоітом. Відомий і його склад - Рb. Cr. О 4. А свого часу «сибірський червоний свинець» викликав чимало розбіжностей серед вчених. Тридцять років сперечалися про його склад, поки, нарешті, в 1797 р. французький хімік Луї Нікола Воклен не виділив з нього метал, який (теж, до речі, після деяких суперечок) назвали хромом. Воклен обробив крокоит поташем До 2 CO 3: хромат свинцю перетворився на хромат калію. Потім за допомогою соляної кислоти хромат калію був перетворений на окис хрому і воду (хромова кислота існує лише в розбавлених розчинах). Нагрівання зелений порошок окису хрому в графітовому тиглі з вугіллям, Воклен отримав новий тугоплавкий метал. Паризька академія наук за всією формою засвідчила відкриття. Але, швидше за все, Воклен виділив не елементарний хром, а його карбіди. Про цесвідчить голкоподібних форма отриманих Вокленом світлосірих кристалів. Назва «хром» запропонували друзі Воклена, але воно йому не сподобалося - метал не відрізнявся особливим кольором. Однак друзям вдалося вмовити хіміка, посилаючись на те, що з яскраво забарвлених сполук хрому можна отримувати гарні фарби. (До речі, саме в роботах Воклена вперше поясненасмарагдова забарвлення деяких природних силікатів берилію та алюмінію; їх, як з'ясував Воклен, фарбували домішки сполук хрому. ) Так і закріпилася за новим елементом цю назву. Між іншим, склад «хром» , саме в сенсі «пофарбований» , входить в багато наукові, технічні і навіть музичні терміни. Широко відомі фотоплівки «ізопанхром» , «панхром» і «ортохром» . Слово «хромосома» в перекладі з грецького означає «тіло, яке фарбується» . Є «хроматична» гамма (в музиці) і є гармоніка «хромка» .
Історія добування Хрому n Мінерал, що містить хром, був відкритий біля Єкатеринбурга в 1766 р. І. Г. Леманном і названий «сибірським червоним свинцем» . Зараз цей мінерал називається Крокоітом. Відомий і його склад - Рb. Cr. О 4. А свого часу «сибірський червоний свинець» викликав чимало розбіжностей серед вчених. Тридцять років сперечалися про його склад, поки, нарешті, в 1797 р. французький хімік Луї Нікола Воклен не виділив з нього метал, який (теж, до речі, після деяких суперечок) назвали хромом. Воклен обробив крокоит поташем До 2 CO 3: хромат свинцю перетворився на хромат калію. Потім за допомогою соляної кислоти хромат калію був перетворений на окис хрому і воду (хромова кислота існує лише в розбавлених розчинах). Нагрівання зелений порошок окису хрому в графітовому тиглі з вугіллям, Воклен отримав новий тугоплавкий метал. Паризька академія наук за всією формою засвідчила відкриття. Але, швидше за все, Воклен виділив не елементарний хром, а його карбіди. Про цесвідчить голкоподібних форма отриманих Вокленом світлосірих кристалів. Назва «хром» запропонували друзі Воклена, але воно йому не сподобалося - метал не відрізнявся особливим кольором. Однак друзям вдалося вмовити хіміка, посилаючись на те, що з яскраво забарвлених сполук хрому можна отримувати гарні фарби. (До речі, саме в роботах Воклена вперше поясненасмарагдова забарвлення деяких природних силікатів берилію та алюмінію; їх, як з'ясував Воклен, фарбували домішки сполук хрому. ) Так і закріпилася за новим елементом цю назву. Між іншим, склад «хром» , саме в сенсі «пофарбований» , входить в багато наукові, технічні і навіть музичні терміни. Широко відомі фотоплівки «ізопанхром» , «панхром» і «ортохром» . Слово «хромосома» в перекладі з грецького означає «тіло, яке фарбується» . Є «хроматична» гамма (в музиці) і є гармоніка «хромка» .
 Добування Хрому n Хроміт застосовується переважно в трьох галузях промисловості: металургії, хімії та виробництві вогнетривів, причому металургія споживає приблизно дві третини всього хроміту. Сталь, легована хромом, володіє підвищеною міцністю, стійкістю проти корозії в агресивних і окисних середовищах. Отримання чистого хрому - дорогий і трудомісткий процес. Тому для легування сталі застосовують головним чином ферохром, який отримують в дугових електропечах безпосередньо з хроміту. Відновлювачем служить кокс. Зміст окису хрому в хромі повинно бути не нижче 48%, а отношеніе. Cr: Fe не менш 3: 1. Отриманий в електропечі феррохром звичайно містить до 80% хрому і 4. . . 7% вуглецю (інше - залізо). Але для легування багатьох якісних сталей потрібен ферохром, містить мало вуглецю (про причини цього - нижче, у розділі «Хром в сплавах» ). Тому частина високовуглецевого ферохрому піддають спеціальній обробці, щоб знизити вміст вуглецю в ньому до десятих і сотих часток відсотка. З хроміту отримують і елементарний, металевий хром. Виробництвотехнічно чистого хрому (97. . . 99%) засновано на методі алюмінотермії, відкритому ще в 1865 р. відомим російським хіміком М. М. Бекетовим. Суть методу - у відновленні оксидів алюмінієм, реакція супроводжується значним виділенням тепла. Але попередньо треба отримати чистий окис хрому Сr 2 О 3. Для цього тонко подрібнений хроміт змішують з содою і додають до цієї суміші вапняк або окис заліза. Вся маса обпалюється, причому утворюється хромат натрію: 2 Сr 2 О 3 + 4 Na 2 CO 3 + 3 О 2 → 4 Na 2 Cr. O 4 + 4 CO 2. Потім хромат натрію витравлюють з обпаленої маси водою; луг фільтрують, упарюють і обробляють кислотою. У результаті виходить біхромат натрію Na 2 Cr 2 O 7. Відновлюючи його сірим або вуглецем при нагріванні, одержують зелену окис хрому. Металевий хром можна отримати, якщо чистий окис хрому змішати з порошком алюмінію, нагріти цю суміш у тиглі до 500. . . 600 ° C і підпалити з допомогою перекису барію, Алюміній забирає в окису хрому кисень. Ця реакція Сr 2 О 3 + 2 Аl → Аl 2 O 3 + 2 Сr - основа промислового (алюмінотермічним) способу одержання хрому, хоча, звичайно, заводська технологія значно складніше. Хром, отриманий алюмінотермічним, містить алюмінію і заліза десяті частки відсотка, а кремнію, вуглецю і сірки - соті частки відсотка. Використовують також силікотермічним спосіб отримання технічно чистого хрому. У цьому випадку хром з окису відновлюється кремнієм з реакції 2 Сr 2 О 3 + 3 Si → 3 Si. O 2 + 4 СR. Ця реакція відбувається в дугових печах. Для зв'язування кремнезему в шихту додають вапняк. Чистота силікотермічним хрому приблизно така ж, як і алюмінотермічним, хоча, зрозуміло, вміст у ньому кремнію трохи вище, а алюмінію трохи нижче. Для одержання хрому намагалися застосувати й інші відновники вуглець, водень, магній. Однак ці способи не отримали широкого розповсюдження. Хром високого ступеня чистоти (приблизно 99, 8%) отримують електролітично. Технічно чистий і електролітичний хром іде головним чином навиробництво складних хромових сплавів.
Добування Хрому n Хроміт застосовується переважно в трьох галузях промисловості: металургії, хімії та виробництві вогнетривів, причому металургія споживає приблизно дві третини всього хроміту. Сталь, легована хромом, володіє підвищеною міцністю, стійкістю проти корозії в агресивних і окисних середовищах. Отримання чистого хрому - дорогий і трудомісткий процес. Тому для легування сталі застосовують головним чином ферохром, який отримують в дугових електропечах безпосередньо з хроміту. Відновлювачем служить кокс. Зміст окису хрому в хромі повинно бути не нижче 48%, а отношеніе. Cr: Fe не менш 3: 1. Отриманий в електропечі феррохром звичайно містить до 80% хрому і 4. . . 7% вуглецю (інше - залізо). Але для легування багатьох якісних сталей потрібен ферохром, містить мало вуглецю (про причини цього - нижче, у розділі «Хром в сплавах» ). Тому частина високовуглецевого ферохрому піддають спеціальній обробці, щоб знизити вміст вуглецю в ньому до десятих і сотих часток відсотка. З хроміту отримують і елементарний, металевий хром. Виробництвотехнічно чистого хрому (97. . . 99%) засновано на методі алюмінотермії, відкритому ще в 1865 р. відомим російським хіміком М. М. Бекетовим. Суть методу - у відновленні оксидів алюмінієм, реакція супроводжується значним виділенням тепла. Але попередньо треба отримати чистий окис хрому Сr 2 О 3. Для цього тонко подрібнений хроміт змішують з содою і додають до цієї суміші вапняк або окис заліза. Вся маса обпалюється, причому утворюється хромат натрію: 2 Сr 2 О 3 + 4 Na 2 CO 3 + 3 О 2 → 4 Na 2 Cr. O 4 + 4 CO 2. Потім хромат натрію витравлюють з обпаленої маси водою; луг фільтрують, упарюють і обробляють кислотою. У результаті виходить біхромат натрію Na 2 Cr 2 O 7. Відновлюючи його сірим або вуглецем при нагріванні, одержують зелену окис хрому. Металевий хром можна отримати, якщо чистий окис хрому змішати з порошком алюмінію, нагріти цю суміш у тиглі до 500. . . 600 ° C і підпалити з допомогою перекису барію, Алюміній забирає в окису хрому кисень. Ця реакція Сr 2 О 3 + 2 Аl → Аl 2 O 3 + 2 Сr - основа промислового (алюмінотермічним) способу одержання хрому, хоча, звичайно, заводська технологія значно складніше. Хром, отриманий алюмінотермічним, містить алюмінію і заліза десяті частки відсотка, а кремнію, вуглецю і сірки - соті частки відсотка. Використовують також силікотермічним спосіб отримання технічно чистого хрому. У цьому випадку хром з окису відновлюється кремнієм з реакції 2 Сr 2 О 3 + 3 Si → 3 Si. O 2 + 4 СR. Ця реакція відбувається в дугових печах. Для зв'язування кремнезему в шихту додають вапняк. Чистота силікотермічним хрому приблизно така ж, як і алюмінотермічним, хоча, зрозуміло, вміст у ньому кремнію трохи вище, а алюмінію трохи нижче. Для одержання хрому намагалися застосувати й інші відновники вуглець, водень, магній. Однак ці способи не отримали широкого розповсюдження. Хром високого ступеня чистоти (приблизно 99, 8%) отримують електролітично. Технічно чистий і електролітичний хром іде головним чином навиробництво складних хромових сплавів.
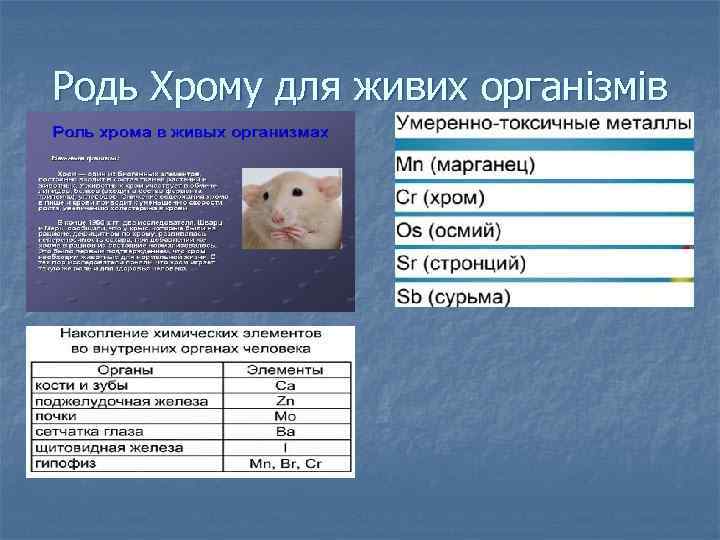 Родь Хрому для живих організмів
Родь Хрому для живих організмів
 Застосування Хрому
Застосування Хрому
 Дякую за Увагу!! Підготувала студентка 1 курсу ППФ-Факультету Дунайчик Аліна
Дякую за Увагу!! Підготувала студентка 1 курсу ППФ-Факультету Дунайчик Аліна


