 ХРОМ
ХРОМ
 Строение атома Атомные свойства: Атомный вес(молярная масса): 51, 9961(г/моль) Электронная конфигурация: 4 s 1 3 d 5 Радиус атома: 130 пм Степени окисления: 0, 2, 3, 6 Термодинамические свойства: Плотность: 7, 19 г/см 3 Температура плавления: 2130 К Температура кипения: 2945 К Уд. теплота плавления: 21 к. Дж/моль Уд. теплота испарения: 342 к. Дж/моль Состояние вещества: твердое
Строение атома Атомные свойства: Атомный вес(молярная масса): 51, 9961(г/моль) Электронная конфигурация: 4 s 1 3 d 5 Радиус атома: 130 пм Степени окисления: 0, 2, 3, 6 Термодинамические свойства: Плотность: 7, 19 г/см 3 Температура плавления: 2130 К Температура кипения: 2945 К Уд. теплота плавления: 21 к. Дж/моль Уд. теплота испарения: 342 к. Дж/моль Состояние вещества: твердое
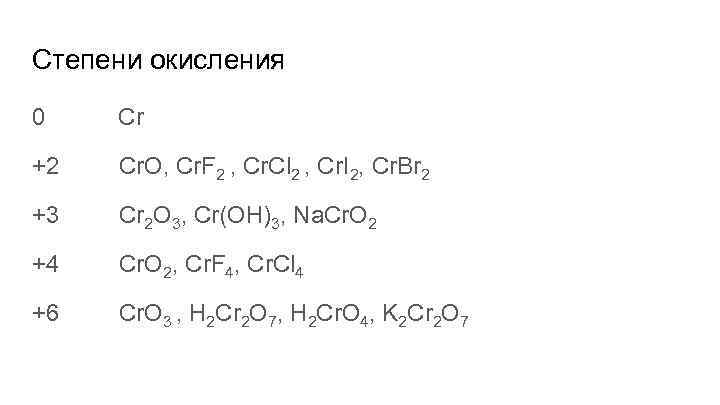 Степени окисления 0 Сr +2 Cr. O, Cr. F 2 , Cr. Cl 2 , Cr. I 2, Cr. Br 2 +3 Cr 2 O 3, Cr(OH)3, Na. Cr. O 2 +4 Cr. O 2, Cr. F 4, Cr. Cl 4 +6 Cr. O 3 , H 2 Cr 2 O 7, H 2 Cr. O 4, K 2 Cr 2 O 7
Степени окисления 0 Сr +2 Cr. O, Cr. F 2 , Cr. Cl 2 , Cr. I 2, Cr. Br 2 +3 Cr 2 O 3, Cr(OH)3, Na. Cr. O 2 +4 Cr. O 2, Cr. F 4, Cr. Cl 4 +6 Cr. O 3 , H 2 Cr 2 O 7, H 2 Cr. O 4, K 2 Cr 2 O 7
 Нахождение в природе Хромистый железняк(хромит) Fe. O*Cr 2 O 3 Магнезиохромит Mg. Cr 2 O 4 Свинцовая красная руда(крокоит) Pb. Cr. O 4
Нахождение в природе Хромистый железняк(хромит) Fe. O*Cr 2 O 3 Магнезиохромит Mg. Cr 2 O 4 Свинцовая красная руда(крокоит) Pb. Cr. O 4
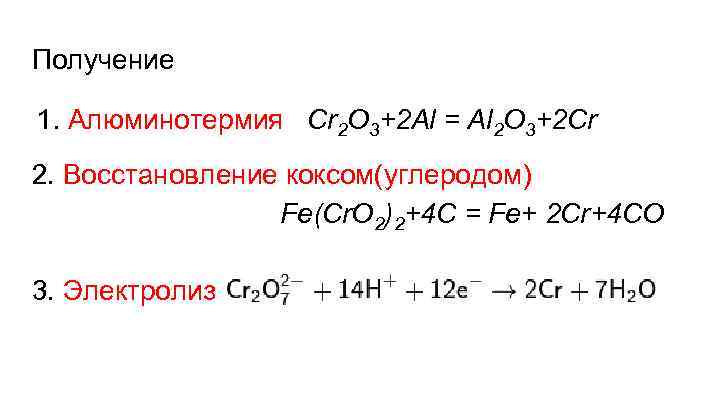 Получение 1. Алюминотермия Сr 2 O 3+2 Al = Al 2 O 3+2 Cr 2. Восстановление коксом(углеродом) Fe(Cr. O 2)2+4 C = Fe+ 2 Cr+4 CO 3. Электролиз
Получение 1. Алюминотермия Сr 2 O 3+2 Al = Al 2 O 3+2 Cr 2. Восстановление коксом(углеродом) Fe(Cr. O 2)2+4 C = Fe+ 2 Cr+4 CO 3. Электролиз
 Физические свойства В свободном виде — голубовато-белый металл. Один из самых твердых чистых металлов. Устойчив на воздухе. Обладает высокими температурами плавления и кипения. Коэффициент отражаемости 62%.
Физические свойства В свободном виде — голубовато-белый металл. Один из самых твердых чистых металлов. Устойчив на воздухе. Обладает высокими температурами плавления и кипения. Коэффициент отражаемости 62%.
 Химические свойства. Взаимодействие с неметаллами и водой. 4 Cr + 3 O 2 = 2 Cr 2 O 3 2 Cr + 3 Cl 2 = 2 Cr. Cl 3. 2 Cr + N 2 = 2 Cr. N 2 Cr + 3 S = Cr 2 S 3. Cr + 2 B = Cr. B 2 Cr + 2 Si = Cr. Si 2 2 Cr + 3 H 2 O = Cr 2 O 3 + 3 H 2
Химические свойства. Взаимодействие с неметаллами и водой. 4 Cr + 3 O 2 = 2 Cr 2 O 3 2 Cr + 3 Cl 2 = 2 Cr. Cl 3. 2 Cr + N 2 = 2 Cr. N 2 Cr + 3 S = Cr 2 S 3. Cr + 2 B = Cr. B 2 Cr + 2 Si = Cr. Si 2 2 Cr + 3 H 2 O = Cr 2 O 3 + 3 H 2
 Взаимодействие с кислотами Cr + 2 HCl = Cr. Cl 2 + H 2 Cr + H 2 SO 4 = Cr. SO 4 + H 2 4 Cr + 12 HCl + 3 O 2 = 4 Cr. Cl 3 + 6 H 2 O. 2 Cr + 6 H 2 SO 4(конц)= Cr 2(SO 4)3 + 3 SO 2 + 6 H 2 O Cr + 6 HNO 3(конц)= Cr(NO 3)3 + 3 NO 2 + 3 H 2 O.
Взаимодействие с кислотами Cr + 2 HCl = Cr. Cl 2 + H 2 Cr + H 2 SO 4 = Cr. SO 4 + H 2 4 Cr + 12 HCl + 3 O 2 = 4 Cr. Cl 3 + 6 H 2 O. 2 Cr + 6 H 2 SO 4(конц)= Cr 2(SO 4)3 + 3 SO 2 + 6 H 2 O Cr + 6 HNO 3(конц)= Cr(NO 3)3 + 3 NO 2 + 3 H 2 O.
 Взаимодействие с щелочью. Восстановление металлов из солей. 2 Cr + 6 KOH = 2 KCr. O 2 + 2 K 2 O + 3 H 2. Cr + KCl. O 3 + 2 KOH = K 2 Cr. O 4 + KCl + H 2 O. 2 Cr + 3 Cu. Cl 2 = 2 Cr. Cl 3 + 3 Cu.
Взаимодействие с щелочью. Восстановление металлов из солей. 2 Cr + 6 KOH = 2 KCr. O 2 + 2 K 2 O + 3 H 2. Cr + KCl. O 3 + 2 KOH = K 2 Cr. O 4 + KCl + H 2 O. 2 Cr + 3 Cu. Cl 2 = 2 Cr. Cl 3 + 3 Cu.
 Соединения Оксид хрома(II) Cr(OH)2+2 HCl = Сr. Cl 2+ 2 H 2 O 2 Сr. Cl 2+2 HCl = 2 Cr. Cl 3 +H 2 4 Cr(OH)2+O 2+2 H 2 O=4 Сr(OH)3 Оксид хрома(III) (NH 4)2 Cr 2 O 7 = N 2+Cr 2 O 3 Cr(OH)3+3 Na. OH = Na 3[Cr(OH)6] Cr 2 O 3+2 Na. OH = 2 Na. Cr. O 2+H 2 O 4 K 2 Cr 2 O 7 = 2 Cr 2 O 3+4 K 2 Cr. O 4+3 O 2
Соединения Оксид хрома(II) Cr(OH)2+2 HCl = Сr. Cl 2+ 2 H 2 O 2 Сr. Cl 2+2 HCl = 2 Cr. Cl 3 +H 2 4 Cr(OH)2+O 2+2 H 2 O=4 Сr(OH)3 Оксид хрома(III) (NH 4)2 Cr 2 O 7 = N 2+Cr 2 O 3 Cr(OH)3+3 Na. OH = Na 3[Cr(OH)6] Cr 2 O 3+2 Na. OH = 2 Na. Cr. O 2+H 2 O 4 K 2 Cr 2 O 7 = 2 Cr 2 O 3+4 K 2 Cr. O 4+3 O 2
 Соединения Гидроксид хрома(III) 2 Cr(OH)3+3 H 2 SO 4 = Cr 2(SO 4)3+ 6 H 2 O Cr(OH) 3+KOH = K[Cr(OH)4] 2 Cr(OH) 3+4 Na. OH(конц)+3 H 2 O 2(конц) = 2 Na 2 Cr. O 4+8 H 2 O Оксид хрома(VI) K 2 Cr 2 O 7+H 2 SO 4 = 2 Cr. O 3+K 2 SO 4+H 2 O K 2 Cr. O 4+H 2 SO 4 = Cr. O 3+K 2 SO 4+H 2 O Cr. O 3+2 KOH = K 2 Cr 2 O 4+H 2 O
Соединения Гидроксид хрома(III) 2 Cr(OH)3+3 H 2 SO 4 = Cr 2(SO 4)3+ 6 H 2 O Cr(OH) 3+KOH = K[Cr(OH)4] 2 Cr(OH) 3+4 Na. OH(конц)+3 H 2 O 2(конц) = 2 Na 2 Cr. O 4+8 H 2 O Оксид хрома(VI) K 2 Cr 2 O 7+H 2 SO 4 = 2 Cr. O 3+K 2 SO 4+H 2 O K 2 Cr. O 4+H 2 SO 4 = Cr. O 3+K 2 SO 4+H 2 O Cr. O 3+2 KOH = K 2 Cr 2 O 4+H 2 O
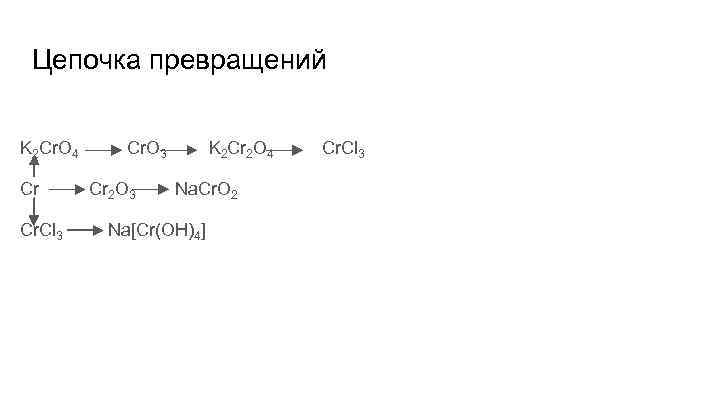 Цепочка превращений K 2 Cr. O 4 Cr Cr. Cl 3 Cr. O 3 Cr 2 O 3 K 2 Cr 2 O 4 Na. Cr. O 2 Na[Cr(OH)4] Cr. Cl 3
Цепочка превращений K 2 Cr. O 4 Cr Cr. Cl 3 Cr. O 3 Cr 2 O 3 K 2 Cr 2 O 4 Na. Cr. O 2 Na[Cr(OH)4] Cr. Cl 3