Презентация ХОБЛ Жук А.Н. (2).pptx
- Количество слайдов: 76

ХОБЛ

• Хрони ческая обструкти вная боле знь лёгких (ХОБЛ) — самостоятельное заболевание, для которого характерно частично необратимое ограничение воздушного потока в дыхательных путях. Ограничение воздушного потока, как правило, имеет неуклонно прогрессирующий характер и спровоцировано аномальной воспалительной реакцией ткани лёгких на раздражение различными патогенными частицами и газами.

Эпидемиология • В связи с подобной терминологической неопределённостью точные эпидемиологические данные назвать крайне трудно. В разных стандартах диагностики и ведения больных ХОБЛ (Канада; США; Европейское респираторное общество[; Россия; Великобритания) подчёркивается, что надёжные и точные эпидемиологические данные по ХОБЛ отсутствуют. • В США в 2010 году зарегистрировано 14 млн больных ХОБЛ, при этом хронический обструктивный бронхит фигурировал в диагнозе только у 12, 5 млн из них. С 1995 число больных возросло на 41, 5 %, и теперь в США страдают ХОБЛ около 6 % мужчин и 3 % женщин, а среди лиц старше 55 лет — 10 % больных. • Члены Европейского респираторного общества подчеркивают, что примерно 25 % случаев ХОБЛ диагностируется своевременно. Смертность в Европе колеблется от 2, 3 (Греция) до 41, 4 (Венгрия) на 100 000 населения.

• В России по результатам подсчетов с использованием эпидемиологических маркеров предположительно около 11 млн больных, а по официальной медицинской статистике — около 1 млн. Это разночтение связано с тем, что заболевание диагностируется в поздних стадиях, когда лечение не позволяет затормозить неуклонно прогрессирующий патологический процесс. Этим объясняется высокая смертность больных ХОБЛ. • По данным Европейского респираторного общества только 25 % случаев заболевания диагностируется своевременно. В последние годы отмечается мировая тенденция к увеличению заболеваемости: с1997 года по 2010 год её значение увеличилось на 25 % у мужчин и 69 % у женщин. Прогнозируется рост заболеваемости ХОБЛ в России

• Европейское респираторное общество приводит следующую классификацию факторов риска в зависимости от их значимости[8]: • Факторы риска ХОБЛ • Курение Профессиональные вредности (кадмий, кремний) • Дефицит α 1 -антитрипсина • Загрязнение окружающего воздуха (SO 2, NO 2, O 3) • Низкое социально-экономическое положение Пассивное курение в детском возрасте • Недоношенность • Высокий уровень Ig. E • Бронхиальная гиперреактивность • Семейный характер заболевания • Возможная. Аденовирусная инфекция Дефицит витамина C • Генетическая предрасположенность (группа крови A(II),

Главный фактор риска (80 -90 % случаев) — курение. Показатели смертности от ХОБЛ среди курильщиков максимальны, у них быстрее развивается обструкция дыхательных путей и одышка. Однако случаи возникновения и прогрессирования ХОБЛ отмечаются и у некурящих лиц. Одышка появляется приблизительно к 40 годам у курильщиков, и на 13 -15 лет позже у некурящих

Профессиональные факторы Выплавка чугуна Самые вредные профессиональные факторы — пыли, содержащие кадмий и кремний. На первом месте по развитию ХОБЛ стоит горнодобывающая промышленность. Профессии повышенного риска: шахтеры, строители, контактирующие с цементом, рабочие металлургической (за счет испарений расплавленных металлов) и целлюлознобумажнойпромышленности, железнодорожники, рабочие, занятые переработкой зерна, хлопка. В России, среди угольщиков имеется большое число лиц с заболеваниями легких пылевой этиологии, в том числе и с пылевым бронхитом. Курение усиливает неблагоприятное действие пыли
Наследственная предрасположенность В пользу роли наследственности указывает факт, что далеко не все курильщики с большим стажем становятся больными ХОБЛ. Наиболее изученным генетическим фактором риска является редкая наследственная недостаточность α 1 антитрипсина (A 1 AT), который ингибирует сериновые протеиназы в системном кровотоке. ВСША среди больных ХНЗЛ врождённый дефицит A 1 AT выявлялся менее, чем в 1 % случаев
В патогенезе ХОБЛ наибольшую роль играют следующие процессы: воспалительный процесс, дисбаланс протеиназ и антипротеиназ в л егких, окислительный стресс. Хроническое воспаление затрагивает все отделы дыхательных путей, паренхиму и сосуды легких. Со временем воспалительный процесс разрушает лёгкие и ведет к необратимым патологическим изменениям. Дисбаланс ферментов и окислительный стресс могут быть следствием воспаления, действия окружающей среды или генетических факторов

При ХОБЛ происходит увеличение количества нейтрофилов, макрофагов и Т-лимфоцитов, преимущественно CD 8+. Нейтрофилы. В мокроте, бронхоальвеолярном лаваже обнаруживается повышенное количество активированных нейтрофилов. Их роль при ХОБЛ ещё не ясна. У курильщиков без ХОБЛ также обнаруживается нейтрофилия мокроты. При исследовании индуцированной мокроты определяется повышенная концентрациямиелопероксидазы и человеческого нейтрофильного липокаина, что свидетельствует об активации нейтрофилов. При обострении также растет число нейтрофилов в бронхоальвеолярном лаваже. Нейтрофилы секретируют протеиназы: нейтрофильную эластазу, нейтрофильный катепсин G и нейтрофильную протеиназу-3.
Макрофаги обнаруживаются в крупных и мелких бронхах, паренхиме легких, а также в местах деструкции альвеолярной стенки при развитии эмфиземы, что выявляется при гистологическом исследовании мокроты и лаважа, биопсии бронха и исследовании индуцированной мокроты. Макрофаги выделяют фактор некроза опухоли α (ФНО-α), интерлейкин 8 (ИЛ 8), лейкотриен-B 4[ru] (ЛТВ 4), что способствует хемотаксису нейтрофилов. T-лимфоциты. Клетки CD 8+, обнаруживаемые при биопсии бронхов, выделяют перфорин[ru], гранзим-B[ru] и ФНО-α, эти агенты вызывают цитолиз и апоптозальвеолярн ых эпителиоцитов .
![• Эозинофилы. • Уровни эозинофильного катионного пептида и эозинофильной пероксидазы[ru] у больных ХОБЛ • Эозинофилы. • Уровни эозинофильного катионного пептида и эозинофильной пероксидазы[ru] у больных ХОБЛ](https://present5.com/presentation/1/214162835_299609411.pdf-img/214162835_299609411.pdf-12.jpg)
• Эозинофилы. • Уровни эозинофильного катионного пептида и эозинофильной пероксидазы[ru] у больных ХОБЛ в индуцированной мокроте повышены. Это указывает на возможность их присутствия. Это может быть не связано с эозинофилией — увеличение активности нейтрофильной эластазы, может обусловливать дегрануляцию эозинофилов при их нормальном количестве.

Эпителиальные клетки. Воздействие воздушных поллютантов, таких как диоксид азота (NO 2), озон (O 3), дизельные выхлопные газы[ru] на назальные и бронхиальные эпителиоциты, приводит к синтезу и высвобождению воспалительных медиаторов (эйкозаноиды, цитокины, молекулы адгезии и др). Происходит нарушение регуляции эпителиоцитами функционирования молекул адгезии E-селектина, отвечающие за вовлечение в процесс нейтрофилов. При этом секреция культурой клеток бронхиального эпителия, полученная от больных ХОБЛ в эксперименте, вырабатывает более низкие количества воспалительных медиаторов, (ФНО -α или ИЛ-8), чем аналогичные культуры от некурящих или курящих, но без ХОБЛ

• Медиаторы воспаления • Наибольшую роль при ХОБЛ играют фактор некроза опухоли α (ФНО-α), интерлейкин 8 (ИЛ-8), лейкотриен-B 4 (ЛТВ 4). Они способны разрушать структуру легких и поддерживать нейтрофильное воспаление. Вызванное ими повреждение в дальнейшем стимулирует воспаление путем выброса хемотактических пептидов измежклеточного матрикса. • ЛТВ 4 — мощный фактор хемотаксиса нейтрофилов. Его содержание в мокроте больных ХОБЛ повышено. Выработку ЛТВ 4 приписывают альвеолярным макрофагам. • ИЛ-8 участвует в избирательном вовлечении нейтрофилов и, возможно, синтезируется макрофагами, нейтрофилами и эпителиоцитами. Присутствует в высоких концентрациях в индуцированной мокроте и лаваже у больных ХОБЛ. • ФНО-α активирует ядерный фактор-к. В фактора транскрипции (NF -к. B), который, в свою очередь, активирует ген IL-8 эпителиоцитов и макрофагов. ФНО-α определяется в высоких концентрациях в мокроте, а также в биоптатах бронхов у пациентов ХОБЛ. У больных с выраженной потерей веса уровень сывороточного ФНО-α повышен, что говорит о возможности участия фактора в развитии кахексии
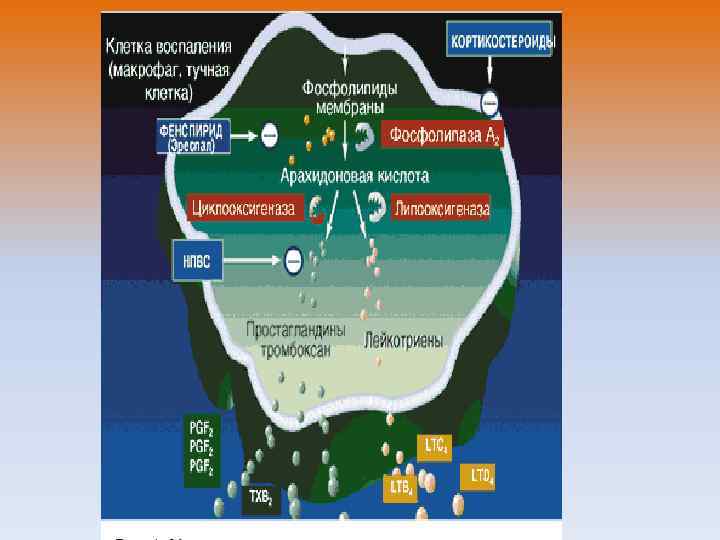

• Дисбаланс в системе протеиназы-антипротеиназы • В 1963 году Laurell и Eriksson привели наблюдение, что лица с дефицитом α 1 -антитрипсина, ингибирущим ряд сывороточных протеиназ, таких как нейтрофильная эластаза, имеют повышенный риск развития эмфиземы, так как нейтрофильная эластаза разрушает эластин, который является основным компонентом стенки альвеол. Помимо этого, фрагменты эластина, воздействуя на макрофаги и нейтрофилы, поддерживают воспаление. Хотя на сегодня дефицит α 1 -антитрипсина разграничен с понятием ХОБЛ, дисбаланс ферментной системы имеет место при ХОБЛ в настоящем понимании этого термина. Известно, что макрофаги, нейтрофилы и эпителиоцитывыделяют комбинацию протеаз. Активность антипротеазной системы снижается из-за окислительного стресса, воздействия табачного дыма и других факторов. Вероятнонейтрофильная эластаза не имеет значения при ХОБЛ, в патогенезе которой из протеаз играют роль нейтрофильный катепсин G, нейтрофильная протеиназа-3, катепсинымакрофагов (особенно катепсины B, L и S), и различные матриксные металлопротеиназы

Окислительный стресс О роли окислительного стресса свидетельствуют маркеры, обнаруживаемые в жидкости на поверхности эпителия, выдыхаемом воздухе и моче курильщиков и больных ХОБЛ — перекись водорода (Н 2 О 2) и оксид азота (NO), образующиеся при курении или высвобождаемые из лейкоцитов и эпителиоцитов при воспалении. Н 2 О 2 появляется в повышенном количестве в выдыхаемом воздухе у больных как в ремиссии, так и при обострении, а содержание NO повышается в выдыхаемом воздухе при обострении. Концентрация изомера простагландина изопростана F 2α-III — биомаркера окислительного стресса в легких in vivo, образующегося при свободнорадикальном окислении арахидоновой кислоты, повышается в конденсате выдыхаемого воздуха и моче у больных ХОБЛ в сравнении со здоровыми людьми и повышается ещё больше при обострении.

Окислительный стресс О роли окислительного стресса свидетельствуют маркеры, обнаруживаемые в жидкости на поверхности эпителия, выдыхаемом воздухе и моче курильщиков и больных ХОБЛ — перекись водорода (Н 2 О 2) и оксид азота (NO), образующиеся при курении или высвобождаемые из лейкоцитов и эпителиоцитов при воспалении. Н 2 О 2 появляется в повышенном количестве в выдыхаемом воздухе у больных как в ремиссии, так и при обострении, а содержание NO повышается в выдыхаемом воздухе при обострении. Концентрация изомера простагландина изопростана F 2α-III — биомаркера окислительного стресса в легких in vivo, образующегося при свободнорадикальном окислении арахидоновой кислоты, повышается в конденсате выдыхаемого воздуха и моче у больных ХОБЛ в сравнении со здоровыми людьми и повышается ещё больше при обострении. Оксиданты разрушают биологические молекулы: белки, жиры, нуклеиновые кислоты, что приводит к дисфункции и смерти клеток, разрушению внеклеточного матрикса. Также благодаря окислительному стресссу усугубляется дисбаланс протеиназы-антипротеиназы за счет инактивации антипротеиназ и путем активации протеиназ, таких как металлопротеиназы. Оксиданты усиливают воспаление благодаря активации фактора NF-к. В, который способствует экспрессии воспалительных генов, таких как ИЛ-8 и ФНО -α. Наконец оксидативный стресс может вызывать обратимую обструкцию бронхов: Н 2 О 2 приводит к сокращению гладкомышечных клеток in vitro, а изопростан F 2α-III у человека является агентом, вызывающим выраженную бронхиальную обструкцию

Новые биомаркеры в патогенезе ХОБЛ: Pentraxin (PTX) 3 участвует в антимикробной защите, апоптозе клеток и очистке внеклеточного матрикса. Как эти процессы изменяются при хронической обструктивной болезни легких (ХОБЛ) неизвестно. Было проведено исследование PTX 3 -экспрессии у пациентов с этим заболеванием. Уровень экспрессии PTX 3 изучался количественно методом иммуногистохимического окрашивания ткани легкого у никогда не куривших, курильщиков без ХОБЛ, а также у пациентов с ХОБЛ стадии I, II и III-IV согласно GOLD. «кспрессию м. РНК в легочной ткани изучали методом количественного RT-PCR. PTX 3 концентрация была измерена в индуцированной мокроте и плазме методом ИФА.

• Молекулы PTX 3 в основном локализованы в интерстиции малых дыхательных путей и альвеолярной стенки. Не было никаких существенных различий в экспрессии PTX 3 в легких, мокроте и плазме крови между исследовательскими группами. Тем не менее, уровни PTX 3 -экспрессии в малых дыхательных путей достоверно коррелировали с объемом форсированного выдоха за 1 с (г = 0, 35, р = 0, 004). В альвеолярных стенках, PTX 3 экспрессия достоверно коррелировала с DLCO (г = 0, 28, р = 0, 04). В мокроте, PTX 3 -экспрессия тесно связана с количеством нейтрофилов. Наконец, системные уровни PTX 3 как правило, ниже у пациентов с тяжелой ХОБЛ по сравнению с легким течением ХОБЛ. • У пациентов с ХОБЛ, ограничения скорости воздушного потока и уменьшения коэффициента передачи для окиси углерода связано с низкой легочной выражение PTX 3.

• Течение патологического процесса • Патофизиологические изменения при ХОБЛ включают следующие патологические изменения: • гиперсекреция слизи, • дисфункция ресничек, • бронхиальная обструкция, • гиперинфляция легких, • деструкция паренхимы и эмфизема легких, • расстройства газообмена, • легочная гипертензия, • легочное сердце, • системные проявления.
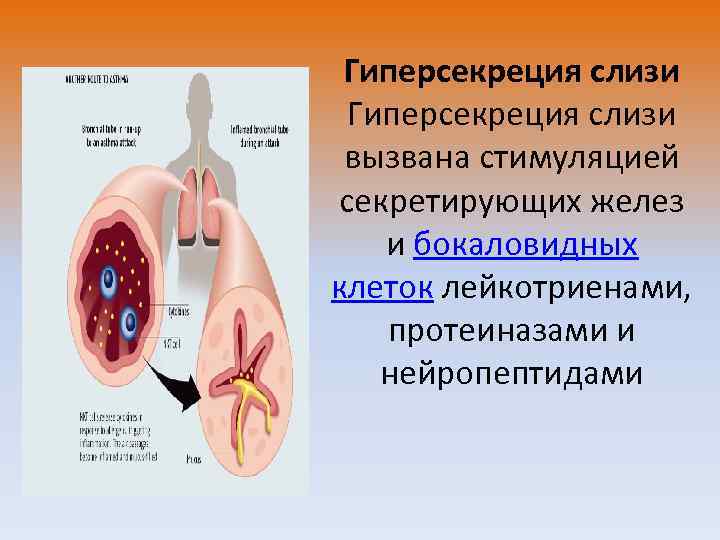
Гиперсекреция слизи вызвана стимуляцией секретирующих желез и бокаловидных клеток лейкотриенами, протеиназами и нейропептидами

Дисфункция ресничек Реснитчатый эпителий подвергается плоскоклеточн ой метаплазии, что приводит к нарушению мукоцилиарного клиренса (нарушению эвакуации мокроты из легких). Эти начальные проявления ХОБЛ могут сохраняться в течение многих лет не прогрессируя
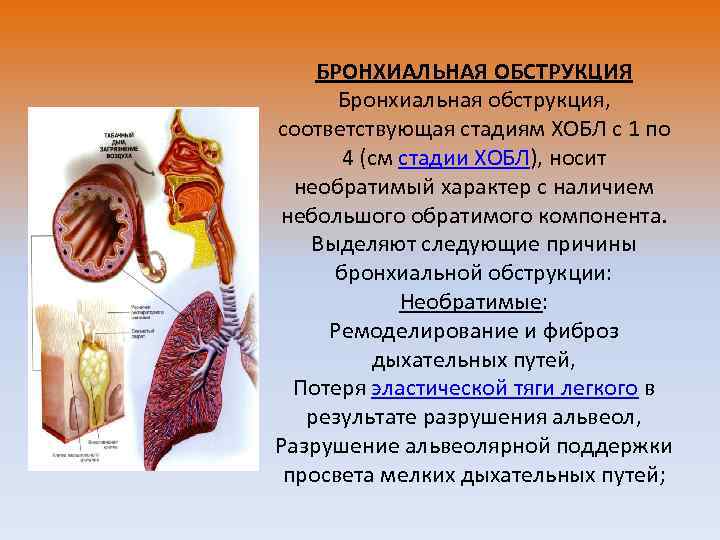
БРОНХИАЛЬНАЯ ОБСТРУКЦИЯ Бронхиальная обструкция, соответствующая стадиям ХОБЛ с 1 по 4 (см стадии ХОБЛ), носит необратимый характер с наличием небольшого обратимого компонента. Выделяют следующие причины бронхиальной обструкции: Необратимые: Ремоделирование и фиброз дыхательных путей, Потеря эластической тяги легкого в результате разрушения альвеол, Разрушение альвеолярной поддержки просвета мелких дыхательных путей;

• Обратимые: • Накопление клеток воспаления, слизи и экссудата плазмы в бронхах, • Сокращение гладкой мускулатуры бронхов, • Динамическая гиперинфляция при физической нагрузке.

• Обструкция при ХОБЛ, в основном, формируется на уровне мелких и мельчайших бронхов. Ввиду большого количества мелких бронхов, при их сужении примерно вдвое возрастает общее сопротивление нижних отделов респираторного тракта. • Спазм бронхиальной гладкой мускулатуры, воспалительный процесс и гиперсекреция слизи могут формировать небольшую часть обструкции, обратимую под влиянием лечения. Воспаление и экссудация имеют особенно важное значение при обострении
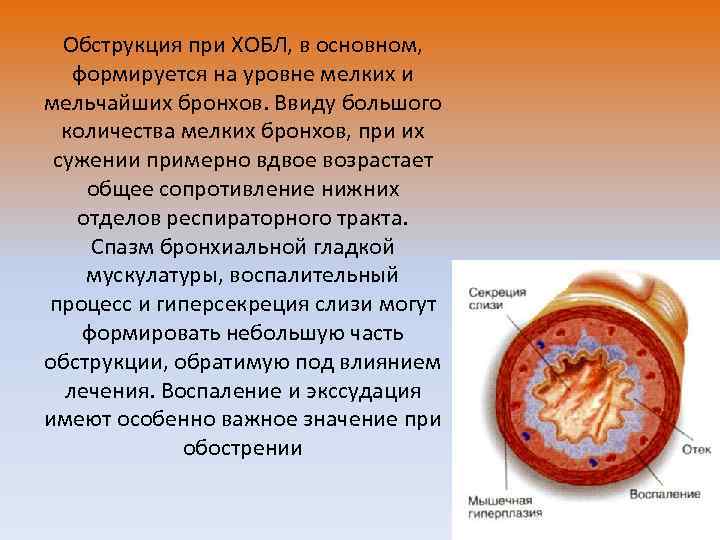
Обструкция при ХОБЛ, в основном, формируется на уровне мелких и мельчайших бронхов. Ввиду большого количества мелких бронхов, при их сужении примерно вдвое возрастает общее сопротивление нижних отделов респираторного тракта. Спазм бронхиальной гладкой мускулатуры, воспалительный процесс и гиперсекреция слизи могут формировать небольшую часть обструкции, обратимую под влиянием лечения. Воспаление и экссудация имеют особенно важное значение при обострении

• Лёгочная гиперинфляция (ЛГИ) — повышение воздушности лёгочной ткани, образование и увеличение «воздушной подушки» в лёгких. В зависимости от причины возникновения подразделяется на два вида: • статическая ЛГИ: вследствие неполного опорожнения альвеол на выдохе вследствие снижения эластической тяги легких • динамическая ЛГИ: вследствие уменьшения времени выдоха в условиях выраженного ограничения экспираторного воздушного потока

• С точки зрения патофизиологии, ЛГИ является адаптационным механизмом, так как приводит к снижению сопротивления воздушных путей, улучшению распределения воздуха и повышению минутной вентиляции в покое. Однако ЛГИ приводит к следующим неблагоприятным последствиям: • Слабость дыхательной мускулатуры. Происходит укорочение и уплощение диафрагмы, что делает её сокращения малоэффективными. • Ограничение нарастания дыхательного объёма при физической нагрузке. У здоровых людей при нагрузке происходит увеличение минутного объёма дыхания за счет увеличения частоты и глубины дыхания. У больных ХОБЛ во время нагрузки увеличивается легочная гиперинфляция, так как увеличение ЧДД при ХОБЛ ведет к укорочению выдоха, и ещё большая часть воздуха задерживается в альвеолах. Увеличение «воздушной подушки» не позволяет значительно увеличить глубину дыхания. • Гиперкапния при физической нагрузке. Вследствие снижения отношения ООЛ к ЖЁЛ за счёт уменьшения ЖЁЛ вследствие ЛГИ происходит увеличение Pa. CO 2 в артериальной крови.

• Создание внутреннего положительного давления в конце выдоха (intrinsic positive end-expiratory pressure, PEEPi). Вследствие роста «воздушной подушки» возникает давление эластической отдачи легких. В норме PEEPi равно нулю, у тяжелых больных ХОБЛ вне обострения — не более 7— 9 см вод. ст. , а при острой дыхательной недостаточности достигает 20— 22 см вод. ст. Это приводит к увеличению нагрузки на дыхательные мышцы, начало сокращения дыхательных мышц не совпадает с началом дыхательного потока, он начинается только тогда, когда давление, развиваемое мышцами, превышает PEEPi, когда альвеолярное давление становится отрицательным, что необходимо для вдоха. • Повышение эластической нагрузки на лёгкие.
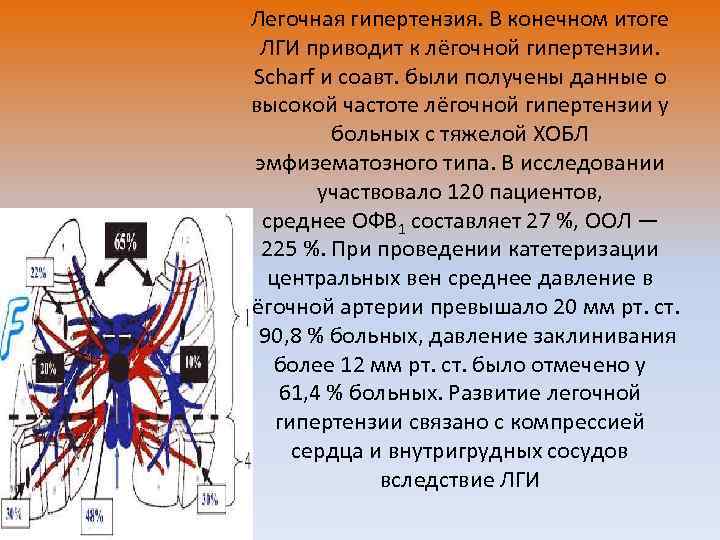
Легочная гипертензия. В конечном итоге ЛГИ приводит к лёгочной гипертензии. Scharf и соавт. были получены данные о высокой частоте лёгочной гипертензии у больных с тяжелой ХОБЛ эмфизематозного типа. В исследовании участвовало 120 пациентов, среднее ОФВ 1 составляет 27 %, ООЛ — 225 %. При проведении катетеризации центральных вен среднее давление в лёгочной артерии превышало 20 мм рт. ст. у 90, 8 % больных, давление заклинивания более 12 мм рт. ст. было отмечено у 61, 4 % больных. Развитие легочной гипертензии связано с компрессией сердца и внутригрудных сосудов вследствие ЛГИ

Эмфизема лёгких Деструкция паренхимы ведет к снижению эластической тяги лёгких, и поэтому имеет прямое отношение к ограничению скорости воздушного потока и увеличению сопротивления воздух лёгких. Мелкие бронхи, теряя связь с альвеолами, до этого находившимися в расправленном состоянии, спадаются и перестают быть проходимыми

Расстройства газообмена Обструкция дыхательных путей, деструкция паренхимы и расстройства легочного кровотока уменьшают легочную способность к газообмену, что приводит сначала кгипоксемии, а затем к гиперкапнии. Корреляция между значениями функции легких и уровнем газов артериальной крови слабо определяется, но при ОФВ 1 более 1 л редко возникают существенные изменения газового состава крови. На начальных стадиях гипоксемия возникает только при физической нагрузке, а по мере прогрессирования болезни — и в состоянии покоя

Лёгочное сердце Лёгочная гипертензия определяется как «гипертрофия правого желудочка в результате заболеваний, поражающих функцию и/или структуру лёгких, за исключением тех расстройств лёгких, которые являются результатом заболеваний, первично поражающих левые отделы сердца, как при врожденных заболеваниях сердца» . Распространённость и течение лёгочного сердца при ХОБЛ до сих пор неясны. Лёгочная гипертензия и редукция сосудистого ложа вследствие эмфиземы ведут к гипертрофии правого желудочка и его недостаточности лишь у части больных

Системные проявления При ХОБЛ наблюдается системное воспаление и дисфункция скелетной мускулатуры. Системное воспаление проявляется наличием системного окислительного стресса, повышенной концентрацией циркулирующих цитокинов и активацией клеток воспаления. Проявлением дисфункции скелетных мышц являются потеря мышечной массы и различные биоэнергетические расстройства. Эти проявления ведут к ограничению физических возможностей пациента, снижают уровень здоровья, ухудшению прогноза заболевания
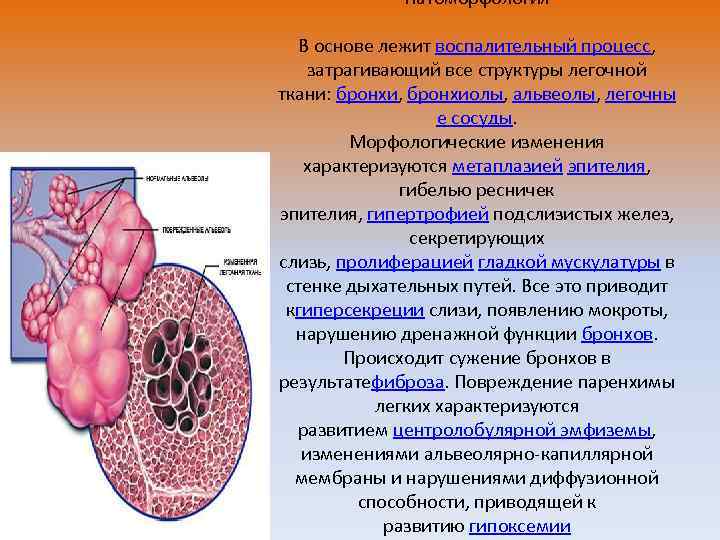
Патоморфология В основе лежит воспалительный процесс, затрагивающий все структуры легочной ткани: бронхи, бронхиолы, альвеолы, легочны е сосуды. Морфологические изменения характеризуются метаплазией эпителия, гибелью ресничек эпителия, гипертрофией подслизистых желез, секретирующих слизь, пролиферацией гладкой мускулатуры в стенке дыхательных путей. Все это приводит кгиперсекреции слизи, появлению мокроты, нарушению дренажной функции бронхов. Происходит сужение бронхов в результатефиброза. Повреждение паренхимы легких характеризуются развитием центролобулярной эмфиземы, изменениями альвеолярно-капиллярной мембраны и нарушениями диффузионной способности, приводящей к развитию гипоксемии
![• Клиническая картина • Кашель — наиболее ранний симптом болезни[9]. Он часто недооценивается • Клиническая картина • Кашель — наиболее ранний симптом болезни[9]. Он часто недооценивается](https://present5.com/presentation/1/214162835_299609411.pdf-img/214162835_299609411.pdf-37.jpg)
• Клиническая картина • Кашель — наиболее ранний симптом болезни[9]. Он часто недооценивается пациентами, будучи ожидаемым при курении и воздействии поллютантов. На первых стадиях заболевания он появляется эпизодически, но позже возникает ежедневно, изредка — появляется только по ночам. Вне обострения кашель, как правило, не сопровождается отделением мокроты. Иногда кашель отсутствует при наличии спирометрических подтверждений бронхиальной обструкции[3]. • Мокрота — относительно ранний симптом заболевания. В начальных стадиях она выделяется в небольшом количестве, как правило, по утрам, и имеет слизистый характер. Гнойная, обильная мокрота — признак обострения заболевания

• Одышка возникает примерно на 10 лет позже кашля и отмечается вначале только при значительной и интенсивной физической нагрузке, усиливаясь при респираторных инфекциях. Одышка чаще смешанного типа, реже встречается экспираторная. На более поздних стадиях одышка варьирует от ощущения нехватки воздуха при обычных физических нагрузках до тяжелой дыхательной недостаточности, и со временем становится более выраженной. Она является частой причиной обращения к врачу

• Для оценки степени выраженности одышки предложена шкала одышки Medical Research Council (MRC) Dyspnea Scale — модификация шкалы Флетчера: • Шкала одышки Medical Research Council (MRC) • Dyspnea Scale • 0 - Одышка только при очень интенсивной нагрузке • 1 Лёгкая - Одышка при быстрой ходьбе, небольшом подъёме • 2 Средняя - Одышка вынуждает пациента передвигаться при ходьбе медленнее, чем здоровые люди того же возраста • 3 Тяжёлая - Одышка заставляет останавливаться при ходьбе примерно через каждые 100 метров • 4 Очень тяжёлая - Одышка не позволяет выйти за пределы дома или появляется при переодевании

• Исследование функции внешнего дыхания • Ограничение скорости воздушного потока выявляется методом спирометрии. Наиболее важные спирометрические показатели — объём форсированного выдоха за 1 -ю секунду (ОФВ 1) и форсированная жизненная емкость легких (ФЖЕЛ). • По мере развития патологического процесса, что проявляется утолщением стенки дыхательных путей и потерей альвеолярного прикрепления эластической тяги легких, снижаются показатели (ОФВ 1) и ФЖЕЛ, превосходя возрастные темпы снижения этих значений. Часто до этих изменений снижается отношение (ОФВ 1 к ФЖЕЛ (индекс Тиффно). Также вследствие снижения эластической тяги легких и преждевременного закрытия дыхательных путей растет функциональная остаточная емкость (ФОЕ). • При легочной гипервентиляции происходит увеличение функциональной остаточной емкости легких (ФОЕЛ), остаточного объёма легких (ООЛ), общей емкости легких (ОЕЛ), снижение жизненной емкости легких (ЖЕЛ = ОЕЛ — (ООЛ)

• Диагностика • При сборе анамнеза необходимо уделить внимание анализу индивидуальных факторов риска, так как при сочетании факторов риска прогрессирование болезни ускоряется. • Для оценки курения как фактора риска используется индекс курильщика (ИК), выраженный в пачках/лет: • ИК (пачка/лет) = (число выкуриваемых сигарет в сутки * стаж курения (годы))/20 • Если ИК более 10 пачек/лет является достоверным фактором риска развития ХОБЛ

Классификация Стратификация тяжести (стадия) В основе стратификации два критерия: клинический, включающий кашель, образование мокроты и одышку, • и функциональный, учитывающий степень необратимости обструкции дыхательных путей. • Также ранее различали риск развития ХОБЛ как стадию 0 заболевания, но в последних текстах GOLD отказались от такой категории, так как недостаточно доказательств, что пациенты, имеющие «риск развития болезни» (хронический кашель, образование мокроты при нормальных показателях функции внешнего дыхания), обязательно развивается стадия I ХОБЛ. • Приводимые значения ОФВ 1 являются постбронходилатационными, то есть степень тяжести оценивается по показателям бронхиальной проходимости после ингаляции бронходилататора • •

Стадия I. Лёгкая ОФВ 1/ФЖЕЛ менее 70 % от должного ОФВ 1 более 80 % от должного Наличие или отсутствие хронических симптомов (кашель, мокрота) • ОФВ 1 остаётся в пределах среднестатистической нормы, а отношение ОФВ 1 к ФЖЕЛ становится ниже 70 % от должной величины. Этот показатель отражает раннее проявление бронхиальной обструкции, выявляемое методом спирометрии. Он характеризует изменение структуры выдоха, то есть за 1 -ю секунду форсированного выдоха пациент выдыхает показатель среднестатистической нормы, однако по отношению к ФЖЕЛ этот процент снижается до 70 от нормы, что выявляет индивидуальное нарушение функции внешнего дыхания • •

• • Стадия II. Средняя ОФВ 1/ФЖЕЛ менее 70 % от должного ОФВ 1 менее 80 % от должного Наличие или отсутствие хронических симптомов (кашель, мокрота, одышка)

• • Стадия III. Тяжёлая ОФВ 1/ФЖЕЛ менее 70 % от должного ОФВ 1 менее 50 % от должного Наличие или отсутствие хронических симптомов (кашель, мокрота, одышка)

• Стадия IV. Крайне-тяжёлая • ОФВ 1/ФЖЕЛ менее 70 % от должного • ОФВ 1 менее 30 % от должного или менее 50 % в сочетании с хронической дыхательной недостаточностью • ХОБЛ возникает, протекает и прогрессирует задолго до появления значимых функциональных нарушений, определяемых инструментально. За это время воспаление вбронхах приводит к грубым необратимым морфологическим изменениям, поэтому данная стратификация не решает вопрос о ранней диагностике и сроках начала лечения.

• Фаза заболевания • Обострение ХОБЛ — ухудшение самочувствия в течение не менее двух дней подряд, возникающее остро. Для обострения характерно усиление кашля, увеличение количества и состава отделяемой мокроты, усиление одышки. Во время обострения модифицируется терапия и добавляются другие лекарства. Промежутки между фазами обострения ХОБЛ соответственно именуются как фазы ремиссии

• Критерии Anthonisen et al. , 2010 год • Большие критерии Усиление одышки Увеличение количества мокроты Усиление «гнойности» мокроты Малые критерии Инфекция верхних дыхательных путей Лихорадка Свистящее дыхание Усиление кашля Учащение ЧСС или ЧДД на 20 % и более

• Обострение диагностируется на основе совокупности критериев. Anthonisen et al. выделяют также 3 типа обострения ХОБЛ: [16] • обострение I типа — сочетание всех трёх больших критериев; • обострение II типа — наличие двух из трёх больших критериев; • обострение III типа — сочетание одного большого критерия с одним или несколькими малыми критериями.

• Формулировка диагноза • Согласно международной программе GOLD (2003), у больных ХОБЛ нужно указывать фазу болезни и степень тяжести заболевания, вариант течения, состояние больного (обострение или ремиссия), а затем перечислять осложнения возникшие в ходе развития заболевания.

Пример формулировки диагноза • ХОБЛ, преимущественно бронхитический тип, стадия IV, крайне тяжелое течение, обострение, хронический гнойный бронхит, обострение. Хроническое декомпенсированное легочное сердце, Н III, ДН III.
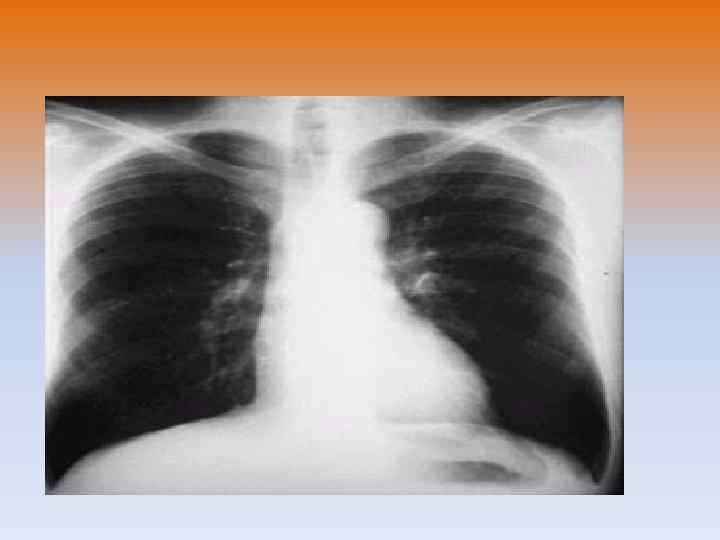
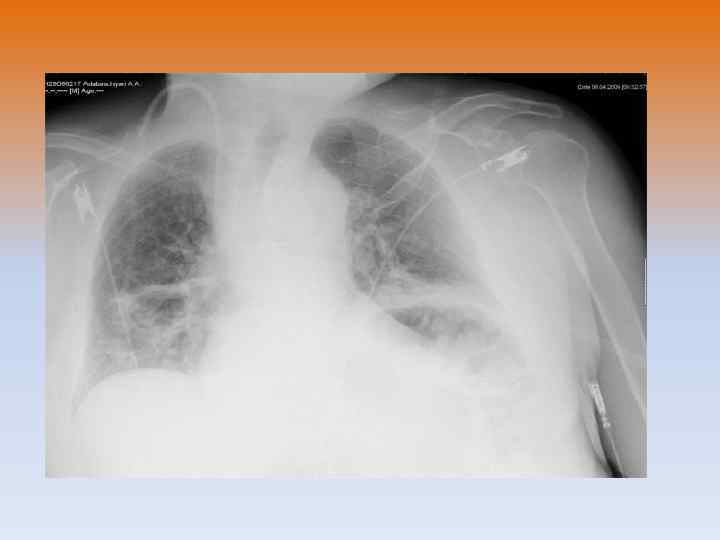
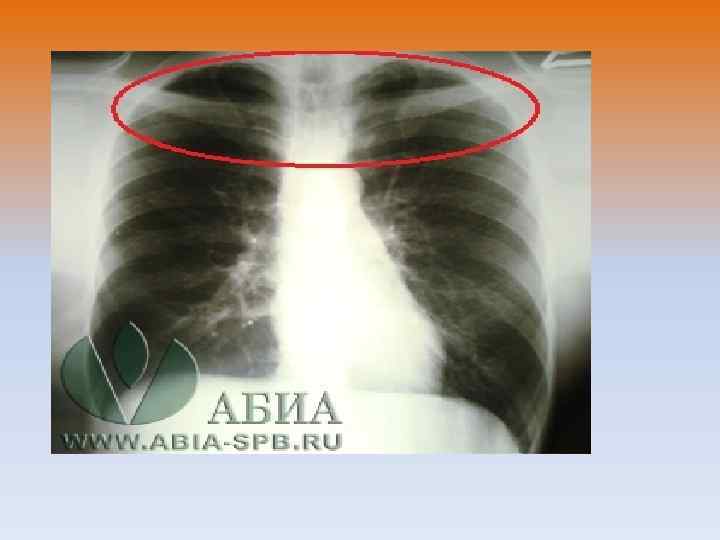

Лечение • Основными направлениями лечения ХОБЛ являются уменьшение воздействия неблагоприятных факторов внешней среды (в том числе отказ от курения), обучение больных, использование лекарственных средств и немедикаментозная терапия (оксигенотерапия, реабилитация и др. ). Различные комбинации этих методов используются у пациентов с ХОБЛ в фазу ремиссии и обострения

• Принципы лечения ХОБЛ стабильного течения следующие: • Объем лечения увеличивается по мере нарастания тяжести болезни. Его уменьшение при ХОБЛ, в отличие от бронхиальной астмы, как правило, невозможно. • Медикаментозная терапия используется для предупреждения осложнений и уменьшения выраженности симптомов, частоты и тяжести обострений, повышения толерантности к физической нагрузке и качества жизни больных. • Следует иметь в виду, что ни одно из имеющихся лекарственных средств не влияет на темпы снижения бронхиальной проходимости, которое является отличительной чертой ХОБЛ. • Бронхолитики занимают центральное место в лечении ХОБЛ. Они уменьшают выраженность обратимого компонента обструкции бронхов. Эти средства используются в режиме «по требованию» или регулярно. • Ингаляционные глюкокортикоиды показаны при тяжелом и крайне тяжелом течении ХОБЛ (при объеме форсированного выдоха за 1 с (ОФВ 1) менее 50% от должного и частыми обострениями, как правило, более трех за последние три года или один-два за один год, для лечения которых используются пероральные стероиды и антибиотики. • Комбинированная терапия ингаляционными глюкокортикоидами и β 2 адреномиметиками длительного действия оказывает существенный дополнительный эффект на функцию легких и клинические симптомы ХОБЛ по сравнению с монотерапией каждым из препаратов. Наибольшее влияние на частоту обострений и качество жизни наблюдается у больных ХОБЛ с ОФВ 1<50% от должного. Эти препараты предпочтительно назначать в ингаляционной форме, содержащей их фиксированные комбинации (салметерол/флутиказон пропионат, формотерол/будесонид).

• Длительное использование таблетированных глюкокортикоидов не рекомендуется в связи с риском развития системных побочных эффектов. • На всех стадиях ХОБЛ высокой эффективностью обладают физические тренирующие программы, повышающие толерантность к физической нагрузке и уменьшающие выраженность одышки и утомления. • Длительное назначение кислорода (более 15 ч в сутки) больным с дыхательной недостаточностью повышает их выживаемость

• Медикаментозное лечение ХОБЛ стабильного течения • Бронхолитики. К их числу относятся β 2 адреномиметики, холинолитики, а также теофиллин

• • Принципы бронхолитической терапии ХОБЛ следующие. Предпочтительным путем введения бронхолитиков является ингаляционный. Изменение легочной функции после кратковременного назначения бронхорасширяющих препаратов не является показателем их длительной эффективности. Относительно небольшой прирост ОФВ 1 может сочетаться со значительными изменениями легочных объемов, в том числе с уменьшением остаточного объема легких, что способствует уменьшению выраженности у больных одышки. Выбор между β 2 -адреномиметиками, холинолитиками, теофиллином зависит от их доступности, индивидуальной чувствительности больных к их действию и отсутствия побочных эффектов. У пожилых пациентов, имеющих сопутствующие заболевания сердечно-сосудистой системы (ИБС, нарушения сердечного ритма, артериальная гипертензия и др. ), в качестве препаратов первого ряда предпочтительны холинолитики. Ксантины эффективны при ХОБЛ, но в связи с возможностью развития побочных эффектов они относятся к препаратам «второго ряда» . При их назначении рекомендуется измерять концентрацию теофиллина в крови. Следует подчеркнуть, что положительным влиянием на течение ХОБЛ обладают только теофиллины длительного действия (но не эуфиллин и теофедрин!). Ингаляционные бронхолитики длительного действия более удобны, но и стоят дороже, чем короткодействующие средства. Регулярное лечение бронхорасширяющими средствами длительного действия (тиотропия бромидом, сальметеролом и формотеролом) показано при ХОБЛ средней тяжести, тяжелого и крайне тяжелого течения. Комбинация нескольких бронхорасширяющих средств (например, холинолитиков и β 2 адреномиметиков, холинолитиков и теофиллинов, β 2 -адреномиметиков и теофиллинов) может повысить эффективность и снизить вероятность развития побочных эффектов по сравнению с монотерапией одним препаратом.

• Для доставки β 2 -адреномиметиков и холинолитиков используются дозированные аэрозоли, порошковые ингаляторы и небулайзеры. Последние рекомендуются при лечении обострений ХОБЛ, а также у пациентов с тяжелым течением болезни, которые испытывают трудности применении других систем доставки. При стабильном течении ХОБЛ предпочтительны дозированные и порошковые ингаляторы.

• Глюкокортикоиды. Данные лекарственные средства обладают выраженной противовоспалительной активностью, хотя у больных ХОБЛ она выражена существенно меньше, чем у пациентов с астмой. Короткие (10– 14 дней) курсы системных стероидов используются для лечения обострений ХОБЛ. Длительное применение этих препаратов не рекомендуется из-за опасности развития побочных эффектов (миопатия, остеопороз и др. )

• • Данные о влиянии ингаляционных глюкокортикоидов на течение ХОБЛ Показано, что они не оказывают влияния на прогрессирующее снижение бронхиальной проходимости у больных ХОБЛ. Их высокие дозы (например, флутиказона пропионат 1000 мкг/сут) могут повышать качество жизни пациентов и снижать частоту обострений ХОБЛ тяжелого и крайне тяжелого течения. Причины относительной стероидной резистентности воспаления дыхательных путей при ХОБЛ являются предметом интенсивных исследований. Возможно, она обусловлена тем, что кортикостероиды увеличивают продолжительность жизни нейтрофилов за счет торможения их апоптоза. Молекулярные механизмы, лежащие в основе устойчивости к действию глюкокортикоидов, изучены недостаточно. Появились сообщения о снижении под влиянием курения и свободных радикалов активности деацетилазы гистонов, являющейся мишенью для действия стероидов, что может уменьшать тормозящее влияние глюкокортикоидов на транскрипцию «воспалительных» генов и ослаблять их противовоспалительное действие.

• В последнее время получены новые данные об эффективности комбинированных препаратов (флутиказона пропионат/сальметерол 500/50 мкг, 1 ингаляция 2 раза в день и будесонид/формотерол 160/4, 5 мкг, 2 ингаляции 2 раза в день, будесонид/сальбутамол 100/200 мгк 2 ингаляции 2 раза в день) у больных ХОБЛ тяжелого и крайне тяжелого течения. Показано, что их длительное (12 мес) назначение улучшает бронхиальную проходимость, снижает выраженность симптомов, потребность в бронхолитиках, частоту средней тяжести и тяжелых обострений, а также улучшает качество жизни пациентов по сравнению с монотерапией ингаляционными глюкокортикоидами, β 2 -адреномиметиками длительного действия и плацебо

• Вакцины. Вакцинация против гриппа снижает тяжесть обострений и смертность больных ХОБЛ примерно на 50%. Вакцины, содержащие убитые или инактивированные живые вирусы гриппа, обычно назначаются однократно в октябре — первой половине ноября. • Данных об эффективности пневмокококковой вакцины, содержащей 23 вирулентных серотипа этого микроорганизма, у больных ХОБЛ недостаточно. Вместе с тем некоторые эксперты рекомендуют ее применение при этом заболевании для профилактики пневмонии

• Антибиотики. В настоящее время не получено убедительных данных об эффективности антибактериальных средств для уменьшения частоты и тяжести неинфекционных обострений ХОБЛ. • Антибиотики показаны для лечения инфекционных обострений болезни, непосредственно влияют на длительность ликвидации симптомов ХОБЛ, а некоторые способствуют удлинению межрецидивного интервала.


• Муколитики (мукокинетики, мукорегуляторы). Муколитики (амброксол, карбоцистеин, препараты йода и др. ) могут применяться у небольшой части больных, имеющих вязкую мокроту. Широкое использование этих средств у пациентов с ХОБЛ не рекомендуется. • Антиоксиданты. N-ацетилцистеин, обладающий антиоксидантной и муколитической активностью, способен снижать продолжительность и частоту обострений ХОБЛ. Этот препарат может использоваться у больных в течение длительного времени (3– 6 мес) в дозе 600 мг/сут.

• Иммунорегуляторы (иммуностимуляторы, иммуномодуляторы). Регулярное использование этих препаратов не рекомендуется из-за отсутствия убедительных доказательств эффективности. • Больные с генетически детерминированным дефицитом α 1 -антитрипсина, у которых ХОБЛ развивается в молодом (до 40 лет) возрасте, являются возможными кандидатами для заместительной терапии. Вместе с тем стоимость такого лечения очень высока, и оно доступно не во всех странах.

• Немедикаментозное лечение ХОБЛ стабильного течения • Оксигенотерапия • Известно, что дыхательная недостаточность — это основная причина смерти больных ХОБЛ. Коррекция гипоксемии с помощью подачи кислорода является патогенетически обоснованным методом лечения. Различают кратковременную и длительную оксигенотерапию [4, 15]. Первая используется при обострениях ХОБЛ. Вторая применяется при крайне тяжелом течении ХОБЛ (при ОФВ 1<30% от должного) постоянно или ситуационно (при физической нагрузке и во время сна). Целью оксигенотерапии является увеличение парциального напряжения кислорода (Ра. O 2) в артериальной крови не ниже 60 мм рт. ст. или сатурации (Sa. O 2) не менее чем до 90% в покое, при физической нагрузке и во время сна.

• При стабильном течении ХОБЛ предпочтительна постоянная длительная оксигенотерапия. Доказано, что она увеличивает выживаемость больных ХОБЛ, уменьшает выраженность одышки, прогрессирование легочной гипертензии, снижает вторичный эритроцитоз, частоту эпизодов гипоксемии во время сна, повышает толерантность к физической нагрузке, качество жизни и нейропсихический статус пациентов

• Показания длительной оксигенотерапии у больных ХОБЛ крайне тяжелого течения (при ОФВ 1< 30% от должного или менее 1, 5 л): • Ра. О 2 менее 55% от должного, Sa. О 2 ниже 88% при наличии или отсутствии гиперкапнии; • Ра. О 2 — 55– 60% от должного, Sa. О 2 — 89% при наличии легочной гипертензии, периферических отеков, связанных с декомпенсацией легочного сердца или полицитемии (гематокрит более 55%).

• Параметры газообмена должны оцениваться только на фоне стабильного течения ХОБЛ и не ранее чем через 3– 4 нед после обострения при оптимально подобранной терапии. Решение о назначении оксигенотерапии должно основываться на показателях, полученных в покое и при выполнении физической нагрузки (например, на фоне 6 минутной ходьбы). Повторная оценка газов артериальной крови должна проводится через 30– 90 дней от начала оксигенотерапии.

• Длительное лечение кислородом следует проводить не менее 15 ч в день. Скорость потока газа обычно составляет 1– 2 л/мин, при необходимости она может быть увеличена до 4 л/мин. Оксигенотерапия никогда не должна назначаться больным, которые продолжают курить или страдают алкоголизмом. • В качестве источников кислорода используются баллоны со сжатым газом, концентраторы кислорода и цилиндры с жидким кислородом. Наиболее экономичны и удобны для домашнего использования концентраторы кислорода.

• Доставка кислорода больному осуществляется с помощью масок, назальных канюль, транстрахеальных катеторов. Наиболее удобны и широко используются назальные канюли, которые позволяют осуществлять поступление больному кислородо-воздушной смеси с 30– 40% О 2. Доставка кислорода в альвеолы осуществляется только в раннюю фазу вдоха (первые 0, 5 с). Газ, поступающий позднее, используется лишь для заполнения мертвого пространства и не участвует в газообмене. Для повышения эффективности доставки имеется несколько типов кислородсберегающих устройств (резервуарные канюли, устройства, осуществляющие подачу газа только во время вдоха, транстрахеальные катетеры и др. ).

• У больных ХОБЛ крайне тяжелого течения, имеющих дневную гиперкапнию, возможно комбинированное использование длительной оксигенотерапии и неинвазивной вентиляции легких с положительным давлением на вдохе. Следует отметить, что оксигенотерапия является одним из наиболее дорогостоящих методов лечения больных ХОБЛ. Внедрение ее в повседневную клиническую практику представляет собой одну из самых актуальных медико-социальных задач в России.
Презентация ХОБЛ Жук А.Н. (2).pptx