Л 3 Т 2 ХЛОР.ppt
- Количество слайдов: 50
![ХЛОР Хлор – неполный электронный аналог фтора: [1 s 22 p 6]3 s 23 ХЛОР Хлор – неполный электронный аналог фтора: [1 s 22 p 6]3 s 23](https://present5.com/presentation/-42637833_141829236/image-1.jpg) ХЛОР Хлор – неполный электронный аналог фтора: [1 s 22 p 6]3 s 23 p 5 E 3 s 3 p 3 d 1
ХЛОР Хлор – неполный электронный аналог фтора: [1 s 22 p 6]3 s 23 p 5 E 3 s 3 p 3 d 1
 Атом хлора имеет один непарный электрон, чем и предопределяется его сходство с фтором и водородом. В то же время у хлора по сравнению со фтором больше размер валентных орбиталей, гораздо меньше значение энергии ионизации Iион, заметно больше сродство к электрону Fсрод, большая поляризуемость атома: rорб, нм Iион, э. В Fсрод, э. В F………… 0, 036 17, 42 3, 45 Cl………. . 0, 072 12, 97 3, 61 2
Атом хлора имеет один непарный электрон, чем и предопределяется его сходство с фтором и водородом. В то же время у хлора по сравнению со фтором больше размер валентных орбиталей, гораздо меньше значение энергии ионизации Iион, заметно больше сродство к электрону Fсрод, большая поляризуемость атома: rорб, нм Iион, э. В Fсрод, э. В F………… 0, 036 17, 42 3, 45 Cl………. . 0, 072 12, 97 3, 61 2
 В большинстве соединений хлор как сильно электроотрицательный элемент (ЭО=3, 0) выступает в отрицательной степени окисления -1. В соединениях с более электроотрицательными фтором, кислородом и азотом он проявляет положительные степени окисления. Особо разнообразны соединения хлора с кислородом, в которых степени окисления хлора +1, +3, +5 и +7, а также +4 и +6. Хлор — типичный неметаллический элемент. Следовательно, для него наиболее характерна тенденция при химических превращениях образовывать простые и сложные 3 анионы.
В большинстве соединений хлор как сильно электроотрицательный элемент (ЭО=3, 0) выступает в отрицательной степени окисления -1. В соединениях с более электроотрицательными фтором, кислородом и азотом он проявляет положительные степени окисления. Особо разнообразны соединения хлора с кислородом, в которых степени окисления хлора +1, +3, +5 и +7, а также +4 и +6. Хлор — типичный неметаллический элемент. Следовательно, для него наиболее характерна тенденция при химических превращениях образовывать простые и сложные 3 анионы.
 • Хлор относится к довольно распространенным на Земле элементам. Встречается он главным образом в виде х л о р и д о в — соединений с наиболее устойчивым состоянием окисления хлора. Из них наиболее важными минералами являются Nа. Сl — каменная соль. Nа. Сl КСl — сильвинит, КСl Мg. Сl 2 6 Н 2 O — карналлит. В огромном количестве хлориды содержатся в морской воде, входят составной частью во все живые организмы и пр. • В природных соединениях хлор находится в виде изотопов 35 Сl (75; 53%) и 37 Сl (24, 47%). Кроме того, искусственно получены его радиоактивные изотопы (33 Сl, 34 Сl, 36 Сl и 39 Сl). 4
• Хлор относится к довольно распространенным на Земле элементам. Встречается он главным образом в виде х л о р и д о в — соединений с наиболее устойчивым состоянием окисления хлора. Из них наиболее важными минералами являются Nа. Сl — каменная соль. Nа. Сl КСl — сильвинит, КСl Мg. Сl 2 6 Н 2 O — карналлит. В огромном количестве хлориды содержатся в морской воде, входят составной частью во все живые организмы и пр. • В природных соединениях хлор находится в виде изотопов 35 Сl (75; 53%) и 37 Сl (24, 47%). Кроме того, искусственно получены его радиоактивные изотопы (33 Сl, 34 Сl, 36 Сl и 39 Сl). 4
 • Простое вещество. • Молекула хлора, подобно молекулам Н 2 и F 2, двухатомна. Энергия диссоциации Сl 2 больше (243 к. Дж/моль), чем у F 2 (151 к. Дж/моль). Распад молекул хлора на атомы становится заметным, начиная с 1000 °С. • Большую устойчивость молекулы Сl 2 по сравнению с F 2 можно объяснить тем, что в молекуле F 2 связывающие электроны отталкиваются друг от друга сильнее, чем в более крупной по размерам молекуле Сl 2. 5
• Простое вещество. • Молекула хлора, подобно молекулам Н 2 и F 2, двухатомна. Энергия диссоциации Сl 2 больше (243 к. Дж/моль), чем у F 2 (151 к. Дж/моль). Распад молекул хлора на атомы становится заметным, начиная с 1000 °С. • Большую устойчивость молекулы Сl 2 по сравнению с F 2 можно объяснить тем, что в молекуле F 2 связывающие электроны отталкиваются друг от друга сильнее, чем в более крупной по размерам молекуле Сl 2. 5
 • Согласно другой точке зрения в отличие от Н 2 и F 2 в молекуле Сl 2 полагают дополнительное -связывание. Последнее возникает по донорно-акцепторному механизму за счет неподеленной электронной пары одного атома и свободной 3 d-орбитали другого. • Считается, что порядок связи в молекуле Сl 2 составляет 1, 12. 6
• Согласно другой точке зрения в отличие от Н 2 и F 2 в молекуле Сl 2 полагают дополнительное -связывание. Последнее возникает по донорно-акцепторному механизму за счет неподеленной электронной пары одного атома и свободной 3 d-орбитали другого. • Считается, что порядок связи в молекуле Сl 2 составляет 1, 12. 6
 • В обычных условиях хлор — газ желтозеленого цвета (Tпл. -101, 0 °С, Tкип. -34, 2 °С). Ограниченно растворяется в воде (1 объем воды растворяет около 2 объемов хлора). При охлаждении из водных растворов выделяются кристаллогидраты, являющиеся клатратами (соединения включения) приблизительного состава Сl 2 6 Н 2 О и Сl 2 8 Н 2 O. 7
• В обычных условиях хлор — газ желтозеленого цвета (Tпл. -101, 0 °С, Tкип. -34, 2 °С). Ограниченно растворяется в воде (1 объем воды растворяет около 2 объемов хлора). При охлаждении из водных растворов выделяются кристаллогидраты, являющиеся клатратами (соединения включения) приблизительного состава Сl 2 6 Н 2 О и Сl 2 8 Н 2 O. 7
 • Весьма энергично реагирует с металлами и большинством неметаллов (за исключением С, N 2, О 2, и инертных газов), легко окисляет многие сложные соединения. Зажженная свеча продолжает гореть в атмосфере Cl 2 сильно коптящим пламенем (образуются HCl и C), скипидар вспыхивает при соприкосновении с Cl 2. • Восстановительные свойства хлор проявляет лишь при взаимодействии с фтором. Вступает также в реакции диспропорционирования, для протекания которых наиболее благоприятна щелочная среда, способствующая образованию простых и сложных анионов: Сl 2 + 2 OН- Сl- + Сl. O- + Н 2 O Сl 2 + 2 Nа. ОН Na. Cl + Nа. Сl. О + Н 2 O 8
• Весьма энергично реагирует с металлами и большинством неметаллов (за исключением С, N 2, О 2, и инертных газов), легко окисляет многие сложные соединения. Зажженная свеча продолжает гореть в атмосфере Cl 2 сильно коптящим пламенем (образуются HCl и C), скипидар вспыхивает при соприкосновении с Cl 2. • Восстановительные свойства хлор проявляет лишь при взаимодействии с фтором. Вступает также в реакции диспропорционирования, для протекания которых наиболее благоприятна щелочная среда, способствующая образованию простых и сложных анионов: Сl 2 + 2 OН- Сl- + Сl. O- + Н 2 O Сl 2 + 2 Nа. ОН Na. Cl + Nа. Сl. О + Н 2 O 8
 • Получают свободный хлор окислением хлоридов: в лаборатории — химическим окислением концентрированной соляной кислоты; Mn. O 2 + 4 HCl = Cl 2 + Mn. Cl 2 + 2 H 2 O; (нагрев) 2 KMn. O 4 + 16 HCl = Cl 2 + 2 Mn. O 2 + 2 KCl + 8 H 2 O. Особо чистый хлор – нагреванием хлорида золота: 2 Au. Cl 3 = 2 Au + 3 Cl 2 • в технике — электролизом водного раствора Nа. Сl и — как побочный продукт — при получении натрия электролизом расплава Nа. Сl. • Хлор применяют для стерилизации питьевой воды, широко используют в качестве окислителя в самых разнообразных отраслях химической промышленности. 9
• Получают свободный хлор окислением хлоридов: в лаборатории — химическим окислением концентрированной соляной кислоты; Mn. O 2 + 4 HCl = Cl 2 + Mn. Cl 2 + 2 H 2 O; (нагрев) 2 KMn. O 4 + 16 HCl = Cl 2 + 2 Mn. O 2 + 2 KCl + 8 H 2 O. Особо чистый хлор – нагреванием хлорида золота: 2 Au. Cl 3 = 2 Au + 3 Cl 2 • в технике — электролизом водного раствора Nа. Сl и — как побочный продукт — при получении натрия электролизом расплава Nа. Сl. • Хлор применяют для стерилизации питьевой воды, широко используют в качестве окислителя в самых разнообразных отраслях химической промышленности. 9
 • Соединения со степенью окисления хлора — 1. Характер химической связи, а следовательно, и свойства хлоридов, как п фторидов, закономерно изменяются по группам и периодам элементов. Так, в ряду хлоридов элементов данного периода тип химической связи изменяется от преимущественно ионной в хлоридах типичных металлов до ковалентной в хлоридах неметаллов. • Ионные хлориды — твердые кристаллические вещества с высокими температурами плавления. • Ковалентные хлориды — газы, жидкости или же легкоплавкие твердые вещества. Промежуточное положение занимают ионно-ковалентные хлориды. 10
• Соединения со степенью окисления хлора — 1. Характер химической связи, а следовательно, и свойства хлоридов, как п фторидов, закономерно изменяются по группам и периодам элементов. Так, в ряду хлоридов элементов данного периода тип химической связи изменяется от преимущественно ионной в хлоридах типичных металлов до ковалентной в хлоридах неметаллов. • Ионные хлориды — твердые кристаллические вещества с высокими температурами плавления. • Ковалентные хлориды — газы, жидкости или же легкоплавкие твердые вещества. Промежуточное положение занимают ионно-ковалентные хлориды. 10
 • Ионные хлориды (хлориды металлов) проявляют основные свойства, ковалентные хлориды (хлориды неметаллов) кислотные, например: Na. Cl Са. Cl 2 Al. Cl 3 (к) Si. Cl 4(ж) PCl 5(к) SCl 4(к) Тпл. , о. С. 800 772 193 – 70 159 ˃– 30 разл Кисл. -основн. св-ва основные амфот. кислотные Большинство хлоридов металлов хорошо растворимо в воде (за исключением Аg. Сl, Сu. Сl, Аu. Сl, Тl. Сl и Рb. Сl 2). Основные хлориды гидролизу практически не подвергаются. • S + Cl 2 = SCl 2 (до 20 °C); 2 S + Cl 2 = S 2 Cl 2 (125 -130 °C) SCl 2 (темно-красн. жидк. ); S 2 Cl 2 (ж) S 100 Cl 2; SCl 4 (г). 2 SCl 2 = S 2 Cl 2 + Cl 2. S 2 Cl 2 - хороший растворитель 11 S 2 Cl 2 + 2 H 2 O = SO 2 + H 2 S + 2 HCl.
• Ионные хлориды (хлориды металлов) проявляют основные свойства, ковалентные хлориды (хлориды неметаллов) кислотные, например: Na. Cl Са. Cl 2 Al. Cl 3 (к) Si. Cl 4(ж) PCl 5(к) SCl 4(к) Тпл. , о. С. 800 772 193 – 70 159 ˃– 30 разл Кисл. -основн. св-ва основные амфот. кислотные Большинство хлоридов металлов хорошо растворимо в воде (за исключением Аg. Сl, Сu. Сl, Аu. Сl, Тl. Сl и Рb. Сl 2). Основные хлориды гидролизу практически не подвергаются. • S + Cl 2 = SCl 2 (до 20 °C); 2 S + Cl 2 = S 2 Cl 2 (125 -130 °C) SCl 2 (темно-красн. жидк. ); S 2 Cl 2 (ж) S 100 Cl 2; SCl 4 (г). 2 SCl 2 = S 2 Cl 2 + Cl 2. S 2 Cl 2 - хороший растворитель 11 S 2 Cl 2 + 2 H 2 O = SO 2 + H 2 S + 2 HCl.
 Хлор очень активно взаимодействует с фосфором 2 Р + 3 Сl 2 = 2 PCl 3 (ж); PCl 3 + Сl 2 = PCl 5 2 Р + 5 Сl 2 = 2 PCl 5 (кр) Галогениды фосфора необратимо гидролизуются (т. е. являются галогенангидридами соответствующих кислот): PCl 3 + 3 H 2 O = H 3 PO 3 + 3 HCl. PCl 5 + H 2 O = POCl 3 + 2 HCl; оксохлорид (III) фосфора: POCl 3 + 3 H 2 O = H 3 PO 4 + 3 HCl. Т. е. эти реакции могут служить и для получения HCl. 12
Хлор очень активно взаимодействует с фосфором 2 Р + 3 Сl 2 = 2 PCl 3 (ж); PCl 3 + Сl 2 = PCl 5 2 Р + 5 Сl 2 = 2 PCl 5 (кр) Галогениды фосфора необратимо гидролизуются (т. е. являются галогенангидридами соответствующих кислот): PCl 3 + 3 H 2 O = H 3 PO 3 + 3 HCl. PCl 5 + H 2 O = POCl 3 + 2 HCl; оксохлорид (III) фосфора: POCl 3 + 3 H 2 O = H 3 PO 4 + 3 HCl. Т. е. эти реакции могут служить и для получения HCl. 12
 • Кислотные хлориды гидролизуются полностью и необратимо с образованием кислот: Si. Сl 4 + 3 НОН = Н 2 Si. O 3 + 4 НСl Аl. Сl 3 + 3 НОН = Н 3 Аl. O 3 + 3 НСl • Различие свойств хлоридов разного типа проявляется также в реакциях их между собой, например: КСl + Аl. Сl 3 = К[Аl. Сl 4] основный кислотный • При этом основные хлориды (за счет ионов Сl) являются донорами электронных пар, а кислотные – акцепторами. • Амфотерные хлориды взаимодействуют как с 13 кислотными, так и с основными соединениями.
• Кислотные хлориды гидролизуются полностью и необратимо с образованием кислот: Si. Сl 4 + 3 НОН = Н 2 Si. O 3 + 4 НСl Аl. Сl 3 + 3 НОН = Н 3 Аl. O 3 + 3 НСl • Различие свойств хлоридов разного типа проявляется также в реакциях их между собой, например: КСl + Аl. Сl 3 = К[Аl. Сl 4] основный кислотный • При этом основные хлориды (за счет ионов Сl) являются донорами электронных пар, а кислотные – акцепторами. • Амфотерные хлориды взаимодействуют как с 13 кислотными, так и с основными соединениями.
 • Хлориды получают хлорированием простых веществ хлором или сухим хлоридом водорода: 2 Fе + 3 Сl 2 = 2 Fе. Сl 3 Fе + 2 НСl (г) = Fе. Сl 2 + Н 2 • взаимодействием оксидов с хлоридами (часто с ССl 4) либо с хлором в присутствии угля: Тi. O 2 + 2 Cl 2 + С = Тi. Сl 4 + СО 2 14
• Хлориды получают хлорированием простых веществ хлором или сухим хлоридом водорода: 2 Fе + 3 Сl 2 = 2 Fе. Сl 3 Fе + 2 НСl (г) = Fе. Сl 2 + Н 2 • взаимодействием оксидов с хлоридами (часто с ССl 4) либо с хлором в присутствии угля: Тi. O 2 + 2 Cl 2 + С = Тi. Сl 4 + СО 2 14
 • Большое применение в технике имеет хлорид водорода НСl. В обычный условиях НСl – бесцветный газ (Тпл. — 114, 2 °С, Ткип. — 84, 9 °С), В промышленности его получают синтезом из простых веществ: Н 2 (г) + Сl 2 (г) = 2 НСl (г), Go 298 = – 190 к. Дж/моль В лабораторных условиях Na. Cl + H 2 SO 4 = Na. HSO 4 + HCl (слабое нагревание) Na. Cl + Na. HSO 4 = Na 2 SO 4 + HCl (сильное нагревание) 15
• Большое применение в технике имеет хлорид водорода НСl. В обычный условиях НСl – бесцветный газ (Тпл. — 114, 2 °С, Ткип. — 84, 9 °С), В промышленности его получают синтезом из простых веществ: Н 2 (г) + Сl 2 (г) = 2 НСl (г), Go 298 = – 190 к. Дж/моль В лабораторных условиях Na. Cl + H 2 SO 4 = Na. HSO 4 + HCl (слабое нагревание) Na. Cl + Na. HSO 4 = Na 2 SO 4 + HCl (сильное нагревание) 15
 • Хлорид водорода очень хорошо поглощается водой (1 объем Н 2 О при 20°С поглощает около 450 объемов НСl). • Водный раствор НСl — сильная кислота, называемая соляной (хлороводородной = хлористоводородной). Как сильная кислота НСl находит широкое применение в технике, медицине, лабораторной практике и т. д. 16
• Хлорид водорода очень хорошо поглощается водой (1 объем Н 2 О при 20°С поглощает около 450 объемов НСl). • Водный раствор НСl — сильная кислота, называемая соляной (хлороводородной = хлористоводородной). Как сильная кислота НСl находит широкое применение в технике, медицине, лабораторной практике и т. д. 16
 • При действии сильных окислителей или при электролизе хлориды проявляют восстановительные свойства. Так, концентрированная соляная кислота проявляет восстановительные свойства при действии на нее оксида марганца (IV): Мn. O 2 + 4 НСl = Мn. Сl 2 + 2 Н 2 O • Этой реакцией пользуются в лаборатории для получения хлора. • При нагревании хлорид водорода окисляется кислородом (катализатор — Сu. Сl 2): 4 НСl (г) + О 2 (г) = 2 Н 2 О (г) + 2 Сl 2 (г). При небольшом нагревании реакция протекает слева направо, при более интенсивном нагреве 17 равновесие сместится справа налево.
• При действии сильных окислителей или при электролизе хлориды проявляют восстановительные свойства. Так, концентрированная соляная кислота проявляет восстановительные свойства при действии на нее оксида марганца (IV): Мn. O 2 + 4 НСl = Мn. Сl 2 + 2 Н 2 O • Этой реакцией пользуются в лаборатории для получения хлора. • При нагревании хлорид водорода окисляется кислородом (катализатор — Сu. Сl 2): 4 НСl (г) + О 2 (г) = 2 Н 2 О (г) + 2 Сl 2 (г). При небольшом нагревании реакция протекает слева направо, при более интенсивном нагреве 17 равновесие сместится справа налево.
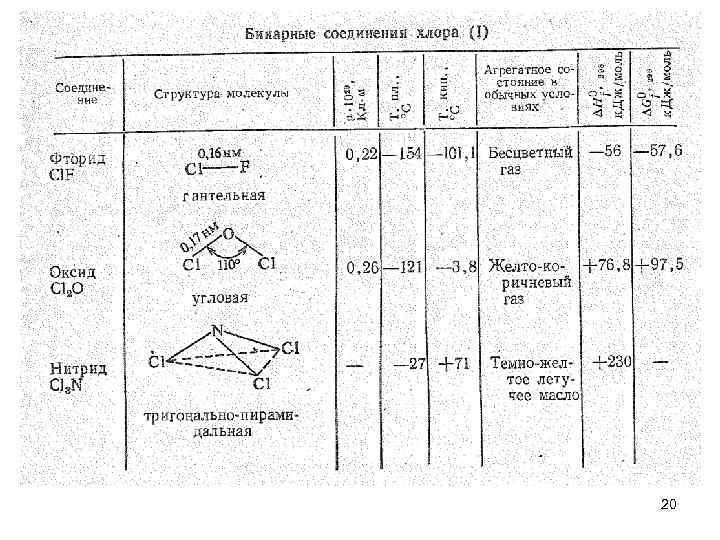
 • Соединения хлора (I). Степень окисления хлора +1 проявляется во фториде Сl. F, оксиде Сl 2 O и нитриде Сl 3 N, а также в соответствующих им сложных анионах [Сl. F 2]-, [Сl. О]- и [Сl. N]2 -. • Из бинарных соединений хлора (I) относительно устойчив лишь Сl. F — слабо экзотермическое соединение. Монофторид хлора образуется при нагревании сухих Сl 2 и F 2 выше 270 °С. • Нитрид Сl 3 N и оксид Сl 2 O — эндотермические соединения и неустойчивы. Оксид Сl 2 О распадается со взрывом на Сl 2 и O 2 при небольшом нагревании, при соприкосновении с органическими веществами и даже при переливании в жидком состоянии. 18
• Соединения хлора (I). Степень окисления хлора +1 проявляется во фториде Сl. F, оксиде Сl 2 O и нитриде Сl 3 N, а также в соответствующих им сложных анионах [Сl. F 2]-, [Сl. О]- и [Сl. N]2 -. • Из бинарных соединений хлора (I) относительно устойчив лишь Сl. F — слабо экзотермическое соединение. Монофторид хлора образуется при нагревании сухих Сl 2 и F 2 выше 270 °С. • Нитрид Сl 3 N и оксид Сl 2 O — эндотермические соединения и неустойчивы. Оксид Сl 2 О распадается со взрывом на Сl 2 и O 2 при небольшом нагревании, при соприкосновении с органическими веществами и даже при переливании в жидком состоянии. 18
 • Сl 2 O может быть получен по реакции: 0 o. C 2 Cl 2 + Hg. O = Cl 2 O + Hg. Cl 2 Сl 2 O (Тпл. -116 о. С, Ткип. 2 о. С) темножелтый газ, ядовит, может взрываться. Окислитель. 2 Сl 2 O + S = SO 2 + 2 Cl 2. • Может медленно разлагаться при н. у. 4 Сl 2 O → 2 Сl. O 2 + 3 Cl 2. Полученный оксид диспропорц. 2 Сl. O 2 + Н 2 О = НСl. O 2 + НСl. O 3 (в начальный момент). 2 Сl. O 2 + 2 Na. ОH = Na. Сl. O 2 + Na. Сl. O 3 + H 2 O t 19 3 Сl 2 O + 6 Na. OH = 2 Na. Cl. O 3 + 4 Na. Cl + H 2 O.
• Сl 2 O может быть получен по реакции: 0 o. C 2 Cl 2 + Hg. O = Cl 2 O + Hg. Cl 2 Сl 2 O (Тпл. -116 о. С, Ткип. 2 о. С) темножелтый газ, ядовит, может взрываться. Окислитель. 2 Сl 2 O + S = SO 2 + 2 Cl 2. • Может медленно разлагаться при н. у. 4 Сl 2 O → 2 Сl. O 2 + 3 Cl 2. Полученный оксид диспропорц. 2 Сl. O 2 + Н 2 О = НСl. O 2 + НСl. O 3 (в начальный момент). 2 Сl. O 2 + 2 Na. ОH = Na. Сl. O 2 + Na. Сl. O 3 + H 2 O t 19 3 Сl 2 O + 6 Na. OH = 2 Na. Cl. O 3 + 4 Na. Cl + H 2 O.
 20
20
 • Бинарные соединения хлора (I) имеют кислотный характер, что подтверждается например, их отношением к воде: • Сl 2 O + HOH = 2 НСl. О • Cl. F + HOH = НСl. О + НF • Cl 3 N + 3 НОН = HCl. O + H 3 N • Из производных оксохлорат (I)-аниона [Сl. O]-, называемых гипохлоритами относительно устойчивы соединения щелочных и щелочноземельных металлов. Гипохлориты этих элементов – соли, растворимые а воде. Их получают, пропуская хлор в охлаждаемые растворы щелочей. 21
• Бинарные соединения хлора (I) имеют кислотный характер, что подтверждается например, их отношением к воде: • Сl 2 O + HOH = 2 НСl. О • Cl. F + HOH = НСl. О + НF • Cl 3 N + 3 НОН = HCl. O + H 3 N • Из производных оксохлорат (I)-аниона [Сl. O]-, называемых гипохлоритами относительно устойчивы соединения щелочных и щелочноземельных металлов. Гипохлориты этих элементов – соли, растворимые а воде. Их получают, пропуская хлор в охлаждаемые растворы щелочей. 21
 • Оксохлорат (I) водорода НСl. О неустойчив и известен только в разбавленных растворах. Это хлорноватистая кислота; она образуется наряду с соляной при гидролизе хлора: Cl 2(р) + НOH Н+ (р) + Сl- (р) + НСl. O • При пропускании Cl 2 в воду, содержащую суспензированный оксид ртути можно получить раствор НСl. O 2 Cl 2 + Н 2 O + 2 Hg. O = Нg 2 OСl 2 + НСl. O (2 Hg. O + НСl = Сl–Hg–O–Hg–Сl + Н 2 O). 2 НСl. O Сl 2 O + H 2 O при действ. водоотн. ср-ва • Хлорноватистая кислота слабая, но сильный окислитель. 22
• Оксохлорат (I) водорода НСl. О неустойчив и известен только в разбавленных растворах. Это хлорноватистая кислота; она образуется наряду с соляной при гидролизе хлора: Cl 2(р) + НOH Н+ (р) + Сl- (р) + НСl. O • При пропускании Cl 2 в воду, содержащую суспензированный оксид ртути можно получить раствор НСl. O 2 Cl 2 + Н 2 O + 2 Hg. O = Нg 2 OСl 2 + НСl. O (2 Hg. O + НСl = Сl–Hg–O–Hg–Сl + Н 2 O). 2 НСl. O Сl 2 O + H 2 O при действ. водоотн. ср-ва • Хлорноватистая кислота слабая, но сильный окислитель. 22
 • При комнатной температуре в насыщенном водном растворе Cl 2 ~70% хлора находится в виде Cl 2. Добавление щелочи сдвигает равновесие вправо. При действии хлора на холодные растворы щелочей протекает реакция, в результате которой получается смесь хлорида и гипохлорида: Cl 2 + 2 KOH = KCl. O + KCl + H 2 O • В промышленности проводят реакции хлора с растворами КОН или Na. OH для получения раствора, называемого «жавелевой водой» , а также с Са(ОН)2 для получения смеси хлорида и гипохлорида кальция – «белильной извести» Са. Сl 2 Ca(OCl)2 (ее формулу часто записывают 23 Са. ОСl 2).
• При комнатной температуре в насыщенном водном растворе Cl 2 ~70% хлора находится в виде Cl 2. Добавление щелочи сдвигает равновесие вправо. При действии хлора на холодные растворы щелочей протекает реакция, в результате которой получается смесь хлорида и гипохлорида: Cl 2 + 2 KOH = KCl. O + KCl + H 2 O • В промышленности проводят реакции хлора с растворами КОН или Na. OH для получения раствора, называемого «жавелевой водой» , а также с Са(ОН)2 для получения смеси хлорида и гипохлорида кальция – «белильной извести» Са. Сl 2 Ca(OCl)2 (ее формулу часто записывают 23 Са. ОСl 2).
 • Вследствие малой стабильности НСl. O диспропорционирует: 2 НСl+1 O = НСl-1 + НСl+3 O 2 3 НСl +1 O = 2 НСl-1 + НСl+5 O 3 (при нагревании) h 2 НСl. O → 2 HCl + O 2 При действии водоотнимающего средства 2 НСl. O = Cl 2 О + H 2 O 24
• Вследствие малой стабильности НСl. O диспропорционирует: 2 НСl+1 O = НСl-1 + НСl+3 O 2 3 НСl +1 O = 2 НСl-1 + НСl+5 O 3 (при нагревании) h 2 НСl. O → 2 HCl + O 2 При действии водоотнимающего средства 2 НСl. O = Cl 2 О + H 2 O 24
 • Производные хлора (I) сильные окислители. Особенно агрессивен Сl. F, который реагирует с веществами еще более энергично, чем свободный фтор. На этом основано его применение в качестве фторирующего агента. • Гипохлориты применяются в качестве отбеливающего средства. Беление основано на окислении загрязняющих веществ хлорноватистой кислотой, которая из растворов гипохлоритов вытесняется угольной кислотой: Nа. Сl. О + Н 2 O + СО 2 = Nа. НСО 3 + НСl. О 25
• Производные хлора (I) сильные окислители. Особенно агрессивен Сl. F, который реагирует с веществами еще более энергично, чем свободный фтор. На этом основано его применение в качестве фторирующего агента. • Гипохлориты применяются в качестве отбеливающего средства. Беление основано на окислении загрязняющих веществ хлорноватистой кислотой, которая из растворов гипохлоритов вытесняется угольной кислотой: Nа. Сl. О + Н 2 O + СО 2 = Nа. НСО 3 + НСl. О 25
 • Соединения хлора (I) также склонны к реакциям диспропорционирования которые легче всего протекают у гипохлоритов: +1 -1 +5 3 КСl. О = 2 КСl + КСl. O 3 • Наибольший практический интерес (как отбеливающее средство, средство для дегазации, дешевый окислитель) представляет гипохлорит кальция Са(Сl. О)2. Получается он при взаимодействии хлора с гашеной известью: 2 Са(ОН)2 + Сl 2 = Са(Сl. О)2 + Са. Сl 2 + 2 Н 2 O 26
• Соединения хлора (I) также склонны к реакциям диспропорционирования которые легче всего протекают у гипохлоритов: +1 -1 +5 3 КСl. О = 2 КСl + КСl. O 3 • Наибольший практический интерес (как отбеливающее средство, средство для дегазации, дешевый окислитель) представляет гипохлорит кальция Са(Сl. О)2. Получается он при взаимодействии хлора с гашеной известью: 2 Са(ОН)2 + Сl 2 = Са(Сl. О)2 + Са. Сl 2 + 2 Н 2 O 26
 • Как видно из приведенного уравнения реакции, одновременно с Са(Сl. O)2 образуется Са. Сl 2, Поэтому получаемый в технике продукт — белильная или хлорная известь — можно рассматривать как смешанное соединение Са(Сl. О)Сl, т. е. гипохлорит — хлорид кальция. Содержание С 1+1 в белильной извести обычно устанавливают по количеству хлора, выделяемого при взаимодействии ее с соляной кислотой: +1 -1 0 Са(Сl. O)Сl + 2 НСl = Са. Сl 2 + Н 2 O 27
• Как видно из приведенного уравнения реакции, одновременно с Са(Сl. O)2 образуется Са. Сl 2, Поэтому получаемый в технике продукт — белильная или хлорная известь — можно рассматривать как смешанное соединение Са(Сl. О)Сl, т. е. гипохлорит — хлорид кальция. Содержание С 1+1 в белильной извести обычно устанавливают по количеству хлора, выделяемого при взаимодействии ее с соляной кислотой: +1 -1 0 Са(Сl. O)Сl + 2 НСl = Са. Сl 2 + Н 2 O 27
 • Соединения хлора (III). Степень окисления хлора +3 проявляется в трифториде Сl. F 3 и тетрафторохлорат (III)-анионе [Сl. F 4]-, а также в диоксохлорат (III)-анионе [Сl. О 2]-. Оксид хлора (III) Cl 2 O 3 неизвестен. • Производные [Сl. О 2]- -аниона называются хлоритами. Хлориты щелочных и щелочноземельных металлов представляют собой белые кристаллические вещества. 28
• Соединения хлора (III). Степень окисления хлора +3 проявляется в трифториде Сl. F 3 и тетрафторохлорат (III)-анионе [Сl. F 4]-, а также в диоксохлорат (III)-анионе [Сl. О 2]-. Оксид хлора (III) Cl 2 O 3 неизвестен. • Производные [Сl. О 2]- -аниона называются хлоритами. Хлориты щелочных и щелочноземельных металлов представляют собой белые кристаллические вещества. 28
 • Диоксохлорат (III) водорода НСl. О 2 в свободном состоянии не получен. Даже в водном растворе НСl. О 2 быстро разлагается. Раствор НСl. О 2 представляет собой кислоту средней силы (Киониз = 1 10 -2), называемой хлористой. • Разложение хлористой кислоты по реакции 4 HCl. O 2 = 2 Cl. O 2 + HCl. O 3 + HCl + H 2 O приводит к образованию диксида Cl. O 2 – желтобурого взрывчатого газа. 2 Na. Cl. O 3 + SO 2 + H 2 SO 4 = 2 Cl. O 2 + 2 Na. HSO 4 Молекула Cl+4 O 2 имеет треугольную структуру с атомом хлора в sp 2 -гибридизации, парамагнитна. 29
• Диоксохлорат (III) водорода НСl. О 2 в свободном состоянии не получен. Даже в водном растворе НСl. О 2 быстро разлагается. Раствор НСl. О 2 представляет собой кислоту средней силы (Киониз = 1 10 -2), называемой хлористой. • Разложение хлористой кислоты по реакции 4 HCl. O 2 = 2 Cl. O 2 + HCl. O 3 + HCl + H 2 O приводит к образованию диксида Cl. O 2 – желтобурого взрывчатого газа. 2 Na. Cl. O 3 + SO 2 + H 2 SO 4 = 2 Cl. O 2 + 2 Na. HSO 4 Молекула Cl+4 O 2 имеет треугольную структуру с атомом хлора в sp 2 -гибридизации, парамагнитна. 29
 • Поэтому в растворе (например ССl 4) имеет место его димеризация Cl 2 O 4. [Имеет структуру хлората (VII) хлора (I) Cl–О–Cl–О 3. ] 6 Cl. O 2 + 3 H 2 O 5 HCl. O 3 + HCl (на свету, медленно) 2 Cl. O 2 + 2 KOH KCl. O 2 + KCl. O 3 + Н 2 О (быстро) 2 Cl. O 2 + 2 О 3 2 О 2 + 2 Cl 2 O 6 (Cl+1 -O-Cl+7 O 3) • Наиболее практически важным хлоритом является Nа. Сl. O 2. Эту соль получают по реакции: 2 Сl. O 2 + Рb. О + 2 Nа. ОН = Рb. О 2 + 2 Nа. Сl. O 2 + Н 2 О • Выше 100 С разлагается в основном по схеме: 3 Nа. Сl. O 2 = 2 Nа. Сl. O 3 + Nа. Сl 30
• Поэтому в растворе (например ССl 4) имеет место его димеризация Cl 2 O 4. [Имеет структуру хлората (VII) хлора (I) Cl–О–Cl–О 3. ] 6 Cl. O 2 + 3 H 2 O 5 HCl. O 3 + HCl (на свету, медленно) 2 Cl. O 2 + 2 KOH KCl. O 2 + KCl. O 3 + Н 2 О (быстро) 2 Cl. O 2 + 2 О 3 2 О 2 + 2 Cl 2 O 6 (Cl+1 -O-Cl+7 O 3) • Наиболее практически важным хлоритом является Nа. Сl. O 2. Эту соль получают по реакции: 2 Сl. O 2 + Рb. О + 2 Nа. ОН = Рb. О 2 + 2 Nа. Сl. O 2 + Н 2 О • Выше 100 С разлагается в основном по схеме: 3 Nа. Сl. O 2 = 2 Nа. Сl. O 3 + Nа. Сl 30
 • Соединения хлора (V). Из соединений, в которых хлор проявляет степень окисления +5, известны пентафторид Cl. F 5, оксотрифторид Cl. OF 3, диоксофторид Cl. O 2 F и производные [Cl. O 3]- - триоксохлорат (V), [Cl. OF 4]- - оксотетрафторохлорат (V) и [Cl. O 3 F]2 - - триоксофторохлорат (V) – анионов. • Молекула Сl. F 5 имеет форму тетрагональной пирамиды. Пентафторид хлора - мало устойчивый газ (Tпл. – 93 °С, Tкип. – 13 о. С). Получают фторированием Сl. F 3 (при 350 °C и 25 МПа): Сl. F 3 + F 2 = Сl. F 5, Ho 298 = – 33, 4 к. Дж/моль Оксид хлора (V) Cl 2 O 5 неизвестен. 31
• Соединения хлора (V). Из соединений, в которых хлор проявляет степень окисления +5, известны пентафторид Cl. F 5, оксотрифторид Cl. OF 3, диоксофторид Cl. O 2 F и производные [Cl. O 3]- - триоксохлорат (V), [Cl. OF 4]- - оксотетрафторохлорат (V) и [Cl. O 3 F]2 - - триоксофторохлорат (V) – анионов. • Молекула Сl. F 5 имеет форму тетрагональной пирамиды. Пентафторид хлора - мало устойчивый газ (Tпл. – 93 °С, Tкип. – 13 о. С). Получают фторированием Сl. F 3 (при 350 °C и 25 МПа): Сl. F 3 + F 2 = Сl. F 5, Ho 298 = – 33, 4 к. Дж/моль Оксид хлора (V) Cl 2 O 5 неизвестен. 31
![• Производные [Cl. O 3]- - называются хлоратами. Из последних наибольшее практическое значение • Производные [Cl. O 3]- - называются хлоратами. Из последних наибольшее практическое значение](https://present5.com/presentation/-42637833_141829236/image-32.jpg) • Производные [Cl. O 3]- - называются хлоратами. Из последних наибольшее практическое значение имеет хлорат калия КСl. О 3 (бертолетова соль); его получают пропусканием хлора через горячий раствор КОН: 6 ОН- + 3 Сl 2 = 5 Cl- + Сl. O 3 - + 3 Н 2 О 0 -1 +5 6 КОН + 3 Cl 2 = 5 КCl + KCl. O 3 + 3 Н 2 O • или электролизом горячего раствора KCl. Поскольку КСl. O 3 мало растворим в воде, его легко отделяют от KCl охлаждением раствора. 32
• Производные [Cl. O 3]- - называются хлоратами. Из последних наибольшее практическое значение имеет хлорат калия КСl. О 3 (бертолетова соль); его получают пропусканием хлора через горячий раствор КОН: 6 ОН- + 3 Сl 2 = 5 Cl- + Сl. O 3 - + 3 Н 2 О 0 -1 +5 6 КОН + 3 Cl 2 = 5 КCl + KCl. O 3 + 3 Н 2 O • или электролизом горячего раствора KCl. Поскольку КСl. O 3 мало растворим в воде, его легко отделяют от KCl охлаждением раствора. 32
 • Триоксохлорат (V) водорода НСl. О 3 в свободном состоянии не выделен. Но (в отличие от НСl. O и НСl. О 2) известны его концентрированные (до 40%) водные растворы. Водных растворах НСl. О 3 сильная кислота, называемая хлорноватой. Ее обычно получают обменной реакцией: Ва(Сl. О 3)2(р) + Н 2 SО 4(р) = Ва. SО 4 (т) + НСl. O 3(р) • Хлорноватая кислота по свойствам напоминает HNО 3, в частности, ее смесь с соляной кислотой сильный окислитель (такого типа, как царская водка). 33
• Триоксохлорат (V) водорода НСl. О 3 в свободном состоянии не выделен. Но (в отличие от НСl. O и НСl. О 2) известны его концентрированные (до 40%) водные растворы. Водных растворах НСl. О 3 сильная кислота, называемая хлорноватой. Ее обычно получают обменной реакцией: Ва(Сl. О 3)2(р) + Н 2 SО 4(р) = Ва. SО 4 (т) + НСl. O 3(р) • Хлорноватая кислота по свойствам напоминает HNО 3, в частности, ее смесь с соляной кислотой сильный окислитель (такого типа, как царская водка). 33
 • При нагревании хлораты диспропорционируют (наряду с выделением кислорода происходит реакция): +5 +7 -1 4 КСl. O 3 = 3 KCl. O 4 + КСl а в присутствии катализатора распадаются с выделением кислорода: +5 -1 0 2 КСl. О 3 = 2 КСl + 3 О 2 При нагревании триоксохлораты (V) — сильные окислители. В смеси с восстановителями они образуют легко взрывающиеся составы. Бертолетову соль используют в производстве спичек и смеси для фейерверков. Хлорат натрия Nа. Сl. О 3 применяется в качестве средства для борьбы с сорняками. 34
• При нагревании хлораты диспропорционируют (наряду с выделением кислорода происходит реакция): +5 +7 -1 4 КСl. O 3 = 3 KCl. O 4 + КСl а в присутствии катализатора распадаются с выделением кислорода: +5 -1 0 2 КСl. О 3 = 2 КСl + 3 О 2 При нагревании триоксохлораты (V) — сильные окислители. В смеси с восстановителями они образуют легко взрывающиеся составы. Бертолетову соль используют в производстве спичек и смеси для фейерверков. Хлорат натрия Nа. Сl. О 3 применяется в качестве средства для борьбы с сорняками. 34
 • Соединения хлора (VII). Высшая степень Окисления хлора +7 проявляется в его оксиде, ряде оксофторидов и отвечающих им анионных комплексах; • Сl 2 O 7 Сl. O 3 F Сl. O 2 F 3 Cl. OF 5 (Cl. F 7) [Cl. O 4]- [Cl. O 3 F 2]- [Сl. O 2 F 4]- — • Оксид хлора (VII) Сl 2 O 7 — бесцветная жидкость (Tпл. -93, 4 °С, Tкип. +83 °С). Получается при нагревании смеси оксохлората (VII) водорода и оксида фосфора (V): 2 НСl. О 4 + Р 2 O 5 = Cl 2 O 7 + 2 НРО 3 35
• Соединения хлора (VII). Высшая степень Окисления хлора +7 проявляется в его оксиде, ряде оксофторидов и отвечающих им анионных комплексах; • Сl 2 O 7 Сl. O 3 F Сl. O 2 F 3 Cl. OF 5 (Cl. F 7) [Cl. O 4]- [Cl. O 3 F 2]- [Сl. O 2 F 4]- — • Оксид хлора (VII) Сl 2 O 7 — бесцветная жидкость (Tпл. -93, 4 °С, Tкип. +83 °С). Получается при нагревании смеси оксохлората (VII) водорода и оксида фосфора (V): 2 НСl. О 4 + Р 2 O 5 = Cl 2 O 7 + 2 НРО 3 35
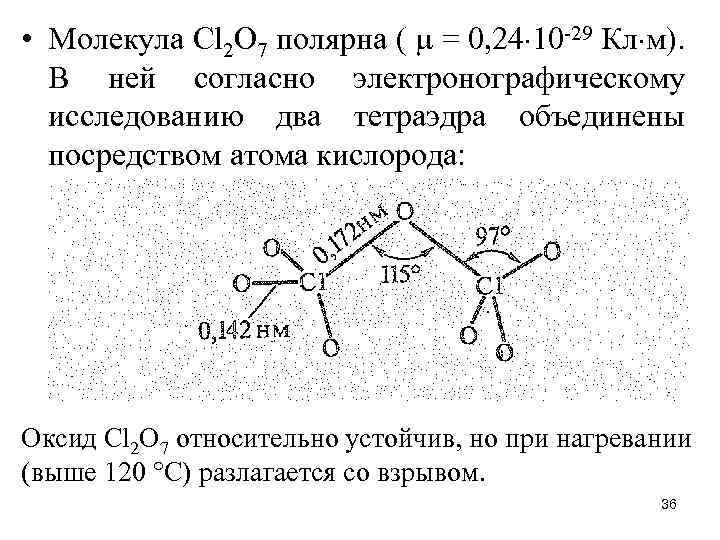 • Молекула Cl 2 O 7 полярна ( = 0, 24 10 -29 Кл м). В ней согласно электронографическому исследованию два тетраэдра объединены посредством атома кислорода: Оксид Cl 2 O 7 относительно устойчив, но при нагревании (выше 120 °С) разлагается со взрывом. 36
• Молекула Cl 2 O 7 полярна ( = 0, 24 10 -29 Кл м). В ней согласно электронографическому исследованию два тетраэдра объединены посредством атома кислорода: Оксид Cl 2 O 7 относительно устойчив, но при нагревании (выше 120 °С) разлагается со взрывом. 36
 • Тетраоксохлорат (VII)-ион Cl. O 4 - имеет тетраэдрическое строение, что в рамках теории валентных связей соответствует sp 3 – гибридизации валентных орбитаей атома хлора, стабилизированной за счет -связей. • Тетраоксохлораты (VII) (называемые еще перхлоратами) весьма многочисленны. Большинство их хорошо растворимо в воде. Тетраоксохлорат (VII) водорода НСl. O 4 бесцветная жидкость (Tпл. – 102 °С), способная взрываться. 37
• Тетраоксохлорат (VII)-ион Cl. O 4 - имеет тетраэдрическое строение, что в рамках теории валентных связей соответствует sp 3 – гибридизации валентных орбитаей атома хлора, стабилизированной за счет -связей. • Тетраоксохлораты (VII) (называемые еще перхлоратами) весьма многочисленны. Большинство их хорошо растворимо в воде. Тетраоксохлорат (VII) водорода НСl. O 4 бесцветная жидкость (Tпл. – 102 °С), способная взрываться. 37
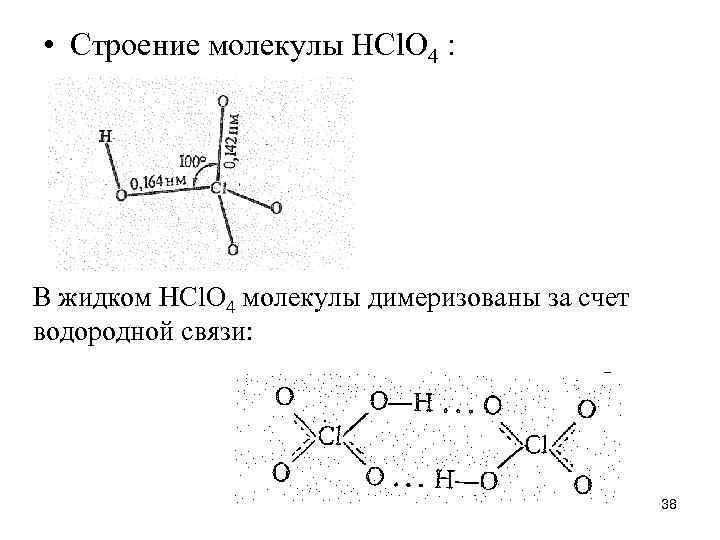 • Строение молекулы НСl. О 4 : В жидком НСl. О 4 молекулы димеризованы за счет водородной связи: 38
• Строение молекулы НСl. О 4 : В жидком НСl. О 4 молекулы димеризованы за счет водородной связи: 38
 • Растворы кислоты вполне устойчивы. Хлорная кислота одна из наиболее сильных кислот, Ее получают действием концентрированной Н 2 SO 4 на КСl. O 4 : (4 КСl. O 3 = 3 KCl. O 4 + КСl при нагревании) КСl. O 4 + Н 2 SО 4 = НСl. O 4 + КНSO 4. Безводная НСl. O 4 – очень сильный окислитель. При нагревании легко разлагается: 4 НСl. O 4 = 4 Сl. O 2 + 3 O 2 + 2 H 2 O. • Известны многочисленные оксохлораты (VII). Наибольшее значение имеет КСl. О 4. Его получают электролизом раствора КСl. О 3. Перхлораты в основном применяются в производстве взрывчатых веществ в реактивной технике. 39
• Растворы кислоты вполне устойчивы. Хлорная кислота одна из наиболее сильных кислот, Ее получают действием концентрированной Н 2 SO 4 на КСl. O 4 : (4 КСl. O 3 = 3 KCl. O 4 + КСl при нагревании) КСl. O 4 + Н 2 SО 4 = НСl. O 4 + КНSO 4. Безводная НСl. O 4 – очень сильный окислитель. При нагревании легко разлагается: 4 НСl. O 4 = 4 Сl. O 2 + 3 O 2 + 2 H 2 O. • Известны многочисленные оксохлораты (VII). Наибольшее значение имеет КСl. О 4. Его получают электролизом раствора КСl. О 3. Перхлораты в основном применяются в производстве взрывчатых веществ в реактивной технике. 39
 • В ряду Сl. O-—Cl. О 2 -—Сl. О 3 -—Сl. O 4 - по мере увеличения степени окисления хлора устойчивость анионов возрастает. Это можно объяснить тем, что при переходе от Сl. O- к Сl. O 4 - увеличивается число электронов, принимающих участие в образовании связей. Особо устойчив ион Сl. O 4 -, в котором все валентные электроны атома хлора принимают участие в образовании связей. 40
• В ряду Сl. O-—Cl. О 2 -—Сl. О 3 -—Сl. O 4 - по мере увеличения степени окисления хлора устойчивость анионов возрастает. Это можно объяснить тем, что при переходе от Сl. O- к Сl. O 4 - увеличивается число электронов, принимающих участие в образовании связей. Особо устойчив ион Сl. O 4 -, в котором все валентные электроны атома хлора принимают участие в образовании связей. 40
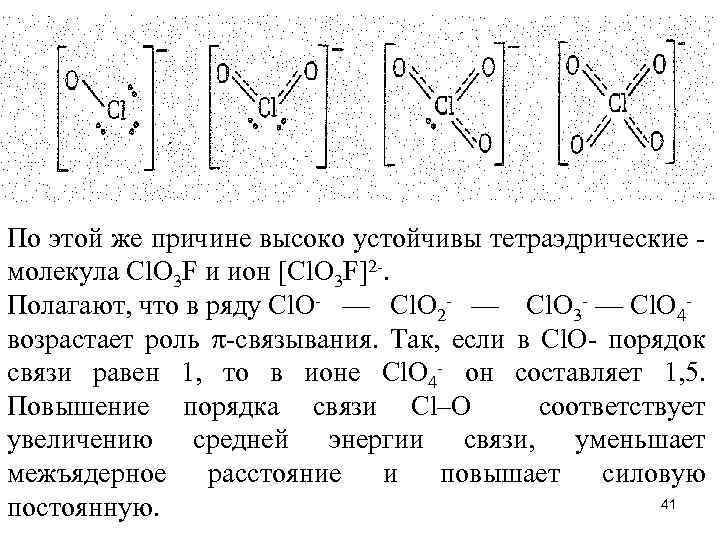 По этой же причине высоко устойчивы тетраэдрические - молекула Сl. О 3 F и ион [Сl. О 3 F]2 -. Полагают, что в ряду Сl. O- — Cl. О 2 - — Сl. О 3 - — Сl. O 4 - возрастает роль -связывания. Так, если в Сl. О- порядок связи равен 1, то в ионе Сl. О 4 - он составляет 1, 5. Повышение порядка связи Сl–О соответствует увеличению средней энергии связи, уменьшает межъядерное расстояние и повышает силовую 41 постоянную.
По этой же причине высоко устойчивы тетраэдрические - молекула Сl. О 3 F и ион [Сl. О 3 F]2 -. Полагают, что в ряду Сl. O- — Cl. О 2 - — Сl. О 3 - — Сl. O 4 - возрастает роль -связывания. Так, если в Сl. О- порядок связи равен 1, то в ионе Сl. О 4 - он составляет 1, 5. Повышение порядка связи Сl–О соответствует увеличению средней энергии связи, уменьшает межъядерное расстояние и повышает силовую 41 постоянную.
 • Вследствие повышения устойчивости в ряду Сl. O-—Cl. О 2 -—Сl. О 3 -—Сl. O 4 уменьшается окислительная активность. • Так, гипохлориты вступают в окислительновосстановительное взаимодействие в любой среде. Хлораты - в растворах окисляют только в сильно кислой среде. Окислительная же способность иона Сl. О 4 - в растворах практически не проявляется при н. у. (увеличивается при нагревании). • По мере увеличения степени окисления хлора в ряду НСl. O — НCl. О 2 — НСl. О 3 — НСl. O 4 сила кислот возрастает. 42
• Вследствие повышения устойчивости в ряду Сl. O-—Cl. О 2 -—Сl. О 3 -—Сl. O 4 уменьшается окислительная активность. • Так, гипохлориты вступают в окислительновосстановительное взаимодействие в любой среде. Хлораты - в растворах окисляют только в сильно кислой среде. Окислительная же способность иона Сl. О 4 - в растворах практически не проявляется при н. у. (увеличивается при нагревании). • По мере увеличения степени окисления хлора в ряду НСl. O — НCl. О 2 — НСl. О 3 — НСl. O 4 сила кислот возрастает. 42
 • Этот факт можно объяснить тем, что по мере увеличения числа атомов кислорода в ряду Сl. O - —Cl. О - — Сl. O - прочность связи О— 2 3 4 Н с определенным атомом кислорода ослабевает. • Соединения хлора (II), (IV) и (VI). Можно считать, что степень окисления +4 и +6 хлор проявляет следующих оксидах: Сl. О 2, Сl 2 О 4 (Cl– О–Cl–О 3), Сl. О 3, Сl 2 О 6 (O 2 Cl+5 -O-Cl+7 O 3). • В обычных условиях диоксид хлора Сl. О 2 зеленовато-желтый газ (Тпл. -59 °С, Ткип. 9, 9 °С) с резким запахом. 43
• Этот факт можно объяснить тем, что по мере увеличения числа атомов кислорода в ряду Сl. O - —Cl. О - — Сl. O - прочность связи О— 2 3 4 Н с определенным атомом кислорода ослабевает. • Соединения хлора (II), (IV) и (VI). Можно считать, что степень окисления +4 и +6 хлор проявляет следующих оксидах: Сl. О 2, Сl 2 О 4 (Cl– О–Cl–О 3), Сl. О 3, Сl 2 О 6 (O 2 Cl+5 -O-Cl+7 O 3). • В обычных условиях диоксид хлора Сl. О 2 зеленовато-желтый газ (Тпл. -59 °С, Ткип. 9, 9 °С) с резким запахом. 43
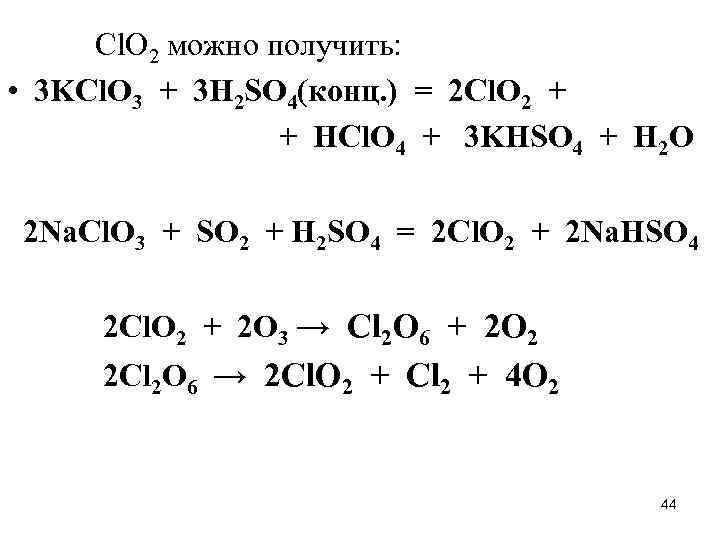 Cl. O 2 можно получить: • 3 KCl. O 3 + 3 H 2 SO 4(конц. ) = 2 Cl. O 2 + + HCl. O 4 + 3 KHSO 4 + H 2 O 2 Na. Сl. O 3 + SO 2 + H 2 SO 4 = 2 Cl. O 2 + 2 Na. HSO 4 2 Cl. O 2 + 2 O 3 → Cl 2 O 6 + 2 O 2 2 Cl 2 O 6 → 2 Cl. O 2 + Cl 2 + 4 O 2 44
Cl. O 2 можно получить: • 3 KCl. O 3 + 3 H 2 SO 4(конц. ) = 2 Cl. O 2 + + HCl. O 4 + 3 KHSO 4 + H 2 O 2 Na. Сl. O 3 + SO 2 + H 2 SO 4 = 2 Cl. O 2 + 2 Na. HSO 4 2 Cl. O 2 + 2 O 3 → Cl 2 O 6 + 2 O 2 2 Cl 2 O 6 → 2 Cl. O 2 + Cl 2 + 4 O 2 44
 • Молекула Сl. О 2 имеет угловую форму ( ОСl. О = 118°, d. Cl. O = 0, 148 нм), поэтому она полярна • Молекула парамагнитна, так как имеет нечетное число элементов. • Таким образом, Сl. О 2 — валентно-ненасыщенное соединение; в нем заложена тенденция к присоединению или потере одного электрона: +4 +3 +4 +5 • Сl. О 2 + е = Сl. О 2 - ; Сl. О 2 - е = Сl. О 2+ 45
• Молекула Сl. О 2 имеет угловую форму ( ОСl. О = 118°, d. Cl. O = 0, 148 нм), поэтому она полярна • Молекула парамагнитна, так как имеет нечетное число элементов. • Таким образом, Сl. О 2 — валентно-ненасыщенное соединение; в нем заложена тенденция к присоединению или потере одного электрона: +4 +3 +4 +5 • Сl. О 2 + е = Сl. О 2 - ; Сl. О 2 - е = Сl. О 2+ 45
 • Тенденция к присоединению и потере электрона легче всего реализуется при диспропорционировании Сl. О 2 в водных (в особенности в щелочных) растворах: +4 +3 +5 2 Сl. О 2 + 2 ОН- = Сl. О 2 - + Сl. О 3 - + Н 2 O • При этом образуются две кислоты (или две соли). • Диоксид хлора постепенно разлагается на свету. • При небольшом нагревании, ударе или соприкосновении с горючими веществами Сl. O 2 разлагается со взрывом. 46
• Тенденция к присоединению и потере электрона легче всего реализуется при диспропорционировании Сl. О 2 в водных (в особенности в щелочных) растворах: +4 +3 +5 2 Сl. О 2 + 2 ОН- = Сl. О 2 - + Сl. О 3 - + Н 2 O • При этом образуются две кислоты (или две соли). • Диоксид хлора постепенно разлагается на свету. • При небольшом нагревании, ударе или соприкосновении с горючими веществами Сl. O 2 разлагается со взрывом. 46
 • Оксид Сl 2 О 4 имеет структуру хлората (VII) хлора (I) Сl—О—Сl. О 3. Это светло -желтая жидкость (Tкип. 44, 5 °С). 47
• Оксид Сl 2 О 4 имеет структуру хлората (VII) хлора (I) Сl—О—Сl. О 3. Это светло -желтая жидкость (Tкип. 44, 5 °С). 47
 • Диоксид хлора взаимодействует с озоном, давая триоксид Cl. O 3 Cl. O 2 + О 3 = Cl. O 3 + О 2 • Триоксид хлора Сl. О 3 — неустойчивый короткоживущий радикал, обнаружен методом ЭПР и легко димеризуется. (Cl. O 3 – парамагнитен). • Оксид Сl 2 О 6 в обычных условиях — темно-красная маслообразная жидкость, замерзающая при +3 °С. Полагают, что его молекула имеет несимметричную +5 +7 структуру O 2 Сl—О—Сl. О 3. В кристаллическом состоянии имеет ионное строение — построен из ионов Сl. О 2+ и Сl. О 4 -. 48
• Диоксид хлора взаимодействует с озоном, давая триоксид Cl. O 3 Cl. O 2 + О 3 = Cl. O 3 + О 2 • Триоксид хлора Сl. О 3 — неустойчивый короткоживущий радикал, обнаружен методом ЭПР и легко димеризуется. (Cl. O 3 – парамагнитен). • Оксид Сl 2 О 6 в обычных условиях — темно-красная маслообразная жидкость, замерзающая при +3 °С. Полагают, что его молекула имеет несимметричную +5 +7 структуру O 2 Сl—О—Сl. О 3. В кристаллическом состоянии имеет ионное строение — построен из ионов Сl. О 2+ и Сl. О 4 -. 48
 • При обычных температурах Сl 2 О 6 постепенно разлагается. Энергично взаимодействует с водой, образуя за счет диспропорционирования хлорноватую и хлорную кислоты: +5 +7 +5 +7 Сl 2 О 6 (O 2 Сl—О—Сl. О 3)+НОН= НСl. О 3 + НСl. О 4 • Т. е. Cl 2 O 6 является смешанным оксидом хлорноватой НCl. O 3 и хлорной кислот НCl. O 4. • При соприкосновении с органическими веществами Сl 2 О 6 взрывается. 49
• При обычных температурах Сl 2 О 6 постепенно разлагается. Энергично взаимодействует с водой, образуя за счет диспропорционирования хлорноватую и хлорную кислоты: +5 +7 +5 +7 Сl 2 О 6 (O 2 Сl—О—Сl. О 3)+НОН= НСl. О 3 + НСl. О 4 • Т. е. Cl 2 O 6 является смешанным оксидом хлорноватой НCl. O 3 и хлорной кислот НCl. O 4. • При соприкосновении с органическими веществами Сl 2 О 6 взрывается. 49
 • Ст. окисл. -1 +1 +4 +6 +7 • Ф-ла OF 2 Cl 2 O Cl. O 2 Cl 2 O 6 Cl 2 O 7 • Агр. сост. газ жид. при н. у. желт. (<10 о. С) темно- бесцв. бурый красная Тпл. о. С -240 -116 -59 3, 5 -90 f. Ho 298, к. Дж/моль 25 79 105 - 251 усиление окислительной активности 50
• Ст. окисл. -1 +1 +4 +6 +7 • Ф-ла OF 2 Cl 2 O Cl. O 2 Cl 2 O 6 Cl 2 O 7 • Агр. сост. газ жид. при н. у. желт. (<10 о. С) темно- бесцв. бурый красная Тпл. о. С -240 -116 -59 3, 5 -90 f. Ho 298, к. Дж/моль 25 79 105 - 251 усиление окислительной активности 50


