ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ГЛАУКОМЫ.ppt
- Количество слайдов: 65

ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ГЛАУКОМЫ Безуглый М. Б. Кафедра глазных болезней ЗМАПО

Антиглаукоматозные операции A. Graefe предложил в 1857 г. первую антиглаукоматозную операцию – иридотомию, которая была практически единственной в течение почти 50 лет. Благодаря работам F. Lagrange и R. Elliot (1906, 1909) в хирургическом лечении глаукомы ведущее положение заняли фистулизирующие операции J. Cairns - 60 -е годы прошлого столетия – трабекулэктомия

Механизм гипотензивного действия антиглаукоматозных операций Увеличение легкости оттока водянистой влаги Уменьшение продукции водянистой влаги Операции второго типа иногда называют циклодеструктивными, поскольку при их выполнении термическое или лазерное воздействие оказывается на отростки цилиарного тела, вызывая гибель части

Операции улучшающие отток ВГЖ Операции фильтрующего типа (трабекулэктомия, синусотрабекулэктомия) «Золотой стандарт» в хирургическом лечении глаукомы (R. Hitchings )

высокий процент интра- и послеоперационных осложнений Гипотония Цилиохориоидальная отслойка (ЦХО) Гифема Макулопатия Прогрессирование катаракты Формирование кистозных фильтрационных подушечек - потенциальных входных ворот для инфекции и т. п.

Антиглаукоматозные операции Непроникающая хирургия глаукомы: 1964 г. , М. М. Краснов – синусотомия 1987 г. , С. Н. Федоров, В. И. Козлов – непроникающая глубокая склерэктомия (НГСЭ)

Механизм действия НГСЭ усиление оттока влаги через неповрежденный трабекулярный аппарат после удаления наружной стенки шлеммова канала, создание принципиально нового пути фильтрации – через дистальные отделы освобожденной десцеметовой мембраны

Недостатки непроникающей хирургии: технические сложности при выполнении основного этапа операции – выкраивания, отсепаровки от десцеметовой мембраны и удаления корнеосклеральной ткани с задней стенкой шлеммова канала непродолжительный гипотензивный эффект

Основная проблема непроникающей хирургии Недостаточно стойкий гипотензивный эффект операции

Отсутствие компенсации ВГД в отдаленном периоде после НГСЭ Без дополнительных лазерных вмешательств и назначения гипотензивных препаратов: 6 – 11 % (В. И. Козлов, С. Н. Федоров, 1991) 21, 2 % через 44 месяца (T. Shaarawy et all. , 2004) 73, 5 % (Х. П. Тахчиди с соавт. , 2003)

Уровни блокад хирургически сформированных путей оттока ВГЖ (Х. П. Тахчиди) блокада фильтрующей зоны корнем радужки (8 – 19%) блокада на уровне десцеметовой мембраны и трабекулы (16 – 69%) блокада на уровне глубоких и средних слоев склеры (до 20%) блокада на уровне эписклеры и теноновой оболочки (6 – 29%) блокада на уровне конъюнктивы (до

непроникающих антиглаукоматозных вмешательств Избыточное развитие рубцовых процессов в зоне фильтрации

Пути решения данной проблемы: Импланты, улучшающие дренажные функции (коллагеновые, гидрогелевые и т. д. ) Интра- и послеоперационное введение антиметаболитов и цитостатиков (митомицин-С, 5 фторурацил) Применение комплекса цитокинов ( «Суперлимф» ) Усовершенствование хирургической

Полимерные дренажи В 1969 г. A. Molteno предложил использовать имплантат, представляющий собой трубочку, соединяющую переднюю камеру с эписклеральной полостью, сформированной над имплантированной под конъюнктиву акриловой пластинкой. Ко второй группе имплантов относятся линейные монолитные (неполые) дренажи, которые нашли широкое применение при непроникающих операциях

Механизм действия имплантов в основном сводится к увеличению объема интрасклеральной полости, в которую осуществляется отток влаги и предотвращению вторичной адгезии наружного склерального лоскута Основными материалами для изготовления дренажей являются коллаген и его сополимеры, полиакриламид, полигидроксиэтилметакрилат, силикон, непористый политетрафторэтилен, гиалуронат

Антиметаболиты Митомицин-С – аппликация на склеральное ложе после выкраивания поверхностного склерального лоскута в течение 2, 5 – 3 минут 5 -фторурацил - субконъюнктивально в дозе по 5 мг с 5 – 7 суток после операции с интервалом от 1 до 5 дней в суммарной дозе 15 – 40 мг на курс (3 – 8 инъекций)

Модификации хирургической техники Иссечение теноновой капсулы, ее отсепаровка на гидравлической подушке, интраоперационное формирование ФП (Ю. Н. Кондратенко, Л. А. Федоров) Интрасаклеральное микродренирование (П. И. Лебехов) и его комбинация с НГСЭ (В. В. Науменко с соавт. ) Проведение лазерной трабекулотомии вторым этапом после НГСЭ (Н. М. Сергиенко, Ю. Н. Кондратенко) Микроинвазивная НГСЭ (Х. П. Тахчиди с

Цель работы: Повышение эффективности НГСЭ путем модификации техники операции и клиническая оценка отсроченных результатов ее применения у больных первичной открытоугольной глаукомой

Украины на полезную модель № 5542 «Способ хирургическог о лечения первичной открытоуголь ной глаукомы» , 2004 г.
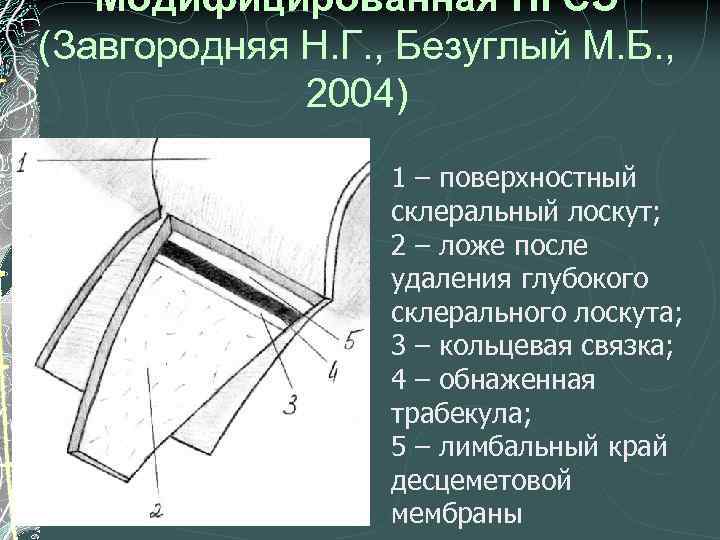
Модифицированная НГСЭ (Завгородняя Н. Г. , Безуглый М. Б. , 2004) 1 – поверхностный склеральный лоскут; 2 – ложе после удаления глубокого склерального лоскута; 3 – кольцевая связка; 4 – обнаженная трабекула; 5 – лимбальный край десцеметовой мембраны

Модифицированная НГСЭ (Завгородняя Н. Г. , Безуглый М. Б. , 2004) 1 – поверхностный склеральный лоскут; 2 – ложе после удаления глубокого склерального лоскута

Материалы и методы Основная группа – Модифицированная НГСЭ: 67 больных с ПОУГ (71 глаз) 42 мужчины (62, 7%) 33 женщины (37, 3 %) Средний возраст 65, 5 ± 7, 3 лет Контрольная группа – «классическая» НГСЭ 20 больных, 20 глаз

ОБСЛЕДОВАНИЕ: Визометрия Динамическая сферопериметрия Тонография по СРОКИ НАБЛЮДЕНИЯ: Нестерову 1, 2 недели, 1, 3, 6, 12, 18, 24 месяца после операции

Исходное распределение глаз по стадиям ПОУГ Основная группа Контрольная группа
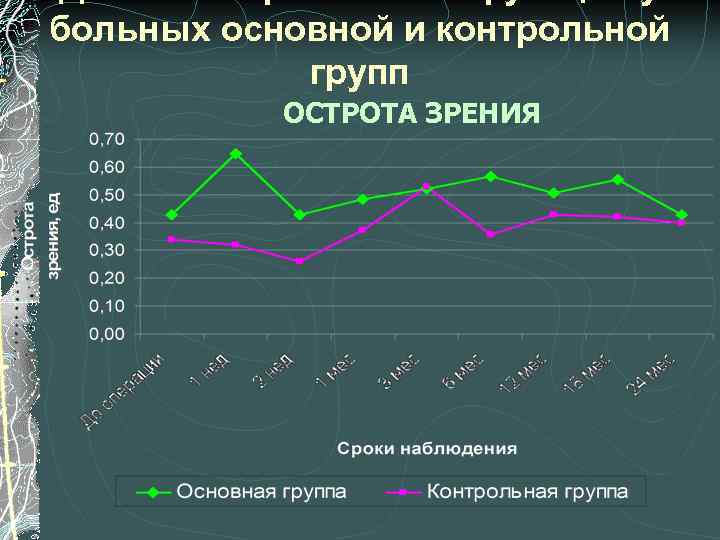
больных основной и контрольной групп ОСТРОТА ЗРЕНИЯ
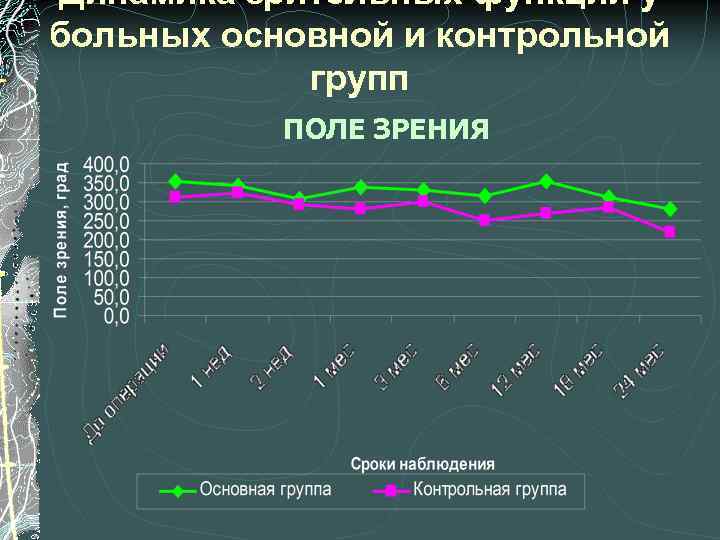
Динамика зрительных функций у больных основной и контрольной групп ПОЛЕ ЗРЕНИЯ
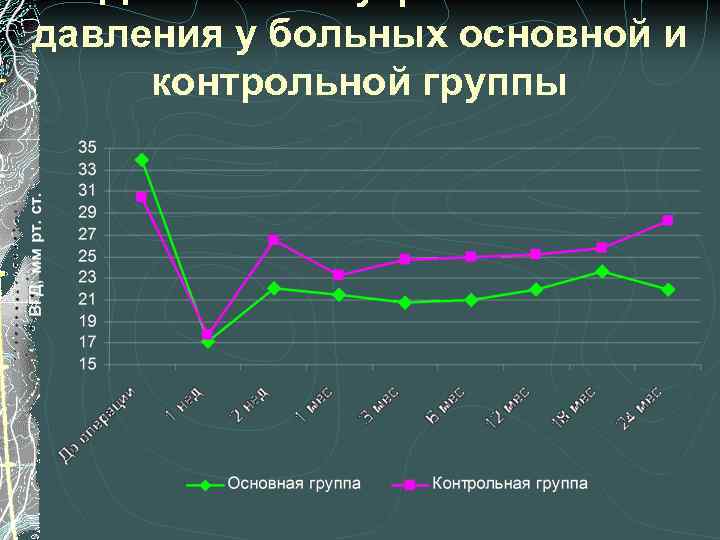
давления у больных основной и контрольной группы
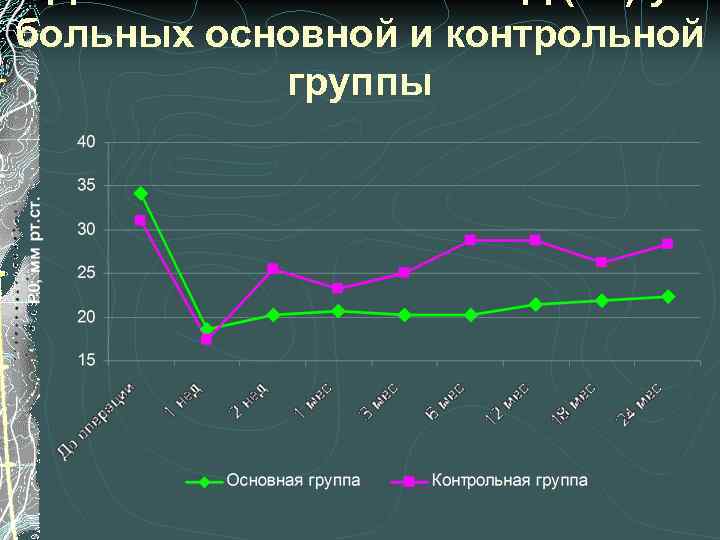
больных основной и контрольной группы
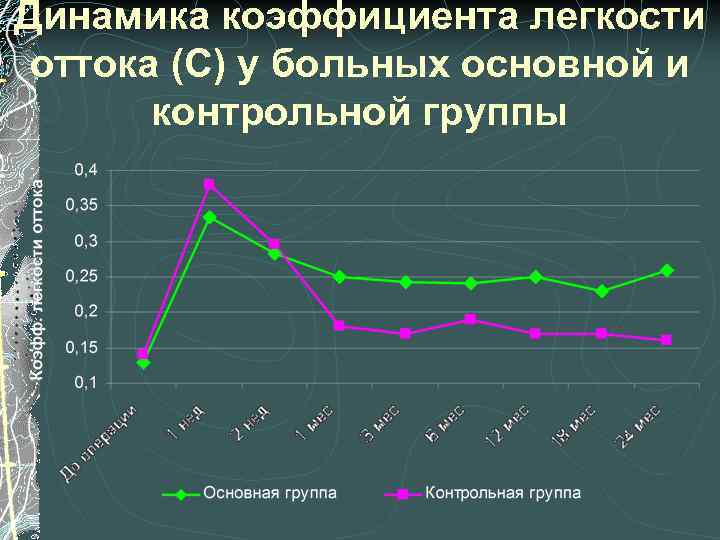
Динамика коэффициента легкости оттока (С) у больных основной и контрольной группы
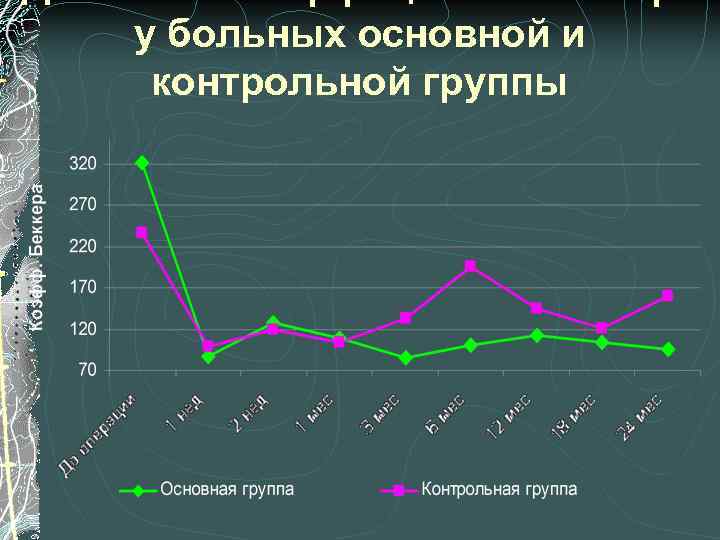
у больных основной и контрольной группы

Эффективность модифицированной НГСЭ В раннем послеоперационном периоде обе группы показали удовлетворительные результаты в плане компенсации ВГД В сроке наблюдения 3 – 6 мес на 24 глазу (33, 8%) основной и 9 глазах (45%) контрольной группы отмечено повышение ВГД > 26 мм рт. ст. , что потребовало проведения дополнительных лазерных вмешательств (трабекулотомия, десцеметогониопунктура) и в некоторых случаях назначения местных гипотензивных препаратов

Эффективность модифицированной НГСЭ Анализ среднестатистических показателей гидродинамики выявил, что в основной группе, где формирование лоскута при выполнении НГСЭ выполнялось в нашей модификации, уровень ВГД и истинного офтальмотонуса был достоверно ниже, а коэффициент легкости оттока – достоверно выше чем в контроле на протяжении всего срока наблюдения (2 года)

послеоперационном периоде (в сроке 24 месяца после операции): Основная группа Без дополнительных лазерных вмешательств и гипотензивных препаратов – 47 глаз (66, 2%) После дополнит. лазерных вмешательств (лазерн. трабекулотомия, десцеметогониопунктура) – 69 глаз (97, 2 %) После лазерных вмешательств с добавлением местных гипотензивных препаратов – 71 глаз (100%) Контрольная группа Без дополнительных лазерных вмешательств и гипотензивных препаратов – 11 глаз (55%) После дополнит. лазерных вмешательств (лазерн. трабекулотомия, десцеметогониопунктура) – 15 глаз (75 %) После лазерных вмешательств с добавлением местных гипотензивных препаратов – 18 глаз (90%) На 2 глазах (10%) потребовались повторные антиглаукоматозные операции

Осложнения: Основная группа Микроперфорация корнеосклеральной пластинки или трабекулы – 9 глаз (12, 7%) Отслойка сосудистой оболочки – 10 глаз (14, 1%) Гифема в виде взвеси форменных элементов– 4 глаза (5, 6%) Контрольная группа Микроперфорация корнеосклеральной пластинки или трабекулы – 3 глаза (15%) Отслойка сосудистой оболочки – 3 глаза (15%) Гифема в виде взвеси форменных элементов– 1 глаз (5%)

ВЫВОДЫ: 1. Предложенный способ формирования глубокого склерального лоскута при НГСЭ препятствует избыточному рубцеванию путей оттока камерной влаги в послеоперационном периоде и значительно повышает эффективность хирургического вмешательства при ПОУГ. 2. Предлагаемый способ не требует специального дорогостоящего оборудования и расходных материалов и может быть применен в условиях любого специализированного глазного стационара.

ВЫВОДЫ: 3. Выполнение операции довольно несложно в техническом плане, для ее проведения не требуется применение антиметаболитов и цитостатиков, что снижает риск развития тяжелых осложнений. Кроме того, нет необходимости введения в зону фильтрации полимерных дренажей, повышающих риск аллергизации организма

Вискоканалостомия (R. Stegmann, 1998) Вмешательство состоит из сочетания НГСЭ и введения в шлеммов канал вискоэластика высокой плотности (Healon®), инъекция которого увеличивает диаметр шлеммова канала от 30 до 150 мкм и предотвращает коллапс его стенок введение вискоэластика препятствует полимеризации фибриногена в фибрин и фибринозной реакции, которая может

Недостатки вискоканалостомии: возможность повышения ВГД в раннем послеоперационном периоде вследствие блокирования вискоэластиком вновь созданных путей оттока возможность закрытия просвета шлеммова канала фибробластами и фибрином новое осложнение – отслойка

Лазерное лечение глаукомы Лазерные операции в настоящее время представляют собой самостоятельное направление в комплексе современных лечебных мероприятий при глаукоме Краснов М. М. впервые в мире в 1972 г. предложил способ «безножевого» лечения первичной открытоугольной глаукомы, получивший название «Лазерная гониопунктура по Краснову»

ЛАЗЕРНЫЕ ОПЕРАЦИИ В ЛЕЧЕНИИ ГЛАУКОМЫ 1. 2. Операции, направленные на увеличение доступности корнеосклеральной трабекулы при узкоугольной глаукоме, функциональном блоке УПК, зрачковом блоке с бомбажем радужки, пигментной глаукоме Операции, направленные на улучшение оттока водянистой влаги через трабекулярную ткань в шлеммов канал

ЛАЗЕРНЫЕ ОПЕРАЦИИ В ЛЕЧЕНИИ ГЛАУКОМЫ 3. Фистулизирующие операции (эксимерлазерная непроникающая глубокая склерэктомия, склероперфорирующие воздействия) 4. Циклодеструктивные операции при далеко зашедших болящих формах глаукомы

ЛАЗЕРНЫЕ ОПЕРАЦИИ В ЛЕЧЕНИИ ГЛАУКОМЫ МЕТОДЫ: метод лезерной фотокоагуляции (или термического повреждения) метод лазерной фотодеструкции (или механического разрушения) биологических тканей

ЛАЗЕРНЫЕ ОПЕРАЦИИ В ЛЕЧЕНИИ ГЛАУКОМЫ Лазерная фотокоагуляция Лазеры с непрерывным излучением Выраженный термический эффект Трансформация энергии света в тепловую энергию Повышение локальной температуры тканей

ЛАЗЕРНЫЕ ОПЕРАЦИИ В ЛЕЧЕНИИ ГЛАУКОМЫ Лазерная фотодеструкция Импульсные лазеры очень больших энергий, но с малой продолжительностью импульса (миллионные доли секунды) Пятно 15 – 25 мкм За время короткого лазерного импульса окружающая ткань не «успевает» нагреться В точке воздействия ткань «испаряется» , образуется облачко ионизированной плазмы

ЛАЗЕРНЫЕ ОПЕРАЦИИ В ЛЕЧЕНИИ ГЛАУКОМЫ Лазерная иридэктомия (иридотомия) Показания: Гиперволемический тип первичной глаукомы - закрытоугольной - открытоугольной с узким вследствие функционального зрачкового блока УПК

Лазерная иридэктомия Nd: YAG лазер «Optimis» фирмы QUANTEL MEDICAL (Франция) Длина волны 1064 нм электрооптический "пробой" ткани вследствие образования плазмы, которая создает ударную волну в точке воздействия и приводит к микроразрыву ткани

Лазерная иридэктомия ПАРАМЕТРЫ базальные колобомы в количестве 3 – 4 в прикорневой зоне радужной оболочки в меридианах 4, 8, 12 или 2, 4, 8, 10 часов импульсы одиночные энергия в импульсе: 5 – 10 м. Дж
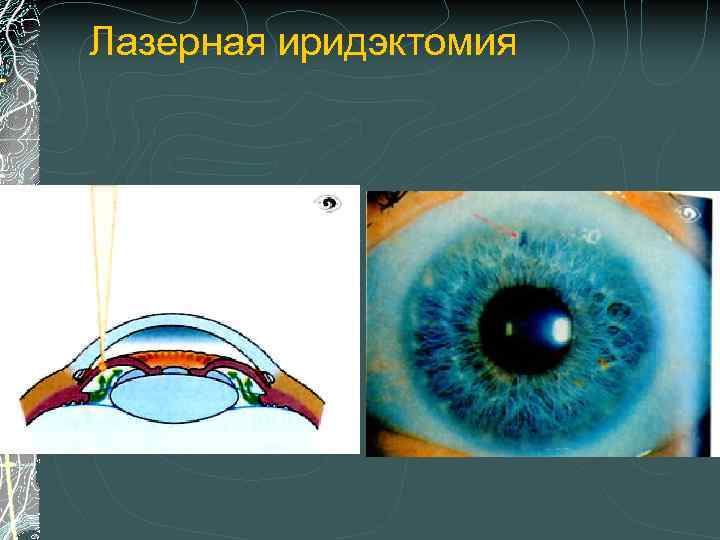
Лазерная иридэктомия

Лазерная иридэктомия
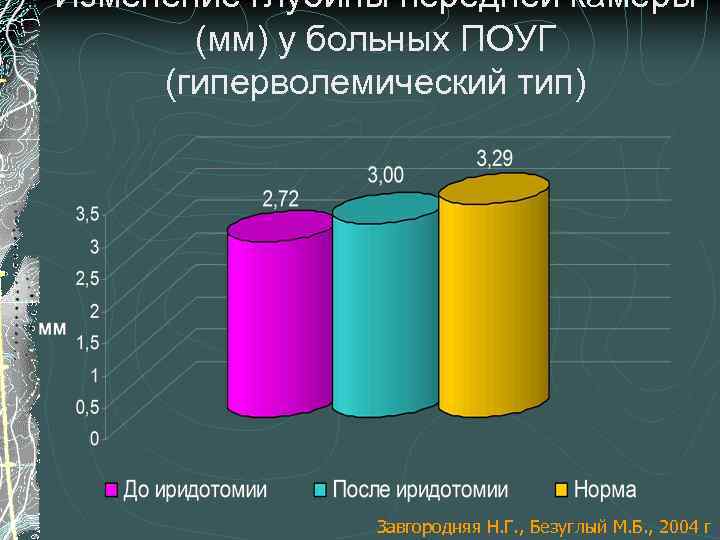
Изменение глубины передней камеры (мм) у больных ПОУГ (гиперволемический тип) Завгородняя Н. Г. , Безуглый М. Б. , 2004 г

процедуры появление в базальной колобоме видимого «фонтана» ВГЖ из задней камеры розовый рефлекс в колобоме Осложнения иридотомии кровотечение из сосудов радужки и гифема несостоятельность одной, двух или трех базальных колобом прогрессирование катаракты

YAG-лазерные вмешательства в зоне УПК с целью восстановления оттока ВГЖ в послеоперационном периоде после фильтрующих и непроникающих антиглаукоматозных операций Лазерная трабекулотомия Лазерная десцеметогониопунктура Передняя синехиотомия Выполняются при блокаде зоны фильтрации корнем радужки, передними синехиями или при недостаточном оттоке ВГЖ в послеоперационнои периоде в

2. Операции на трабекуле Перфорационные Традиционная трабекулопластика -аргоновый, диодный или «зеленый» лазер 532 нм Селективная трабекулопластика Тракционные Трабекулоспазис – коагуляция прикорневой зоны радужки, в результате чего формирующиеся рубцы «растягивают» трабекулу, расширяя просвет Шлеммова

Трабекулопластика «Классическая» аргон-лазерная трабекулопластика (ALT) J. Wise, S. Witter, 1979 Лазерные коагуляты в проекции ШК Диаметр пятна – 50 мкм Мощность – 400 – 1200 м. Вт Экспозиция – 0, 1 с
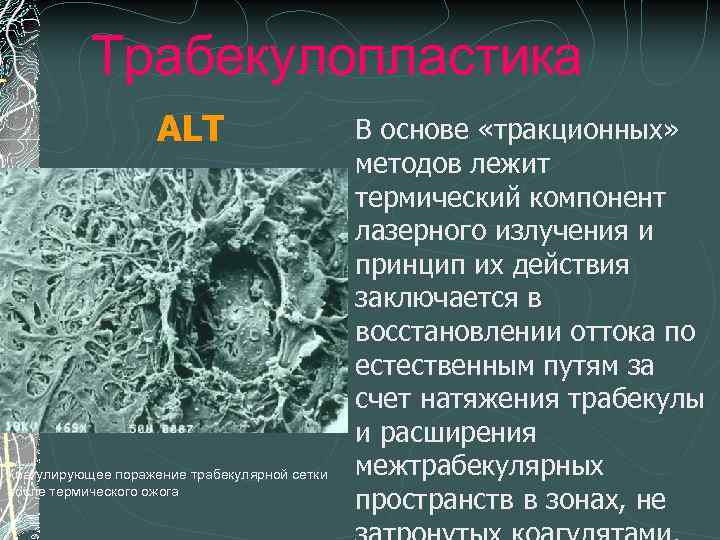
Трабекулопластика ALT Коагулирующее поражение трабекулярной сетки после термического ожога В основе «тракционных» методов лежит термический компонент лазерного излучения и принцип их действия заключается в восстановлении оттока по естественным путям за счет натяжения трабекулы и расширения межтрабекулярных пространств в зонах, не

Селективная лазерная трабекулопластика (SLT) • Дополнительное или вспомогательный метод для лекарственной терапии • Альтернатива для пациентов, не переносящих лекарственные препараты • Альтернатива аргон-лазерной трабекулопластике (ALT) • Cнижение ВГД, сравнимое с действием медикаментов • Лечебное воздействие только на прицельную ткань, в отличие от традиционной ALT

Что такое SLT? Селективная лазерная трабекулопластика воздействует на пигментированные меланинсодержащие клетки (желтые)

Ключевые моменты – ALT против SLT Процедура SLT передает энергию, в 1500 раз меньшую чем процедура ALT Одна вспышка ALT имеет энергию в 1000 раз больше, чем процедура SLT ALT SLT для участка в 180° ALT Размер пятна Выходная мощность Длительность импульса Флюенс 1 Latina SLT 50 микрон 400 микрон 500 – 1, 000 м. Вт 0. 8 – 1. 5 м. Дж 10 мс 3 нс 60, 000 м. Дж/см 2 600 м. Дж/см 2 MA, Tumbocon JA. Selective Laser Trabeculoplasty: The Evolution of Laser Treatment for Open Angle Glaucoma

Механизм SLT Действие макрофагов (большие синие клетки) по удалению из трабекулярной сетки остатков клеток и внеклеточного меланина. 3 Макрофаги стимулируют высвобождение цитокина (маленькие синие/желтые), способствуя 3: - стимуляции клеточного деления - увеличению синтеза металлопротеина - увеличению пористости слоев эндотелия трабекулярной сетки и Шлеммова канала - стимуляции повторного синтеза внеклеточного матрикса 3 Katz LJ. CME: Selective Laser Trabeculoplasty for Glaucoma Therapy. Review of Ophthalmology. 2003
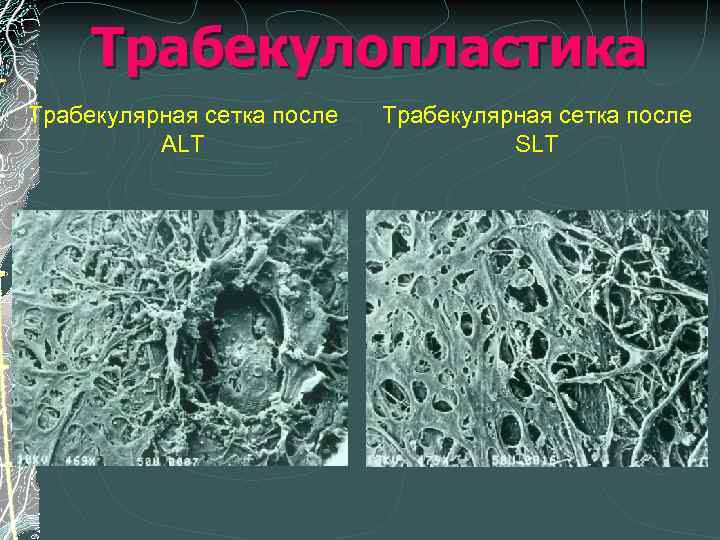
Трабекулопластика Трабекулярная сетка после ALT Трабекулярная сетка после SLT

ФИСТУЛИЗИРУЮЩИЕ ОПЕРАЦИИ ЭКСИМЕРЛАЗЕРНАЯ НЕПРОНИКАЮЩАЯ ГЛУБОКАЯ СКЛЕРЭКТОМИЯ ПРЕИМУЩЕСТВА: глубокий склеральный лоскут более ровный и гладкий отсутствует механическое раздавливание ткани более точная и дозированная абляция корнеосклеральной мембраны низкий риск перфорации трабекулы и десцеметовой оболочки т. к. ЭНЕРГИЯ ЭКСИМЕРНОГО ЛАЗЕРА ГАСИТСЯ ВО ВЛАЖНОЙ СРЕДЕ
Эксимер-лазерная установка MEL -60 “Asclepion Meditec”

ЦИКЛОДЕСТРУКТИВНЫЕ ОПЕРАЦИИ ТРАНССКЛЕРАЛЬНАЯ ЦИКЛОФОТОКОАГУЛЯЦИЯ ПОКАЗАНИЯ: Далекозашедшая и терминальная глаукома Болевой синдром МЕХАНИЗМ ДЕЙСТВИЯ - ожоги цилиарного тела с исходом в атрофию цилиарных отростков, что приводит к снижению секреции водянистой влаги. Кроме того, в области лазерного воздействия формируются "полупроницаемые мембраны". Это увеличивает доступность структур глаза медикаментозным гипотензивным средствам, применяемым местно в инстилляциях.

ТРАНССКЛЕРАЛЬНАЯ ЦИКЛОФОТОКОАГУЛЯЦИЯ Диодный лазер MILON (Россия) 810 нм Мощность 2, 0 – 2, 7 Вт Длительность импульса 0, 6 – 1 с Количество импульсов 30 70 Ретробульбарная анестезия ЭФФЕКТЫ: Аналгетический Гипотензивный

www. visus. net. ua СПАСИБО ЗА ВНИМАНИЕ!
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ГЛАУКОМЫ.ppt