Хирургические заболевания щитовидной железы.ppt
- Количество слайдов: 53

Хирургические заболевания щитовидной железы
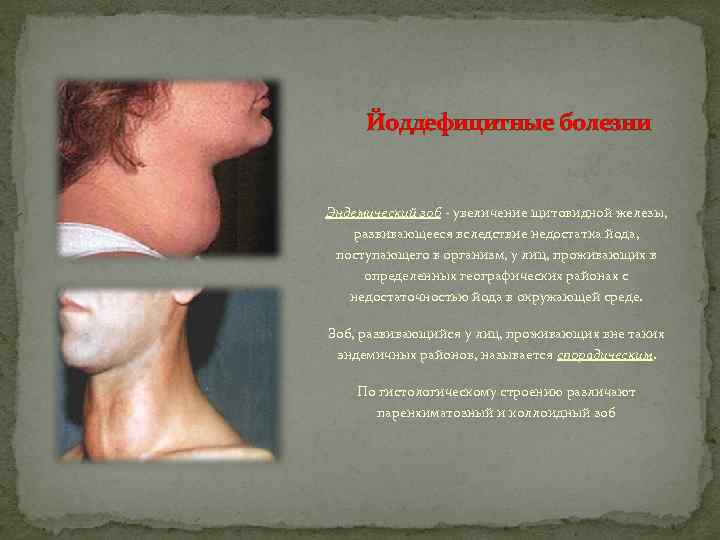
Йоддефицитные болезни Эндемический зоб - увеличение щитовидной железы, развивающееся вследствие недостатка йода, поступающего в организм, у лиц, проживающих в определенных географических районах с недостаточностью йода в окружающей среде. Зоб, развивающийся у лиц, проживающих вне таких эндемичных районов, называется спорадическим. По гистологическому строению различают паренхиматозный и коллоидный зоб

Клиническая картина определяется формой, величиной зоба, функциональным состоянием щитовидной железы. При больших размерах зоба появляются симптомы сдавления соседних органов: чувство давления в области шеи, затрудненное дыхание, иногда – приступы удушья, сухой кашель. Различают диффузную, узловую и диффузно-узловую (смешанную) формы эндемического зоба. Локализации: на передней поверхности шеи, загрудинная, кольцевая, язычная, затрахеальная, из добавочных элементов щитовидной железы. Осложнения: сдавление пищевода, трахеи, прилежащих нервов и сосудов; развитие «зобного сердца» , т. е. гиперфункция и расширение правых отделов сердца вследствие механического затруднения кровообращения; кровоизлияния в паренхиму щитовидной железы с последующим ее обызвествлением; струмит; подозрение на малигнизацию. Диагностика Анализ эпидемиологических и клинических данных Лабораторная диагностика: при эутирозе – содержание Т 3 и Т 4 в пределах нормы, при гипотиреозе содержание Т 3 и Т 4 снижено, повышен уровень тиреотропина. Радиоизотопное исследование выявляет увеличение поглощения Y 131 щитовидной железой (через 24 часа – более 20 %), что является следствием дефицита йода в щитовидной железе. Радиоизотопное сканирование щитовидной железы выявляет равномерное распределение изотопа и диффузное увеличение размеров железы различных степеней (при диффузной форме) или наличие «холодных» или «теплых» узлов при узловой форме. По данным УЗИ при диффузной форме выявляется увеличение щитовидной железы, возможно обнаружение участков фиброза и кальцификации. При узловых формах обычно выявляются множественные узлы, имеющие округлую, овальную или неправильную форму.

Пункционная биопсия щитовидной железы под контрлем УЗИ позволяет подтвердить диагноз при выявлении в пунктате характерные изменения: v при коллоидном зобе – большое количество гомогенных масс коллоида, небольшое количество клеток тиреоидного эпителия v при паренхиматозном зобе – отсутствие коллоида, много клеток тиреодного эпителия, признаки повышенной васкуляризации железы v при узловом зобе – наличие коллоида, макрофагов, дистрофические изменения тиреоцитов, лимфоидных элементов. Лечение в большинстве случаев медикаментозное. Хирургическое лечение эндемического зоба может быть показано в следующих случаях: v при узловых и диффузно-узловых формах зоба (во избежание малигнизации) v при зобе больших размеров (для ликвидации угрозы сдавления соседних органов) v при подозрении на малигнизацию
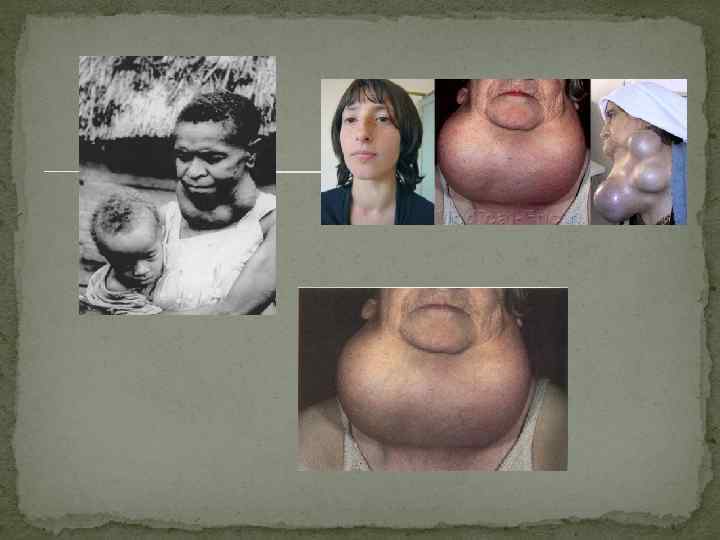

Эутиреоидный зоб ЭПИДЕМИОЛОГИЯ Основным фактором, который определяет распространенность зоба, является уровень потребления йода в популяции. По данным ВОЗ, у 13% всего человечества имеют место те или иные ЙДЗ, а среди 1, 57 биллиона человек, испытывающих тот или иной дефицит йода, у 655 миллионов имеет место зоб. В регионах с нормальным потреблением йода зоб имеет спорадический характер и его распространенность составляет около 5%. На сегодняшний день отсутствуют данные о расовых отличиях в распространенности зоба; у женщин, по разным данным, зоб встречается в 4— 8 раз чаще, чем у мужчин. Формирование в ЩЖ узловых образований многие расценивают как возрастную инволюцию органа. Действительно, вне зависимости от йодного обеспечения, распространенность узлового и многоузлового зоба увеличивается с возрастом. Распространенность пальпируемых узловых образований ЩЖ в регионе с нормальным йодным обеспечением у лиц старше 60 лет достигает 5— 6%, тогда как по данным УЗИ - 50%. Эти показатели существенно увеличиваются пропорционально утяжелению йодного дефицита в популяции.

ЭТИОЛОГИЯ И ПАТОГЕНЕЗ Наиболее частой причиной эутиреоидного, т. е. протекающего без нарушения функции ЩЖ, зоба является дефицит йода, который определяется на всей территории России. В эндемичных регионах с йодным дефицитом связано около 90— 95% случаев увеличения ЩЖ; у детей — до 99%. Дэвид Марин (D. Marine, 1880— 1976) в начале XX в. впервые научно обосновал связь между йодным дефицитом и гиперпластическими процессами в ЩЖ. В 1917 г. Марин провел исследование, в котором продемонстрировал эффективность йодной профилактики среди девочек-подростков, проживающих в штате Огайо, в результате которой распространенность зоба уменьшилась с 20 до 5 % [13]. Наряду с этим Марин впервые обнаружил зависимость между объемом ЩЖ и содержанием в ней йода, а также описал гистологические изменения, характерные для эндемического зоба (табл. 1). Содержание йода в ЩЖ при ее различных гистологических изменениях Гистологические изменения Содержание йода (мг/г ткани ЩЖ) Норма 0. 7 -0. 9 Коллоидный зоб 0. 4 -0. 6 Начальная гиперплазия 0. 2 -0. 3 Гиперплазия 0. 1 -0. 2 Выраженная гиперплазия <0. 1

Как и почему йодный дефицит приводит к образованию зоба, в то время еще не знали. После того как была описана регуляция ЩЖ гипоталамо-гипофизарной системой, в частности отрицательная обратная связь ТТГ—Т 4, в экспериментах на животных было показано, что искусственно смоделированный тяжелейший йодный дефицит приводит к повышению уровня ТТГ и образованию зоба, а также то, что экзогенно вводимый ТТГ может приводить к формированию зоба. Таким образом, была выдвинута теория, согласно которой ТТГ обладает не только специфическим эффектом, который заключается в стимуляции продукции тиреоидных гормонов, но и обуславливает увеличение ЩЖ. Тем не менее у пациентов, проживающих в регионе с умеренным дефицитом йода, более высокий уровень ТТГ по сравнению с лицами, проживающими в регионе с нормальным йодным обеспечением, не обнаруживался. Этот феномен стали объяснять так называемым «повышением чувствительности щитовидной железы к эффектам ТТГ в условиях йодного дефицита» . До последнего десятилетия эта концепция абсолютно доминировала и обуславливала основной подход к лечению зоба — супрессивную терапию, направленную на подавление эндогенной продукции ТТГ препаратами L-T 4 (левотироксин). Поскольку до последнего времени контролируемые работы, изучающие эффективность супрессивной терапии, не проводились, на протяжении многих десятилетий целесообразность такого подхода практически не подвергалась сомнению . Однако клинический опыт, который свидетельствовал о том, что отмена терапии L-T 4 приводит к значительному и еще большему увеличению размера зоба, возродил сомнения в том плане, что это лечение имеет этиотропный характер. Уже первые мультицентровые проспективные и рандомизированные исследования показали, что использование для лечения йододефицитного зоба препаратов йода оказалось сопоставимо по эффективности с супрессивной терапией L-T 4. Мало того, терапия препаратами йода приводила к значительно более стойкой стабилизации объем ЩЖ

Кроме того, эту концепцию подтвердили результаты ряда исследований in vitro и in vivo, в которых были получены новые данные об ауторегуляции ЩЖ йодом и аутокринными ростовыми факторами (АРФ). По современным представлениям, повышение продукции ТТГ или повышение к нему чувствительности тироцитов имеет лишь второстепенное значение в патогенезе йододефицитного зоба. Основную роль в этом плане отводится АРФ, в частности, инсулиноподобному ростовому фактору 1 -го типа (ИРФ-1), эпидермальному ростовому фактору (ЭРФ) и фактору роста фибробластов (ФРФ), которые в условиях снижения содержания йода в ЩЖ оказывают мощное стимулирующее воздействие на тироциты. Основным физиологическим блокатором продукции АРФ является йод, связанный с непредельными жирными кислотами (йодлактоны). В экспериментальных работах было показано, что аутокринная продукция тироцитами ИРФ-1 может быть полностью блокирована йодом . Более того, рост изолированных интактных фолликулов ЩЖ, содержащих достаточное количество йода, не удается простимулировать введением ТТГ , а при блокаде рецепторов ИРФ-1 специфическими антителами ТТГ не способен оказать трофические эффекты на тироциты. Приведенные факты отчетливо указывают на то, что сам ТТГ не оказывает непосредственного влияния на рост тироцитов, а при йодном дефиците этот эффект опосредован АРФ.

КЛАССИФИКАЦИЯ И ДИАГНОСТИКА Эутиреоидный зоб в клинической практике чаще всего классифицируется на основании макроскопических изменений ЩЖ, которые наиболее точно можно охарактеризовать при УЗИ ЩЖ, рассчитав ее объем и оценив размер узловых образований. Выделяют диффузный зоб (объем ЩЖ более 18 мл у женщин и менее 25 мл у мужчин), а также узловой, многоузловой и смешанный зоб. Диагностика эутиреоидного зоба подразумевает использование достаточно простых методов, доступных для широкой клинической практики. Наиболее просто обстоит дело с диффузным зобом, для диагностики которого достаточно определения уровня ТТГ и УЗ И ЩЖ; определение АТ-ТПО может помочь в дифференциальной диагностике с АИТ. При обнаружении в ЩЖ узловых образований дополнительно проводится пункционная биопсия для исключения опухоли ЩЖ и сцинтиграфия для исключения функциональной автономии, что существенным образом отразится на подходах к лечению.

КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ РАЗЛИЧНЫХ ФОРМ ЭУТИРЕОИДНОГО ЗОБА Прежде чем обсуждать лечение эутиреоидного зоба, как в целом, так и для отдельно взятого пациента, необходимо четко представлять, какое патологическое значение он имеет, т. е. какую опасность он несет для человека. По современным представлениям, патологическое значение эутиреоидного зоба исчерпывается следующим: 1. Относительно низким риском значительного увеличения ЩЖ со сдавлением окружающих органов и формированием косметического дефекта; 2. Риском прогрессирования процесса в соответствии с этапами естественного течения йододефицитного зоба; 3. Риском развития автономии ЩЖ и тиреотоксикоза спустя десятки лет после формирования зоба; 4. Относительно небольшим риском того, что узловое образование ЩЖ является раком, который, в свою очередь, является достаточно редким заболеванием (около 25 новых случаев на 1 миллион населения в год). Последний пункт традиционно вызывает наибольшие обсуждения. Не углубляясь в проблему дифференциальной диагностики узлового зоба, заметим лишь несколько принципиальных аспектов: 1. В настоящее время наиболее принята концепция, в соответствии с которой узловой коллоидный пролиферирующий зоб не может подвергаться так называемой малигнизации [17]; т. е. случаи, когда рак выявляется при повторной пункционной биопсии узла ЩЖ, не свидетельствуют об опухолевой трансформации последнего, а связаны с ошибкой, допущенной при первичном обследовании; 2. Тонкоигольная биопсия ЩЖ, особенно выполненная под контролем УЗИ с привлечением опытного цитолога, специализирующего на патологии ЩЖ, является надежным методом диагностики опухолей; 3. Динамическое наблюдение пациентов с узловым зобом и, при необходимости, повторная биопсия, практически полностью нивелируют опасность поздней диагностики высокодифференцированного рака ЩЖ; 4. При соблюдении принятых во всем мире алгоритмов лечения высокодифференцированного рака ЩЖ (тиреоидэктомия, терапия радиоактивным йодом, динамическая оценка уровня тиреоглобулина на фоне эндогенной или экзогенной стимуляции ТТГ) десятилетняя выживаемость пациентов приближается к 99% [17], т. е. в большинстве случаев речь идет об излечимом заболевании.

КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ ЭУТИРЕОИДНОГО ЗОБА На сегодняшний день существует три варианта консервативной терапии эутиреоидного зоба: 1) монотерапия препаратами йода, 2) супрессивная терапия левотироксином (L-T 4), 3) комбинированная терапия йодом и L-T 4. Как уже можно было заключить из сказанного, супрессивная терапия L-T 4, по современным патогенетическим представлениям, не является лечением выбора при диффузном эутиреоидном зобе, который диагностируется в регионах умеренного йодного дефицита у 30% всего населения. На первом этапе лечения подавляющему большинству детей, подростков и молодых людей (моложе 40— 50 лет) показано назначение йода в дозе 100 -200 мкг в день, что приводит к достаточно быстрому подавлению гипертрофического компонента зоба (увеличение размеров тироцитов). В контролируемых клинических исследованиях было показано, что на фоне терапии йодом за первые 6 месяцев объем ЩЖ в среднем уменьшается на 30%. Основными преимуществами монотерапии препаратами йода являются ее этиотропный характер (иододефицитный зоб — практически единственное заболевание в эндокринологии, при котором осуществима этиотропная терапия), безопасность, отсутствие необходимости в подборе дозы и в проведении частых гормональных исследований. На этом фоне основными недостатками супрессивной монотерапии L-T 4 является высокая вероятность рецидива зоба после отмены препарата (тироксин легко назначить, но сложно отменить), риск осложнений медикаментозного тиреотоксикоза, необходимость подбора дозы, что требует частых гормональных исследований (целью такого лечения должно быть поддержание уровня ТТГ в пределах 0, 1— 0, 4 м. МЕ/л, что у взрослых, как правило, требует назначения не менее 100— 150 мкг L-T 4). Назначая терапию L-T 4, всегда следует помнить о том, что в организм вводится активный гормон, оказывающий свое воздействие на большинство органов и тканей, а не на одну ЩЖ. В то же время йод в организме оказывает воздействие практически исключительно на ЩЖ и в физиологических дозах абсолютно безопасен. В указанной группе пациентов монотерапия йодом сопоставима по эффективности с супрессивной терапией L-T.

При обнаружении в щитовидной железе одного или нескольких пальпируемых и/или превышающих 1 -1, 5 см в диаметре узловых образований пациенту показаны дополнительные исследования: пункционная биопсия «узла» и, в большинстве случаев, особенно если речь идет о лицах старше 40 лет, сцинтиграфия ЩЖ с целью исключения функциональной автономии. В последнем случае назначение пациенту препаратов йода не показано, поскольку оно может вызвать декомпенсацию автономии с развитием тиреотоксикоза. Хорошо себя зарекомендовавшей в клинических исследованиях альтернативой монотерапии L-T 4 является комбинированное назначение препаратов йода и L-T 4. Основным плюсом комбинированной терапии является более быстрое достижение уменьшения объема ЩЖ (за счет L-T 4) и нивелировка феномена отмены L-T 4 (рецидив зоба) за счет йода, который предотвращает снижение интратиреоидного содержания йода, возникающего при монотерапии L-T 4. В принципе, L-T 4 и йод можно назначать и последовательно: сначала быстрое достижение регресса объема железы на фоне супрессивной терапии L-T 4, а затем добавление 100— 200 мкг йода. Аргументом в пользу последовательного, а не одновременного назначения L-T 4 и йода является тот факт, что супрессия ТТГ, которая развивается на фоне назначения Ь-Т 4, подавляет транспорт в ЩЖ йода (получается, что один компонент терапии как бы «мешает» другому). Тем не менее этот феномен вряд ли имеет существенное клиническое значение, о чем свидетельствуют как экспериментальные работы, изучавшие интратиреоидное содержание йода на фоне различных вариантов терапии (рис. 5), так и клинические исследования, показавшие высокую и долгосрочную эффективность весьма популярных во многих странах фиксированных комбинаций L-T 4 и йода (на фармацевтическом рынке ФРГ можно насчитать около десятка комбинированных препаратов, содержащих различные дозы L -T 4 и KI - калия йодида). Среди подобных комбинаций наиболее популярны препараты, содержащие 75— 100 мкг L-T 4 и 100— 150 мкг йода.

Здесь хотелось бы заметить, что, по данным многих клинических исследований, сравнивающих эффективность терапии йодом, L-T 4 и их комбинации, конечное уменьшение ЩЖ (в % от исходного объема) на фоне всех трех схем существенно не отличалось. Как уже указывалось, отличался прогноз: с окончанием монотерапии L-T 4 очень часто развивался рецидив зоба. Есть ли ситуации, в которых более предпочтительно назначение монотерапии L-T 4? Безусловно есть, но они имеют лишь косвенное отношение к проблеме йододефицитного зоба. В этом контексте часто обсуждается безопасность назначения йода в ситуации, когда данные обследования не позволяют исключить у пациента аутоиммунный тиреоидит (АИТ) как причину увеличения ЩЖ. Сразу хотелось бы оговориться, что в соответствии с рекомендациями практически всех без исключения эндокринологических сообществ сам по себе АИТ в фазе эутиреоза не является показанием к назначению какой-либо терапии. Вопрос о назначении супрессивной терапии может рассматриваться при АИТ в относительно редких ситуациях значительного увеличения ЩЖ (гигантский зоб Хашимото встречается относительно редко, к тому же у большинства пациентов к этому времени уже имеется гипотиреоз, сам по себе требующий заместительной терапии). В целом следует исходить из того, что в йододефицитных регионах случаи значительного увеличения ЩЖ без нарушения ее функции в подавляющем большинстве случаев связаны с йододефицитным зобом. Последнему зачастую сопутствуют те изменения, которые описываются и при АИТ: умеренное повышение уровня антител к ЩЖ и снижение ее эхогенности, поэтому обнаружение последних, особенно порознь, не может быть основанием для постановки диагноза АИТ. Если диагноз АИТ представляется весьма вероятным (с абсолютной уверенностью об этом можно говорить только при наличии гипотиреоза) и при этом у пациента имеется небольшое увеличение ЩЖ на фоне эутиреоза, наиболее оптимальной тактикой, по нашему представлению, является динамическое наблюдение. В заключение обсуждения проблемы АИТ заметим, что ошибочное назначение физиологических доз йода (100— 200 мкг в день) при гипертрофической форме АИТ, когда его путают с йододефицитным зобом, не несет для пациента никакой опасности. В этом случае, по мере динамического наблюдения, не будет отмечаться уменьшения объема ЩЖ, а возможно, вследствие естественного течения процесса, появятся другие маркеры АИТ, что позволит пересмотреть диагностическую концепцию и изменить тактику.

ОПЕРАТИВНОЕ ЛЕЧЕНИЕ И ТЕРАПИЯ РАДИОАКТИВНЫМ ЙОДОМ-131 Если речь идет о диффузном эутиреоидном зобе, операция может быть показана лишь при его гигантском размере и/или при явлениях компрессии окружающих органов. В случае многоузлового и узлового зоба, в ситуациях, когда при помощи тонкоигольной биопсии исключена опухолевая природа этих образований, показанием для операции является лишь значительный размер узлов (более 4— 5 см в диаметре). И в том, и в другом случае, а также в целом для лечения как токсического, так и эутиреоидного зоба серьезной альтернативой операции является терапия радиоактивным йодом. Последний метод, как известно, является лечением выбора при функциональной автономии ЩЖ, а также в большинстве случаев болезни Грейвса (диффузного токсического зоба). Наряду с этим в последние несколько десятилетий в мире накоплен большой опыт лечения при помощи радиоактивного йода-131 эутиреоидного зоба. Метод позволяет неинвазивно буквально в течение нескольких месяцев достичь уменьшения объема ЩЖ на 40— 50 % даже после однократного введения изотопа

Болезнь Грейвса (болезнь Базедова, диффузный токсический зоб) - системное аутоиммунное заболевание, развивающееся вследствие выработки антител к рецептору тиреоторопного гормона, клинически проявляющееся поражением щитовидной железы с развитием синдрома тиреотоксикоза в сочетании с экстратиреоидной патологией: эндокринной офтальмопатией, претибиальной микседемой, акропатией. Впервые заболевание было описано в 1825 г. Калебом Парри, в 1835 г. - Робертом Грейвсом, а в 1840 г. - Карлом фон Базедовым.

Этиология диффузного токсического зоба Диффузный токсический зоб является мультифакторным заболеванием, при котором генетические особенности иммунного реагирования реализуются на фоне действия факторов окружающей среды. Наряду с этнически ассоциированной генетической предрасположенностью (носительство гаплотипов HLA-B 8, -DR 3 и -DQA 1*0501 у европейцев), в патогенезе диффузного токсического зоба определенное значение придается психосоциальным передовым факторам. Эмоциональные стрессорные и экзогенные факторы, такие как курение, могут способствовать реализации генетической предрасположенности к диффузному токсическому зобу. Курение повышает риск развития диффузного токсического зоба в 1, 9 раза. Диффузный токсический зоб в ряде случаев сочетается с другими аутоиммунными эндокринными заболеваниями (сахарный диабет 1 типа, первичный гипокортицизм). В результате нарушения иммунологической толерантности, аутореактивные лимфоциты (CD 4+ и CD 8+ Т-лимфоциты, В-лимфоциты) при участии адгезивных молекул (ICAM-1, ICAM-2, Еселектин, VCAM-1, LFA-3, CD 44) инфильтрируют паренхиму щитовидной железы, где распознают ряд антигенов, которые презентируются дендридными клетками, макрофагами и В-лимфоцитами. В дальнейшем цитокины и сигнальные молекулы инициируют антигенспецифическую стимуляцию В-лимфоцитов, в результате чего начинается продукция специфических иммуноглобулинов против различных компонентов тироцитов. В патогенезе диффузного токсического зоба основное значение придается образованию стимулирующих антител к рецептору ТТГ (АТ-р. ТТГ). В отличие от других аутоиммунных заболеваний при диффузном токсическом зобе происходит не разрушение, а стимуляция органа-мишени. В данном случае аутоантитела вырабатываются к фрагменту рецептора ТТГ, который находится на мембране тироцитов. В результате взаимодействия с антителом этот рецептор приходит в активное состояние, запуская пострецепторный каскад синтеза тиреоидных гормонов (тиреотоксикоз) и, кроме того, стимулируя гипертрофию тироцитов (увеличение щитовидной железы). По не вполне понятным причинам сенсибилизированные к антигенам щитовидной железы Т-лимфоциты инфильтрируют и вызывают иммунное воспаление в ряде других структур, таких как ретробульбарная клетчатка (эндокринная офтальмопатия), клетчатка передней поверхности голени (претибиальная микседема).

Патогенез диффузного токсического зоба Клинически наиболее значимым синдромом, развивающимся при диффузном токсическом зобе вследствие гиперстимуляции щитовидной железы антителами к рецептору ТТГ, является тиреотоксикоз. Патогенез изменений со стороны органов и систем, развивающихся при тиреотоксикозе, заключается в значительном повышении уровня основного обмена, которое со временем приводит к дистрофическим изменениям. Самыми чувствительными к тиреотоксикозу структурами, в которых наиболее высока плотность рецепторов к тиреоидным гормонам, являются сердечно-сосудистая (особенно миокард предсердий) и нервная системы. Эпидемиология диффузного токсического зоба В регионах с нормальным потреблением йода диффузный токсический зоб является наиболее частым заболеванием в нозологической структуре синдрома тиреотоксикоза (если не принимать в расчет заболевания, протекающие с транзиторным тиреотоксикозом, такие как послеродовый тиреоидит и др. ). Женщины болеют в 8 -10 раз чаще, в большинстве случаев между 30 и 50 годами. Заболеваемость диффузным токсическим зобом одинакова среди представителей европейской и азиатской расы, но ниже среди негроидной расы. У детей и пожилых людей заболевание встречается достаточно редко.

Клинические проявления диффузного токсического зоба Для диффузного токсического зоба, в большинстве случаев, характерен относительно короткий анамнез: первые симптомы обычно появляются за 4 -6 месяцев до обращения к доктору и постановки диагноза. Как правило, ключевые жалобы связаны с изменениями со стороны сердечно-сосудистой системы, так называемым катаболическим синдромом и эндокринной офтальмопатией. Основным симптомом со стороны сердечно-сосудистой системы является тахикардия и достаточно выраженные ощущения сердцебиений. Пациенты могут ощущать сердцебиения не только в грудной клетке, но и голове, руках, животе. ЧСС в покое при синусовой тахикардии, обусловленной тиреотоксикозом, может достигать 120 -130 ударов в минуту. При длительно существующем тиреотоксикозе, особенно у пожилых пациентов, развиваются выраженные дистрофические изменения в миокарде, частым проявлением которых являются суправентрикулярные нарушения ритма, а именно фибрилляция (мерцание) предсердий. Это осложнение тиреотоксикоза достаточно редко развивается у пациентов моложе 50 лет. Дальнейшее прогрессирование миокардиодистрофии приводит к развитию изменений миокарда желудочков и застойной сердечной недостаточности.

Как правило, выражен катаболический синдром, проявляющийся прогрессирующим похудением (порой на 10 -15 кг и более, особенно у лиц с исходным избытком веса) на фоне нарастающей слабости и повышенного аппетита. Кожа больных горячая, иногда имеется выраженный гипергидроз. Характерно чувство жара, пациенты не мерзнут при достаточно низкой температуре в помещении. У некоторых пациентов (особенно в пожилом возрасте) может быть выявлен вечерний субфебрилитет. Изменения со стороны нервной системы характеризуются психической лабильностью: эпизоды агрессивности, возбуждения, хаотичной непродуктивной деятельности сменяются плаксивостью, астенией (раздражительная слабость). Многие пациенты некритичны к своему состоянию и пытаются сохранить активный образ жизни на фоне достаточно тяжелого соматического состояния. Длительно существующий тиреотоксикоз сопровождается стойкими изменениями психики и личности пациента. Частым, но неспецифичным симптомом тиреотоксикоза является мелкий тремор: мелкая дрожь пальцев вытянутых рук выявляется у большинства пациентов. При тяжелом тиретоксикозе тремор может определяться во всем теле и даже затруднять речь пациента. Для тиреотоксикоза характерны мышечная слабость и уменьшение объема мускулатуры, особенно проксимальных мышц рук и ног. Иногда развивается достаточно выраженная миопатия. Весьма редким осложнением является тиреотоксический гипокалиемический периодический паралич, который проявляется периодически возникающими резкими приступами мышечной слабости. При лабораторном исследовании выявляется гипокалиемия, повышение уровня КФК. Чаще встречается у представителей азиатской расы. Интенсификация костной резорбции приводит к развитию синдрома остеопении, а сам тиреотоксикоз рассматривается как один из наиболее важных факторов риска остеопороза. Частыми жалобами пациентов являются выпадение волос, ломкость ногтей. Изменения со стороны желудочно-кишечного тракта развиваются достаточно редко. У пожилых пациентов в ряде случаев может быть диарея. При длительно существующем тяжелом тиреотоксикозе могут развиваться дистрофические изменения в печени (тиреотоксический гепатоз).

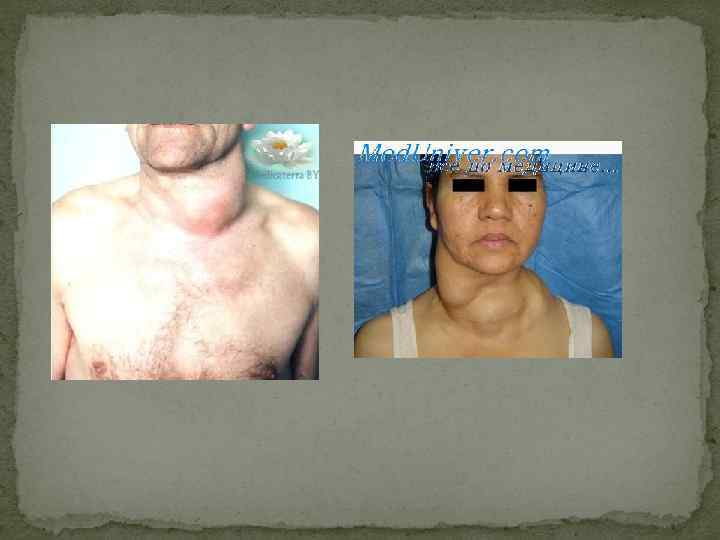
Нарушения менструального цикла встречаются достаточно редко. В отличие от гипотиреоза, тиреотоксикоз умеренной выраженности может не сопровождаться снижением фертильности и не исключает возможности наступления беременности. Антитела к рецептору ТТГ проникают через плаценту, в связи с чем у детей, рожденных (1 %) от женщин с диффузным токсическим зобом (иногда спустя годы после проведенного радикального лечения), может развиться транзиторный неонатальный тиреотоксикоз. У мужчин тиреотоксикоз достаточно часто сопровождается эректильной дисфункцией. При тяжелом тиреотоксикозе уряда пациентов выражены симптомы тиреогенной (относительной) надпочечниковой недостаточности, которую необходимо дифференцировать от истинной. К уже перечисленным симптомам добавляются гиперпигментация кожи, открытых частей тела (симптом Еллинека), артериальная гипотензия. В большинстве случаев при диффузном токсическом зобе происходит увеличение размеров щитовидной железы, которое, как правило, имеет диффузный характер. Нередко железа увеличена значительно. В ряде случаев над щитовидной железой можно выслушать систолический шум. Тем не менее зоб не является облигатным симптомом диффузного токсического зоба, поскольку он отсутствует не менее чем у 25 -30 % пациентов. Ключевое значение в диагностике диффузного токсического зоба имеют изменения со стороны глаз, которые являются своеобразной «визитной карточкой» диффузного токсическогго зоба, т. е. их обнаружение у пациента с тиреотоксикозом практически однозначно свидетельствует именно о диффузном токсическом зобе, а не о другом заболевании. Очень часто благодаря наличию выраженной офтальмопатии в сочетании с симптомами тиреотоксикоза диагноз диффузный токсический зоб очевиден уже при осмотре пациента. Другим редким (менее 1 % случаев), ассоциированным с диффузным токсическим зобом, заболеванием является претибиальная микседема. Кожа передней поверхности голени становится отечной, уплотненной, пурпурно-красного цвета ( «апельсиновая корка» ), часто сопровождается эритемой и зудом.

Клиническая картина тиреотоксикоза может иметь отклонения от классического варианта. Так, если у молодых диффузным токсическим зобом характеризуется развернутой клинической картиной, у пожилых пациентов ее течение зачастую олиго- или даже моносимптомное (нарушение ритма сердца, субфебрилитет). При «апатическом» варианте течения диффузного токсического зоба, который встречается у пожилых пациентов, клинические проявления включают потерю аппетита, депрессию, гиподинамию. Весьма редким осложнением диффузного токсического зоба является тиреотоксический криз, патогенез которого не вполне понятен, так криз может развиваться и без запредельного повышения уровня тиреоидных гормонов в крови. Причиной тиреотоксического криза могут оказаться сопутствующие диффузному токсическому зобу острые инфекционные заболевания, проведение оперативного вмешательства или терапии радиоактивным йодом на фоне выраженного тиреотоксикоза, отмена тиреостатической терапии, введение пациенту контрастного йодсодержащего препарата. Клинические проявления тиреотоксического криза включают резкое утяжеление симптомов тиреотоксикоза, гипертермию, спутанность сознания, тошноту, рвоту, иногда диарею. Регистрируется синусовая тахикардия свыше 120 уд/мин. Нередко отмечается мерцательная аритмия, высокое пульсовое давление с последующей выраженной гипотонией. В клинической картине может доминировать сердечная недостаточность, респираторный дистресс-синдром. Нередко выражены проявления относительной надпочечниковой недостаточности в виде гиперпигментации кожи. Кожные покровы могут быть желтушны вследствие развития токсического гепатоза. При лабораторном исследовании может выявляться лейкоцитоз (даже при отсутствии сопутствующей инфекции), умеренная гиперкальциемия, повышение уровня щелочной фосфатазы. Смертность при тиреотоксическом кризе достигает 30 -50 %.
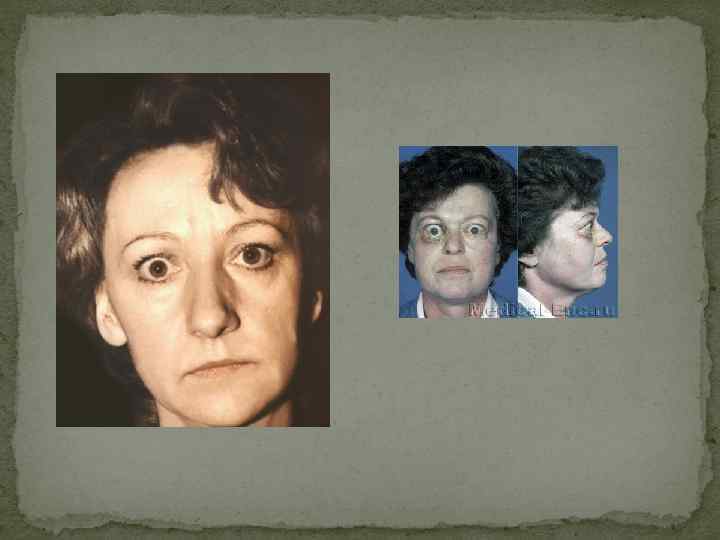
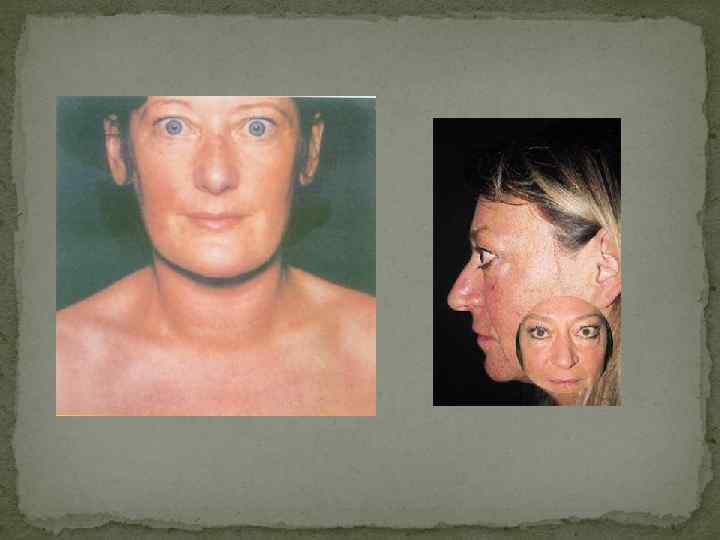
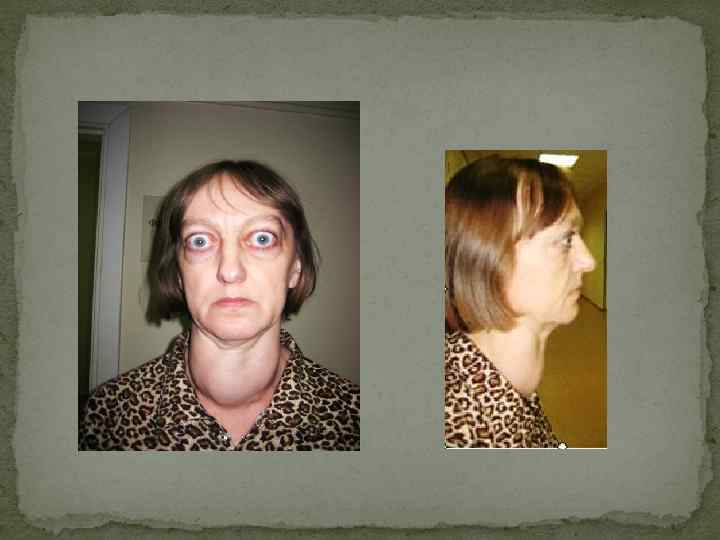


Диагностика К диагностическим критериям диффузного токсического зоба относят: Лабораторно подтвержденный тиреотоксикоз (уменьшение ТТГ, увеличение Т 4 и/или ТЗ). Эндокринную офтальмопатию (60 -80 % случаев). Диффузное увеличение объема щитовидной железы (60 -70 %). Диффузное усиление захвата 99 m. Tc по данным сцинтиграфии щитовидной железы. Повышенный уровень антител к рецептору ТТГ. На первом этапе диагностики диффузного токсического зоба необходимо подтвердить, что имеющаяся у пациента клиническая симптоматика (тахикардия, похудение, тремор) обусловлена синдромом тиреотоксикоза. С этой целью проводят гормональное исследование, которое обнаруживает снижение или даже полное подавление уровня ТТГ и повышение уровней Т 4 и/или ТЗ. Дальнейшая диагностика направлена на дифференцировку диффузного токсического зоба от других заболеваний, протекающих с тиреотоксикозом. При наличии клинически выраженной эндокринной офтальмопатии диагноз диффузный токсический зоб практически очевиден. В ряде случаев при отсутствии явной эндокринной офтальмопатии имеет смысл осуществить ее активный поиск при помощи инструментальных методов (УЗИ и МРТ орбит). УЗИ при диффузном токсическом зобе, как правило, обнаруживает диффузное увеличение щитовидной железы и характерную для всех ее аутоиммунных заболеваний гипоэхогенность. Определение объема щитовидной железы помимо всего необходимо для выбора метода лечения, так как прогноз консервативной тиреостатической терапии при зобе большого размера достаточно плохой. Проведение сцинтиграфии щитовидной железы в типичных случаях (тиреотоксикоз, эндокринная офтальмопатия, диффузный зоб, молодой возраст пациента) не обязательно. В менее очевидных ситуациях этот метод позволяет дифференцировать диффузный токсический зоб от заболеваний, протекающих с деструктивным тиреотоксикозом (послеродовый, подострый тиреоидиты и проч. ) или от функциональной автономии щитовидной железы (многоузловой токсический зоб с «горячими» узлами). При диффузном токсическом зобе не менее чем у 70 -80 % пациентов определяются циркулирующие антитела к тиреоидной пероксидазе (АТ-ТПО) и тиреоглобулину (АТ-ТГ), тем не менее, они неспецифичны для этого заболевания и встречаются при любой другой аутоиммунной патологии щитовидной железы (аутоиммунный тиреоидит, послеродовый тиреоидит). В ряде случаев повышение уровня АТ-ТПО можно расценивать как косвенный диагностический признак диффузного токсического зоба, когда речь идет о ее дифференциальной диагностики от неаутоиммунных заболеваний, протекающих с тиреотоксикозом (функциональная автономия щитовидной железы). Достаточно специфическим тестом для диагностики и дифференциальной диагностики диффузного токсического зоба является определение уровня антител к рецептору ТТГ, которым при этом заболевании придается основное патогенетическое значение. Тем не менее следует учесть, что в ряде случаев эти антитела не выявляются у пациентов с явным диффузным токсическим зобом, что связано с несовершенством относительно недавно появившихся тест-систем.

Лечение диффузного токсического зоба Существует три метода лечения диффузного токсического зоба (консервативное лечение тиреостатическими препаратами, хирургическое лечение и терапия 131 I), при этом ни один из них не является этиотропным. В разных странах удельный вес использования указанных методов лечения традиционно отличается. Так, в Европейских странах в качестве первичного метода лечения наиболее принята консервативная терапия тиреостатиками, в США подавляющее большинство пациентов получает терапию 131 I. Консервативная терапия осуществляется при помощи препаратов тиомочевины, к которым относится тиамазол (мерказолил, тирозол, метизол) и пропилтиоурацила (ПТУ, пропицил). Механизм действия обоих препаратов заключается в том, что они активно накапливаются в щитовидной железе и блокируют синтез тиреоидных гормонов благодаря ингибированию тиреоидной пероксидазы, которая осуществляет присоединение йода к остаткам тирозина в тиреоглобулине.

Хирургическому лечению подвергаются около 40% больных диффузным токсическим зобом. Показания к оперативному лечению: q Неэффективность лекарственного лечения в течение 1 -1, 5 лет, рецидив тиреотоксикоза после курса консервативной терапии q Непереносимость антитиреоидных препаратов q Рецидив тиреотоксикоза после перенесенной ранее хирургической операции при невозможности лечения радиоактивным йодом q Сочетание с неопластическими процессами q Зоб больших размеров, вызывающий сдавление окружающих органов и тканей q Осложненное течение тиреотоксикоза q Загрудинное (внутригрудинное) расположение зоба Обязательным условием проведения хирургического лечения является предварительное устранение тиреотоксикоза антитиреоидными препаратами. Операция должна проводится при достижении стойкого эутиреоза. За 2 недели до операции назначается раствор Люголя до 30 капель 3 раза в день на фоне поддерживающих дох антитиреоидных препаратов и βблокаторов. Неорганический йод вызывает транзиторную инволюцию ткани щитовидной железы, что облегчает проведение операции. Операцией выбора является субтотальная резекция щитовидной железы. Операция может быть в 2 модификациях. Модификация Драчинской - удаляется вся ткань железы за исключением верхнего полюса левой доли. Модификация Николаева – удаляется вся железа, кроме небольших (массой по 2 -3 г) прилегающих к трахее пластинок тиреоидной ткани на задней поверхности каждой из долей.

Модификация Николаева предпочтительна для уменьшения риска повреждения возвратных нервов и паращитовидных желез. Преимуществом методики, предложенной Драчинской, является возможность хорошей ревизии и точного дозирования оставляемой тиреоидной ткани (4 -6 г), что особенно важно для профилактики развития рецидивов. Кроме того, на фоне диффузного токсического зоба могут иметь место узловые образования, которые в 14 -18% наблюдений оказываются злокачественными. В таких случаях модификация по Николаеву может оказаться онкологически неадекватной. , так как не будет исключена возможность оставления фокусов злокачественного роста с той или иной стороны трахеи. Из особенностей операции при диффузном токсическом зобе следует отметить довольно выраженный спаечный процесс в окружающих железу тканях, который обусловлен аутоиммунной природой заболевания. Это вызывает определенные технические трудности при осуществлении доступа и мобилизации. Кроме того, следует отметить хрупкость тиреоидной ткани и повышенную кровоточивость при операции, в связи с чем необходима особая деликатность манипуляций и проведение особенно тщательного гемостаза.

После операции отменяют антитиреоидные препараты и постепенно отходят от лечения препаратами неорганического йода, уменьшая дозы раствора Люголя ежедневно по 3 капли на прием. Частота рецидивов тиреотоксикоза в первые 5 лет после проведения операции достигает 10 -18%. Основной причиной рецидива заболевания является значительный объем оставленной тиреоиднйо ткани, в меньшей стпени – иммунный статус. И развитие аденоматозной трансформации остатка тиреоидной ткани. С целью уменьшения риска рецидива рекомендуется выполнение суперсубтотальной резекции щитовидной железы с оставлением не более 2 г ткани.

Операцию на щитовидной железе, сводящую до минимума осложнения, предложил советский хирург О. В. Николаев. Эта операция называется субтотальной, субфасциальной резекцией щитовидной железы. Субтотальной она называется потому, что производится удаление почти всей ткани железы, а субфасциальной потому, что резекция производится в пределах фасциальной капсулы железы, т. е. под этой капсулой. Как сказано в разделе о топографии щитовидной железы, околощитовидные железы располагаются под фасциальной капсулой, а возвратные гортанные нервы лежат кнаружи от капсулы. Следовательно, вмешательство внутри фасциальной капсулы не может привести к повреждению возвратного гортанного нерва, а сохранение небольшого слоя щитовидной железы на ее задней поверхности оставляет неприкосновенными околощитовидные железы.
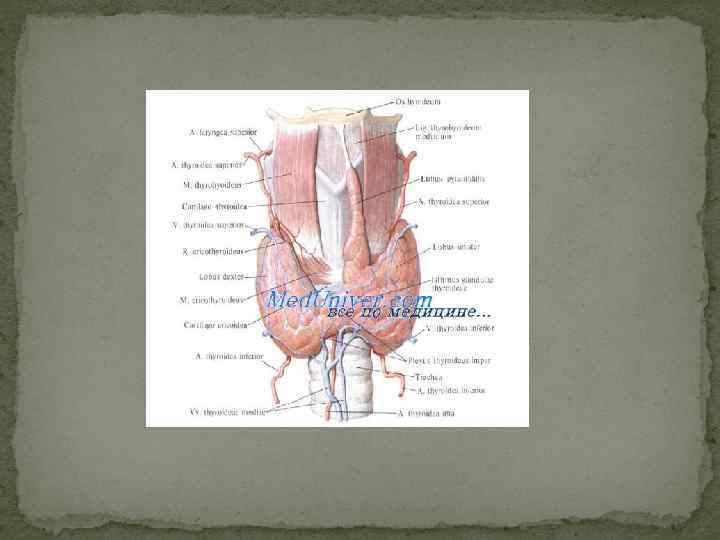

Субтотальная резекция щитовидной железы по Николаеву. Субфасциальная резекция щитовидной железы по Николаеву. Субтотальная резекция щитовидной железы по Николаеву производится из поперечного, слегка дугообразного доступа, на 1, 0 -1, 5 см выше яремной вырезки между передними краями грудино-ключичнососцевидных мышц. После рассечения кожи, подкожной клетчатки и поверхностной мышцы шеи с поверхностной фасцией верхний лоскут оттягивают до уровня верхнего края щитовидного хряща. 2 -ю и 3 -ю фасции шеи рассекают продольно посередине между грудиноподъязычными и грудино-щитовидными мышцами. Для обнажения щитовидной железы грудино-подъязычные, а иногда и грудинощитовидные мышцы рассекают в поперечном направлении. Введение под фасциальную капсулу щитовидной железы 0, 25 % раствора новокаина блокирует её нервное сплетение и облегчает выделение железы из капсулы. Выведенную из капсулы железу резецируют, останавливая кровотечение кровоостанавливающими зажимами. После тщательного гемостаза над культей непрерывным кетгутовым швом сшивают края фасциальной капсулы. Грудино-подъязычные мышцы сшивают кетгутовыми П-образными швами. Края фасций сшивают узловыми кетгутовыми швами, кожные края - узловыми шелковыми или синтетическими швами.

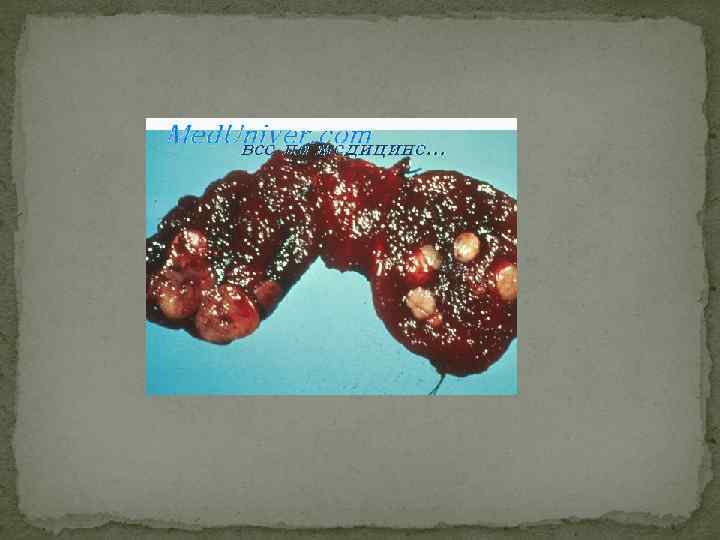
РАК ЩИТОВИДНОЙ ЖЕЛЕЗЫ Проблема рака щитовидной железы остается актуальной в связи с тем, что узловой зоб встречается более чем у 4% населения и более чем в 90% случаев рак щитовидной железы при обследовании выявляется как аденома. Рак щитовидной железы встречается в 2 раза чаще у женщин, чем у мужчин. Формы рака щитовидной железы Опухоли щитовидной железы делятся на доброкачественные (фолликулярная и папиллярная аденома) и злокачаственные. Рак щитовидной железы подразделяют на: ▪ папиллярный (около 76%) ▪ фолликулярный (около 14%) ▪ медуллярный (около 5 -6 %) ▪ недифференцированный и анапластический рак (около 3, 5 -4%). Значительно реже встречается саркома, лимфома, фибросаркома, эпидермоидный рак, метастатический рак, на долю которых приходится 1 -2 % от всех злокачественных новообразований щитовидной железы. Папиллярный рак встречается у детей, но чаще у взрослых, достигая пика заболеваемости в возрасте 30 -40 лет. Выявляется при сканировании как плотный, одиночный “холодный” узел. При многоузловом зобе обычно один из узлов, имеющий более плотную консистенцию по сравнению с другими участками и узлами щитовидной железы и превышающий их, как правило, по размеру, является папиллярным раком. Как при первой, так и при второй клинической форме может отмечаться сравнительно “благоприятное” течение на протяжении нескольких лет. Почти в 30% случаев при папиллярном раке имеются метастазы. У детей (до пубертатного возраста) папиллярный рак протекает более агрессивно по сравнению со взрослыми, чаще имеют место метастазы как в шейные лимфатические узлы, так и в легкие. Тем не менее прогноз у детей и лиц в возрасте до 40 лет более благоприятный, чем у больных старше 45 лет.

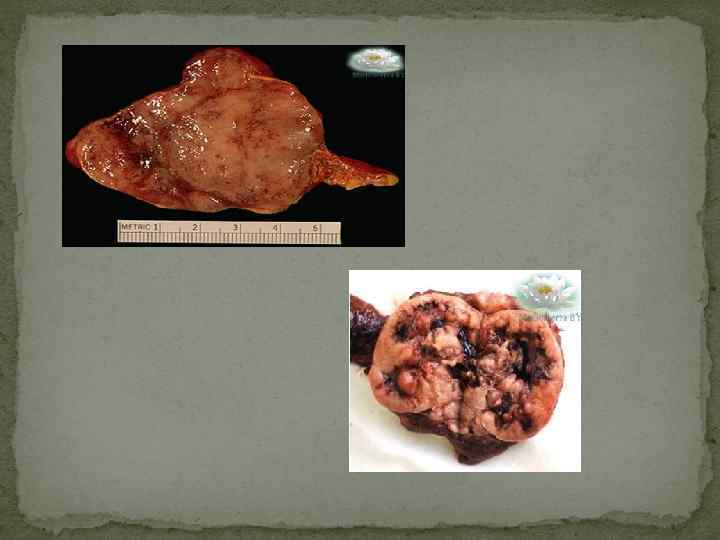
Фолликулярный рак встречается у взрослых, чаще в возрасте 50 -60 лет. Характеризуется медленным ростом. При обследовании выявляется как одиночная “аденома”, которую действительно трудно отличить от фолликулярной аденомы. Течение фолликулярного рака более агрессивное, чем папиллярного, и часто он дает метастазы в лимфатические узлы шеи и реже - отдаленные метастазы в кости, легкие и другие органы. Метастазы фолликулярного рака способны также захватывать йод (осуществлять синтез тироглобулина и реже тироидных гормонов), что используется как в диагностике, так и в лечении их радиоактивным йодом. Как правило, “функционирующая” злокачественная опухоль щитовидной железы является фолликулярным раком. Длительность заболевания короче, а летальность от фолликулярного рака выше (почти в 2 раза) по сравнению с папиллярным раком. Медуллярный рак развивается из парафолликулярных или С-клеток, характеризуется наличием фиброза и избыточным отложением амилоида, иногда с явлениями кальцификации. Иногда такие опухоли секретируют АКТГ, серотонин, простагландины, что может сопровождаться стертой клинической картиной синдрома Иценко-Кушинга, “приливами”, покраснением лица, диареей. Медуллярный рак является солитарной опухолью желто-серого цвета. При иммунногистохимическом исследовании в опухолях определяется содержание кальцитонина, тироглобулина, тироидной пероксидазы и кератина. Медуллярный рак по течению более агрессивен по сравнению с папиллярным и фолликулярным раком, дает метастазы в близлежащие лимфатические узлы и может распространяться на трахею и мышцы. Сравнительно реже имеют место метастазы в легкие и различные внутренние органы. Анапластический рак (недифференцированный рак) представляет собой опухоль, состоящую из так называемых клеток карциносаркомы и эпидермоидного рака. Обычно такой опухоли предшествует узловой зоб, который наблюдался в течение многих лет. Заболевание развивается у лиц пожилого возраста, когда щитовидная железа начинает быстро увеличиваться, приводя к явлениям нарушения функции органов средостения (удушье, затруднение при глотании, дисфония). Опухоль быстро растет, прорастая близлежащие структуры, и приводит к летальному исходу в течение около года. Реже встречаются метастазы злокачественной опухоли в щитовидную железу. К таким опухолям относятся меланома, рак молочной железы, желудка, легких, поджелудочной железы, кишечника, а также лимфомы. Последние относятся к быстрорастущим опухолям. Лимфома - диффузная опухоль, которая может возникнуть на фоне предшествующего аутоиммунного тиреоидита, в связи с чем имеются большие трудности в дифференциальной диагностике этих двух заболеваний. Лимфома может возникать в щитовидной железе и как самостоятельное заболевание. Заболевание встречается, как правило, у взрослых, щитовидная железа быстро увеличивается в размерах, часто болезненная, быстро вовлекаются в процесс лимфатические узлы и развиваются симптомы сдавления средостения. Следует подчеркнуть, что лимфома является лишь одной из быстрорастущих опухолей щитовидной железы, которая хорошо отвечает на терапию ионизирующей радиацией. В последние годы многие исследователи указывают, что рак щитовидной железы может протекать с картиной тиреотоксикоза и наличие последнего еще не исключает рака щитовидной железы, как это считалось раньше.

ПАТОГЕНЕЗ ИЛИ ПРИЧИНЫ РАЗВИТИЯ Почти во всех странах мира отмечается увеличение частоты рака щитовидной железы. Хотя причина его точно не установлена, но определенная роль в этом отводится йодной недостаточности, воздействию ионизирующей радиации (внешнего облучения или приема радиоактивного йода), нарушению иммуннонейро-эндокринного гомеостаза. Рак щитовидной железы может развиваться на фоне предшествующих доброкачественных аденом, многоузлового зоба, кист. Генетические факторы (наследственность) также включены в патогенез рака щитовидной железы.

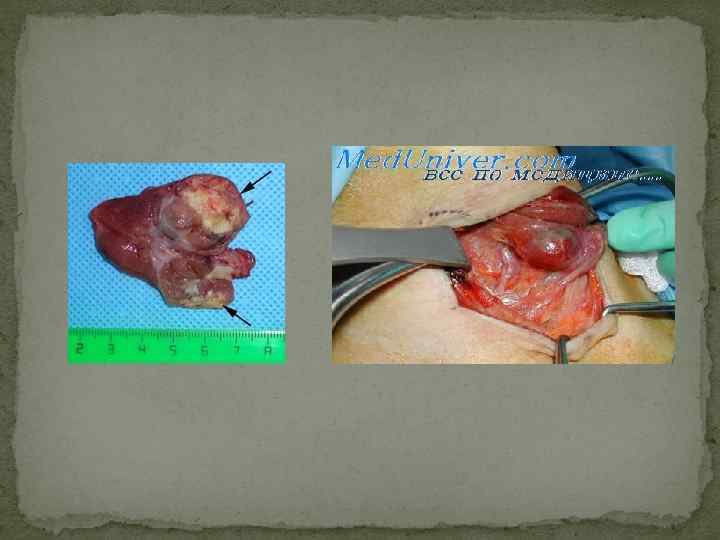
КЛИНИЧЕСКАЯ КАРТИНА Очень часто рак щитовидной железы представляет собой одиночный безболезненный узел, который расценивается как аденома или узловой зоб, реже в начале заболевания имеется диффузное увеличение щитовидной железы. Такая “аденома” склонна к более быстрому росту, чем обычный узловой зоб, приобретая более плотную консистенцию и вызывая чувство давления в области щитовидной железы. При обследовании выявляется увеличение регионарных лимфатических узлов, свидетельствующих о злокачественном течении опухоли щитовидной железы. Функциональное состояние щитовидной железы, как правило, остается в пределах нормы и лишь при значительных размерах опухоли могут развиваться явления гипотиреоза и значительно реже - умеренного тиреотоксикоза. В других случаях первые клинические признаки рака щитовидной железы являются следствием его метастазирования в легкие, кости или реже в головной мозг и надпочечники. Опухоль щитовидной железы может достигать больших размеров, прорастая капсулу железы и фиксируя трахею и другие органы средостения (пищевод, возвратный нерв), может вызывать нарушение глотания, одышку, осиплость и огрубение голоса. Щитовидная железа при этом становится неподвижной.

Диагноз и дифференциальный диагноз. Необходимо дифференцировать рак щитовидной железы от единичного и многоузлового зоба. Единичные аденомы растут медленно, в течение нескольких лет, и обычно обнаруживаются пальпаторно при достижении диаметра не менее 0, 5 -1 см, как правило, случайно. Нарушение глотания, затруднение дыхания, боль характерны для опухолей больших размеров. Около 60 -70% узлов или аденом щитовидной железы гипофункциональны и плохо поглощают радиоактивный йод (“холодный” узел), 20 -25% по своей способности поглощать радиоактивный йод не отличаются от нормальной (близлежащей) ткани железы и около 5 -10% имеет повышенную функциональную активность (“горячий” узел), вызывая клиническую картину тиреотоксикоза; такие узлы, как правило, имеют диаметр 3 см и более. Это различие в поглощении радионуклида выявляется при сканировании.

Сканограмма при раке щитовидной железы Многоузловой зоб развивается в течение многих лет, чаще у лиц, проживающих в йоддефицитных районах. Онкологическая настороженность в йоддефицитных регионах должна быть даже повышена. Аутоиммунный тиреоидит, как и диффузный токсический зоб, как правило, не малигнизируется, однако сочетание аутоиммунного тиреоидита или диффузного токсического зоба и рака щитовидной железы не является редкостью. “Горячие” узлы также редко малигнизируются, “холодные” узлы озлокачествляются чаще. Часто диагноз рака щитовидной железы основывается на клинической картине. Правильной диагностике помогает биопсия щитовидной железы.

Лечение рака щитовидной железы В настоящее время применяется тиреоидэктомия, лечение радиоактивным йодом, рентгенотерапия. Во всех случаях оперативного лечения узлового зоба удаленную опухоль направляют на экспрессдиагностику и операцию заканчивают только после получения результатов гистологического исследования. При раке щитовидной железы объем вмешательства зависит от стадии процесса: производится тотальная (полная) или частичная резекция щитовидной железы с удалением лимфатических узлов и вовлеченных в процесс окружающих тканей. В тех случаях, когда опухоль локализуется в области одной доли щитовидной железы, резекции подлежит и вторая доля, так как в большинстве случаев через внутриорганные лимфатические пути опухоль распространяется и на вторую долю железы. Некоторые авторы при папиллярном или фолликулярном раке, при которых размер опухоли не более 2 см, рекомендуют проводить удаление лишь одной пораженной доли щитовидной железы. После удаления злокачественной опухоли щитовидной железы назначается не менее чем на 8 недель терапия тиреоидными гормонами для подавления секреции ТТГ и возможного подавления оставшихся единичных клеток опухоли. Через 2 -3 недели после прекращения приема тиреоидных гормонов уровень ТТГ в сыворотке крови повышается до 45 -50 мк. ЕД/мл, происходит стимуляция оставшейся ткани, которая способна накапливать йод. Больному после приема радиоактивного йода производят сканирование ткани щитовидной железы. Если обнаруживается только оставшаяся тироидная ткань в области щитовидной железы, проводят лечение радиоактивным йодом. В случае обнаружения отдаленных метастазов дозу радиоактивного йода увеличивают. При наличии отдаленных метастазов дозу йода можно повторять через 2 -3 мес. Рентгенотерапия применяется при анапластическом раке и злокачественных лимфомах, которые являются рентгеночувствительными. Рентгенотерапия может проводиться в сочетании с химиотерапией. Лечение радиоактивным йодом проводят при неоперабельной опухоли, а также во всех случаях после удаления гистологически подтвержденного рака щитовидной железы. Прогноз рака щитовидной железы несколько лучше по сравнению с раком других органов.
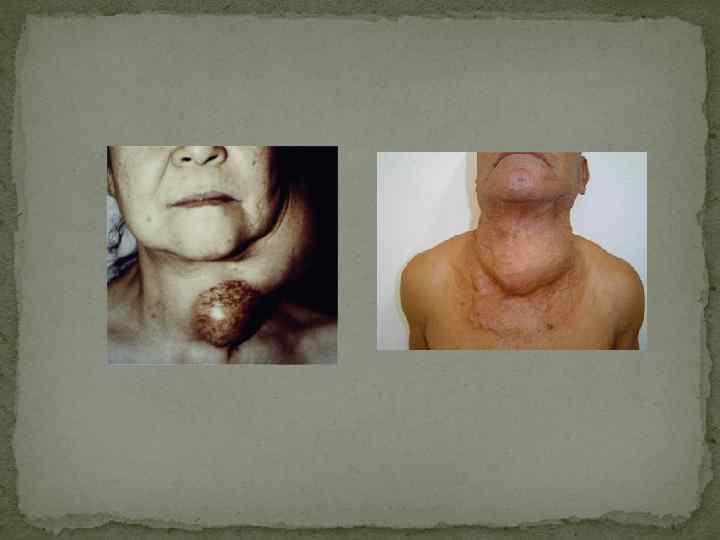

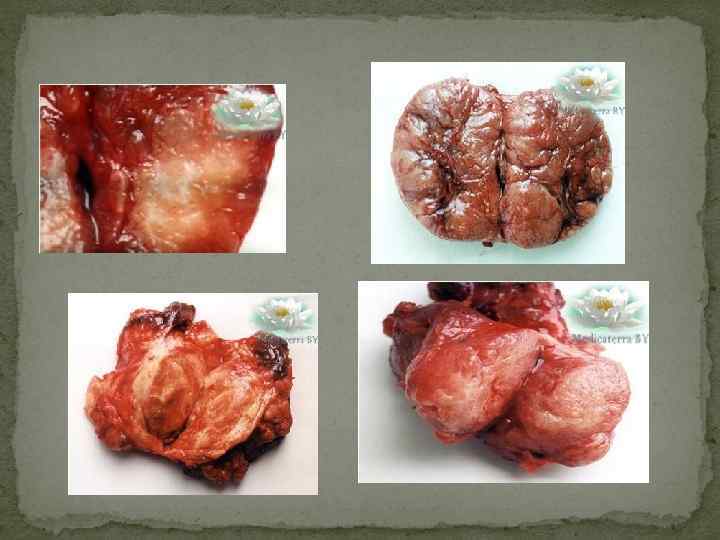
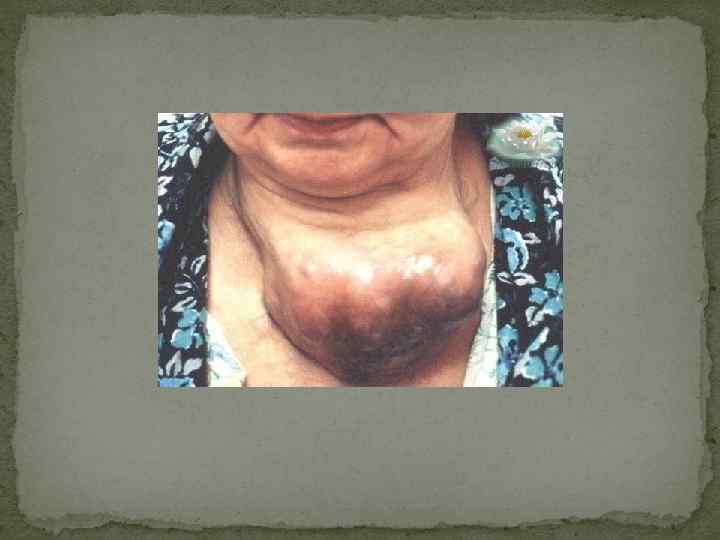
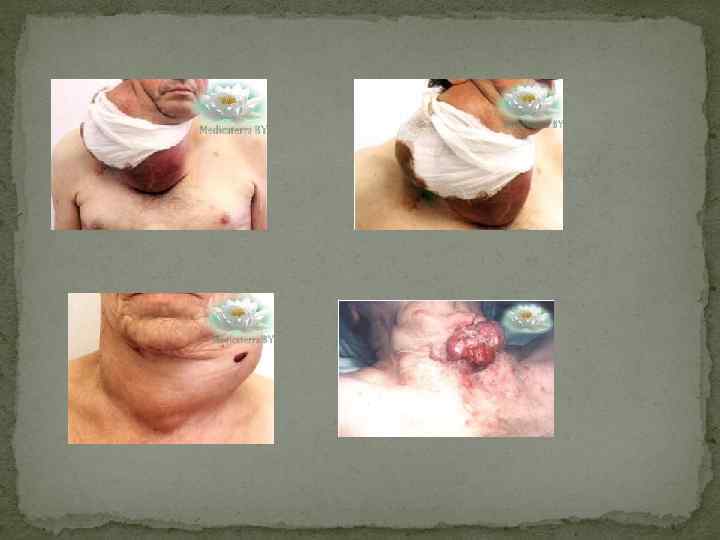

Ø Ø Тиреоидэктомия. Данное вмешательство подразумевает удаление всей щитовидной железы. Технически это может быть выполнено экстра- и субфасциально. Выполнение первого типа вмешательства более опасно в связи с риском повреждения паращитовидных желез и возвратных гортанных нервов, однако обеспечивает необходимую онкологическую радикальность и возможность проведения радиойодной диагностики и лечения при высокодифференцированных карциномах. Напротив, при лечении доброкачественного многоузлового или рецидивного зоба нет необходимости тщательного удаления всей ткани щитовидной железы. В таких ситуациях обычно хирург стремится оставить макроскопически неизмененную ткань, если таковая имеется, а при необходимости тиреоидэктомии она выполняется субфасциально, как и при лечении хронических тиреоидитов. С точки зрения объема оставляемой ткани и последующей функции тиреоидэктомия остается операцией, при которой удаляется вся щитовидная железа. В практической деятельности используется еще термин “Окончательная тиреоидэктомия”, отражающий повторное вмешательство, необходимое после нерадикальных операций при раке щитовидной железы. Предельно субтотальная резекция щитовидной железы. Объем этой операции находится между субтотальной резекцией, при которой оставляются культи ткани около 5 г с каждой стороны и тиреоидэктомией, когда макроскопически определяемой ткани нет. Чаще всего такая ситуация возникает при многоузловых зобах с почти полным поражением щитовидной железы. В этом случае, когда у хирурга нет оснований предполагать озлокачествление, там, где это возможно, оставляются, минимальные кусочки ткани на капсуле железы (их размер обычно не превышает 0, 5 см). Субтотальная резекция щитовидной железы. По объему вмешательства этот тип операции подразумевает формирование культей с общим объемом около 10 г (обычно две по 5). Безусловно, большинство субтотальных резекций производятся при диффузном тиреотоксическом зобе, но это не аксиома. Так, например, наличие злокачественной опухоли или многоузловое поражение могут послужить основанием к выполнению тиреоидэктомии при тиреотоксикозе, а иногда субтотальный объем резекции необходим при эутиреоидных формах зоба. Гемитиреоидэктомия. Собственно гемитиреоидэктомия тоже может быть выполнена по экстра- или субфасциальной методике, но в подавляющем большинстве оказывается субфасциальной, так как экстрафасциальное ее проведение не может иметь смысла ввиду наличия противоположной доли. Редким исключением являются ситуации, когда, из-за невозможности окончательно подтвердить или опровергнуть наличие злокачественного роста во время операции, приходится допускать возможность повторного вмешательства (окончательной тиреоидэктомии). Тогда при выполнении гемитиреоидэктомии ее совершают экстрафасциально. На практике же оказывается, что сам факт наличия злокачественного процесса обычно выясняется при получении результата экспресс-гистологического анализа, то есть после проведения гемитиреоидэктомии, а значит тип ее определяется дооперационной настроенностью хирурга. Так или иначе, относительно объема оставляемой ткани, эти операции могут считаться идентичными.

Ø Гемитиреоидэктомия и субтотальная резекция контралатеральной доли. Ø Ø Ø Как следует из названия этот термин соответствует полному удалению одной доли и резекции противоположной с оставлением около 5 г ткани железы, что соответствует половинному объему субтотальной резекции. Гемитиреоидэктомия и резекция контралатеральной доли. В отличие от предыдущего типа вмешательства, в данном случае подразумевается удаление меньшего количества ткани контралатеральной доли. Следуя логике он должен быть более 5 г. Резекция обеих долей щитовидной железы. Обычно эта операция выполняется при наличии доброкачественных узлов в обеих долях, когда с обеих сторон хирург оставляет более 5 г (1/3 нормального объема доли). Субтотальная резекция доли щитовидной железы. Результатом этой операции (на одной доле) является оставление с одной стороны культи около 5 г. Резекция доли щитовидной железы. Как менее обширное вмешательство на одной доле щитовидной железы, этот тип операции обозначает, что объем оставленой ткани превышает 5 г. Удаление перешейка щитовидной железы. Эта операция выделена как самостоятельная единица для тех случаев, когда только в перешейке определяется небольшой узел и объем резекции каждой из долей не превышает 1/3 (5 г). Вскрытие абсцесса щитовидной железы и открытая биопсия приведены для полноты описания возможных вмешательств и не являются предметом дискуссии.
Хирургические заболевания щитовидной железы.ppt