органика байланыс турлери.ppt
- Количество слайдов: 71

Химиялық байланыстың (типтері), валенттілік, тотығу дәрежесі

ДЕМОКРИТ (б. э. д. 460 – 370 ж. ж. ) Әлемде тек қана атомдар, бос кеңістік және қозғалыс бар, деп оқытты. Ол атомдардың бос кеңістікте соқтығысуының механикалық қажеттілігін ойлап тапты. Түсінікті болуы үшін, атомдарды бір-бірімен бекіту үшін ілгешекпен, ілгекті пайдаланды.

ПЛАТОН (б. э. д. 427 – 347 ж. ж. ) Атомдар – бұл екі түрлі тік бұрышты үшбұрыштар: катеті тең бүйірлі және гипотенузаның жартысына тең. Платон өзінің шәкірттеріне өте көрнекі түрде үшбұрыштың бөлшектері арқылы орындалатын барлық өзгерістерді көрсетті.

ЙЁНС-ЯКОБ БЕРЦЕЛИУС (1779 – 1848 ж. ж. ) Электрохимиялық теория Химиялық элементтер арасындағы байланысты олардың электрлік қасиеті тұрғысынан қарастырды. Яғни, химиялық элементтердің бір түрінде оң, ал екіншілерінде теріс заряд басым болады. Оң заряды басым элементтерге металдарды, ал теріс заряды бар элементтерге металл еместерді жатқыза отырып, химиялық қосылыстар осылардың арасындағы тартылыстан туындайды деп есептелінді.

ХИМИЯЛЫҚ БАЙЛАНЫС - химиялық қосылыстағы атомдардың бір-біріне әсері арқылы жүзеге асатын күштер жиынтығы
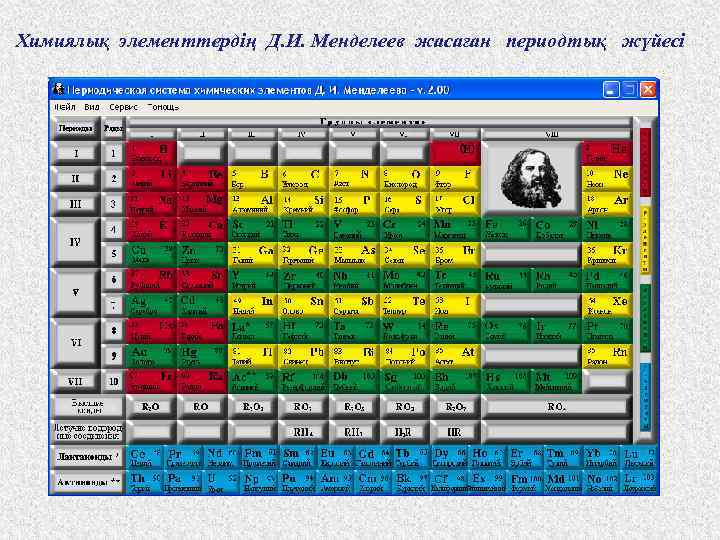
Химиялық элементтердің Д. И. Менделеев жасаған периодтық жүйесі

Химиялық байланыс түзілуде ең басты рольді электрондар атқарады. Химиялық байланыс түзілген кезде атомдардың электрондық құрылымы өзгеріске ұшырайды. Атомдардың электрондық құрылымы анағұрлым тұрақты болған жағдайда ғана химиялық байланыс түзіледі.

Сыртқы электрондық қабаты ns 2 np 6 типті болған жағдайда электронды октет және 1 s 2 аяқталған, анағұрлым тұрақты болады. Басқа элементтің атомдары химиялық байланыс түзу кезінде осындай электрондық құрылым түзуге ұмтылады. Атомдар арасында тұрақты (аяқталған) электрондық құрылымда болатын ең маңызды екі түрлі химиялық байланыстың түрі иондық (электровалентті) және ковалентті байланыс бар.

Иондық химиялық байланыс электртерістілігі бойынша айырмашылығы үлкен металл мен бейметалл атомдары арасында түзіледі. Иондық химиялық байланыс қарама – қарсы зарядталған иондардың электростатикалық тартылысы нәтижесінде жүзеге асады.

КОССЕЛЬ (Kossel), Вальтер 1888 – 1956 ж. ж. Иондық байланыс теориясын 1916 жылы неміс ғалымы В. Коссель ұсынған болатын. Бұл теория типтік металдар мен типтік бейметалдар атомдары арасында: Cs. F, Cs. Cl, Na. Cl, KF, KCl, Na 2 O, Ca. O түзілетін байланысты түсіндіреді. Осы теорияға байланысты иондық байланыстың түзілу кезінде типтік металл атомдары электронды береді, ал типтік бейметалл атомдары электронды қосып алады.

Металдар химиялық әрекеттесуде валенттік электрондарын беріп, оң зарядты иондарға (катиондарға): Na 0 – e = Na+ Бейметалдар электрондар қосып алып, теріс зарядты иондарға (аниондарға) айналады: Cl 0 + e = Cl-. Әр аттас зарядты иондар бірін-бірі тартып молекула құрайды:

Иондар түзілу арқылы жүзеге асатын байланыстарды иондық байланыс, қосылыстың өзін иондық қосылыс деп атайды. Иондық қосылыстардың қайнау, балқу температурасы жоғары, қызуға тұрақты, олар полюстік еріткіштерде тез ериді, ерітінділері электр тогын жақсы өткізеді. Na Na. Cl Cl
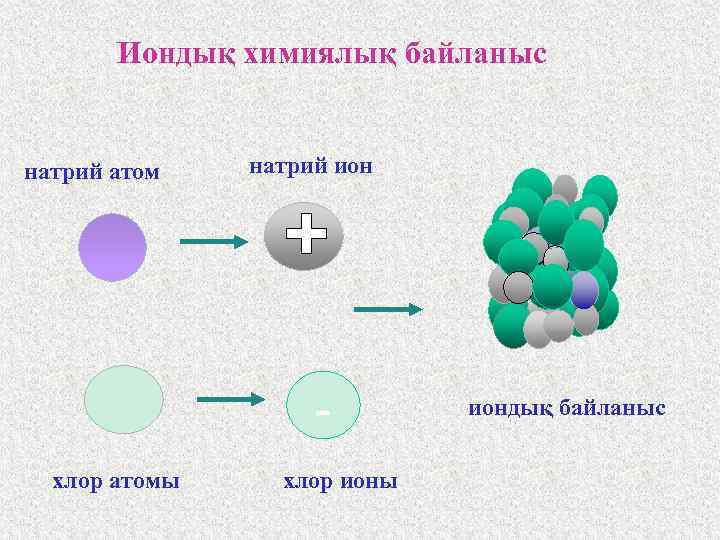
Иондық химиялық байланыс натрий атом натрий ион хлор атомы хлор ионы иондық байланыс

Иондық қосылыстар молекуласындағы барлық иондар зарядтарының алгебралық қосындысы нөлге тең болу қажет. Осыған байланысты кез келген молекула электр бейтарап бөлшек болып табылады.

Ковалентті байланыс – бұл атомдар арасында ортақ электрондық жұп есебінен жүзеге асырылатын химиялық байланыс. Ковалентті химиялық байланыста электрон жұбының атомдардың арасында орналасуына қарай полюсті және полюссіз деп екіге бөлінеді.

Джильбер Льюис Ковалентті байланыс теориясын 1916 жылы американдық ғалым Джильбер Льюис ұсынды. Осы теорияға сай, ковалентті байланыс түзілуінің негізгі себебі атомдар арасында ортақ электрондық жұптың түзілуі болып табылады. Ковалентті байланыс жай зат молекулалары арасында (H 2), Cl 2 , O 2, N 2 және әр түрлі бейметалдар атомдары арасында (HCl, H 2 O, PCl 3 , NH 3 CO 2 түзіледі.

Полюссіз ковалентті химиялық байланысты молекулада электрон жұбы атомға ауыспай, симметриялы түрде ортада орналасады. Полюссіз химиялық байланыстағы қосылыстардың қайнау және балқу температуралары төмен, полюсті еріткіштерде иондар түзбейді, электр тоғын өткізбейді.

Сутек атомының электрондық формуласы 1 s 1. Сутектің электртерістілігі 2, 1. S – электрондарының электрон бұлттары сфера (шар) тәрізді, олардың өзара әсерлесуін былай көрсетуге болады: сонда s электрондарының бұлттары өзара қабысып, екі электрон екі ядроға да ортақ, олардан бірдей қашықтықта орналасады.

Сутегі молекуласындағы атомдардың ұсталып тұрған күштерінің табиғатын алғаш 1927 жылы ағылшын ғалымдары Гейтлер мен Лондон кванттық механика тұрғысынан түсіндірді. Олар Шредингер теңдеуі бойынша байланыстың екі сипатын - энергия мен ядро аралық ұзындықты есептеді. Сутегі молекуласы төрт микробөлшектен тұрады. Екі атом бір – біріне жақындаған кезде тартылыс күші, ал екі ядро мен екі электрон арасында тебілу күші пайда болады. Осы тартылыс және тебілу күші теңескен жағдайда молекула тұрақты күйге келеді.
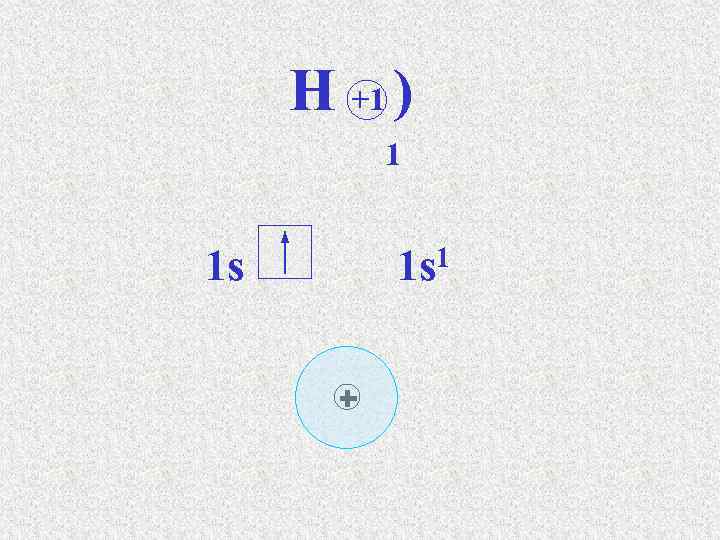
H +1 ) 1 1 s
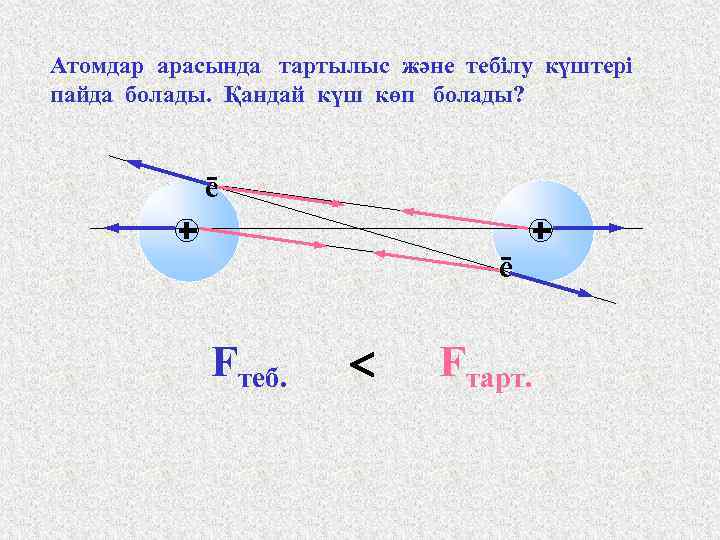
Атомдар арасында тартылыс және тебілу күштері пайда болады. Қандай күш көп болады? ē ē Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fотт. Fпр.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fотт. Fпр.
Fотт. Fпр.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.
Fтеб. Fтарт.

АТОМДАР ЖАҚЫНДАСҚАНДА ОЛАРДЫҢ ЭЛЕКТРОНДЫҚ БҰЛТТАРЫ БҮРКЕСУІНЕН ЯДРОЛАРДЫҢ АРАСЫНДАҒЫ КЕҢІСТІКТЕ МАКСИМАЛ ЭЛЕКТРОН ТЫҒЫЗДЫҒЫ БАР МОЛЕКУЛАЛЫҚ БҰЛТ ТҮЗІЛЕДІ.
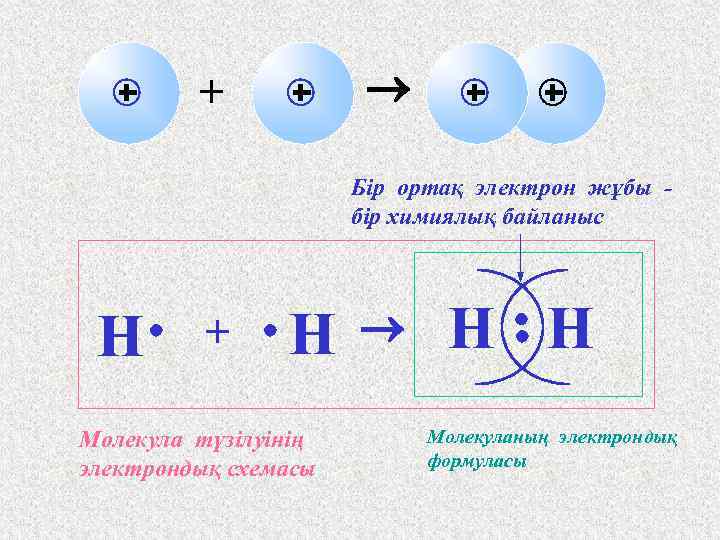
+ Бір ортақ электрон жұбы бір химиялық байланыс 2ē Н + Н Молекула түзілуінің электрондық схемасы Н Н 2ē Молекуланың электрондық формуласы
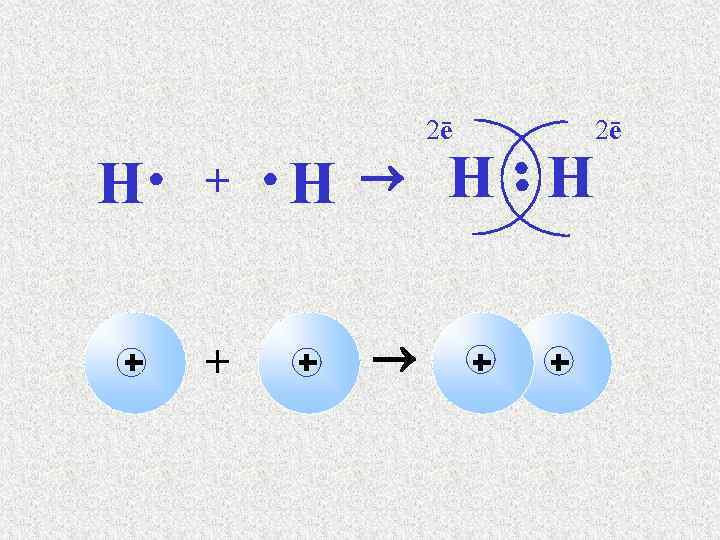
2ē Н + + Н Н Н 2ē
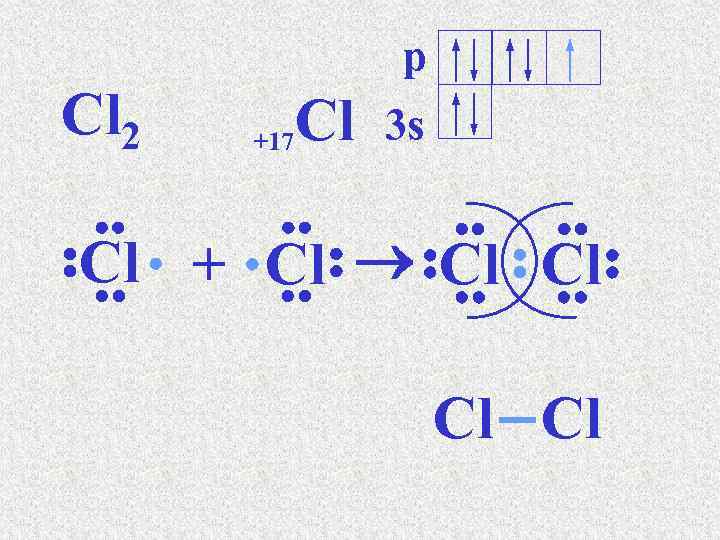
p Cl 2 +17 Cl 3 s Cl + Cl Cl

Электронды-графикалық формуласын қарасақ, валенттілік электрондар саны 6, оның екеуі дара күйінде, міне, осы электрондар екінші оттек атомындағы дәл осындай электрондармен екі жұп түзеді, яғни байланыс саны екі. Енді әр атом ядросын 8 электроннан айналатын болады. Сөйтіп, бұл мысалдан да көретініміз молекула түзілгенде аяқталған 8 электронды қабаттың пайда болуы. Оттек атомдарының тотығу дәрежелері нөлге тең, валенттіліктері ІІ-ге тең болады. Еселі байланыс дара байланысқа қарағанда беріктеу болады.
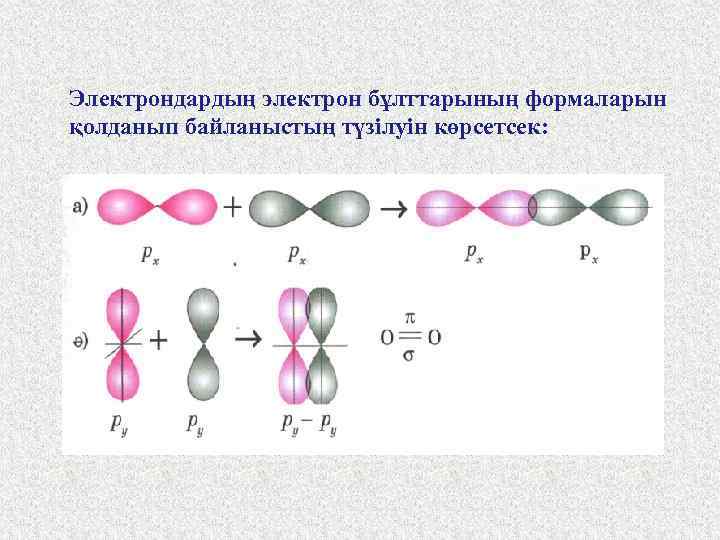
Электрондардың электрон бұлттарының формаларын қолданып байланыстың түзілуін көрсетсек:

α - байланыс дегеніміз электрон бұлттарының қабысу ауданы ядролардың қосылу сызығының бойында жатқанда түзілетін байланыс (а). Ал π-байланыс — электрон бұлттарының қабысу ауданы ядроларды қосатын сызықтың екі жағында орналасқанда түзіледі. Оттегі молекуласында атомдар бірбірімен екі байланыспен байланысқан, оның бірі - α болса, екіншісінің π-байланыс екендігін байқайсыңдар. Олай болса π - байланыс, тек қайталанған байланыстарда болса, α -байланыс дара байланыс кезінде түзіледі.
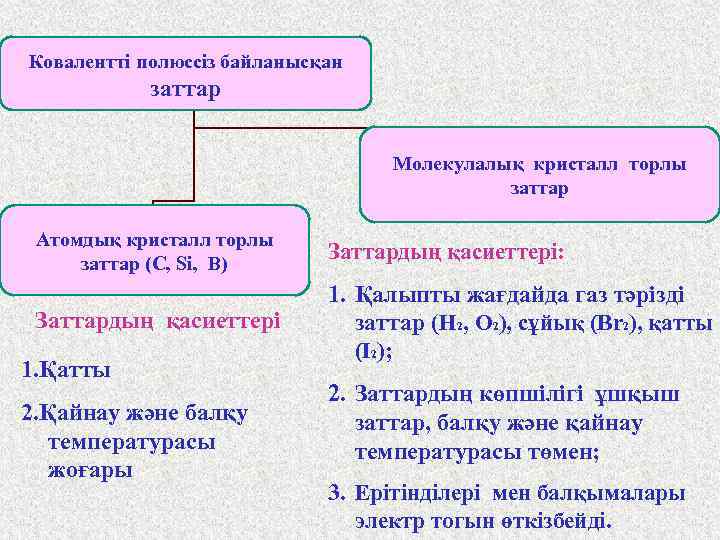
Ковалентті полюссіз байланысқан Вещества с КНС имеют: заттар Молекулалық кристалл торлы Молекулярную кристаллическую решетку (заттар все остальные) Атомдық кристалл торлы Атомную кристаллическую заттар (С, Si, B) решетку (C, Si, B) Заттардың қасиеттері 1. Қатты 2. Қайнау және балқу температурасы жоғары Заттардың қасиеттері: 1. Қалыпты жағдайда газ тәрізді заттар (H 2, O 2), сұйық (Br 2), қатты (I 2); 2. Заттардың көпшілігі ұшқыш заттар, балқу және қайнау температурасы төмен; 3. Ерітінділері мен балқымалары электр тогын өткізбейді.

Полюсті коваленттік байланыс дегеніміз байланыстырушы электрон жұбының бұлты электртерістігі басым элемент атомына қарай ығыса орналасқан байланыс. Молекуланың полюстілігі диполь моменті арқылы көрсетіледі. Полюсті молекулалардың қайнау және балқу температурасы төмен, полюсті еріткіштерде үйектеліп иондарға ыдырайды.
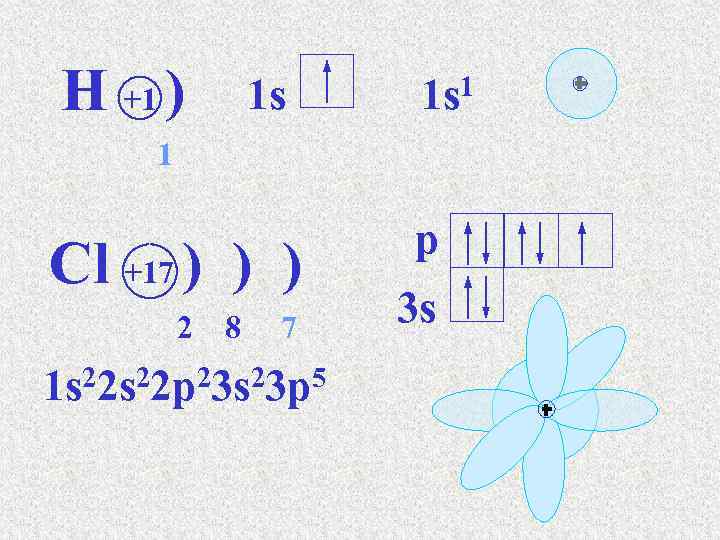
H +1 ) 1 s 1 1 s 1 Cl +17 ) ) ) 2 8 7 22 s 22 p 23 s 23 p 5 1 s p 3 s
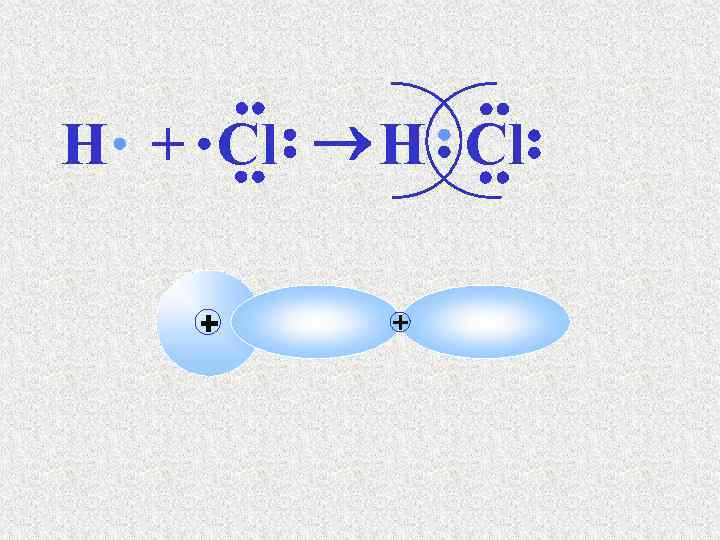
H + Cl H Cl

Ковалентті полюсті байланысқан заттар Вещества с КПС имеют: Молекулалық кристалл торын Молекулярную кристаллическую (барлық басқа заттар) решетку (все остальные) Атомдық кристалл Атомную торлар крисаллическую Решетку (Si. C, 2) 2) (Si. C, Si. O Заттардың қасиеттері: 1. Қалыпты жағдайда газтәрізді, сұйық, қатты; Заттардың қасиеттері: 2. Заттардың көпшілігі ұшқыш заттар, қайнау, балқу температурасы to төмен; 1. Қатты; 2. Балқу to жоғары. 3. Ерітінді және балқыма күйінде электр тогын өткізеді.

Металдық кристалл торының түйіндерінде атомдар немесе олардың иондары орналасатыны белгілі. Металдық тордағы бостау күйдегі делокальданған электрондар көптеген ядролардың арасында өзара тарту күштерін тудырып, металдық байланыс түзеді. Металдық байланыстың түзілу схемасы (М – металл): Me – ne- → Me+n Мұндай қабілетті металдар бос күйде де, химиялық әрекеттесу кезінде де көрсетеді. Бос күйдегі металдың белгілі физикалық қасиеттері: электр және жылу өткізгіштігі, қаттылығы, иілімділігі, созылғыштығы, өзіне тән жылтыры, т. б. бұлардың барлығы да металдық байланысқа тәуелді. _

Химиялық байланыстың негізгі сипаттамалары: • байланыс энергиясы • байланыс ұзындығы • валенттік бұрыш Байланыс энергиясы – өзара байланысқан атомдарды не иондарды бір – бірінен ажырату үшін жұмсалатын энергия. Байланыс ұзындығы – химиялық байланыстағы атомдар ядроларының арасындағы қашықтық, валенттік бұрыш – байланысқан атомдар ядролары арқылы жүргізілетін жорамал сызықтар арасындағы бұрыш. Бұл көрсеткіштер зат молекуласының құрылысын, пішінін және беріктігін сипаттайды.

Тотығу дәрежесі, тотығу саны – химиялық қосылысты тек иондардан тұрады деп қарастырғанда әр атомда болатын шартты зарядтың сан шамасы. Бұл ұғым молекуладағы атомдардың күйін сипаттау үшін қолданылады. Кез келген қосылысты ионды қосылыс деп қарастыруға болмайтындықтан, тотығу дәрежесі шартты түрде алынады.

1. Барлық күрделі қосылыстағы металдар тек қана оң тотығу дәрежесін көрсетеді. 2. Бейметалдар оң және теріс тотығу дәрежесін көрсете алады. Бейметалдар сутекпен және металдармен қосылыстарында үнемі теріс мәнге ие. 3. Элементтің ең жоғарғы (максимальді) тотығу дәрежесі периодтық кестедегі топтың нөміріне байланысты болады. 4. Металдардың ең кіші тотығу дәрежесі нөлге тең болады. 5. Ең жоғарғы тотығу дәрежесі мен ең төмен тотығу дәрежесіндегі аралықты аралық тотығу дәрежесі деп атайды.
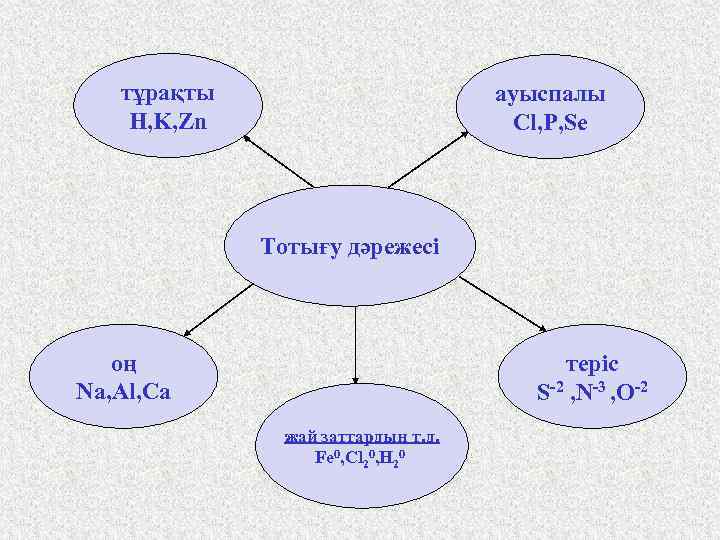
тұрақты H, K, Zn ауыспалы Cl, P, Se Тотығу дәрежесі оң Na, Al, Ca теріс S-2 , N-3 , O-2 жай заттардың т. д. Fe 0, Cl 20, H 20

Тотығу дәрежесі бойынша химиялық формуланы құрастыру. АЛГОРИТМ: 1. Химиялық элементтердің таңбасын жазамыз. Al S 2. Д. И. Менделеев кестесінен элементтердің ТОТ дәрежесін табамыз Al+3 S-2 3. ЕКОЕ тауып индекстерді анықтаймыз. Al 2 S 3 +3 S-2 Al S ЕКОЕ=6 Al 2 3 1. ЕРЕЖЕ: элементтердің тотығу дәрежесінің алгебралық 2. қосындысының жиынтығы нөльге тең.
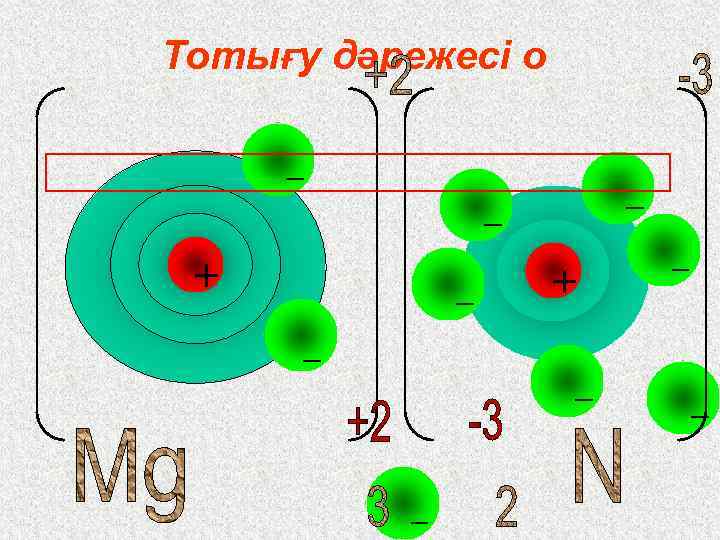
Тотығу дәрежесі о

Күкірттің тотығу дәрежесі қандай? S+16 ))) 1 s 22 p 63 s 23 p 43 d 0 2 8 6 _ 2 жұптасп. е т. д. -2 3 s 2 S* 3 s 2 3 p 4 3 d 0 H 2 S 3 d 1 _ 4 жұптасп. е т. д. +4 SO 2 _ 6 жұптасп. е т. д. +6 S** 3 s 2 3 p 3 3 d 2 SO 3

Элементтің тотығу дәрежесін анықта Al 2 O 3 Ca 3 N 2 K 2 Se P 2 O 5 Cl 2 O 7 As 2 O 3 Al 2+3 O 3 -2 Ca 3+2 N 2 -3 K 2+ Se-2 P 2+5 O 5 -2 +7 O -2 Cl 2 7 +3 O -2 As 2 3

Кез келген молекула электробейтарап бөлшек. Молекуладағы барлық атомдардың тотығу дәрежесінің қосындысы нөльге тең болады. Әр түрлі қосылыстағы көміртектің тотығу дәрежесін анықтап көрейік. Көміртектің валенттілігін көрсету үшін графикалық формуласын көрсетеміз. Бұл қосылыстарда көміртек барлық уақытта төрт валентті болады, ал тотығу дәрежесі -4 тен + 4 дейін өзгеріп отырады. Барлық уақытта элементтің тотығу дәрежесі валенттілігіне сай келе бермейді.


Валенттілік. Атом құрылысы мен химиялық байланыс тұрғысынан қарағанда валенттілік әрбір атомның молекула түзуге жұмсайтын электрондарының санымен анықталады. Атом, химиялық байланыс түзуге неше электрон жұмсаса, оның валенттігі де сонша болады. Мысалы, сутек молекуласын түзуге әрбір сутек атомы бір электроннан, оттек молекуласын түзуге оттектің әрбір атомы екі электроннан, азот молекуласын түзуге әрбір азот атомы 3 электроннан жұмсайды.

Сондықтан сутек атомы молекуласында сутек атомдары 1 валентті, оттек молекуласында оттек атомдары екі 2 валентті, азот молекуласында азот атомдары 3 валентті болады. Молекуладағы атомдар арасындағы әрбір қос электрондарды бір сызықшамен ауыстыру арқылы заттың құрылымдық формуласын құрады. Құрылымдық формула молекуладағы атомдардың валенттілігін көрсетеді.

Бір сызықша бір валенттілік байланысқа сәйкес келеді. Сонымен бірге құрылымдық формуласы молекуладағы элементтердің бір – бірімен байланысу ретін де білдереді. Әрбір элементтен шығатын сызықша саны сол элементтің валенттілігін көрсетеді. Мысалы, мына көрсетілген │ Н -, О= , -N-, - C - │

Элементтің валенттілігі - бұл берілген молекуладағы атомның басқа атоммен түзетін химиялық байланыстың саны. Бір химиялық байланыс түзу үшін атом бір жұптаспаған электрон ұсынады. Сондықтан элементтің валенттілігі атомдағы жұптаспаған электрон санымен анықталады. Көптеген элемент атомдары өздерінің валенттілігін (жұптаспаған электрон санын) қалыпты жағдайдан қозған жағдайға ауысқан жағдайда көбейте алады. Атомның қозған жағдайы - бұл қалыпты жағдаймен салыстырғанда жоғары энергиясы мөлшерімен ерекшелінеді.
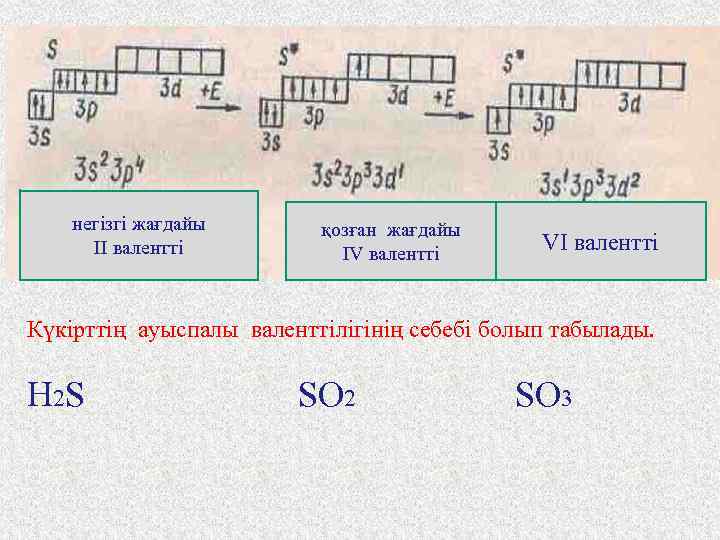
негізгі жағдайы ІІ валентті қозған жағдайы IV валентті VI валентті Күкірттің ауыспалы валенттілігінің себебі болып табылады. H 2 S SO 2 SO 3

Назарларыңызға рахмет!
органика байланыс турлери.ppt