
химия Хи мия (от араб. , کﻴﻤﻴﺎﺀ произошедшего, предположительно, от египетского слова km. t (чёрный), откуда возникло также название Египта, чернозёма и свинца — «черная земля» ; другие возможные варианты: др. -греч. χυμος — «сок» , «эссенция» , «влага» , «вкус» , др. -греч. χυμα — «сплав (металлов)» , «литье» , «поток» , др. -греч. χυμευσις — «смешивание» ) — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются. Поскольку все вещества состоят из атомов, которые благодаря химическим связям способны формировать молекулы, то химия занимается прежде всего рассмотрением перечисленных выше задач на атомно-молекулярном уровне, т. е. на уровне химических элементов и их соединений. Химия имеет немало связей сфизикой и биологией, по сути граница между ними условна, а пограничные области изучаются квантовой химией, химической физикой, физической химией, геохимией, биохимией и другими науками.

История возникновении химии • История возникновения химии делится на несколько этапов, начиная от древнего мира и до современности. • Химия – это одна из естественных наук, т. е. наук об окружающем мире, природе и явлениях, происходящих в ней, превращениях веществ. • Еще в глубокой древности человек заметил, что вещества способны изменяться, превращаться в другие, обладающие новыми свойствами. • Костер стал первой химической лабораторией человека. После обжига глины в огне она становилась прочной, из нее можно было делать нехитрую посуду. На огне человек научился готовить пищу из мяса убитых животных, плодов растительного мира. Здесь же человек случайно получил первые металлы – медь, олово, свиней, а также стеклянные изделия из, казалось бы, обыкновенных камней. • Так появились первые, как мы сейчас говорим, химические ремесла – гончарное и металлургическое. Примерно 7000 лет назад человек научился выплавлять медь и делать из нее различные изделия – орудия труда, предметы домашнего обихода, оружие. Этот период в истории древней цивилизации получил название медный век. • К 4000 г. до н. э. наступил новый этап в истории возникновении химии, люди научились выплавлять бронзу – сплав меди с оловом, который был гораздо более твердым, чем медь. Бронза же сразу стала использоваться для изготовления мечей, наконечников стрел и копий, щитов. Наступил бронзовый век. • В последнее тысячелетие до новой эры человек овладел способом получения железа из руд. Это стало поворотным моментом и в истории металлургии, и в истории общества. Так пришло время железного века, который на самом деле продолжался много сотен лет. • В те давние времена люди могли получать не только металлы. Стекло фаянс, минеральные и растительные краски, чернила, косметика и лекарственные препараты – вот далеко не полный перечень изделий, которые мог изготовить человек уже тогда с помощью различных химических превращений. • На рубеже старой и новой эры зародилось и само понятие «химия» . Есть несколько версий проявления этого термина. По одной из них это связано с древним названием Египта «Хем» и производным от него «хеми» – египетское искусство. По другой версии считается, что слово «химейя» – выделения соков, а затем и плавки металлов, происходит от древнегреческого «химос» , т. е. сок, литье.

• В середине первого тысячелетия новой эры, после падения Древнего Рима, центр цивилизации переместился на Ближний Восток. Именно там арабы преобразовали слово «химейя» в «алхимия» . Под этим словом понимались все знания, связанные с превращением веществ как практические, так и теоретические. • А главной теоретической идеей алхимии в течение почти полутора тысячи лет было превращение неблагородных металлов в благородные (золото и серебро) под действием так называемого философского камня. С помощью этого мифического «эликсира» надеялись также излечить все болезни и даже сделать человека бессмертным. Последователей этой идеи на арабском Востоке, а затем и в Европе стали называть алхимиками. Алхимиками были практически все ученые средневековья, монахи, врачеватели и даже короли. • Все их усилия получить дешевое золото оказались, конечно, бесплодными. Однако целый ряд практических достижений как алхимиков, так и ремесленников-практиков оставил заметный след в истории возникновении химии. Было получено много новых веществ, прежде всего важнейшие кислоты (серная, соляная, азотная), изобретены различные приборы и приспособления, которые с тех пор стали широко использоваться в химии. • Химия постепенно становилась все более практической областью деятельности, основной задачей которой становилось удовлетворение растущих потребностей общества: получение металлов из руд, пороха, стекла, красок, мыла и многих других, не менее необходимых для жизни веществ. Появились первые книги по практическим способам получения металлов, обработки различных веществ. Поиск эликсира долголетия привел к развитию медицинского направления – иатрохимии, которая с начала XVI в. стала основным видом деятельности химиков, постепенно заменяя прежние – попытки получения благородных металлов из неблагородных. • В алхимию все больше и больше проникало научное начало, желание узнать элементарную природу веществ, причины их способности превращаться в другие вещества. Ученые пытались дать разумные объяснения таким важнейшим для практики процессам, как горение, восстановление металлов из руд и окисление металлов. • В работе английского химика и физика Роберта Бойля было впервые дано научное определение понятия химический элемент, положено начало химическому анализу. Экспериментальные исследования Бойля стали началом химии как настоящей науки. Именно Бойль отбросил от названия «алхимия» приставку «ал» , тем самым как бы открыв новый период в жизни истории возникновения химии. • Превращению химии в настоящую науку в XVIII в. способствовали многие ученые, в том числе русский ученый М. В. Ломоносов и французский – А. Лавуазье. На основе многочисленных опытов по изучению процессов горения и окисления металлов они независимо друг от друга пришли к формулировке одного из самых важных законов химии – закона сохранения массы веществ при химических реакциях. • В XVIII в. было открыто много новых элементов, в том числе кислород, водород, азот. Было доказано, что воздух является смесью газов, а вода – сложным веществом. • В начале XIX в. английский ученый Д. Дальтон заложил основы химической атомистики, составил первую таблицу атомных весов, а итальянец А. Авогардо ввел в обиход понятие молекула. Атомномолекулярное учение стало основной химической теорией. Особенно большая роль в ее развитии в начале XIX в. принадлежит виднейшему шведскому химику Я. Берцелиусу. На основе теории Дальтона он осуществил реформу химии: разработал систему символов элементов, с помощью которых стали записывать формулы и уравнения. Он построил шкалу атомных масс, близкую к современной, ввел в обиход множество терминов и понятий, которые мы используем и сейчас. • В середине XIX в. русский ученый А. М. Бутлеров заложил основы теории строения органических соединений. В 1869 г. другой русский ученый Д. И. Менделеев открыл периодический закон химических элементов. Эти две научные идеи вместе с атомно-молекулярным учением стали основой современной химии. • Химия становилась такой большой наукой, что разделилась на отдельные ветки, такие, как органическая, неорганическая, аналитическая химия, и а позже – физическая химия, биохимия, агрохимия, химия твердого тела и др. • В настоящее время химия стала не только одной из важнейших областей человеческого знания, но и полем практической деятельности многих людей – ученых, инженеров, рабочих и др. Без химии невозможна жизнь современного общества. Она играет ключевую роль в обеспечении людей продовольствием, одеждой, энергией, тысячами самых разнообразных веществ, многих из которых просто нет в природе. • Химия – это наука, которая постоянно изменяет окружающий мир. Вместе с другими естественными науками она помогает глубже познать тайны природы и законы ее развития, сделать жизнь на Земле лучше для каждого человека.

Квантовая химия • Квантовая химия — это направление химии, рассматривающее строение и свойства химических соединений, реакционную способность, кинетику и механизм химических реакций на основе квантовой механики. Разделами квантовой химии являются: квантовая теория строения молекул, квантовая теория химических связей и межмолекулярных взаимодействий, квантовая теория химических реакций и реакционной способности и др. . Квантовая химия находится на стыке химии и квантовой физики (квантовой механики). Она занимается рассмотрением химических и физических свойств веществ на атомарном уровне (моделях электронно-ядерного строения и взаимодействий, представленных с точки зрения квантовой механики). Вследствие того, что сложность изучаемых объектов во многих случаях не позволяет находить явные решения уравнений, описывающих процессы в химических системах, применяют приближенные методы расчета. С квантовой химией неразрывно связана вычислительная химия — дисциплина, использующая математические методы квантовой химии, адаптированные для составления специальных компьютерных программ, используемых для расчета молекулярных свойств, амплитуды вероятности нахождения электронов в атомах, симуляции молекулярного поведения.

Строение атома • А том (от др. -греч. ἄτομος — неделимый) — наименьшая часть химического элемента, являющаяся носителем его свойств. Атом состоит из атомного ядра и электронов. При этом порядковый номер элемента (Z) соответствует числу протонов (Z) в атомном ядре, определяет суммарный положительный электрический заряд (Ze) атомного ядра, несущего почти всю массу атома (более чем 99, 9 %), а также число электронов (Z) в нейтральном атоме, определяющих его размер. Электроны образуют электронную оболочку атома. Заполнение электронных оболочек подчиняется принципу Паули — в атоме не может быть двух электронов, имеющих одинаковый набор всех четырёх квантовых чисел. Ёмкость уровней электронных оболочек по мере удаления от ядра увеличивается и составляет 2(n=1), 8(n=2), 18(n=3), 32(n=4) и т. д. электронов. Слои электронных оболочек с главным квантовым числом n=1, 2, 3, 4… обозначаются соответственно прописными буквами K, L, M, N… Порядок заполнения подслоя электронных оболочек подчиняется правилу Хунда - суммарное спиновое число электронов данного подслоя должно быть максимальным. Распределение электронов в атомах называют электронной конфигурацией. Электронная конфигурация обозначается при помощи показателей степени, которые указывают число электронов на электронной оболочке 1 s, 2 p и т. д. Буквы s, p, d, f символизируют последовательные значения орбитального квантового числа l (l соответственно равно 0, 1, 2, 3). • Согласно представлениям квантовой механики, атомы не имеют определённых границ, однако вероятность найти электрон, связанный с данным ядром, на расстоянии r от ядра быстро падает с увеличением r. Поэтому атому можно приписать некоторый размер. • Радиальная функция распределения вероятности нахождения электрона в атоме водорода обладает максимум при α 0, как показано на рис. 1. Этот наиболее вероятный радиус для электрона совпадает сборовским радиусом. Более размытое облако плотности вероятности, полученные при квантовомеханическом рассмотрении, значительно отличается от боровской модели атома и согласуется с принципом неопределённости Гейзенберга. • Лучшим описанием эффективных размеров изолированного атома является теоретически рассчитанное положение его наружных электронов. Это так называемый орбитальный радиус атома. В зависимости от порядкового номера элемента (Z) проявляется чёткая периодичность в изменении значений орбитальных атомных радиусов. На рис. 2 представлена зависимость орбитальных радиусов от порядкового номера элемента. • Размер электронной оболочки атома более чем в 10 тысяч раз превышает размер его атомного ядра. • Ядро атома состоит из положительно заряженных протонов и незаряженных нейтронов. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. Атомы классифицируются по количеству протонов и нейтронов в ядре: количество протонов определяет принадлежность атома некоторому химическому элементу, а число нейтронов — изотопу этого элемента.

Молекула • Частица, состоящая из двух или более атомов, которая может самостоятельно существовать. Имеет постоянный качественный и количественный состав. Её свойства зависят от атомов, входящих в её состав, и от характера связей между ними, от молекулярной структуры и от пространственного расположения (изомеры). Может иметь несколько разных состояний и переходить от одного состояния к другому под действием внешних факторов. Свойства вещества, состоящего из определённых молекул, зависят от состояния молекул и от свойств молекулы.

Химический элемент • совокупность атомов с одинаковым зарядом ядра и числом протонов, совпадающим с порядковым (атомным) номером в таблице Менделеева. Каждый химический элемент имеет своё латинское название и химический символ, состоящий из одной или пары латинских букв, регламентированные ИЮПАК и приводятся, в частности, в таблиц Периодической системы элементов Менделеева. • Формой существования химических элементов в свободном виде являются простые вещества (одноэлементные). • При совпадении названий химических элементов и соответствующих им простых веществ важно не допускать смешения этих понятий с последующим закреплением данной путаницы. Из контекста следует уяснять, идёт ли речь о химическом элементе как абстрактном понятии, описываемом посредством своих характеристик, или же о простом веществе с определёнными физико-химическими свойствами, которое — за исключением не имеющих запаха бесцветных газов — можно увидеть, потрогать или уловить носом. • По состоянию на декабрь 2013 года известно 118 химических элементов (из них не все официально признаны).

Не металы Группа III IV V VI VII 1 -й период 2 -й период 3 -й период 4 -й период 5 -й период 6 -й период VIII He B C N O F Ne Si P S Cl Ar As Se Br Kr Te I Xe At Rn Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов, и проявлению более высокой окислительной активности, чем у металлов. Неметаллы имеют высокие значения сродства к электрону, большую электроотрицательность и высокий окислительно-восстановительный потенциал. Благодаря высоким значениям энергии ионизации неметаллов, их атомы могут образовывать ковалентные химические связи с атомами других неметаллов и амфотерных элементов. В отличие от преимущественно ионной природы строения соединений типичных металлов, простые неметаллические вещества, а также соединения неметаллов имеют ковалентную природу строения. В свободном виде могут быть газообразные неметаллические простые вещества — фтор, хлор, кислород, азот, водород, инертные газы, твёрдые — иод, астат, сера, селен, теллур, фосфор, мышьяк, углерод, кремний, бор, при комнатной температуре в жидком состоянии существует бром. У некоторых неметаллов наблюдается проявление аллотропии. Так, для газообразного кислорода характерны две аллотропных модификации — кислород (O 2) и озон (O 3), у твёрдого углерода множество форм — алмаз, астралены, графен, графан, графит, карбин, лонсдейлит, фуллерены, стеклоуглерод, диуглерод, углеродные наноструктуры (нанопена, наноконусы, нанотрубки, нановолокна) и аморфный углерод уже открыты, а ещё возможны и другие модификации, например, чаоит и металлический углерод. В молекулярной форме в виде простых веществ в природе встречаются азот, кислород и сера. Чаще неметаллы находятся в химически связанном виде: это вода, минералы, горные породы, различные силикаты, фосфаты, бораты. По распространённости в земной коре неметаллы существенно различаются. Наиболее распространёнными являются кислород, кремний, водород; наиболее редкими — мышьяк, селен, иод.

металы • Мета ллы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ, обладающих характерными металлическими свойствами, такими, как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск. • Из 118[1] химических элементов, открытых на данный момент (из них не все официально признаны), к металлам относят: • 6 элементов в группе щелочных металлов, • 6 в группе щёлочноземельных металлов, • 38 в группе переходных металлов, • 11 в группе лёгких металлов, • 7 в группе полуметаллов, • 14 в группе лантаноиды + лантан, • 14 в группе актиноиды (физические свойства изучены не у всех элементов) + актиний, • вне определённых групп бериллий и магний. • Таким образом, к металлам, возможно, относится 96 элементов из всех открытых. • В астрофизике термин «металл» может иметь другое значение и обозначать все химические элементы тяжелее гелия (см. Металличность).

Ионная связь • Ионная связь — очень прочная химическая связь, образующаяся между атомами с большой разностью (>1, 5 по шкале Полинга) электроотрицательностей, при которой общая электронная пара полностью переходит к атому с большей электроотрицательностью. Это притяжение ионов как разноименно заряженных тел. Примером может служить соединение Cs. F, в котором «степень ионности» составляет 97 %. Рассмотрим способ образования на примере хлорида натрия Na. Cl. Электронную конфигурацию атомов натрия и хлора можно представить: 11 Na 1 s 2 2 p 6 3 s 1; 17 Cl 1 s 2 2 p 6 Зs 2 3 р5 Это атомы с незавершенными энергетическими уровнями. Очевидно, для их завершения атому натрия легче отдать один электрон, чем присоединить семь, а атому хлора легче присоединить один электрон, чем отдать семь. При химическом взаимодействии атом натрия полностью отдает один электрон, а атом хлора принимает его. Схематично это можно записать так: Na. — l е —> Na+ ион натрия, устойчивая восьмиэлектронная 1 s 2 2 p 6 оболочка за счет второго энергетического уровня. : Cl + 1 е -->. Cl - ион хлора, устойчивая восьмиэлектронная оболочка. Между ионами Na+ и Cl- возникают силы электростатического притяжения, в результате чего образуется соединение. Ионная связь — крайний случай поляризации ковалентной полярной связи. Образуется между типичными металлом и неметаллом. При этом электроны у металла полностью переходят к неметаллу. Образуются ионы. • Если химическая связь образуется между атомами, которые имеют очень большую разность электроотрицательностей (ЭО > 1. 7 по Полингу), то общая электронная пара полностью переходит к атому с большей ЭО. Результатом этого является образование соединения противоположно заряженных ионов: • A⋅+⋅B→A+[: B−] • Между образовавшимися ионами возникает электростатическое притяжение, которое называется ионной связью. Вернее, такой взгляд удобен. На деле ионная связь между атомами в чистом виде не реализуется нигде или почти нигде, обычно на деле связь носит частично ионный, а частично ковалентный характер. В то же время связь сложных молекулярных ионов часто может считаться чисто ионной. Важнейшие отличия ионной связи от других типов химической связи заключаются в ненаправленности и ненасыщаемости. Именно поэтому кристаллы, образованные за счёт ионной связи, тяготеют к различным плотнейшим упаковкам соответствующих ионов. • Характеристикой подобных соединений служит хорошая растворимость в полярных растворителях (вода, кислоты и т. д. ). Это происходит из-за заряженности частей молекулы. При этом диполи растворителя притягиваются к заряженным концам молекулы, и, в результате Броуновского движения, «растаскивают» молекулу вещества на части и окружают их, не давая соединиться вновь. В итоге получаются ионы, окружённые диполями растворителя. • При растворении подобных соединений, как правило, выделяется энергия, так как суммарная энергия образованных связей растворитель-ион больше энергии связи анион-катион. Исключения составляют многие соли азотной кислоты (нитраты), которые при растворении поглощают тепло (растворы охлаждаются). Последний факт объясняется на основе законов, которые рассматриваются в физической химии.

Ковалентная связь • Ковалентная связь (атомная связь, гомеополярная связь) — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. Обеспечивающие связь электронные облака (электроны) называются общей электронной парой. • Термин ковалентная связь был впервые введён лауреатом Нобелевской премии Ирвингом Ленгмюром в 1919 году. Этот термин относился к химической связи, обусловленной совместным обладанием электронами, в отличие от металлической связи, в которой электроны были свободными, или от ионной связи, в которой один из атомов отдавал электрон и становилсякатионом, а другой атом принимал электрон и становился анионом. • Позднее (1927 год) Ф. Лондон и В. Гайтлер на примере молекулы водорода дали первое описание ковалентной связи с точки зрения квантовой механики. • С учётом статистической интерпретации волновой функции М. Борна плотность вероятности нахождения связывающих электронов концентрируется в пространстве между ядрами молекулы (рис. 1). В теории отталкивания электронных пар рассматриваются геометрические размеры этих пар. Так, для элементов каждого периода существует некоторый средний радиус электронной пары (Å): • 0, 6 для элементов вплоть до неона; 0, 75 для элементов вплоть до аргона; 0, 75 для элементов вплоть до криптона и 0, 8 для элементов вплоть до ксенона. • Характерные свойства ковалентной связи — направленность, насыщаемость, полярность, поляризуемость — определяют химические и физические свойства соединений. • Направленность связи обусловлена молекулярным строением вещества и геометрической формы их молекулы. Углы между двумя связями называют валентными. • Насыщаемость — способность атомов образовывать ограниченное число ковалентных связей. Количество связей, образуемых атомом, ограничено числом его внешних атомных орбиталей. • Полярность связи обусловлена неравномерным распределением электронной плотности вследствие различий в электроотрицательностях атомов. По этому признаку ковалентные связи подразделяются на неполярные и полярные (неполярные — двухатомная молекула состоит из одинаковых атомов (H 2, Cl 2, N 2) и электронные облака каждого атома распределяются симметрично относительно этих атомов; полярные — двухатомная молекула состоит из атомов разных химических элементов, и общее электронное облако смещается в сторону одного из атомов, образуя тем самым асимметрию распределения электрического заряда в молекуле, порождаядипольный момент молекулы). • Поляризуемость связи выражается в смещении электронов связи под влиянием внешнего электрического поля, в том числе и другой реагирующей частицы. Поляризуемость определяется подвижностью электронов. Полярность и поляризуемость ковалентных связей определяет реакционную способность молекул по отношению к полярным реагентам. • Электроны тем подвижнее, чем дальше они находятся от ядер. • Однако, дважды лауреат Нобелевской премии Л. Полинг указывал, что «в некоторых молекулах имеются ковалентные связи, обусловленные одним или тремя электронами вместо общей пары» . Одноэлектронная химическая связь реализуется в молекулярном ионе водорода H 2+. • Молекулярный ион водорода H 2+ содержит два протона и один электрон. Единственный электрон молекулярной системы компенсирует электростатическое отталкивание двух протонов и удерживает их на расстоянии 1, 06 Å (длина химической связи H 2+). Центр электронной плотности электронного облака молекулярной системы равноудалён от обоих протонов на боровский радиус α 0=0, 53 А и является центром симметрии молекулярного иона водорода H 2+.
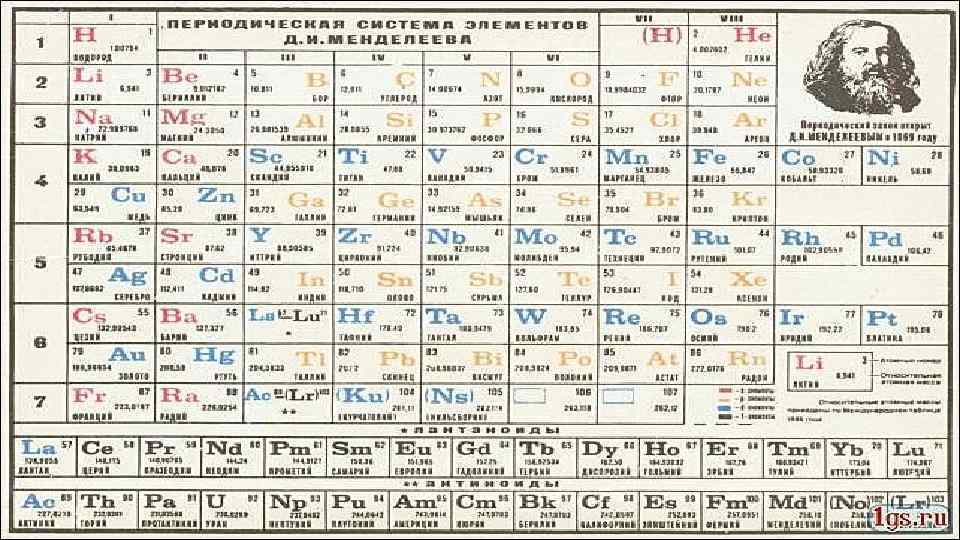

Научная деятельность Д. И. Менделеева • Д. И. Менделеев — автор фундаментальных исследований по химии, физике, метрологии, метеорологии, экономике, основополагающих трудов по воздухоплаванию, сельскому хозяйству, химической технологии, народному просвещению и других работ, тесно связанных с потребностями развития производительных сил России. • Д. И. Менделеев исследовал (в 1854— 1856 годах) явления изоморфизма, раскрывающие отношения между кристаллической формой и химическим составом соединений, а также зависимость свойств элементов от величины их атомных объёмов. • Открыл в 1860 году «температуру абсолютного кипения жидкостей» , или критическую температуру. • 16 декабря 1860 года он пишет из Гейдельберга попечителю Санкт-Петербургского учебного округа И. Д. Делянову: «…главный предмет моих занятий есть физическая химия» . • Д. И. Менделеев является автором первого русского учебника «Органическая химия» (1861 год). • Сконструировал в 1859 году пикнометр — прибор для определения плотности жидкости. Создал в 1865— 1887 годах гидратную теорию растворов. Развил идеи о существовании соединений переменного состава. • Исследуя газы, Менделеев нашёл в 1874 году общее уравнение состояния идеального газа, включающее как частность зависимость состояния газа от температуры, обнаруженную в 1834 году физиком Б. П. Э. Клапейроном (уравнение Клапейрона — Менделеева). • В 1877 году Менделеев выдвинул гипотезу происхождения нефти из карбидов тяжёлых металлов, которая, правда, на сегодня большинством учёных не принимается; предложил принцип дробной перегонки при переработке нефти. • Выдвинул в 1880 году идею подземной газификации углей. Занимался вопросами химизации сельского хозяйства, пропагандировал использование минеральных удобрений, орошение засушливых земель. Совместно с И. М. Чельцовым принимал в 1890— 1892 годах участие в разработке бездымного пороха. Является автором ряда работ по метрологии. Создал точную теорию весов, разработал наилучшие конструкции коромысла и арретира, предложил точнейшие приёмы взвешивания. • В своё время интересы Д. И. Менделеева были близки к минералогии, его коллекция минералов бережно хранится и сейчас в Музее кафедры минералогии Санкт-Петербургского университета, а друза горного хрусталя с его стола является одним из лучших экспонатов в витрине кварца. Рисунок этой друзы он поместил в первое издание «Общей химии» (1903 год). Студенческая работа Д. И. Менделеева была посвящена изоморфизму в минералах.

Исследование газов. • Эта тема в творчестве Д. И. Менделеева связана, прежде всего, с поиском учёным физических причин периодичности. • • • Так как свойства элементов находились в периодической зависимости от атомных весов, массы, исследователь мыслил возможность пролить свет на эту проблему, выясняя причины сил тяготения и посредством изучения свойств передающей их среды. Концепция «мирового эфира» имела в XIX веке большое влияние на возможное решение данной проблемы. Предполагалось, что «эфир» , заполняющий межпланетное пространство, является средой, передающей свет, тепло и гравитацию. Исследование сильно разреженных газов представлялось возможным средством к доказательству существования названной субстанции, когда свойства «обычного» вещества уже не способны бы были скрывать свойства «эфира» . Одна из гипотез Д. И. Менделеева сводилась к тому, что специфическим состоянием газов воздуха при большом разрежении и мог оказаться «эфир» или некий-то газ с очень малым весом. Д. И. Менделеевым написано на оттиске из «Основ химии» , на периодической системе 1871 года: «Легче всех эфир, в миллионы раз» ; а в рабочей тетради 1874 года учёный выражает ещё более ясно ход мысли: «При нулевом давлении у воздуха есть некоторая плотность, это и есть эфир!» . Тем не менее, среди его публикаций этого времени таких определённых соображений не высказано (Д. И. Менделеев. Попытка химического понимания мирового эфира. 1902). В контексте предположений, связанных с поведением сильно разреженного газа (инертного — «наилегчайшего химического элемента» ) в космическом пространстве, Д. И. Менделеев опирается на сведения, полученные астрономом А. А. Белопольским: «Инспектор Главной Палаты мер и весов, обязательно снабдил меня следующими результатами новейших исследований, в том числе и г. Белопольского» . А далее он прямо ссылается на эти данные в своих выводах. При всей гипотетической направленности исходных предпосылок этих исследований, основным и наиболее важным результатом в области физики, полученным благодаря им Д. И. Менделеевым, явился вывод уравнения идеального газа, содержащего универсальную газовую постоянную. Также очень важным, но несколько преждевременным, было предложенное Д. И. Менделеевым введение термодинамической шкалы температур. Учёным также было избрано правильное направление для описания свойств реальных газов. Вириальные разложения, использованные им, соответствуют первым приближениям в известных сейчас уравнениях для реальных газов. В разделе, имеющем отношение к исследованиям газов и жидкостей, Д. И. Менделеевым сделано 54 работы.

Учение о растворах. • Эта тема в творчестве Д. И. Менделеева связана, прежде всего, с поиском учёным физических причин периодичности. Так как свойства элементов находились в периодической зависимости от атомных весов, массы, исследователь мыслил возможность пролить свет на эту проблему, выясняя причины сил тяготения и посредством изучения свойств передающей их среды. • Концепция «мирового эфира» имела в XIX веке большое влияние на возможное решение данной проблемы. Предполагалось, что «эфир» , заполняющий межпланетное пространство, является средой, передающей свет, тепло и гравитацию. Исследование сильно разреженных газов представлялось возможным средством к доказательству существования названной субстанции, когда свойства «обычного» вещества уже не способны бы были скрывать свойства «эфира» . • Одна из гипотез Д. И. Менделеева сводилась к тому, что специфическим состоянием газов воздуха при большом разрежении и мог оказаться «эфир» или некий-то газ с очень малым весом. Д. И. Менделеевым написано на оттиске из «Основ химии» , на периодической системе 1871 года: «Легче всех эфир, в миллионы раз» ; а в рабочей тетради 1874 года учёный выражает ещё более ясно ход мысли: «При нулевом давлении у воздуха есть некоторая плотность, это и есть эфир!» . Тем не менее, среди его публикаций этого времени таких определённых соображений не высказано (Д. И. Менделеев. Попытка химического понимания мирового эфира. 1902).

• При всей гипотетической направленности исходных предпосылок этих исследований, основным и наиболее важным результатом в области физики, полученным благодаря им Д. И. Менделеевым, явился вывод уравнения идеального газа, содержащего универсальную газовую постоянную. Также очень важным, но несколько преждевременным, было предложенное Д. И. Менделеевым введение термодинамической шкалы температур. • Учёным также было избрано правильное направление для описания свойств реальных газов. Вириальные разложения, использованные им, соответствуют первым приближениям в известных сейчас уравнениях для реальных газов. • В разделе, имеющем отношение к исследованиям газов и жидкостей, Д. И. Менделеевым сделано 54 работы[1]. • Учение о растворах[править | править вики-текст] • В 1905 году Д. И. Менделеев скажет: «Всего более четыре предмета составили моё имя: периодический закон, исследование упругости газов, понимание растворов как ассоциации и „Основы химии“. Тут моё богатство. Оно не отнято у кого-нибудь, а произведено мною…» .