Химическая картина мира.pptx
- Количество слайдов: 25
 ХИМИЯ
ХИМИЯ
 Введение. НАУКА ХИМИЯ Из чего состоят физические тела? Физические тела состоят из вещества. Раздел естествознания, исследующий строение и свойства вещества, а также их превращения друг в друга, называется – Химия. Поэтому, прежде чем продолжить рассматривать эволюцию физической картины мира, необходимо обратиться к химической картине мира – ХКМ, которая внесла весомый вклад в становление современной естественнонаучной картины мира – ЕНКМ. Химия – раздел естествознания, исследующий свойства вещества и их превращения. Химия - наука о веществах, их свойствах, строении и взаимных превращениях друг в друга. Химия делится на два больших раздела: неорганическая химия и органическая химия. Предмет неорганической химии – химические элементы и их соединения, а также закономерности, которым подчиняются различные химические реакции.
Введение. НАУКА ХИМИЯ Из чего состоят физические тела? Физические тела состоят из вещества. Раздел естествознания, исследующий строение и свойства вещества, а также их превращения друг в друга, называется – Химия. Поэтому, прежде чем продолжить рассматривать эволюцию физической картины мира, необходимо обратиться к химической картине мира – ХКМ, которая внесла весомый вклад в становление современной естественнонаучной картины мира – ЕНКМ. Химия – раздел естествознания, исследующий свойства вещества и их превращения. Химия - наука о веществах, их свойствах, строении и взаимных превращениях друг в друга. Химия делится на два больших раздела: неорганическая химия и органическая химия. Предмет неорганической химии – химические элементы и их соединения, а также закономерности, которым подчиняются различные химические реакции.
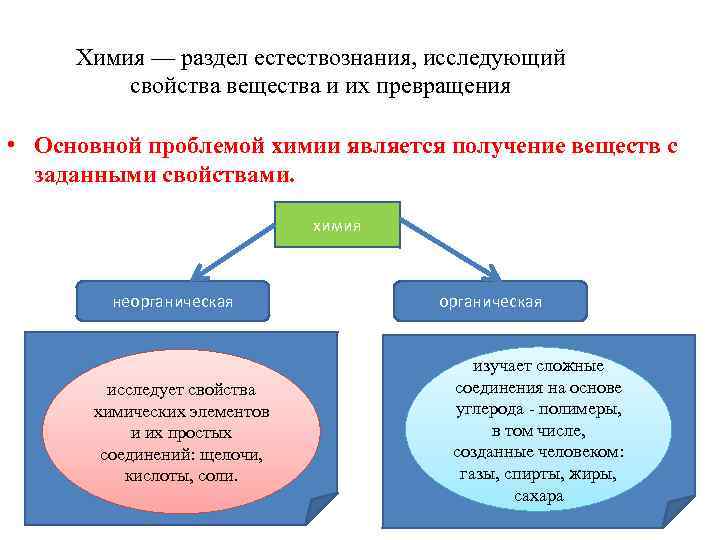 Химия — раздел естествознания, исследующий свойства вещества и их превращения • Основной проблемой химии является получение веществ с заданными свойствами. химия неорганическая исследует свойства химических элементов и их простых соединений: щелочи, кислоты, соли. органическая изучает сложные соединения на основе углерода - полимеры, в том числе, созданные человеком: газы, спирты, жиры, сахара
Химия — раздел естествознания, исследующий свойства вещества и их превращения • Основной проблемой химии является получение веществ с заданными свойствами. химия неорганическая исследует свойства химических элементов и их простых соединений: щелочи, кислоты, соли. органическая изучает сложные соединения на основе углерода - полимеры, в том числе, созданные человеком: газы, спирты, жиры, сахара

 ОСНОВНЫЕ ПОНЯТИЯ ХКМ Вещество – вид материи, из которого состоят физические тела. Количество вещества - это число структурных элементов (атомов, молекул, ионов и др. ) в веществе. Единицей измерения количества вещества является моль. Моль - количество вещества, которое содержит столько определенных структурных элементов (молекул, атомов, электронов и т. д. ), сколько атомов содержится в 0, 012 кг изотопа углерода - 12. Молярная масса (М) - масса одного моля вещества. Основной единицей измерения молярной массы является килограмм на моль (кг/моль) или грамм на моль (г/моль). Химический элемент — это совокупность определенных атомов с одинаковым порядковым или атомным номером в Z в Периодической таблице элементов Д. И. Менделеева. Современное определение «химического элемента» - множество атомов с одинаковым зарядом ядра (числом протонов в ядре).
ОСНОВНЫЕ ПОНЯТИЯ ХКМ Вещество – вид материи, из которого состоят физические тела. Количество вещества - это число структурных элементов (атомов, молекул, ионов и др. ) в веществе. Единицей измерения количества вещества является моль. Моль - количество вещества, которое содержит столько определенных структурных элементов (молекул, атомов, электронов и т. д. ), сколько атомов содержится в 0, 012 кг изотопа углерода - 12. Молярная масса (М) - масса одного моля вещества. Основной единицей измерения молярной массы является килограмм на моль (кг/моль) или грамм на моль (г/моль). Химический элемент — это совокупность определенных атомов с одинаковым порядковым или атомным номером в Z в Периодической таблице элементов Д. И. Менделеева. Современное определение «химического элемента» - множество атомов с одинаковым зарядом ядра (числом протонов в ядре).
 ОСНОВНЫЕ ПОНЯТИЯ ХКМ Вещество – вид материи, из которого состоят физические тела. Количество вещества - это число структурных элементов (атомов, молекул, ионов и др. ) в веществе. Единицей измерения количества вещества является моль. Моль - количество вещества, которое содержит столько определенных структурных элементов (молекул, атомов, электронов и т. д. ), сколько атомов содержится в 0, 012 кг изотопа углерода - 12. Молярная масса (М) - масса одного моля вещества. Основной единицей измерения молярной массы является килограмм на моль (кг/моль) или грамм на моль (г/моль). Химический элемент — это совокупность определенных атомов с одинаковым порядковым или атомным номером в Z в Периодической таблице элементов Д. И. Менделеева. Современное определение «химического элемента» - множество атомов с одинаковым зарядом ядра (числом протонов в ядре).
ОСНОВНЫЕ ПОНЯТИЯ ХКМ Вещество – вид материи, из которого состоят физические тела. Количество вещества - это число структурных элементов (атомов, молекул, ионов и др. ) в веществе. Единицей измерения количества вещества является моль. Моль - количество вещества, которое содержит столько определенных структурных элементов (молекул, атомов, электронов и т. д. ), сколько атомов содержится в 0, 012 кг изотопа углерода - 12. Молярная масса (М) - масса одного моля вещества. Основной единицей измерения молярной массы является килограмм на моль (кг/моль) или грамм на моль (г/моль). Химический элемент — это совокупность определенных атомов с одинаковым порядковым или атомным номером в Z в Периодической таблице элементов Д. И. Менделеева. Современное определение «химического элемента» - множество атомов с одинаковым зарядом ядра (числом протонов в ядре).
 ОСНОВНЫЕ ПОНЯТИЯ ХКМ •
ОСНОВНЫЕ ПОНЯТИЯ ХКМ •
 ЗАКОН АВОГАДРО ЧИСЛО АВОГАДРО Закон Авога дро — одно из важных основных положений химии. Закон Авогадро был сформулирован ещё в 1811 году Амедео Авогадро (1776— 1856), профессором физики в Турине. «В равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул» . Из закона Авогадро следует: один моль любого газа при одинаковых условиях занимает одинаковый объём. При нормальных условиях, т. е. при температуре = 0 °C (273 К) и давлении = 101, 3 к. Па, объём 1 моля газа равен 22, 4 л. Число Авога дро, конста нта Авогадро, постоянная Авогадро — физическая величина, численно равная количеству структурных единиц (атомов, молекул) в 1 моль вещества. Значение числа Авогадро: NA = 6, 022 141 29(27)· 1023 моль− 1.
ЗАКОН АВОГАДРО ЧИСЛО АВОГАДРО Закон Авога дро — одно из важных основных положений химии. Закон Авогадро был сформулирован ещё в 1811 году Амедео Авогадро (1776— 1856), профессором физики в Турине. «В равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул» . Из закона Авогадро следует: один моль любого газа при одинаковых условиях занимает одинаковый объём. При нормальных условиях, т. е. при температуре = 0 °C (273 К) и давлении = 101, 3 к. Па, объём 1 моля газа равен 22, 4 л. Число Авога дро, конста нта Авогадро, постоянная Авогадро — физическая величина, численно равная количеству структурных единиц (атомов, молекул) в 1 моль вещества. Значение числа Авогадро: NA = 6, 022 141 29(27)· 1023 моль− 1.
 • КЛАССИФИКАЦИЯ ВЕЩЕСТВ
• КЛАССИФИКАЦИЯ ВЕЩЕСТВ
 МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ (МКТ) Молекулярно-кинетическая теория – основная теория ХКМ. В 19 в. стало понятно, что химические свойства, химические процессы, химические превращения одного вещества в другое невозможно объяснить без создания теории строения вещества. К середине 19 в. была создана такая теория - МКТ. Авторами этой теории были знаменитые ученые: Рудольф Клаузиуса, Людвиг Больцман и Джеймс Максвелл. Фундаментом окончательно сформировавшейся к середине 19 в. , молекулярно-кинетической теории (МКТ) была МКТ вещества, автором которой был выдающийся русский ученыйэнциклопедист – М. В. Ломоносов.
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ (МКТ) Молекулярно-кинетическая теория – основная теория ХКМ. В 19 в. стало понятно, что химические свойства, химические процессы, химические превращения одного вещества в другое невозможно объяснить без создания теории строения вещества. К середине 19 в. была создана такая теория - МКТ. Авторами этой теории были знаменитые ученые: Рудольф Клаузиуса, Людвиг Больцман и Джеймс Максвелл. Фундаментом окончательно сформировавшейся к середине 19 в. , молекулярно-кинетической теории (МКТ) была МКТ вещества, автором которой был выдающийся русский ученыйэнциклопедист – М. В. Ломоносов.
 Михаи л Васи льевич Ломоно сов (19 ноября 1765 г. – 15 апреля 1765 г. ) М. В. Ломоносов — первый русский учёный-естествоиспытатель мирового значения, энциклопедист, химик и физик. М. В. Ломоносов вошёл в науку как первый химик, который дал физической химии определение, весьма близкое к современному, и предначертал обширную программу физикохимических исследований. М. В. Ломоносов заложил фундамент современной МКТ, создав молекулярнокинетическую теорию тепла, которая во многом превосходила современное представление о строении материи. М. В. Ломоносов - астроном, приборостроитель, географ, металлург, геолог, поэт, утвердил основания современного русского литературного языка, художник, историк и родослов, поборник развития отечественного просвещения, науки и экономики. Разработал роект п Московского университета, впоследствии названного в его честь. Открыл наличие атмосферы у планеты Венера. Статский советник, профессор химии (с 1745), и действительный член Санкт-Петербургской Императорской и почётный член Королевской Шведской академий наук.
Михаи л Васи льевич Ломоно сов (19 ноября 1765 г. – 15 апреля 1765 г. ) М. В. Ломоносов — первый русский учёный-естествоиспытатель мирового значения, энциклопедист, химик и физик. М. В. Ломоносов вошёл в науку как первый химик, который дал физической химии определение, весьма близкое к современному, и предначертал обширную программу физикохимических исследований. М. В. Ломоносов заложил фундамент современной МКТ, создав молекулярнокинетическую теорию тепла, которая во многом превосходила современное представление о строении материи. М. В. Ломоносов - астроном, приборостроитель, географ, металлург, геолог, поэт, утвердил основания современного русского литературного языка, художник, историк и родослов, поборник развития отечественного просвещения, науки и экономики. Разработал роект п Московского университета, впоследствии названного в его честь. Открыл наличие атмосферы у планеты Венера. Статский советник, профессор химии (с 1745), и действительный член Санкт-Петербургской Императорской и почётный член Королевской Шведской академий наук.
 Основные положения молекулярно- кинетической теории (МКТ) вещества и ее опытные доказательства Первое положение МКТ вещества: Все вещества состоят из частиц (молекул) Опытное подтверждение этого положения: • • • Смешивание разных жидкостей, например, воды и спирта, показывает, что объём смеси меньше суммарного объёма, занимаемого двумя жидкостями до их смешивания. Это можно объяснить тем, что между молекулами жидкостей есть пустоты, и при смешивании жидкостей молекулы одной из них проникают в свободное пространство между молекулами другой жидкости. Расширение тел при нагревании и сжатие при охлаждении также можно объяснить тем, что вещества состоят из молекул, расположенных друг от друга на некотором расстоянии. При нагревании расстояния между молекулами увеличиваются, а при охлаждении уменьшаются. Проявление дискретной структуры при наблюдении веществ под электронными или ионными микроскопами. В современные электронные микроскопы можно «увидеть» очертания крупных белковых молекул.
Основные положения молекулярно- кинетической теории (МКТ) вещества и ее опытные доказательства Первое положение МКТ вещества: Все вещества состоят из частиц (молекул) Опытное подтверждение этого положения: • • • Смешивание разных жидкостей, например, воды и спирта, показывает, что объём смеси меньше суммарного объёма, занимаемого двумя жидкостями до их смешивания. Это можно объяснить тем, что между молекулами жидкостей есть пустоты, и при смешивании жидкостей молекулы одной из них проникают в свободное пространство между молекулами другой жидкости. Расширение тел при нагревании и сжатие при охлаждении также можно объяснить тем, что вещества состоят из молекул, расположенных друг от друга на некотором расстоянии. При нагревании расстояния между молекулами увеличиваются, а при охлаждении уменьшаются. Проявление дискретной структуры при наблюдении веществ под электронными или ионными микроскопами. В современные электронные микроскопы можно «увидеть» очертания крупных белковых молекул.
 Второе положение МКТ: Частицы (молекулы) непрерывно и беспорядочно движутся Некоторые факты, подтверждающие это положение: • Молекулы газа распространяются по всему объему сосуда. • Броуновское движение. Движение частиц, взвешенных в жидкости или газе, под действием некомпенсированных ударов молекул жидкости или газа называется Броуновским движением. Если приготовить водный раствор с частицами краски, которые не видны глазом, и рассматривать приготовленную взвесь под микроскопом, то мы «увидим» следующую картину: частицы краски будут хаотически и беспорядочно двигаться. Микроскопические частицы краски хаотически движутся под ударами хаотически и беспорядочно движущихся молекул воды. • Диффузия – взаимное проникновение одного вещества в другое без механического перемешивания веществ. Это также является косвенным доказательством хаотического и беспорядочного движения молекул, в результате которого они проникают в промежутки между другими молекулами.
Второе положение МКТ: Частицы (молекулы) непрерывно и беспорядочно движутся Некоторые факты, подтверждающие это положение: • Молекулы газа распространяются по всему объему сосуда. • Броуновское движение. Движение частиц, взвешенных в жидкости или газе, под действием некомпенсированных ударов молекул жидкости или газа называется Броуновским движением. Если приготовить водный раствор с частицами краски, которые не видны глазом, и рассматривать приготовленную взвесь под микроскопом, то мы «увидим» следующую картину: частицы краски будут хаотически и беспорядочно двигаться. Микроскопические частицы краски хаотически движутся под ударами хаотически и беспорядочно движущихся молекул воды. • Диффузия – взаимное проникновение одного вещества в другое без механического перемешивания веществ. Это также является косвенным доказательством хаотического и беспорядочного движения молекул, в результате которого они проникают в промежутки между другими молекулами.
 Третье положение МКТ: Частицы (молекулы) взаимодействуют друг с другом. Факты, подтверждающие это положение: • Существуют как силы молекулярного притяжения, так и силы молекулярного отталкивания. • Существование трех агрегатных состояний: из-за разного взаимодействия молекул проявляются разные свойства агрегатных состояний, отражённые в таблице: Агрегатное состояние веществагаз жидкость Внешние свойства вещества не имеет собственной формы и объема не имеет собственной формы, но имеет собственный объём жидкостьтвердое тело не имеет собственной формы, но имеет собственный объём имеет собственную форму и объем твердое тело имеет собственную форму и объем
Третье положение МКТ: Частицы (молекулы) взаимодействуют друг с другом. Факты, подтверждающие это положение: • Существуют как силы молекулярного притяжения, так и силы молекулярного отталкивания. • Существование трех агрегатных состояний: из-за разного взаимодействия молекул проявляются разные свойства агрегатных состояний, отражённые в таблице: Агрегатное состояние веществагаз жидкость Внешние свойства вещества не имеет собственной формы и объема не имеет собственной формы, но имеет собственный объём жидкостьтвердое тело не имеет собственной формы, но имеет собственный объём имеет собственную форму и объем твердое тело имеет собственную форму и объем
 МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ (МКТ) ГАЗОВ Дальнейшее развитие МКТ был о связано с газообразным состоянием вещества, потому что в этом состоянии молекулы и атомы вещества могут достаточно свободно совершать поступательное хаотическое тепловое движение. Поступательное хаотическое и непрестанное тепловое движение молекул и атомов объясняет физико-химические свойства вещества, которые характеризуются макропараметрами, такими как: температура, давление и т. д. Была введена модель «идеальный газ» . Идеальный газ - это газ, состоящий из точечных материальных частиц с конечной массой, силами взаимодействия между которыми можно пренебречь, и которые сталкиваются между собой по законам соударения абсолютно упругих шаров. При этом не учитываются силы молекулярного взаимодействия и поэтому потенциальной энергией взаимодействия молекул можно пренебречь. Следовательно, молекулы идеального газа обладают только кинетической энергией поступательного теплового движения молекул.
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ (МКТ) ГАЗОВ Дальнейшее развитие МКТ был о связано с газообразным состоянием вещества, потому что в этом состоянии молекулы и атомы вещества могут достаточно свободно совершать поступательное хаотическое тепловое движение. Поступательное хаотическое и непрестанное тепловое движение молекул и атомов объясняет физико-химические свойства вещества, которые характеризуются макропараметрами, такими как: температура, давление и т. д. Была введена модель «идеальный газ» . Идеальный газ - это газ, состоящий из точечных материальных частиц с конечной массой, силами взаимодействия между которыми можно пренебречь, и которые сталкиваются между собой по законам соударения абсолютно упругих шаров. При этом не учитываются силы молекулярного взаимодействия и поэтому потенциальной энергией взаимодействия молекул можно пренебречь. Следовательно, молекулы идеального газа обладают только кинетической энергией поступательного теплового движения молекул.
 СКОРОСТИ ДВИЖЕНИЯ МОЛЕКУЛ •
СКОРОСТИ ДВИЖЕНИЯ МОЛЕКУЛ •
 ОСНОВНОЕ УРАВНЕНИЕ МОЛЕКУЛЯРНОКИНЕТИЧЕСКОЙ ТЕОРИИ ДЛЯ ИДЕАЛЬНОГО ГАЗА •
ОСНОВНОЕ УРАВНЕНИЕ МОЛЕКУЛЯРНОКИНЕТИЧЕСКОЙ ТЕОРИИ ДЛЯ ИДЕАЛЬНОГО ГАЗА •
 ВЗАИМОДЕЙСТВИЕ АТОМОВ ХИМИЧЕСКИЕ СВЯЗИ ВАЛЕНТНОСТЬ Атомы взаимодействуют между собой. В результате этого взаимодействия образуются химические связи между ними. Каждый атом способен связываться с конкретным количеством других атомов, причем «связанные» атомы располагаются в пространстве строго определенным образом (кристаллическая решетка). Различают 4 вида химических связей: ковалентная неполярная связь, ковалентная полярная связь, ионная связь, металлическая связь. Химические связи между атомами реализуются с помощью электронов, которые находятся внутри атомов, и, прежде всего, внешних электронов во внешнем электронном слое атома и слабее всего связаны с ним. Однако, атомы не могут связываться друг с другом произвольно. Внешние оболочки всех химических элементов, кроме благородных газов, являются «незавершенными» , т. е. незаполненными до конца электронами. В процессе химического взаимодействия между атомами они «завершаются» , т. е. полностью «заполняются» . Количество внешних электронов зависит от природы атомов, поэтому разные химические элементы имеют неодинаковое количество внешних электронов. Внешние электроны также называются валентными электронами. Валентность химического элемента – способность его атомов образовывать определенное число химических связей между ними.
ВЗАИМОДЕЙСТВИЕ АТОМОВ ХИМИЧЕСКИЕ СВЯЗИ ВАЛЕНТНОСТЬ Атомы взаимодействуют между собой. В результате этого взаимодействия образуются химические связи между ними. Каждый атом способен связываться с конкретным количеством других атомов, причем «связанные» атомы располагаются в пространстве строго определенным образом (кристаллическая решетка). Различают 4 вида химических связей: ковалентная неполярная связь, ковалентная полярная связь, ионная связь, металлическая связь. Химические связи между атомами реализуются с помощью электронов, которые находятся внутри атомов, и, прежде всего, внешних электронов во внешнем электронном слое атома и слабее всего связаны с ним. Однако, атомы не могут связываться друг с другом произвольно. Внешние оболочки всех химических элементов, кроме благородных газов, являются «незавершенными» , т. е. незаполненными до конца электронами. В процессе химического взаимодействия между атомами они «завершаются» , т. е. полностью «заполняются» . Количество внешних электронов зависит от природы атомов, поэтому разные химические элементы имеют неодинаковое количество внешних электронов. Внешние электроны также называются валентными электронами. Валентность химического элемента – способность его атомов образовывать определенное число химических связей между ними.
 ТИПЫ ХИМИЧЕСКИХ СВЯЗЕЙ •
ТИПЫ ХИМИЧЕСКИХ СВЯЗЕЙ •
 ХИМИЧЕСКИЕ РЕАКЦИИ И ИХ ОБЩАЯ ХАРАКТЕРИСТИКА Химические реакции (химические явления) – это процессы, в результате которых из одних веществ образуются другие, отличающиеся от исходных по составу и строению, а, следовательно, и по свойствам. Исходные вещества, участвующие в химической реакции, называются – реагенты. Вещества, получившиеся в результате реакции – продукты реакции. При химической реакции из атомов и молекул реагентов образуются новые молекулы продуктов реакции. Химия использует такие процессы для получения соединений с новыми, полезными для человека свойствами. При протекании любых химических реакций строго соблюдаются законы сохранения массы вещества и его энергии, закон сохранения импульса и закон сохранения электрического заряда. Кинетические энергии атомов и молекул реагентов не равны кинетическим энергиям продуктов реакции. Разница между энергиями атомов и молекул реагентов и энергиями атомов и молекул продуктов реакции выделяется или поглощается в виде теплоты химической реакции. Химические реакции могут протекать с выделением энергии в виде тепла Q (экзотермические реакции) и с поглощением тепла Q (эндотермические реакции).
ХИМИЧЕСКИЕ РЕАКЦИИ И ИХ ОБЩАЯ ХАРАКТЕРИСТИКА Химические реакции (химические явления) – это процессы, в результате которых из одних веществ образуются другие, отличающиеся от исходных по составу и строению, а, следовательно, и по свойствам. Исходные вещества, участвующие в химической реакции, называются – реагенты. Вещества, получившиеся в результате реакции – продукты реакции. При химической реакции из атомов и молекул реагентов образуются новые молекулы продуктов реакции. Химия использует такие процессы для получения соединений с новыми, полезными для человека свойствами. При протекании любых химических реакций строго соблюдаются законы сохранения массы вещества и его энергии, закон сохранения импульса и закон сохранения электрического заряда. Кинетические энергии атомов и молекул реагентов не равны кинетическим энергиям продуктов реакции. Разница между энергиями атомов и молекул реагентов и энергиями атомов и молекул продуктов реакции выделяется или поглощается в виде теплоты химической реакции. Химические реакции могут протекать с выделением энергии в виде тепла Q (экзотермические реакции) и с поглощением тепла Q (эндотермические реакции).
 ОСНОВНАЯ КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ •
ОСНОВНАЯ КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ •
 СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ •
СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ •
 КАТАЛИТИЧЕСКИЕ ХИМИЧЕСКИЕ РЕАКЦИИ •
КАТАЛИТИЧЕСКИЕ ХИМИЧЕСКИЕ РЕАКЦИИ •
 ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ •
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ХИМИЧЕСКИЕ РЕАКЦИИ •