л.1.химия тв. тела.ppt
- Количество слайдов: 126
 Химия твердого тела Введение: Цели и задачи. Место среди других наук. Основные химические Классификация твердых тел. понятия.
Химия твердого тела Введение: Цели и задачи. Место среди других наук. Основные химические Классификация твердых тел. понятия.
 Химия твердого тела имеет дело со всем, что касается получения, свойств, применения материалов, находящихся в твердом состоянии. В большинстве случаев это неорганические соединения.
Химия твердого тела имеет дело со всем, что касается получения, свойств, применения материалов, находящихся в твердом состоянии. В большинстве случаев это неорганические соединения.
 • Органические твердые тела исследуются в химии твердого тела, если они проявляют например, высокую электропроводность или вступают в топохимически контролируемые реакции (зависящие от геометрических особенностей упаковки молекул в кристалле).
• Органические твердые тела исследуются в химии твердого тела, если они проявляют например, высокую электропроводность или вступают в топохимически контролируемые реакции (зависящие от геометрических особенностей упаковки молекул в кристалле).
 • Химия твердого тела связана с физикой твердого тела, кристаллографией, минералогией, физической химией, механикой, механохимией, радиационной технологии химией, является неорганических, композиционных материалов. основой полимерных и
• Химия твердого тела связана с физикой твердого тела, кристаллографией, минералогией, физической химией, механикой, механохимией, радиационной технологии химией, является неорганических, композиционных материалов. основой полимерных и
 • Выйдя из недр физической химии в настоящее время является самостоятельной научной дисциплиной. • Накопление фактов в областях, ныне относимых к химии твердого тела, шло в течение нескольких столетий, однако как самостоятельная наука она сформировалась в середине 20 в. главным образом в связи с развитием электроники и технологии неорганических материалов.
• Выйдя из недр физической химии в настоящее время является самостоятельной научной дисциплиной. • Накопление фактов в областях, ныне относимых к химии твердого тела, шло в течение нескольких столетий, однако как самостоятельная наука она сформировалась в середине 20 в. главным образом в связи с развитием электроники и технологии неорганических материалов.
 • Особенности строения твердых веществ проявляются прежде всего в наличии у них ближнего (аморфные вещества и стекла) и дальнего (кристаллы) порядка, а также в способности многих твердых отклоняться от законов стехиометрии. веществ
• Особенности строения твердых веществ проявляются прежде всего в наличии у них ближнего (аморфные вещества и стекла) и дальнего (кристаллы) порядка, а также в способности многих твердых отклоняться от законов стехиометрии. веществ
 • Еще в начале 19 в. эта способность вызвала научную дискуссию отстаивавшем между возможность К. Бертолле, непрерывного изменения состава твердого вещества, и Ж. Прустом, который придерживался победившей тогда точки зрения о постоянстве состава.
• Еще в начале 19 в. эта способность вызвала научную дискуссию отстаивавшем между возможность К. Бертолле, непрерывного изменения состава твердого вещества, и Ж. Прустом, который придерживался победившей тогда точки зрения о постоянстве состава.
 • После введения в конце 19 в. понятия твердого раствора (Я. Вант-Гофф, 1890) и разработки основ физ. -хим. анализа (Г. Тамман, нач. 20 в. ; Н. С. Курнаков, противопоставления 1913) веществ проблема постоянного состава (дальтонидов) и веществ переменного состава (бертоллидов) возникла вновь, причем бертоллиды рассматривались как твердые растворы неустойчивых в твердом состоянии веществ.
• После введения в конце 19 в. понятия твердого раствора (Я. Вант-Гофф, 1890) и разработки основ физ. -хим. анализа (Г. Тамман, нач. 20 в. ; Н. С. Курнаков, противопоставления 1913) веществ проблема постоянного состава (дальтонидов) и веществ переменного состава (бертоллидов) возникла вновь, причем бертоллиды рассматривались как твердые растворы неустойчивых в твердом состоянии веществ.
 • Основы химии твердых тел, как считается, заложил А. Муассан, который в 1892 ввел в лабораторную практику электродуговые печи и положил начало исследованиям свойств твердых тел при высоких температурах.
• Основы химии твердых тел, как считается, заложил А. Муассан, который в 1892 ввел в лабораторную практику электродуговые печи и положил начало исследованиям свойств твердых тел при высоких температурах.
 • Открытие дифракции рентгеновских лучей (М. Лауэ, 1912) и развитие кристаллохимии (В. Гольдшмидт, Л. Полинг, А. В. Шубников, Н. В. Белов, А. И. Китайгородский) позволили глубже понять структуру твердых веществ и не только обосновать существование обширного класса нестехиометрических веществ, но и ввести понятие нестехиометрии.
• Открытие дифракции рентгеновских лучей (М. Лауэ, 1912) и развитие кристаллохимии (В. Гольдшмидт, Л. Полинг, А. В. Шубников, Н. В. Белов, А. И. Китайгородский) позволили глубже понять структуру твердых веществ и не только обосновать существование обширного класса нестехиометрических веществ, но и ввести понятие нестехиометрии.
 • На свойства и поведение твердых тел влияет состояние (кристаллическое или твердого аморфное), тела тип кристаллической модификации, наличие и характер фазовых переходов.
• На свойства и поведение твердых тел влияет состояние (кристаллическое или твердого аморфное), тела тип кристаллической модификации, наличие и характер фазовых переходов.
 • Твердые неорганические соединения в большинстве своем построены не из отдельных молекул, их структура характеризуется определенным способом упаковки атомов или молекул сложность в пространстве. образуемых Разнообразие структурных и типов является центральным вопросом химии твердого тела.
• Твердые неорганические соединения в большинстве своем построены не из отдельных молекул, их структура характеризуется определенным способом упаковки атомов или молекул сложность в пространстве. образуемых Разнообразие структурных и типов является центральным вопросом химии твердого тела.
 • Подразумевается не только классификация и описание кристаллических структур, но и изучение факторов, ответственных за возникновение той или иной структуры. • Структура и свойства молекулярных соединений определяется структурой и свойствами индивидуальных молекул, поэтому объектами химии твердого тела преимущественно соединения. являются немолекулярные
• Подразумевается не только классификация и описание кристаллических структур, но и изучение факторов, ответственных за возникновение той или иной структуры. • Структура и свойства молекулярных соединений определяется структурой и свойствами индивидуальных молекул, поэтому объектами химии твердого тела преимущественно соединения. являются немолекулярные
 • Препаративные методы, используемые в химии твердого тела, весьма разнообразны. Они включают реакции в твердом состоянии, транспортные реакции, реакции осаждения, электрохимические процессы.
• Препаративные методы, используемые в химии твердого тела, весьма разнообразны. Они включают реакции в твердом состоянии, транспортные реакции, реакции осаждения, электрохимические процессы.
 Применяя различные методы, одни и те же вещества можно получить в различных формах – в виде монокристаллов, порошков, поликристаллических образцов и т. д. Многие приемы, используемые в химии твердого тела уникальны и не встречаются в других областях химии.
Применяя различные методы, одни и те же вещества можно получить в различных формах – в виде монокристаллов, порошков, поликристаллических образцов и т. д. Многие приемы, используемые в химии твердого тела уникальны и не встречаются в других областях химии.
 • В химии твердого тела используется особый набор методов исследования ( дифракционные методы, электронная микроскопия и др. ). • Многие методы анализа, используемые в химии твердого тела оригинальны и не применяются в других химических науках.
• В химии твердого тела используется особый набор методов исследования ( дифракционные методы, электронная микроскопия и др. ). • Многие методы анализа, используемые в химии твердого тела оригинальны и не применяются в других химических науках.
 • Одни из рентгеновская главных методов дифракция и анализа – электронная микроскопия. • Две важнейшие задачи, решаемые методом рентгеновской установление соединений; дифракции: структуры во-первых, кристаллических
• Одни из рентгеновская главных методов дифракция и анализа – электронная микроскопия. • Две важнейшие задачи, решаемые методом рентгеновской установление соединений; дифракции: структуры во-первых, кристаллических
 во-вторых, поскольку каждое порошкообразное кристаллическое только для вещество него дает картину характерную рентгеновских отражений, то ее используют подобно отпечатку пальцев при идентификации фаз. С помощью этого метода образование можно твердых изучать полиморфизм, растворов, параметры элементарной ячейки, определять размер частиц и фазовые диаграммы.
во-вторых, поскольку каждое порошкообразное кристаллическое только для вещество него дает картину характерную рентгеновских отражений, то ее используют подобно отпечатку пальцев при идентификации фаз. С помощью этого метода образование можно твердых изучать полиморфизм, растворов, параметры элементарной ячейки, определять размер частиц и фазовые диаграммы.
 • Важное значение имеют взаимодействия и прочности связей в твердых веществах. • Количественные затруднены расчеты, тем, что как в правило большинстве неорганических соединений химическую связь нельзя считать ковалентной. чисто ионной или чисто
• Важное значение имеют взаимодействия и прочности связей в твердых веществах. • Количественные затруднены расчеты, тем, что как в правило большинстве неорганических соединений химическую связь нельзя считать ковалентной. чисто ионной или чисто
 • Правильнее рассматривать ее как сочетание этих двух вкладов. В ионных соединениях связи обладают известной долей ковалентности, электронные т. е. оболочки внешние ионов поляризованы в сторону положительно заряженных катионов.
• Правильнее рассматривать ее как сочетание этих двух вкладов. В ионных соединениях связи обладают известной долей ковалентности, электронные т. е. оболочки внешние ионов поляризованы в сторону положительно заряженных катионов.
 • В ковалентных соединениях химические связи вследствие различия электроотрицательностей связанных атомов оказываются полярными. • Большей универсальностью обладает зонная теория. С ее позиций удается качественно объяснить особенности электрической полупроводников. структуры, проводимости спектров, металлов и
• В ковалентных соединениях химические связи вследствие различия электроотрицательностей связанных атомов оказываются полярными. • Большей универсальностью обладает зонная теория. С ее позиций удается качественно объяснить особенности электрической полупроводников. структуры, проводимости спектров, металлов и
 • Выявление свойств взаимосвязи твердофазных структуры материалов и – фундаментальная задача химии твердого тела. • Кроме того, она решает задачи обоснования путей создания материалов с улучшенными эксплуатационными свойствами, разработки теории строения и реакционной способности твердых тел. • .
• Выявление свойств взаимосвязи твердофазных структуры материалов и – фундаментальная задача химии твердого тела. • Кроме того, она решает задачи обоснования путей создания материалов с улучшенными эксплуатационными свойствами, разработки теории строения и реакционной способности твердых тел. • .
 • Следует рассматривать как минимум три уровня структурной организации. • 1) структуру идеальных кристаллов; • 2) дефектную структуру реальных кристаллов, включая структуру поверхностных слоев; • 3) микроструктуру или поликристаллических твердых тел текстуру
• Следует рассматривать как минимум три уровня структурной организации. • 1) структуру идеальных кристаллов; • 2) дефектную структуру реальных кристаллов, включая структуру поверхностных слоев; • 3) микроструктуру или поликристаллических твердых тел текстуру
 • Еще одна важнейшая особенность строения твердых веществ - отличие идеальной структуры кристаллов от реальной, дефектной структуры. Основой физической химии кристаллов с дефектами послужили работы Я. И. Френкеля (1926), В. Шоттки и К. Вагнера (1930). Вагнер в работах 1930 -40 -х гг. установил зависимость реакционной способности характера дефектов. твердых тел от
• Еще одна важнейшая особенность строения твердых веществ - отличие идеальной структуры кристаллов от реальной, дефектной структуры. Основой физической химии кристаллов с дефектами послужили работы Я. И. Френкеля (1926), В. Шоттки и К. Вагнера (1930). Вагнер в работах 1930 -40 -х гг. установил зависимость реакционной способности характера дефектов. твердых тел от
 • Дефектообразование является важным структурным объектом химии твердого тела. Дефекты того или иного вида присущи всем без исключения твердым телам и часто оказывают влияние на многие свойства материалов (электропроводимость, механическую прочность и реакционную способность).
• Дефектообразование является важным структурным объектом химии твердого тела. Дефекты того или иного вида присущи всем без исключения твердым телам и часто оказывают влияние на многие свойства материалов (электропроводимость, механическую прочность и реакционную способность).
 • С дефектообразованием связано существование твердых растворов, переменным составом характеризующихся твердой фазы при сохранении типа кристаллической решетки. Меняя состав регулировать твердого и свойства материалов. раствора модифицировать можно многие
• С дефектообразованием связано существование твердых растворов, переменным составом характеризующихся твердой фазы при сохранении типа кристаллической решетки. Меняя состав регулировать твердого и свойства материалов. раствора модифицировать можно многие
 • Реакции твердых тел носят топохимический характер и зачастую определяются скоростью диффузии в твердых телах. Диффузия здесь отличается от диффузии в газах и жидкостях: она может протекать на внешней поверхности, по границам кристаллитов, в объеме твердого тела и характеризуется высокими кажущейся энергии активации. значениями
• Реакции твердых тел носят топохимический характер и зачастую определяются скоростью диффузии в твердых телах. Диффузия здесь отличается от диффузии в газах и жидкостях: она может протекать на внешней поверхности, по границам кристаллитов, в объеме твердого тела и характеризуется высокими кажущейся энергии активации. значениями
 • Одна из важнейших концепций в кинетике твердофазных реакций (введена С. Хиншелвудом в 1925) состоит в протекании процессов в результате последовательного образования и роста на поверхности или в объеме исходной фазы зародышей новой твердой фазы.
• Одна из важнейших концепций в кинетике твердофазных реакций (введена С. Хиншелвудом в 1925) состоит в протекании процессов в результате последовательного образования и роста на поверхности или в объеме исходной фазы зародышей новой твердой фазы.
 • В химии твердого тела используется очень широкий набор методов синтеза - с применением низких и сверхвысоких температур, рекордно высоких давлений и сверхглубокого вакуума, сильнейших разнообразных центробежных физических полей, методов активирования процессов, при полном отсутствии гравитации.
• В химии твердого тела используется очень широкий набор методов синтеза - с применением низких и сверхвысоких температур, рекордно высоких давлений и сверхглубокого вакуума, сильнейших разнообразных центробежных физических полей, методов активирования процессов, при полном отсутствии гравитации.
 • Выбор способа получения того или иного твердого вещества в сильнейшей степени влияет на его свойства. • Значительное место в химии твердого тела занимает получение и исследование свойств пленок и покрытий.
• Выбор способа получения того или иного твердого вещества в сильнейшей степени влияет на его свойства. • Значительное место в химии твердого тела занимает получение и исследование свойств пленок и покрытий.
 • Важными этапами в развитии химии твердого тела явилось создание современных методов выращивания монокристаллов больших размеров из расплава, из перегретых водных растворов, разработка процесса выращивания по механизму пар - жидкость - кристалл, методов зонной плавки кристаллов, методов управления свойствами кристалла путем наложения при его выращивании магнитных и электрических полей.
• Важными этапами в развитии химии твердого тела явилось создание современных методов выращивания монокристаллов больших размеров из расплава, из перегретых водных растворов, разработка процесса выращивания по механизму пар - жидкость - кристалл, методов зонной плавки кристаллов, методов управления свойствами кристалла путем наложения при его выращивании магнитных и электрических полей.
 • Новую область в химии твердого тела открыло аморфных создание твердых методов получения материалов путем химического осаждения из газовой фазы с плазменной активацией.
• Новую область в химии твердого тела открыло аморфных создание твердых методов получения материалов путем химического осаждения из газовой фазы с плазменной активацией.
 • Таким путем получены необычные "сплавы" полупроводниковых элементов с водородом, фтором, азотом и др. легкими элементами, тройные и более сложные композиции, многие из которых обладают уникальными свойствами перспективы практического и имеют применения. широкие Основой микроэлектроники является планарная технология, разработанная в США в 1959.
• Таким путем получены необычные "сплавы" полупроводниковых элементов с водородом, фтором, азотом и др. легкими элементами, тройные и более сложные композиции, многие из которых обладают уникальными свойствами перспективы практического и имеют применения. широкие Основой микроэлектроники является планарная технология, разработанная в США в 1959.
 • Среди новейших направлений развития химии твердого тела - синтез и изучение высокотемпературных сверхпроводников, открытых К. Мюллером и Дж. Беднорцем (1986), создание и исследование свойств "наноструктурированных" материалов, которые состоят из частиц размером 115 нм или пленок толщиной 1 -15 нм.
• Среди новейших направлений развития химии твердого тела - синтез и изучение высокотемпературных сверхпроводников, открытых К. Мюллером и Дж. Беднорцем (1986), создание и исследование свойств "наноструктурированных" материалов, которые состоят из частиц размером 115 нм или пленок толщиной 1 -15 нм.
 • Относительно большая доля пограничных (приповерхностных) слоев определяет значительные (иногда на несколько порядков) отличия свойств наноструктурированных кристаллов и материалов стекол того Разрабатываются методы (нанотехнология) наноматериалов, гетероструктур с размерами элементов (слоев) от 1 до 10 нм. от же свойств состава. получения а также составляющих их
• Относительно большая доля пограничных (приповерхностных) слоев определяет значительные (иногда на несколько порядков) отличия свойств наноструктурированных кристаллов и материалов стекол того Разрабатываются методы (нанотехнология) наноматериалов, гетероструктур с размерами элементов (слоев) от 1 до 10 нм. от же свойств состава. получения а также составляющих их
 Классификация твердых тел • Твердые тела могут быть получены в виде: • а) монокристаллов максимально возможной чистоты и минимально возможным количеством дефектов; • б) монокристаллов с дефектной структурой, созданной путем целенаправленного введения примесей; • в) порошков, состоящих из большого числа маленьких кристалликов;
Классификация твердых тел • Твердые тела могут быть получены в виде: • а) монокристаллов максимально возможной чистоты и минимально возможным количеством дефектов; • б) монокристаллов с дефектной структурой, созданной путем целенаправленного введения примесей; • в) порошков, состоящих из большого числа маленьких кристалликов;
 • г) поликристаллических изделий (таблеток, цилиндрических трубочек и т. д. ), состоящих также из большого числа кристалликов с различной ориентацией, но плотно и прочно связанных между собой; • д) тонких пленок; • е) аморфные, стеклообразные материалы; • ж) наноматериалы.
• г) поликристаллических изделий (таблеток, цилиндрических трубочек и т. д. ), состоящих также из большого числа кристалликов с различной ориентацией, но плотно и прочно связанных между собой; • д) тонких пленок; • е) аморфные, стеклообразные материалы; • ж) наноматериалы.
 • Важный класс твердофазных материалов составляю некристаллические (аморфные или стеклообразные материалы), из которых могут также приготовлены объемные материалы или аморфные пленки.
• Важный класс твердофазных материалов составляю некристаллические (аморфные или стеклообразные материалы), из которых могут также приготовлены объемные материалы или аморфные пленки.
 Получение твердофазных материалов • Твердофазные материалы можно получать разными методами. Выбор того или иного метода зависит от целей, которые стоят перед исследователем.
Получение твердофазных материалов • Твердофазные материалы можно получать разными методами. Выбор того или иного метода зависит от целей, которые стоят перед исследователем.
 Твердофазные реакции • Для получения поликристаллических порошковых материалов чаще всего используют прямое взаимодействие реагентов друг с другом. • Твердые тела, как правило, не взаимодействуют друг с другом при обычной температуре.
Твердофазные реакции • Для получения поликристаллических порошковых материалов чаще всего используют прямое взаимодействие реагентов друг с другом. • Твердые тела, как правило, не взаимодействуют друг с другом при обычной температуре.
 • Для проведения необходимо температуры свидетельствует твердофазных между использовать до 1000 о том, ними повышенные - реакций термодинамическим факторами. реакции 15000 С. что протекание контролируется и Это и кинетическим
• Для проведения необходимо температуры свидетельствует твердофазных между использовать до 1000 о том, ними повышенные - реакций термодинамическим факторами. реакции 15000 С. что протекание контролируется и Это и кинетическим
 • Расчет свободной энергии твердофазной реакции может сказать лишь в принципе, может или не может протекать эта реакция, тогда как кинетический фактор определяет ее скорость. • Например, согласно термодинамическому расчету Mg. O и Al 2 O 3 должны взаимодействовать в соотношении 1 : 1 и давать шпинель Mg. Al 2 O 4. На практике скорость этой реакции при обычной температуре очень мала.
• Расчет свободной энергии твердофазной реакции может сказать лишь в принципе, может или не может протекать эта реакция, тогда как кинетический фактор определяет ее скорость. • Например, согласно термодинамическому расчету Mg. O и Al 2 O 3 должны взаимодействовать в соотношении 1 : 1 и давать шпинель Mg. Al 2 O 4. На практике скорость этой реакции при обычной температуре очень мала.
 • Взаимодействие смеси порошков Mg. O и Al 2 O 3 становится заметным лишь при температуре выше 12000 С, а для завершения реакции необходима выдержка этой смеси в течение суток при температуре выше 15000 С. • При приведении в контакт кристаллов Mg. O и Al 2 O 3 при комнатной температуре за счет теплового движение имеет место взаимодействие по плоскости их соприкосновения (рис. 1 а).
• Взаимодействие смеси порошков Mg. O и Al 2 O 3 становится заметным лишь при температуре выше 12000 С, а для завершения реакции необходима выдержка этой смеси в течение суток при температуре выше 15000 С. • При приведении в контакт кристаллов Mg. O и Al 2 O 3 при комнатной температуре за счет теплового движение имеет место взаимодействие по плоскости их соприкосновения (рис. 1 а).
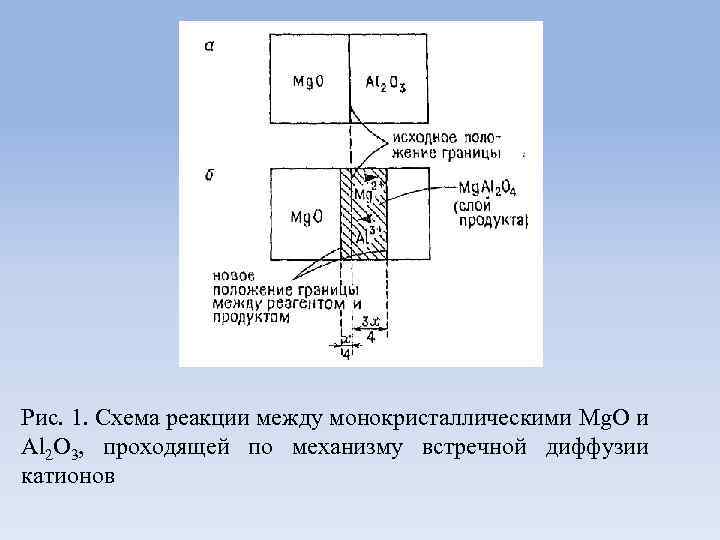 Рис. 1. Схема реакции между монокристаллическими Mg. O и Al 2 O 3, проходящей по механизму встречной диффузии катионов
Рис. 1. Схема реакции между монокристаллическими Mg. O и Al 2 O 3, проходящей по механизму встречной диффузии катионов
 • В результате теплового воздействия образуются зародыши Mg. Al 2 O 4 (рис. 1. б). Значительные структурные различия исходных веществ и продукта мешают зародышеобразования, протеканию процесса поскольку требуется разрыв старых связей и образование новых, а также миграция расстояния. атомов на значительные
• В результате теплового воздействия образуются зародыши Mg. Al 2 O 4 (рис. 1. б). Значительные структурные различия исходных веществ и продукта мешают зародышеобразования, протеканию процесса поскольку требуется разрыв старых связей и образование новых, а также миграция расстояния. атомов на значительные
 • Только при высокой температуре ионам сообщается достаточная энергия, для того чтобы они могли начать диффундировать через кристалл. Таким образом, образование Mg. Al 2 O 4 требует перегруппировки кислородных ионов в месте локализации будущего зародыша и одновременного взаимного обмена ионами Mg+2 и Al+3 кристаллов. через поверхность раздела двух
• Только при высокой температуре ионам сообщается достаточная энергия, для того чтобы они могли начать диффундировать через кристалл. Таким образом, образование Mg. Al 2 O 4 требует перегруппировки кислородных ионов в месте локализации будущего зародыша и одновременного взаимного обмена ионами Mg+2 и Al+3 кристаллов. через поверхность раздела двух
 • Следующий этап – рост образовавшегося слоя продукта может протекать еще более затрудненно. Для того, чтобы толщина слоя шпинели увеличивалась необходима взаимная диффузия Mg+2 и Al+3 через уже имеющийся слой продукта (рси. 1 б). При этом появляются две новые поверхности: одна отделяет Mg. O от Mg. Al 2 O 4, а другая Mg. Al 2 O 4 от Al 2 O 3.
• Следующий этап – рост образовавшегося слоя продукта может протекать еще более затрудненно. Для того, чтобы толщина слоя шпинели увеличивалась необходима взаимная диффузия Mg+2 и Al+3 через уже имеющийся слой продукта (рси. 1 б). При этом появляются две новые поверхности: одна отделяет Mg. O от Mg. Al 2 O 4, а другая Mg. Al 2 O 4 от Al 2 O 3.
 • Если принять, что диффузия ионов Mg+2 и Al+3 к этим поверхностям является стадией, лимитирующей скорость реакции в целом, то понятно почему взаимодействие между Mg. O и Al 2 O 3 протекает медленно даже при высоких температурах. При этом скорость будет постепенно убывать, так как толщина слоя будет увеличиваться.
• Если принять, что диффузия ионов Mg+2 и Al+3 к этим поверхностям является стадией, лимитирующей скорость реакции в целом, то понятно почему взаимодействие между Mg. O и Al 2 O 3 протекает медленно даже при высоких температурах. При этом скорость будет постепенно убывать, так как толщина слоя будет увеличиваться.
 • Эксперимент показал, что действительно встречная диффузия ионов через слой образовавшейся шпинели является лимитирующей стадией. Простая модель диффузии через плоский слой описывается параболической зависимостью: • dx/dt = kx-1 или x = (k't)1/2 (1. 1) • где х – количество образовавшегося продукта, • t –время, k и k‘ –константы скорости реакции
• Эксперимент показал, что действительно встречная диффузия ионов через слой образовавшейся шпинели является лимитирующей стадией. Простая модель диффузии через плоский слой описывается параболической зависимостью: • dx/dt = kx-1 или x = (k't)1/2 (1. 1) • где х – количество образовавшегося продукта, • t –время, k и k‘ –константы скорости реакции
 Реакционная способность твердых тел – зародышеобразование и скорость диффузии • Взаимодействие двух твердых тел можно разделить на две стадии – образование зародышей и их Зародышеобразование последующий проходит рост. быстрее, если продукт реакции структурно близок хотя бы к одному из реагентов.
Реакционная способность твердых тел – зародышеобразование и скорость диффузии • Взаимодействие двух твердых тел можно разделить на две стадии – образование зародышей и их Зародышеобразование последующий проходит рост. быстрее, если продукт реакции структурно близок хотя бы к одному из реагентов.
 • Это уменьшает число структурных перестроек, необходимых для образования зародышей. Так, при взаимодействии Mg. O и Al 2 O 3, образующаяся шпинель имеет упаковку кислородных ионов, похожую на упаковку в Mg. O. Зародыши шпинели могут поэтому образовываться на поверхности Mg. O, при этом кислородная подрешетка на границе Mg. O/шпинель остается почти непрерывной.
• Это уменьшает число структурных перестроек, необходимых для образования зародышей. Так, при взаимодействии Mg. O и Al 2 O 3, образующаяся шпинель имеет упаковку кислородных ионов, похожую на упаковку в Mg. O. Зародыши шпинели могут поэтому образовываться на поверхности Mg. O, при этом кислородная подрешетка на границе Mg. O/шпинель остается почти непрерывной.
 Топотаксические и эпитаксиальные реакции • Все явления ориентационного зародышеобразования можно разделить на два типа: топотаксические и эпитаксиальные реакции. • В случае эпитаксиальных реакций соответствие наблюдается только на поверхности раздела двух фаз
Топотаксические и эпитаксиальные реакции • Все явления ориентационного зародышеобразования можно разделить на два типа: топотаксические и эпитаксиальные реакции. • В случае эпитаксиальных реакций соответствие наблюдается только на поверхности раздела двух фаз
 • Гипотетически возможна ситуация, когда две структуры имеют идентичную структуру кислорода в разделяющей их общей плоскости, но при удалении от этой плоскости идентичность не сохраняется. Следовательно, эпитаксиальные это такие реакции, которые требуют лишь двумерного структурного сходства на границе двух кристаллов.
• Гипотетически возможна ситуация, когда две структуры имеют идентичную структуру кислорода в разделяющей их общей плоскости, но при удалении от этой плоскости идентичность не сохраняется. Следовательно, эпитаксиальные это такие реакции, которые требуют лишь двумерного структурного сходства на границе двух кристаллов.
 • Для топотаксических процессов требования сходства структуры не ограничивается поверхностью раздела, а распространяется так же и на примыкающие к ней объемы обеих фаз. Такое соответствие наблюдается в частности при нарастании Mg. Al 2 O 4 на поверхности Mg. O.
• Для топотаксических процессов требования сходства структуры не ограничивается поверхностью раздела, а распространяется так же и на примыкающие к ней объемы обеих фаз. Такое соответствие наблюдается в частности при нарастании Mg. Al 2 O 4 на поверхности Mg. O.
 • Для того чтобы зародышеобразование имело ориентационное место, не достаточно одного сходства мотивов структур на разделяющей их границе. Необходимо также соответствие размеров элементарных ячеек и межатомных расстояний.
• Для того чтобы зародышеобразование имело ориентационное место, не достаточно одного сходства мотивов структур на разделяющей их границе. Необходимо также соответствие размеров элементарных ячеек и межатомных расстояний.
 • Если же компоненты имеют сильно различающиеся межатомные расстояния (Ba. O Mg. O) фазы не могут срастаться на большой площади контакта. Было показано, что для осуществления зародышеобразования ориентационного разность параметров решетки на поверхности раздела между фазой субстрата и зародышем не должна превышать 15%
• Если же компоненты имеют сильно различающиеся межатомные расстояния (Ba. O Mg. O) фазы не могут срастаться на большой площади контакта. Было показано, что для осуществления зародышеобразования ориентационного разность параметров решетки на поверхности раздела между фазой субстрата и зародышем не должна превышать 15%
 Структура поверхности и реакционная способность • Рассмотрение кристаллических структур различных типов показывает, что в большинстве случаев структура поверхности не может быть одинаковой для всего кристалла в целом. Исключения составляют лишь вещества со структурой каменной соли, в частности Mg. O, кристаллы которых образуют тдеальные кубы (рис. 2. 2 в)
Структура поверхности и реакционная способность • Рассмотрение кристаллических структур различных типов показывает, что в большинстве случаев структура поверхности не может быть одинаковой для всего кристалла в целом. Исключения составляют лишь вещества со структурой каменной соли, в частности Mg. O, кристаллы которых образуют тдеальные кубы (рис. 2. 2 в)
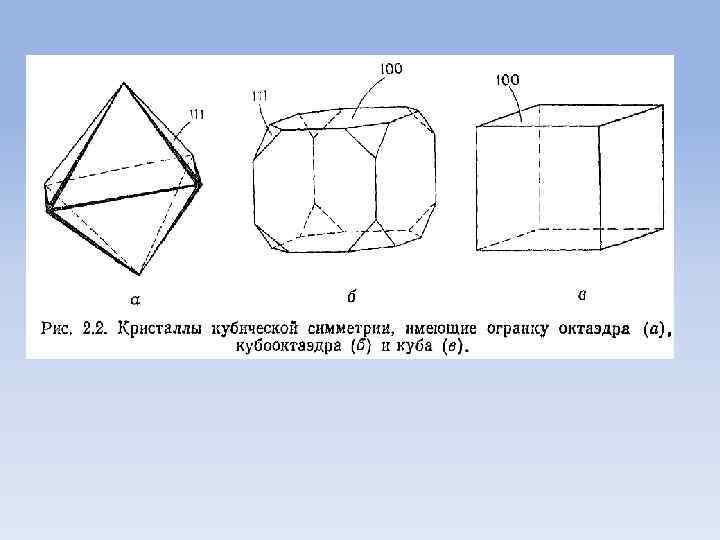
 • Каждая грань куба 100 имеет одинаковое строение, причем анионы и катионы располагаются в вершинах квадрата (рис. 2. 3. а) • Две различные структуры поверхности приведены на рис. 2. 3. б. При срезании вершин того же кубического кристалла Mg. O обнаруживаются грании 111 , параллельные плоскостям (111), проходящим через чередующиеся слои ионов Mg+2 и ионов O-2. В итоге на гранях 111 лежат либо только ионы Mg+2, либо только ионы O-2.
• Каждая грань куба 100 имеет одинаковое строение, причем анионы и катионы располагаются в вершинах квадрата (рис. 2. 3. а) • Две различные структуры поверхности приведены на рис. 2. 3. б. При срезании вершин того же кубического кристалла Mg. O обнаруживаются грании 111 , параллельные плоскостям (111), проходящим через чередующиеся слои ионов Mg+2 и ионов O-2. В итоге на гранях 111 лежат либо только ионы Mg+2, либо только ионы O-2.

 • Очевидное различие структур поверхностей 100 и 111 приводит и к различию их реакционных способностей. • Хорошо известный пример этого наблюдается при росте кристаллов Na. Cl из раствора. Обычной морфологии отвечают кубы с гранями 100 (рис. 2. 2. в), но если в раствор добавить мочевины, то начинают расти октаэдры (рис. 2. 2 а), каждая грань которых является плоскостью 100.
• Очевидное различие структур поверхностей 100 и 111 приводит и к различию их реакционных способностей. • Хорошо известный пример этого наблюдается при росте кристаллов Na. Cl из раствора. Обычной морфологии отвечают кубы с гранями 100 (рис. 2. 2. в), но если в раствор добавить мочевины, то начинают расти октаэдры (рис. 2. 2 а), каждая грань которых является плоскостью 100.
 • Мочевина при этом не входит в состав кристалла, но влияет на реакционную способность отдельных граней. • Основная морфологическая закономерность при росте кристаллов заключается в том, что наиболее предпочтительные медленнее остальных. грани растут
• Мочевина при этом не входит в состав кристалла, но влияет на реакционную способность отдельных граней. • Основная морфологическая закономерность при росте кристаллов заключается в том, что наиболее предпочтительные медленнее остальных. грани растут
 • Представим себе кристалл (рис. 2. 2. б), имеющий и грани 100 и 111 (куб со срезанными вершинами), растет только по граням 111. В итоге будут достроены вершины и получится идеальный куб. Напротив, если рост будет идти только по граням 100 , то получится завершенный октаэдр (рис. 2. 2. а). Таким образом, мочевина замедляет рост сравнении с гранями 100. граней 111 в
• Представим себе кристалл (рис. 2. 2. б), имеющий и грани 100 и 111 (куб со срезанными вершинами), растет только по граням 111. В итоге будут достроены вершины и получится идеальный куб. Напротив, если рост будет идти только по граням 100 , то получится завершенный октаэдр (рис. 2. 2. а). Таким образом, мочевина замедляет рост сравнении с гранями 100. граней 111 в
 Можно сделать вывод о том, что реакционная особность кристаллов на отдельных участках их верхности, различающихся по структуре, также злична. Однако невозможно предсказать на какой граней будет проявляться наибольшая акционная способность. Реакционная способность твердых тел в ачительной степени зависит от наличия дефектов руктуры.
Можно сделать вывод о том, что реакционная особность кристаллов на отдельных участках их верхности, различающихся по структуре, также злична. Однако невозможно предсказать на какой граней будет проявляться наибольшая акционная способность. Реакционная способность твердых тел в ачительной степени зависит от наличия дефектов руктуры.
 • Влияние дефектов на объемные свойства достаточно хорошо изучено. В гораздо меньшей степени исследованы вопросы влияния на свойства кристалла поверхностных или приповерхностных дефектов. • Влияние винтовых дислокаций на рост кристалла и образование спиральных ступеней роста показано на рис. 2. 4
• Влияние дефектов на объемные свойства достаточно хорошо изучено. В гораздо меньшей степени исследованы вопросы влияния на свойства кристалла поверхностных или приповерхностных дефектов. • Влияние винтовых дислокаций на рост кристалла и образование спиральных ступеней роста показано на рис. 2. 4

 • Такая картина наблюдается, если исходная поверхность кристаллического зародыша не является строго плоской, а несколько искажена в области выхода дислокаций. • Приведенное уравнение скорости реакции (1. 1) связывает скорость реакции с диффузией ионов. Наличие таких дефектов кристаллической структуры как вакансии, межузельные ионы, дислокационные трубки, резко укоряет диффузию.
• Такая картина наблюдается, если исходная поверхность кристаллического зародыша не является строго плоской, а несколько искажена в области выхода дислокаций. • Приведенное уравнение скорости реакции (1. 1) связывает скорость реакции с диффузией ионов. Наличие таких дефектов кристаллической структуры как вакансии, межузельные ионы, дислокационные трубки, резко укоряет диффузию.
 Экспериментальное осуществление твердофазных реакций • Рассмотрим типичную последовательность операций при синтезе, например, шпинели. • Исходные реагенты должны быть тщательно высушены (особенно Mg. O) в течение нескольких часов при температуре 200 – 8000 С. Для увеличения контакта необходимо использовать как можно более тонкодисперсный порошок.
Экспериментальное осуществление твердофазных реакций • Рассмотрим типичную последовательность операций при синтезе, например, шпинели. • Исходные реагенты должны быть тщательно высушены (особенно Mg. O) в течение нескольких часов при температуре 200 – 8000 С. Для увеличения контакта необходимо использовать как можно более тонкодисперсный порошок.
 Приготовление реакционной смеси • Из взятых компонентов в надо нужных весовых приготовить количествах смесь. Если используются небольшие количества смесь можно растереть в агатовой ступке. При этом можно использовать небольшое количество легколетучих жидкостей (ацетон). • Если нужны значительные количества, используются шаровые мельницы.
Приготовление реакционной смеси • Из взятых компонентов в надо нужных весовых приготовить количествах смесь. Если используются небольшие количества смесь можно растереть в агатовой ступке. При этом можно использовать небольшое количество легколетучих жидкостей (ацетон). • Если нужны значительные количества, используются шаровые мельницы.
 Материал контейнера • Необходимо выбрать в качестве материала контейнера такой, который не взаимодействовал бы с компонентами реакции при данной температуре. • Как правило лучше всего подходит платина (платиновые тигли).
Материал контейнера • Необходимо выбрать в качестве материала контейнера такой, который не взаимодействовал бы с компонентами реакции при данной температуре. • Как правило лучше всего подходит платина (платиновые тигли).
 • Для реакций, протекающих при более низких температурах возможно использование других металлов (никель) или неметаллических огнеупорных материалов.
• Для реакций, протекающих при более низких температурах возможно использование других металлов (никель) или неметаллических огнеупорных материалов.
 Термообработка • Рациональный многом зависит режим от термообработки вида и во реакционной способности реагентов. Так, смесь Mg. O и Al 2 O 3 следует сразу помещать в печь, нагретую до 1400 – 16000 С. При использовании кислородсодержащей соли, например Mg. CO 3, первой стадией будет ее разложение.
Термообработка • Рациональный многом зависит режим от термообработки вида и во реакционной способности реагентов. Так, смесь Mg. O и Al 2 O 3 следует сразу помещать в печь, нагретую до 1400 – 16000 С. При использовании кислородсодержащей соли, например Mg. CO 3, первой стадией будет ее разложение.
 • В таких случаях смесь следует выдержать при температуре разложения этой соли, с тем, чтобы разложение контролируемом режиме. протекало в
• В таких случаях смесь следует выдержать при температуре разложения этой соли, с тем, чтобы разложение контролируемом режиме. протекало в
 Анализ • Продукты твердофазных реакций обычно представляют собой порошки или спеченную поликристаллическую массу. Рентгеновская дифракция на порошках является основным методом идентификации кристаллических фаз. присутствующих
Анализ • Продукты твердофазных реакций обычно представляют собой порошки или спеченную поликристаллическую массу. Рентгеновская дифракция на порошках является основным методом идентификации кристаллических фаз. присутствующих
 • Рентгенограмма позволяет установить прошла ли реакция до конца, образовался ли желаемый продукт, присутствуют ли побочные или промежуточные фазы. • С помощью рентгеновского метода однако невозможно определить состав продукта. Для этого используются рентгенолюминисцентный или атомно-абсорбционный методы.
• Рентгенограмма позволяет установить прошла ли реакция до конца, образовался ли желаемый продукт, присутствуют ли побочные или промежуточные фазы. • С помощью рентгеновского метода однако невозможно определить состав продукта. Для этого используются рентгенолюминисцентный или атомно-абсорбционный методы.
 Совместное осаждение как пример интенсификации твердофазных реакций • Помимо очевидного влияния температуры на скорость твердофазной реакции между веществами, смешанными механическим путем, сильное воздействие оказывает размер частиц реагентов, смешивании степень их и степень отдельных зерен. гомогенизации при контактирования
Совместное осаждение как пример интенсификации твердофазных реакций • Помимо очевидного влияния температуры на скорость твердофазной реакции между веществами, смешанными механическим путем, сильное воздействие оказывает размер частиц реагентов, смешивании степень их и степень отдельных зерен. гомогенизации при контактирования
 • Используя прием совместного осаждения компонентов реакции, в ряде случаев можно получить одновременно малый размер частиц и высокую степень гомогенизации, что соответствует ускорению реакции. Примером может служить синтез феррита цинка Zn. Fe 2 O 4. • В одном из методов получения этого вещества и родственных ему ферритов исходят из оксалатов цинка и железа, которые по отдельности растворяются в воде, затем смешивают эти растворы, соблюдая эквивалентное соотношение катионов, и постепенно испаряют воду.
• Используя прием совместного осаждения компонентов реакции, в ряде случаев можно получить одновременно малый размер частиц и высокую степень гомогенизации, что соответствует ускорению реакции. Примером может служить синтез феррита цинка Zn. Fe 2 O 4. • В одном из методов получения этого вещества и родственных ему ферритов исходят из оксалатов цинка и железа, которые по отдельности растворяются в воде, затем смешивают эти растворы, соблюдая эквивалентное соотношение катионов, и постепенно испаряют воду.
 • Из раствора постепенно осаждается мелкодисперсный осадок смеси оксалатов, в котором достигается высокая степень смешения компонентов. Осадок отделяют фильтрованием, сушат и прокаливают. • Благодаря высокой степени гомогенизации для окончания реакции образования Zn. Fe 2 O 4 требуется гораздо более низкая температура (~10000 С), чем при работе со смесью оксидов, полученной механическим смешением.
• Из раствора постепенно осаждается мелкодисперсный осадок смеси оксалатов, в котором достигается высокая степень смешения компонентов. Осадок отделяют фильтрованием, сушат и прокаливают. • Благодаря высокой степени гомогенизации для окончания реакции образования Zn. Fe 2 O 4 требуется гораздо более низкая температура (~10000 С), чем при работе со смесью оксидов, полученной механическим смешением.
 • Суммарная реакция выражается уравнением: • Fe 2(C 2 O 4)3 + Zn. C 2 O 4 Zn. Fe 2 O 4 + 4 CO 4 • Таким же образом могут быть получены ферриты кобальта, никеля, марганца, а также их твердые растворы. Описанный прием мало пригоден для реагентов сильно различающихся по растворимости в воде, или по скорости образования осадков, в том числе систем, склонных к образованию пересыщенных растворов.
• Суммарная реакция выражается уравнением: • Fe 2(C 2 O 4)3 + Zn. C 2 O 4 Zn. Fe 2 O 4 + 4 CO 4 • Таким же образом могут быть получены ферриты кобальта, никеля, марганца, а также их твердые растворы. Описанный прием мало пригоден для реагентов сильно различающихся по растворимости в воде, или по скорости образования осадков, в том числе систем, склонных к образованию пересыщенных растворов.
 Другие приемы предварительной гомогенизации • Один из способов гомогенизации заключается в осаждении смешанных солей стехиометрического состава. Например феррит Ni. Fe 2 O 4 со структурой шпинели был синтезирован через промежуточный пиридиновый аддукт двойного основного ацетата никеля и железа Ni 3 Fe 6(CH 3 COO)17 O 3 OH·C 5 H 5 N
Другие приемы предварительной гомогенизации • Один из способов гомогенизации заключается в осаждении смешанных солей стехиометрического состава. Например феррит Ni. Fe 2 O 4 со структурой шпинели был синтезирован через промежуточный пиридиновый аддукт двойного основного ацетата никеля и железа Ni 3 Fe 6(CH 3 COO)17 O 3 OH·C 5 H 5 N
 • Стехиометрия последнего обеспечивает молярное соотношение Ni: Fe, в точности равное двум, причем для очистки можно использовать перекристаллизацию из пиридина. Пиридиновый аддукт готовят из кристаллогидрата двойного основного ацетата никеля и железа. Кристаллы двойного аддукта с пиридином медленно нагревают до 200 – 3000 С для окисления органического компонента с последующей выдержкой остатка при ~10000 С на воздухе в течение 2 – 3 суток
• Стехиометрия последнего обеспечивает молярное соотношение Ni: Fe, в точности равное двум, причем для очистки можно использовать перекристаллизацию из пиридина. Пиридиновый аддукт готовят из кристаллогидрата двойного основного ацетата никеля и железа. Кристаллы двойного аддукта с пиридином медленно нагревают до 200 – 3000 С для окисления органического компонента с последующей выдержкой остатка при ~10000 С на воздухе в течение 2 – 3 суток
 • Подобная методика использована при получении шпинелей хромитов MCr. O 4 (Mg, Zn, Cu, Mn, Fe, Co, Ni). • Получение конечных продуктов в случае ферритов и хромитов с точной стехиометрией очень важно, так как свойства приготовленных из них магнитных материалов, чрезвычайно чувствительны к стереометрии и чистоте.
• Подобная методика использована при получении шпинелей хромитов MCr. O 4 (Mg, Zn, Cu, Mn, Fe, Co, Ni). • Получение конечных продуктов в случае ферритов и хромитов с точной стехиометрией очень важно, так как свойства приготовленных из них магнитных материалов, чрезвычайно чувствительны к стереометрии и чистоте.
 Кинетика твердофазных реакций • Изучение кинетики ставит своей целью выявление той стадии, которая является лимитирующей для скорости процесса в целом. • Поскольку реакции между твердыми веществами протекают на границе раздела, может быть лимитирующей одна из трех стадий:
Кинетика твердофазных реакций • Изучение кинетики ставит своей целью выявление той стадии, которая является лимитирующей для скорости процесса в целом. • Поскольку реакции между твердыми веществами протекают на границе раздела, может быть лимитирующей одна из трех стадий:
 1) перенос вещества к границе раздела; 2) взаимодействие на границе; 3) перенос вещества от границы в объем фазы. Для большинства реакций в твердых телах понятие порядка реакции лишено смысла, иак как в этих реакциях нет отдельно участвующих в элементарном акте молекул. • Однако для эмпирического описания кинетики твердофазных реакций уравнение • dc/dt = - kcn применяется • •
1) перенос вещества к границе раздела; 2) взаимодействие на границе; 3) перенос вещества от границы в объем фазы. Для большинства реакций в твердых телах понятие порядка реакции лишено смысла, иак как в этих реакциях нет отдельно участвующих в элементарном акте молекул. • Однако для эмпирического описания кинетики твердофазных реакций уравнение • dc/dt = - kcn применяется • •
 Кристаллизация растворов, расплавов, стекол и гелей • Состояние исходных веществ – водных растворов, расплавов, стекол и гелей характеризуется гомогенностью, однофазностью и аморфностью. Образование конечных кристаллических продуктов может протекать легче, чем при твердофазном синтезе, так как уже устранена необходимость диффузионного массопереноса на макроскопическое расстояние.
Кристаллизация растворов, расплавов, стекол и гелей • Состояние исходных веществ – водных растворов, расплавов, стекол и гелей характеризуется гомогенностью, однофазностью и аморфностью. Образование конечных кристаллических продуктов может протекать легче, чем при твердофазном синтезе, так как уже устранена необходимость диффузионного массопереноса на макроскопическое расстояние.
 • В некоторых случаях метод предварительной кристаллизации позволяет получить метастабильные фазы, что не удается сделать при других подходах.
• В некоторых случаях метод предварительной кристаллизации позволяет получить метастабильные фазы, что не удается сделать при других подходах.
 Кристаллизация из растворов и гелей • Кристаллизация из водных растворов, протекающая при более низких температурах (25 – 1000 С), чем твердофазные взаимодействия, имеет другими неоспоримые преимущества методами кристаллогидратов, при смешанных перед получении солей, в особенности, если эти соединения неустойчивы при высоких температурах.
Кристаллизация из растворов и гелей • Кристаллизация из водных растворов, протекающая при более низких температурах (25 – 1000 С), чем твердофазные взаимодействия, имеет другими неоспоримые преимущества методами кристаллогидратов, при смешанных перед получении солей, в особенности, если эти соединения неустойчивы при высоких температурах.
 • Например, синтез цеолитов. Эти соединения представляют собой гидратированные алюмосиликаты, в структуре которых имеются довольно значительные полости и каналы (диаметр. 4 – 6 А 0). • В этих пустотах могут задерживаться молекулы органических и неорганических веществ, благодаря чему цеолиты находят применение в качестве молекулярных сит.
• Например, синтез цеолитов. Эти соединения представляют собой гидратированные алюмосиликаты, в структуре которых имеются довольно значительные полости и каналы (диаметр. 4 – 6 А 0). • В этих пустотах могут задерживаться молекулы органических и неорганических веществ, благодаря чему цеолиты находят применение в качестве молекулярных сит.
 • Синтетические цеолиты могут быть получены из водных растворов, содержащих силикаты и алюминаты щелочных металлов. В результате конденсации силикат- и алюминатионов, произвольно протекающей в таких растворах, образуются гели.
• Синтетические цеолиты могут быть получены из водных растворов, содержащих силикаты и алюминаты щелочных металлов. В результате конденсации силикат- и алюминатионов, произвольно протекающей в таких растворах, образуются гели.
 • Термическая или их гидротермальная обработка (т. е. нагревание при высоком давлении паров воды) приводит к кристаллизации цеолитов. • Na. Al(OH)4 + Na 2 Si. O 3 + Na. OH • • Водный раствор 250 С • [Naa(Al. O 2)b (Si. O 2)c ·Na. OH·H 2 O ] • гель 25 1750 С • [Naх(Al. O 2)х (Si. O 2)y ]·m. H 2 O • Кристаллический цеолит
• Термическая или их гидротермальная обработка (т. е. нагревание при высоком давлении паров воды) приводит к кристаллизации цеолитов. • Na. Al(OH)4 + Na 2 Si. O 3 + Na. OH • • Водный раствор 250 С • [Naa(Al. O 2)b (Si. O 2)c ·Na. OH·H 2 O ] • гель 25 1750 С • [Naх(Al. O 2)х (Si. O 2)y ]·m. H 2 O • Кристаллический цеолит
 • Опыт, накопленный гидротермальных при реакций, осуществлении позволяет сделать следующие обобщения (по Бреку): • в качестве исходных веществ следует использовать свежеосажденные гели или аморфные осадки; • важное значение имеет р. Н; в геле следует поддерживать высокое сильных щелочей; р. Н путем добавления
• Опыт, накопленный гидротермальных при реакций, осуществлении позволяет сделать следующие обобщения (по Бреку): • в качестве исходных веществ следует использовать свежеосажденные гели или аморфные осадки; • важное значение имеет р. Н; в геле следует поддерживать высокое сильных щелочей; р. Н путем добавления
 • наиболее подходят мягкие гидротермальные условия, т. е. невысокая температура и невысокое давление насыщенного водяного пара, развивающееся в результате испарения воды, содержащейся в геле; • для появления кристаллов большого желательна пересыщения геля. количества высокая степень
• наиболее подходят мягкие гидротермальные условия, т. е. невысокая температура и невысокое давление насыщенного водяного пара, развивающееся в результате испарения воды, содержащейся в геле; • для появления кристаллов большого желательна пересыщения геля. количества высокая степень
 Кристаллизация из расплавов • Кристаллизация из расплавов как препаративный метод имеет очень много общего с кристаллизацией из растворов: совместное плавление исходных твердых веществ способствует высокой степени гомогенизации, а при охлаждении расплава образование и рост кристаллов. происходит
Кристаллизация из расплавов • Кристаллизация из расплавов как препаративный метод имеет очень много общего с кристаллизацией из растворов: совместное плавление исходных твердых веществ способствует высокой степени гомогенизации, а при охлаждении расплава образование и рост кристаллов. происходит
 • Кристаллизация из растворов и кристаллизация из расплавов отличаются только температурными диапазонами осуществления этих процессов. • Кристаллизация лежит в основе большинства методов получения монокристаллов, в особенности крупных, так как интенсивный массоперенос в жидкой фазе при малом числе центров кристаллизации способствует росту единичных кристаллов.
• Кристаллизация из растворов и кристаллизация из расплавов отличаются только температурными диапазонами осуществления этих процессов. • Кристаллизация лежит в основе большинства методов получения монокристаллов, в особенности крупных, так как интенсивный массоперенос в жидкой фазе при малом числе центров кристаллизации способствует росту единичных кристаллов.
 • Для грамотного подхода к процессу кристаллизации необходимо знание диаграмм состояния соответствующих систем, которые в графическом виде отражают взаимосвязь температуры и состава кристаллизующихся веществ. • При кристаллизации конгруэнтно плавящихся соединений состав жидкости и кристаллов идентичен, так что для роста последних необходимо знать лишь температуру плавления.
• Для грамотного подхода к процессу кристаллизации необходимо знание диаграмм состояния соответствующих систем, которые в графическом виде отражают взаимосвязь температуры и состава кристаллизующихся веществ. • При кристаллизации конгруэнтно плавящихся соединений состав жидкости и кристаллов идентичен, так что для роста последних необходимо знать лишь температуру плавления.
 • Однако чаще образующиеся из всего жидкая нее кристаллы фаза и имеют различный состав. Рассмотрим простейшую систему А—В, в которой образуется эвтектика (рис. 2. 5).
• Однако чаще образующиеся из всего жидкая нее кристаллы фаза и имеют различный состав. Рассмотрим простейшую систему А—В, в которой образуется эвтектика (рис. 2. 5).
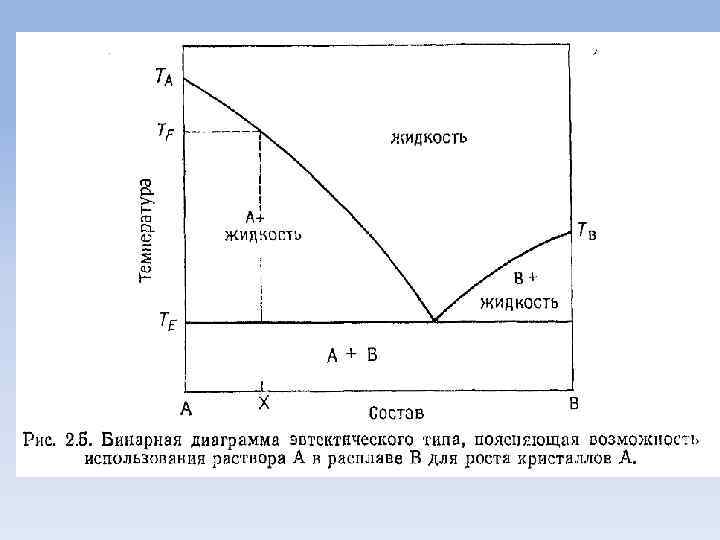
 • Предположим, что необходимо получить кристаллы вещества А, имеющего температуру плавления ТА. Добавление вещества В к веществу А приводит к тому, что плавление происходит теперь в некотором интервале температур, от ТЕ ДО ТА Например, для смеси состава X плавление начинается при ТЕ И заканчивается лишь при достижении ТF
• Предположим, что необходимо получить кристаллы вещества А, имеющего температуру плавления ТА. Добавление вещества В к веществу А приводит к тому, что плавление происходит теперь в некотором интервале температур, от ТЕ ДО ТА Например, для смеси состава X плавление начинается при ТЕ И заканчивается лишь при достижении ТF
 • В интервале ТЕ TF смесь расплавлена частично и состоит из кристаллов А и жидкости, состав которой непрерывно меняется с температурой. Для получения кристаллов А смесь X следует медленно охлаждать от ТF до ТЕ или выдерживать при постоянной превышающей ТЕ. температуре, несколько
• В интервале ТЕ TF смесь расплавлена частично и состоит из кристаллов А и жидкости, состав которой непрерывно меняется с температурой. Для получения кристаллов А смесь X следует медленно охлаждать от ТF до ТЕ или выдерживать при постоянной превышающей ТЕ. температуре, несколько
 • При последующем охлаждении до комнатной температуры остающаяся кристаллизуется, жидкость образуя эвтектическую структуру—мелкозернистую смесь кристаллов А и В. Более крупные кристаллы образовавшиеся в результате кристаллизации при высокой А, первичной температуре, распределены в этой эвтектической смеси.
• При последующем охлаждении до комнатной температуры остающаяся кристаллизуется, жидкость образуя эвтектическую структуру—мелкозернистую смесь кристаллов А и В. Более крупные кристаллы образовавшиеся в результате кристаллизации при высокой А, первичной температуре, распределены в этой эвтектической смеси.
 • Хорошие условия массопереноса, имеющиеся в расплаве, позволяют при длительном росте получить кристаллы значительных размеров. В этом отношении кристаллизация из расплавов также во многом похожа на кристаллизацию из водных растворов.
• Хорошие условия массопереноса, имеющиеся в расплаве, позволяют при длительном росте получить кристаллы значительных размеров. В этом отношении кристаллизация из расплавов также во многом похожа на кристаллизацию из водных растворов.
 • На рис. 2. 6 изображена фазовая диаграмма системы, в которой образуется химическое соединение, плавящееся инконгруэнтно. При охлаждении жидкости, состав которой в точности соответствует этому соединению, ниже ТF из расплава в первую очередь кристаллизуется вещество А.
• На рис. 2. 6 изображена фазовая диаграмма системы, в которой образуется химическое соединение, плавящееся инконгруэнтно. При охлаждении жидкости, состав которой в точности соответствует этому соединению, ниже ТF из расплава в первую очередь кристаллизуется вещество А.
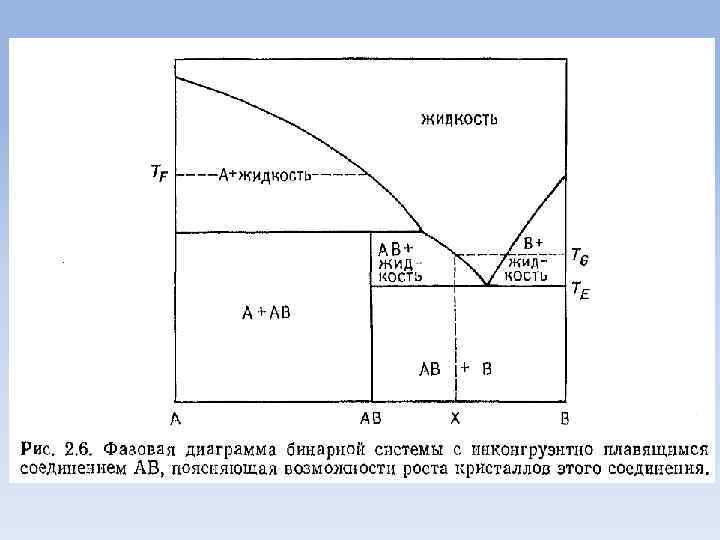
 • Поэтому при необходимости получения кристаллов соединения АВ следует выбирать для кристаллизации такие составы, в которых в равновесии с расплавом находится именно эта фаза. Например, кристаллы АВ вырастают из расплава состава X при охлаждении его от ТG до Т Е.
• Поэтому при необходимости получения кристаллов соединения АВ следует выбирать для кристаллизации такие составы, в которых в равновесии с расплавом находится именно эта фаза. Например, кристаллы АВ вырастают из расплава состава X при охлаждении его от ТG до Т Е.
 Кристаллизация стекол • В некоторых кристаллических случаях фаз при синтезе целесообразно использовать промежуточное образование стекол. Переходы из стеклообразного состояния в кристаллическое играют важную роль в производстве стеклокерамических материалов (ситаллов).
Кристаллизация стекол • В некоторых кристаллических случаях фаз при синтезе целесообразно использовать промежуточное образование стекол. Переходы из стеклообразного состояния в кристаллическое играют важную роль в производстве стеклокерамических материалов (ситаллов).
 • Так, при распространенного необходимости компонента получения ситаллов ортосиликата лития Li 2 Si 205 можно поступить следующим образом: расплавить смесь оксидов Li 2 О и Si 02, взятых в отношении 1: 2 (tпл Li 2 Si 205 1032 °С), и затем быстро охладить расплав от — 1100 °С до комнатной температуры.
• Так, при распространенного необходимости компонента получения ситаллов ортосиликата лития Li 2 Si 205 можно поступить следующим образом: расплавить смесь оксидов Li 2 О и Si 02, взятых в отношении 1: 2 (tпл Li 2 Si 205 1032 °С), и затем быстро охладить расплав от — 1100 °С до комнатной температуры.
 • Образовавшееся при этом прозрачное стекло характеризуется температурой перехода ~450°С, так что нагревание до 500— 700 °С вызывает кристаллизацию Li 2 Si 205, которая завершается за несколько применение часов. этого Очевидно, однако, синтетического что приема ограничено не слишком широким кругом систем, склонных к стеклообразованию.
• Образовавшееся при этом прозрачное стекло характеризуется температурой перехода ~450°С, так что нагревание до 500— 700 °С вызывает кристаллизацию Li 2 Si 205, которая завершается за несколько применение часов. этого Очевидно, однако, синтетического что приема ограничено не слишком широким кругом систем, склонных к стеклообразованию.
 Транспортные реакции в паровой фазе • Интересным препаративным методом является метод, основанный на химическом транспорте через паровую фазу. Химический транспорт используют как для очистки соединений, так и для получения новых фаз, в том числе в виде монокристаллов.
Транспортные реакции в паровой фазе • Интересным препаративным методом является метод, основанный на химическом транспорте через паровую фазу. Химический транспорт используют как для очистки соединений, так и для получения новых фаз, в том числе в виде монокристаллов.
 • Для этого на одном конце прозрачной трубки, как правило из кварцевого стекла, помещают вещество А. Трубку заполняют газом – переносчиком или вакуумируют и запаивают (рис. 2. 7). Трубку помещают в печь или иное нагревательное устройство, обеспечивающее градиент температуры по длине трубки. Перепад температуры на концах трубки обычно составляет 500 С.
• Для этого на одном конце прозрачной трубки, как правило из кварцевого стекла, помещают вещество А. Трубку заполняют газом – переносчиком или вакуумируют и запаивают (рис. 2. 7). Трубку помещают в печь или иное нагревательное устройство, обеспечивающее градиент температуры по длине трубки. Перепад температуры на концах трубки обычно составляет 500 С.
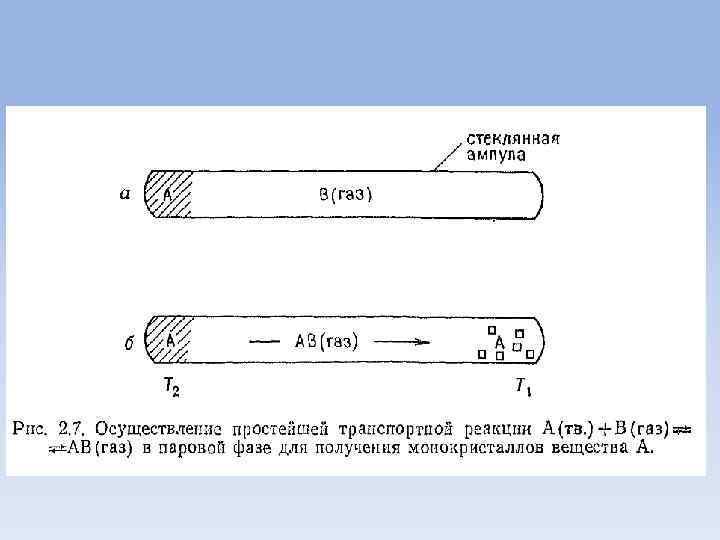
 • Вещество А и В при нагревании образуют газообразное вещество АВ, которое разлагается на другом конце трубки, образуя вещество А (рис. 2. 7). Этот метод основан на том, что реакции образования вещества АВ и его распада легко достигают равновесного состояния.
• Вещество А и В при нагревании образуют газообразное вещество АВ, которое разлагается на другом конце трубки, образуя вещество А (рис. 2. 7). Этот метод основан на том, что реакции образования вещества АВ и его распада легко достигают равновесного состояния.
 • Если образование эндотермическая поглощением вещества реакция тепла), то (происходит это АВ с соединение возникает в более горячем пространстве, конце трубки (Т 2), а в холодном (Т 1) молекулы, перенесенные через паровую фазу, распадаются.
• Если образование эндотермическая поглощением вещества реакция тепла), то (происходит это АВ с соединение возникает в более горячем пространстве, конце трубки (Т 2), а в холодном (Т 1) молекулы, перенесенные через паровую фазу, распадаются.
 • Напротив, если соединение АВ образуется по экзотермической реакции, то исходное вещество А располагается в холодном конце трубки, а продукт транспорта – в горячем конце. Константа равновесия реакции, проходящей в объеме трубки, зависит от температуры, и следовательно концентрации температурах Т 1 и Т 2 различны. АВ при
• Напротив, если соединение АВ образуется по экзотермической реакции, то исходное вещество А располагается в холодном конце трубки, а продукт транспорта – в горячем конце. Константа равновесия реакции, проходящей в объеме трубки, зависит от температуры, и следовательно концентрации температурах Т 1 и Т 2 различны. АВ при
 • Это приводит к градиенту концентрации АВ, который определяет движущую силу диффузионного массопереноса в паровой фазе. Эффективный массоперенос удается получить, когда равновесие транспортной реакции несильно смещено в ту или другую стороны.
• Это приводит к градиенту концентрации АВ, который определяет движущую силу диффузионного массопереноса в паровой фазе. Эффективный массоперенос удается получить, когда равновесие транспортной реакции несильно смещено в ту или другую стороны.
 • Рассмотрим, например, эндотермическую реакцию окисления платины с образованием при >1200°С газообразного оксида • Pt (тв. ) + 02 Рt. О 2 (газ) • Оксид диффундирует в зону более низкой температуры и там металлическую платину. разлагается, давая
• Рассмотрим, например, эндотермическую реакцию окисления платины с образованием при >1200°С газообразного оксида • Pt (тв. ) + 02 Рt. О 2 (газ) • Оксид диффундирует в зону более низкой температуры и там металлическую платину. разлагается, давая
 • Последствия этого можно всегда наблюдать в высокотемпературных печах с нагревателями из платины и ее сплавов: на менее нагретых, чем сам нагреватель, кристаллики стенках металлической печи видны платины, образовавшиеся здесь в результате транспортной реакции.
• Последствия этого можно всегда наблюдать в высокотемпературных печах с нагревателями из платины и ее сплавов: на менее нагретых, чем сам нагреватель, кристаллики стенках металлической печи видны платины, образовавшиеся здесь в результате транспортной реакции.
 • Предложенный Ван-Аркелем способ очистки некоторых металлов основан на экзотермических реакциях с парами иода, при которых образуются газообразные иодиды, например: • Сг+ I 2 Сг I 2 (газ) • Прямая реакция экзотермична, поэтому металлический хром переносится и осаждается в более нагретой зоне.
• Предложенный Ван-Аркелем способ очистки некоторых металлов основан на экзотермических реакциях с парами иода, при которых образуются газообразные иодиды, например: • Сг+ I 2 Сг I 2 (газ) • Прямая реакция экзотермична, поэтому металлический хром переносится и осаждается в более нагретой зоне.
 • Таким образом, можно подвергать очистке от примесей Ti, Hf, V, Nb, Си, Та, Fe и Th ИЛИ извлекать эти металлы из их карбидов, нитридов и оксидов.
• Таким образом, можно подвергать очистке от примесей Ti, Hf, V, Nb, Си, Та, Fe и Th ИЛИ извлекать эти металлы из их карбидов, нитридов и оксидов.
 • Элегантная разновидность иодидного метода, позволяющая разделить смесь двух веществ, транспортируя их в противоположных направлениях, основана на одновременном прохождении двух реакций с разным знаком теплового эффекта. Например, таким образом можно разделить WO 2 и W, используя в качестве переносчиков пары I 2 и Н 2 О. При этом происходят реакции:
• Элегантная разновидность иодидного метода, позволяющая разделить смесь двух веществ, транспортируя их в противоположных направлениях, основана на одновременном прохождении двух реакций с разным знаком теплового эффекта. Например, таким образом можно разделить WO 2 и W, используя в качестве переносчиков пары I 2 и Н 2 О. При этом происходят реакции:
 В итоге вольфрам осаждается в зоне 10000 С, а WO 2 - 8000 С. Применяя HCl в качестве переносчика, можно разделить Cu и Cu 2 O:
В итоге вольфрам осаждается в зоне 10000 С, а WO 2 - 8000 С. Применяя HCl в качестве переносчика, можно разделить Cu и Cu 2 O:
 • Поскольку Cu. Cl образуется из Cu 2 O по экзотермической реакции, а из Cu – по эндотермической, то в зоне более высоких температур происходит осаждение Cu 2 O. А в зоне более низких температур – осаждение меди. • Рассмотренные реакции являются примером наиболее простых транспортных процессов. В которых исходное вещество и продукт идентичны.
• Поскольку Cu. Cl образуется из Cu 2 O по экзотермической реакции, а из Cu – по эндотермической, то в зоне более высоких температур происходит осаждение Cu 2 O. А в зоне более низких температур – осаждение меди. • Рассмотренные реакции являются примером наиболее простых транспортных процессов. В которых исходное вещество и продукт идентичны.
 • В тоже время транспортные реакции могут играть важную бинарных, роль тройных при и синтезе даже многих четверных соединений. Взаимодействие может проходить в соответствии, например со следующей схемой: • при Т 2: А(тв) + В(газ) • при Т 1: АВ (газ) + С(тв) АВ (газ) АС(тв) + В(газ) • суммарный процесс: А(тв)+С(тв) АС (тв)
• В тоже время транспортные реакции могут играть важную бинарных, роль тройных при и синтезе даже многих четверных соединений. Взаимодействие может проходить в соответствии, например со следующей схемой: • при Т 2: А(тв) + В(газ) • при Т 1: АВ (газ) + С(тв) АВ (газ) АС(тв) + В(газ) • суммарный процесс: А(тв)+С(тв) АС (тв)
 • Рассмотрим несколько примеров
• Рассмотрим несколько примеров

 • В итоге в более холодной (7000 С) части реактора вырастают большие бесцветные кристаллы Al 2 S 3
• В итоге в более холодной (7000 С) части реактора вырастают большие бесцветные кристаллы Al 2 S 3
 • Приведенные примеры иллюстрируют важную роль газовой фазы как среды, в которой осуществляется массоперенос, и ее влияние реакции на скорость возрастает реакции. по Скорость сравнению с твердофазным взаимодействием потому, что подвижность молекул в газах гораздо выше, чем в твердых телах.
• Приведенные примеры иллюстрируют важную роль газовой фазы как среды, в которой осуществляется массоперенос, и ее влияние реакции на скорость возрастает реакции. по Скорость сравнению с твердофазным взаимодействием потому, что подвижность молекул в газах гораздо выше, чем в твердых телах.


