1-ATOM.ppt
- Количество слайдов: 39

Химия - теоретические основы Анатолий Анатольевич БАРУНИН 1. А. П. КИСЕЛЕВ, А. А. КРАШЕНИННИКОВ Основы общей химии Часть 1 Строение вещества Часть 2 Термодин. и кинетика химического процесса Часть 3 Электрохим. и коррозионные процессы 2. А. И. Горбунов, А. А. Гуров, Г. Г. Филиппов, В. Н. Шаповал Теоретические основы общей химии 3. Физико-химические основы общей химии. Уч. пос. под ред. Б. Т. Плаченова 4. В. В. Фролов 5. Н. В. Коровин
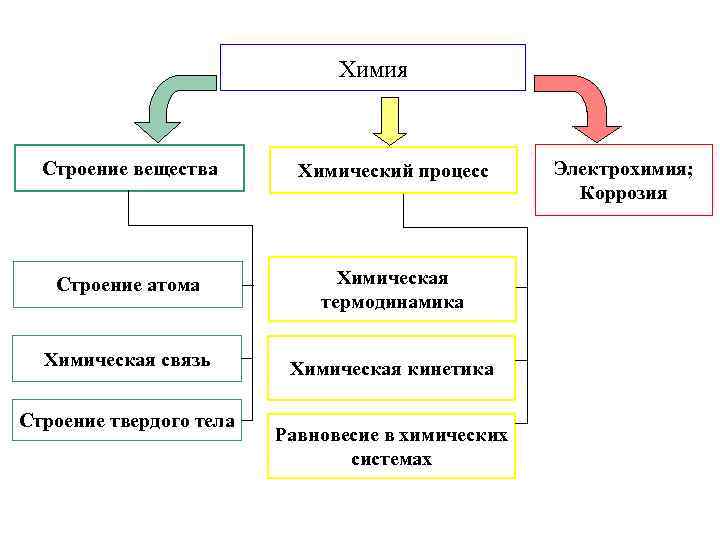
Химия Строение вещества Химический процесс Строение атома Химическая термодинамика Химическая связь Химическая кинетика Строение твердого тела Равновесие в химических системах Электрохимия; Коррозия

Строение атома 3 этапа развития учения о строении атома 1 – Натурфилософские представления об атомном строении материи. V в. до н. э. Демокрит – понятие «атом» . Эпикур, Аристотель 2 – Химическая гипотеза об атоме, как наименьшей частице химического элемента. Атомы отличаются массой. Парацельс, Бойль, Берцелиус 3 – Физические модели. Описывают сложное строение атома Исследование электролиза Открытие каналовых (1886) и катодных лучей (1896) Открытие и измерение свойств электрона (1897) Джозеф Джон Томсон Открытие радиоактивности (1896) Анри Беккерель Атомы содержат разноименно заряженные частицы

1. Строение атома. Физические модели Эрнест Резерфорд - Планетарная модель атома Атом - сложная частица, состоящая из положительно заряженного ядра (~10 -15 м) и отрицательно заряженных электронов вращающихся вокруг ядра на расстоянии ~10 -10 м • Энергия электрона • Координаты Нильс Бор – теория (модель) строения атома водорода (постулаты) Эрвин Шредингер - квантовая (волновая) механика Теория, устанавливающая способ описания и законы движения микрочастиц

1. 1 Корпускулярно-волновой дуализм свойств материи Частица: m - масса p = mv - импульс E= mv 2/2 - кинетическая энергия Волна: - длина волны n- частота Т - период 1. Электромагнитное излучение Макс Планк 1900 г. E = h n квант энергии h = 6, 6262 10 -34 Дж с - постоянная Планка n- частота излучения [с– 1] Альберт Эйнштейн 1905 г. E = m c 2 квант энергии– частица - фотон m - масса фотона c = 2, 9979 108 м/сек - скорость света hn = mc 2 p = m c - импульс фотона

2. Частицы (корпускулы) Частица: m - масса, v – скорость Луи де Бройль 1924 г. электрон Кинетическая энергия Длина волны - m = 9, 11 10 -31 кг Ek = 100 э. В (1 э. В=1, 602 10 -19 Дж) , = 1. 2 Å (1 Å =10 -10 м) Дифракционная решетка = 1. 2 Å
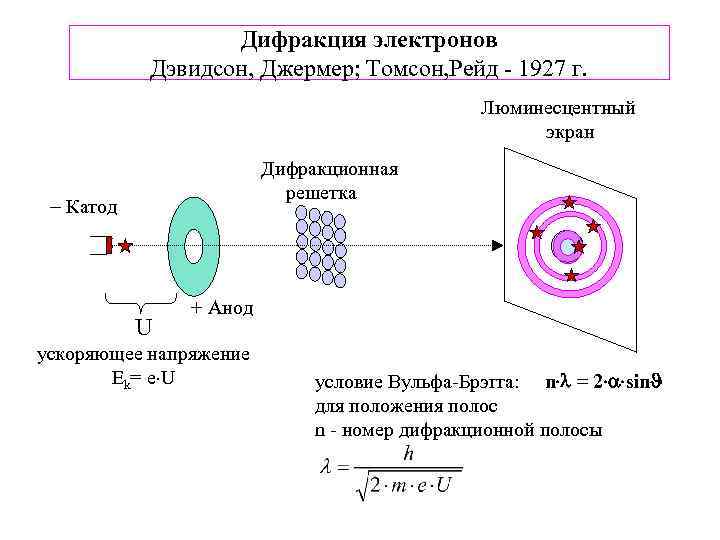
Дифракция электронов Дэвидсон, Джермер; Томсон, Рейд - 1927 г. Люминесцентный экран Дифракционная решетка Катод U + Анод ускоряющее напряжение Ek= e U условие Вульфа-Брэгга: n = 2 sin для положения полос n - номер дифракционной полосы

Принцип неопределенности Вернер Гейзенберг 1927 г. Точное определение координат частицы и ее импульса заменяется в квантовой(волновой) механике определением вероятности нахождения частицы в какой-то области пространства * Р - вероятность 0 Р 1
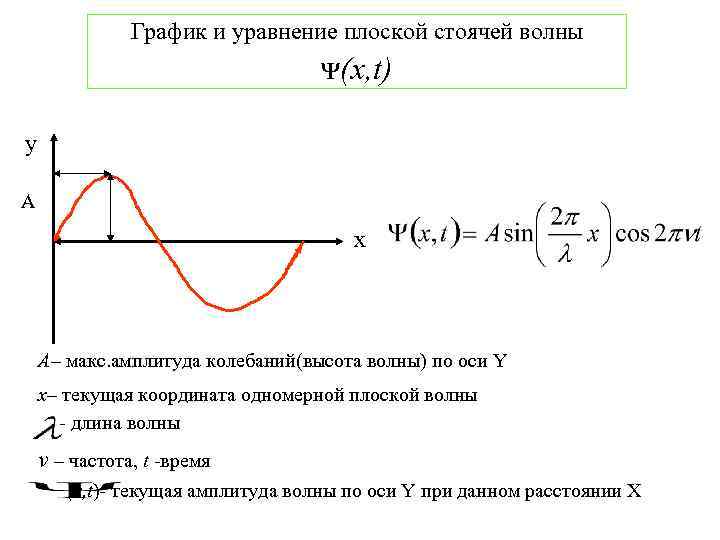
График и уравнение плоской стоячей волны ᴪ(x, t) y A x А– макс. амплитуда колебаний(высота волны) по оси Y х– текущая координата одномерной плоской волны - длина волны ν – частота, t -время (x, t)- текущая амплитуда волны по оси Y при данном расстоянии X

1. 2 Уравнение Шрёдингера 1. Уравнение отображающее волновой характер движения электрона в пространстве с координатами (x, y, z) (x, y, z, t) - волновая функция - пси функция (стоячая волна) - Текущая амплитуда, функция координат (x, y, z) и времени (t) (x, y, z) – (стоячая волна)стационарный процесс – Текущая амплитуда, функция координат (x, y, z); cos 2πνt=1 Дифф. уравнение 2 -го порядка стоячей волны для стационарного процесса - длина волны 2 - оператор Лапласа(набла два)

2. Уравнение должно содержать в себе характеристики электрона как частицы m, Ek Длина волны де Бройля Волновое уравнение движения свободного электрона E = Ek + V E - полная энергия Эрвин Шрeдингер: 1926 г. V- потенциальная энергия Волновое уравнение микрочастицы в потенциальном поле

Физический смысл волновой функции (x, y, z) - пси функция - волновая функция Макс Борн, 1926 г. • волновая функция(амплитудная) и физического смысла не имеет • 2(x, y, z) - квадрат волновой функции пропорционален вероятности (d. P) нахождения частицы в элементарном объеме (d. V) d. P = 2(x, y, z) d. V вероятность нахождения частицы в объеме V плотность вероятности (электронная плотность) Принцип нормирования PV = ∫v A 2 |Ψ(x, y, z) |2 d. V = 1, А –нормирующий множитель

1. 3 Электрон в одномерном потенциальном ящике(яме) Потенциальная яма (ящик) - область пространства, вне которой потенциальная энергия электрона обращается в бесконечность, т. е электрон не может выйти за границы ящика (связанное состояние)V 0 a модель для электрона в атоме • Одномерный потенциальный ящик Граничные условия: внутри ящика: на границах ящика: V=0 V= (x) (0)=0; (а)=0 Решение – нахождение собственных функций(конечны, однозначны, непрерывны) и расчет соответствующих этим функциям значений собственных энергий x

• Нахождение волновой функции Общее решение Граничные условия A 0 n=1, 2, 3…. . Из условия нормировки Набор волн. функций Ψ(х) a - параметр потенциального ящика n = 1, 2, 3…- квантовое число

• Нахождение энергии электрона Набору ᴪ(x) соответствует набор Е, n = 1, 2, 3…- квантовое
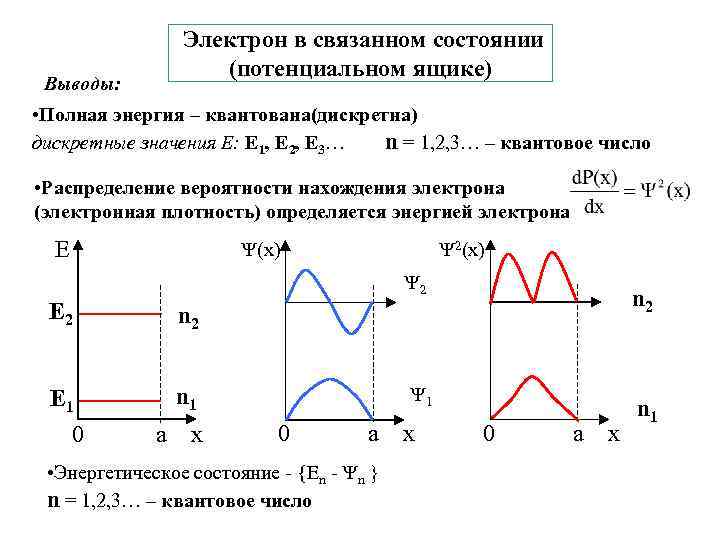
Электрон в связанном состоянии (потенциальном ящике) Выводы: • Полная энергия – квантована(дискретна) дискретные значения Е: E 1, E 2, E 3… n = 1, 2, 3… – квантовое число • Распределение вероятности нахождения электрона (электронная плотность) определяется энергией электрона E 2(x) 2 E 2 n 2 E 1 0 n 1 n 2 а x 1 0 а • Энергетическое состояние - {En - n } n = 1, 2, 3… – квантовое число x 0 а x n 1

Электрон в трехмерном потенциальном ящике Решение: • Набор волновых функций: a, b, c – параметры ящика nx, ny, nz – квантовые числа • Набор энергий: Выводы: 1. Энергия электрона квантована. 2. Энергетическое состояние определяется набором из трех квантовых чисел nx. ny, nz.

Вырожденные энергетические состояния одно значение энергии – несколько наборов квантовых чисел несколько волновых функций а=b=c Е, Е 5 = 12 Е 4 = 11 [2, 2, 2] [3, 1, 1] [1, 3, 1] [1, 1, 3] Е 3 = 9 [2, 2, 1] [1, 2, 2] [2, 1, 2] Е 2 = 6 [2, 1, 1] [1, 2, 1] [1, 1, 2] Е 1 = 3 [1, 1, 1] трехкратно вырожденные состояния
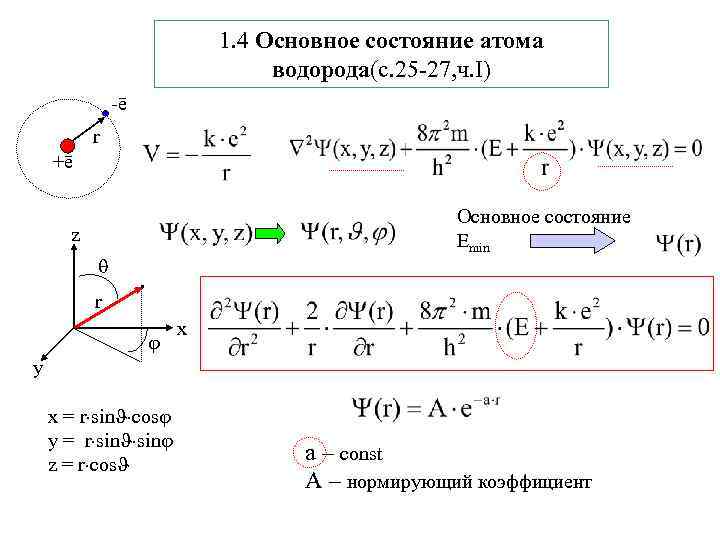
1. 4 Основное состояние атома водорода(с. 25 -27, ч. I) -ē r +ē Основное состояние Еmin z r x y x = r sin cos y = r sin z = r cos а – const А – нормирующий коэффициент

Решение уравнения Шредингера для основного состояния атома водорода подставляем в уравнение Шредингера
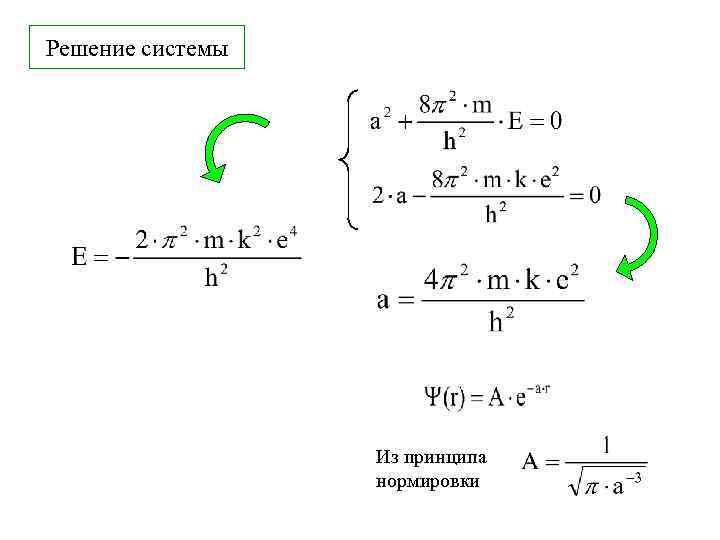
Решение системы Из принципа нормировки
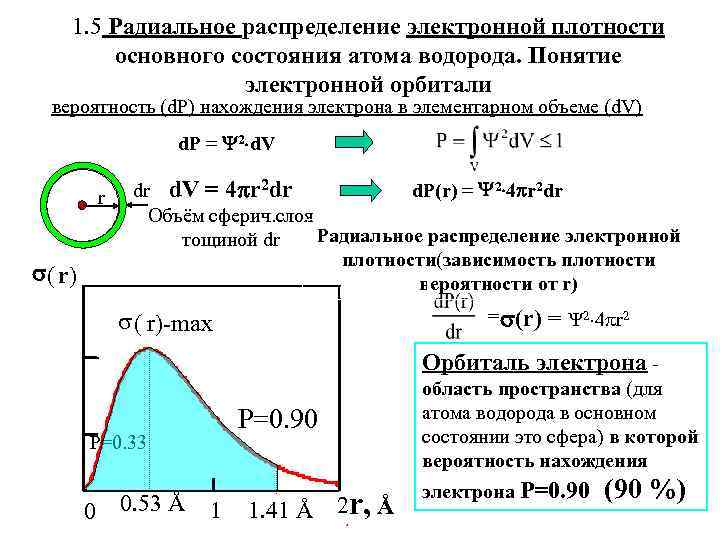
1. 5 Радиальное распределение электронной плотности основного состояния атома водорода. Понятие электронной орбитали вероятность (d. P) нахождения электрона в элементарном объеме (d. V) d. P = 2 d. V r ( r) d. P(r) = 2 4 r 2 dr dr d. V = 4 r 2 dr Объём сферич. слоя Радиальное распределение электронной тощиной dr плотности(зависимость плотности вероятности от r) = (r) ( r)-max = 2 4 r 2 Орбиталь электрона - P=0. 90 P=0. 33 0 0. 53 Å 1 1. 41 Å 2 r, Å область пространства (для атома водорода в основном состоянии это сфера) в которой вероятность нахождения электрона P=0. 90 (90 %)
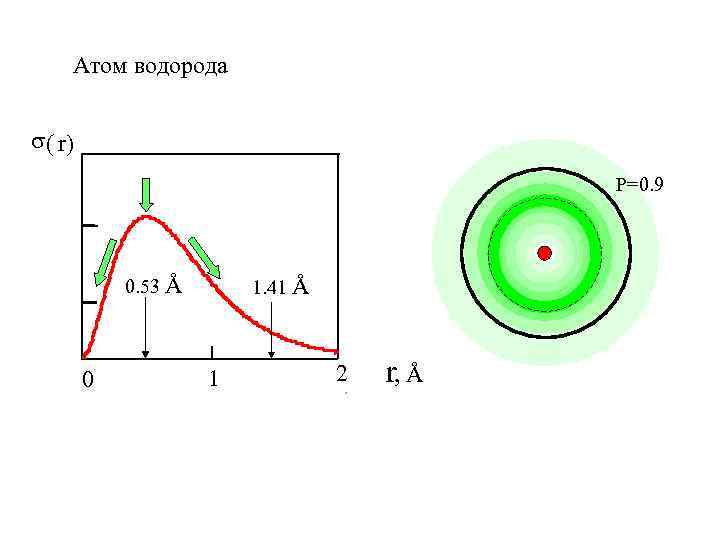
Атом водорода ( r) Р=0. 9 0. 53 Å 0 1. 41 Å 1 2 r, Å

1. 6 Возбужденные состояния атома водорода Общий вид волновой функции- (r, , ) = R(r) Y( , )-[метод разделения переменных] R(r)n, l -функция радиального распределения электронной плотности в явном виде Y( , )l, m-функция углового распределения электронной плотности в явном виде n, l, m - целочисленные параметры волновых функций в явном виде - квантовые числа Определяют набор волн. функций и соответствующий им набор энергетических состояний{En- n, l, m } Квантовые числа: главное – n = 1, 2, 3, 4… орбитальное – l = 0, 1, 2, 3. . . (n -1) магнитное – m = -l, (-l+1), . . . , 0, . . . , (+l– 1), +l спиновое – ms =± 1/2 (1933 г. ) Поль Дирак
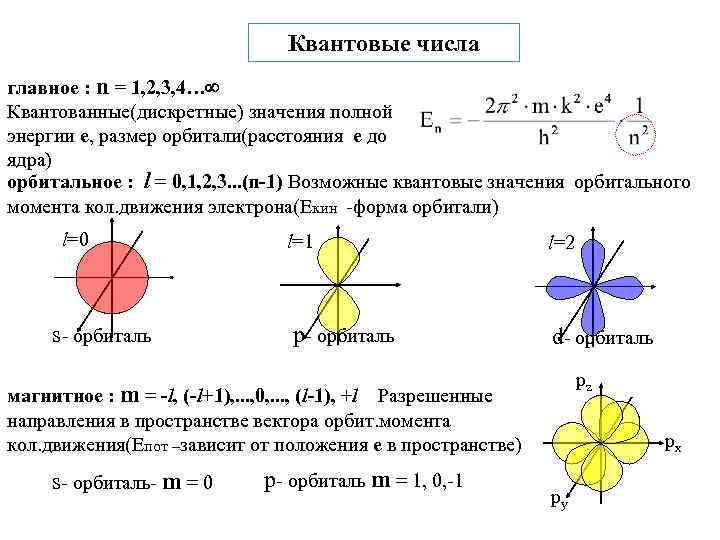
Квантовые числа главное : n = 1, 2, 3, 4… Квантованные(дискретные) значения полной энергии е, размер орбитали(расстояния е до ядра) орбитальное : l = 0, 1, 2, 3. . . (n-1) Возможные квантовые значения орбитального момента кол. движения электрона(Екин -форма орбитали) l=0 s- орбиталь l=1 р- орбиталь l=2 d- орбиталь pz магнитное : m = -l, (-l+1), . . . , 0, . . . , (l-1), +l Разрешенные направления в пространстве вектора орбит. момента кол. движения(Епот –зависит от положения е в пространстве) s- орбиталь- m = 0 р- орбиталь m = 1, 0, -1 px py

Электронные орбитали атома водорода n l = 0, 1…(n-1) 1 2 3 4 m = -l, … 0, …+l Число орбиталей Энергия 0 – 1 s 0 – 2 s 1 – 2 p 0 – 3 s 1 – 3 p 2 – 3 d 0 0 +1, 0, -1 1 E 1 1 3 E 2 0 +1, 0, -1 +2, +1, 0, -1, -2 0 – 4 s 1 – 4 p 2 – 4 d 3 – 4 f 0 +1, 0, -1 +2, +1, 0, -1, -2 +3, +2, +1, 0, -1, -2, -3 1 3 5 7 E 3 E 4
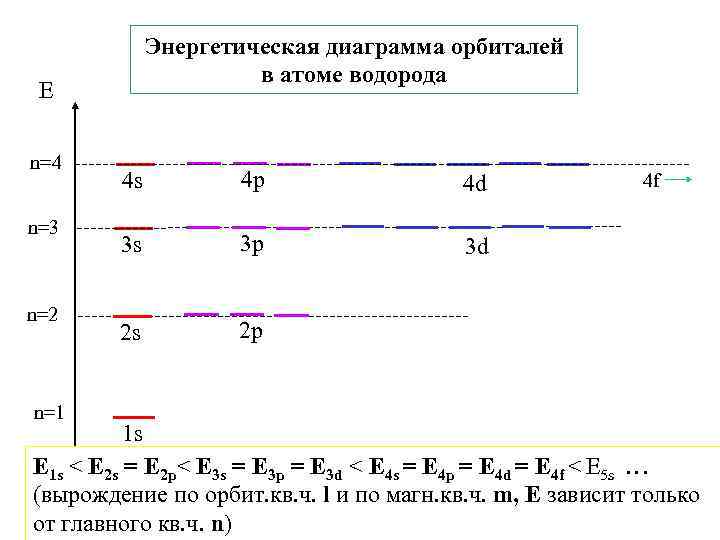
Энергетическая диаграмма орбиталей в атоме водорода Е n=4 n=3 n=2 n=1 4 s 4 p 4 d 3 s 3 p 3 d 2 s 2 p 4 f 1 s E 1 s < E 2 s = E 2 p< E 3 s = E 3 p = E 3 d < E 4 s = E 4 p = E 4 d = E 4 f < E 5 s … (вырождение по орбит. кв. ч. l и по магн. кв. ч. m, Е зависит только от главного кв. ч. n)
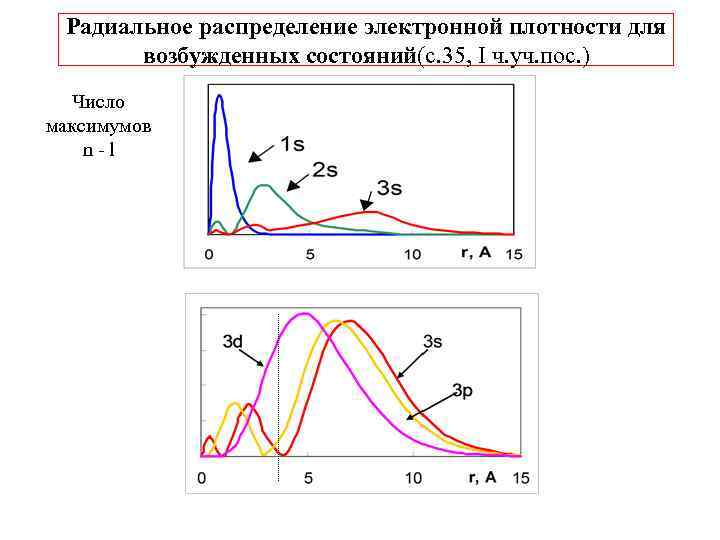
Радиальное распределение электронной плотности для возбужденных состояний(c. 35, I ч. уч. пос. ) Число максимумов n-l

1. 7 Многоэлектронный атом (одноэлектронное приближение) Zэ +Z -(Z-1) ē Zэ = Z - n, l Z – заряд ядра Zэ - эффективный заряд ядра n, l - константа экранирования
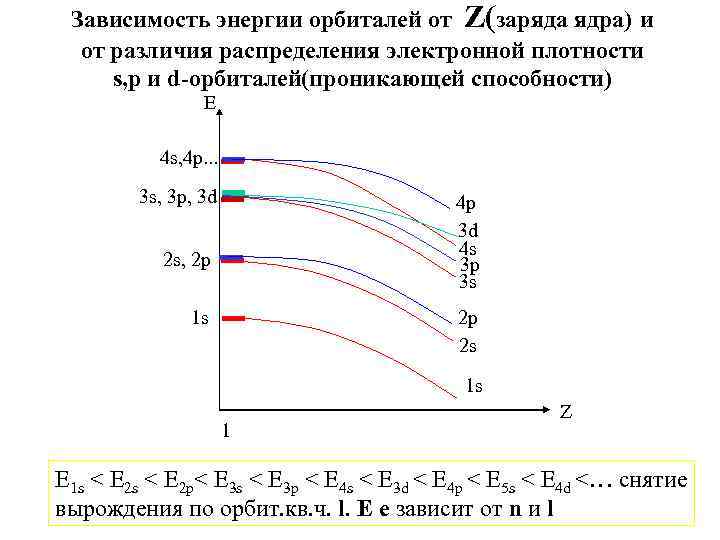
Зависимость энергии орбиталей от Z(заряда ядра) и от различия распределения электронной плотности s, p и d-орбиталей(проникающей способности) Е 4 s, 4 p. . . 3 s, 3 p, 3 d 4 p 3 d 4 s 3 p 3 s 2 s, 2 p 2 p 2 s 1 s 1 s 1 Z E 1 s < E 2 p< E 3 s < E 3 p < E 4 s < E 3 d < E 4 p < E 5 s < E 4 d <… снятие вырождения по орбит. кв. ч. l. E e зaвисит от n и l
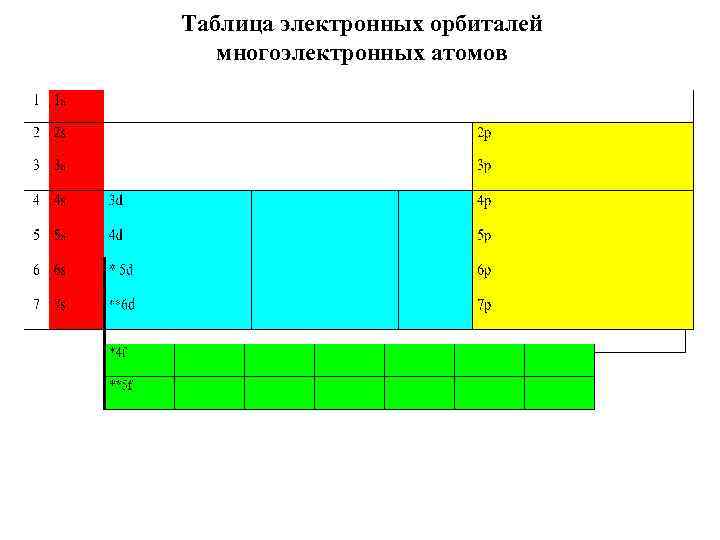
Таблица электронных орбиталей многоэлектронных атомов
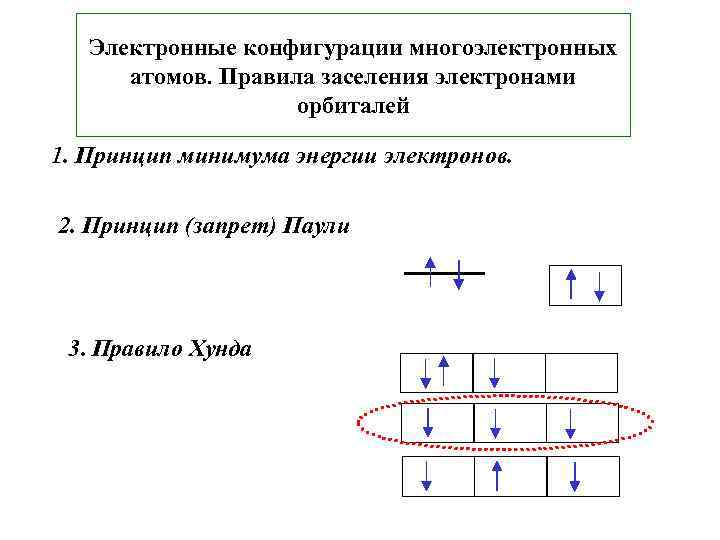
Электронные конфигурации многоэлектронных атомов. Правила заселения электронами орбиталей 1. Принцип минимума энергии электронов. 2. Принцип (запрет) Паули 3. Правило Хунда
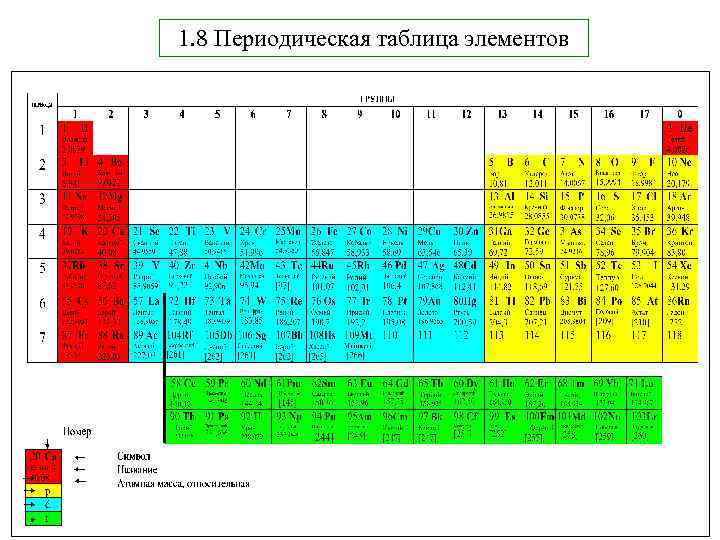
1. 8 Периодическая таблица элементов
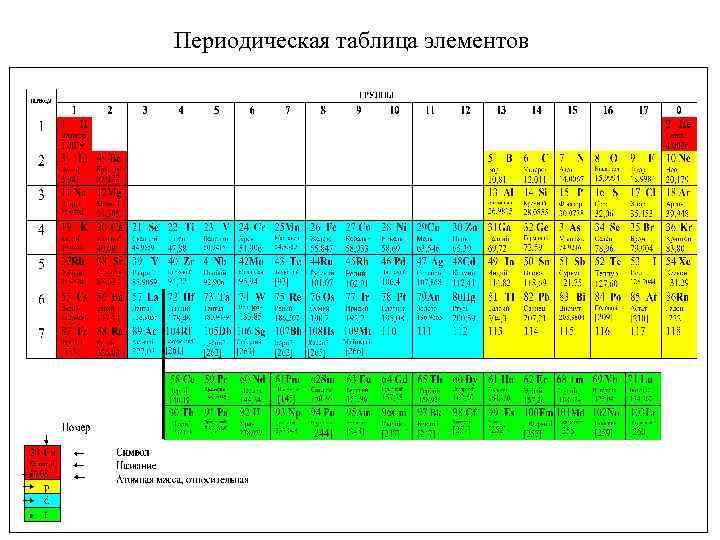
Периодическая таблица элементов Периодическое повторение электронных структур атомов – периодическое повторение свойств элементов и их химических соединений Валентные электроны – электроны, принимающие участие в образовании химической связи. ns 2 np 6 - благородные (инертные) газы (0 группа) • Типичные элементы: s- и p-элементы (главные группы) s- элементы (1 -2 группы) -nsx - x 2 p-элементы (13 -17 группы) - ns 2 npy y<6 • Переходные элементы (d-металлы) - ns 2(n-1)dy - (3 -12 группы)
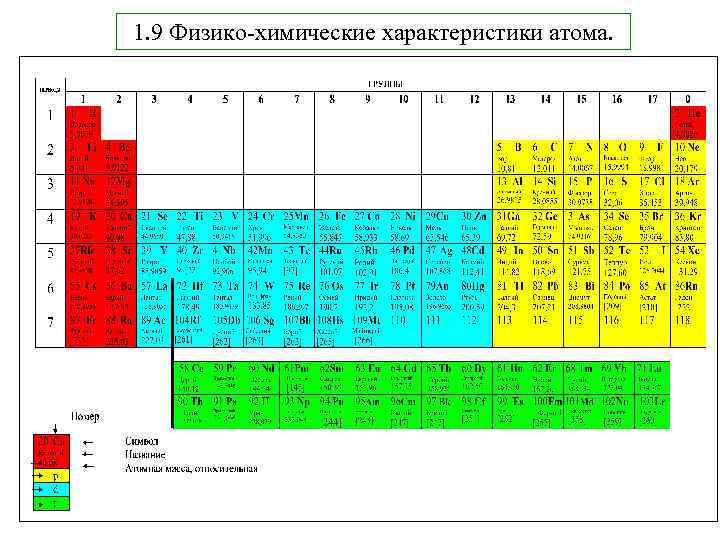
1. 9 Физико-химические характеристики атома. • Радиус атома и иона K Li Rb Na Ne Ar Kr
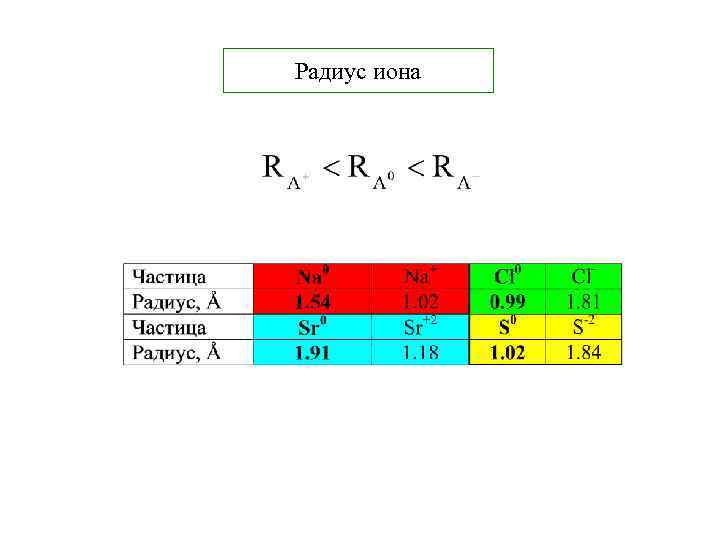
Радиус иона
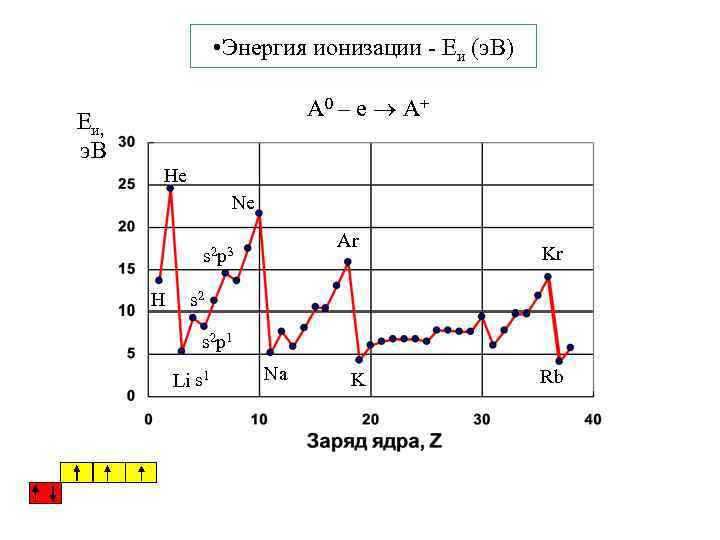
• Энергия ионизации - Eи (э. В) А 0 – е А+ Eи, э. В He Ne Ar s 2 p 3 Н Kr s 2 p 1 Li s 1 Na K Rb
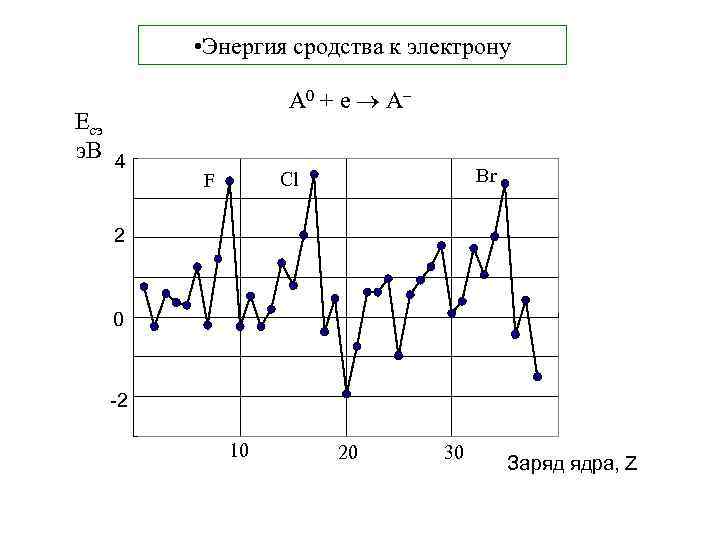
• Энергия сродства к электрону Eсэ э. В 4 A 0 + e A– Br Cl F 2 0 -2 10 20 30 Заряд ядра, Z
• Электроотрицательность • по Малликену • по Полингу (э. В) у. е. F = 4. 0
1-ATOM.ppt