 Химия - теоретические основы 1. А. П. КИСЕЛЕВ, А. А. КРАШЕНИННИКОВ Основы общей химии Часть 1. Строение вещества Часть 2. Термодинамика и кинетика химического процесса Часть 3. Электрохимические и коррозионные процессы 2. А. И. Горбунов, А. А. Гуров, Г. Г. Филиппов, В. Н. Шаповал Теоретические основы общей химии 3. Коровин Н. В. ; Фролов В. В. 4. Физико-химические основы общей химии под редакцией Б. Т. Плаченова
Химия - теоретические основы 1. А. П. КИСЕЛЕВ, А. А. КРАШЕНИННИКОВ Основы общей химии Часть 1. Строение вещества Часть 2. Термодинамика и кинетика химического процесса Часть 3. Электрохимические и коррозионные процессы 2. А. И. Горбунов, А. А. Гуров, Г. Г. Филиппов, В. Н. Шаповал Теоретические основы общей химии 3. Коровин Н. В. ; Фролов В. В. 4. Физико-химические основы общей химии под редакцией Б. Т. Плаченова
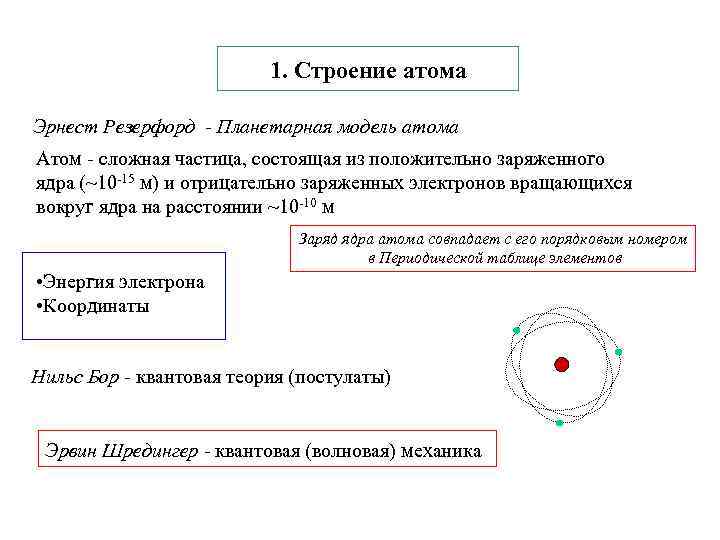 1. Строение атома Эрнест Резерфорд - Планетарная модель атома Атом - сложная частица, состоящая из положительно заряженного ядра (~10 -15 м) и отрицательно заряженных электронов вращающихся вокруг ядра на расстоянии ~10 -10 м Заряд ядра атома совпадает с его порядковым номером в Периодической таблице элементов • Энергия электрона • Координаты Нильс Бор - квантовая теория (постулаты) Эрвин Шредингер - квантовая (волновая) механика
1. Строение атома Эрнест Резерфорд - Планетарная модель атома Атом - сложная частица, состоящая из положительно заряженного ядра (~10 -15 м) и отрицательно заряженных электронов вращающихся вокруг ядра на расстоянии ~10 -10 м Заряд ядра атома совпадает с его порядковым номером в Периодической таблице элементов • Энергия электрона • Координаты Нильс Бор - квантовая теория (постулаты) Эрвин Шредингер - квантовая (волновая) механика
 1. 1 Корпускулярно-волновой дуализм свойств материи Частица: m - масса p = mv - импульс E= mv 2/2 - кинетическая энергия Волна: - длина волны n- частота Т - период 1. Электромагнитное излучение Макс Планк E = h n квант энергии h = 6, 6262 10 -34 Дж сек - постоянная Планка n- частота излучения [с– 1] Альберт Эйнштейн E = m c 2 квант энергии– частица - фотон m - масса фотона c = 2, 9979 108 м/сек - скорость света hn = mc 2 p = m c - импульс фотона
1. 1 Корпускулярно-волновой дуализм свойств материи Частица: m - масса p = mv - импульс E= mv 2/2 - кинетическая энергия Волна: - длина волны n- частота Т - период 1. Электромагнитное излучение Макс Планк E = h n квант энергии h = 6, 6262 10 -34 Дж сек - постоянная Планка n- частота излучения [с– 1] Альберт Эйнштейн E = m c 2 квант энергии– частица - фотон m - масса фотона c = 2, 9979 108 м/сек - скорость света hn = mc 2 p = m c - импульс фотона
 2. Частицы (корпускулы) Частица: m - масса, v – скорость Луи де Бройль электрон Кинетическая энергия Длина волны - m = 9, 11 10 -31 кг Ek = 100 э. В (1 э. В=1, 602 10 -19 Дж) , = 1. 2 Å (1 Å =10 -10 м) Дифракционная решетка = 1. 2 Å
2. Частицы (корпускулы) Частица: m - масса, v – скорость Луи де Бройль электрон Кинетическая энергия Длина волны - m = 9, 11 10 -31 кг Ek = 100 э. В (1 э. В=1, 602 10 -19 Дж) , = 1. 2 Å (1 Å =10 -10 м) Дифракционная решетка = 1. 2 Å
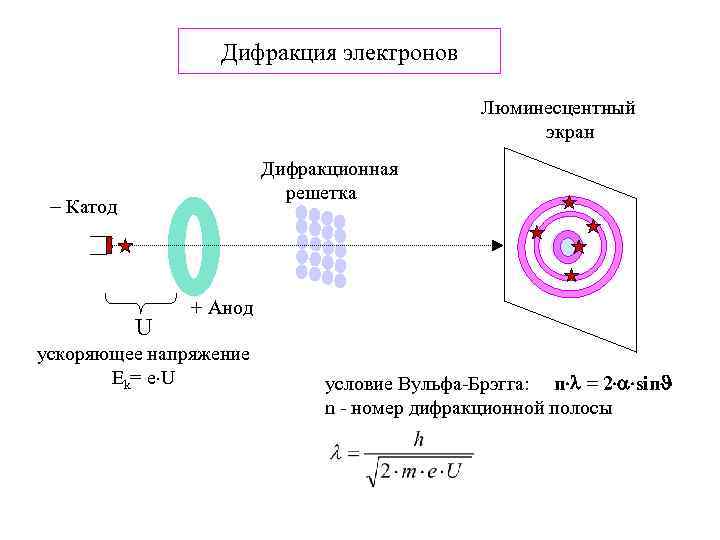 Дифракция электронов Люминесцентный экран Дифракционная решетка Катод U + Анод ускоряющее напряжение Ek= e U условие Вульфа-Брэгга: n = 2 sin n - номер дифракционной полосы
Дифракция электронов Люминесцентный экран Дифракционная решетка Катод U + Анод ускоряющее напряжение Ek= e U условие Вульфа-Брэгга: n = 2 sin n - номер дифракционной полосы
 Принцип неопределенности Вернер Гейзенберг Точное определение координат электрона заменяется определением вероятности нахождения электрона в какой-то области пространства * Р - вероятность 0 Р 1
Принцип неопределенности Вернер Гейзенберг Точное определение координат электрона заменяется определением вероятности нахождения электрона в какой-то области пространства * Р - вероятность 0 Р 1
 1. 2 Уравнение Шрёдингера 1. Уравнение должно отражать волновой характер движения электрона (x, y, z, t) - волновая функция - пси функция - амплитуда функция координат и времени (x, y, z) - стационарный процесс - стоячая волна; Уравнение стоячей волны - длина волны 2 - оператор Лапласа
1. 2 Уравнение Шрёдингера 1. Уравнение должно отражать волновой характер движения электрона (x, y, z, t) - волновая функция - пси функция - амплитуда функция координат и времени (x, y, z) - стационарный процесс - стоячая волна; Уравнение стоячей волны - длина волны 2 - оператор Лапласа
 2. Уравнение должно содержать в себе характеристики электрона как частицы m, Ek Длина волны де Бройля Волновое уравнение свободного электрона E = Ek + V E Эрвин Шредингер - полная энергия V- потенциальная энергия волновое уравнение частицы в потенциальном поле
2. Уравнение должно содержать в себе характеристики электрона как частицы m, Ek Длина волны де Бройля Волновое уравнение свободного электрона E = Ek + V E Эрвин Шредингер - полная энергия V- потенциальная энергия волновое уравнение частицы в потенциальном поле
 Физический смысл волновой функции (x, y, z) - пси функция - волновая функция Макс Борн • волновая функция физического смысла не имеет • 2(x, y, z) - квадрат волновой функции пропорционален вероятности (d. P) нахождения частицы в элементарном объеме (d. V) плотность вероятности (электронная плотность) • вероятность нахождения частицы в объеме V d. P = 2(x, y, z) d. V принцип нормирования А – нормирующий множитель
Физический смысл волновой функции (x, y, z) - пси функция - волновая функция Макс Борн • волновая функция физического смысла не имеет • 2(x, y, z) - квадрат волновой функции пропорционален вероятности (d. P) нахождения частицы в элементарном объеме (d. V) плотность вероятности (электронная плотность) • вероятность нахождения частицы в объеме V d. P = 2(x, y, z) d. V принцип нормирования А – нормирующий множитель
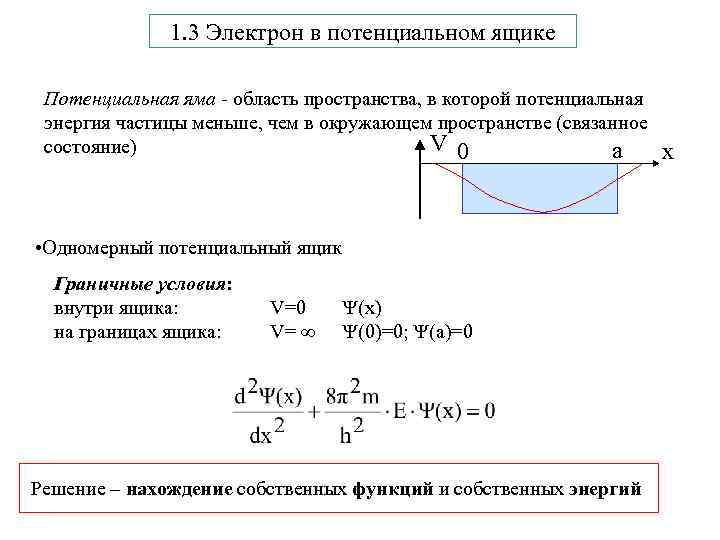 1. 3 Электрон в потенциальном ящике Потенциальная яма - область пространства, в которой потенциальная энергия частицы меньше, чем в окружающем пространстве (связанное V 0 состояние) a • Одномерный потенциальный ящик Граничные условия: внутри ящика: на границах ящика: V=0 V= (x) (0)=0; (а)=0 Решение – нахождение собственных функций и собственных энергий x
1. 3 Электрон в потенциальном ящике Потенциальная яма - область пространства, в которой потенциальная энергия частицы меньше, чем в окружающем пространстве (связанное V 0 состояние) a • Одномерный потенциальный ящик Граничные условия: внутри ящика: на границах ящика: V=0 V= (x) (0)=0; (а)=0 Решение – нахождение собственных функций и собственных энергий x
 • Нахождение волновой функции. Общее решение Граничные условия A 0 n=1, 2, 3…. . нормировка a - параметр потенциального ящика n = 1, 2, 3…- квантовое число
• Нахождение волновой функции. Общее решение Граничные условия A 0 n=1, 2, 3…. . нормировка a - параметр потенциального ящика n = 1, 2, 3…- квантовое число
 • Нахождение энергии электрона n = 1, 2, 3…- квантовое число
• Нахождение энергии электрона n = 1, 2, 3…- квантовое число
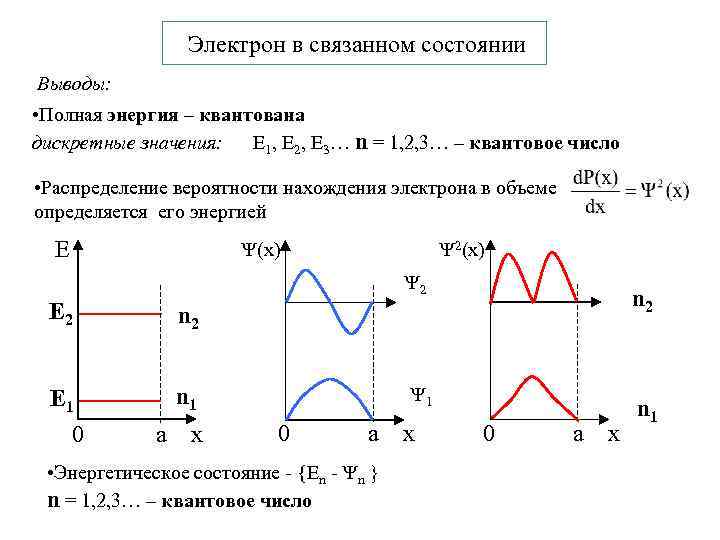 Электрон в связанном состоянии Выводы: • Полная энергия – квантована дискретные значения: E 1, E 2, E 3… n = 1, 2, 3… – квантовое число • Распределение вероятности нахождения электрона в объеме определяется его энергией E 2(x) 2 E 2 n 2 E 1 0 n 1 n 2 а x 1 0 а • Энергетическое состояние - {En - n } n = 1, 2, 3… – квантовое число x 0 а x n 1
Электрон в связанном состоянии Выводы: • Полная энергия – квантована дискретные значения: E 1, E 2, E 3… n = 1, 2, 3… – квантовое число • Распределение вероятности нахождения электрона в объеме определяется его энергией E 2(x) 2 E 2 n 2 E 1 0 n 1 n 2 а x 1 0 а • Энергетическое состояние - {En - n } n = 1, 2, 3… – квантовое число x 0 а x n 1
 Электрон в трехмерном потенциальном ящике. Решение: • Набор волновых функций: a, b, c – параметры ящика nx, ny, nz – квантовые числа • Набор энергий: Выводы: 1. Энергия электрона квантована. 2. Энергетическое состояние определяется набором из трех квантовых чисел.
Электрон в трехмерном потенциальном ящике. Решение: • Набор волновых функций: a, b, c – параметры ящика nx, ny, nz – квантовые числа • Набор энергий: Выводы: 1. Энергия электрона квантована. 2. Энергетическое состояние определяется набором из трех квантовых чисел.
 Вырожденные энергетические состояния одно значение энергии – несколько наборов квантовых чисел несколько волновых функций а=b=c Е, Е 5 = 12 Е 4 = 11 [2, 2, 2] [3, 1, 1] [1, 3, 1] [1, 1, 3] Е 3 = 9 [2, 2, 1] [1, 2, 2] [2, 1, 2] Е 2 = 6 [2, 1, 1] [1, 2, 1] [1, 1, 2] Е 1 = 3 [1, 1, 1] трехкратно вырожденные состояния
Вырожденные энергетические состояния одно значение энергии – несколько наборов квантовых чисел несколько волновых функций а=b=c Е, Е 5 = 12 Е 4 = 11 [2, 2, 2] [3, 1, 1] [1, 3, 1] [1, 1, 3] Е 3 = 9 [2, 2, 1] [1, 2, 2] [2, 1, 2] Е 2 = 6 [2, 1, 1] [1, 2, 1] [1, 1, 2] Е 1 = 3 [1, 1, 1] трехкратно вырожденные состояния
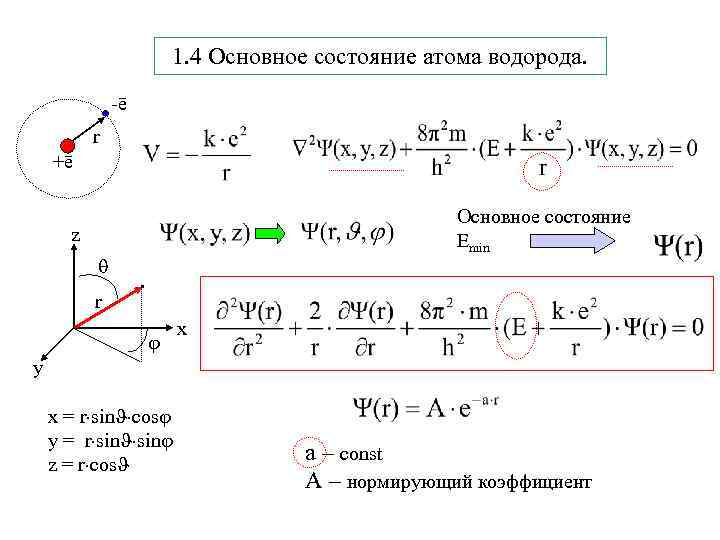 1. 4 Основное состояние атома водорода. -ē r +ē Основное состояние Еmin z r x y x = r sin cos y = r sin z = r cos а – const А – нормирующий коэффициент
1. 4 Основное состояние атома водорода. -ē r +ē Основное состояние Еmin z r x y x = r sin cos y = r sin z = r cos а – const А – нормирующий коэффициент
 Решение уравнения Шредингера для основного состояния атома водорода подставляем в уравнение Шредингера
Решение уравнения Шредингера для основного состояния атома водорода подставляем в уравнение Шредингера
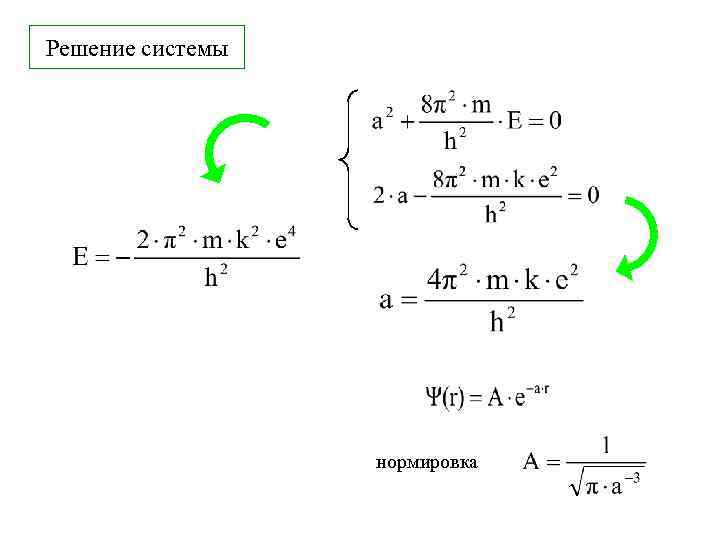 Решение системы нормировка
Решение системы нормировка
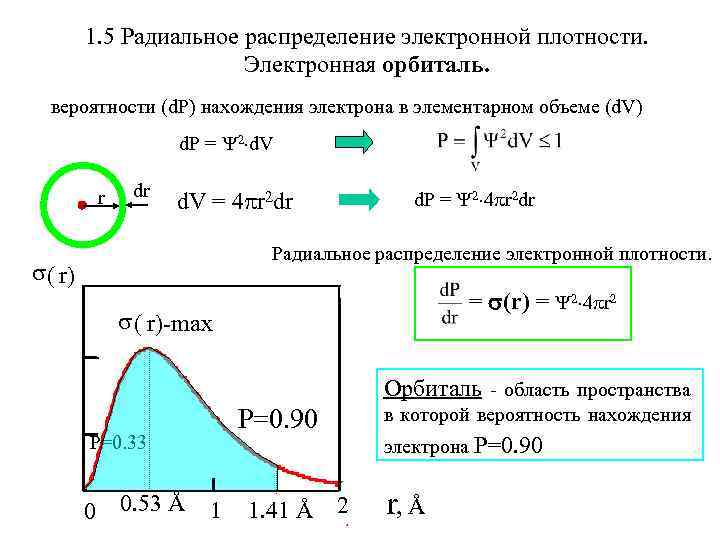 1. 5 Радиальное распределение электронной плотности. Электронная орбиталь. вероятности (d. P) нахождения электрона в элементарном объеме (d. V) d. P = 2 d. V r dr d. V = 4 r 2 dr d. P = 2 4 r 2 dr Радиальное распределение электронной плотности. ( r) = (r) = 2 4 r 2 ( r)-max Орбиталь - область пространства P=0. 90 P=0. 33 0 0. 53 Å 1 1. 41 Å 2 в которой вероятность нахождения электрона P=0. 90 r, Å
1. 5 Радиальное распределение электронной плотности. Электронная орбиталь. вероятности (d. P) нахождения электрона в элементарном объеме (d. V) d. P = 2 d. V r dr d. V = 4 r 2 dr d. P = 2 4 r 2 dr Радиальное распределение электронной плотности. ( r) = (r) = 2 4 r 2 ( r)-max Орбиталь - область пространства P=0. 90 P=0. 33 0 0. 53 Å 1 1. 41 Å 2 в которой вероятность нахождения электрона P=0. 90 r, Å
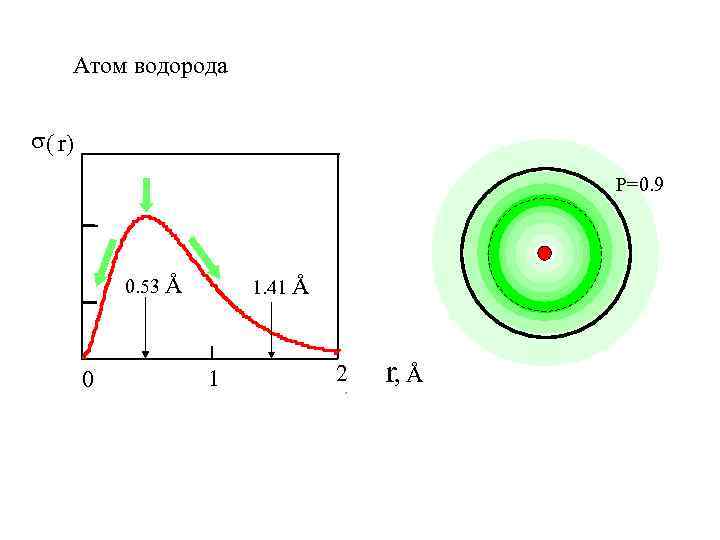 Атом водорода ( r) Р=0. 9 0. 53 Å 0 1. 41 Å 1 2 r, Å
Атом водорода ( r) Р=0. 9 0. 53 Å 0 1. 41 Å 1 2 r, Å
 1. 6 Возбужденные состояния атома водорода Волновая функции - (r, , ) = R(r) Y( , ) R(r)n, l - функция радиального распределения электронной плотности Y( , )l, m - функция углового распределения электронной плотности n, l, m - целочисленные параметры - квантовые числа Набор энергетических состояний{En- n, l, m } Квантовые числа: главное – n = 1, 2, 3, 4… орбитальное – l = 0, 1, 2, 3. . . (n -1) магнитное – m = -l, (-l+1), . . . , 0, . . . , (+l– 1), +l спиновое – ms =± 1/2
1. 6 Возбужденные состояния атома водорода Волновая функции - (r, , ) = R(r) Y( , ) R(r)n, l - функция радиального распределения электронной плотности Y( , )l, m - функция углового распределения электронной плотности n, l, m - целочисленные параметры - квантовые числа Набор энергетических состояний{En- n, l, m } Квантовые числа: главное – n = 1, 2, 3, 4… орбитальное – l = 0, 1, 2, 3. . . (n -1) магнитное – m = -l, (-l+1), . . . , 0, . . . , (+l– 1), +l спиновое – ms =± 1/2
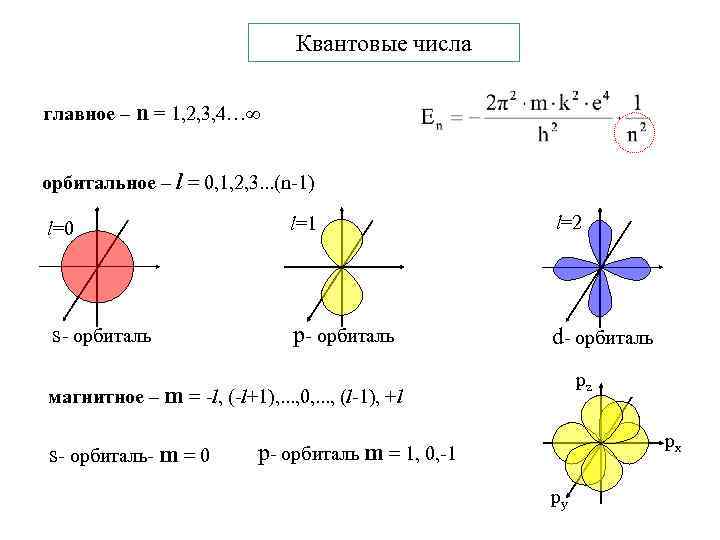 Квантовые числа главное – n = 1, 2, 3, 4… орбитальное – l = 0, 1, 2, 3. . . (n-1) l=0 l=1 l=2 s- орбиталь р- орбиталь d- орбиталь pz магнитное – m = -l, (-l+1), . . . , 0, . . . , (l-1), +l s- орбиталь- m = 0 px р- орбиталь m = 1, 0, -1 py
Квантовые числа главное – n = 1, 2, 3, 4… орбитальное – l = 0, 1, 2, 3. . . (n-1) l=0 l=1 l=2 s- орбиталь р- орбиталь d- орбиталь pz магнитное – m = -l, (-l+1), . . . , 0, . . . , (l-1), +l s- орбиталь- m = 0 px р- орбиталь m = 1, 0, -1 py
 Электронные орбитали атома водорода n l = 0, 1…(n-1) 1 2 3 4 m = -l, … 0, …+l Число Энергия 0–s 1–p 2–d 0 0 +1, 0, -1 1 E 1 1 3 E 2 0 +1, 0, -1 +2, +1, 0, -1, -2 0–s 1–p 2–d 3–f 0 +1, 0, -1 +2, +1, 0, -1, -2 +3, +2, +1, 0, -1, -2, -3 1 3 5 7 E 3 E 4
Электронные орбитали атома водорода n l = 0, 1…(n-1) 1 2 3 4 m = -l, … 0, …+l Число Энергия 0–s 1–p 2–d 0 0 +1, 0, -1 1 E 1 1 3 E 2 0 +1, 0, -1 +2, +1, 0, -1, -2 0–s 1–p 2–d 3–f 0 +1, 0, -1 +2, +1, 0, -1, -2 +3, +2, +1, 0, -1, -2, -3 1 3 5 7 E 3 E 4
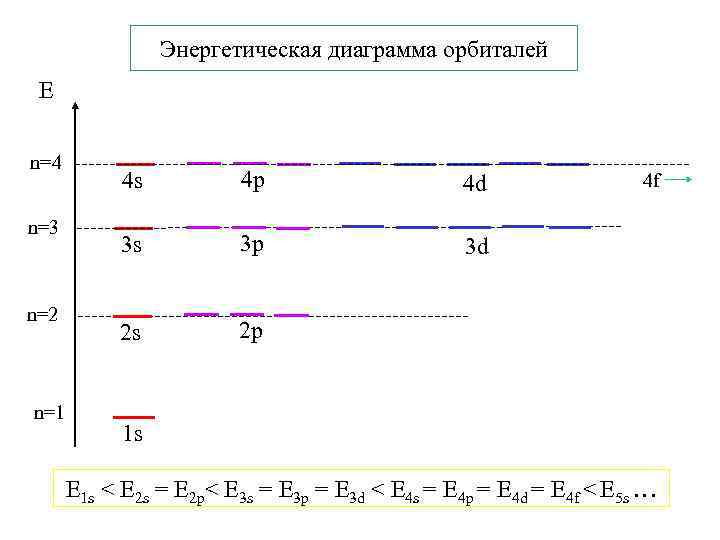 Энергетическая диаграмма орбиталей Е n=4 n=3 n=2 n=1 4 s 4 p 4 d 3 s 3 p 3 d 2 s 2 p 4 f 1 s E 1 s < E 2 s = E 2 p< E 3 s = E 3 p = E 3 d < E 4 s = E 4 p = E 4 d = E 4 f < E 5 s …
Энергетическая диаграмма орбиталей Е n=4 n=3 n=2 n=1 4 s 4 p 4 d 3 s 3 p 3 d 2 s 2 p 4 f 1 s E 1 s < E 2 s = E 2 p< E 3 s = E 3 p = E 3 d < E 4 s = E 4 p = E 4 d = E 4 f < E 5 s …
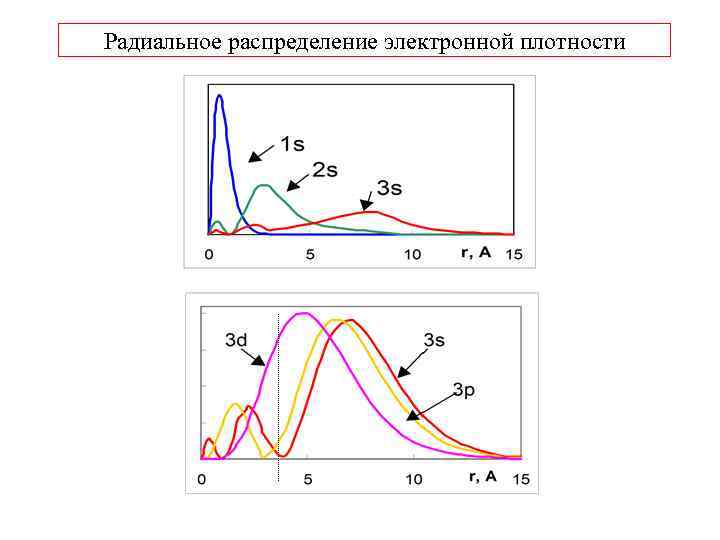 Радиальное распределение электронной плотности
Радиальное распределение электронной плотности
 1. 7 Многоэлектронный атом Zэ +Z -(Z-1) ē Zэ = Z - n, l Zэ - эффективный заряд ядра n, l - константы экранирования
1. 7 Многоэлектронный атом Zэ +Z -(Z-1) ē Zэ = Z - n, l Zэ - эффективный заряд ядра n, l - константы экранирования
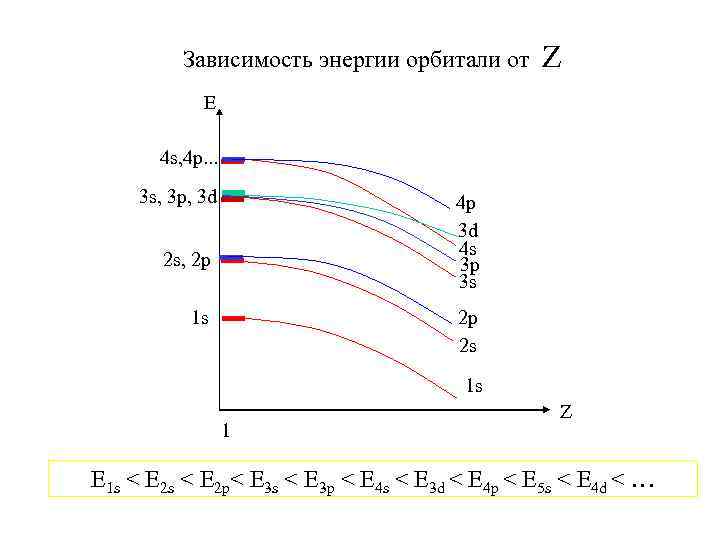 Зависимость энергии орбитали от Z Е 4 s, 4 p. . . 3 s, 3 p, 3 d 4 p 3 d 4 s 3 p 3 s 2 s, 2 p 2 p 2 s 1 s 1 s 1 Z E 1 s < E 2 p< E 3 s < E 3 p < E 4 s < E 3 d < E 4 p < E 5 s < E 4 d < …
Зависимость энергии орбитали от Z Е 4 s, 4 p. . . 3 s, 3 p, 3 d 4 p 3 d 4 s 3 p 3 s 2 s, 2 p 2 p 2 s 1 s 1 s 1 Z E 1 s < E 2 p< E 3 s < E 3 p < E 4 s < E 3 d < E 4 p < E 5 s < E 4 d < …
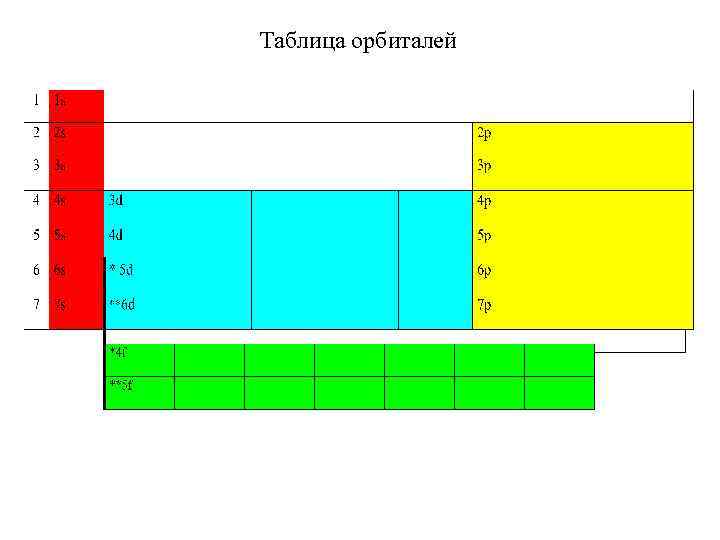 Таблица орбиталей
Таблица орбиталей
 Правила заселения орбиталей: 1. Принцип минимума энергии электронов. 2. Принцип (запрет) Паули 3. Правило Хунда
Правила заселения орбиталей: 1. Принцип минимума энергии электронов. 2. Принцип (запрет) Паули 3. Правило Хунда
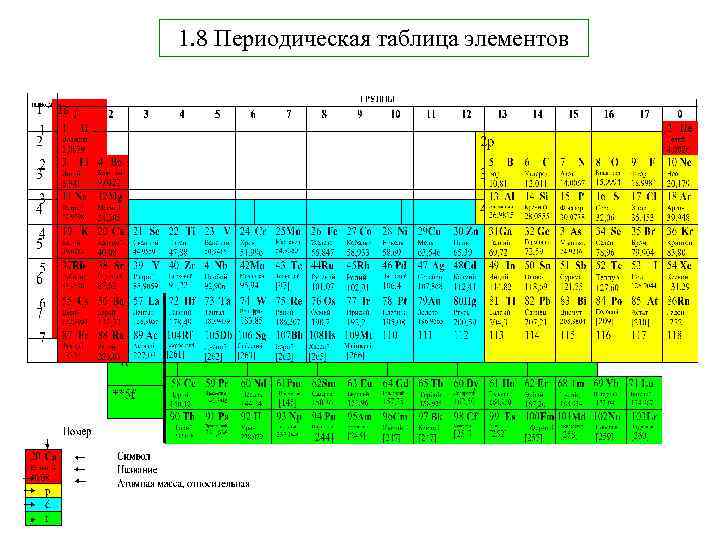 1. 8 Периодическая таблица элементов
1. 8 Периодическая таблица элементов
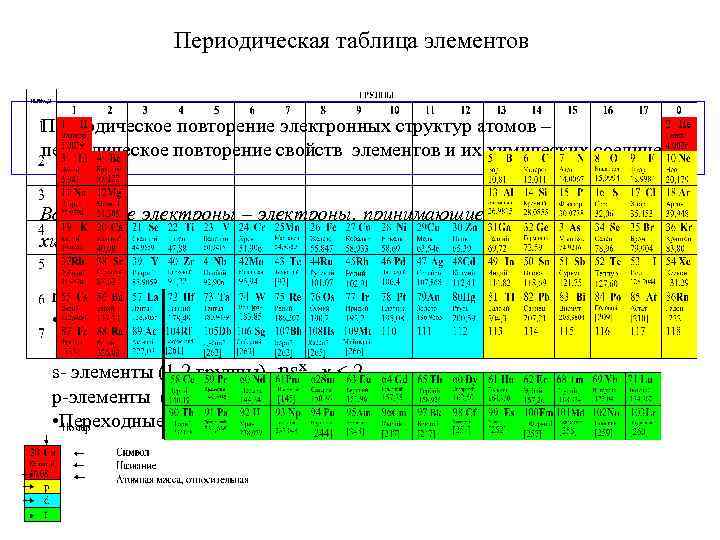 Периодическая таблица элементов Периодическое повторение электронных структур атомов – периодическое повторение свойств элементов и их химических соединений Валентные электроны – электроны, принимающие участие в образовании химической связи. ns 2 np 6 - благородные (инертные) газы (0 группа) • Типичные элементы: s- и p-элементы (главные группы) s- элементы (1 -2 группы) -nsx - x 2 p-элементы (13 -17 группы) - ns 2 npy y<6 • Переходные элементы (d-металлы) - ns 2(n-1)dy - (3 -12 группы)
Периодическая таблица элементов Периодическое повторение электронных структур атомов – периодическое повторение свойств элементов и их химических соединений Валентные электроны – электроны, принимающие участие в образовании химической связи. ns 2 np 6 - благородные (инертные) газы (0 группа) • Типичные элементы: s- и p-элементы (главные группы) s- элементы (1 -2 группы) -nsx - x 2 p-элементы (13 -17 группы) - ns 2 npy y<6 • Переходные элементы (d-металлы) - ns 2(n-1)dy - (3 -12 группы)
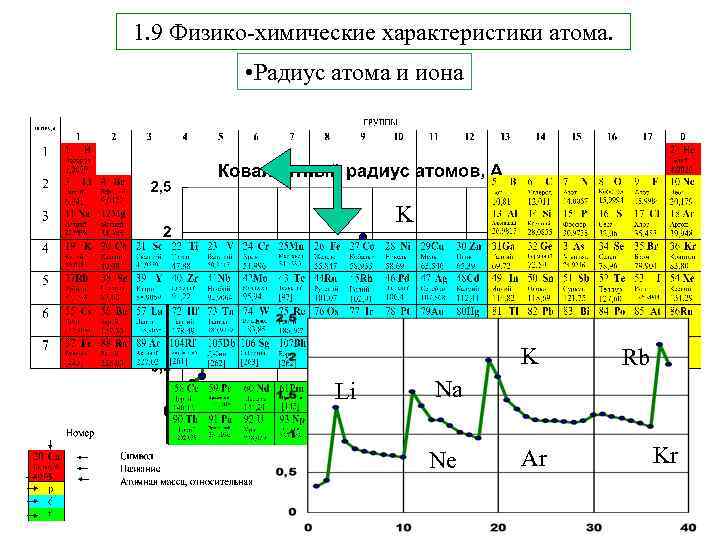 1. 9 Физико-химические характеристики атома. • Радиус атома и иона K Li Rb Na Kr K Ar Ne Li Rb Na Ne Ar Kr
1. 9 Физико-химические характеристики атома. • Радиус атома и иона K Li Rb Na Kr K Ar Ne Li Rb Na Ne Ar Kr
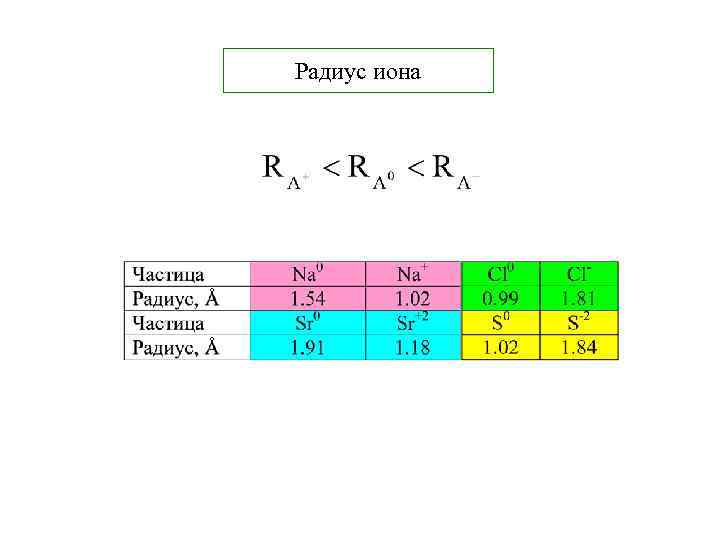 Радиус иона
Радиус иона
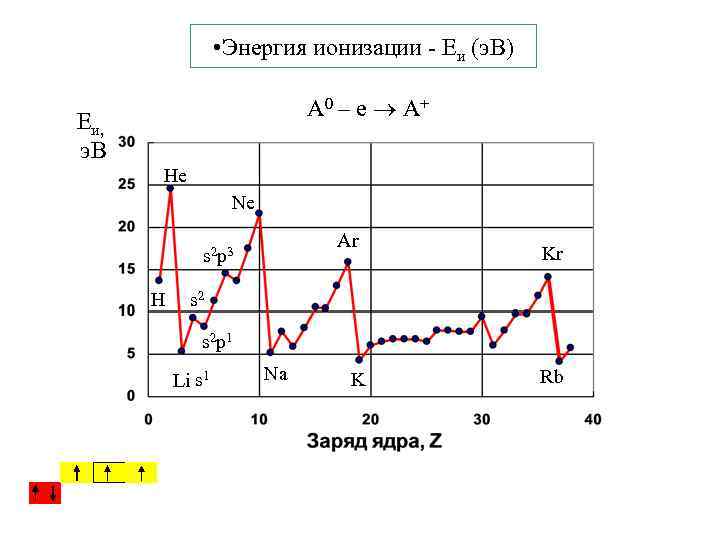 • Энергия ионизации - Eи (э. В) А 0 – е А+ Eи, э. В He Ne Ar s 2 p 3 Н Kr s 2 p 1 Li s 1 Na K Rb
• Энергия ионизации - Eи (э. В) А 0 – е А+ Eи, э. В He Ne Ar s 2 p 3 Н Kr s 2 p 1 Li s 1 Na K Rb
 • Энергия сродства к электрону - Eсв (э. В) Eсэ э. В 4 A 0 + e A– Br Cl F 2 0 -2 10 20 30 Заряд ядра, Z
• Энергия сродства к электрону - Eсв (э. В) Eсэ э. В 4 A 0 + e A– Br Cl F 2 0 -2 10 20 30 Заряд ядра, Z
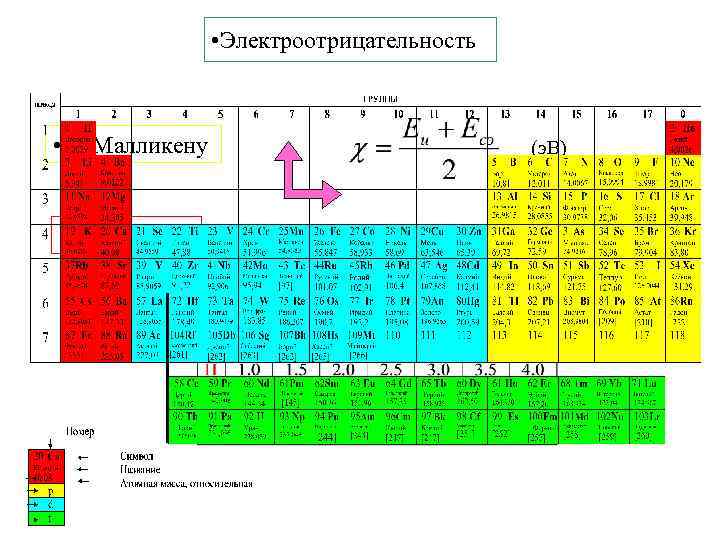 • Электроотрицательность • по Малликену • по Полингу (э. В) у. е. F = 4. 0 Li =1. 0
• Электроотрицательность • по Малликену • по Полингу (э. В) у. е. F = 4. 0 Li =1. 0


