Лекция S элементы.ppt
- Количество слайдов: 22

Химия s-элементов.

Общая характеристика s - элементов IА-группа: Li, Na, K, Rb, Cs, Fr щелочные металлы IIA-группа: Be, Mg; Ca, Sr, Ba, Ra щёлочноземельные металлы Общая электронная формула: […] ns 1 2 np 0 […] ns 1 M+I […] ns 2 …ns 1 np 1 M+II Характерно существование ионов M+ и M 2+
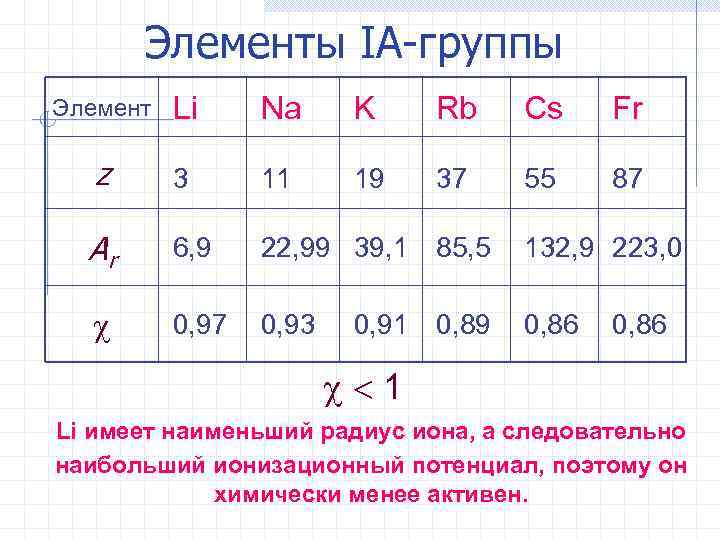
Элементы IА-группы Элемент Li Na K Rb Cs Fr z 3 11 19 37 55 87 Ar 6, 9 22, 99 39, 1 85, 5 132, 9 223, 0 0, 97 0, 93 0, 89 0, 86 0, 91 0, 86 1 Li имеет наименьший радиус иона, а следовательно наибольший ионизационный потенциал, поэтому он химически менее активен.
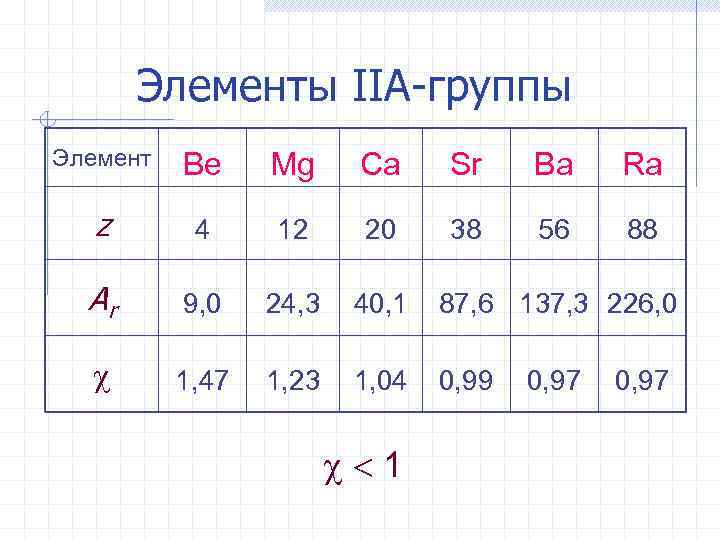
Элементы IIА-группы Элемент Be Mg Ca Sr Ba Ra z 4 12 20 38 56 88 Ar 9, 0 24, 3 40, 1 87, 6 137, 3 226, 0 1, 47 1, 23 1, 04 0, 99 1 0, 97
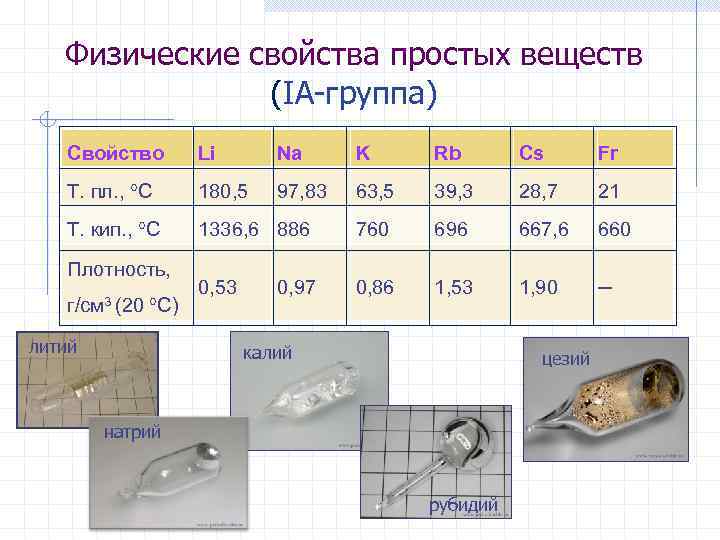
Физические свойства простых веществ (IА-группа) Свойство Li Na K Rb Cs Fr Т. пл. , С 180, 5 97, 83 63, 5 39, 3 28, 7 21 Т. кип. , С 1336, 6 886 760 696 667, 6 660 0, 53 0, 86 1, 53 1, 90 ─ Плотность, г/см 3 (20 С) литий 0, 97 калий цезий натрий рубидий
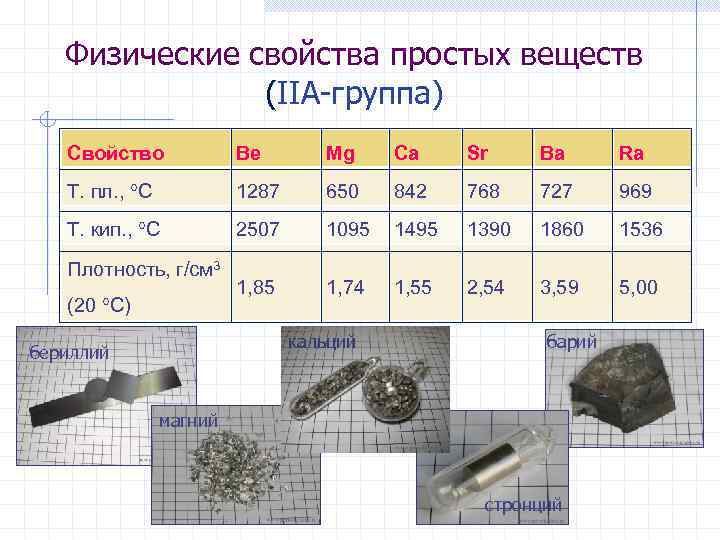
Физические свойства простых веществ (IIА-группа) Свойство Be Mg Ca Sr Ba Ra Т. пл. , С 1287 650 842 768 727 969 Т. кип. , С 2507 1095 1495 1390 1860 1536 1, 85 1, 74 1, 55 2, 54 3, 59 5, 00 Плотность, г/см 3 (20 С) кальций бериллий барий магний стронций

Общая характеристика s -элементов. Простые вещества : все – активные металлы (кроме Be) • Реагируют как восстановители M – ne – = Mn+ (n = 1, 2) • В ЭХРН – самые левые: E – 3, 01 – 2, 92 – 2, 90 – 2, 34 В Li Cs Ba Be

Общая характеристика s – элементов. Взаимодействие металлов с водой и кислотами 2 Na + 2 H 2 O = 2 Na. OH + H 2 Na –e – = Na+ 2 H 2 O + 2 e – = H 2 + 2 ОH Mg + 2 H 3 O+ = Mg 2+ + H 2 + 2 H 2 O Mg + 2 H 2 O (на холоду) Mg + 2 H 2 O + t = Mg(OH)2 + H 2 (при нагревании)

Общая характеристика s – элементов. Сложные вещества: оксиды , гидроксиды Mn+ – катионы в ионных кристаллах M 2 O, MOH; MO, M(OH)2 – имеют основный характер (кроме оксида и гидроксида Be) В водн. р-ре MOН, M(OH)2 – сильные электролиты и сильные основания (кроме гидроксидов Be и Mg): • Na. OH = Na+ + OH p. H 7 • Ba(OH)2 = Ba 2+ + 2 OH p. H 7 Для гидроксидов Mg, Be – фазовое равновесие: • Mg(OH)2(т) Mg 2+ + 2 OH p. H 7

Общая характеристика s – элементов. Сложные вещества: соли Соли: аквакатионы – непротолиты (кроме солей Be и Mg): • Na. Cl = Na+ + Cl р. Н = 7 непротолит Для бериллия и магния : [Be(H 2 O)4]2+ + H 2 O [Be(H 2 O)3(OH)]+ + H 3 O+ ; р. Н 7 [Mg(H 2 O)6]2+ + H 2 O [Mg(H 2 O)5(OH)]+ + H 3 O+ ; р. Н 7 • Be 2+·H 2 O + H 2 O Be. OH+ + H 3 O+ ; KK= 2, 0· 10 6 • Mg 2+·H 2 O + H 2 O Mg. OH+ + H 3 O+ ; KK= 3, 8· 10 12

Общая характеристика s – элементов. Сложные вещества Бинарные соединения: гидриды MH, MH 2; пероксиды M 2 O 2, MO 2; нитриды M 3 N, M 3 N 2 KH + H 2 O = KOH + H 2 Na 2 O 2(т) + H 2 O 2 Na+ + OH + HO 2 2 Na. O 2 + H 2 O = Na. OH + Na. HO 2 + O 2 4 Na. O 2 + 2 H 2 O = 4 Na. OH + 3 O 2 2 Cs. O 3 + 2 H 2 O = 2 Cs. OH + H 2 O 2 + 2 O 2 Li 3 N + 3 H 2 O = 3 Li. OH + NH 3 Ca. C 2 + 2 H 2 O = Ca(OH)2 + C 2 H 2 Be 2 C + 4 H 2 O = 2 Be(OH)2 + CH 4

Распространение в природе 5. Ca – 3, 38 % 6. Na – 2, 63 % 7. K – 2, 41 % 8. Mg – 1, 95 % по массе. 17. Rb 19. Ba Редкие и 23. Sr рассеянные 28. Li элементы 42. Cs 48. Be 92. Fr 226 Ra радиоактивный элемент Соли Na, K, Ca и Mg – в природных соленых и пресных водах (моря, океаны, озера, реки, подземные воды)

карналлит Важнейшие минералы сильвин галит лепидолит поллуцит сподумен IА-группа Галит (каменная соль) Na. Cl Карналлит KMg. Cl 3. 6 H 2 O Мирабилит Na 2 SO 4· 10 H 2 O Поллуцит (Cs, Na)Al(Si. O 3)2. n. H 2 O Сильвин KCl Сильвинит (K, Na)Cl Сподумен Li. Al(Si. O 3)2 Лепидолит K 2 Li 3 Al 4 Si 7 O 21(OH, F)3 Петалит Li. Al. Si 4 O 10

Важнейшие минералы IIА-группа Фенакит Be 2 Si. O 4 Берилл (Be 3 Al 2)Si 6 O 18 (аквамарин, изумруд). Гипс Ca. SO 4· 2 H 2 O Кальцит Ca. CO 3 (известняк, мрамор, мел) Магнезит Mg. CO 3 Оливин (Mg, Fe. II)2 Si. O 4 Тальк Mg 3 Si 4 O 10(OH)2 Хризоберилл (Be. Al 2)O 4 Целестин Sr. SO 4 Шпинель (Mg. Al 2)O 4 Стронцианит Sr. CO 3 Барит Ba. SO 4 магнезит целестин кальцит шпинель аквамарин барит

История открытия Г. Дэви: Na, K, Ca, Ba, Mg (1807 -1808) Й. Арведсон: Li (1817) Н. Воклен: Be (1798) Р. Бунзен, Г. Кирхгоф: Rb, Cs (1861) М. Склодовская-Кюри, П. Кюри, Ж. Бемон: Ra (1898) М. Пере: Fr (1939)

Бериллий Амфотерность Be + 2 HCl = Be. Cl 2 + H 2 Be + 2 Na. OH + 2 H 2 O = Na 2[Be(OH)4] + H 2 t°(сплавление) Be + 2 Na. OH(т) = Na 2 Be. O 2 + H 3 O Be(OH)2 (Кs 10– 22) OH – [Be(H 2 O)4]2+ [Be(OH)4]2–

Магний Mg + H 2 O t° Mg + 2 H 2 O = Mg(OH)2 + H 2 Mg + 2 NH 4 Cl + 2 H 2 O = = Mg. Cl 2 + 2 NH 3·H 2 O + H 2 + O [Mg(H 2 O)6]2+ H 3 Mg(OH)2 (Кs 10– 10) OH –

Взаимодействие Mg(OH)2 и солей аммония Mg(OH)2(т) + 2 NH 4 Cl = Mg. Cl 2 + 2 NH 3·H 2 O Mg 2+ + 2 OH– 2 NH 4+ + 2 Cl– 2 NH 3·H 2 O Mg(OH)2(т) + 2 NH 4+ = Mg 2+ + 2 NH 3·H 2 O

Разделение катионов Be 2+ и Mg 2+ при их совместном присутствии в растворе 1. Действие избытка щелочи: Be 2+ + 4 OH– = [Be(OH)4]2– Mg 2+ + 2 OH– = Mg(OH)2 2. Действие NH 4 Cl + NH 3·H 2 O: Be 2+ + 2 NH 3·H 2 O = Be(OH)2 Mg 2+ + NH 3·H 2 O + NH 4+

Разделение катионов Sr 2+ и Ba 2+ при их совместном присутствии в растворе 1. Осаждение хроматов: Sr 2+ + Cr. O 42– = Sr. Cr. O 4 Ba 2+ + Cr. O 42– = Ba. Cr. O 4 2. Растворение хромата стронция в уксусной кислоте: 2 Sr. Cr. O 4(т) + 2 CH 3 COOH = = Sr. Cr 2 O 7 + Sr(CH 3 COO)2 + H 2 O
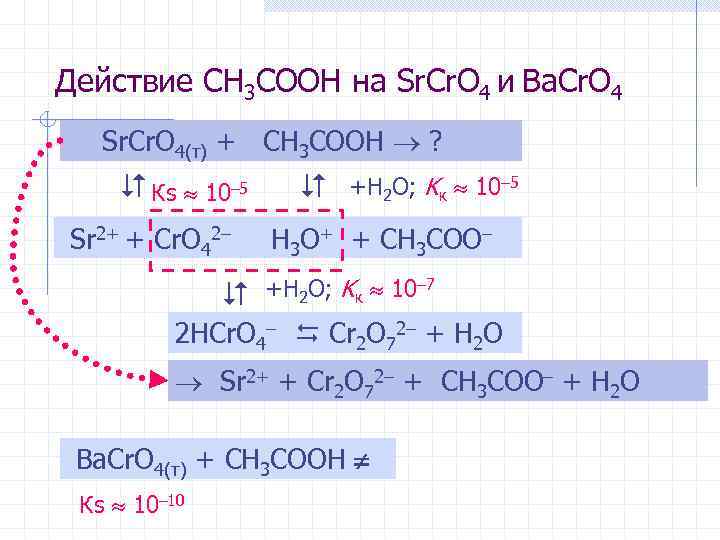
Действие CH 3 COOH на Sr. Cr. O 4 и Ba. Cr. O 4 Sr. Cr. O 4(т) + CH 3 COOH ? Кs 10– 5 Sr 2+ + Cr. O 42– +H 2 O; Kк 10– 5 H 3 O+ + CH 3 COO– +H 2 O; Kк 10– 7 2 HCr. O 4– Cr 2 O 72– + H 2 O Sr 2+ + Cr 2 O 72– + CH 3 COO– + H 2 O Ba. Cr. O 4(т) + CH 3 COOH Кs 10– 10
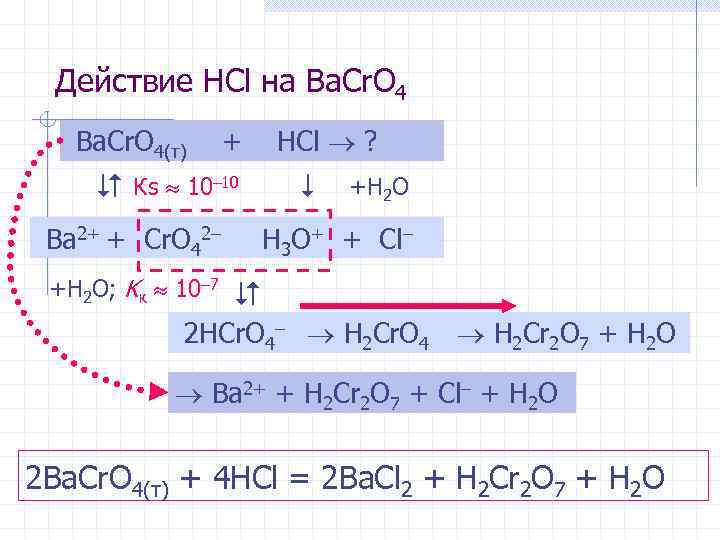
Действие HCl на Ba. Cr. O 4(т) + Кs 10– 10 Ba 2+ + Cr. O 42– +H 2 O; Kк 10– 7 HCl ? +H 2 O H 3 O+ + Cl– 2 HCr. O 4– H 2 Cr. O 4 H 2 Cr 2 O 7 + H 2 O Ba 2+ + H 2 Cr 2 O 7 + Cl– + H 2 O 2 Ba. Cr. O 4(т) + 4 HCl = 2 Ba. Cl 2 + H 2 Cr 2 O 7 + H 2 O
Лекция S элементы.ppt