ХРМ_Лекция-01_кристаллы.ppt
- Количество слайдов: 66
 Химия радиоматериалов Пащенко Константин Петрович, доцент кафедры «Органическая, биологическая и физколлоидная химия» , 2. 210, тел. 614 -158.
Химия радиоматериалов Пащенко Константин Петрович, доцент кафедры «Органическая, биологическая и физколлоидная химия» , 2. 210, тел. 614 -158.
 Литература: 1. Сорокин В. С. Материалы и элементы электронной техники. В 2 -х томах. М. : Академия, 2006. (есть в локальной сети!) 2. Пасынков В. В. , Сорокин B. C. Материалы электронной техники. – СПб. : Издательство «Лань» , 2002. – 368 с. (библиотека АГТУ, локальная сеть) 3. Электрорадиоматериалы / Б. М. Тареев, Н. В. Короткова, В. М. Петров, A. A. Преображенский. Под ред. Б. М. Тареева. – М. : Высшая школа, 1978. (библ. АГТУ, локальная сеть) 4. Ивлев Ю. Н. Химия радиоматериалов. Введение в физикохимические основы технологии радиоматериалов. – М. : МТУСИ, 2002. – 134 с. (локальная сеть) 5. Ивлев Ю. Н. Химия радиоматериалов. Сборник задач с решениями и контрольное задание. – М. : МТУСИ, 2002. – 32 с. (локальная сеть) 6. Материаловедение / Б. Н. Арзамасов, И. И. Сидорин, Г. Ф. Косолапов и др. Под общ. ред. Б. Н. Арзамасова. – М. : Машиностроение, 1986. – 384 с. (библ. АГТУ)
Литература: 1. Сорокин В. С. Материалы и элементы электронной техники. В 2 -х томах. М. : Академия, 2006. (есть в локальной сети!) 2. Пасынков В. В. , Сорокин B. C. Материалы электронной техники. – СПб. : Издательство «Лань» , 2002. – 368 с. (библиотека АГТУ, локальная сеть) 3. Электрорадиоматериалы / Б. М. Тареев, Н. В. Короткова, В. М. Петров, A. A. Преображенский. Под ред. Б. М. Тареева. – М. : Высшая школа, 1978. (библ. АГТУ, локальная сеть) 4. Ивлев Ю. Н. Химия радиоматериалов. Введение в физикохимические основы технологии радиоматериалов. – М. : МТУСИ, 2002. – 134 с. (локальная сеть) 5. Ивлев Ю. Н. Химия радиоматериалов. Сборник задач с решениями и контрольное задание. – М. : МТУСИ, 2002. – 32 с. (локальная сеть) 6. Материаловедение / Б. Н. Арзамасов, И. И. Сидорин, Г. Ф. Косолапов и др. Под общ. ред. Б. Н. Арзамасова. – М. : Машиностроение, 1986. – 384 с. (библ. АГТУ)
 Литература в локальной сети АГТУ: \172. 20. 20ITi. KSviaz210402 Средства связи с подвижными объектами3 курсХимия радиоматериалов
Литература в локальной сети АГТУ: \172. 20. 20ITi. KSviaz210402 Средства связи с подвижными объектами3 курсХимия радиоматериалов
 Литература, используемая при изучении химии радиоматериалов в МТУСИ (головной вуз по подготовке специалистов в области связи): 1. Материалы микроэлектронной техники / Под ред. В. М. Андреева. – М. : Радио и связь, 1989. – 352 с. (Есть в библиотеке АГТУ. ) 2. Богородицкий Н. П. , Пасынков В. В. , Тареев Б. М. Электротехнические материалы. 6 -е изд. Л. : Энергия, 1977. – 352 с. (Есть в библиотеке АГТУ. ) 3. Коровин Н. В. Общая химия: Учебник для технических направлений и специальностей вузов. – 2 -е изд. М. : Высшая школа, 2000. – 558 с. (Есть в библиотеке АГТУ. )
Литература, используемая при изучении химии радиоматериалов в МТУСИ (головной вуз по подготовке специалистов в области связи): 1. Материалы микроэлектронной техники / Под ред. В. М. Андреева. – М. : Радио и связь, 1989. – 352 с. (Есть в библиотеке АГТУ. ) 2. Богородицкий Н. П. , Пасынков В. В. , Тареев Б. М. Электротехнические материалы. 6 -е изд. Л. : Энергия, 1977. – 352 с. (Есть в библиотеке АГТУ. ) 3. Коровин Н. В. Общая химия: Учебник для технических направлений и специальностей вузов. – 2 -е изд. М. : Высшая школа, 2000. – 558 с. (Есть в библиотеке АГТУ. )
 Цель курса ХРМ – познакомить будущих инженеров, специализирующихся в области СРЕДСТВ СВЯЗИ, ИНФОРМАТИКИ и ТЕЛЕКОММУНИКАЦИЙ с основными материалами, применяемыми в производстве радиоэлектронной аппаратуры (РЭА), технологиями получения и обработки этих материалов.
Цель курса ХРМ – познакомить будущих инженеров, специализирующихся в области СРЕДСТВ СВЯЗИ, ИНФОРМАТИКИ и ТЕЛЕКОММУНИКАЦИЙ с основными материалами, применяемыми в производстве радиоэлектронной аппаратуры (РЭА), технологиями получения и обработки этих материалов.
 Основные разделы курса ХРМ (структура курса): 1. Строение и свойства материалов. 2. Физико-химический анализ и учение о фазовых равновесиях. 3. Методы формирования материалов с заданными свойствами. 4. Базовые материалы микроэлектроники (проводники, полупроводники, диэлектрики, магнитные материалы).
Основные разделы курса ХРМ (структура курса): 1. Строение и свойства материалов. 2. Физико-химический анализ и учение о фазовых равновесиях. 3. Методы формирования материалов с заданными свойствами. 4. Базовые материалы микроэлектроники (проводники, полупроводники, диэлектрики, магнитные материалы).
 1. Строение и свойства материалов 1. 1. Кристаллическое и аморфное состояния вещества
1. Строение и свойства материалов 1. 1. Кристаллическое и аморфное состояния вещества
 Кристаллическое и аморфное состояния вещества Свойства жидкостей и газов определяются в основном их химическим составом.
Кристаллическое и аморфное состояния вещества Свойства жидкостей и газов определяются в основном их химическим составом.
 Кристаллическое и аморфное состояния вещества Свойства ТВЕРДЫХ ТЕЛ (химические, физические) в огромной степени зависят от структуры!
Кристаллическое и аморфное состояния вещества Свойства ТВЕРДЫХ ТЕЛ (химические, физические) в огромной степени зависят от структуры!
 Кристаллическое и аморфное состояния вещества Все твердые тела делятся на: кристаллические и аморфные (бесформенные). Примером аморфного состояния является стеклообразное.
Кристаллическое и аморфное состояния вещества Все твердые тела делятся на: кристаллические и аморфные (бесформенные). Примером аморфного состояния является стеклообразное.
 Кристаллическое и аморфное состояния вещества В кристаллах структурные единицы (атомы, ионы или молекулы) расположены регулярно (упорядоченно).
Кристаллическое и аморфное состояния вещества В кристаллах структурные единицы (атомы, ионы или молекулы) расположены регулярно (упорядоченно).
 Кристаллическое и аморфное состояния вещества В монокристалле эта регулярность распространяется на весь объем твердого тела.
Кристаллическое и аморфное состояния вещества В монокристалле эта регулярность распространяется на весь объем твердого тела.
 Кристаллическое и аморфное состояния вещества Поликристалл состоит из отдельных регулярных областей (зёрен). На границах зёрен ориентация регулярности резко меняется.
Кристаллическое и аморфное состояния вещества Поликристалл состоит из отдельных регулярных областей (зёрен). На границах зёрен ориентация регулярности резко меняется.
 Кристаллическое и аморфное состояния вещества В аморфном твердом теле расположение структурных единиц полностью разупорядочено.
Кристаллическое и аморфное состояния вещества В аморфном твердом теле расположение структурных единиц полностью разупорядочено.
 Кристаллическое и аморфное состояния вещества Аморфное тело может рассматриваться как жидкость с большой вязкостью! Истинно твердыми телами следует считать кристаллические тела.
Кристаллическое и аморфное состояния вещества Аморфное тело может рассматриваться как жидкость с большой вязкостью! Истинно твердыми телами следует считать кристаллические тела.
 Кристаллическое и аморфное состояния вещества КРИСТАЛЛЫ переходят из твердого состояния в жидкое при определенной температуре (температуре плавления). АМОРФНЫЕ ТЕЛА при нагревании постепенно размягчаются – их вязкость постепенно уменьшается.
Кристаллическое и аморфное состояния вещества КРИСТАЛЛЫ переходят из твердого состояния в жидкое при определенной температуре (температуре плавления). АМОРФНЫЕ ТЕЛА при нагревании постепенно размягчаются – их вязкость постепенно уменьшается.
 Кристаллическое и аморфное состояния вещества Одинаковые по химическому составу вещества могут быть как в кристаллическом, так и в аморфном состоянии! Например, диоксид кремния Si. O 2 существует в аморфном (кварцевое стекло) и в трех кристаллических модификациях.
Кристаллическое и аморфное состояния вещества Одинаковые по химическому составу вещества могут быть как в кристаллическом, так и в аморфном состоянии! Например, диоксид кремния Si. O 2 существует в аморфном (кварцевое стекло) и в трех кристаллических модификациях.
 Кристаллическое и аморфное состояния вещества C точки зрения ТЕРМОДИНАМИКИ кристаллические формы всегда более устойчивы, так как характеризуются меньшим значением свободной энергии Гиббса (G) по сравнению с аморфным состоянием. .
Кристаллическое и аморфное состояния вещества C точки зрения ТЕРМОДИНАМИКИ кристаллические формы всегда более устойчивы, так как характеризуются меньшим значением свободной энергии Гиббса (G) по сравнению с аморфным состоянием. .
 Кристаллическое и аморфное состояния вещества Возможны самопроизвольные переходы вещества из аморфного состояния в кристаллическое (например, процесс «расстекловывания» диоксида кремния).
Кристаллическое и аморфное состояния вещества Возможны самопроизвольные переходы вещества из аморфного состояния в кристаллическое (например, процесс «расстекловывания» диоксида кремния).
 Закон гранных углов Кристалл – это определенной формы многогранник с плоскими гранями, которые для заданной модификации кристалла пересекаются под определенными углами независимо от их размеров и искажений роста.
Закон гранных углов Кристалл – это определенной формы многогранник с плоскими гранями, которые для заданной модификации кристалла пересекаются под определенными углами независимо от их размеров и искажений роста.
 Кристаллическое и аморфное состояния вещества Таким образом, кристалл представляет собой совокупность структурных единиц, упорядоченно расположенных в определенных местах (узлах) и образующих кристаллическую решетку.
Кристаллическое и аморфное состояния вещества Таким образом, кристалл представляет собой совокупность структурных единиц, упорядоченно расположенных в определенных местах (узлах) и образующих кристаллическую решетку.
 Элементарная ячейка кристалла ЭЛЕМЕНТАРНАЯ (КРИСТАЛЛИЧЕСКАЯ) ЯЧЕЙКА – наименьшая часть кристаллической решетки, содержащая все структурные единицы кристалла и передающая все характерные особенности их взаимного расположения.
Элементарная ячейка кристалла ЭЛЕМЕНТАРНАЯ (КРИСТАЛЛИЧЕСКАЯ) ЯЧЕЙКА – наименьшая часть кристаллической решетки, содержащая все структурные единицы кристалла и передающая все характерные особенности их взаимного расположения.
 Векторы элементарной ячейки В любом кристалле можно выделить три направления (x, y, z) вдоль векторов a, b и с, не лежащих в одной плоскости таким образом, что расположение частиц, образующих кристалл, вдоль этих направлений периодично (т. е. повторяется). Отрезки a, b и с есть расстояния между частицами.
Векторы элементарной ячейки В любом кристалле можно выделить три направления (x, y, z) вдоль векторов a, b и с, не лежащих в одной плоскости таким образом, что расположение частиц, образующих кристалл, вдоль этих направлений периодично (т. е. повторяется). Отрезки a, b и с есть расстояния между частицами.
 Операция трансляции Элементарная ячейка представляет собой параллелепипед, построенный на векторах a, b и с. Перемещение элементарной ячейки в пространстве на расстояния a, b и с вдоль кристаллографических осей x, у и z воспроизводит строение всей кристаллической решетки.
Операция трансляции Элементарная ячейка представляет собой параллелепипед, построенный на векторах a, b и с. Перемещение элементарной ячейки в пространстве на расстояния a, b и с вдоль кристаллографических осей x, у и z воспроизводит строение всей кристаллической решетки.
 Параметры решётки Величины отрезков a, b, с, а также углы α, β и γ между ними называются параметрами решетки. Таким образом: любой структурный элемент кристаллической решетки встречается в кристалле в данном направлении через равные промежутки (дальний порядок решётки). В аморфных телах дальний порядок отсутствует!
Параметры решётки Величины отрезков a, b, с, а также углы α, β и γ между ними называются параметрами решетки. Таким образом: любой структурный элемент кристаллической решетки встречается в кристалле в данном направлении через равные промежутки (дальний порядок решётки). В аморфных телах дальний порядок отсутствует!
 Операции симметрии СИММЕТРИЯ – свойство объекта после некоторой произведенной над ним операции совмещаться со своим первоначальным положением. Одной из операций симметрии является трансляция. Таким образом, кристалл обладает трансляционной симметрией.
Операции симметрии СИММЕТРИЯ – свойство объекта после некоторой произведенной над ним операции совмещаться со своим первоначальным положением. Одной из операций симметрии является трансляция. Таким образом, кристалл обладает трансляционной симметрией.
 Операции симметрии ЭЛЕМЕНТ СИММЕТРИИ – воображаемый геометрический элемент, при помощи которого осуществляется операция симметрии. Элементы симметрии: ОСИ, ПЛОСКОСТИ, ЦЕНТР СИММЕТРИИ.
Операции симметрии ЭЛЕМЕНТ СИММЕТРИИ – воображаемый геометрический элемент, при помощи которого осуществляется операция симметрии. Элементы симметрии: ОСИ, ПЛОСКОСТИ, ЦЕНТР СИММЕТРИИ.
 Ось симметрии Осью симметрии n-ого порядка называется прямая, при повороте вокруг которой на угол = 360 /n все части кристалла совмещаются с их первоначальным положением. Оси симметрии в кристаллах могут быть 1, 2, 3, 4 и 6 порядков.
Ось симметрии Осью симметрии n-ого порядка называется прямая, при повороте вокруг которой на угол = 360 /n все части кристалла совмещаются с их первоначальным положением. Оси симметрии в кристаллах могут быть 1, 2, 3, 4 и 6 порядков.
 Плоскость симметрии делит кристалл на две части, являющиеся зеркальным изображением друга (зеркальная симметрия).
Плоскость симметрии делит кристалл на две части, являющиеся зеркальным изображением друга (зеркальная симметрия).
 Центр симметрии – точка внутри кристалла, в которой пересекаются и делятся пополам все прямые, соединяющие противоположные точки поверхности. Зеркальное отражение всех узлов решетки в центре симметрии приводит к их совмещению.
Центр симметрии – точка внутри кристалла, в которой пересекаются и делятся пополам все прямые, соединяющие противоположные точки поверхности. Зеркальное отражение всех узлов решетки в центре симметрии приводит к их совмещению.
 Сингонии Математически доказано, что могут существовать только 32 кристаллографических класса, каждый из которых состоит из соответствующего множества (набора) элементов симметрии. Они разбиваются на семь групп, называемых сингониями. (См. , напр. : Павлов П. В. , Хохлов А. Ф. Физика твердого тела. – М. : Высшая школа, 2000. – 494 с. ; Ивлев Ю. Н. Химия радиоматериалов. – и др. )
Сингонии Математически доказано, что могут существовать только 32 кристаллографических класса, каждый из которых состоит из соответствующего множества (набора) элементов симметрии. Они разбиваются на семь групп, называемых сингониями. (См. , напр. : Павлов П. В. , Хохлов А. Ф. Физика твердого тела. – М. : Высшая школа, 2000. – 494 с. ; Ивлев Ю. Н. Химия радиоматериалов. – и др. )
 Виды элементарных ячеек Если узлы решетки находятся только в вершинах элементарной ячейки, то она называется ПРИМИТИВНОЙ (обозначается символом Ρ). Если в центре ячейки находится дополнительный узел, то она называется ОБЪЕМНОЦЕНТРИРОВАННОЙ (символ I). Если узел находится в центре одной из граней – ячейка БАЗОЦЕНТРИРОВАННАЯ (символ С), если в центре всех граней – ГРАНЕЦЕНТРИРОВАННАЯ (символ F).
Виды элементарных ячеек Если узлы решетки находятся только в вершинах элементарной ячейки, то она называется ПРИМИТИВНОЙ (обозначается символом Ρ). Если в центре ячейки находится дополнительный узел, то она называется ОБЪЕМНОЦЕНТРИРОВАННОЙ (символ I). Если узел находится в центре одной из граней – ячейка БАЗОЦЕНТРИРОВАННАЯ (символ С), если в центре всех граней – ГРАНЕЦЕНТРИРОВАННАЯ (символ F).
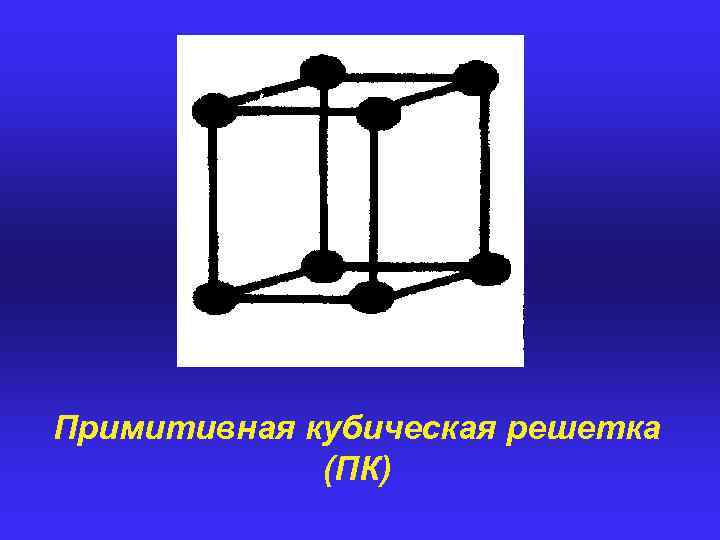 Примитивная кубическая решетка (ПК)
Примитивная кубическая решетка (ПК)
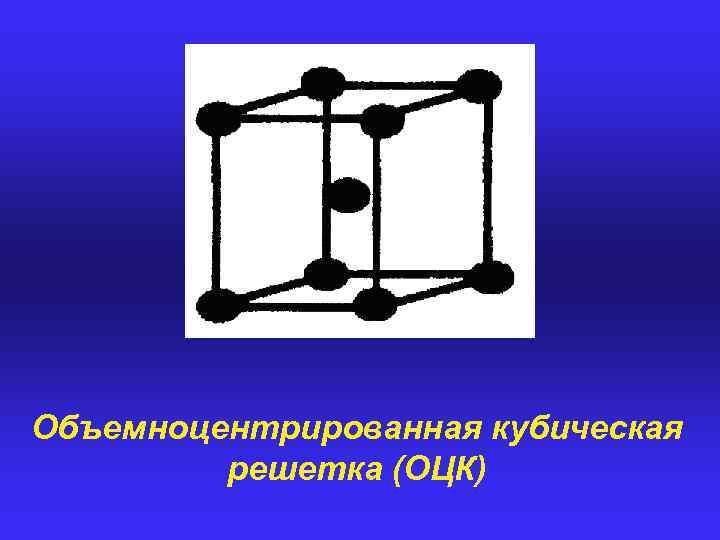 Объемноцентрированная кубическая решетка (ОЦК)
Объемноцентрированная кубическая решетка (ОЦК)
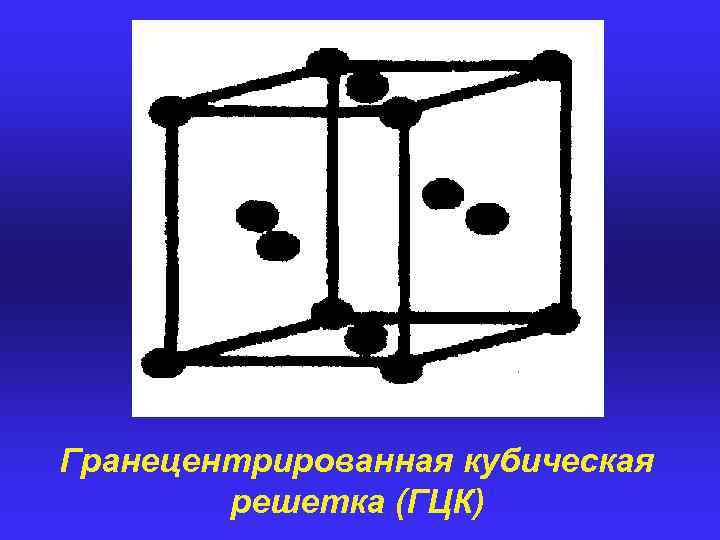 Гранецентрированная кубическая решетка (ГЦК)
Гранецентрированная кубическая решетка (ГЦК)
 Решетки Бравэ (14 возможных типов элементарных ячеек)
Решетки Бравэ (14 возможных типов элементарных ячеек)
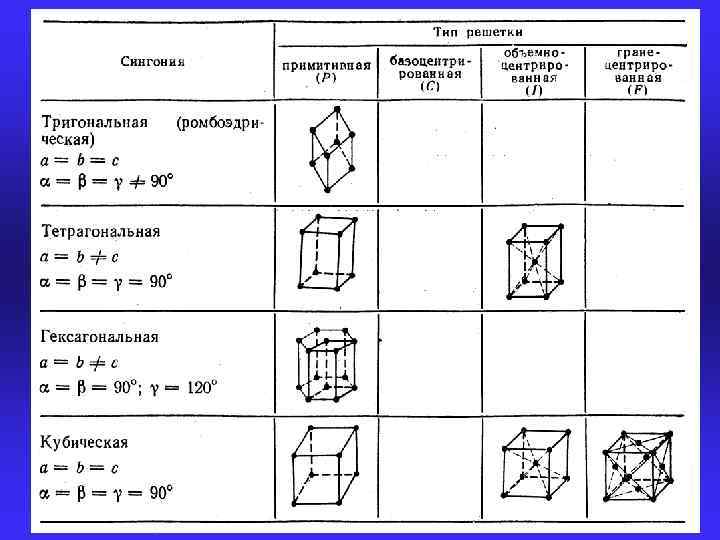
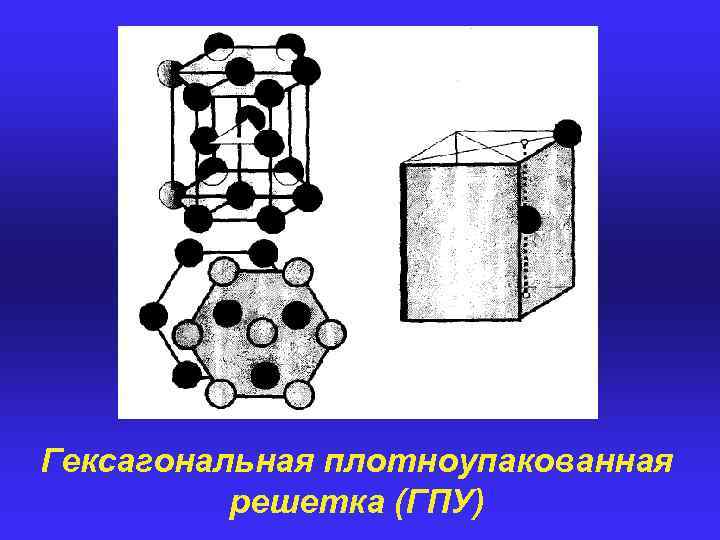 Гексагональная плотноупакованная решетка (ГПУ)
Гексагональная плотноупакованная решетка (ГПУ)


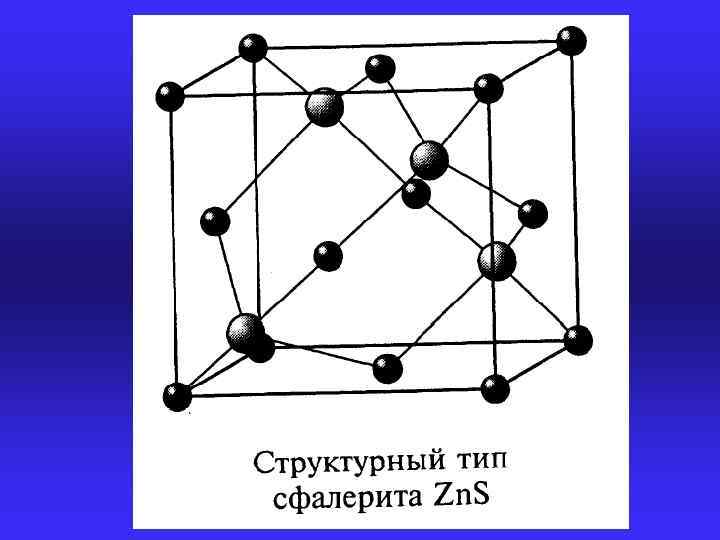
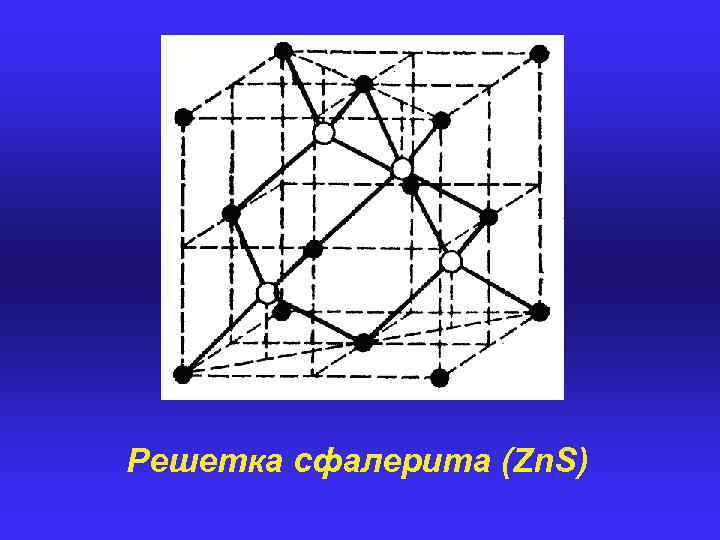 Решетка сфалерита (Zn. S)
Решетка сфалерита (Zn. S)
 Изотропия и анизотропия Формирование кристаллов в форме многогранников является следствием неодинаковости скоростей роста его граней в различных направлениях (в противном случае кристалл имел бы шарообразную форму). Это – самое наглядное проявление одного из основных свойств кристаллических тел – АНИЗОТРОПИИ.
Изотропия и анизотропия Формирование кристаллов в форме многогранников является следствием неодинаковости скоростей роста его граней в различных направлениях (в противном случае кристалл имел бы шарообразную форму). Это – самое наглядное проявление одного из основных свойств кристаллических тел – АНИЗОТРОПИИ.
 Изотропия и анизотропия Анизотропия – зависимость так называемых ВЕКТОРНЫХ СВОЙСТВ (электро - и теплопроводности, прочности, коэффициента преломления, скорости роста и растворения и т. д. ) от направления в кристалле. Анизотропия возникает вследствие различия расстояний между атомами, прочности, (а иногда и природы) химической связи между ними в различных направлениях.
Изотропия и анизотропия Анизотропия – зависимость так называемых ВЕКТОРНЫХ СВОЙСТВ (электро - и теплопроводности, прочности, коэффициента преломления, скорости роста и растворения и т. д. ) от направления в кристалле. Анизотропия возникает вследствие различия расстояний между атомами, прочности, (а иногда и природы) химической связи между ними в различных направлениях.
 Изотропия и анизотропия Это относится к монокристаллам, так как в поликристаллических образцах анизотропия свойств нивелируется за счет различной ориентации множества зерен. Наиболее сильно анизотропия проявляется в кристаллах со структурами, характеризующимися малой симметрией.
Изотропия и анизотропия Это относится к монокристаллам, так как в поликристаллических образцах анизотропия свойств нивелируется за счет различной ориентации множества зерен. Наиболее сильно анизотропия проявляется в кристаллах со структурами, характеризующимися малой симметрией.
 Изотропия и анизотропия Так как в структуре аморфных тел дальний порядок отсутствует, их векторные свойства от направления не зависят, т. е. АМОРФНЫЕ ТЕЛА ИЗОТРОПНЫ!
Изотропия и анизотропия Так как в структуре аморфных тел дальний порядок отсутствует, их векторные свойства от направления не зависят, т. е. АМОРФНЫЕ ТЕЛА ИЗОТРОПНЫ!
 Плотность упаковки решётки Плотность упаковки: r = n Vатома / V, где n – число частиц в элементарной ячейке. Объем куба равен а 3. Для простого куба радиус атома равен: r = a / 2, плотность упаковки = 1 4/3 (a/2)3 / а 3 = / 6 = 0, 524 (52, 4%).
Плотность упаковки решётки Плотность упаковки: r = n Vатома / V, где n – число частиц в элементарной ячейке. Объем куба равен а 3. Для простого куба радиус атома равен: r = a / 2, плотность упаковки = 1 4/3 (a/2)3 / а 3 = / 6 = 0, 524 (52, 4%).
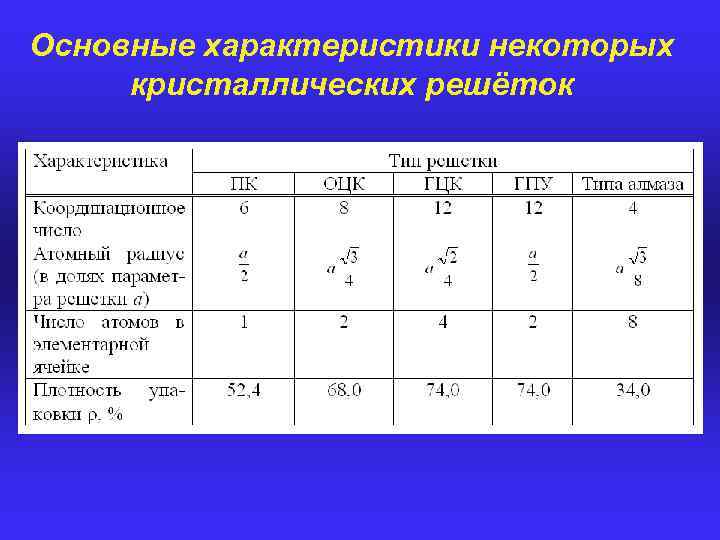 Основные характеристики некоторых кристаллических решёток
Основные характеристики некоторых кристаллических решёток
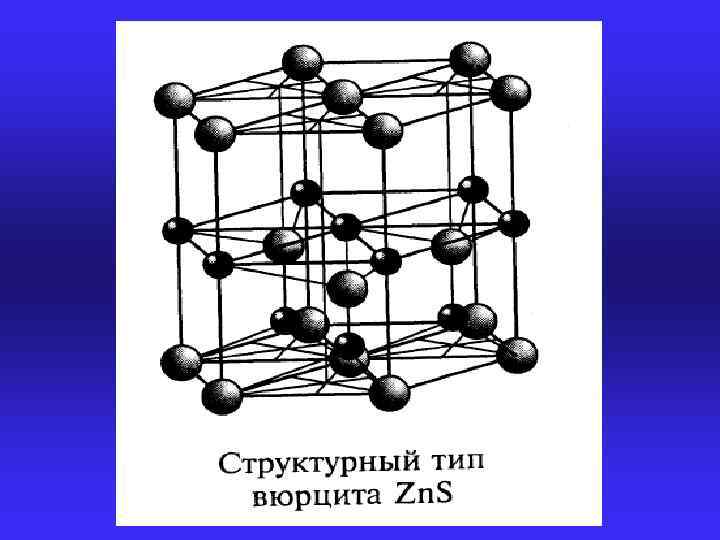
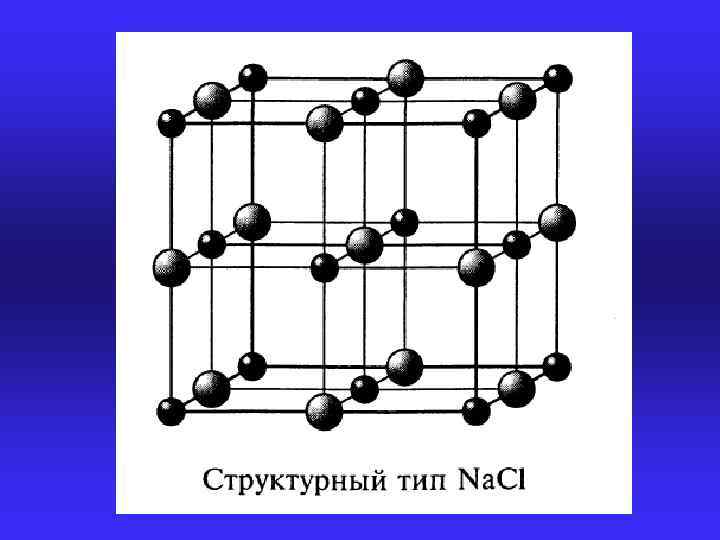
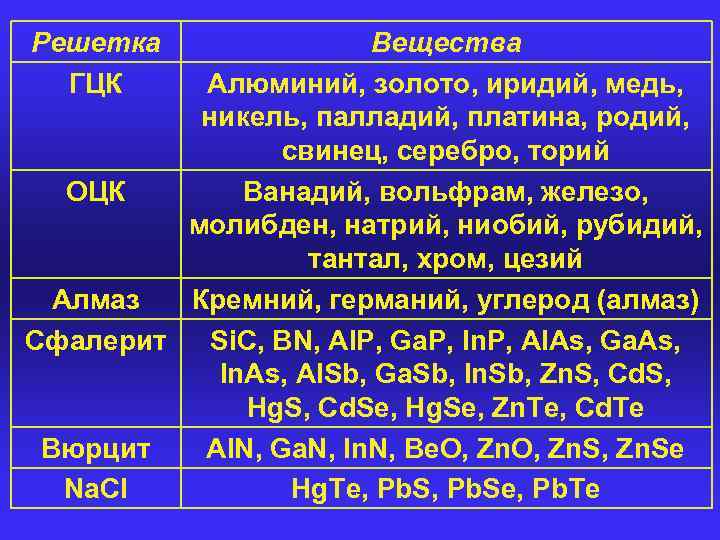 Решетка ГЦК Вещества Алюминий, золото, иридий, медь, никель, палладий, платина, родий, свинец, серебро, торий ОЦК Ванадий, вольфрам, железо, молибден, натрий, ниобий, рубидий, тантал, хром, цезий Алмаз Кремний, германий, углерод (алмаз) Сфалерит Si. C, BN, Al. P, Ga. P, In. P, Al. As, Ga. As, In. As, Al. Sb, Ga. Sb, In. Sb, Zn. S, Cd. S, Hg. S, Cd. Se, Hg. Se, Zn. Te, Cd. Te Вюрцит Al. N, Ga. N, In. N, Be. O, Zn. S, Zn. Se Na. Cl Hg. Te, Pb. Se, Pb. Te
Решетка ГЦК Вещества Алюминий, золото, иридий, медь, никель, палладий, платина, родий, свинец, серебро, торий ОЦК Ванадий, вольфрам, железо, молибден, натрий, ниобий, рубидий, тантал, хром, цезий Алмаз Кремний, германий, углерод (алмаз) Сфалерит Si. C, BN, Al. P, Ga. P, In. P, Al. As, Ga. As, In. As, Al. Sb, Ga. Sb, In. Sb, Zn. S, Cd. S, Hg. S, Cd. Se, Hg. Se, Zn. Te, Cd. Te Вюрцит Al. N, Ga. N, In. N, Be. O, Zn. S, Zn. Se Na. Cl Hg. Te, Pb. Se, Pb. Te
 Виды кристаллов по типу связи: • ковалентные • ионные • металлические • молекулярные • со смешанными связями
Виды кристаллов по типу связи: • ковалентные • ионные • металлические • молекулярные • со смешанными связями
 КОВАЛЕНТНЫЕ КРИСТАЛЛЫ § химическая связь – ковалентная полярная или слабополярная § структурные единицы в узлах – атомы § весь кристалл – одна гигантская молекула § высокая энергия связи § высокая температура плавления и низкая летучесть § неплотная упаковка – из-за направленности ковалентной связи
КОВАЛЕНТНЫЕ КРИСТАЛЛЫ § химическая связь – ковалентная полярная или слабополярная § структурные единицы в узлах – атомы § весь кристалл – одна гигантская молекула § высокая энергия связи § высокая температура плавления и низкая летучесть § неплотная упаковка – из-за направленности ковалентной связи
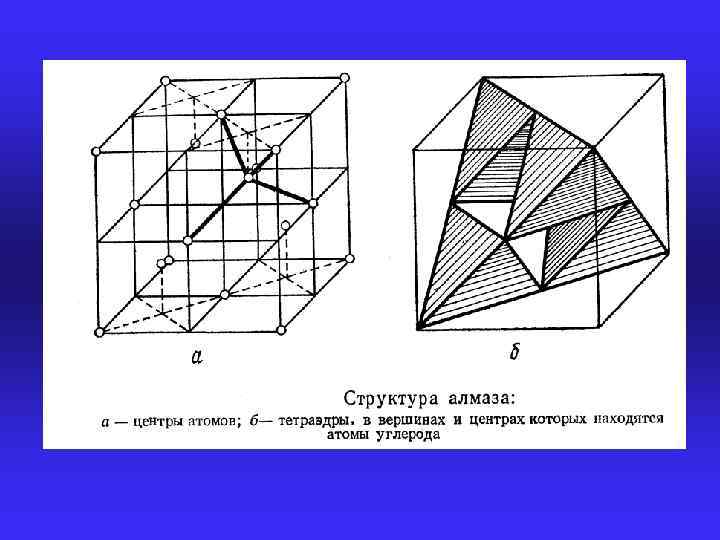
 КОВАЛЕНТНЫЕ КРИСТАЛЛЫ § твердость и хрупкость § невысокая электропроводность, растущая с увеличением температуры § типичные представители: алмаз, кремний, германий, соединения АIIIBV
КОВАЛЕНТНЫЕ КРИСТАЛЛЫ § твердость и хрупкость § невысокая электропроводность, растущая с увеличением температуры § типичные представители: алмаз, кремний, германий, соединения АIIIBV
 ИОННЫЕ КРИСТАЛЛЫ § химическая связь – ионная § структурные единицы в узлах – катионы и анионы § состоят из атомов элементов с сильно отличающейся электроотрицательностью § высокая энергия связи (имеющей электростатический характер) и высокая энергия решетки § высокая температура плавления и низкая летучесть
ИОННЫЕ КРИСТАЛЛЫ § химическая связь – ионная § структурные единицы в узлах – катионы и анионы § состоят из атомов элементов с сильно отличающейся электроотрицательностью § высокая энергия связи (имеющей электростатический характер) и высокая энергия решетки § высокая температура плавления и низкая летучесть
 ИОННЫЕ КРИСТАЛЛЫ § плотная упаковка решетки – из-за ненаправленности ионной связи (сферическая симметрия электростатического поля) § сухие кристаллы при низких температурах – диэлектрики (валентные электроны локализованы) § растворы и расплавы – электролиты (проводники второго рода)
ИОННЫЕ КРИСТАЛЛЫ § плотная упаковка решетки – из-за ненаправленности ионной связи (сферическая симметрия электростатического поля) § сухие кристаллы при низких температурах – диэлектрики (валентные электроны локализованы) § растворы и расплавы – электролиты (проводники второго рода)
 МЕТАЛЛИЧЕСКИЕ КРИСТАЛЛЫ § в узлах решётки – катионы металлов, связь между которыми осуществляют свободные электроны (электронный газ) § металлическая связь не имеет направленности и насыщаемости (подобно ионной) § плотная упаковка § высокая электропроводность § высокая теплопроводность
МЕТАЛЛИЧЕСКИЕ КРИСТАЛЛЫ § в узлах решётки – катионы металлов, связь между которыми осуществляют свободные электроны (электронный газ) § металлическая связь не имеет направленности и насыщаемости (подобно ионной) § плотная упаковка § высокая электропроводность § высокая теплопроводность
 МЕТАЛЛИЧЕСКИЕ КРИСТАЛЛЫ § пластичность (ковкость) § энергия связи – и, соответственно, температура плавления, твердость – может варьироваться в широких пределах: Тпл(W) = 3420 C, Тпл(Fe) = 1539 C, Тпл(Al) = 660 C, Тпл(Cs) = 28 C, Тпл(Hg) = – 39 C
МЕТАЛЛИЧЕСКИЕ КРИСТАЛЛЫ § пластичность (ковкость) § энергия связи – и, соответственно, температура плавления, твердость – может варьироваться в широких пределах: Тпл(W) = 3420 C, Тпл(Fe) = 1539 C, Тпл(Al) = 660 C, Тпл(Cs) = 28 C, Тпл(Hg) = – 39 C
 МОЛЕКУЛЯРНЫЕ КРИСТАЛЛЫ § структурные единицы в узлах – молекулы, слабосвязанные между собой (водородные связи, силы Ван-дер-Ваальса) § малая твердость § низкая температура плавления § высокая летучесть, способность к сублимации (возгонке) § малая электропроводность (преимущественно диэлектрики) § типичные представители: вода (лёд), СО 2 ( «сухой лёд» ), йод и др. галогены, углеводороды
МОЛЕКУЛЯРНЫЕ КРИСТАЛЛЫ § структурные единицы в узлах – молекулы, слабосвязанные между собой (водородные связи, силы Ван-дер-Ваальса) § малая твердость § низкая температура плавления § высокая летучесть, способность к сублимации (возгонке) § малая электропроводность (преимущественно диэлектрики) § типичные представители: вода (лёд), СО 2 ( «сухой лёд» ), йод и др. галогены, углеводороды
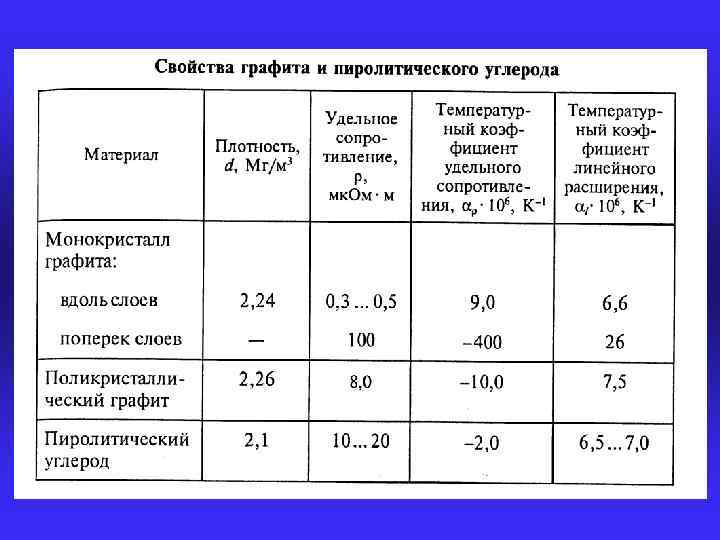
 КРИСТАЛЛЫ СО СМЕШАННЫМИ СВЯЗЯМИ § структурные единицы в различных направлениях связаны между собой химическими связями различного типа § характерна сильная анизотропия свойств § типичный представитель – графит
КРИСТАЛЛЫ СО СМЕШАННЫМИ СВЯЗЯМИ § структурные единицы в различных направлениях связаны между собой химическими связями различного типа § характерна сильная анизотропия свойств § типичный представитель – графит
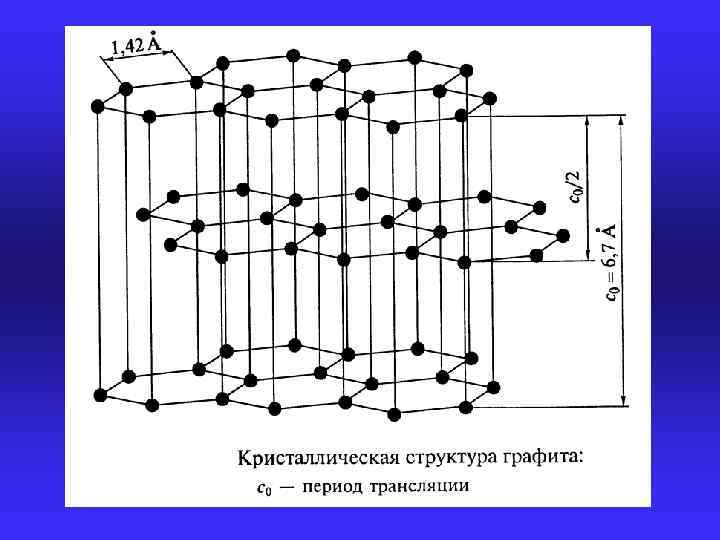
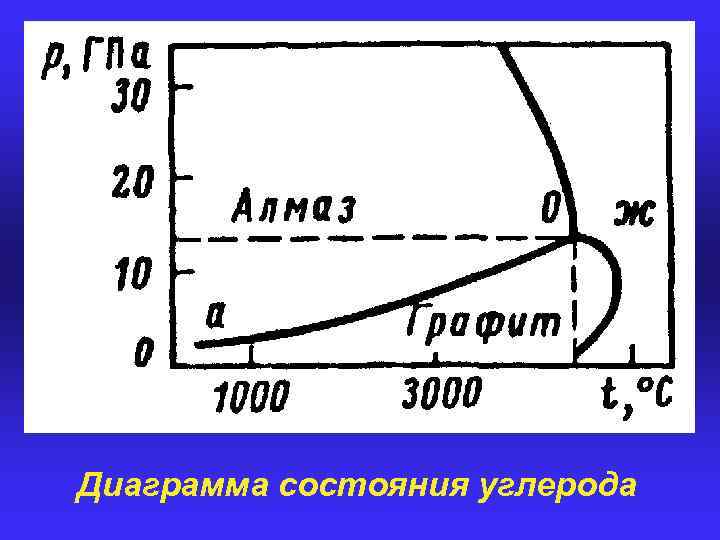 Диаграмма состояния углерода
Диаграмма состояния углерода