Радиохимия. Плутоний (2015).ppt
- Количество слайдов: 46
 Химия плутония Ядерные свойства и получение q Химические свойства q Плутоний в растворах q Аналитическая химия: методы очистки, выделения и идентификации q Свечение блока 238 Pu. O 2 (Самонагрев)
Химия плутония Ядерные свойства и получение q Химические свойства q Плутоний в растворах q Аналитическая химия: методы очистки, выделения и идентификации q Свечение блока 238 Pu. O 2 (Самонагрев)
 Ядерные свойства n Изотопы 228≤A≤ 247 200 т – гражданский плутоний 250 т – оружейный плутоний 70 -75 т/год
Ядерные свойства n Изотопы 228≤A≤ 247 200 т – гражданский плутоний 250 т – оружейный плутоний 70 -75 т/год
 Ядерные свойства q q q 238 Pu - исторически первый открытый изотоп Не делится тепловыми нейтронами Поперечное сечение захвата тепловых нейтронов σ= 5⋅10 -26 м 2 237 Np(n, )238 Np q q Бета-распад 238 Np Разделение Pu и Np – ионный обмен Распад 242 Cm 238 U(α, 4 n)238 Pu; 235 U(α, p)238 Np→ 238 Pu n Применяется как источник тока в космической технике и в медицине.
Ядерные свойства q q q 238 Pu - исторически первый открытый изотоп Не делится тепловыми нейтронами Поперечное сечение захвата тепловых нейтронов σ= 5⋅10 -26 м 2 237 Np(n, )238 Np q q Бета-распад 238 Np Разделение Pu и Np – ионный обмен Распад 242 Cm 238 U(α, 4 n)238 Pu; 235 U(α, p)238 Np→ 238 Pu n Применяется как источник тока в космической технике и в медицине.
 n n 239 Pu Ядерные свойства – практически самый важный Сечение деления тепловыми нейтронами - 738 барн Единственный изотоп, используемый в атомном оружии. Взрыв 1 кг плутония равен взрыву 20000 тонн тротила. Может образовываться в урановых рудах n (n, ) реакция q Нейтроны в результате спонтанного деления U и под действием -частиц на входящие в состав урановой руды элементы q Содержание в рудах 0, 4 -15 частей на 1012 частей урана
n n 239 Pu Ядерные свойства – практически самый важный Сечение деления тепловыми нейтронами - 738 барн Единственный изотоп, используемый в атомном оружии. Взрыв 1 кг плутония равен взрыву 20000 тонн тротила. Может образовываться в урановых рудах n (n, ) реакция q Нейтроны в результате спонтанного деления U и под действием -частиц на входящие в состав урановой руды элементы q Содержание в рудах 0, 4 -15 частей на 1012 частей урана
 Ядерные свойства 236 Pu q q Используют для изучения метаболизма плутония в организме и в радиоэкологических исследованиях. q 240 Pu q 241 Pu q -излучатель (241 Am) q 242 Pu Редко захватывает нейтроны и «выгорает» в реакторе медленнее остальных изотопов q
Ядерные свойства 236 Pu q q Используют для изучения метаболизма плутония в организме и в радиоэкологических исследованиях. q 240 Pu q 241 Pu q -излучатель (241 Am) q 242 Pu Редко захватывает нейтроны и «выгорает» в реакторе медленнее остальных изотопов q
![Металл n Строение электронной оболочки [Rn]5 f 67 s 2 n Восстановление Ca q Металл n Строение электронной оболочки [Rn]5 f 67 s 2 n Восстановление Ca q](https://present5.com/presentation/3/-73373343_392306372.pdf-img/-73373343_392306372.pdf-6.jpg) Металл n Строение электронной оболочки [Rn]5 f 67 s 2 n Восстановление Ca q Pu. F 4 и Ca q Прямое восстановление оксида n Pu. O 2, Ca и Ca. Cl 2 n Электрорафинирование q 740 ºC в Na. Cl/KCl с Mg. Cl 2 (окислитель) n Окисление до Pu(III) - анод n Увеличение тока – восстановление Pu(III) на катоде
Металл n Строение электронной оболочки [Rn]5 f 67 s 2 n Восстановление Ca q Pu. F 4 и Ca q Прямое восстановление оксида n Pu. O 2, Ca и Ca. Cl 2 n Электрорафинирование q 740 ºC в Na. Cl/KCl с Mg. Cl 2 (окислитель) n Окисление до Pu(III) - анод n Увеличение тока – восстановление Pu(III) на катоде
 Металл n n n 6 аллотропных модификаций q 7 ая – при повышенном давлении Энергии аллотропных модификаций близки q Pu чувствителен к изменению температуры, давлению Плотности существенно отличаются q значительные изменения объемов при фазовых переходах ( -максимально плотная, Pu – 6 по плотности после Os, Ir, Pt, Re, Np) Pu расширятся при затвердевании из расплава Температура плавления – 640 C Жидкий Pu – очень большое поверхностное натяжение при высокой вязкости
Металл n n n 6 аллотропных модификаций q 7 ая – при повышенном давлении Энергии аллотропных модификаций близки q Pu чувствителен к изменению температуры, давлению Плотности существенно отличаются q значительные изменения объемов при фазовых переходах ( -максимально плотная, Pu – 6 по плотности после Os, Ir, Pt, Re, Np) Pu расширятся при затвердевании из расплава Температура плавления – 640 C Жидкий Pu – очень большое поверхностное натяжение при высокой вязкости
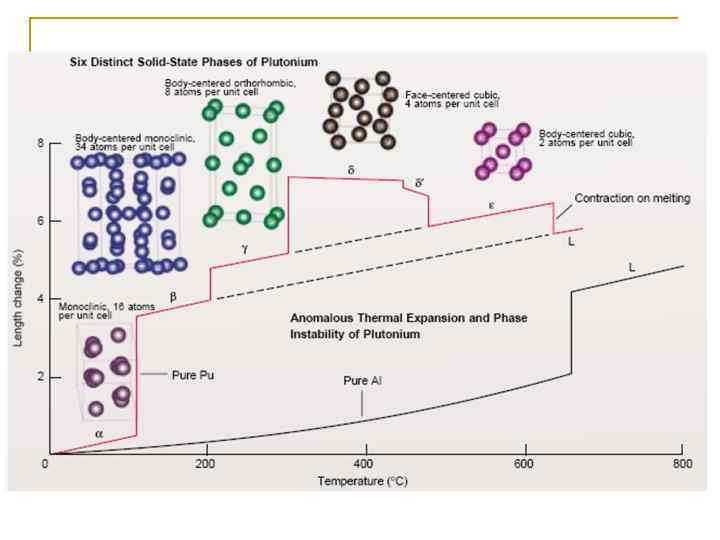
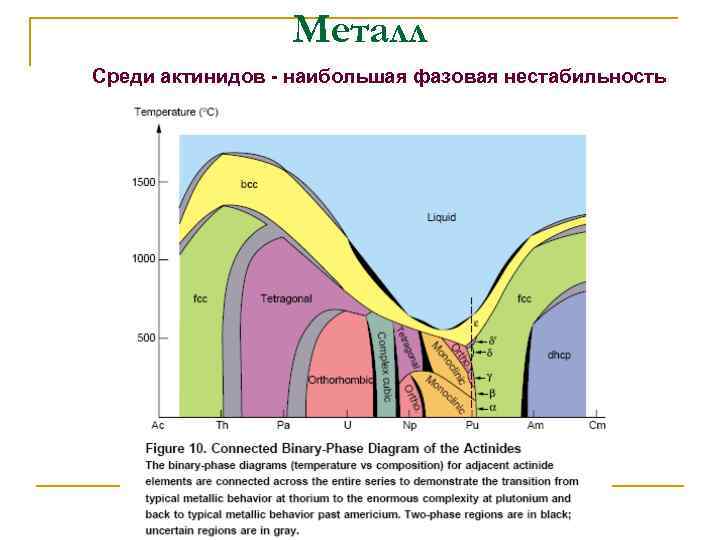 Металл Среди актинидов - наибольшая фазовая нестабильность
Металл Среди актинидов - наибольшая фазовая нестабильность
 Металл n n n Металл пирофорен Образование оксидной пленки q Может включать различные оксиды q Медленное окисление в сухом воздухе n Скорость существенно возрастает в присутствии воды Pu 2 O 3 образуется в отсутствии или низкой концентрации O 2 Гидрид Pu (Pu. Hx, где 1. 9 < x < 3) увеличивает скорость окисления до 1013 Pu. O 2+x - в присутствии воды
Металл n n n Металл пирофорен Образование оксидной пленки q Может включать различные оксиды q Медленное окисление в сухом воздухе n Скорость существенно возрастает в присутствии воды Pu 2 O 3 образуется в отсутствии или низкой концентрации O 2 Гидрид Pu (Pu. Hx, где 1. 9 < x < 3) увеличивает скорость окисления до 1013 Pu. O 2+x - в присутствии воды
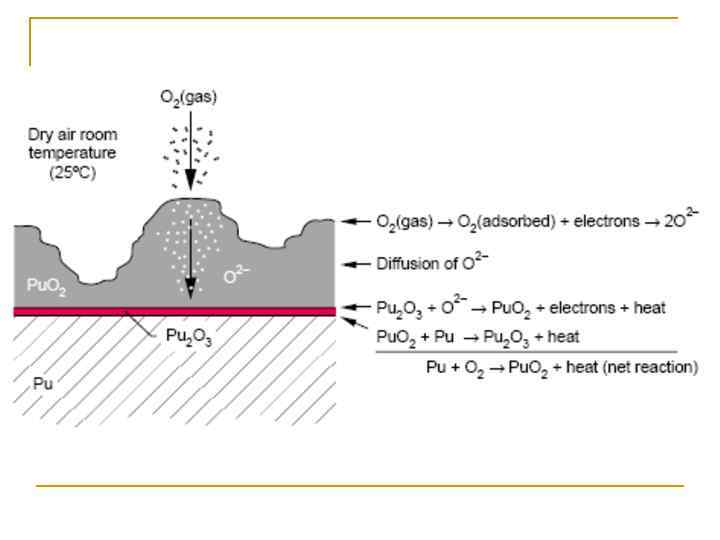
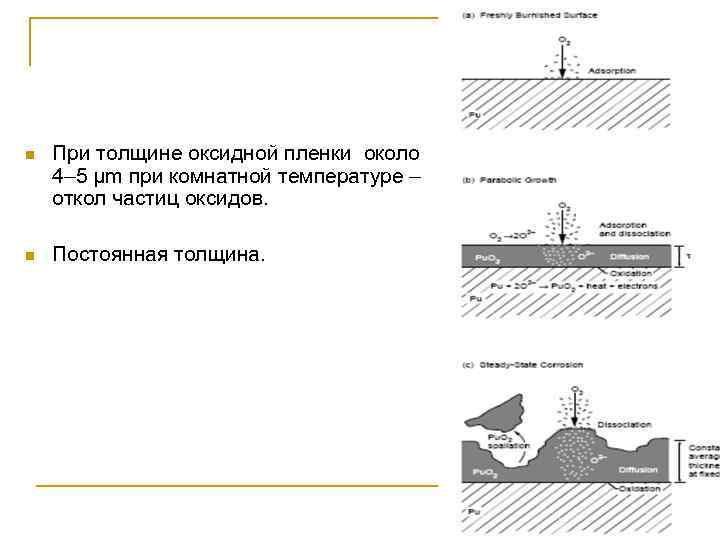 n При толщине оксидной пленки около 4– 5 μm при комнатной температуре – откол частиц оксидов. n Постоянная толщина.
n При толщине оксидной пленки около 4– 5 μm при комнатной температуре – откол частиц оксидов. n Постоянная толщина.
 Гидриды n Pu с H 2 q Гомогенная смесь Pu. H 2 и Pu. H 3 q Область составов Pu. Hx 2 - 2. 7 (кубическая решетка) – наиболее типична q Pu. H 2 более устойчив, чем Pu. H 3 q Pu. H 2 - исходное вещество для синтеза других соединений Pu q Аналогичные дейтериды менее устойчивы
Гидриды n Pu с H 2 q Гомогенная смесь Pu. H 2 и Pu. H 3 q Область составов Pu. Hx 2 - 2. 7 (кубическая решетка) – наиболее типична q Pu. H 2 более устойчив, чем Pu. H 3 q Pu. H 2 - исходное вещество для синтеза других соединений Pu q Аналогичные дейтериды менее устойчивы
 Бориды n Pu. Bx x= 2, 4, 6, 12, 66 n Получение q n n Вакуум, 900 °C и 1200 °C Гидрид Pu – исходное вещество Структура q Преобладание B-B связей n n Подобны боридам большинства металлов Pu занимает вакантные места
Бориды n Pu. Bx x= 2, 4, 6, 12, 66 n Получение q n n Вакуум, 900 °C и 1200 °C Гидрид Pu – исходное вещество Структура q Преобладание B-B связей n n Подобны боридам большинства металлов Pu занимает вакантные места
 Карбиды n Pu 3 C 2, Pu. C 1 -x, Pu 2 C 3 и Pu. C 2 q n Pu. C: Pu. C 0. 6 до Pu. C 0. 92 Получение q При высоких температурах с C: n Металлический Pu n Гидриды Pu n Оксиды Pu n Pu. C 1 -x из Pu. H 2 и Pu 2 C 3 при 700 °C q Конечный состав зависит от температуры, атмосферы (вакуум, Ar) и времени
Карбиды n Pu 3 C 2, Pu. C 1 -x, Pu 2 C 3 и Pu. C 2 q n Pu. C: Pu. C 0. 6 до Pu. C 0. 92 Получение q При высоких температурах с C: n Металлический Pu n Гидриды Pu n Оксиды Pu n Pu. C 1 -x из Pu. H 2 и Pu 2 C 3 при 700 °C q Конечный состав зависит от температуры, атмосферы (вакуум, Ar) и времени
 Карбиды q q Pu. C 1 -x окисляется на воздухе при 200 °C Взаимодействует с N 2 n Pu. N при 1400 °C q q n Pu 2 C 3 подобен Pu. C 1 -x Все карбиды растворяются в смеси HNO 3 -HF Образование смешанных карбидов q Pu-U-C n q M 3 C 2, MC 1 -x, M 2 C 3 MC 2 Pu-Th-C
Карбиды q q Pu. C 1 -x окисляется на воздухе при 200 °C Взаимодействует с N 2 n Pu. N при 1400 °C q q n Pu 2 C 3 подобен Pu. C 1 -x Все карбиды растворяются в смеси HNO 3 -HF Образование смешанных карбидов q Pu-U-C n q M 3 C 2, MC 1 -x, M 2 C 3 MC 2 Pu-Th-C
 Силициды 5 Pu-Si соединений q q n Получение q n 5: 3, 3: 2, 1: 1, 3: 5 и 1: 2 (Pu: Si) Наибольшая температура плавления у 3: 5 силицида 1646 °C 1200 °C, вакуум: 4 Pu. F 3 + (3+4 x)Si 4 Pu. Six + 3 Si. F 4 q Pu. O 2 с Si или Si. C при 1400 °C в вакууме Свойства q q Металлический блеск Пирофорны Окисляются на воздухе до Pu. O 2 Взаимодействуют с водой
Силициды 5 Pu-Si соединений q q n Получение q n 5: 3, 3: 2, 1: 1, 3: 5 и 1: 2 (Pu: Si) Наибольшая температура плавления у 3: 5 силицида 1646 °C 1200 °C, вакуум: 4 Pu. F 3 + (3+4 x)Si 4 Pu. Six + 3 Si. F 4 q Pu. O 2 с Si или Si. C при 1400 °C в вакууме Свойства q q Металлический блеск Пирофорны Окисляются на воздухе до Pu. O 2 Взаимодействуют с водой
 Нитриды Только Pu. N достоверно известен q q Получение n Гидрид Pu с N 2 при температурах от 500 °C до 1000 °C n Реакция в жидком аммиаке q Pu. I 3 + NH 3 + 3 Na Pu. N + 3 Na. I + 1. 5 H 2 Свойства §Высокая температура плавления(2830 °C) §Взаимодействует с O 2 при 200 °C §Растворяется в кислотах (быстро в HNO 3)
Нитриды Только Pu. N достоверно известен q q Получение n Гидрид Pu с N 2 при температурах от 500 °C до 1000 °C n Реакция в жидком аммиаке q Pu. I 3 + NH 3 + 3 Na Pu. N + 3 Na. I + 1. 5 H 2 Свойства §Высокая температура плавления(2830 °C) §Взаимодействует с O 2 при 200 °C §Растворяется в кислотах (быстро в HNO 3)
 Pu с P, As, Sb, S, Se, Te n Pu. P, Pu. As и Pu. Sb (Pu 4 Sb 3) n S, Se, Te: Pu. X, Pu 2 X 3, Pu. X 2 -x q Pu. Te 3 n n n q Pu. S: цвет золота Pu. Se: цвет меди Pu. Te: черный Полупроводники
Pu с P, As, Sb, S, Se, Te n Pu. P, Pu. As и Pu. Sb (Pu 4 Sb 3) n S, Se, Te: Pu. X, Pu 2 X 3, Pu. X 2 -x q Pu. Te 3 n n n q Pu. S: цвет золота Pu. Se: цвет меди Pu. Te: черный Полупроводники
 Интерметаллические соединения n Соединения Со всеми металлами и металлоидами побочных подгрупп. n Металлы, отличающиеся от плутония атомными диаметрами не более чем на 15% способны образовать с ним твердые растворы. Zr, Hf, Та, Nb, Ti, W и Мо. n Сплавы Al, Be, Мn, Fe, Co и Ni Тройные сплавы (U-Рu-Мо, Рu-Се-Со и др. )
Интерметаллические соединения n Соединения Со всеми металлами и металлоидами побочных подгрупп. n Металлы, отличающиеся от плутония атомными диаметрами не более чем на 15% способны образовать с ним твердые растворы. Zr, Hf, Та, Nb, Ti, W и Мо. n Сплавы Al, Be, Мn, Fe, Co и Ni Тройные сплавы (U-Рu-Мо, Рu-Се-Со и др. )
 Оксиды n 3 оксида Pu q Pu. O Восстановление Pu. OCl или фторидов парами Ba q Pu 2 O 3 Pu. O 2+Pu 2 O 3 при 1500 °C 2 Pu. O 2+C Pu 2 O 3 + CO q Pu. O 2 Прокаливание на воздухе любых кислородных соединений Pu
Оксиды n 3 оксида Pu q Pu. O Восстановление Pu. OCl или фторидов парами Ba q Pu 2 O 3 Pu. O 2+Pu 2 O 3 при 1500 °C 2 Pu. O 2+C Pu 2 O 3 + CO q Pu. O 2 Прокаливание на воздухе любых кислородных соединений Pu
 Оксиды Прокаленный Pu. O 2 трудно растворим Для растворения используют 16 M HNO 3 и 1 M HF Полученный при низких температурах легко растворим в концентрированной азотной и серной кислотах При высокой температуре Pu. O 2 реагирует с графитом - карбид; с сероводородом - Pu 2 S 3
Оксиды Прокаленный Pu. O 2 трудно растворим Для растворения используют 16 M HNO 3 и 1 M HF Полученный при низких температурах легко растворим в концентрированной азотной и серной кислотах При высокой температуре Pu. O 2 реагирует с графитом - карбид; с сероводородом - Pu 2 S 3
 Оксоплутонаты щелочных металлов n n Из Pu. O 2 и оксидов, гидроксидов, карбонатов щелочных металлов Pu(IV) q Li 8 Pu. O 6 n Pu(V) q Li 7 Pu. O 6, Li 3 Pu. O 4, Na 3 Pu. O 4 n Pu(VI) q M 6 Pu. O 6, M 4 Pu. O 5 (Li, Na) q M 2 Pu. O 4 (K, Rb, Cs) n Pu(VII) q M 5 Pu. O 4 (Li, Na) q M 3 Pu. O 5 (Rb, Cs)
Оксоплутонаты щелочных металлов n n Из Pu. O 2 и оксидов, гидроксидов, карбонатов щелочных металлов Pu(IV) q Li 8 Pu. O 6 n Pu(V) q Li 7 Pu. O 6, Li 3 Pu. O 4, Na 3 Pu. O 4 n Pu(VI) q M 6 Pu. O 6, M 4 Pu. O 5 (Li, Na) q M 2 Pu. O 4 (K, Rb, Cs) n Pu(VII) q M 5 Pu. O 4 (Li, Na) q M 3 Pu. O 5 (Rb, Cs)
 Группа II n n Pu(III) q Ba. Pu 2 O 4 Pu(IV) q Только Sr и Ba q MPu. O 3 Pu(V) q Ba 3 Pu. O 5. 5 Pu(VI) q MPu. O 4, M 3 Pu. O 6 (Ca, Sr и Ba) q Ba 2 MPu. O 6 (Sr, Pb, Mg, Ca) Структура n Перовскиты q Ca. Ti. O 3 (ABO 3) n Двойные перовскиты q (Ba, Sr)3 Pu. O 6 и Ba(Mg, Ca, Sr)Pu. O 6
Группа II n n Pu(III) q Ba. Pu 2 O 4 Pu(IV) q Только Sr и Ba q MPu. O 3 Pu(V) q Ba 3 Pu. O 5. 5 Pu(VI) q MPu. O 4, M 3 Pu. O 6 (Ca, Sr и Ba) q Ba 2 MPu. O 6 (Sr, Pb, Mg, Ca) Структура n Перовскиты q Ca. Ti. O 3 (ABO 3) n Двойные перовскиты q (Ba, Sr)3 Pu. O 6 и Ba(Mg, Ca, Sr)Pu. O 6
 Соединения с галогенами n Pu. Xn (3, 4, 6) q q n Pu. F 4 – твердое вещество, Pu. Cl 4 обнаруживается в газовой фазе Pu. F 6 летуч Оксогалогениды q Pu. OX Pu. OF 3, Pu. OF 4, Pu. O 2 F 2 Галогенплутонаты n Mx. Pu. F 4+x q q x = 1, 2, 3, 4 M 7 Pu 6 F 31 и MPu. F 6
Соединения с галогенами n Pu. Xn (3, 4, 6) q q n Pu. F 4 – твердое вещество, Pu. Cl 4 обнаруживается в газовой фазе Pu. F 6 летуч Оксогалогениды q Pu. OX Pu. OF 3, Pu. OF 4, Pu. O 2 F 2 Галогенплутонаты n Mx. Pu. F 4+x q q x = 1, 2, 3, 4 M 7 Pu 6 F 31 и MPu. F 6
 Фториды n n 2 Pu. O 2 + H 2 + 6 HF 2 Pu. F 3 + 4 H 2 O при 600 °C Pu 2(C 2 O 4)3 + 6 HF 2 Pu. F 3 + 3 CO 2 + 3 H 2 O при 600 °C q При низких температурах (до 150 °C) образуются Pu(OH)2 F 2 или Pu(OH)F 3 § Pu. O 2 + 3 F 2 Pu. F 6 + O 2 при 300 °C § Pu. F 4 + F 2 Pu. F 6 при 300 °C
Фториды n n 2 Pu. O 2 + H 2 + 6 HF 2 Pu. F 3 + 4 H 2 O при 600 °C Pu 2(C 2 O 4)3 + 6 HF 2 Pu. F 3 + 3 CO 2 + 3 H 2 O при 600 °C q При низких температурах (до 150 °C) образуются Pu(OH)2 F 2 или Pu(OH)F 3 § Pu. O 2 + 3 F 2 Pu. F 6 + O 2 при 300 °C § Pu. F 4 + F 2 Pu. F 6 при 300 °C
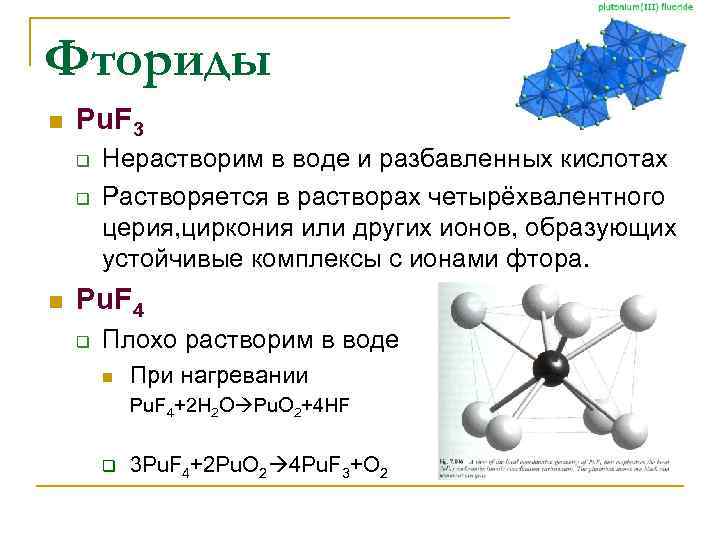 Фториды n Pu. F 3 q q n Нерастворим в воде и разбавленных кислотах Растворяется в растворах четырёхвалентного церия, циркония или других ионов, образующих устойчивые комплексы с ионами фтора. Pu. F 4 q Плохо растворим в воде n При нагревании Pu. F 4+2 H 2 O Pu. O 2+4 HF q 3 Pu. F 4+2 Pu. O 2 4 Pu. F 3+O 2
Фториды n Pu. F 3 q q n Нерастворим в воде и разбавленных кислотах Растворяется в растворах четырёхвалентного церия, циркония или других ионов, образующих устойчивые комплексы с ионами фтора. Pu. F 4 q Плохо растворим в воде n При нагревании Pu. F 4+2 H 2 O Pu. O 2+4 HF q 3 Pu. F 4+2 Pu. O 2 4 Pu. F 3+O 2
 Фториды n q q q Pu. F 6 Пары окрашены подобно NO 2. Менее летуч, чем UF 6 и Np. F 6 Pu. F 4+F 2 Сильный фторирующий агент и окислитель Бурно реагирует с водой - Pu. O 2 и Pu. F 4. Твердый Pu. F 6 самопроизвольно разлагается вследствие α-излучения плутония. n q Механизм не ясен Хранят в газовой фазе при пониженном давлении
Фториды n q q q Pu. F 6 Пары окрашены подобно NO 2. Менее летуч, чем UF 6 и Np. F 6 Pu. F 4+F 2 Сильный фторирующий агент и окислитель Бурно реагирует с водой - Pu. O 2 и Pu. F 4. Твердый Pu. F 6 самопроизвольно разлагается вследствие α-излучения плутония. n q Механизм не ясен Хранят в газовой фазе при пониженном давлении
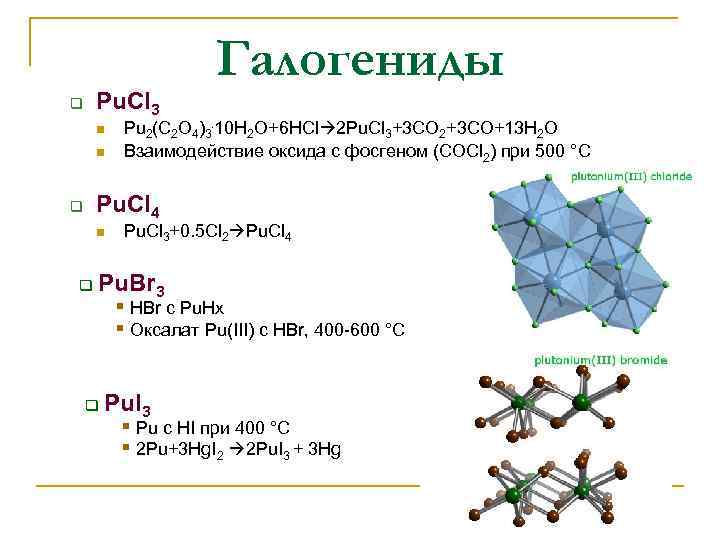 Pu. Cl 3 q n n Галогениды Pu 2(C 2 O 4)3. 10 H 2 O+6 HCl 2 Pu. Cl 3+3 CO 2+3 CO+13 H 2 O Взаимодействие оксида с фосгеном (COCl 2) при 500 °C Pu. Cl 4 q n q Pu. Cl 3+0. 5 Cl 2 Pu. Cl 4 Pu. Br 3 § HBr с Pu. Hx § Оксалат Pu(III) с HBr, 400 -600 °C q Pu. I 3 § Pu с HI при 400 °C § 2 Pu+3 Hg. I 2 2 Pu. I 3 + 3 Hg
Pu. Cl 3 q n n Галогениды Pu 2(C 2 O 4)3. 10 H 2 O+6 HCl 2 Pu. Cl 3+3 CO 2+3 CO+13 H 2 O Взаимодействие оксида с фосгеном (COCl 2) при 500 °C Pu. Cl 4 q n q Pu. Cl 3+0. 5 Cl 2 Pu. Cl 4 Pu. Br 3 § HBr с Pu. Hx § Оксалат Pu(III) с HBr, 400 -600 °C q Pu. I 3 § Pu с HI при 400 °C § 2 Pu+3 Hg. I 2 2 Pu. I 3 + 3 Hg
 Оксогалогениды, галогенплутонаты n Оксогалогениды q q Pu. OX: Pu. X 3 и вода Pu(VI) n Избыток Pu. F 6 с водой и HF q Pu. O 2 F 2 n Pu. O 2 Cl 2 n Галогенплутонаты q q n n n Галогениды Pu(III-VI) с группами 1, 2 и некоторыми переходными металлами Получение Галогениды металлов и Pu. F 4 при 300 -600 °C в среде HF Pu. F 6 или Pu. F 4 со фторидами 1 или 2
Оксогалогениды, галогенплутонаты n Оксогалогениды q q Pu. OX: Pu. X 3 и вода Pu(VI) n Избыток Pu. F 6 с водой и HF q Pu. O 2 F 2 n Pu. O 2 Cl 2 n Галогенплутонаты q q n n n Галогениды Pu(III-VI) с группами 1, 2 и некоторыми переходными металлами Получение Галогениды металлов и Pu. F 4 при 300 -600 °C в среде HF Pu. F 6 или Pu. F 4 со фторидами 1 или 2
 Плутоний в растворах
Плутоний в растворах
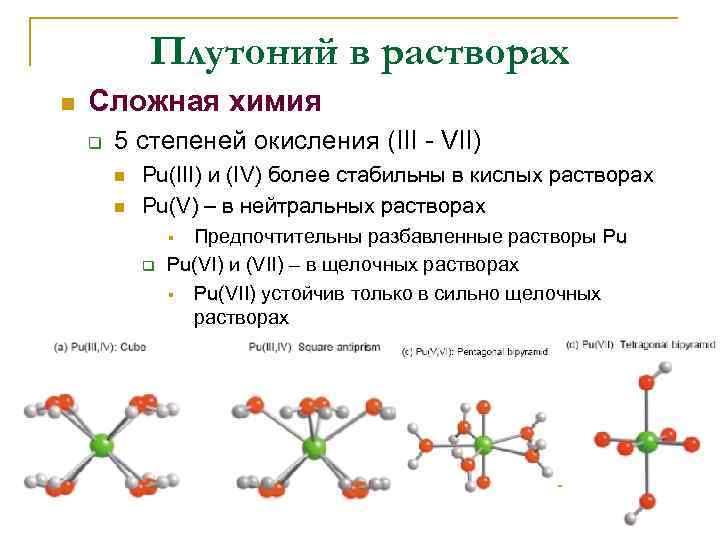 Плутоний в растворах n Сложная химия q 5 степеней окисления (III - VII) n n Pu(III) и (IV) более стабильны в кислых растворах Pu(V) – в нейтральных растворах Предпочтительны разбавленные растворы Pu Pu(VI) и (VII) – в щелочных растворах § Pu(VII) устойчив только в сильно щелочных растворах § q
Плутоний в растворах n Сложная химия q 5 степеней окисления (III - VII) n n Pu(III) и (IV) более стабильны в кислых растворах Pu(V) – в нейтральных растворах Предпочтительны разбавленные растворы Pu Pu(VI) и (VII) – в щелочных растворах § Pu(VII) устойчив только в сильно щелочных растворах § q
 Плутоний в растворах n n Гидратированные катионы Pu 3+ и Pu 4+ Плутонил и плутоноил-ионы Pu. O 22+ и Pu. O 2+ q Pu(V): эффективный заряд 2. 2 q Pu(VI): 3. 2 Pu. O 4 Координационное число 8 -10 1 М НСl 1 М НNO 3
Плутоний в растворах n n Гидратированные катионы Pu 3+ и Pu 4+ Плутонил и плутоноил-ионы Pu. O 22+ и Pu. O 2+ q Pu(V): эффективный заряд 2. 2 q Pu(VI): 3. 2 Pu. O 4 Координационное число 8 -10 1 М НСl 1 М НNO 3
 Плутоний в растворах n n n Диспропорционирование q 3 Pu 4++2 H 2 O 2 Pu 3++Pu. O 22++4 H+ q 3 Pu. O 2++4 H+ Pu 3++2 Pu. O 22++2 H 2 O Концентрация Pu Ионная сила p. H Легко обратимы Pu 4+ / Pu 3+ и Pu. O 22+ /Pu. O 2+ Избыток Pu Избыток гидразина
Плутоний в растворах n n n Диспропорционирование q 3 Pu 4++2 H 2 O 2 Pu 3++Pu. O 22++4 H+ q 3 Pu. O 2++4 H+ Pu 3++2 Pu. O 22++2 H 2 O Концентрация Pu Ионная сила p. H Легко обратимы Pu 4+ / Pu 3+ и Pu. O 22+ /Pu. O 2+ Избыток Pu Избыток гидразина
 Плутоний в растворах n Aвторадиолиз q q Образование Н 2 и Н 2 О 2, радикалов Н, ОН, НО 2 ОВ реакции Восстановление плутония продуктами радиолиза. В растворах Pu(VI) с кислотностью 0. 2 М Pu(V), при более высоких концентрациях Pu(IV), при выдерживании - Pu(III).
Плутоний в растворах n Aвторадиолиз q q Образование Н 2 и Н 2 О 2, радикалов Н, ОН, НО 2 ОВ реакции Восстановление плутония продуктами радиолиза. В растворах Pu(VI) с кислотностью 0. 2 М Pu(V), при более высоких концентрациях Pu(IV), при выдерживании - Pu(III).
 Гидролиз n Размер и заряд q Меньшие ионы одинакового заряда – больше гидролиз n Для тетравалентных актинидов q Pu>Np>U>Pa>Th Склонность к коллоидообразованию Pu(IV)
Гидролиз n Размер и заряд q Меньшие ионы одинакового заряда – больше гидролиз n Для тетравалентных актинидов q Pu>Np>U>Pa>Th Склонность к коллоидообразованию Pu(IV)
 Плутоний в растворах n Комплексообразование q Pu(IV)>Pu(VI)≈Pu(III)>Pu(V) q Комплексы Pu Cl. O 4 -
Плутоний в растворах n Комплексообразование q Pu(IV)>Pu(VI)≈Pu(III)>Pu(V) q Комплексы Pu Cl. O 4 -
 Плутоний в растворах n Нитраты q q q Комплексы Pu важное значение в переработке и очистке Pu(III) неустойчивы Pu(IV) n q q q Pu(NO 3)n 4 -n, n=1 -6 Pu(NO 3)62 Для Pu(IV): пента или гексанитрокомплекс? Смешанные комплексы n TБФ, амиды Нитратных комплексов Pu(V) не обнаружено Известен мононитрат Pu(VI) в растворе n Pu. O 2(NO 3)2. x. H 2 O; x=3, 6
Плутоний в растворах n Нитраты q q q Комплексы Pu важное значение в переработке и очистке Pu(III) неустойчивы Pu(IV) n q q q Pu(NO 3)n 4 -n, n=1 -6 Pu(NO 3)62 Для Pu(IV): пента или гексанитрокомплекс? Смешанные комплексы n TБФ, амиды Нитратных комплексов Pu(V) не обнаружено Известен мононитрат Pu(VI) в растворе n Pu. O 2(NO 3)2. x. H 2 O; x=3, 6
![Плутоний в растворах Сульфаты q Pu(III) n q q [Pu(SO 4)4]5 - Pu(IV) n Плутоний в растворах Сульфаты q Pu(III) n q q [Pu(SO 4)4]5 - Pu(IV) n](https://present5.com/presentation/3/-73373343_392306372.pdf-img/-73373343_392306372.pdf-39.jpg) Плутоний в растворах Сульфаты q Pu(III) n q q [Pu(SO 4)4]5 - Pu(IV) n [Pu(SO 4)3]2 - n Галогениды q Pu(III) [Pu. Cl]2+ q Pu(IV) [Pu. F 3]+ [Pu. Cl 6]2 - q Pu(VI) [Pu. O 2 Cl]+, [Pu. O 2 F 3]n Фосфаты q q Pu(III) n [Pu(H 2 PO 4)n]3 -n n=1 -4 Pu(IV) n [Pu(HPO 4)n]4 -2 n n= 1, 2, 3, 4, 5 n Оксалаты q q Pu(IV) [Pu(C 2 O 4)n]3 -2 n Pu (V) [Pu. O 2 (C 2 O 4)]- и [Pu. O 2(C 2 O 4)2]3 -
Плутоний в растворах Сульфаты q Pu(III) n q q [Pu(SO 4)4]5 - Pu(IV) n [Pu(SO 4)3]2 - n Галогениды q Pu(III) [Pu. Cl]2+ q Pu(IV) [Pu. F 3]+ [Pu. Cl 6]2 - q Pu(VI) [Pu. O 2 Cl]+, [Pu. O 2 F 3]n Фосфаты q q Pu(III) n [Pu(H 2 PO 4)n]3 -n n=1 -4 Pu(IV) n [Pu(HPO 4)n]4 -2 n n= 1, 2, 3, 4, 5 n Оксалаты q q Pu(IV) [Pu(C 2 O 4)n]3 -2 n Pu (V) [Pu. O 2 (C 2 O 4)]- и [Pu. O 2(C 2 O 4)2]3 -
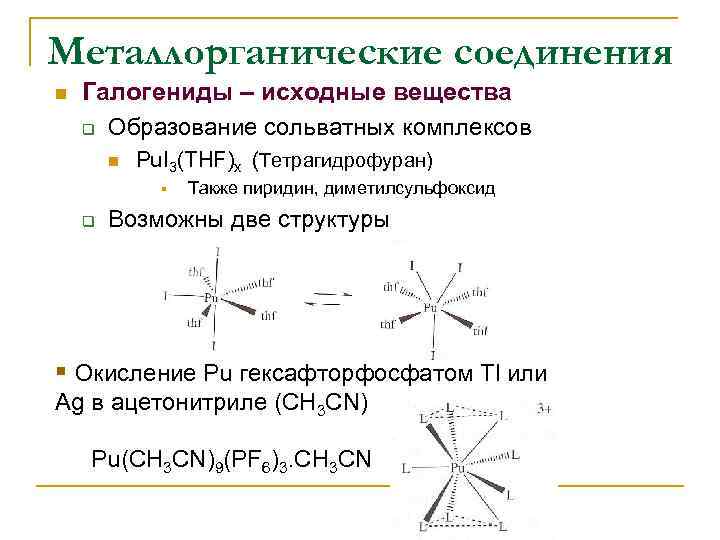 Металлорганические соединения n Галогениды – исходные вещества q Образование сольватных комплексов n Pu. I 3(THF)x (Тетрагидрофуран) § q Также пиридин, диметилсульфоксид Возможны две структуры § Окисление Pu гексафторфосфатом Tl или Ag в ацетонитриле (CH 3 CN) Pu(CH 3 CN)9(PF 6)3. CH 3 CN
Металлорганические соединения n Галогениды – исходные вещества q Образование сольватных комплексов n Pu. I 3(THF)x (Тетрагидрофуран) § q Также пиридин, диметилсульфоксид Возможны две структуры § Окисление Pu гексафторфосфатом Tl или Ag в ацетонитриле (CH 3 CN) Pu(CH 3 CN)9(PF 6)3. CH 3 CN
![Металлорганические соединения n Циклотетраены (C 8 H 8) q n [NEt 4]2 Pu. Cl Металлорганические соединения n Циклотетраены (C 8 H 8) q n [NEt 4]2 Pu. Cl](https://present5.com/presentation/3/-73373343_392306372.pdf-img/-73373343_392306372.pdf-41.jpg) Металлорганические соединения n Циклотетраены (C 8 H 8) q n [NEt 4]2 Pu. Cl 6 + 2 K 2 C 8 H 8 Pu(C 8 H 8)2+ 4 KCl + 2[NEt 4]Cl в тетрагидрофуране Циклопентадиенилы (C 5 H 5) q Pu. Cl 3 с (C 5 H 5)2 Be Реакция возможна с Na, Mg и Li Cp q Cs 2 Pu. Cl 6 + 3 Tl(C 5 H 5) в ацетонитриле
Металлорганические соединения n Циклотетраены (C 8 H 8) q n [NEt 4]2 Pu. Cl 6 + 2 K 2 C 8 H 8 Pu(C 8 H 8)2+ 4 KCl + 2[NEt 4]Cl в тетрагидрофуране Циклопентадиенилы (C 5 H 5) q Pu. Cl 3 с (C 5 H 5)2 Be Реакция возможна с Na, Mg и Li Cp q Cs 2 Pu. Cl 6 + 3 Tl(C 5 H 5) в ацетонитриле
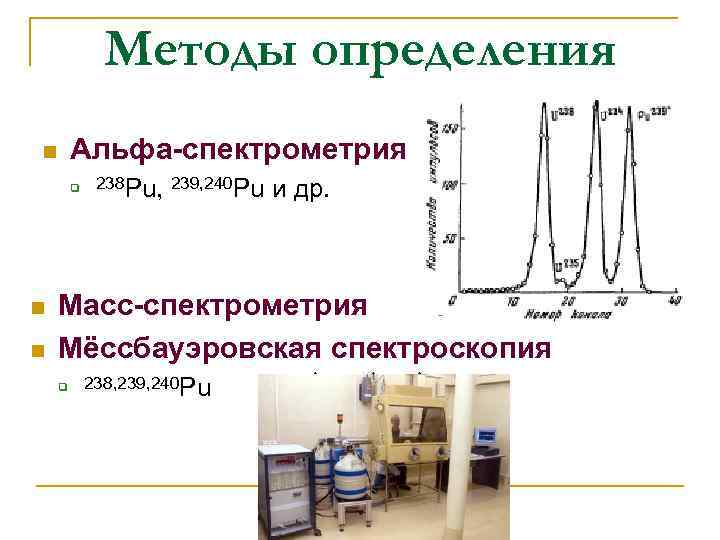 Методы определения Альфа-спектрометрия n q n n 238 Pu, 239, 240 Pu и др. Масс-спектрометрия Mëccбауэровская спектроскопия q 238, 239, 240 Pu
Методы определения Альфа-спектрометрия n q n n 238 Pu, 239, 240 Pu и др. Масс-спектрометрия Mëccбауэровская спектроскопия q 238, 239, 240 Pu
 Методы разделения q q n Водный (PUREX) Неводный (Пиропроцесинг) Осадительные методы q Соосаждение с фосфатом висмута n q n La. F 3– Pu (III, IV) Экстракционные методы q q n Bi. PO 4 в кислой среде – Pu (III, IV) Pu(V) < Pu(III) < Pu(VI) < Pu(IV) - экстрагируемость Основаны на растворимости нитратов плутония в различных органических растворителях. Ионный обмен q Катиониты и аниониты
Методы разделения q q n Водный (PUREX) Неводный (Пиропроцесинг) Осадительные методы q Соосаждение с фосфатом висмута n q n La. F 3– Pu (III, IV) Экстракционные методы q q n Bi. PO 4 в кислой среде – Pu (III, IV) Pu(V) < Pu(III) < Pu(VI) < Pu(IV) - экстрагируемость Основаны на растворимости нитратов плутония в различных органических растворителях. Ионный обмен q Катиониты и аниониты
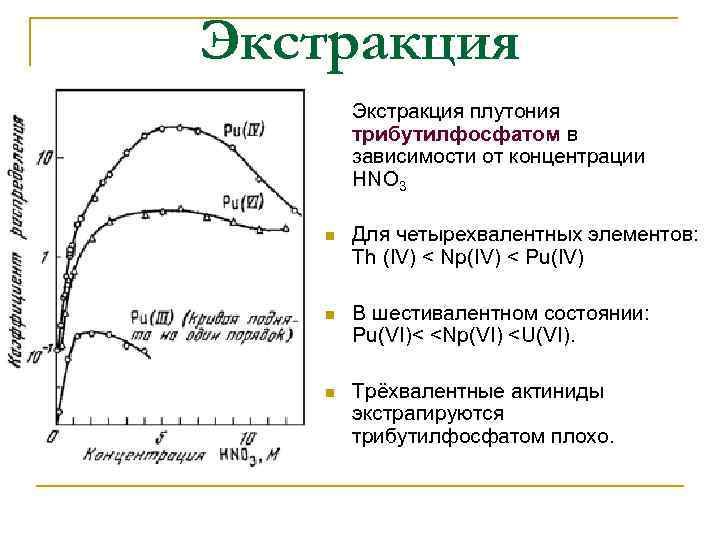 Экстракция плутония трибутилфосфатом в зависимости от концентрации HNO 3 n Для четырехвалентных элементов: Th (IV) < Np(IV) < Pu(IV) n В шестивалентном состоянии: Pu(VI)<
Экстракция плутония трибутилфосфатом в зависимости от концентрации HNO 3 n Для четырехвалентных элементов: Th (IV) < Np(IV) < Pu(IV) n В шестивалентном состоянии: Pu(VI)<
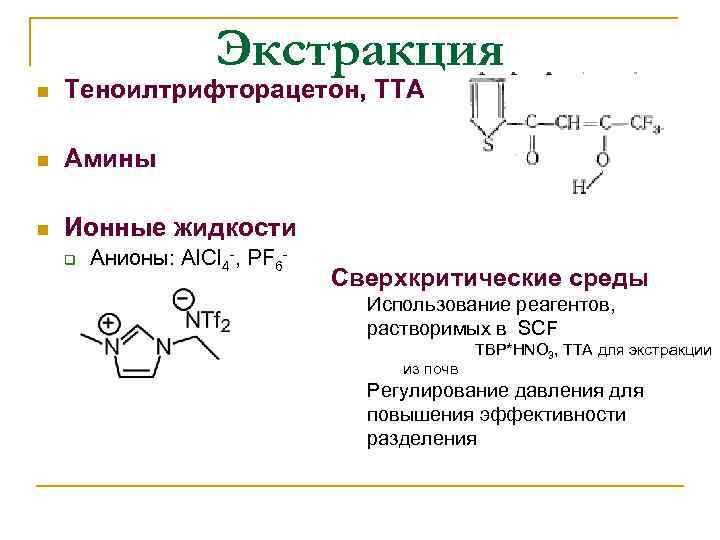 Экстракция n Теноилтрифторацетон, ТТА n Амины n Ионные жидкости q Анионы: Al. Cl 4 -, PF 6 - Сверхкритические среды Использование реагентов, растворимых в SCF из почв TBP*HNO 3, TTA для экстракции Регулирование давления для повышения эффективности разделения
Экстракция n Теноилтрифторацетон, ТТА n Амины n Ионные жидкости q Анионы: Al. Cl 4 -, PF 6 - Сверхкритические среды Использование реагентов, растворимых в SCF из почв TBP*HNO 3, TTA для экстракции Регулирование давления для повышения эффективности разделения
 Хроматография n Хроматография q q q Сорбция на анионите в 7 -8 M HNO 3 Pu 4+ в виде анионных комплексов из азотнокислых растворов Восстановительная десорбция Элюент - 0. 35 M HNO 3 + 0, 01 М НF На катионитах сорбция из разбавленных кислых растворов. Для десорбции часто применяют растворы комплексообразующих реагентов.
Хроматография n Хроматография q q q Сорбция на анионите в 7 -8 M HNO 3 Pu 4+ в виде анионных комплексов из азотнокислых растворов Восстановительная десорбция Элюент - 0. 35 M HNO 3 + 0, 01 М НF На катионитах сорбция из разбавленных кислых растворов. Для десорбции часто применяют растворы комплексообразующих реагентов.


