HOS_Lecture_2012_anl.ppt
- Количество слайдов: 178
 Химия окружающей среды Вторушина Анна Николаевна ТПУ - 2012
Химия окружающей среды Вторушина Анна Николаевна ТПУ - 2012
 Литература • Хентов В. Я. Химия окружающей среды для технических вузов : учебное пособие для втузов / В. Я. Хентов. — Ростов н/Дону : Феникс, 2005. — 144 с. • Голдовская Л. Ф. Химия окружающей среды : учебник / Л. Ф. Голдовская. — М. : Мир, 2007. — 296 с. • Ахмеджанов Р. Р. Химия окружающей среды : учебное пособие / Р. Р. Ахмеджанов ; Томский политехнический университет (ТПУ), Институт дистанционного образования (ИДО). — Томск : Изд-во ТПУ, 2007. — 108 с.
Литература • Хентов В. Я. Химия окружающей среды для технических вузов : учебное пособие для втузов / В. Я. Хентов. — Ростов н/Дону : Феникс, 2005. — 144 с. • Голдовская Л. Ф. Химия окружающей среды : учебник / Л. Ф. Голдовская. — М. : Мир, 2007. — 296 с. • Ахмеджанов Р. Р. Химия окружающей среды : учебное пособие / Р. Р. Ахмеджанов ; Томский политехнический университет (ТПУ), Институт дистанционного образования (ИДО). — Томск : Изд-во ТПУ, 2007. — 108 с.
 Литература • Чернобаев И. П. Химия окружающей среды : учебное пособие / И. П. Чернобаев. — Киев : Высшая школа, 1990. — 190 с. • Гусакова, Н. В. Химия окружающей среды : учебное пособие для вузов / Н. В. Гусакова. — Ростов-на-Дону : Феникс, 2004 . — 192 с. • Химия окружающей среды : учебное пособие / под ред. Т. И. Хаханиной. — М. : Высшее образование, 2009. — 130 с.
Литература • Чернобаев И. П. Химия окружающей среды : учебное пособие / И. П. Чернобаев. — Киев : Высшая школа, 1990. — 190 с. • Гусакова, Н. В. Химия окружающей среды : учебное пособие для вузов / Н. В. Гусакова. — Ростов-на-Дону : Феникс, 2004 . — 192 с. • Химия окружающей среды : учебное пособие / под ред. Т. И. Хаханиной. — М. : Высшее образование, 2009. — 130 с.
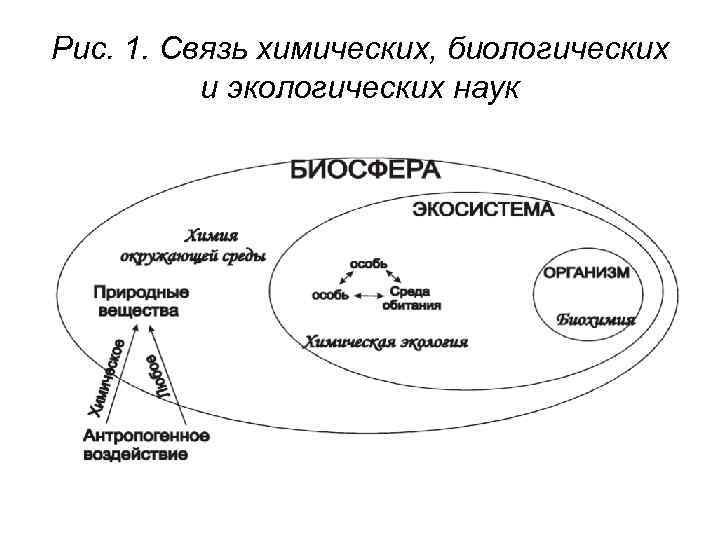 Рис. 1. Связь химических, биологических и экологических наук
Рис. 1. Связь химических, биологических и экологических наук
 • Аутоэкология - экология отдельных особей (внутривидовые взаимосвязи); • Синэкология - экология многовидовых сообществ (межвидовые взаимосвязи); • Демэкология – рассматривает динамику популяций; • Биогеоценология - учение об экологических системах. • Экосферология - изучает в планетарном масштабе сферу взаимодействия между современной биосферой и техносферой.
• Аутоэкология - экология отдельных особей (внутривидовые взаимосвязи); • Синэкология - экология многовидовых сообществ (межвидовые взаимосвязи); • Демэкология – рассматривает динамику популяций; • Биогеоценология - учение об экологических системах. • Экосферология - изучает в планетарном масштабе сферу взаимодействия между современной биосферой и техносферой.
 Биосфера. Строение, свойства, функции
Биосфера. Строение, свойства, функции
 Основные термины и определения • Биосфера – это своеобразная оболочка Земли, содержащая всю совокупность живых организмов и ту часть вещества планеты, которая находится в непрерывном обмене с этими организмами. • Биосфера - живые организмы и продукты их жизнедеятельности
Основные термины и определения • Биосфера – это своеобразная оболочка Земли, содержащая всю совокупность живых организмов и ту часть вещества планеты, которая находится в непрерывном обмене с этими организмами. • Биосфера - живые организмы и продукты их жизнедеятельности
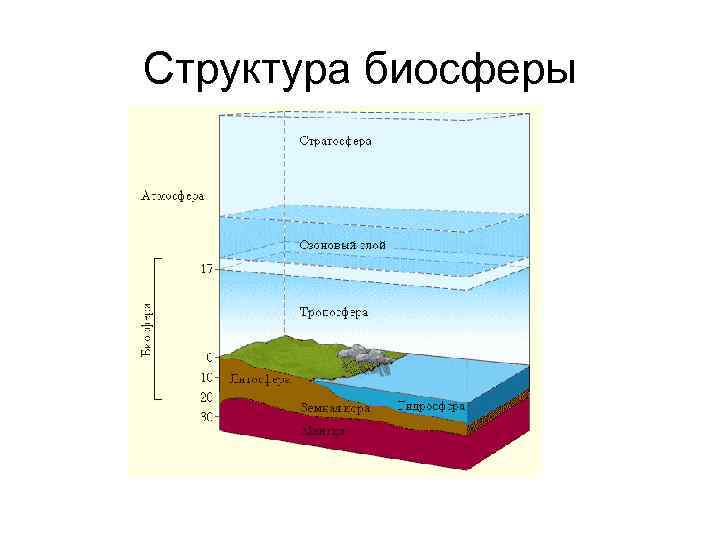 Структура биосферы
Структура биосферы
 Основные термины и определения • Экологические факторы – это определенные условия и элементы среды, которые оказывают специфическое воздействие на живой организм. • Экологическая система – взаимосвязанная, единая функциональная совокупность живых организмов и среды их обитания.
Основные термины и определения • Экологические факторы – это определенные условия и элементы среды, которые оказывают специфическое воздействие на живой организм. • Экологическая система – взаимосвязанная, единая функциональная совокупность живых организмов и среды их обитания.
 Основные термины и определения • Биотоп – это неорганическая, неживая среда с определенными физикохимическими условиями, например, температурой, влажностью, круговоротом веществ. • Живые существа, населяющие биотоп, образуют природное сообщество – БИОЦЕНОЗ.
Основные термины и определения • Биотоп – это неорганическая, неживая среда с определенными физикохимическими условиями, например, температурой, влажностью, круговоротом веществ. • Живые существа, населяющие биотоп, образуют природное сообщество – БИОЦЕНОЗ.
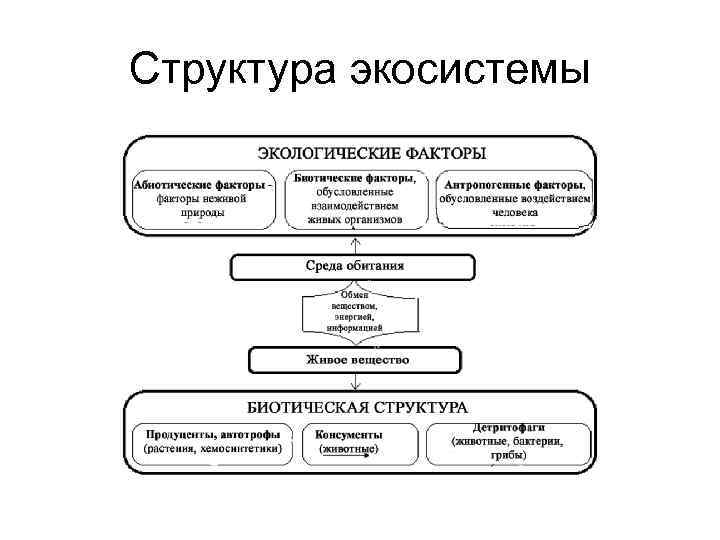 Структура экосистемы
Структура экосистемы
 • Биотическая структура экосистемы – это совокупность организмов различных категорий, пути взаимодействия их между собой и окружающей средой. • Автотрофы – организмы, синтезирующие органические вещества из неорганических соединений с использованием энергии Солнца. • Продуценты – комплексы автотрофных организмов, обеспечивающих органическими веществами, следовательно, и энергией все остальные организмы (растения и фотосинтезирующие бактерии).
• Биотическая структура экосистемы – это совокупность организмов различных категорий, пути взаимодействия их между собой и окружающей средой. • Автотрофы – организмы, синтезирующие органические вещества из неорганических соединений с использованием энергии Солнца. • Продуценты – комплексы автотрофных организмов, обеспечивающих органическими веществами, следовательно, и энергией все остальные организмы (растения и фотосинтезирующие бактерии).
 • Гетеротрофы – организмы, питающиеся готовыми органическими веществами. • Консументы – комплексы гетеротрофных организмов (животные, бесхлорофилльные растения). • Первичные консументы – животные, которые питаются непосредственно продуцентами (например, кролик ест морковку) – растительноядные. • Вторичные консументы – животные, которые питаются первичными консументами (лиса, питающаяся кроликом) – плотоядные.
• Гетеротрофы – организмы, питающиеся готовыми органическими веществами. • Консументы – комплексы гетеротрофных организмов (животные, бесхлорофилльные растения). • Первичные консументы – животные, которые питаются непосредственно продуцентами (например, кролик ест морковку) – растительноядные. • Вторичные консументы – животные, которые питаются первичными консументами (лиса, питающаяся кроликом) – плотоядные.
 • Редуценты или деструкторы – комплексы организмов, разлагающих органические соединения до минерального состояния (бактерии, грибы, простейшие – редуценты, а также организмы, которые питаются мертвыми органическими веществами – грифы, раки, муравьи – детритофаги). • Абиотическое окружение – весь комплекс неживой природы, откуда биоценоз черпает средства для существования и куда выделяет продукты обмена.
• Редуценты или деструкторы – комплексы организмов, разлагающих органические соединения до минерального состояния (бактерии, грибы, простейшие – редуценты, а также организмы, которые питаются мертвыми органическими веществами – грифы, раки, муравьи – детритофаги). • Абиотическое окружение – весь комплекс неживой природы, откуда биоценоз черпает средства для существования и куда выделяет продукты обмена.
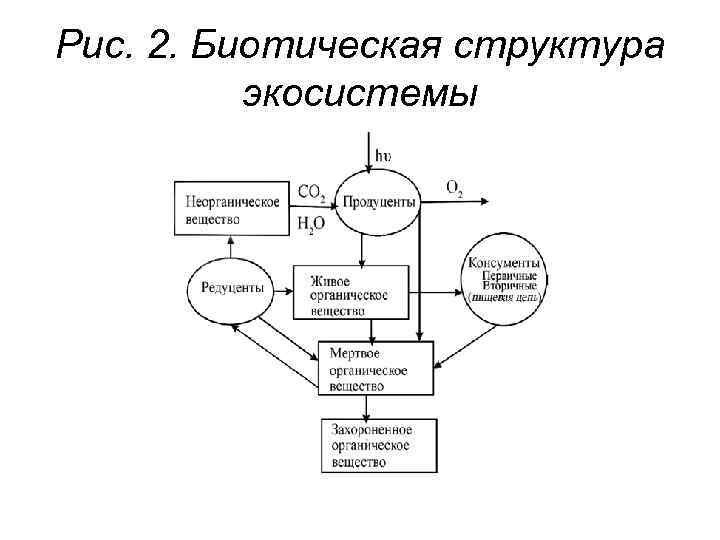 Рис. 2. Биотическая структура экосистемы
Рис. 2. Биотическая структура экосистемы
 • Биологический вид – совокупность популяций особей, способных к скрещиванию с образованием плодовитого потомства, обладающего рядом общих морфофизиологических признаков, населяющих определенный ареал, обособленных от других нескрещиваемостью в природных условиях. • Популяция – совокупность особей одного вида, длительно занимающих определенное пространство и воспроизводящая себя в течение большого числа поколений. Население одного вида на определенной территории. В современной биологии популяция рассматривается как элементарная единица процесса эволюции, способная реагировать на изменения среды перестройкой своего генофонда.
• Биологический вид – совокупность популяций особей, способных к скрещиванию с образованием плодовитого потомства, обладающего рядом общих морфофизиологических признаков, населяющих определенный ареал, обособленных от других нескрещиваемостью в природных условиях. • Популяция – совокупность особей одного вида, длительно занимающих определенное пространство и воспроизводящая себя в течение большого числа поколений. Население одного вида на определенной территории. В современной биологии популяция рассматривается как элементарная единица процесса эволюции, способная реагировать на изменения среды перестройкой своего генофонда.
 Тема 1. Химические элементы в биосфере
Тема 1. Химические элементы в биосфере
 Возникновение химических элементов • 1946 г. Гамов – теория возникновения элементов в результате «Большого взрыва» (первичное образование тяжелых элементов) • 1990 г. Озима - первичное образование легких элементов
Возникновение химических элементов • 1946 г. Гамов – теория возникновения элементов в результате «Большого взрыва» (первичное образование тяжелых элементов) • 1990 г. Озима - первичное образование легких элементов
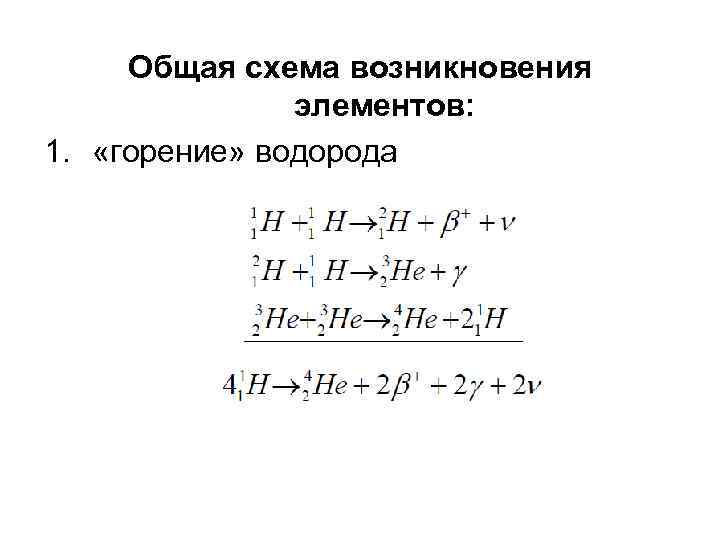 Общая схема возникновения элементов: 1. «горение» водорода
Общая схема возникновения элементов: 1. «горение» водорода
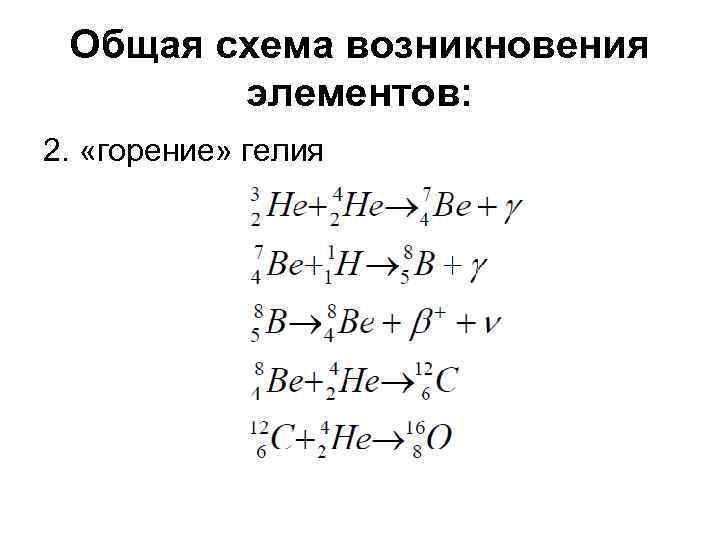 Общая схема возникновения элементов: 2. «горение» гелия
Общая схема возникновения элементов: 2. «горение» гелия
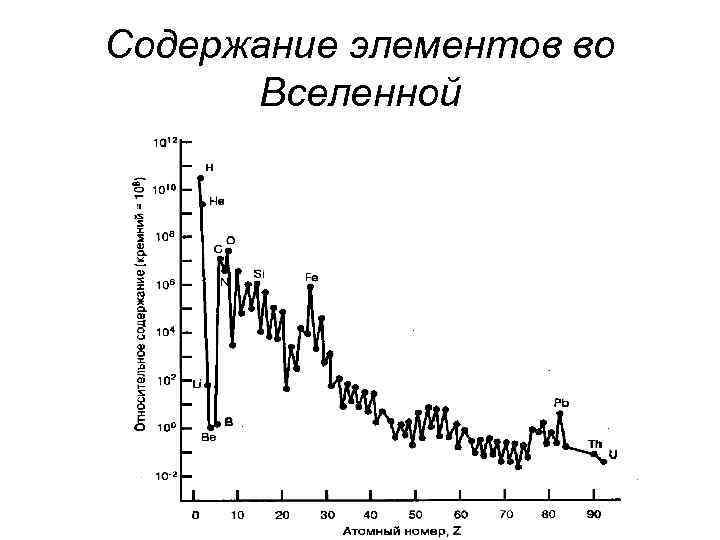 Содержание элементов во Вселенной
Содержание элементов во Вселенной
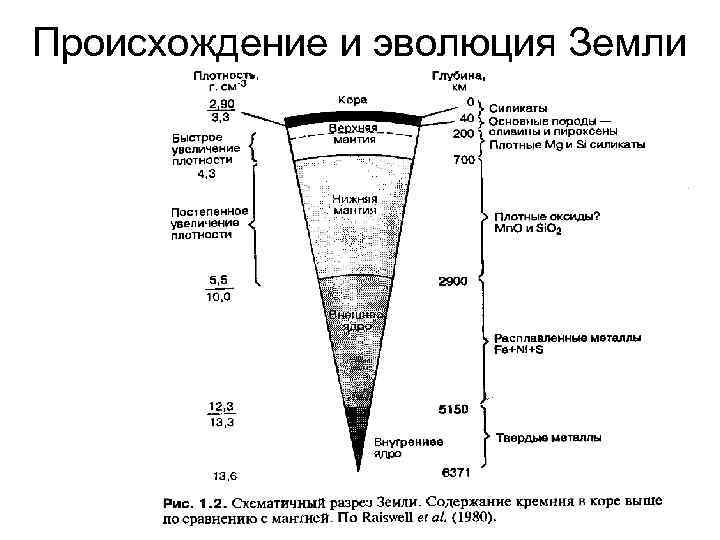 Происхождение и эволюция Земли
Происхождение и эволюция Земли
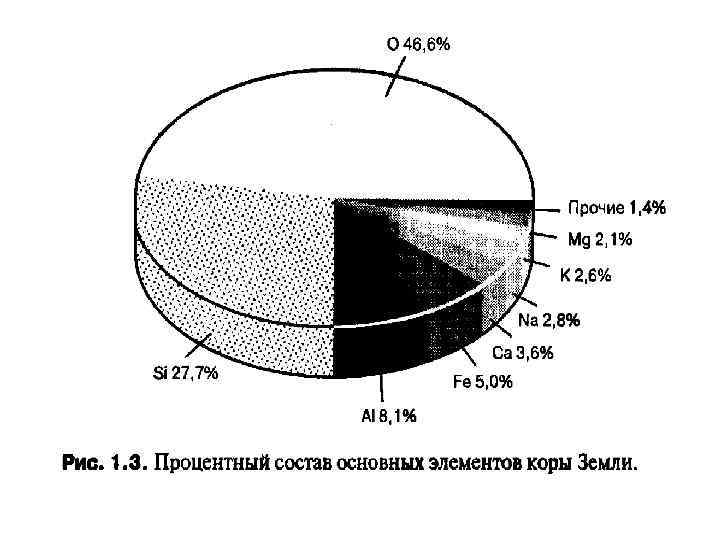
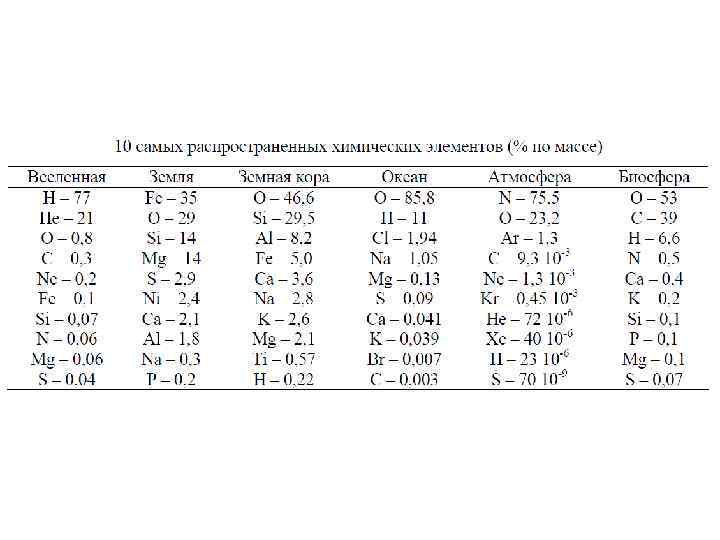
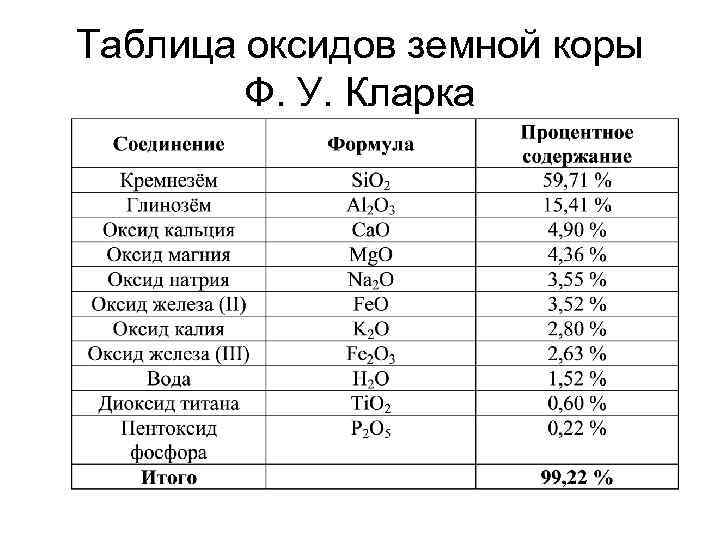 Таблица оксидов земной коры Ф. У. Кларка
Таблица оксидов земной коры Ф. У. Кларка
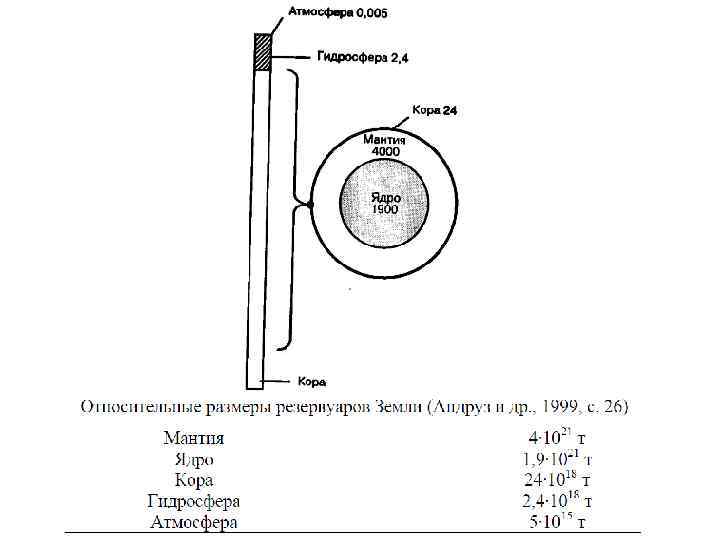 Атмосфера
Атмосфера
 Атмосфера
Атмосфера
 Гипотезы происхождения атмосферы: 1. Непрерывное образование атмосферы (за счет выделения газов из мантии); 2. Взрывообразное образование атмосферы (например, за счет расслоения Земли на ядро и мантию)
Гипотезы происхождения атмосферы: 1. Непрерывное образование атмосферы (за счет выделения газов из мантии); 2. Взрывообразное образование атмосферы (например, за счет расслоения Земли на ядро и мантию)
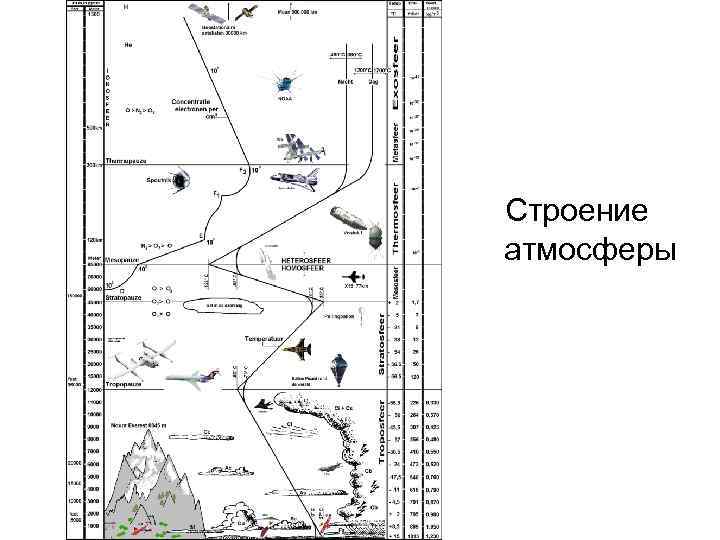 Строение атмосферы
Строение атмосферы
 Закон парциального давления Дальтона P = P 0 exp(–h/H 0) P 0 –давление на поверхности земли h – отсчет высот от уровня океана H 0 – высота/ мера скорости с которой давление падает с высотой
Закон парциального давления Дальтона P = P 0 exp(–h/H 0) P 0 –давление на поверхности земли h – отсчет высот от уровня океана H 0 – высота/ мера скорости с которой давление падает с высотой
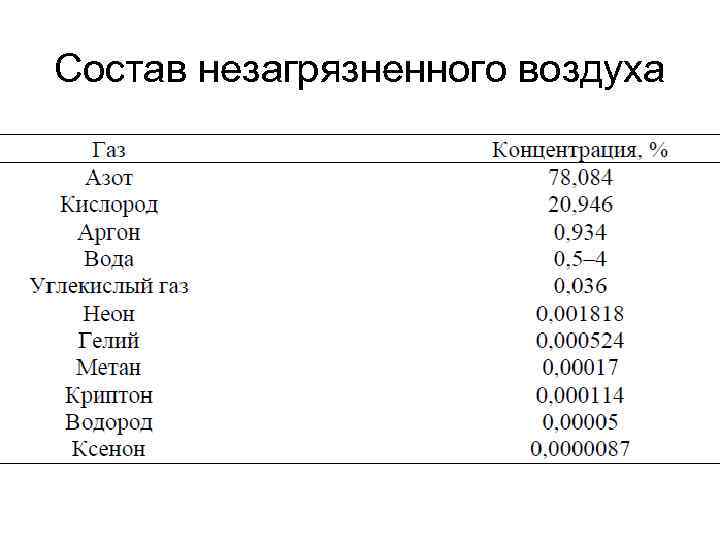 Состав незагрязненного воздуха
Состав незагрязненного воздуха
 Состав атмосферы Газы в атмосфере не всегда находятся в равновесии. Сбалансированное состояние атмосферы: Где , ‑ потоки в атмосферу и из нее, А – общее количество газа в атмосфере, ‑ время пребывания газа в атмосфере.
Состав атмосферы Газы в атмосфере не всегда находятся в равновесии. Сбалансированное состояние атмосферы: Где , ‑ потоки в атмосферу и из нее, А – общее количество газа в атмосфере, ‑ время пребывания газа в атмосфере.
 Время пребывания – величина, описывающая системы в устойчивом состоянии. Источники компонентов в атмосфере: 1. Геохимические 2. Биологические 3. Антропогенные
Время пребывания – величина, описывающая системы в устойчивом состоянии. Источники компонентов в атмосфере: 1. Геохимические 2. Биологические 3. Антропогенные
 Геохимические источники компонентов: 1. Пыль от выветривания почвы (химическое влияние не велико из-за слабой хим. активности) 2. Морские брызги (более реакционноспособны) 3. Частицы привнесенные метеорами (металлы в верхних слоях атмосферы) 4. Выбросы вулканического происхождения (изменение температуры, нарушение химических процессов на больших высотах) 5. Радиоактивные элементы пород
Геохимические источники компонентов: 1. Пыль от выветривания почвы (химическое влияние не велико из-за слабой хим. активности) 2. Морские брызги (более реакционноспособны) 3. Частицы привнесенные метеорами (металлы в верхних слоях атмосферы) 4. Выбросы вулканического происхождения (изменение температуры, нарушение химических процессов на больших высотах) 5. Радиоактивные элементы пород
 Биологические источники компонентов 1. Лес: • Лесные пожары (значительный источник углерода); • Процессы дыхания и фотосинтеза (О 2, СО 2); • Источник следовых количеств органических кислот, альдегидов и др. соединений. 2. Микроорганизмы почв
Биологические источники компонентов 1. Лес: • Лесные пожары (значительный источник углерода); • Процессы дыхания и фотосинтеза (О 2, СО 2); • Источник следовых количеств органических кислот, альдегидов и др. соединений. 2. Микроорганизмы почв
 Биологические источники компонентов Растения поглощают почвенные 3. Микроорганизмы океанов 4. Малоизученные процессы (CH 3 Cl, бром, йодсодержащие органические соединения)
Биологические источники компонентов Растения поглощают почвенные 3. Микроорганизмы океанов 4. Малоизученные процессы (CH 3 Cl, бром, йодсодержащие органические соединения)

 Состав атмосферы: • Постоянные составляющие • Переменные составляющие (СО 2, водяной пар) • Случайные составные части (радиоактивные примеси, аммиак, сернистый газ и др. )
Состав атмосферы: • Постоянные составляющие • Переменные составляющие (СО 2, водяной пар) • Случайные составные части (радиоактивные примеси, аммиак, сернистый газ и др. )
 Состав атмосферы: Диссипация – это процесс преодоления атомами и ионами поля притяжения Земли. Кинетическая теория газов: T – абсолютная температура, m – средняя масса частицы, V – средняя скорость частицы, k. B – константа Больцмана
Состав атмосферы: Диссипация – это процесс преодоления атомами и ионами поля притяжения Земли. Кинетическая теория газов: T – абсолютная температура, m – средняя масса частицы, V – средняя скорость частицы, k. B – константа Больцмана
 Химические реакции в атмосфере можно разделить на: 1. 2. 3. 4. 5. Реакции фотодиссоциации Реакции фотоионизации Реакции диссоциативной рекомбинации Реакции с переносом заряда Реакции обмена
Химические реакции в атмосфере можно разделить на: 1. 2. 3. 4. 5. Реакции фотодиссоциации Реакции фотоионизации Реакции диссоциативной рекомбинации Реакции с переносом заряда Реакции обмена
 Химические реакции в атмосфере 1. Реакции фотодиссоциации Фотодиссоциация – это распад молекул с образованием свободных радикалов в результате поглощения фотона.
Химические реакции в атмосфере 1. Реакции фотодиссоциации Фотодиссоциация – это распад молекул с образованием свободных радикалов в результате поглощения фотона.
 Химические реакции в атмосфере 2. Реакции фотоионизации Фотоионизация – это образование ионов из молекул и атомов под действием квантов света.
Химические реакции в атмосфере 2. Реакции фотоионизации Фотоионизация – это образование ионов из молекул и атомов под действием квантов света.
 Химические реакции в атмосфере 3. Реакции диссоциативной рекомбинации – это реакции иона с электронами с образованием нейтральных молекул, которые в разряженных условиях верхней атмосферы будут быстро диссоциировать.
Химические реакции в атмосфере 3. Реакции диссоциативной рекомбинации – это реакции иона с электронами с образованием нейтральных молекул, которые в разряженных условиях верхней атмосферы будут быстро диссоциировать.
 Химические реакции в атмосфере 4. Перенос заряда – реакция молекулярного иона с нейтральной частицей, сопровождающаяся переносом электрона.
Химические реакции в атмосфере 4. Перенос заряда – реакция молекулярного иона с нейтральной частицей, сопровождающаяся переносом электрона.
 Химические реакции в атмосфере 5. Реакции обмена – реакции сопровождающиеся разрывом связей.
Химические реакции в атмосфере 5. Реакции обмена – реакции сопровождающиеся разрывом связей.
 Реакции следовых веществ в атмосфере Причина короткого пребывания газа в атмосфере – протекание хим. реакций.
Реакции следовых веществ в атмосфере Причина короткого пребывания газа в атмосфере – протекание хим. реакций.
 Реакции следовых веществ в атмосфере Наиболее реакционноспособная единица в атмосфере – гидроксильный радикал. а) фоторазложение озона: б) Фотодиссоциация воды:
Реакции следовых веществ в атмосфере Наиболее реакционноспособная единица в атмосфере – гидроксильный радикал. а) фоторазложение озона: б) Фотодиссоциация воды:
 Реакции следовых веществ в атмосфере Гидроксильный радикал реагирует со многими соединениями, поэтому у него короткое время пребывания, и скорости реакций больше нежели у О 2. В стратосфере преобладает атомарный кислород. Газы просачиваясь в стратосферу мешают образованию озона.
Реакции следовых веществ в атмосфере Гидроксильный радикал реагирует со многими соединениями, поэтому у него короткое время пребывания, и скорости реакций больше нежели у О 2. В стратосфере преобладает атомарный кислород. Газы просачиваясь в стратосферу мешают образованию озона.
 ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ • • Источники антропогенного загрязнения: транспорт - 60% общего количества загрязнений, промышленность – 17%, энергетика – 14%, отопление и уничтожение отходов – 9%.
ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ • • Источники антропогенного загрязнения: транспорт - 60% общего количества загрязнений, промышленность – 17%, энергетика – 14%, отопление и уничтожение отходов – 9%.
 ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Классификация атмосферных загрязнений (по пути поступления в атмосферу): 1. первичные (поступающие непосредственно в атмосферу) 2. вторичные (являющиеся результатом превращения первичных).
ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Классификация атмосферных загрязнений (по пути поступления в атмосферу): 1. первичные (поступающие непосредственно в атмосферу) 2. вторичные (являющиеся результатом превращения первичных).
 ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Около 85% общего выброса вредных веществ в атмосферу составляют: • сернистый газ, • окись углерода, • оксиды углерода • аэрозольная пыль.
ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Около 85% общего выброса вредных веществ в атмосферу составляют: • сернистый газ, • окись углерода, • оксиды углерода • аэрозольная пыль.
 ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Аэрозоли – дисперсные системы, в которых дисперсионной средой служит газ, а дисперсными фазами являются твердые или жидкие частицы. Аэрозоли: 1. пыли – дисперсные системы, состоящие из твердых частиц, диспергированных в газообразной среде. 2. дымы – аэрозоли, которые получаются при конденсации газа. 3. туман – дисперсная система, состоящая из жидких частиц в газообразной среде.
ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Аэрозоли – дисперсные системы, в которых дисперсионной средой служит газ, а дисперсными фазами являются твердые или жидкие частицы. Аэрозоли: 1. пыли – дисперсные системы, состоящие из твердых частиц, диспергированных в газообразной среде. 2. дымы – аэрозоли, которые получаются при конденсации газа. 3. туман – дисперсная система, состоящая из жидких частиц в газообразной среде.
 ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Источники аэрозолей: • Естественные (вулканы, гейзеры, разрушающиеся горные породы, пылевые бури, почвенная эрозия, лесные пожары), • Антропогенные (выбросы промышленных предприятий и др. )
ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Источники аэрозолей: • Естественные (вулканы, гейзеры, разрушающиеся горные породы, пылевые бури, почвенная эрозия, лесные пожары), • Антропогенные (выбросы промышленных предприятий и др. )
 ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Основной параметр, характеризующий взвешенные частицы, – это их размер. Закон Стокса: где F – сила трения, r – радиус частицы, V – ее скорость и – вязкость среды.
ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ Основной параметр, характеризующий взвешенные частицы, – это их размер. Закон Стокса: где F – сила трения, r – радиус частицы, V – ее скорость и – вязкость среды.
 Загрязнение атмосферы автотранспортом Количество загрязнения определяется: • составом топлива • объемом сжигаемого топлива • организация процесса сгорания
Загрязнение атмосферы автотранспортом Количество загрязнения определяется: • составом топлива • объемом сжигаемого топлива • организация процесса сгорания
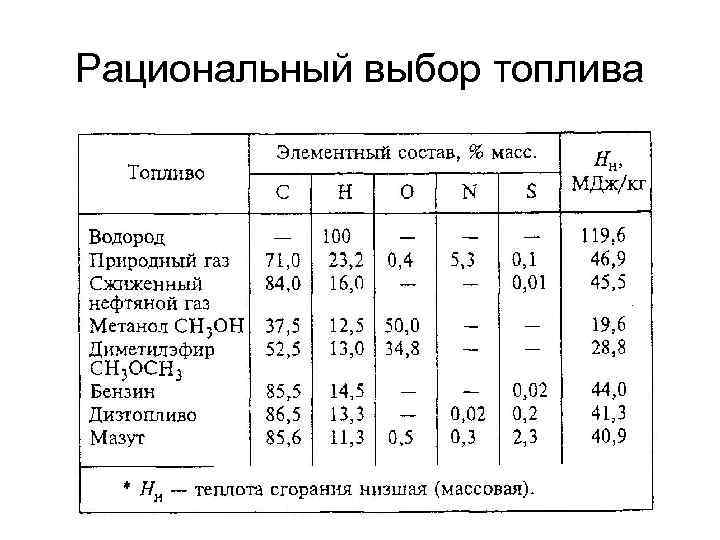 Рациональный выбор топлива
Рациональный выбор топлива
 Загрязнение атмосферы автотранспортом Выбросы в атмосферу при сжигании различных видов топлива: • нетоксичные: углекислый газ, водяной пар (парниковые газы). • вредные вещества: оксид углерода (II), оксиды серы, азота, соединения свинца, сажа, углеводороды, бенз(а)пирен (С 20 Н 12), несгоревшие частицы топлива и т. п.
Загрязнение атмосферы автотранспортом Выбросы в атмосферу при сжигании различных видов топлива: • нетоксичные: углекислый газ, водяной пар (парниковые газы). • вредные вещества: оксид углерода (II), оксиды серы, азота, соединения свинца, сажа, углеводороды, бенз(а)пирен (С 20 Н 12), несгоревшие частицы топлива и т. п.
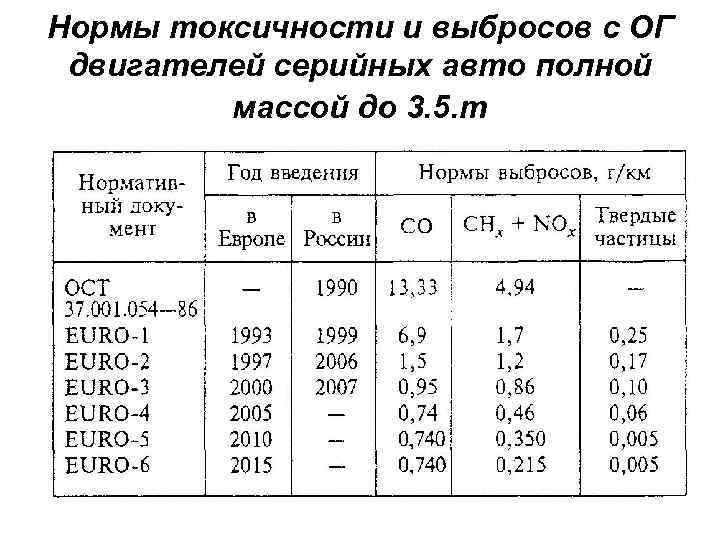 Нормы токсичности и выбросов с ОГ двигателей серийных авто полной массой до 3. 5. т
Нормы токсичности и выбросов с ОГ двигателей серийных авто полной массой до 3. 5. т
 Загрязнение атмосферы автотранспортом Горение топлива Идеальная ситуация: Реальная ситуация:
Загрязнение атмосферы автотранспортом Горение топлива Идеальная ситуация: Реальная ситуация:
 Горение топлива - СО связывает гемоглобин в 210 раз эффективнее О 2
Горение топлива - СО связывает гемоглобин в 210 раз эффективнее О 2
 Горение топлива - Промышленные выбросы SO 2 – 200 Мт/год - Природные источники – 300 Мт/год (Эткинс, 1991)
Горение топлива - Промышленные выбросы SO 2 – 200 Мт/год - Природные источники – 300 Мт/год (Эткинс, 1991)
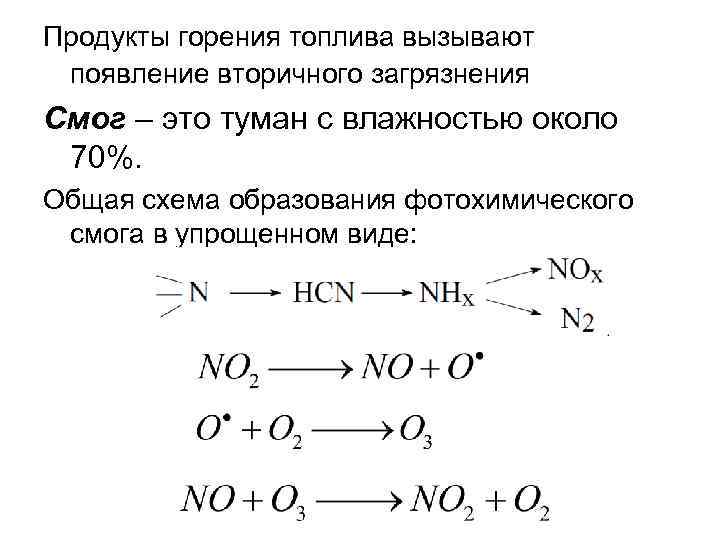 Продукты горения топлива вызывают появление вторичного загрязнения Смог – это туман с влажностью около 70%. Общая схема образования фотохимического смога в упрощенном виде:
Продукты горения топлива вызывают появление вторичного загрязнения Смог – это туман с влажностью около 70%. Общая схема образования фотохимического смога в упрощенном виде:
 Некоторые составляющие фотохимического смога
Некоторые составляющие фотохимического смога
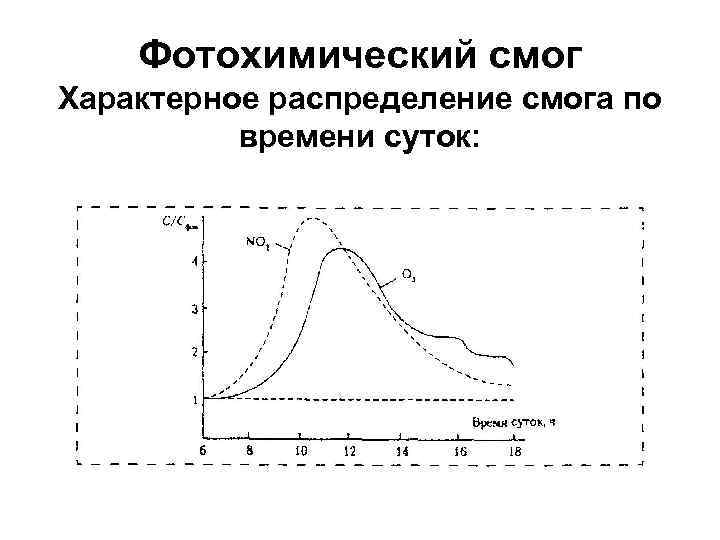 Фотохимический смог Характерное распределение смога по времени суток:
Фотохимический смог Характерное распределение смога по времени суток:

 Загрязнение воздуха и здоровье • Свинец – снижение умственных способностей у детей • Бензол – увеличение фотохимического смога, онкологические заболевания. • Толуол - онкологические заболевания; образует пероксибензилнитрат – раздражитель глаз.
Загрязнение воздуха и здоровье • Свинец – снижение умственных способностей у детей • Бензол – увеличение фотохимического смога, онкологические заболевания. • Толуол - онкологические заболевания; образует пероксибензилнитрат – раздражитель глаз.
 Последствия загрязнения атмосферы • Диоксид серы, серная кислота – разрушает известняк до гипса; • Озон – разрушение двойных связей органических молекул (разрушение резин, красителей, нарушение жизнедеятельности растений); • Окиси азота – затруднение дыхания, инициирование фотохимических процессов с образованием альдегидов и др.
Последствия загрязнения атмосферы • Диоксид серы, серная кислота – разрушает известняк до гипса; • Озон – разрушение двойных связей органических молекул (разрушение резин, красителей, нарушение жизнедеятельности растений); • Окиси азота – затруднение дыхания, инициирование фотохимических процессов с образованием альдегидов и др.
 Озоновый слой Механизм образования озона: Факторы влияющие на концентрацию озона:
Озоновый слой Механизм образования озона: Факторы влияющие на концентрацию озона:
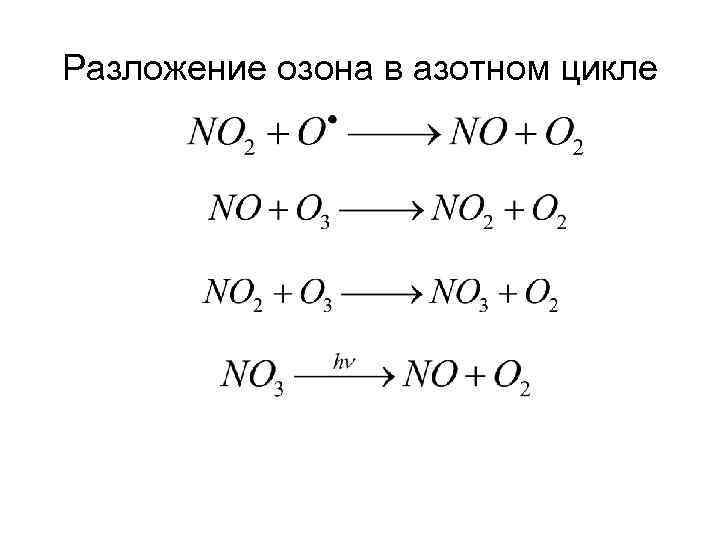 Разложение озона в азотном цикле
Разложение озона в азотном цикле
 Разложение озона под действием водяного пара Таблица 2 Число частиц в 1 см 3 атмосферы по расчетным данным
Разложение озона под действием водяного пара Таблица 2 Число частиц в 1 см 3 атмосферы по расчетным данным
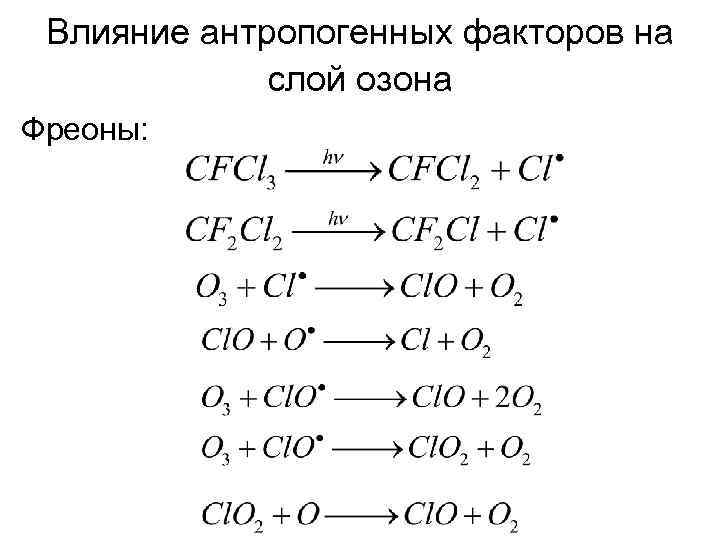 Влияние антропогенных факторов на слой озона Фреоны:
Влияние антропогенных факторов на слой озона Фреоны:
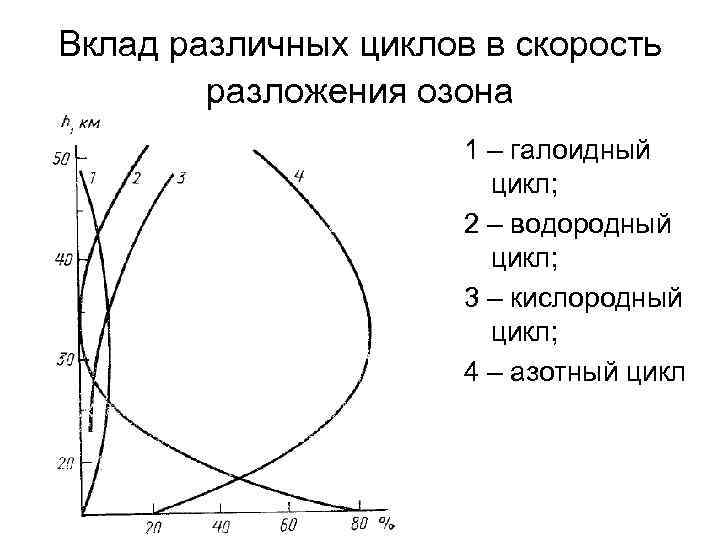 Вклад различных циклов в скорость разложения озона 1 – галоидный цикл; 2 – водородный цикл; 3 – кислородный цикл; 4 – азотный цикл
Вклад различных циклов в скорость разложения озона 1 – галоидный цикл; 2 – водородный цикл; 3 – кислородный цикл; 4 – азотный цикл
 Изменения глобального климата
Изменения глобального климата
 Естественная эволюция климата Причины изменения климата: 1. Астрономические факторы (колебания климата с периодичностью в десятки тысяч лет). 2. Состав атмосферы (влияние естественных изменений содержания СО 2 существенно для интервалов времени более 100 тыс. лет).
Естественная эволюция климата Причины изменения климата: 1. Астрономические факторы (колебания климата с периодичностью в десятки тысяч лет). 2. Состав атмосферы (влияние естественных изменений содержания СО 2 существенно для интервалов времени более 100 тыс. лет).
 Естественная эволюция климата Причины изменения климата: 3. Рельеф земной поверхности (сказывается на изменениях климата на больших пространствах за периоды не меньше сотен тысяч – миллионов лет). 4. Солнечная постоянная. Порядок времени – сотни миллионов, миллиарды лет.
Естественная эволюция климата Причины изменения климата: 3. Рельеф земной поверхности (сказывается на изменениях климата на больших пространствах за периоды не меньше сотен тысяч – миллионов лет). 4. Солнечная постоянная. Порядок времени – сотни миллионов, миллиарды лет.
 Причины изменения климата: 5. Другие факторы, влияние которых сказывается за меньшие промежутки времени: • • Солнечная активность; Скорость вращения Земли; Вулканическая активность; Автоколебательные процессы в системе «атмосфера – гидросфера - криосфера» .
Причины изменения климата: 5. Другие факторы, влияние которых сказывается за меньшие промежутки времени: • • Солнечная активность; Скорость вращения Земли; Вулканическая активность; Автоколебательные процессы в системе «атмосфера – гидросфера - криосфера» .
 Основные антропогенные факторы, оказывающие влияние на климат: • Рост производства энергии (нагрев тропосферы); • Увеличение содержания СО 2 и др. парниковых газов в атмосфере; • Снижение содержания О 3 в стратосфере и увеличение в тропосфере; • Увеличение содержания аэрозолей в атмосфере (рост облачности, уменьшение приземной температуры воздуха).
Основные антропогенные факторы, оказывающие влияние на климат: • Рост производства энергии (нагрев тропосферы); • Увеличение содержания СО 2 и др. парниковых газов в атмосфере; • Снижение содержания О 3 в стратосфере и увеличение в тропосфере; • Увеличение содержания аэрозолей в атмосфере (рост облачности, уменьшение приземной температуры воздуха).
 Темы докладов: 1. 2. 3. 4. 5. Происхождение и эволюция Земли. Образование атмосферы. Состав и строение атмосферы. Функции атмосферы. Основные химические процессы, протекающие в атмосфере. 6. Парниковый эффект. 7. Причины глобальных климатических изменений. 8. Разрушение озонового слоя. Влияние хлорфторуглеродов и других компонентов антропогенного происхождения на процессы в озоновом слое.
Темы докладов: 1. 2. 3. 4. 5. Происхождение и эволюция Земли. Образование атмосферы. Состав и строение атмосферы. Функции атмосферы. Основные химические процессы, протекающие в атмосфере. 6. Парниковый эффект. 7. Причины глобальных климатических изменений. 8. Разрушение озонового слоя. Влияние хлорфторуглеродов и других компонентов антропогенного происхождения на процессы в озоновом слое.
 Темы докладов: 9. Причины и механизм образования кислотных дождей (реакции, протекающие в атмосфере, основные характеристики компонентов кислотных дождей и сопуствующих газов, состав кислотного дождя, кислотные туманы и облака). 10. Воздействие угарного и углекислого газов на здоровье человека. 11. Воздействие оксидов азота и серного ангидрида на здоровье человека.
Темы докладов: 9. Причины и механизм образования кислотных дождей (реакции, протекающие в атмосфере, основные характеристики компонентов кислотных дождей и сопуствующих газов, состав кислотного дождя, кислотные туманы и облака). 10. Воздействие угарного и углекислого газов на здоровье человека. 11. Воздействие оксидов азота и серного ангидрида на здоровье человека.
 Темы докладов: 12. Воздействие тяжелых металлов на здоровье человека. 13. Источники загрязнения атмосферы бензапиреном. Механизм токсического воздействия. 14. Атмосферная радиоактивность: механизм влияния на окр. среду, реакции, аллергены, механизм появления этих частиц в атмосфере, их свойства.
Темы докладов: 12. Воздействие тяжелых металлов на здоровье человека. 13. Источники загрязнения атмосферы бензапиреном. Механизм токсического воздействия. 14. Атмосферная радиоактивность: механизм влияния на окр. среду, реакции, аллергены, механизм появления этих частиц в атмосфере, их свойства.

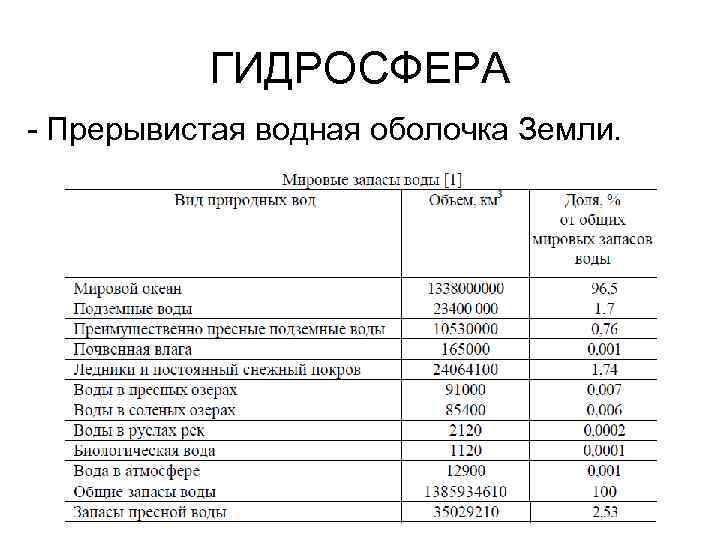 ГИДРОСФЕРА - Прерывистая водная оболочка Земли.
ГИДРОСФЕРА - Прерывистая водная оболочка Земли.
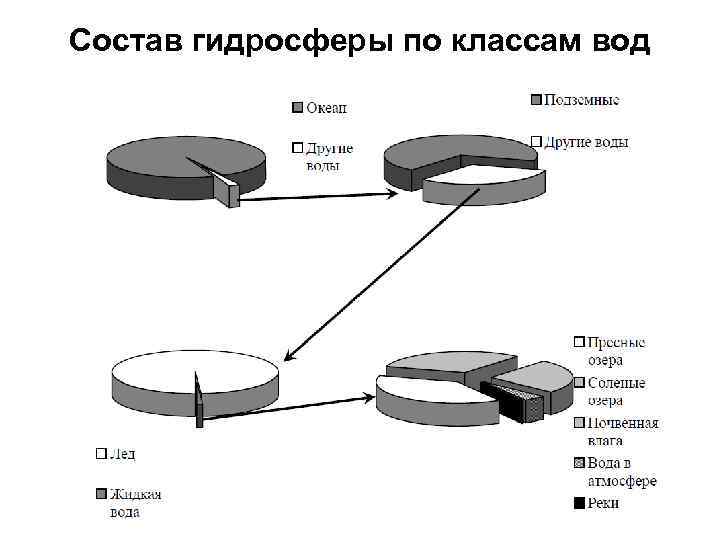 Состав гидросферы по классам вод
Состав гидросферы по классам вод
 Состав гидросферы • Общая масса воды 2× 1018 т – 0. 025% массы Земли. • Объем гидросферы – 1375 × 106 км 3 • Мировой океан – 71%
Состав гидросферы • Общая масса воды 2× 1018 т – 0. 025% массы Земли. • Объем гидросферы – 1375 × 106 км 3 • Мировой океан – 71%
 Свойства воды • Зависимость плотности от температурного режима • Теплоемкость • Удельная энтальпия плавления • Удельная энтальпия испарения • Диэлектрическая проницаемость • Поверхностное натяжение
Свойства воды • Зависимость плотности от температурного режима • Теплоемкость • Удельная энтальпия плавления • Удельная энтальпия испарения • Диэлектрическая проницаемость • Поверхностное натяжение
 Показатели качества воды 1. Физические: Цветность, запах, вкус, прозрачность 2. Химические: p. H, жесткость, щелочность, окисляемость (ХПК, БПК)
Показатели качества воды 1. Физические: Цветность, запах, вкус, прозрачность 2. Химические: p. H, жесткость, щелочность, окисляемость (ХПК, БПК)
 Роль гидросферы: • Среда, в которой произошло зарождение и развитие живого вещества; • Обязательный компонент в составе живого организма; • Переносчик растворенных веществ между литосферой и гидросферой, атмосферой и гидросферой, между живыми организмами и окружающей средой; • Универсальный растворитель – взаимодействует со всеми веществами, как правило, не вступая в реакции.
Роль гидросферы: • Среда, в которой произошло зарождение и развитие живого вещества; • Обязательный компонент в составе живого организма; • Переносчик растворенных веществ между литосферой и гидросферой, атмосферой и гидросферой, между живыми организмами и окружающей средой; • Универсальный растворитель – взаимодействует со всеми веществами, как правило, не вступая в реакции.
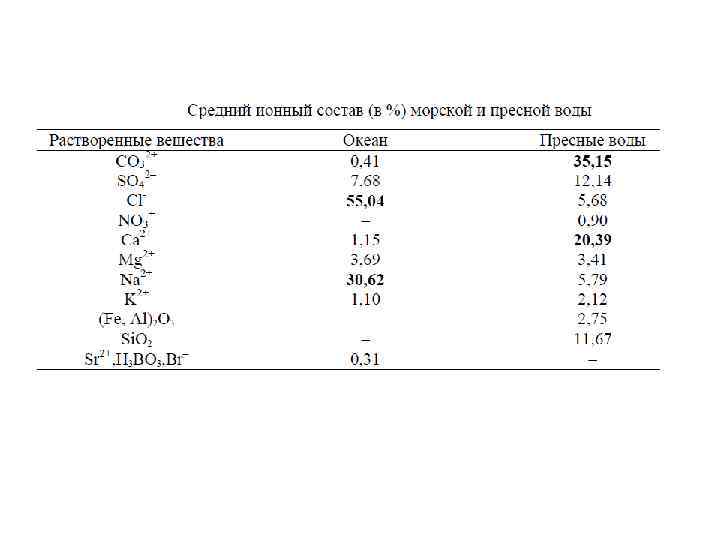
 Состав Мирового океана 1) главные ионы – одиннадцать компонентов составляют 99, 98 % по массе от всех растворенных в океанской воде солей (табл. 5) 2) биогенные элементы – С, Н, N, P, Si, Fe, Mn, из которых состоят организмы; 3) растворенные в морской воде газы – О 2, N 2, CO 2, углеводороды и инертные газы; 4) микроэлементы; 5) органические вещества.
Состав Мирового океана 1) главные ионы – одиннадцать компонентов составляют 99, 98 % по массе от всех растворенных в океанской воде солей (табл. 5) 2) биогенные элементы – С, Н, N, P, Si, Fe, Mn, из которых состоят организмы; 3) растворенные в морской воде газы – О 2, N 2, CO 2, углеводороды и инертные газы; 4) микроэлементы; 5) органические вещества.
 Источники элементов в океане: • речные воды (основной источник) • высокотемпературные гидротермальные излияния • глубинные источники Изъятие элементов из вод океана: • Осаждение на дно • Испарение
Источники элементов в океане: • речные воды (основной источник) • высокотемпературные гидротермальные излияния • глубинные источники Изъятие элементов из вод океана: • Осаждение на дно • Испарение
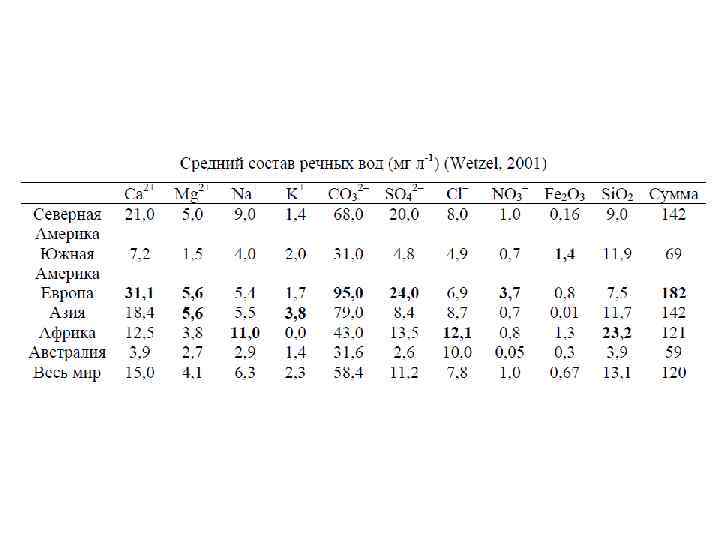
 Характеристики вод океана: • Соленость • Водородный показатель (p. H) • Прозрачность Ресурсы океана: • Среда обитания для многих видов животных и растений • Источник химических элементов • Регулятор баланса СО 2 - О 2
Характеристики вод океана: • Соленость • Водородный показатель (p. H) • Прозрачность Ресурсы океана: • Среда обитания для многих видов животных и растений • Источник химических элементов • Регулятор баланса СО 2 - О 2
 Процессы в дельтах рек и эстуариях 1. Агрегация коллоидного материала Рис. Двойной электрический слой, включающий в себя неподвижный слой отрицательных зарядов на частице и подвижный слой ионов из раствора
Процессы в дельтах рек и эстуариях 1. Агрегация коллоидного материала Рис. Двойной электрический слой, включающий в себя неподвижный слой отрицательных зарядов на частице и подвижный слой ионов из раствора
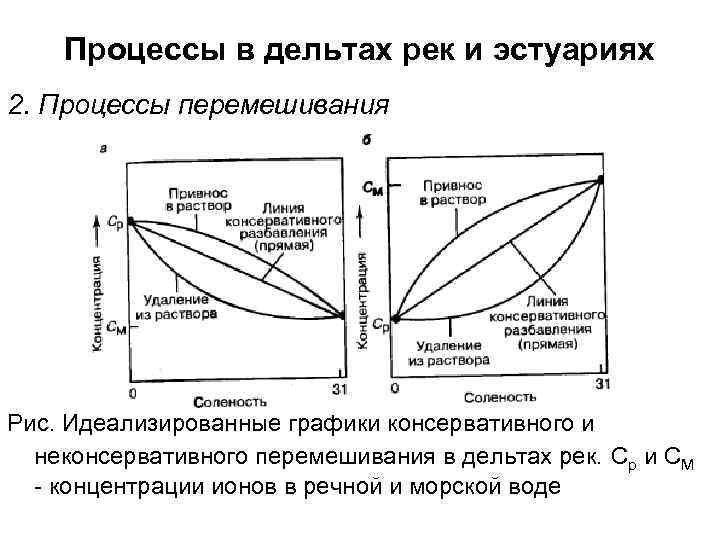 Процессы в дельтах рек и эстуариях 2. Процессы перемешивания Рис. Идеализированные графики консервативного и неконсервативного перемешивания в дельтах рек. Ср и СМ - концентрации ионов в речной и морской воде
Процессы в дельтах рек и эстуариях 2. Процессы перемешивания Рис. Идеализированные графики консервативного и неконсервативного перемешивания в дельтах рек. Ср и СМ - концентрации ионов в речной и морской воде
 Процессы в дельтах рек и эстуариях 3. Гальморолиз и ионный обмен в дельтах Гальморолиз - процесс, с помощью которого материал суши приводится в соответствие с морскими условиями. Понятие гальморолиза определено неточно. Считают, что он включает в себя все те реакции, которые оказывают влияние на частицу в океане до захоронения ее в виде осадка.
Процессы в дельтах рек и эстуариях 3. Гальморолиз и ионный обмен в дельтах Гальморолиз - процесс, с помощью которого материал суши приводится в соответствие с морскими условиями. Понятие гальморолиза определено неточно. Считают, что он включает в себя все те реакции, которые оказывают влияние на частицу в океане до захоронения ее в виде осадка.
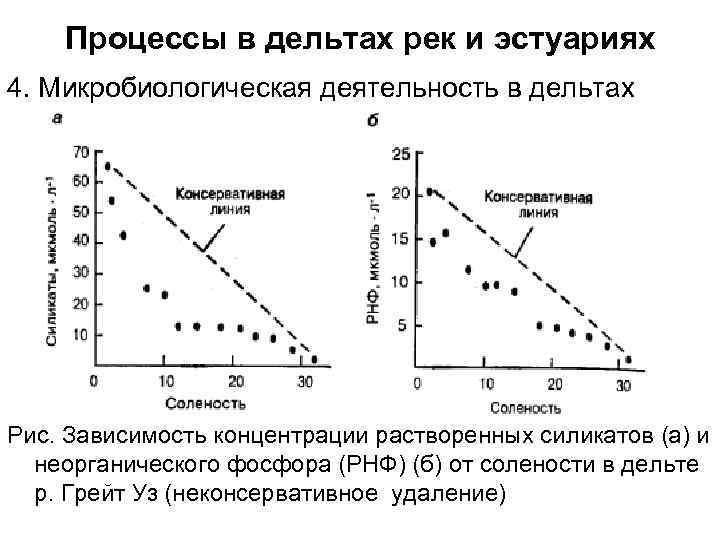 Процессы в дельтах рек и эстуариях 4. Микробиологическая деятельность в дельтах Рис. Зависимость концентрации растворенных силикатов (а) и неорганического фосфора (РНФ) (б) от солености в дельте р. Грейт Уз (неконсервативное удаление)
Процессы в дельтах рек и эстуариях 4. Микробиологическая деятельность в дельтах Рис. Зависимость концентрации растворенных силикатов (а) и неорганического фосфора (РНФ) (б) от солености в дельте р. Грейт Уз (неконсервативное удаление)
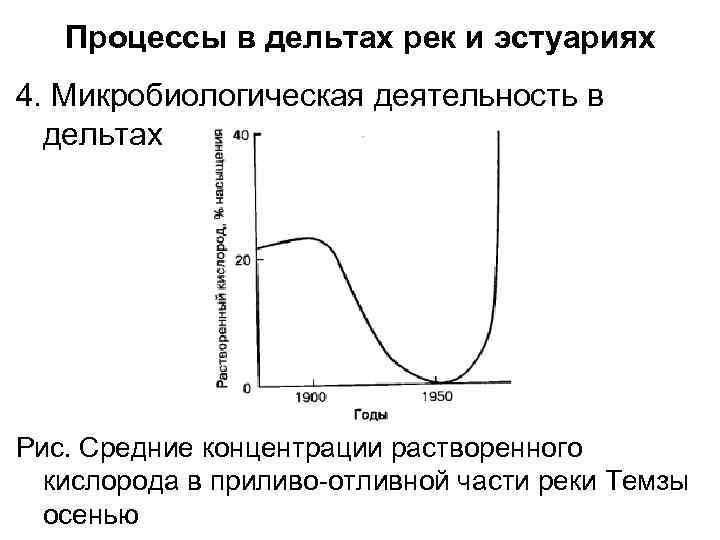 Процессы в дельтах рек и эстуариях 4. Микробиологическая деятельность в дельтах Рис. Средние концентрации растворенного кислорода в приливо-отливной части реки Темзы осенью
Процессы в дельтах рек и эстуариях 4. Микробиологическая деятельность в дельтах Рис. Средние концентрации растворенного кислорода в приливо-отливной части реки Темзы осенью
 Химия основных ионов морской воды Свойства морской воды: 1. Высокая ионная сила морской воды, которая содержит около 35 г/л солей. 2. Химический состав морской воды, с высоким содержанием ионов Na+ и Сl-. 3. Постоянные относительные концентрации основных ионов морской воды во всех океанах Земли.
Химия основных ионов морской воды Свойства морской воды: 1. Высокая ионная сила морской воды, которая содержит около 35 г/л солей. 2. Химический состав морской воды, с высоким содержанием ионов Na+ и Сl-. 3. Постоянные относительные концентрации основных ионов морской воды во всех океанах Земли.
 Постоянство химии главных ионов в морской воде в геологическом временном масштабе • Эвапориты — соли, которые выпали природным путем из испаряющейся морской воды в бассейнах, по большей части отрезанных от открытого океана.
Постоянство химии главных ионов в морской воде в геологическом временном масштабе • Эвапориты — соли, которые выпали природным путем из испаряющейся морской воды в бассейнах, по большей части отрезанных от открытого океана.
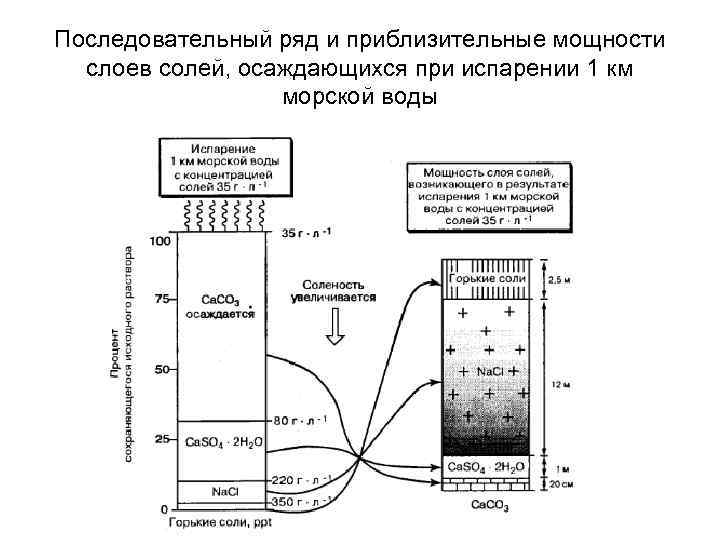 Последовательный ряд и приблизительные мощности слоев солей, осаждающихся при испарении 1 км морской воды
Последовательный ряд и приблизительные мощности слоев солей, осаждающихся при испарении 1 км морской воды
 Химический круговорот главных ионов Времена пребывания ионов в морской воде – индикатор путей их обращения.
Химический круговорот главных ионов Времена пребывания ионов в морской воде – индикатор путей их обращения.
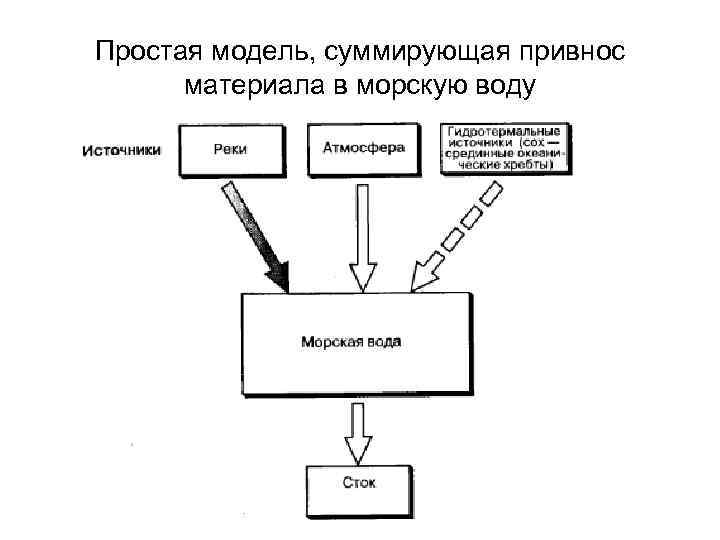 Простая модель, суммирующая привнос материала в морскую воду
Простая модель, суммирующая привнос материала в морскую воду
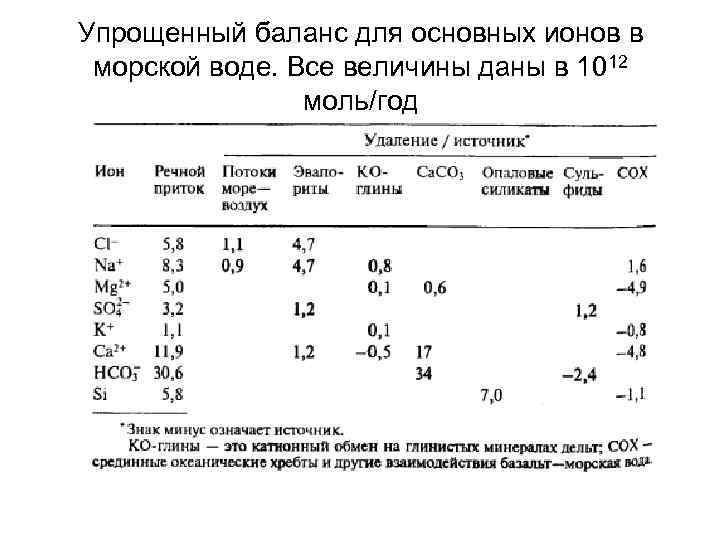 Упрощенный баланс для основных ионов в морской воде. Все величины даны в 1012 моль/год
Упрощенный баланс для основных ионов в морской воде. Все величины даны в 1012 моль/год
 Процессы выноса главных ионов морской воды 1. Потоки море – воздух 2. Эвапориты 3. Катионный обмен 4. Осаждение карбонатов
Процессы выноса главных ионов морской воды 1. Потоки море – воздух 2. Эвапориты 3. Катионный обмен 4. Осаждение карбонатов
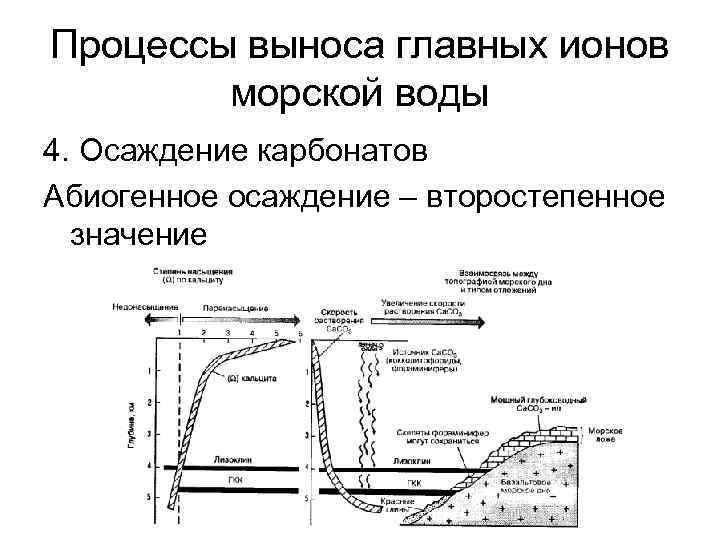 Процессы выноса главных ионов морской воды 4. Осаждение карбонатов Абиогенное осаждение – второстепенное значение
Процессы выноса главных ионов морской воды 4. Осаждение карбонатов Абиогенное осаждение – второстепенное значение
 Процессы выноса главных ионов морской воды 5. Опаловые силикаты (опал) — это разновидность продуцируемого биологически диоксида кремния (Si. O 4 n. Н 2 О), выделяемого как скелетный материал морским фитопланктоном (диатомеями) и одной группой морского зоопланктона (радиоляриями)
Процессы выноса главных ионов морской воды 5. Опаловые силикаты (опал) — это разновидность продуцируемого биологически диоксида кремния (Si. O 4 n. Н 2 О), выделяемого как скелетный материал морским фитопланктоном (диатомеями) и одной группой морского зоопланктона (радиоляриями)
 Процессы выноса главных ионов морской воды 6. Сульфиды
Процессы выноса главных ионов морской воды 6. Сульфиды
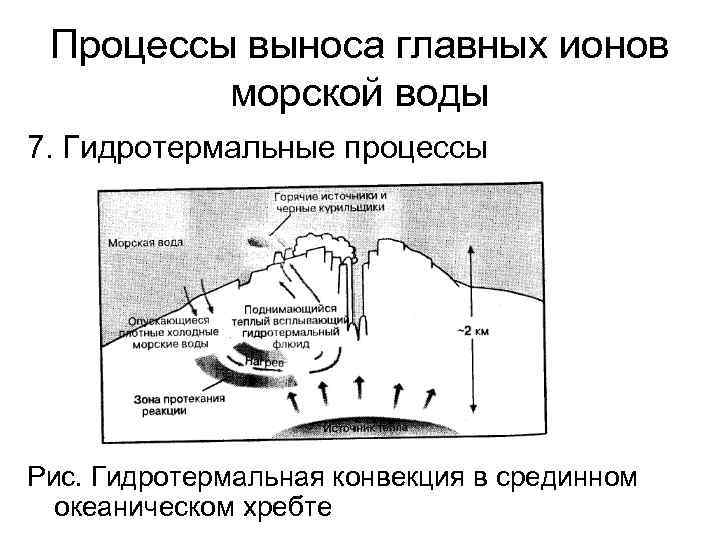 Процессы выноса главных ионов морской воды 7. Гидротермальные процессы Рис. Гидротермальная конвекция в срединном океаническом хребте
Процессы выноса главных ионов морской воды 7. Гидротермальные процессы Рис. Гидротермальная конвекция в срединном океаническом хребте
 Процессы выноса главных ионов морской воды 7. Гидротермальные процессы: а) гидротермальные реакции как сток главных ионов. б) гидротермальные реакции как источники главных ионов в) гидротермальные реакции с участием сульфатов и калия
Процессы выноса главных ионов морской воды 7. Гидротермальные процессы: а) гидротермальные реакции как сток главных ионов. б) гидротермальные реакции как источники главных ионов в) гидротермальные реакции с участием сульфатов и калия
 БАЛАНС ЗАПАСОВ ГЛАВНЫХ ИОНОВ МОРСКОЙ ВОДЫ Запасы главных ионов в морской воде сбалансированы (приход=расходу), кроме К+ 1. «Обратные реакции выветривания» 2. Фиксация К+ на глинистых минералах в результате реакций ионного обмена
БАЛАНС ЗАПАСОВ ГЛАВНЫХ ИОНОВ МОРСКОЙ ВОДЫ Запасы главных ионов в морской воде сбалансированы (приход=расходу), кроме К+ 1. «Обратные реакции выветривания» 2. Фиксация К+ на глинистых минералах в результате реакций ионного обмена
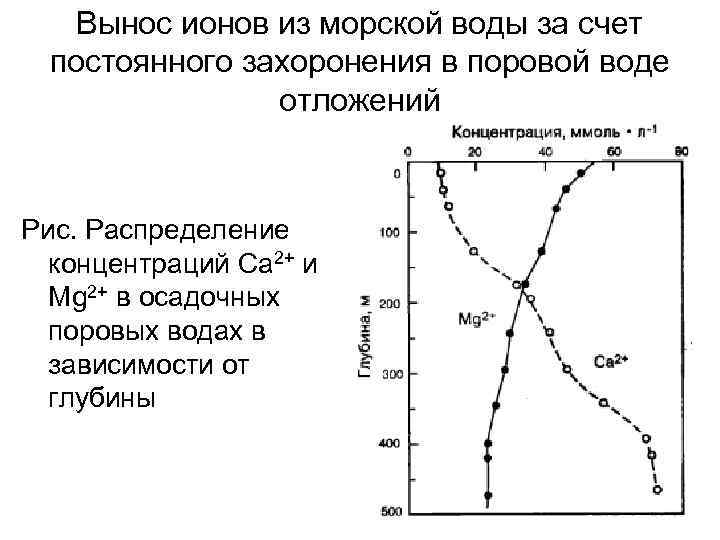 Вынос ионов из морской воды за счет постоянного захоронения в поровой воде отложений Рис. Распределение концентраций Ca 2+ и Mg 2+ в осадочных поровых водах в зависимости от глубины
Вынос ионов из морской воды за счет постоянного захоронения в поровой воде отложений Рис. Распределение концентраций Ca 2+ и Mg 2+ в осадочных поровых водах в зависимости от глубины
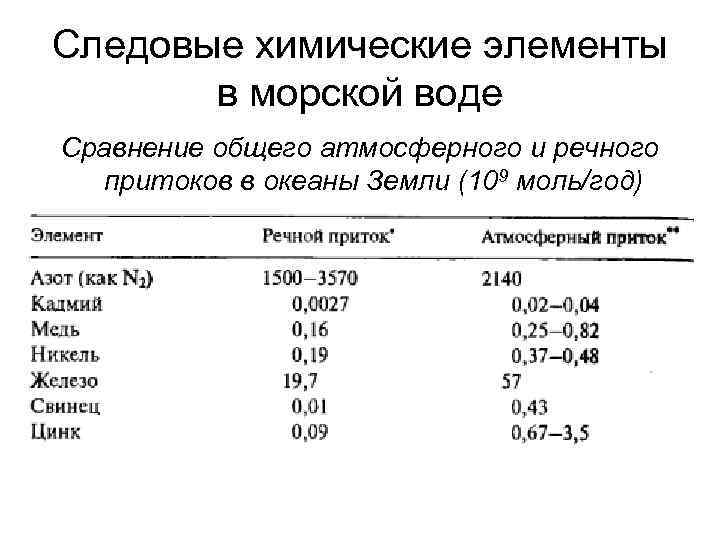 Следовые химические элементы в морской воде Сравнение общего атмосферного и речного притоков в океаны Земли (109 моль/год)
Следовые химические элементы в морской воде Сравнение общего атмосферного и речного притоков в океаны Земли (109 моль/год)
 Металлы (по поведению в процессе химического круговорота) делятся: 1. Консервативное поведение ( практически постоянные концентрации по всей глубине, длительные времена пребывания, хорошо перемешаны), например: Mo, W, Br-, Cs+ 2. Поведение по типу питательных веществ 3. Класс выноса - извлечение элементов
Металлы (по поведению в процессе химического круговорота) делятся: 1. Консервативное поведение ( практически постоянные концентрации по всей глубине, длительные времена пребывания, хорошо перемешаны), например: Mo, W, Br-, Cs+ 2. Поведение по типу питательных веществ 3. Класс выноса - извлечение элементов
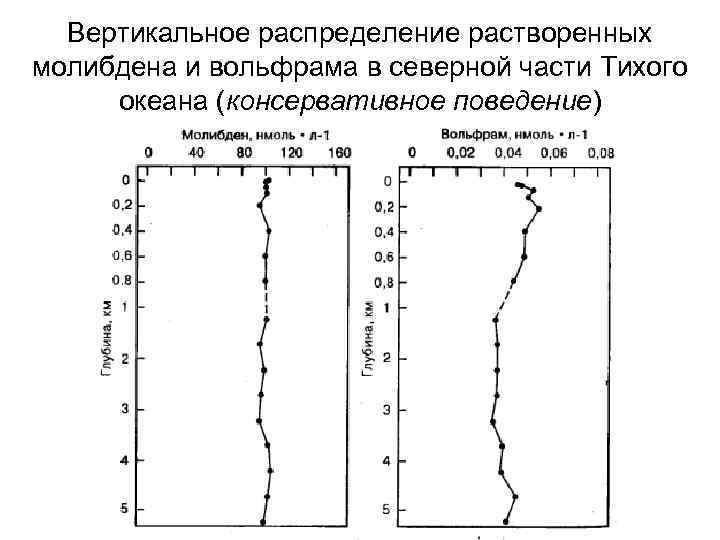 Вертикальное распределение растворенных молибдена и вольфрама в северной части Тихого океана (консервативное поведение)
Вертикальное распределение растворенных молибдена и вольфрама в северной части Тихого океана (консервативное поведение)
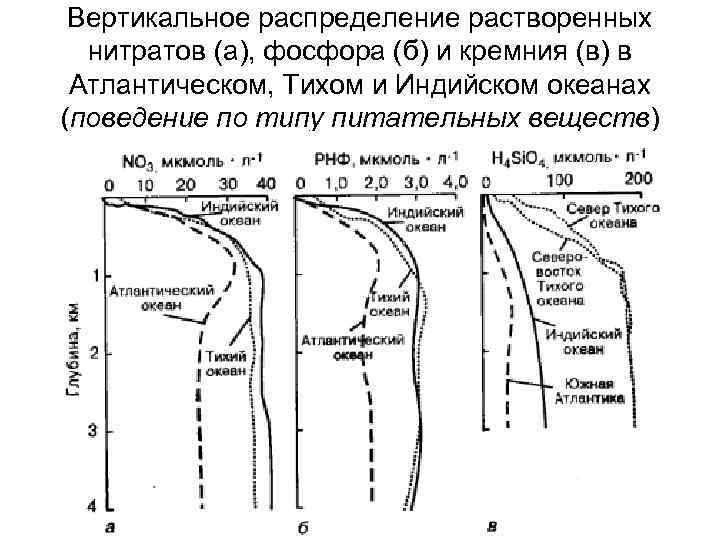 Вертикальное распределение растворенных нитратов (а), фосфора (б) и кремния (в) в Атлантическом, Тихом и Индийском океанах (поведение по типу питательных веществ)
Вертикальное распределение растворенных нитратов (а), фосфора (б) и кремния (в) в Атлантическом, Тихом и Индийском океанах (поведение по типу питательных веществ)
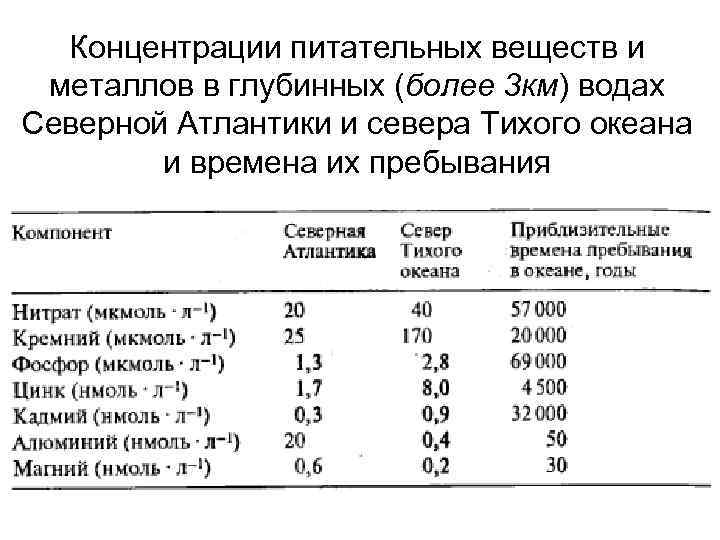 Концентрации питательных веществ и металлов в глубинных (более 3 км) водах Северной Атлантики и севера Тихого океана и времена их пребывания
Концентрации питательных веществ и металлов в глубинных (более 3 км) водах Северной Атлантики и севера Тихого океана и времена их пребывания
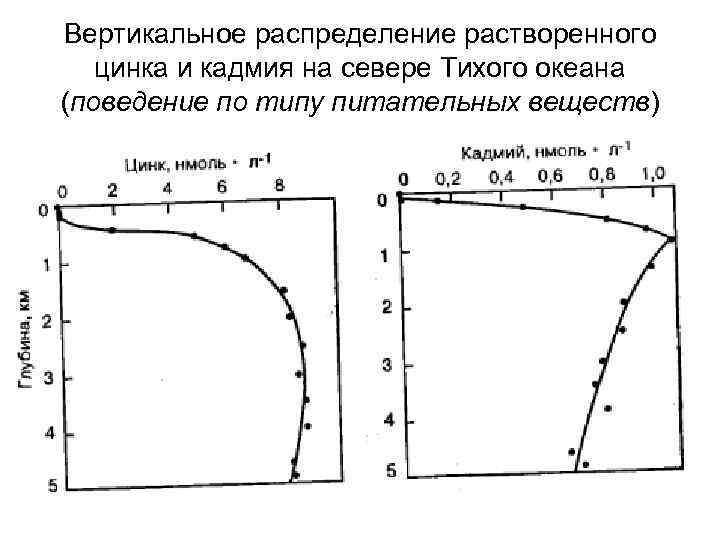 Вертикальное распределение растворенного цинка и кадмия на севере Тихого океана (поведение по типу питательных веществ)
Вертикальное распределение растворенного цинка и кадмия на севере Тихого океана (поведение по типу питательных веществ)
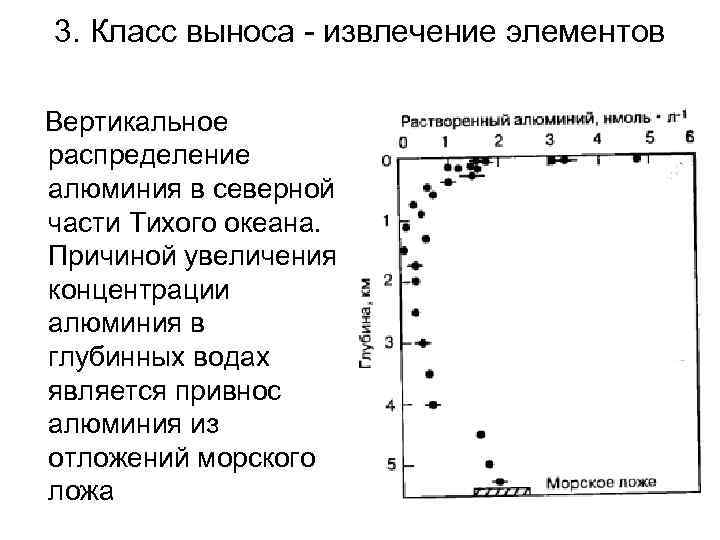 3. Класс выноса - извлечение элементов Вертикальное распределение алюминия в северной части Тихого океана. Причиной увеличения концентрации алюминия в глубинных водах является привнос алюминия из отложений морского ложа
3. Класс выноса - извлечение элементов Вертикальное распределение алюминия в северной части Тихого океана. Причиной увеличения концентрации алюминия в глубинных водах является привнос алюминия из отложений морского ложа
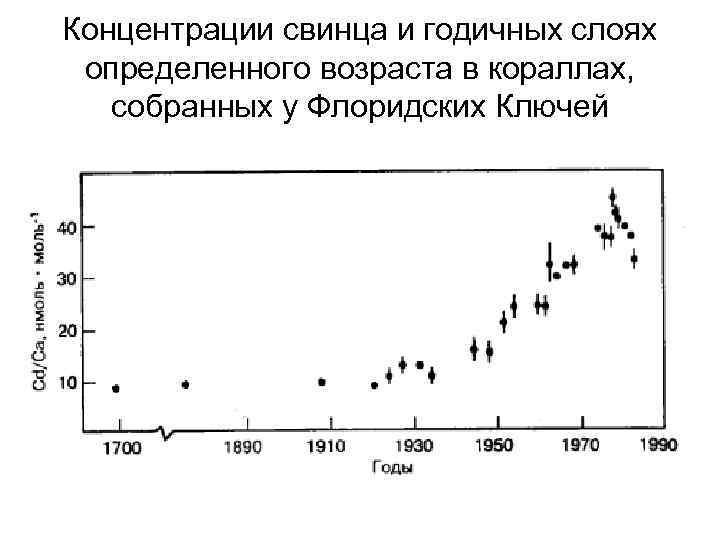 Концентрации свинца и годичных слоях определенного возраста в кораллах, собранных у Флоридских Ключей
Концентрации свинца и годичных слоях определенного возраста в кораллах, собранных у Флоридских Ключей
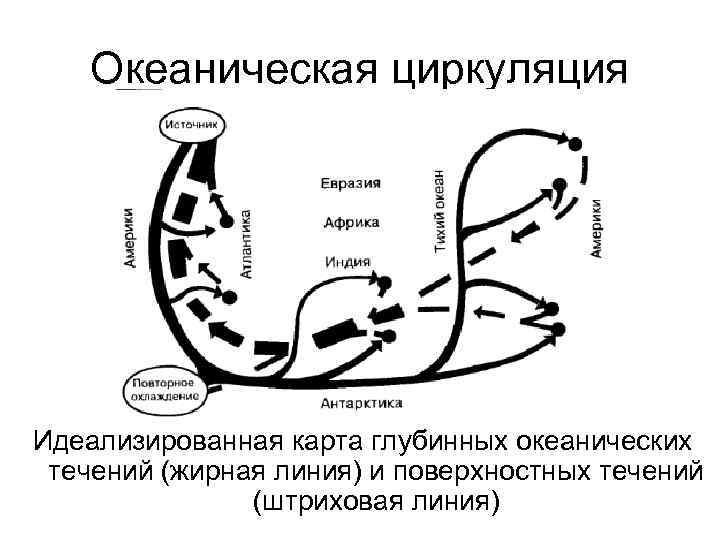 Океаническая циркуляция Идеализированная карта глубинных океанических течений (жирная линия) и поверхностных течений (штриховая линия)
Океаническая циркуляция Идеализированная карта глубинных океанических течений (жирная линия) и поверхностных течений (штриховая линия)
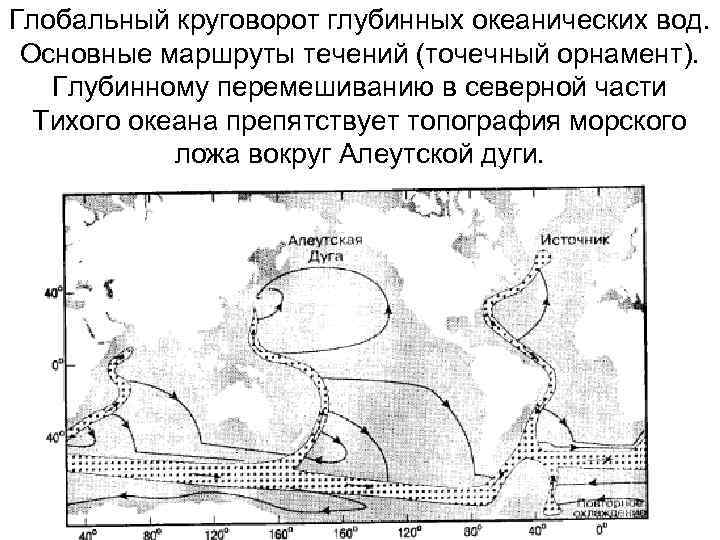 Глобальный круговорот глубинных океанических вод. Основные маршруты течений (точечный орнамент). Глубинному перемешиванию в северной части Тихого океана препятствует топография морского ложа вокруг Алеутской дуги.
Глобальный круговорот глубинных океанических вод. Основные маршруты течений (точечный орнамент). Глубинному перемешиванию в северной части Тихого океана препятствует топография морского ложа вокруг Алеутской дуги.

 Загрязнение вод Способы проникновения загрязнений: 1. Сброс сточных вод 2. Утечка или просачивание с последующим переносом 3. Перенос речным потоком 4. Взаимодействие и перенос на поверхности раздела воздух-вода и вода-воздух
Загрязнение вод Способы проникновения загрязнений: 1. Сброс сточных вод 2. Утечка или просачивание с последующим переносом 3. Перенос речным потоком 4. Взаимодействие и перенос на поверхности раздела воздух-вода и вода-воздух
 Источники загрязнения гидросферы: 1. Естественные (вулканическая деятельность, разрушение горных пород, продукты жизнедеятельности организмов и т. д. ) 2. Антропогенные: - токсичное (пестициды и др. ) - эвтрофирующее
Источники загрязнения гидросферы: 1. Естественные (вулканическая деятельность, разрушение горных пород, продукты жизнедеятельности организмов и т. д. ) 2. Антропогенные: - токсичное (пестициды и др. ) - эвтрофирующее

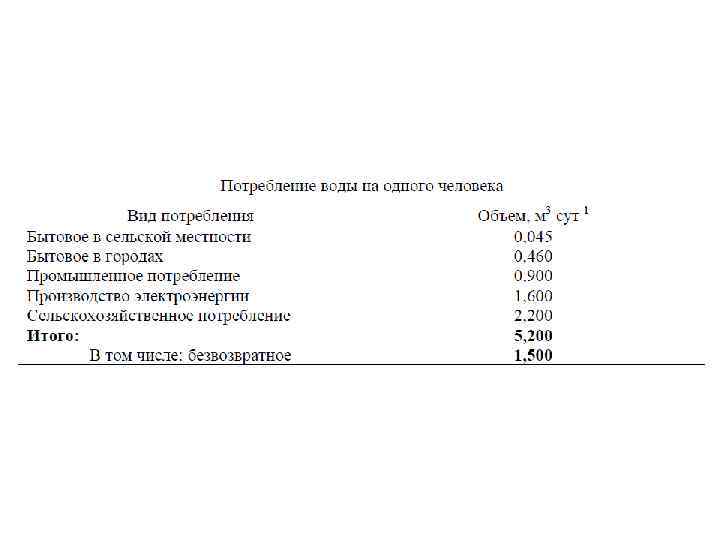
 Эвтрофицирование водоемов Эвтрофикация вод – повышение биологической продуктивности водных объектов, в первую очередь малых рек и водохранилищ на них, в результате накопления в воде биогенных веществ (азота и фосфора) под воздействием антропогенных или естественных факторов. Эвтрофицирование: естественное антропогенное
Эвтрофицирование водоемов Эвтрофикация вод – повышение биологической продуктивности водных объектов, в первую очередь малых рек и водохранилищ на них, в результате накопления в воде биогенных веществ (азота и фосфора) под воздействием антропогенных или естественных факторов. Эвтрофицирование: естественное антропогенное
 Естественное эвтрофирование – длительный процесс. Определяется действием абиотических факторов: 1. интенсивность солнечной радиации, 2. изменение климатических условий (зональные и сезонные различия величины и характера атмосферных осадков, колебание температуры, воздействие ветра), 3. величина водного стока, 4. зональное различие в гидрохимическом стоке (общая минерализация воды, различное содержание химических ингредиентов), Действие биотических факторов - биологические процессы в водоеме.
Естественное эвтрофирование – длительный процесс. Определяется действием абиотических факторов: 1. интенсивность солнечной радиации, 2. изменение климатических условий (зональные и сезонные различия величины и характера атмосферных осадков, колебание температуры, воздействие ветра), 3. величина водного стока, 4. зональное различие в гидрохимическом стоке (общая минерализация воды, различное содержание химических ингредиентов), Действие биотических факторов - биологические процессы в водоеме.
 Антропогенное эвтрофирование – очень быстрый процесс. Определяется: • сбросом в водоемы бытовых и промышленных сточных вод; • выносом с полей минеральных удобрений, пестицидов и ядохимикатов; • окультированием земель на площади водосбора и побережья водоемов; • регулированием режимов работы гидросооружений; • рекреационным использованием водоемов.
Антропогенное эвтрофирование – очень быстрый процесс. Определяется: • сбросом в водоемы бытовых и промышленных сточных вод; • выносом с полей минеральных удобрений, пестицидов и ядохимикатов; • окультированием земель на площади водосбора и побережья водоемов; • регулированием режимов работы гидросооружений; • рекреационным использованием водоемов.
 Критерии определения уровня трофности водоема: • уменьшение концентрации растворенного кислорода; • увеличение концентрации биогенных веществ; • увеличение содержания взвешенных частиц, особенно органического вещества; • последовательная смена популяций водорослей с преобладанием сине-зеленых или зеленых водорослей; • увеличение мутности (не проникновения света) водной среды; • увеличение концентрации фосфора в донных отложениях.
Критерии определения уровня трофности водоема: • уменьшение концентрации растворенного кислорода; • увеличение концентрации биогенных веществ; • увеличение содержания взвешенных частиц, особенно органического вещества; • последовательная смена популяций водорослей с преобладанием сине-зеленых или зеленых водорослей; • увеличение мутности (не проникновения света) водной среды; • увеличение концентрации фосфора в донных отложениях.
 Темы докладов: 1. Классификация природных вод. Показатели качества вод и способы их определения. 2. Загрязнение водных объектов пестицидами. 3. Загрязнение водных объектов синтетическими поверхностноактивными веществами (СПАВ).
Темы докладов: 1. Классификация природных вод. Показатели качества вод и способы их определения. 2. Загрязнение водных объектов пестицидами. 3. Загрязнение водных объектов синтетическими поверхностноактивными веществами (СПАВ).
 Темы докладов: 4. р. Н, механизм стабилизации р. Н в реках, озёрах, болотах, океанах, влияние изменения р. Н на гидросферу. 5. Влияние серосодержащих веществ на экосистемы водоёмов (механизм воздействия, возможные последствия). 6. Источники загрязнения гидросферы радиоактивными веществами, механизм радиационного загрязнения и возможные последствия.
Темы докладов: 4. р. Н, механизм стабилизации р. Н в реках, озёрах, болотах, океанах, влияние изменения р. Н на гидросферу. 5. Влияние серосодержащих веществ на экосистемы водоёмов (механизм воздействия, возможные последствия). 6. Источники загрязнения гидросферы радиоактивными веществами, механизм радиационного загрязнения и возможные последствия.
 Темы докладов: 7. Загрязнение водных объектов бытовыми сточными водами (источники загрязнения, последствия и т. д. ). 8. Загрязнение водных объектов нефтепродуктами. 9. Проблемы мирового океана.
Темы докладов: 7. Загрязнение водных объектов бытовыми сточными водами (источники загрязнения, последствия и т. д. ). 8. Загрязнение водных объектов нефтепродуктами. 9. Проблемы мирового океана.

 Литосфера – каменная оболочка Земли, включающая земную кору мощностью от 6 до 80 км (горные системы). Континентальная кора – громадный резервуар магматических и метаморфических пород (80%), покрытых осадочными породами (20%). Масса конт. коры составляет 23. 6*1024 т.
Литосфера – каменная оболочка Земли, включающая земную кору мощностью от 6 до 80 км (горные системы). Континентальная кора – громадный резервуар магматических и метаморфических пород (80%), покрытых осадочными породами (20%). Масса конт. коры составляет 23. 6*1024 т.
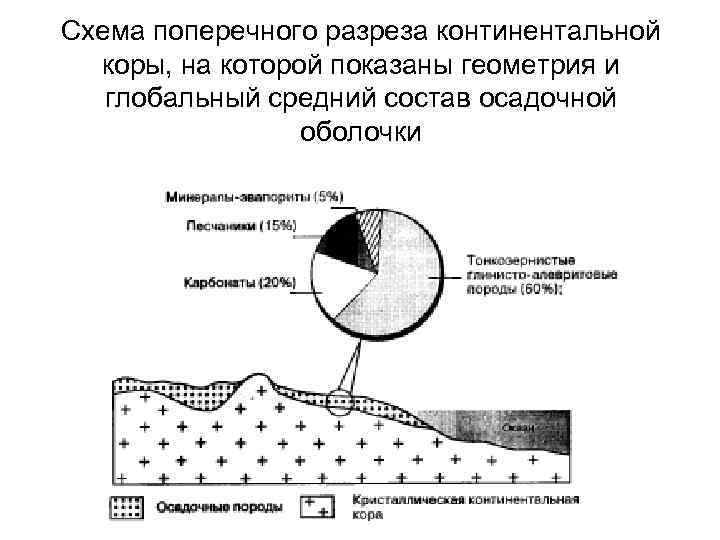 Схема поперечного разреза континентальной коры, на которой показаны геометрия и глобальный средний состав осадочной оболочки
Схема поперечного разреза континентальной коры, на которой показаны геометрия и глобальный средний состав осадочной оболочки
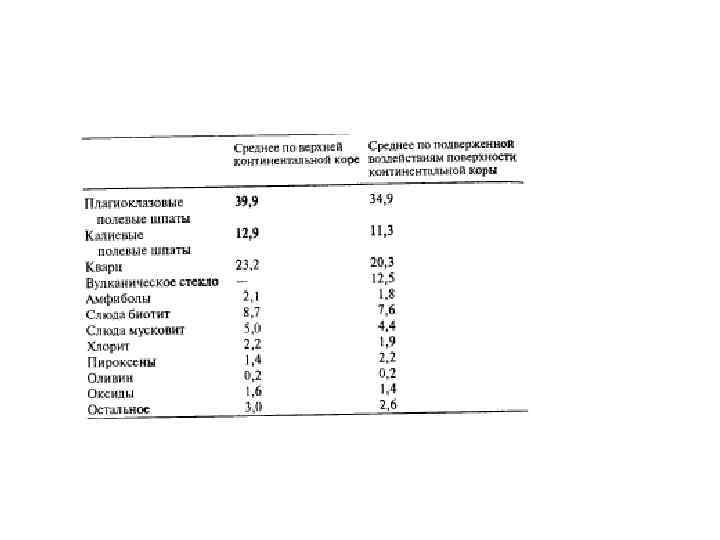
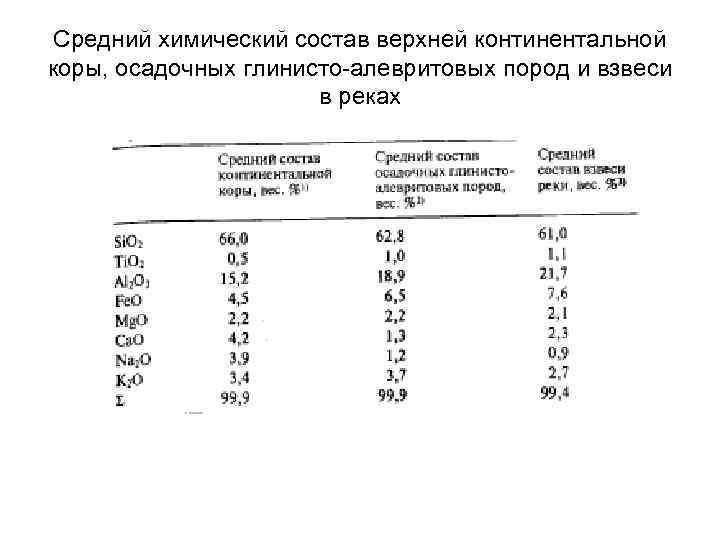 Средний химический состав верхней континентальной коры, осадочных глинисто-алевритовых пород и взвеси в реках
Средний химический состав верхней континентальной коры, осадочных глинисто-алевритовых пород и взвеси в реках
 Структура континентальной коры Многие твердые вещества коры реакционноспособны: • Радиоактивные элементы (уран, калий и т. д. ) • Некоторые нестабильные минералы (выветривание при изменении t или P)
Структура континентальной коры Многие твердые вещества коры реакционноспособны: • Радиоактивные элементы (уран, калий и т. д. ) • Некоторые нестабильные минералы (выветривание при изменении t или P)
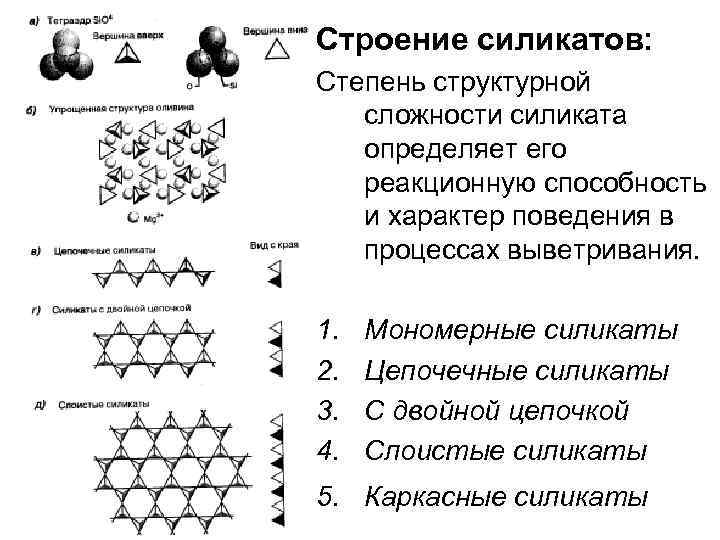 Строение силикатов: Степень структурной сложности силиката определяет его реакционную способность и характер поведения в процессах выветривания. 1. 2. 3. 4. Мономерные силикаты Цепочечные силикаты С двойной цепочкой Слоистые силикаты 5. Каркасные силикаты
Строение силикатов: Степень структурной сложности силиката определяет его реакционную способность и характер поведения в процессах выветривания. 1. 2. 3. 4. Мономерные силикаты Цепочечные силикаты С двойной цепочкой Слоистые силикаты 5. Каркасные силикаты
 Процессы выветривания Выветривание – процесс разрушения и изменения горных пород и минералов в приповерхностных условиях под воздействием физико-химических факторов атмосферы, гидросферы и биосферы. Факторы выветривания: • Колебания температур; • Химические агенты (О 2, Н 2 О, СО 2); • Органические кислоты; • Микроорганизмы.
Процессы выветривания Выветривание – процесс разрушения и изменения горных пород и минералов в приповерхностных условиях под воздействием физико-химических факторов атмосферы, гидросферы и биосферы. Факторы выветривания: • Колебания температур; • Химические агенты (О 2, Н 2 О, СО 2); • Органические кислоты; • Микроорганизмы.
 Процессы выветривания 1. Физическое выветривание – механический процесс размельчения породы до частиц меньшего размера без существенных изменений в химическом составе: 2. Химическое выветривание – разрушение горных пород с изменением их химического состава: • растворение; • окисление; • гидратация; • гидролиз.
Процессы выветривания 1. Физическое выветривание – механический процесс размельчения породы до частиц меньшего размера без существенных изменений в химическом составе: 2. Химическое выветривание – разрушение горных пород с изменением их химического состава: • растворение; • окисление; • гидратация; • гидролиз.
 Механизмы химического выветривания • Растворение минералов (не зависит от р. Н): • Окисление: В окисление сульфидов вовлечены микроорганизмы : (окисление пирита)
Механизмы химического выветривания • Растворение минералов (не зависит от р. Н): • Окисление: В окисление сульфидов вовлечены микроорганизмы : (окисление пирита)
 Механизмы химического выветривания Затем окисление 2 -х валентного железа (при низких значениях р. Н): При р. Н менее 3. 5 окисление катализируется железобактериями. Окисленное железо взаимодействует с пиритом:
Механизмы химического выветривания Затем окисление 2 -х валентного железа (при низких значениях р. Н): При р. Н менее 3. 5 окисление катализируется железобактериями. Окисленное железо взаимодействует с пиритом:
 Механизмы химического выветривания При значениям р. Н значительно выше 3 железо (III) осаждается как обычный оксид (гетит): Восстановленные железосодержащие силикаты также могут окисляться (напр. фаялит (богатый железом оливин):
Механизмы химического выветривания При значениям р. Н значительно выше 3 железо (III) осаждается как обычный оксид (гетит): Восстановленные железосодержащие силикаты также могут окисляться (напр. фаялит (богатый железом оливин):
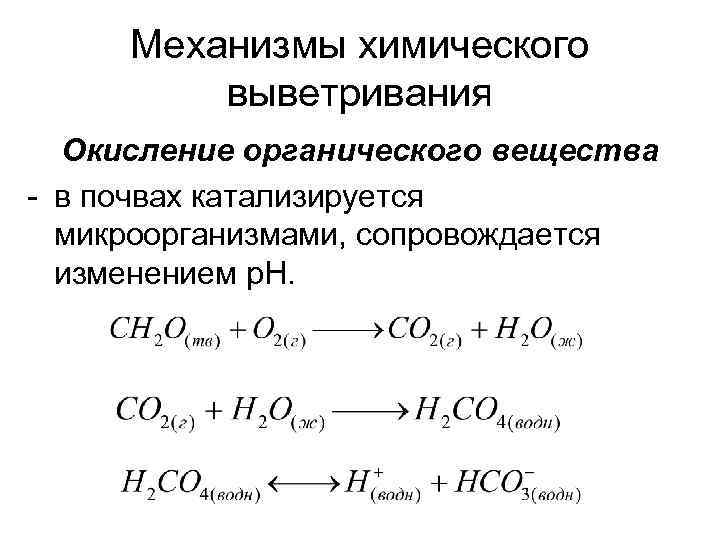 Механизмы химического выветривания Окисление органического вещества - в почвах катализируется микроорганизмами, сопровождается изменением р. Н.
Механизмы химического выветривания Окисление органического вещества - в почвах катализируется микроорганизмами, сопровождается изменением р. Н.
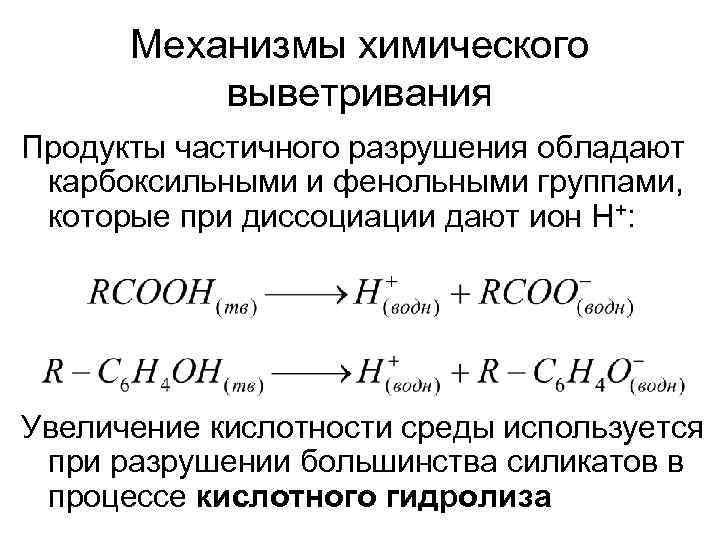 Механизмы химического выветривания Продукты частичного разрушения обладают карбоксильными и фенольными группами, которые при диссоциации дают ион Н+: Увеличение кислотности среды используется при разрушении большинства силикатов в процессе кислотного гидролиза
Механизмы химического выветривания Продукты частичного разрушения обладают карбоксильными и фенольными группами, которые при диссоциации дают ион Н+: Увеличение кислотности среды используется при разрушении большинства силикатов в процессе кислотного гидролиза
 Механизмы химического выветривания Кислотный гидролиз - реакция между минералом и кислыми агентами выветривания. Выветривание Сa. CO 3: Кислотный гидролиз силиката богатого магнием оливина (форстерит):
Механизмы химического выветривания Кислотный гидролиз - реакция между минералом и кислыми агентами выветривания. Выветривание Сa. CO 3: Кислотный гидролиз силиката богатого магнием оливина (форстерит):
 Механизмы химического выветривания Усредненный процесс химического выветривания сложных силикатов (на примере плагиоклаза богатого Са):
Механизмы химического выветривания Усредненный процесс химического выветривания сложных силикатов (на примере плагиоклаза богатого Са):

 Темы докладов: 1. Источники загрязнения литосферы радиоактивными отходами, механизм воздействия этого явления. 2. Токсикация почв тяжёлыми металлами. 3. Влияние атмосферных и гидросферных загрязнений на деградацию литосферы. 4. Руды: извлечение, обогащение, получение основных компонентов, образование отходов, их свойства.
Темы докладов: 1. Источники загрязнения литосферы радиоактивными отходами, механизм воздействия этого явления. 2. Токсикация почв тяжёлыми металлами. 3. Влияние атмосферных и гидросферных загрязнений на деградацию литосферы. 4. Руды: извлечение, обогащение, получение основных компонентов, образование отходов, их свойства.
 Темы докладов: 5. Генная инженерия в сельском хозяйстве: за и против! 6. Глобальное потепление: человек или природа? 7. Массовое вымирание видов 8. Потеря почвенных ресурсов 9. Переработка и утилизация ТБО 10. Ядерные катастрофы. Их последствия.
Темы докладов: 5. Генная инженерия в сельском хозяйстве: за и против! 6. Глобальное потепление: человек или природа? 7. Массовое вымирание видов 8. Потеря почвенных ресурсов 9. Переработка и утилизация ТБО 10. Ядерные катастрофы. Их последствия.

 Биогеохимические циклы
Биогеохимические циклы
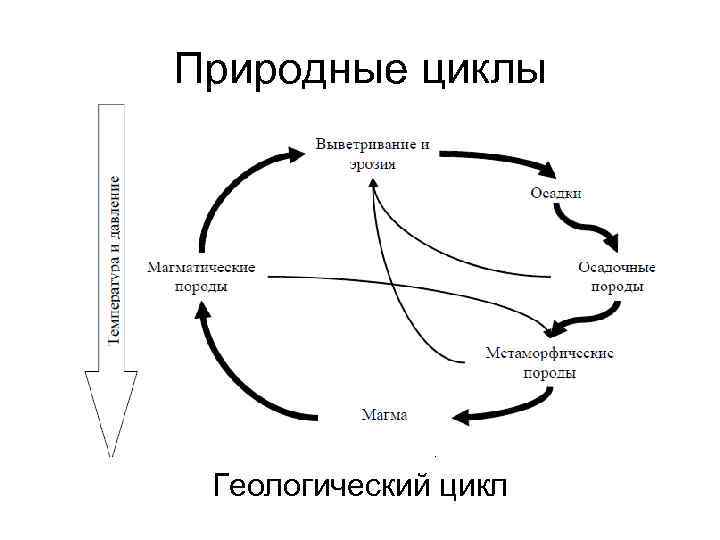 Природные циклы Геологический цикл
Природные циклы Геологический цикл
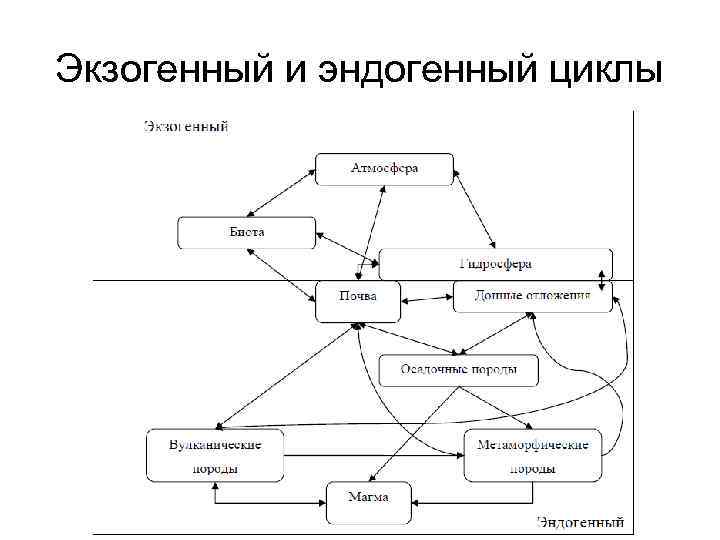 Экзогенный и эндогенный циклы
Экзогенный и эндогенный циклы
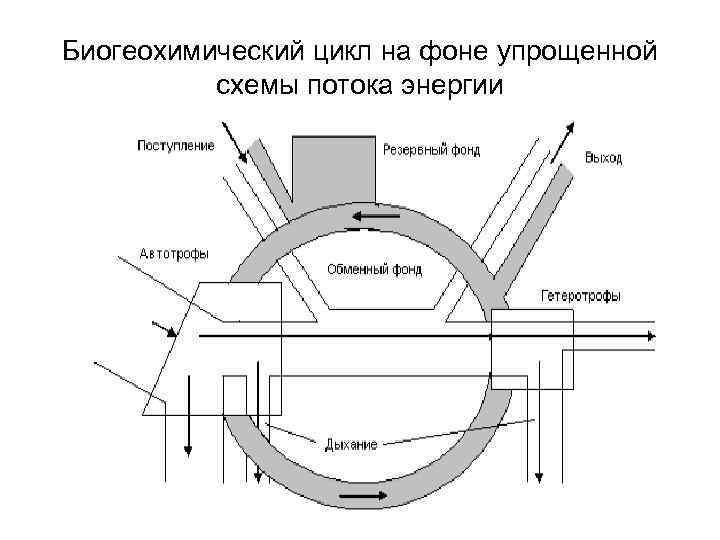 Биогеохимический цикл на фоне упрощенной схемы потока энергии
Биогеохимический цикл на фоне упрощенной схемы потока энергии
 • Обменный фонд – вещество которого совершает постоянную циркуляцию между живыми организмами и окружающей их средой. • Резервный фонд - вещество которого не участвует в данный момент в круговороте, но которое может быть вовлечено.
• Обменный фонд – вещество которого совершает постоянную циркуляцию между живыми организмами и окружающей их средой. • Резервный фонд - вещество которого не участвует в данный момент в круговороте, но которое может быть вовлечено.
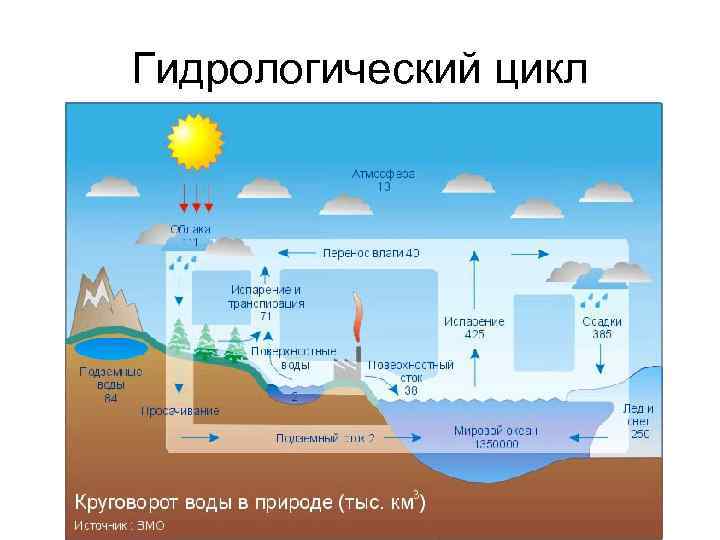 Гидрологический цикл
Гидрологический цикл
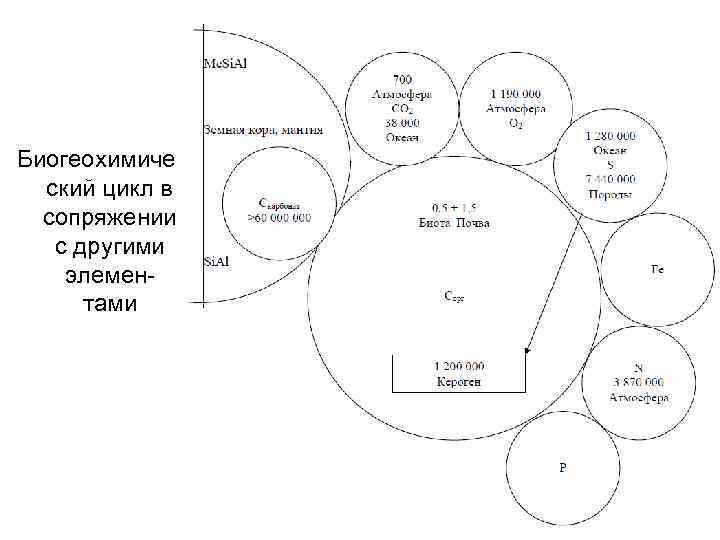 Биогеохимиче ский цикл в сопряжении с другими элементами
Биогеохимиче ский цикл в сопряжении с другими элементами
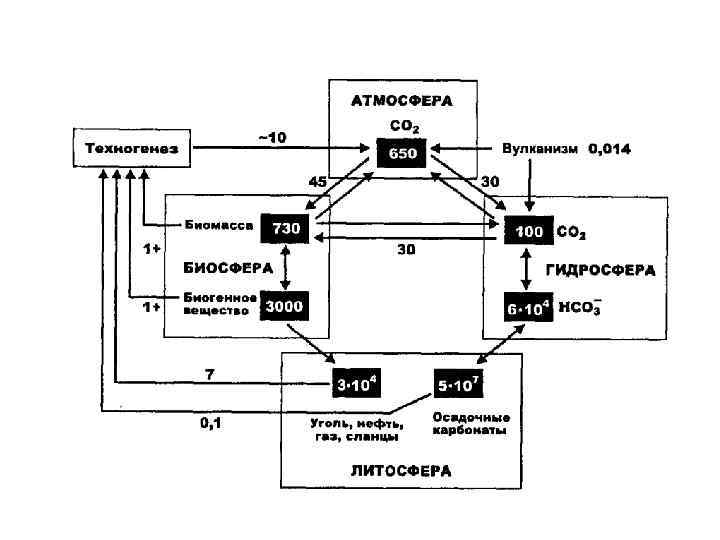
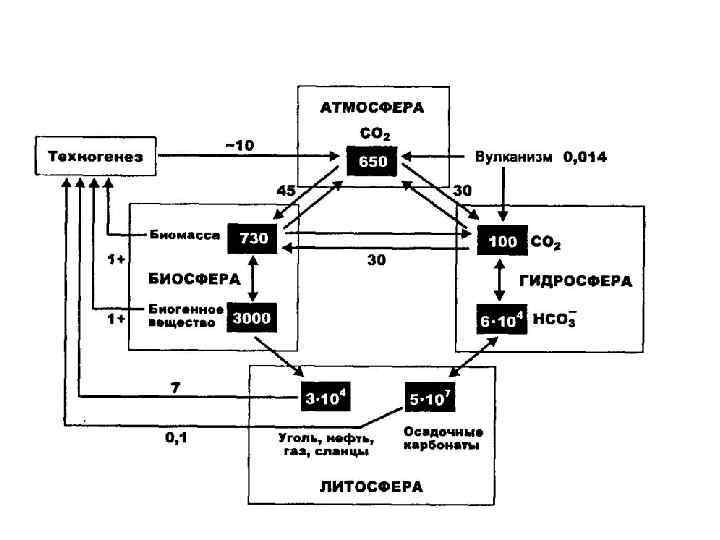
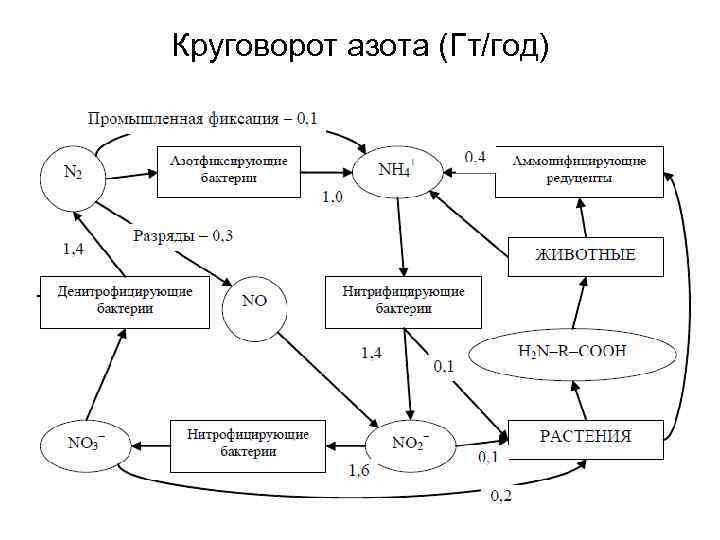 Круговорот азота (Гт/год)
Круговорот азота (Гт/год)
 Фиксация азота Микроорганизмы путём прямой фиксации непосредственно извлекают азот из атмосферы и связывают его в почве: • некоторые свободноживущие почвенные бактерии; • симбионтные клубеньковые бактерии (существующие в симбиозе с бобовыми); • цианобионты, которые также бывают симбионтами грибов, мхов, папоротников, а иногда и высших растений. Фиксация азота организмами происходит в нитритную форму (соединения на основе NH 3), далее связываясь с почвенной влагой он переходит в нитратную форму.
Фиксация азота Микроорганизмы путём прямой фиксации непосредственно извлекают азот из атмосферы и связывают его в почве: • некоторые свободноживущие почвенные бактерии; • симбионтные клубеньковые бактерии (существующие в симбиозе с бобовыми); • цианобионты, которые также бывают симбионтами грибов, мхов, папоротников, а иногда и высших растений. Фиксация азота организмами происходит в нитритную форму (соединения на основе NH 3), далее связываясь с почвенной влагой он переходит в нитратную форму.
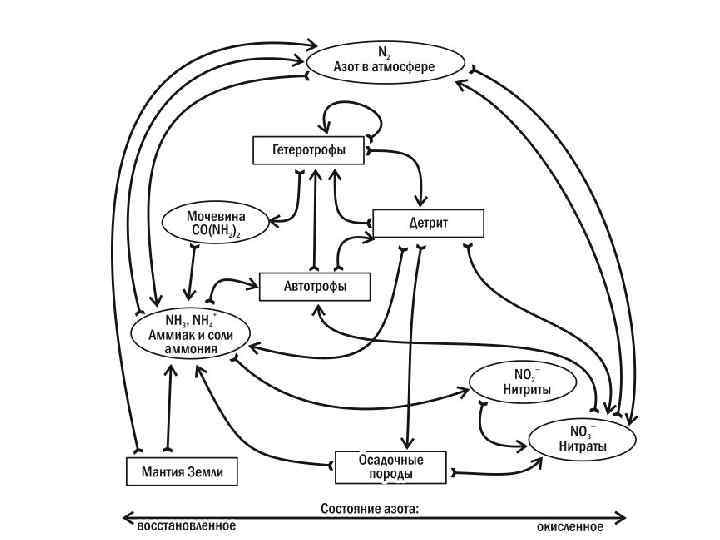
 Основные специфические черты круговорота азота • преимущественную концентрацию в атмосфере, играющей исключительную роль резервуара, из которой живые организмы черпают запасы необходимого им азота; • ведущую роль в круговороте азота почв и почвенных микроорганизмов, деятельность которых обеспечивает переход азота в биосфере из одних форм в другие. • • Содержание азота в связанном виде в биосфере: органическое вещество почвенного покрова (1, 5 х1011 т), биомасса растений (1, 1 х109 т), биомасса животных (6, 1 х107 т). некоторые биогенные ископаемые (селитры).
Основные специфические черты круговорота азота • преимущественную концентрацию в атмосфере, играющей исключительную роль резервуара, из которой живые организмы черпают запасы необходимого им азота; • ведущую роль в круговороте азота почв и почвенных микроорганизмов, деятельность которых обеспечивает переход азота в биосфере из одних форм в другие. • • Содержание азота в связанном виде в биосфере: органическое вещество почвенного покрова (1, 5 х1011 т), биомасса растений (1, 1 х109 т), биомасса животных (6, 1 х107 т). некоторые биогенные ископаемые (селитры).
 Фиксация азота бактериями, делает его доступным для остальной части биоты: С учетом азота и фосфора уравнение фотосинтеза/дыхания имеет вид:
Фиксация азота бактериями, делает его доступным для остальной части биоты: С учетом азота и фосфора уравнение фотосинтеза/дыхания имеет вид:
 • Мочевина, накапливаемая биологическим путем (в моче животных), в результате гидролиза разлагается (в щелочной среде): • в кислой среде : Некоторые микроорганизмы, например Nitrosomonas, окисляют NH 4+, используя его в качестве источника энергии в процессе дыхания:
• Мочевина, накапливаемая биологическим путем (в моче животных), в результате гидролиза разлагается (в щелочной среде): • в кислой среде : Некоторые микроорганизмы, например Nitrosomonas, окисляют NH 4+, используя его в качестве источника энергии в процессе дыхания:
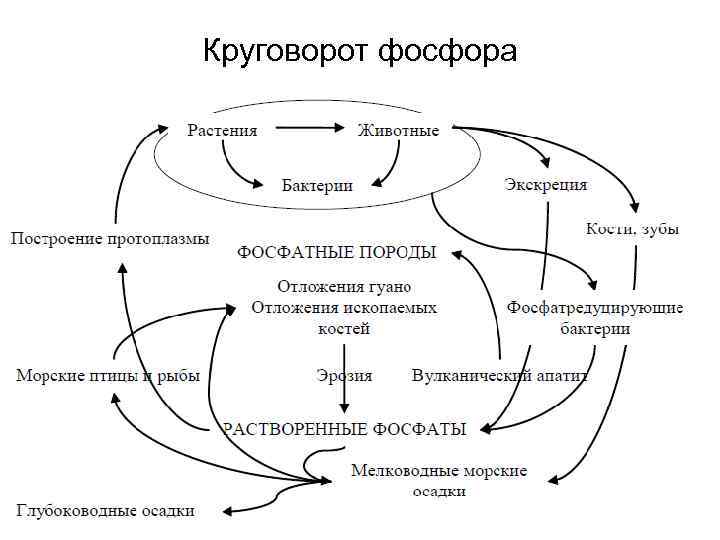 Круговорот фосфора
Круговорот фосфора
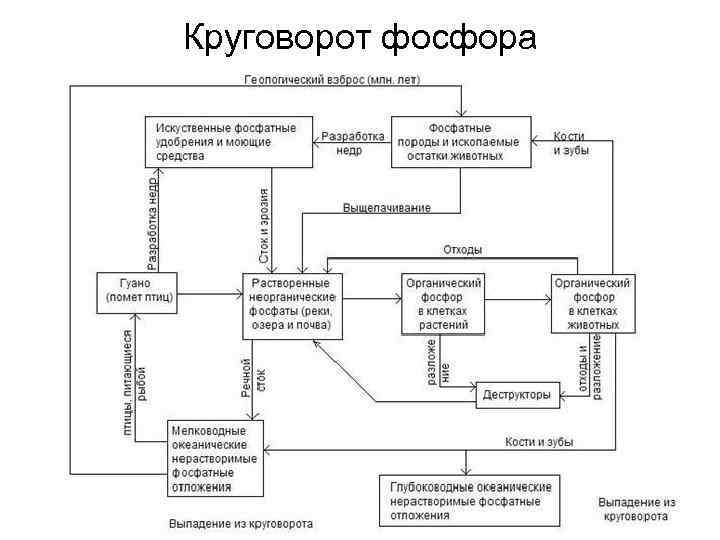 Круговорот фосфора
Круговорот фосфора
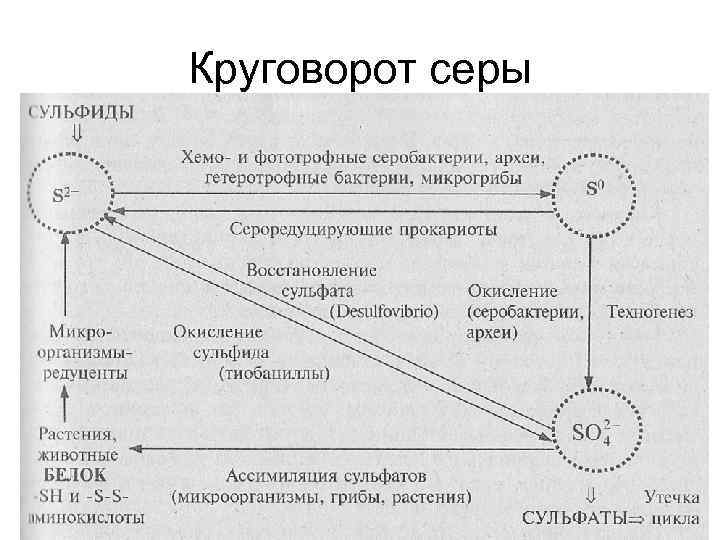 Круговорот серы
Круговорот серы
 Основной источник серы – выветривание из осадочного резервного фонда (сульфидсодержащих горных пород): Сульфатредуцирующие бактерии в отсутствии кислорода образуют H 2 S:
Основной источник серы – выветривание из осадочного резервного фонда (сульфидсодержащих горных пород): Сульфатредуцирующие бактерии в отсутствии кислорода образуют H 2 S:
 В присутствии кислорода ряд бактерий окисляют H 2 S до: Некоторые бактерии окисляют сульфиты до серы и сульфатов:
В присутствии кислорода ряд бактерий окисляют H 2 S до: Некоторые бактерии окисляют сульфиты до серы и сульфатов:
 Связи между циклами элементов В отсутствии О 2 некоторые бактерии окисляют серу и сульфиты, используя нитраты (циклы азота и серы): Зеленые серные бактерии используют серу в хемосинтезе орган. вещества: И пурпурные бактерии:
Связи между циклами элементов В отсутствии О 2 некоторые бактерии окисляют серу и сульфиты, используя нитраты (циклы азота и серы): Зеленые серные бактерии используют серу в хемосинтезе орган. вещества: И пурпурные бактерии:
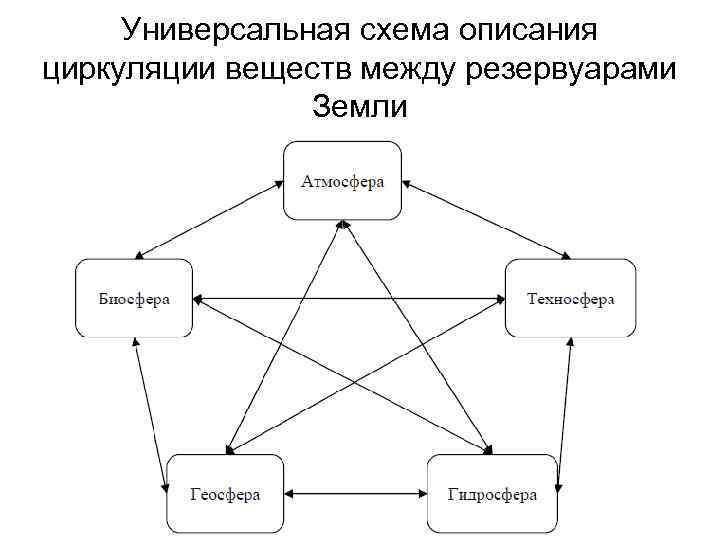 Универсальная схема описания циркуляции веществ между резервуарами Земли
Универсальная схема описания циркуляции веществ между резервуарами Земли


