Химия презентация Кузьмина Алиса 7б.pptx
- Количество слайдов: 11
 химия Металлы
химия Металлы
 Мета ллы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ обладающих характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск
Мета ллы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ обладающих характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск
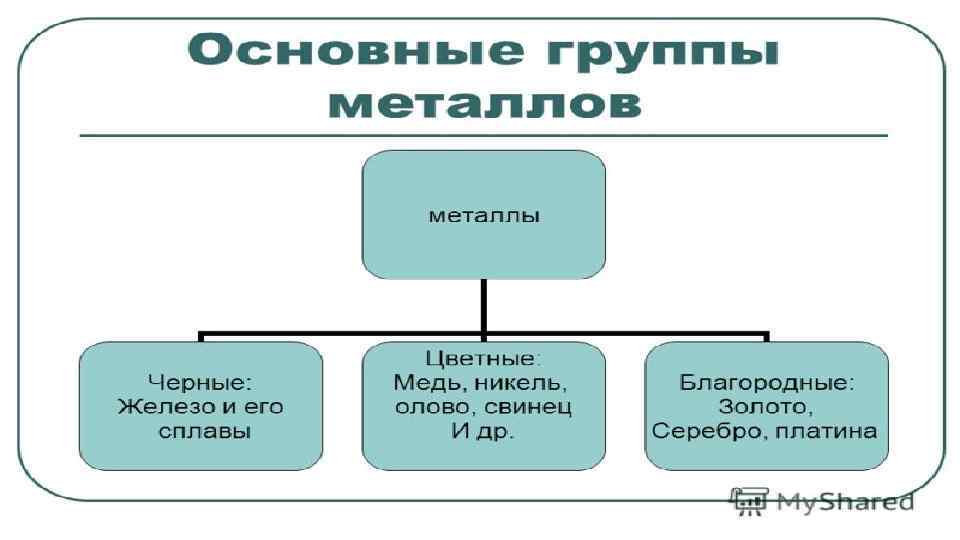
 На сегодня известно 114 химических элементов. Из них 96 – это металлы. Без металлов жизнь на Земле была бы невозможной, так как они в чистом виде или их соединения являются важнейшей составляющей органической и минеральной среды, активно участвуя в процессах жизнедеятельности всех живых организмов. Разделяют металлы на переходные и непереходные. Такая классификация исходит из месторасположения элемента в таблице периодичности Менделеева. Переходные металлы относят к побочным подгруппам, а непереходные – к главным.
На сегодня известно 114 химических элементов. Из них 96 – это металлы. Без металлов жизнь на Земле была бы невозможной, так как они в чистом виде или их соединения являются важнейшей составляющей органической и минеральной среды, активно участвуя в процессах жизнедеятельности всех живых организмов. Разделяют металлы на переходные и непереходные. Такая классификация исходит из месторасположения элемента в таблице периодичности Менделеева. Переходные металлы относят к побочным подгруппам, а непереходные – к главным.
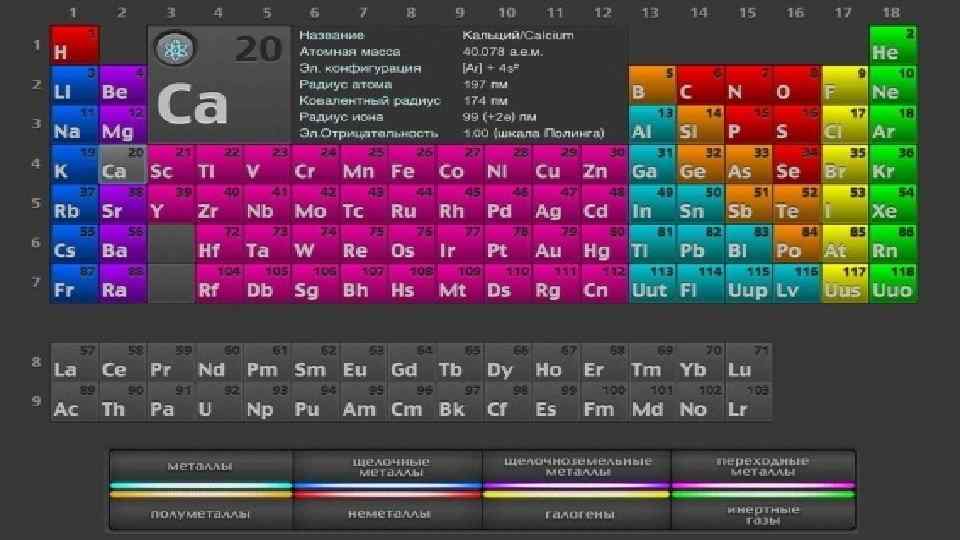
 Если в периодической таблице элементов Д. И. Менделеева провести диагональ от бериллия к астату, то слева внизу по диагонали будут находиться элементы-металлы (к ним же относятся элементы побочных подгрупп), а справа вверху – элементынеметаллы.
Если в периодической таблице элементов Д. И. Менделеева провести диагональ от бериллия к астату, то слева внизу по диагонали будут находиться элементы-металлы (к ним же относятся элементы побочных подгрупп), а справа вверху – элементынеметаллы.
 - Пластичность - способность изменять форму при ударе, вытягиваться в проволоку, прокатываться в тонкие листы - Блеск - обычно серый цвет и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл квантами света. Общие - Электропроводность -Объясняется направленным движением свободных физические электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. При нагревании электропроводность уменьшается, т. к. с повышением температуры усиливаются колебания атомов и свойства ионов в узлах кристаллической решетки, что затрудняет направленное движение "электронного газа". металлов - Теплопроводность. Закономерность та же. Обусловлена высокой подвижностью свободных электронов и колебательным движением атомов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность - у висмута и ртути -Твердость. Самый твердый – хром (режет стекло); самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом -Плотность. Она тем меньше, чем меньше атомная масса металла и чем больше радиус его атома - Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т. пл. = 390 C), самый тугоплавкий металл – вольфрам (t 0 пл. = 33900 C). Металлы с t 0 пл. выше 10000 C считаются тугоплавкими, ниже – низкоплавкими.
- Пластичность - способность изменять форму при ударе, вытягиваться в проволоку, прокатываться в тонкие листы - Блеск - обычно серый цвет и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл квантами света. Общие - Электропроводность -Объясняется направленным движением свободных физические электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. При нагревании электропроводность уменьшается, т. к. с повышением температуры усиливаются колебания атомов и свойства ионов в узлах кристаллической решетки, что затрудняет направленное движение "электронного газа". металлов - Теплопроводность. Закономерность та же. Обусловлена высокой подвижностью свободных электронов и колебательным движением атомов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность - у висмута и ртути -Твердость. Самый твердый – хром (режет стекло); самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом -Плотность. Она тем меньше, чем меньше атомная масса металла и чем больше радиус его атома - Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т. пл. = 390 C), самый тугоплавкий металл – вольфрам (t 0 пл. = 33900 C). Металлы с t 0 пл. выше 10000 C считаются тугоплавкими, ниже – низкоплавкими.
 Общие способы получения металлов Электрометаллургия-получение металлов электролизом расплавов (для наиболее активных металлов) или растворов солей. Пирометаллургия-восстановление металлов из руд при высокой температуре (например, получение железа в доменном процессе) Гидрометаллургия-выделение металлов из растворов их солей более активными металлами (например, получение меди из раствора Cu. SO 4 действием цинка, железа или алюминия).
Общие способы получения металлов Электрометаллургия-получение металлов электролизом расплавов (для наиболее активных металлов) или растворов солей. Пирометаллургия-восстановление металлов из руд при высокой температуре (например, получение железа в доменном процессе) Гидрометаллургия-выделение металлов из растворов их солей более активными металлами (например, получение меди из раствора Cu. SO 4 действием цинка, железа или алюминия).

 Физические свойства металлов Тверды они все, кроме ртути, Блестящи и твёрды по сути. Беда у них тоже одна Коррозия ест их до дна. Химические свойства металлов Они расходятся, как в море корабли, И целые союзы заключают. Металл бывает очень многололик. Во многие реакции вступает: С кислородом, водой, щелочами. И, конечно же, с водою и солями. Не признают металлы водород: При встрече вытесняют из кислот. Металл всегда восстановитель, Так называемый "строитель".
Физические свойства металлов Тверды они все, кроме ртути, Блестящи и твёрды по сути. Беда у них тоже одна Коррозия ест их до дна. Химические свойства металлов Они расходятся, как в море корабли, И целые союзы заключают. Металл бывает очень многололик. Во многие реакции вступает: С кислородом, водой, щелочами. И, конечно же, с водою и солями. Не признают металлы водород: При встрече вытесняют из кислот. Металл всегда восстановитель, Так называемый "строитель".
 Презентацию подготовила Кузьмина Алиса 7 б
Презентацию подготовила Кузьмина Алиса 7 б


