b42858d853fb564c9c81248784f277d5.ppt
- Количество слайдов: 59
 Химия как наука. Основные понятия химии. Великие химические открытия Еремин Вадим Владимирович Химический факультет МГУ
Химия как наука. Основные понятия химии. Великие химические открытия Еремин Вадим Владимирович Химический факультет МГУ
 Часть 1. Химия как наука
Часть 1. Химия как наука
 Наука – способ познания реального мира, основанный на построении проверяемых моделей этой реальности. Три ключевых слова: 1)Реальный мир – мир опытный 2)Модели – приближенное описание 3)Проверяемые – эксперимент 3
Наука – способ познания реального мира, основанный на построении проверяемых моделей этой реальности. Три ключевых слова: 1)Реальный мир – мир опытный 2)Модели – приближенное описание 3)Проверяемые – эксперимент 3
 Другие способы познания НАУКА ИСКУССТВО рациональное эмоциональное мир опытный. . . . мир сверхопытный рациональное эмоциональное ФИЛОСОФИЯ РЕЛИГИЯ 4
Другие способы познания НАУКА ИСКУССТВО рациональное эмоциональное мир опытный. . . . мир сверхопытный рациональное эмоциональное ФИЛОСОФИЯ РЕЛИГИЯ 4
 Науки о природе Физика изучает наиболее общие свойства и законы движения объектов материального мира Химия наука о веществах, их строении, свойствах и превращениях Биология наука о живых системах 5
Науки о природе Физика изучает наиболее общие свойства и законы движения объектов материального мира Химия наука о веществах, их строении, свойствах и превращениях Биология наука о живых системах 5
 6 атомно-молекулярная картина мира В основе химического мышления –
6 атомно-молекулярная картина мира В основе химического мышления –
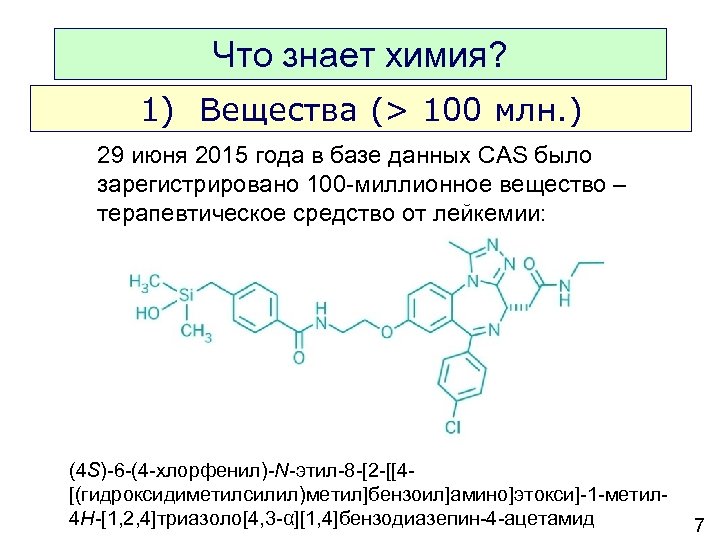 Что знает химия? 1) Вещества (> 100 млн. ) 29 июня 2015 года в базе данных CAS было зарегистрировано 100 -миллионное вещество – терапевтическое средство от лейкемии: (4 S)-6 -(4 -хлорфенил)-N-этил-8 -[2 -[[4[(гидроксидиметилсилил)метил]бензоил]амино]этокси]-1 -метил 4 H-[1, 2, 4]триазоло[4, 3 -α][1, 4]бензодиазепин-4 -ацетамид 7
Что знает химия? 1) Вещества (> 100 млн. ) 29 июня 2015 года в базе данных CAS было зарегистрировано 100 -миллионное вещество – терапевтическое средство от лейкемии: (4 S)-6 -(4 -хлорфенил)-N-этил-8 -[2 -[[4[(гидроксидиметилсилил)метил]бензоил]амино]этокси]-1 -метил 4 H-[1, 2, 4]триазоло[4, 3 -α][1, 4]бензодиазепин-4 -ацетамид 7
 Что надо знать о веществах? 1. 2. 3. 4. 5. Формула (из чего состоит) Структура (как устроено) Физические свойства Химические свойства Способы получения (лаб. и промышл. ) 6. Практическое применение 8
Что надо знать о веществах? 1. 2. 3. 4. 5. Формула (из чего состоит) Структура (как устроено) Физические свойства Химические свойства Способы получения (лаб. и промышл. ) 6. Практическое применение 8
 Что знает химия? 2) Химические реакции (> 80 млн. ) Что надо знать о химической реакции? 1. Условия проведения – температура, давление, агрегатное состояние веществ, растворитель, катализатор. 2. Энергетические и временные характеристики – теплота и скорость реакции. 9
Что знает химия? 2) Химические реакции (> 80 млн. ) Что надо знать о химической реакции? 1. Условия проведения – температура, давление, агрегатное состояние веществ, растворитель, катализатор. 2. Энергетические и временные характеристики – теплота и скорость реакции. 9
 Особенности химии как науки • Отсутствие собственных, чисто химических законов – все законы химии имеют физическую природу • Многообразие объектов • Создание собственного предмета для изучения – большинство из 100 млн. веществ не существует в природе. • Химия сама создает свой предмет! 10
Особенности химии как науки • Отсутствие собственных, чисто химических законов – все законы химии имеют физическую природу • Многообразие объектов • Создание собственного предмета для изучения – большинство из 100 млн. веществ не существует в природе. • Химия сама создает свой предмет! 10
 Основные вопросы химии • Какие бывают вещества? • Как они устроены? Как связано строение веществ с их свойствами? • Как создать вещество с заданными свойствами? (Зачем? – На этот вопрос химия не отвечает) • Почему и как идут химические реакции? • Как из одного вещества получить другое, более полезное или интересное? 11
Основные вопросы химии • Какие бывают вещества? • Как они устроены? Как связано строение веществ с их свойствами? • Как создать вещество с заданными свойствами? (Зачем? – На этот вопрос химия не отвечает) • Почему и как идут химические реакции? • Как из одного вещества получить другое, более полезное или интересное? 11
 Стругацкие. «Понедельник начинается в субботу» «А чем вы занимаетесь? » – спросил я. «Как и всякая наука, – сказал горбоносый. – Счастьем человеческим» «Понятно, – сказал я. – Что-нибудь с космосом? » «И с космосом тоже» 12
Стругацкие. «Понедельник начинается в субботу» «А чем вы занимаетесь? » – спросил я. «Как и всякая наука, – сказал горбоносый. – Счастьем человеческим» «Понятно, – сказал я. – Что-нибудь с космосом? » «И с космосом тоже» 12
 Цели химии 1) Понять, как устроен мир веществ 2) Изменить мир, сделать его более удобным для проживания Основная практическая задача химии – создание веществ с полезными свойствами 13
Цели химии 1) Понять, как устроен мир веществ 2) Изменить мир, сделать его более удобным для проживания Основная практическая задача химии – создание веществ с полезными свойствами 13
 Никто не сделал так много для улучшения условий жизни людей, как химики. Г. Крото, Нобелевский лауреат по химии 1996 г. Может ли химия сделать людей лучше? – Нет! – А что может? – Поэзия, музыка, живопись … Знание не заботится о том, чтобы нравиться или не нравиться. Оно безжалостно. Оно не пленяет и не утешает. Это дело поэзии. Вот почему поэзия более необходима, чем знание. (Анатоль Франс) Мудрость – это ум, настоенный на совести. (Фазиль Искандер) 14
Никто не сделал так много для улучшения условий жизни людей, как химики. Г. Крото, Нобелевский лауреат по химии 1996 г. Может ли химия сделать людей лучше? – Нет! – А что может? – Поэзия, музыка, живопись … Знание не заботится о том, чтобы нравиться или не нравиться. Оно безжалостно. Оно не пленяет и не утешает. Это дело поэзии. Вот почему поэзия более необходима, чем знание. (Анатоль Франс) Мудрость – это ум, настоенный на совести. (Фазиль Искандер) 14
 Часть 2. Основные понятия химии
Часть 2. Основные понятия химии
 1. Вещество – любая совокупность атомов, молекул, ионов (заряженных частиц) • Индивидуальные (чистые) • Смеси – воздух, бензин, морская вода • Простые • Сложные (химические соединения) 16
1. Вещество – любая совокупность атомов, молекул, ионов (заряженных частиц) • Индивидуальные (чистые) • Смеси – воздух, бензин, морская вода • Простые • Сложные (химические соединения) 16
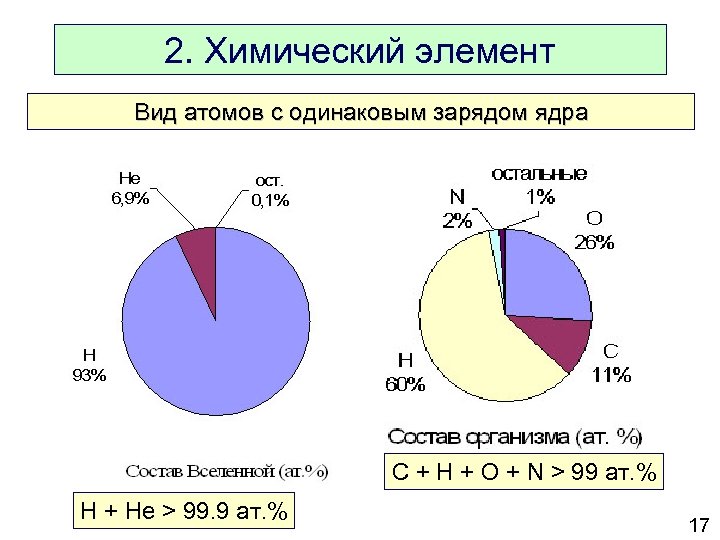 2. Химический элемент Вид атомов с одинаковым зарядом ядра C + H + O + N > 99 ат. % H + He > 99. 9 ат. % 17
2. Химический элемент Вид атомов с одинаковым зарядом ядра C + H + O + N > 99 ат. % H + He > 99. 9 ат. % 17
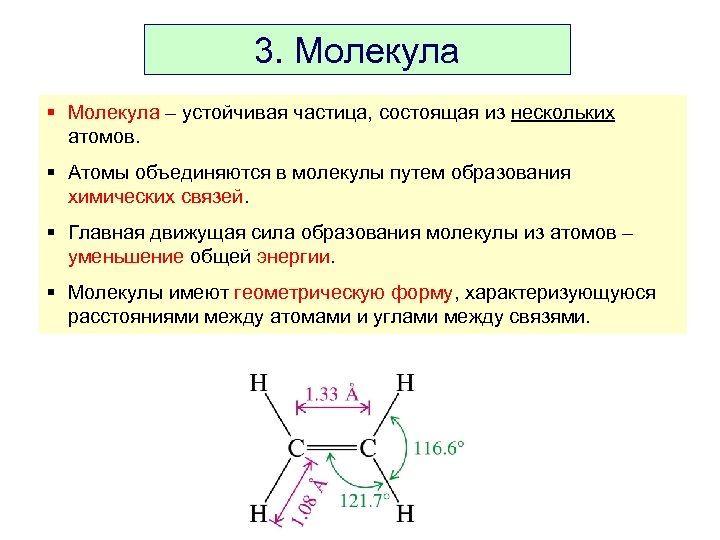 3. Молекула § Молекула – устойчивая частица, состоящая из нескольких атомов. § Атомы объединяются в молекулы путем образования химических связей. § Главная движущая сила образования молекулы из атомов – уменьшение общей энергии. § Молекулы имеют геометрическую форму, характеризующуюся расстояниями между атомами и углами между связями.
3. Молекула § Молекула – устойчивая частица, состоящая из нескольких атомов. § Атомы объединяются в молекулы путем образования химических связей. § Главная движущая сила образования молекулы из атомов – уменьшение общей энергии. § Молекулы имеют геометрическую форму, характеризующуюся расстояниями между атомами и углами между связями.
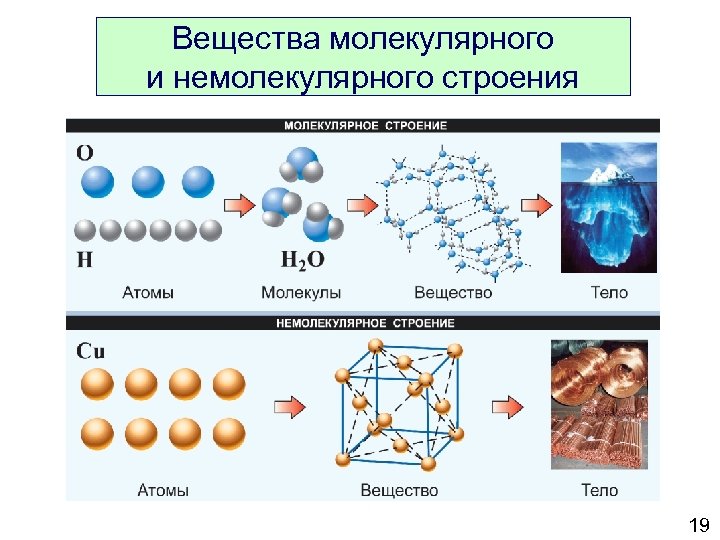 Вещества молекулярного и немолекулярного строения 19
Вещества молекулярного и немолекулярного строения 19
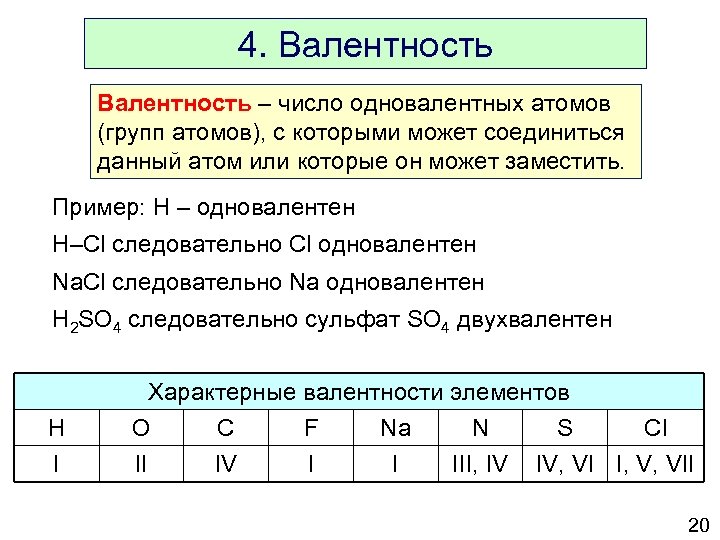 4. Валентность – число одновалентных атомов (групп атомов), с которыми может соединиться данный атом или которые он может заместить. Пример: H – одновалентен H–Cl следовательно Cl одновалентен Na. Cl следовательно Na одновалентен H 2 SO 4 следовательно сульфат SO 4 двухвалентен H Характерные валентности элементов O C F Na N S I II IV I I III, IV Cl IV, VI I, V, VII 20
4. Валентность – число одновалентных атомов (групп атомов), с которыми может соединиться данный атом или которые он может заместить. Пример: H – одновалентен H–Cl следовательно Cl одновалентен Na. Cl следовательно Na одновалентен H 2 SO 4 следовательно сульфат SO 4 двухвалентен H Характерные валентности элементов O C F Na N S I II IV I I III, IV Cl IV, VI I, V, VII 20
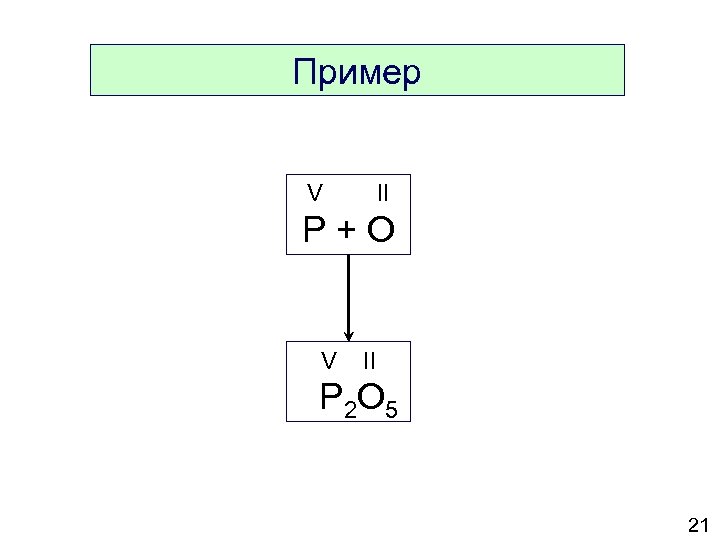 Пример V II P + O V II P 2 O 5 21
Пример V II P + O V II P 2 O 5 21
 Пример с ошибкой 22
Пример с ошибкой 22
 5. Химическая реакция Это - превращение одних веществ (реагентов) в другие (продукты), происходящее за счет разрыва старых и/или образования новых химических связей. Продукты отличаются от реагентов составом и/или строением. При химических реакциях атомы не изменяются, общее число атомов каждого вида остается неизменным. 23
5. Химическая реакция Это - превращение одних веществ (реагентов) в другие (продукты), происходящее за счет разрыва старых и/или образования новых химических связей. Продукты отличаются от реагентов составом и/или строением. При химических реакциях атомы не изменяются, общее число атомов каждого вида остается неизменным. 23
 А если число ядер меняется? Тогда это – не химическая, а ядерная реакция Самопроизвольный распад радия: 88 Ra = 86 Rn + 4 He Щелочноземельный металл распадается на два инертных газа 24
А если число ядер меняется? Тогда это – не химическая, а ядерная реакция Самопроизвольный распад радия: 88 Ra = 86 Rn + 4 He Щелочноземельный металл распадается на два инертных газа 24
 Часть 3. Язык химии
Часть 3. Язык химии
 1. Химическая формула Характеризует состав и/или строение вещества. Молекулярная формула показывает число атомов каждого вида в молекуле, эмпирическая (или брутто-) формула показывает простейшее соотношение между элементами. Перекись водорода Молекулярная формула – H 2 O 2 Эмпирическая формула – HO 26
1. Химическая формула Характеризует состав и/или строение вещества. Молекулярная формула показывает число атомов каждого вида в молекуле, эмпирическая (или брутто-) формула показывает простейшее соотношение между элементами. Перекись водорода Молекулярная формула – H 2 O 2 Эмпирическая формула – HO 26
 Что можно узнать из формулы? Например, элементный состав – содержание элементов в процентах 27
Что можно узнать из формулы? Например, элементный состав – содержание элементов в процентах 27
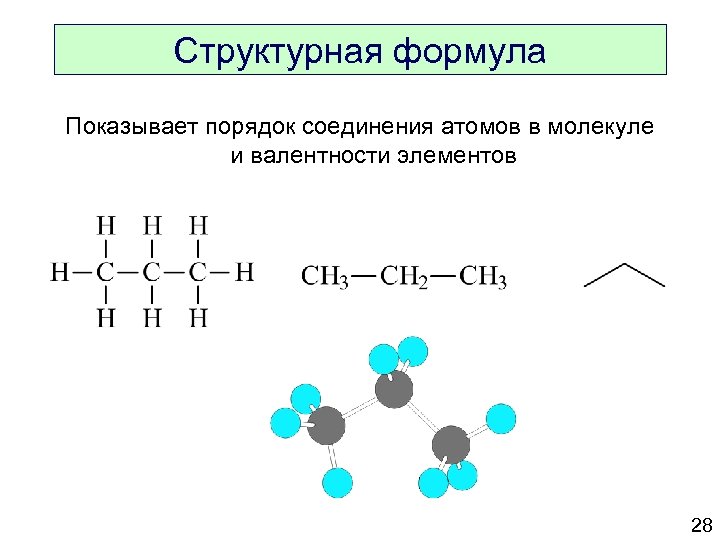 Структурная формула Показывает порядок соединения атомов в молекуле и валентности элементов 28
Структурная формула Показывает порядок соединения атомов в молекуле и валентности элементов 28
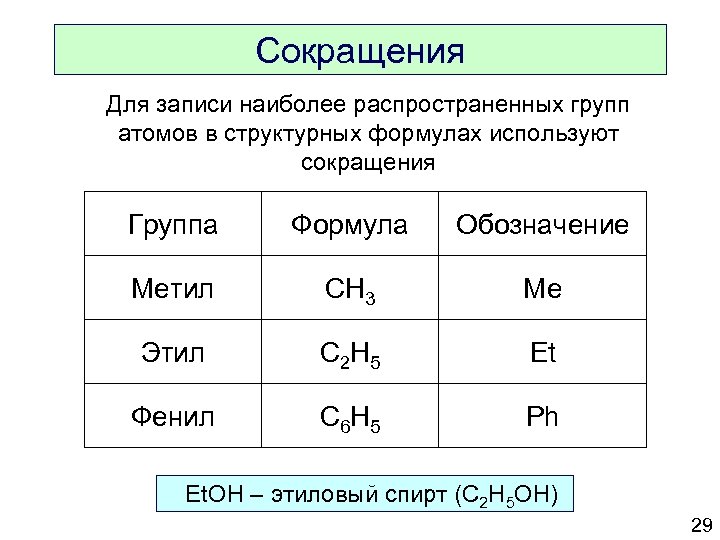 Сокращения Для записи наиболее распространенных групп атомов в структурных формулах используют сокращения Группа Формула Обозначение Метил CH 3 Me Этил C 2 H 5 Et Фенил C 6 H 5 Ph Et. OH – этиловый спирт (C 2 H 5 OH) 29
Сокращения Для записи наиболее распространенных групп атомов в структурных формулах используют сокращения Группа Формула Обозначение Метил CH 3 Me Этил C 2 H 5 Et Фенил C 6 H 5 Ph Et. OH – этиловый спирт (C 2 H 5 OH) 29
 2. Названия По номенклатуре – длинные, предпочитают использовать тривиальные 2 -Гидроксипропан-1, 2, 3 -трикарбоновая кислота (лимонная кислота) Забавно: полиэтилен имеет 9409 названий-синонимов 30
2. Названия По номенклатуре – длинные, предпочитают использовать тривиальные 2 -Гидроксипропан-1, 2, 3 -трикарбоновая кислота (лимонная кислота) Забавно: полиэтилен имеет 9409 названий-синонимов 30
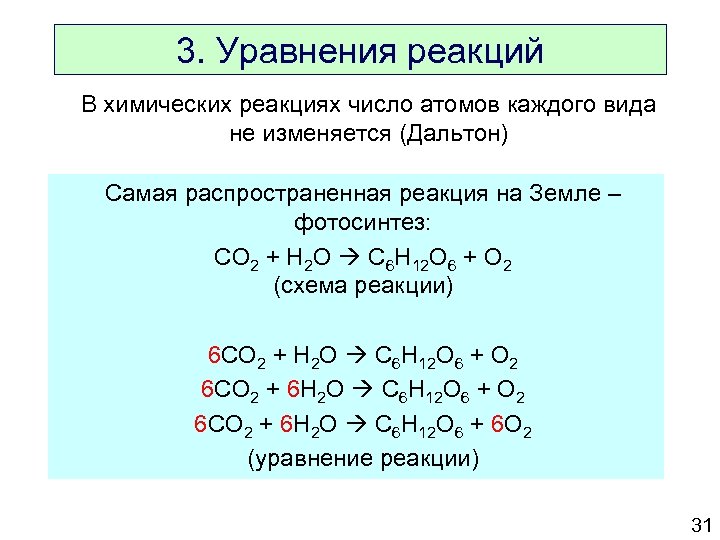 3. Уравнения реакций В химических реакциях число атомов каждого вида не изменяется (Дальтон) Самая распространенная реакция на Земле – фотосинтез: CO 2 + H 2 O C 6 H 12 O 6 + O 2 (схема реакции) 6 CO 2 + H 2 O C 6 H 12 O 6 + O 2 6 CO 2 + 6 H 2 O C 6 H 12 O 6 + 6 O 2 (уравнение реакции) 31
3. Уравнения реакций В химических реакциях число атомов каждого вида не изменяется (Дальтон) Самая распространенная реакция на Земле – фотосинтез: CO 2 + H 2 O C 6 H 12 O 6 + O 2 (схема реакции) 6 CO 2 + H 2 O C 6 H 12 O 6 + O 2 6 CO 2 + 6 H 2 O C 6 H 12 O 6 + 6 O 2 (уравнение реакции) 31
 Часть 4. Великие химические открытия 1. Открытие атомов и молекул. Создание атомномолекулярной теории (Дальтон, Авогадро, Берцелиус, Канниццаро). 2. Классификация элементов. Периодический закон (Д. И. Менделеев) 3. Молекулярная форма углерода – фуллерен (Крото, Кёрл, Смолли) 32
Часть 4. Великие химические открытия 1. Открытие атомов и молекул. Создание атомномолекулярной теории (Дальтон, Авогадро, Берцелиус, Канниццаро). 2. Классификация элементов. Периодический закон (Д. И. Менделеев) 3. Молекулярная форма углерода – фуллерен (Крото, Кёрл, Смолли) 32
 Предпосылки к открытию атомов. 1. Закон постоянства состава (Ж. -Л. Пруст, 1798 -1806) Все химически чистые соединения содержат элементы в строго определенных весовых соотношениях независимо от способа и условий получения. Ca. CO 3: m(Ca) : m(C) : m(O) = >3. 3 : 1 : 4 33
Предпосылки к открытию атомов. 1. Закон постоянства состава (Ж. -Л. Пруст, 1798 -1806) Все химически чистые соединения содержат элементы в строго определенных весовых соотношениях независимо от способа и условий получения. Ca. CO 3: m(Ca) : m(C) : m(O) = >3. 3 : 1 : 4 33
 2. Закон кратных отношений (Дж. Дальтон, 1803) Если два элемента образуют между собой несколько соединений, то на единицу массы одного из элементов приходятся кратные массы второго. Оксиды углерода Низший оксид: m(C) : m(O) = 3 : 4 Высший оксид: m(C) : m(O) = 3 : 8 34
2. Закон кратных отношений (Дж. Дальтон, 1803) Если два элемента образуют между собой несколько соединений, то на единицу массы одного из элементов приходятся кратные массы второго. Оксиды углерода Низший оксид: m(C) : m(O) = 3 : 4 Высший оксид: m(C) : m(O) = 3 : 8 34
 Атомная теория Дальтона 1. Вещества состоят из очень маленьких частиц, называемых атомами. 2. Все атомы одного и того же элемента имеют одинаковый размер, массу и др. свойства. Атомы разных элементов отличаются по свойствам. 3. Атомы нельзя создать, уничтожить или разделить. 4. Атомы разных элементов соединяются между собой в простых соотношениях и образуют химические соединения. 5. В химических реакциях атомы могут соединяться между собой, разъединяться или переходить от одного соединения к другому. 35
Атомная теория Дальтона 1. Вещества состоят из очень маленьких частиц, называемых атомами. 2. Все атомы одного и того же элемента имеют одинаковый размер, массу и др. свойства. Атомы разных элементов отличаются по свойствам. 3. Атомы нельзя создать, уничтожить или разделить. 4. Атомы разных элементов соединяются между собой в простых соотношениях и образуют химические соединения. 5. В химических реакциях атомы могут соединяться между собой, разъединяться или переходить от одного соединения к другому. 35
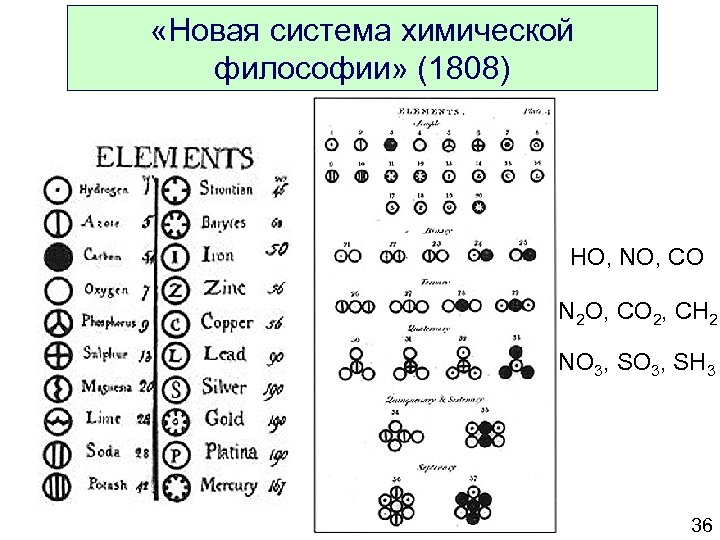 «Новая система химической философии» (1808) HO, NO, CO N 2 O, CO 2, CH 2 NO 3, SH 3 36
«Новая система химической философии» (1808) HO, NO, CO N 2 O, CO 2, CH 2 NO 3, SH 3 36
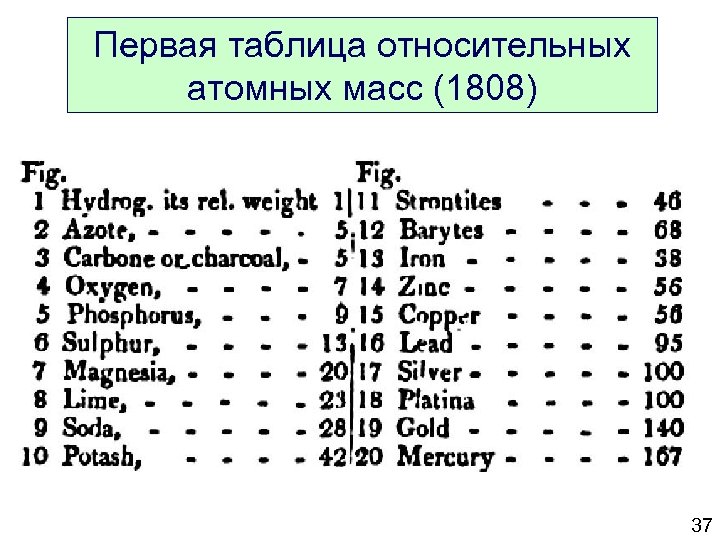 Первая таблица относительных атомных масс (1808) 37
Первая таблица относительных атомных масс (1808) 37
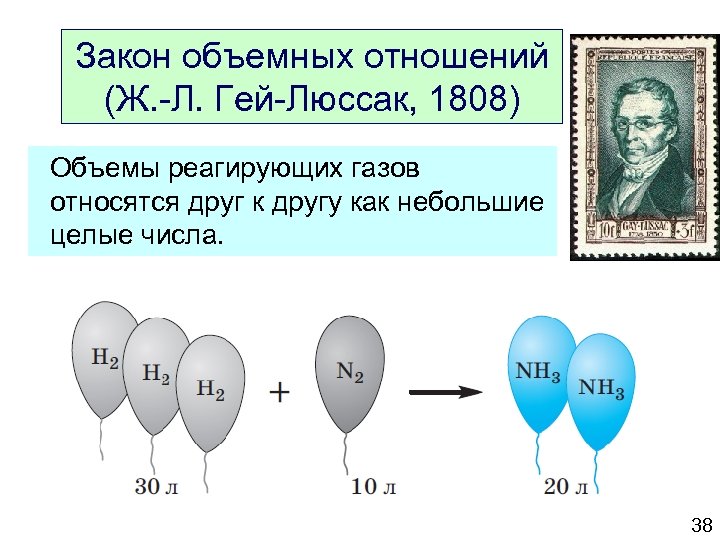 Закон объемных отношений (Ж. -Л. Гей-Люссак, 1808) Объемы реагирующих газов относятся друг к другу как небольшие целые числа. 38
Закон объемных отношений (Ж. -Л. Гей-Люссак, 1808) Объемы реагирующих газов относятся друг к другу как небольшие целые числа. 38
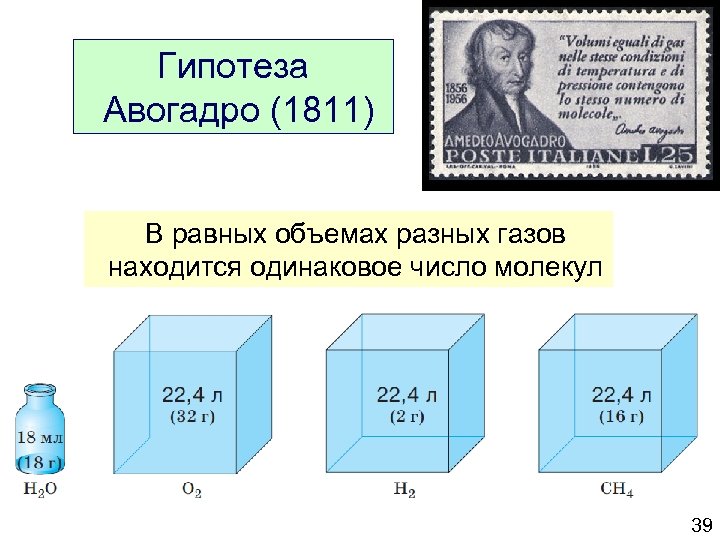 Гипотеза Авогадро (1811) В равных объемах разных газов находится одинаковое число молекул 39
Гипотеза Авогадро (1811) В равных объемах разных газов находится одинаковое число молекул 39
 Как установить правильную формулу? Реакция соединения водорода с хлором протекает без изменения объема Если H + Cl = HCl то объем уменьшается в 2 раза: 1 + 1 1 Если же H 2 + Cl 2 = 2 HCl то объем не изменяется: 1 + 1 2 40
Как установить правильную формулу? Реакция соединения водорода с хлором протекает без изменения объема Если H + Cl = HCl то объем уменьшается в 2 раза: 1 + 1 1 Если же H 2 + Cl 2 = 2 HCl то объем не изменяется: 1 + 1 2 40
 Й. -Я. Берцелиус (1779 -1848) 1. Подтвердил закон кратных отношений и составил правильную таблицу атомных масс. 2. Ввел современные символы для химических элементов, с помощью которых стали записывать химические формулы и химические уравнения. 3. Открыл 4 химических элемента: Si, Se, Ce, Th. 4. Ввел важнейшие химические понятия: «катализ» , «изомер» , «полимер» . 41
Й. -Я. Берцелиус (1779 -1848) 1. Подтвердил закон кратных отношений и составил правильную таблицу атомных масс. 2. Ввел современные символы для химических элементов, с помощью которых стали записывать химические формулы и химические уравнения. 3. Открыл 4 химических элемента: Si, Se, Ce, Th. 4. Ввел важнейшие химические понятия: «катализ» , «изомер» , «полимер» . 41
 Периодический закон. История открытия 1862 – Б. де Шанкуртуа (Франция) расположил элементы в порядке возрастания атомной массы по спирали и заметил периодичность 1864 – Дж. Ньюлендс (Англия) расположил элементы в виде таблицы и заметил повторяемость через 7 номеров: «закон октав» (7 элементов – 7 нот) 1870 – Л. Мейер (Германия) построил график зависимости атомного объема элементов от их атомной массы и обнаружил периодическую зависимость 42
Периодический закон. История открытия 1862 – Б. де Шанкуртуа (Франция) расположил элементы в порядке возрастания атомной массы по спирали и заметил периодичность 1864 – Дж. Ньюлендс (Англия) расположил элементы в виде таблицы и заметил повторяемость через 7 номеров: «закон октав» (7 элементов – 7 нот) 1870 – Л. Мейер (Германия) построил график зависимости атомного объема элементов от их атомной массы и обнаружил периодическую зависимость 42
 Периодический закон. История открытия 1869 – Д. И. Менделеев (Россия). Периодический закон: 1. Элементы, расположенные по величине атомного веса, представляют явственную периодичность свойств. 2. Должно ожидать открытия еще многих неизвестных простых тел, например, сходных с Al и Si элементов с атомным весом 65– 75. 3. Величина атомного веса элемента иногда может быть исправлена, зная его аналогии. 4. Некоторые аналогии элементов открываются по величине веса их атомов. 43
Периодический закон. История открытия 1869 – Д. И. Менделеев (Россия). Периодический закон: 1. Элементы, расположенные по величине атомного веса, представляют явственную периодичность свойств. 2. Должно ожидать открытия еще многих неизвестных простых тел, например, сходных с Al и Si элементов с атомным весом 65– 75. 3. Величина атомного веса элемента иногда может быть исправлена, зная его аналогии. 4. Некоторые аналогии элементов открываются по величине веса их атомов. 43
 Как был открыт Периодический закон «Невольно зародилась мысль о том, что между массой и химическими свойствами необходимо должна быть связь. А так как масса вещества, хотя и не абсолютная, а лишь относительная, выражается окончательно в виде весов атомов, то надо искать функциональное соответствие между индивидуальными свойствами элементов и их атомными весами. Искать же что-либо, хотя бы грибы или какую-нибудь зависимость, нельзя иначе, как смотря и пробуя. Вот я и стал подбирать, написав на отдельных карточках элементы с их атомными весами и коренными свойствами, сходные элементы и близкие атомные веса, что быстро и привело к тому заключению, что свойства элементов стоят в периодической зависимости от их атомного веса, причем, сомневаясь во многих неясностях, я ни минуты не сомневался в общности сделанного вывода, так как случайность допустить было невозможно» 44
Как был открыт Периодический закон «Невольно зародилась мысль о том, что между массой и химическими свойствами необходимо должна быть связь. А так как масса вещества, хотя и не абсолютная, а лишь относительная, выражается окончательно в виде весов атомов, то надо искать функциональное соответствие между индивидуальными свойствами элементов и их атомными весами. Искать же что-либо, хотя бы грибы или какую-нибудь зависимость, нельзя иначе, как смотря и пробуя. Вот я и стал подбирать, написав на отдельных карточках элементы с их атомными весами и коренными свойствами, сходные элементы и близкие атомные веса, что быстро и привело к тому заключению, что свойства элементов стоят в периодической зависимости от их атомного веса, причем, сомневаясь во многих неясностях, я ни минуты не сомневался в общности сделанного вывода, так как случайность допустить было невозможно» 44
 Первые наброски. 17. 02. 1869 45
Первые наброски. 17. 02. 1869 45

 Периодическая таблица. Самая первая (1869) Д. И. Менделеев, портрет 1869 г. «Опыт системы элементов, основанной на их атомном весе и химическом сродстве» 47
Периодическая таблица. Самая первая (1869) Д. И. Менделеев, портрет 1869 г. «Опыт системы элементов, основанной на их атомном весе и химическом сродстве» 47
 Предсказания на основе Периодического закона Предсказания Д. И. Менделеева: 1) Экабор (скандий, Sc) – открыт в 1879 г. 2) Экаалюминий (галлий, Ga) – открыт в 1875 г. 3) Экасилиций (германий, Ge) – открыт в 1886 г. 4) Экамарганец (Технеций, Tc) – синтезирован в 1937. Свойства 118 -го элемента: Открыт: в 2002 г. (Россия, США) – один атом, а в 2005 г. – еще два Положение в Периодической системе: группа VIIIA (инертный газ) Температура плавления: – 10 о. С. Температура кипения: – 6 о. С Высший оксид: RO 4 48
Предсказания на основе Периодического закона Предсказания Д. И. Менделеева: 1) Экабор (скандий, Sc) – открыт в 1879 г. 2) Экаалюминий (галлий, Ga) – открыт в 1875 г. 3) Экасилиций (германий, Ge) – открыт в 1886 г. 4) Экамарганец (Технеций, Tc) – синтезирован в 1937. Свойства 118 -го элемента: Открыт: в 2002 г. (Россия, США) – один атом, а в 2005 г. – еще два Положение в Периодической системе: группа VIIIA (инертный газ) Температура плавления: – 10 о. С. Температура кипения: – 6 о. С Высший оксид: RO 4 48
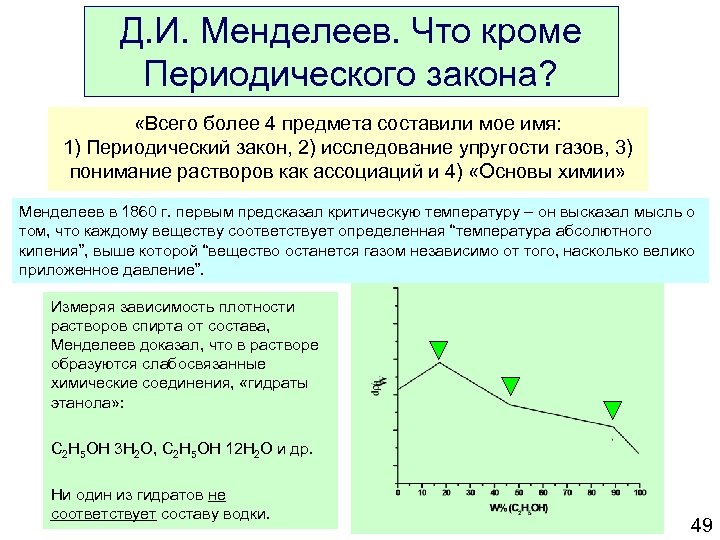 Д. И. Менделеев. Что кроме Периодического закона? «Всего более 4 предмета составили мое имя: 1) Периодический закон, 2) исследование упругости газов, 3) понимание растворов как ассоциаций и 4) «Основы химии» Менделеев в 1860 г. первым предсказал критическую температуру – он высказал мысль о том, что каждому веществу соответствует определенная “температура абсолютного кипения”, выше которой “вещество останется газом независимо от того, насколько велико приложенное давление”. Измеряя зависимость плотности растворов спирта от состава, Менделеев доказал, что в растворе образуются слабосвязанные химические соединения, «гидраты этанола» : C 2 H 5 OH 3 H 2 O, C 2 H 5 OH 12 H 2 O и др. Ни один из гидратов не соответствует составу водки. 49
Д. И. Менделеев. Что кроме Периодического закона? «Всего более 4 предмета составили мое имя: 1) Периодический закон, 2) исследование упругости газов, 3) понимание растворов как ассоциаций и 4) «Основы химии» Менделеев в 1860 г. первым предсказал критическую температуру – он высказал мысль о том, что каждому веществу соответствует определенная “температура абсолютного кипения”, выше которой “вещество останется газом независимо от того, насколько велико приложенное давление”. Измеряя зависимость плотности растворов спирта от состава, Менделеев доказал, что в растворе образуются слабосвязанные химические соединения, «гидраты этанола» : C 2 H 5 OH 3 H 2 O, C 2 H 5 OH 12 H 2 O и др. Ни один из гидратов не соответствует составу водки. 49
 Кабинет Д. И. Менделеева 50
Кабинет Д. И. Менделеева 50
 51
51
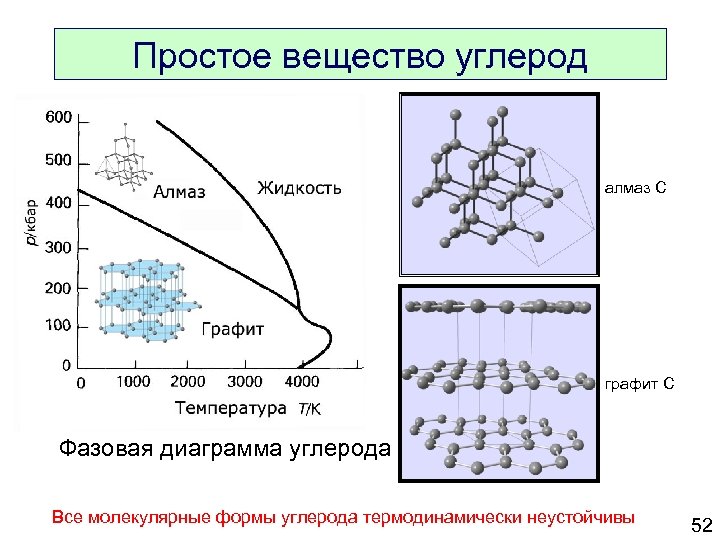 Простое вещество углерод алмаз C графит C Фазовая диаграмма углерода Все молекулярные формы углерода термодинамически неустойчивы 52
Простое вещество углерод алмаз C графит C Фазовая диаграмма углерода Все молекулярные формы углерода термодинамически неустойчивы 52
 Фуллерен. История открытия 1970 – Э. Осава (Япония) предсказывает возможность существования молекулы C 60. 1973 – Д. Бочвар, Е. Галперн (СССР) выполнили расчет электронной структуры этой молекулы. 1981 – Р. Дэвидсон (США) на основании расчетов предсказывает устойчивость молекулы C 60. 1984 – молекулы C 60 получены в углеродных кластерах, но не замечены. 1985 – Г. Крото, Р. Кёрл, Р. Смолли получили молекулы C 60 в углеродной плазме и обнаружили их с помощью массспектрометрии. 1990 – В. Крёчмер и Д. Хофман разработали простой способ получения макроскопических количеств C 60, что позволило доказать его строение. 53
Фуллерен. История открытия 1970 – Э. Осава (Япония) предсказывает возможность существования молекулы C 60. 1973 – Д. Бочвар, Е. Галперн (СССР) выполнили расчет электронной структуры этой молекулы. 1981 – Р. Дэвидсон (США) на основании расчетов предсказывает устойчивость молекулы C 60. 1984 – молекулы C 60 получены в углеродных кластерах, но не замечены. 1985 – Г. Крото, Р. Кёрл, Р. Смолли получили молекулы C 60 в углеродной плазме и обнаружили их с помощью массспектрометрии. 1990 – В. Крёчмер и Д. Хофман разработали простой способ получения макроскопических количеств C 60, что позволило доказать его строение. 53
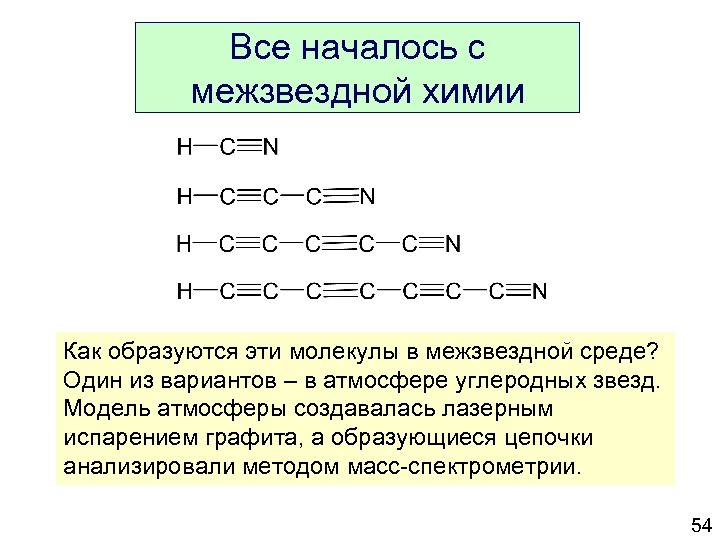 Все началось с межзвездной химии Как образуются эти молекулы в межзвездной среде? Один из вариантов – в атмосфере углеродных звезд. Модель атмосферы создавалась лазерным испарением графита, а образующиеся цепочки анализировали методом масс-спектрометрии. 54
Все началось с межзвездной химии Как образуются эти молекулы в межзвездной среде? Один из вариантов – в атмосфере углеродных звезд. Модель атмосферы создавалась лазерным испарением графита, а образующиеся цепочки анализировали методом масс-спектрометрии. 54
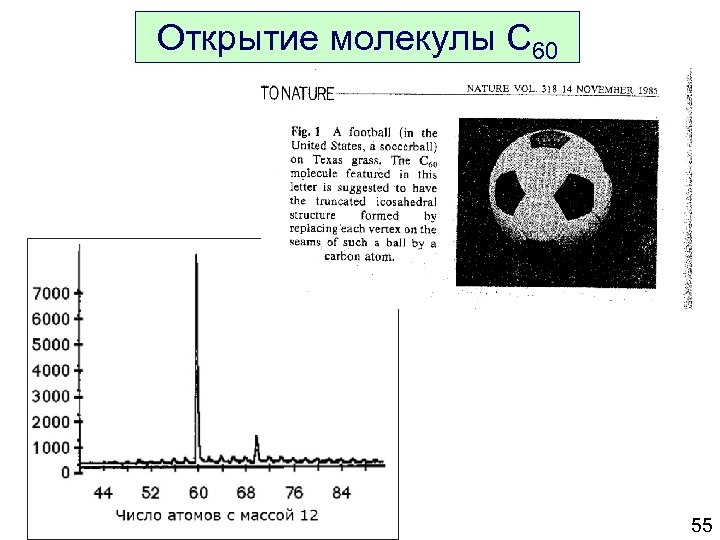 Открытие молекулы C 60 55
Открытие молекулы C 60 55
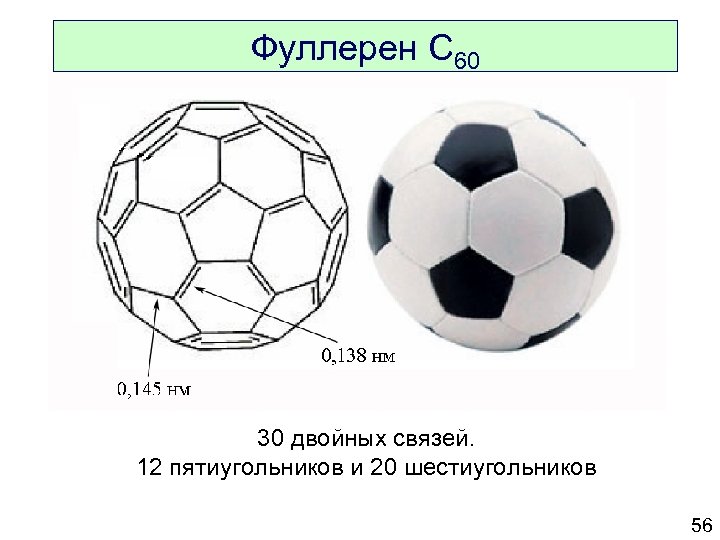 Фуллерен C 60 30 двойных связей. 12 пятиугольников и 20 шестиугольников 56
Фуллерен C 60 30 двойных связей. 12 пятиугольников и 20 шестиугольников 56
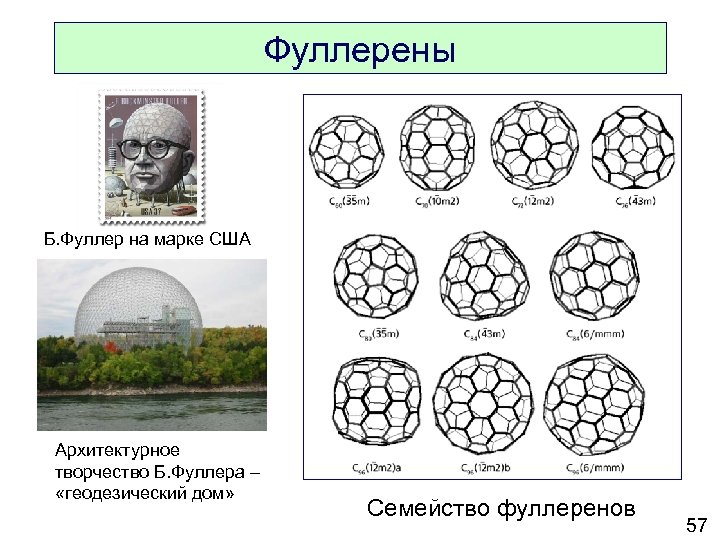 Фуллерены Б. Фуллер на марке США Архитектурное творчество Б. Фуллера – «геодезический дом» Семейство фуллеренов 57
Фуллерены Б. Фуллер на марке США Архитектурное творчество Б. Фуллера – «геодезический дом» Семейство фуллеренов 57
 Эндо-фуллерены Сборная России по химии внутри модели фуллерена Gd@C 82 «Гадофуллерен» 58
Эндо-фуллерены Сборная России по химии внутри модели фуллерена Gd@C 82 «Гадофуллерен» 58
 Коротко о главном 1. Химия – одна из наук о природе. Она изучает вещества и их превращения (реакции). Задачи химии – понять мир веществ и сделать его более удобным для жизни людей. Но химия не оперирует понятиями «добра» и «зла» . 2. Основные понятия химии – вещество, элемент, молекула, валентность, реакция. 3. Язык химии составляют химические формулы, названия веществ и уравнения реакций. 4. Первооткрывателем атомов считается английский химик Дж. Дальтон (1808). Правильные массы атомов были определены Й. -Я. Берцелиусом, а состав молекул – А. Авогадро. 5. Приоритет в создании Периодического закона и составлении периодической таблицы химических элементов принадлежит Д. И. Менделееву (1869). На его основе он правильно предсказал 5 не известных ранее элементов. 6. Первая молекулярная форма углерода – фуллерен – была открыта в 1985 г. Г. Крото и Р. Смолли в экспериментах по лазерному испарению графита.
Коротко о главном 1. Химия – одна из наук о природе. Она изучает вещества и их превращения (реакции). Задачи химии – понять мир веществ и сделать его более удобным для жизни людей. Но химия не оперирует понятиями «добра» и «зла» . 2. Основные понятия химии – вещество, элемент, молекула, валентность, реакция. 3. Язык химии составляют химические формулы, названия веществ и уравнения реакций. 4. Первооткрывателем атомов считается английский химик Дж. Дальтон (1808). Правильные массы атомов были определены Й. -Я. Берцелиусом, а состав молекул – А. Авогадро. 5. Приоритет в создании Периодического закона и составлении периодической таблицы химических элементов принадлежит Д. И. Менделееву (1869). На его основе он правильно предсказал 5 не известных ранее элементов. 6. Первая молекулярная форма углерода – фуллерен – была открыта в 1985 г. Г. Крото и Р. Смолли в экспериментах по лазерному испарению графита.


