лекция1.pptx
- Количество слайдов: 20
 Химия и наука о материалах. Специфика химии твердого тела. Классификация твердофазных материалов по составу, структуре и свойствам.
Химия и наука о материалах. Специфика химии твердого тела. Классификация твердофазных материалов по составу, структуре и свойствам.
 Литература
Литература
 Говоря о какой-то области науки, неизбежно хочется понять, почему она появилась и с чего начиналось ее развитие. Поэтому, начиная говорить о химии твердого тела, хочется вначале обратиться к истории. Пожалуй, наиболее ранние опыты человечества в области химии твердого тела относятся к получению керамических изделий: сосудов, фигурок и орнаментов. Керамика известна с глубокой древности и является, возможно, Первым созданным человеком материалом. Ещё недавно первые известные нам образцы керамики относились к эпохе верхнего палеолита (граветтская культура). Однако, найденные в 1993 году горшки из сяньжэньдон слеплены 20 тысяч лет назад. Древнейший предмет из обожженной глины датируется 29 -25 тысячелетиями до нашей эры. Это вестоницкая венера, хранящаяся в моравском музее в Брно.
Говоря о какой-то области науки, неизбежно хочется понять, почему она появилась и с чего начиналось ее развитие. Поэтому, начиная говорить о химии твердого тела, хочется вначале обратиться к истории. Пожалуй, наиболее ранние опыты человечества в области химии твердого тела относятся к получению керамических изделий: сосудов, фигурок и орнаментов. Керамика известна с глубокой древности и является, возможно, Первым созданным человеком материалом. Ещё недавно первые известные нам образцы керамики относились к эпохе верхнего палеолита (граветтская культура). Однако, найденные в 1993 году горшки из сяньжэньдон слеплены 20 тысяч лет назад. Древнейший предмет из обожженной глины датируется 29 -25 тысячелетиями до нашей эры. Это вестоницкая венера, хранящаяся в моравском музее в Брно.
 На следующем этапе стала развиваться металлургия Оказалось, что уголь, образующийся в результате горения дерева при высокой температуре, способен восстанавливать некоторые минералы. При этом в результате взаимодействия камня, дерева и огня образовывался материал, обладающий принципиально новыми свойствами. Это казалось чудом человеку, тогда еще не знакомому не только с атомно-молекулярной теорией и периодической системой, но и с основами химии. Казалось, что комбинируя различные вещества, можно продолжить эти чудесные превращения еще дальше, например, превратить железо, медь, свинец или ртуть в самый дорогой металл – золото. Так возникла алхимия. Своими трудами алхимики создали или наметили многие основные направления современной химии твердого тела. Опираясь на их труды, новый толчок в своем развитии получила металлургия.
На следующем этапе стала развиваться металлургия Оказалось, что уголь, образующийся в результате горения дерева при высокой температуре, способен восстанавливать некоторые минералы. При этом в результате взаимодействия камня, дерева и огня образовывался материал, обладающий принципиально новыми свойствами. Это казалось чудом человеку, тогда еще не знакомому не только с атомно-молекулярной теорией и периодической системой, но и с основами химии. Казалось, что комбинируя различные вещества, можно продолжить эти чудесные превращения еще дальше, например, превратить железо, медь, свинец или ртуть в самый дорогой металл – золото. Так возникла алхимия. Своими трудами алхимики создали или наметили многие основные направления современной химии твердого тела. Опираясь на их труды, новый толчок в своем развитии получила металлургия.
 Российские ученые металлурги Павел Петрович Аносов – выдающийся русский ученый металлург, крупный организатор горнозаводской промышленности. Работал в Златоустовском горном округе, он создал новый метод получения литой стали, объединив в единый процесс науглероживание и плавление металла. Аносов раскрыл утерянный в середине века секрет изготовления булатной стали. Он впервые применил микроскоп для исследования микроструктуры стали, заложив основы микроструктурных исследований. 29 июня 1796 г. – 13 мая 1851 г. Дмитрий Константинович Чернов – ученый металлург, металловед и специалист в области термической обработки металлов. Он является родоначальником металлографии железа. Чернов первым сделал набросок диаграммы состояния «железо-углерод» . 1 ноября 1839 г. – 2 января 1921 г. Термин «химия твердого тела» был введен в научную практику в 1902 году с легкой руки российского химика Флавиана Михайловича Флавицкого. 18 января 1848 г. – 1 ноября 1917 г.
Российские ученые металлурги Павел Петрович Аносов – выдающийся русский ученый металлург, крупный организатор горнозаводской промышленности. Работал в Златоустовском горном округе, он создал новый метод получения литой стали, объединив в единый процесс науглероживание и плавление металла. Аносов раскрыл утерянный в середине века секрет изготовления булатной стали. Он впервые применил микроскоп для исследования микроструктуры стали, заложив основы микроструктурных исследований. 29 июня 1796 г. – 13 мая 1851 г. Дмитрий Константинович Чернов – ученый металлург, металловед и специалист в области термической обработки металлов. Он является родоначальником металлографии железа. Чернов первым сделал набросок диаграммы состояния «железо-углерод» . 1 ноября 1839 г. – 2 января 1921 г. Термин «химия твердого тела» был введен в научную практику в 1902 году с легкой руки российского химика Флавиана Михайловича Флавицкого. 18 января 1848 г. – 1 ноября 1917 г.
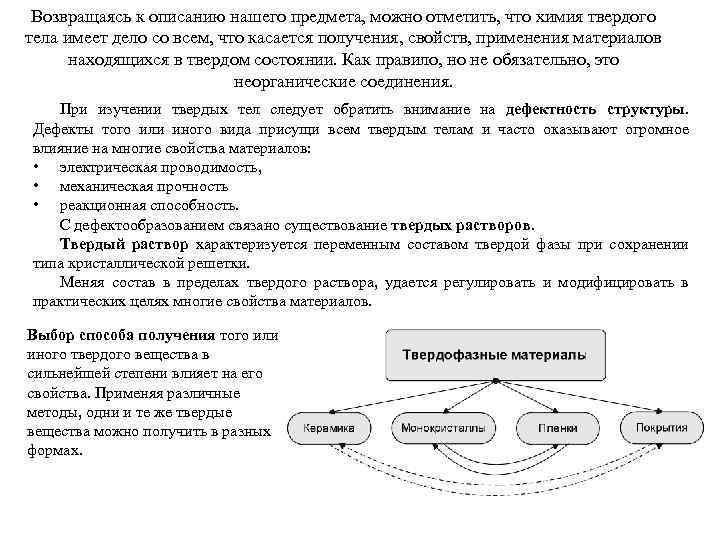 Возвращаясь к описанию нашего предмета, можно отметить, что химия твердого тела имеет дело со всем, что касается получения, свойств, применения материалов находящихся в твердом состоянии. Как правило, но не обязательно, это неорганические соединения. При изучении твердых тел следует обратить внимание на дефектность структуры. Дефекты того или иного вида присущи всем твердым телам и часто оказывают огромное влияние на многие свойства материалов: • электрическая проводимость, • механическая прочность • реакционная способность. С дефектообразованием связано существование твердых растворов. Твердый раствор характеризуется переменным составом твердой фазы при сохранении типа кристаллической решетки. Меняя состав в пределах твердого раствора, удается регулировать и модифицировать в практических целях многие свойства материалов. Выбор способа получения того или иного твердого вещества в сильнейшей степени влияет на его свойства. Применяя различные методы, одни и те же твердые вещества можно получить в разных формах.
Возвращаясь к описанию нашего предмета, можно отметить, что химия твердого тела имеет дело со всем, что касается получения, свойств, применения материалов находящихся в твердом состоянии. Как правило, но не обязательно, это неорганические соединения. При изучении твердых тел следует обратить внимание на дефектность структуры. Дефекты того или иного вида присущи всем твердым телам и часто оказывают огромное влияние на многие свойства материалов: • электрическая проводимость, • механическая прочность • реакционная способность. С дефектообразованием связано существование твердых растворов. Твердый раствор характеризуется переменным составом твердой фазы при сохранении типа кристаллической решетки. Меняя состав в пределах твердого раствора, удается регулировать и модифицировать в практических целях многие свойства материалов. Выбор способа получения того или иного твердого вещества в сильнейшей степени влияет на его свойства. Применяя различные методы, одни и те же твердые вещества можно получить в разных формах.
 Методы получения порошков принципиально можно разделить на две большие группы: диспергирование (измельчение) исходных материалов конденсация, т. е. выделение твердых веществ из жидкой или газообразной фазы. Методы первой группы подразделяются в зависимости от принципов, положенных в основу процессов диспергирования: истирание, удар, давление, взрыв, ультразвуковое воздействие, электромагнитный импульс, электроискровое или дуговое диспергирование, электрохимическая или химическая коррозия, лазерное воздействие, разрушение материала за счет последовательных теплосмен и пр. Ко второй группе относятся, например, разложение металлоорганических соединений (МОС), различные варианты осаждения из растворов, упаривание солевых растворов, осаждение за счет реакций в газовой фазе, конденсация паров, криохимический метод, распылительная сушка и т. д. Методы получения компактных сложнооксидных материалов можно подразделить на керамические и методы с использованием растворных (в частности, солевых) технологий.
Методы получения порошков принципиально можно разделить на две большие группы: диспергирование (измельчение) исходных материалов конденсация, т. е. выделение твердых веществ из жидкой или газообразной фазы. Методы первой группы подразделяются в зависимости от принципов, положенных в основу процессов диспергирования: истирание, удар, давление, взрыв, ультразвуковое воздействие, электромагнитный импульс, электроискровое или дуговое диспергирование, электрохимическая или химическая коррозия, лазерное воздействие, разрушение материала за счет последовательных теплосмен и пр. Ко второй группе относятся, например, разложение металлоорганических соединений (МОС), различные варианты осаждения из растворов, упаривание солевых растворов, осаждение за счет реакций в газовой фазе, конденсация паров, криохимический метод, распылительная сушка и т. д. Методы получения компактных сложнооксидных материалов можно подразделить на керамические и методы с использованием растворных (в частности, солевых) технологий.
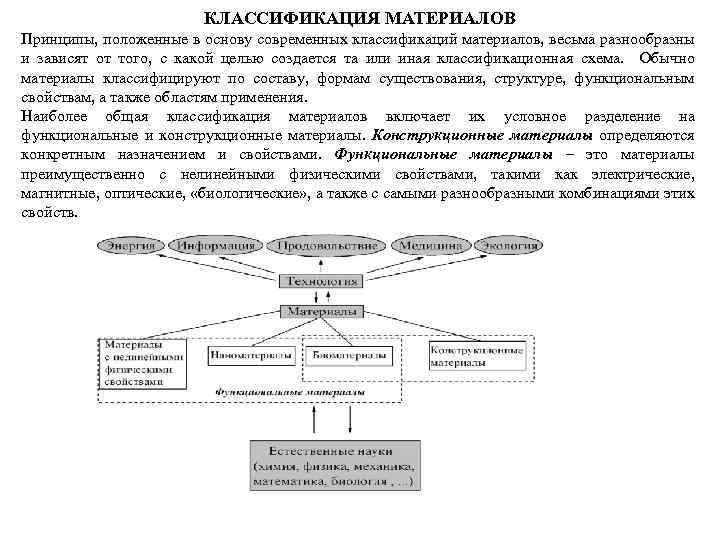 КЛАССИФИКАЦИЯ МАТЕРИАЛОВ Принципы, положенные в основу современных классификаций материалов, весьма разнообразны и зависят от того, с какой целью создается та или иная классификационная схема. Обычно материалы классифицируют по составу, формам существования, структуре, функциональным свойствам, а также областям применения. Наиболее общая классификация материалов включает их условное разделение на функциональные и конструкционные материалы. Конструкционные материалы определяются конкретным назначением и свойствами. Функциональные материалы – это материалы преимущественно с нелинейными физическими свойствами, такими как электрические, магнитные, оптические, «биологические» , а также с самыми разнообразными комбинациями этих свойств.
КЛАССИФИКАЦИЯ МАТЕРИАЛОВ Принципы, положенные в основу современных классификаций материалов, весьма разнообразны и зависят от того, с какой целью создается та или иная классификационная схема. Обычно материалы классифицируют по составу, формам существования, структуре, функциональным свойствам, а также областям применения. Наиболее общая классификация материалов включает их условное разделение на функциональные и конструкционные материалы. Конструкционные материалы определяются конкретным назначением и свойствами. Функциональные материалы – это материалы преимущественно с нелинейными физическими свойствами, такими как электрические, магнитные, оптические, «биологические» , а также с самыми разнообразными комбинациями этих свойств.
 Особый случай с точки зрения классификации представляют собой биоматериалы. При ближайшем рассмотрении оказывается, что биоматериалы – имплантанты, костезаменители, цементы и пр. – по своей сути гораздо ближе к конструкционным материалам, чем к остальным функциональным материалам. Наноматериалы – достаточно обширный и универсальный класс материалов, объединяющий различные семейства материалов с любыми свойствами, лишь бы вещество находилось в особом, «наноразмерном» , состоянии. Более того, почти любую фазу, составляющую функциональный материал, можно получить в виде наночастиц (и далеко не всегда, скажем, в виде стекла или монокристаллов). Естественно поэтому, что такие материалы стоит рассматривать как «функциональные» , однако их следует выделять в особый класс «наноматериалов» из-за того, что функциональные свойства в существенной степени могут трансформироваться из-за «размерного фактора» и огромного вклада поверхностной энергии. Ниже будут приведены четыре альтернативные и, с другой стороны, все же взаимодополняющие друга, схемы классификации материалов по составу, структуре, форме существования и функциональным свойствам. Кстати, именно такая последовательность – отражение обычно реализующегося алгоритма создания новых материалов. Предпосылки для успешного поиска новых материалов заключаются в правильном выборе химической системы и далее – диапазона составов будущего материала, для которых наблюдаются желаемые функциональные свойства. Затем для выбранного диапазона составов проводится синтез вещества с определенной структурой или (для кристаллических веществ) в виде определенной полиморфной модификации заданного состава. Тем самым определяется наилучший фазовый состав будущего материала.
Особый случай с точки зрения классификации представляют собой биоматериалы. При ближайшем рассмотрении оказывается, что биоматериалы – имплантанты, костезаменители, цементы и пр. – по своей сути гораздо ближе к конструкционным материалам, чем к остальным функциональным материалам. Наноматериалы – достаточно обширный и универсальный класс материалов, объединяющий различные семейства материалов с любыми свойствами, лишь бы вещество находилось в особом, «наноразмерном» , состоянии. Более того, почти любую фазу, составляющую функциональный материал, можно получить в виде наночастиц (и далеко не всегда, скажем, в виде стекла или монокристаллов). Естественно поэтому, что такие материалы стоит рассматривать как «функциональные» , однако их следует выделять в особый класс «наноматериалов» из-за того, что функциональные свойства в существенной степени могут трансформироваться из-за «размерного фактора» и огромного вклада поверхностной энергии. Ниже будут приведены четыре альтернативные и, с другой стороны, все же взаимодополняющие друга, схемы классификации материалов по составу, структуре, форме существования и функциональным свойствам. Кстати, именно такая последовательность – отражение обычно реализующегося алгоритма создания новых материалов. Предпосылки для успешного поиска новых материалов заключаются в правильном выборе химической системы и далее – диапазона составов будущего материала, для которых наблюдаются желаемые функциональные свойства. Затем для выбранного диапазона составов проводится синтез вещества с определенной структурой или (для кристаллических веществ) в виде определенной полиморфной модификации заданного состава. Тем самым определяется наилучший фазовый состав будущего материала.
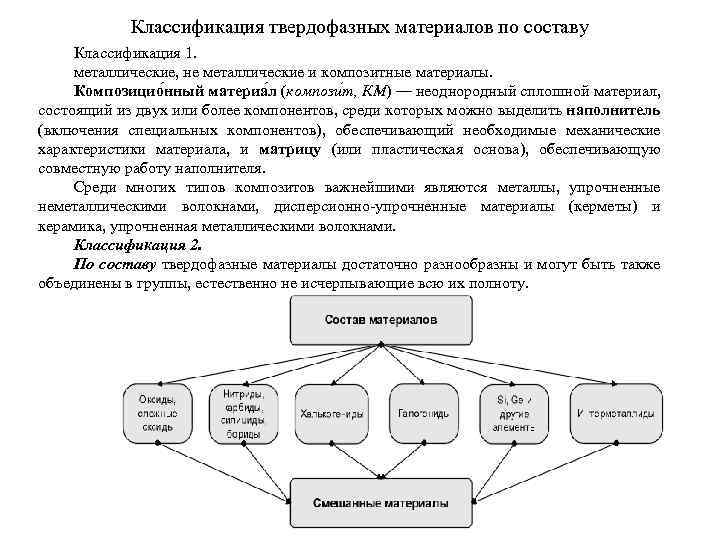 Классификация твердофазных материалов по составу Классификация 1. металлические, не металлические и композитные материалы. Композицио нный материа л (компози т, КМ) — неоднородный сплошной материал, состоящий из двух или более компонентов, среди которых можно выделить наполнитель (включения специальных компонентов), обеспечивающий необходимые механические характеристики материала, и матрицу (или пластическая основа), обеспечивающую совместную работу наполнителя. Среди многих типов композитов важнейшими являются металлы, упрочненные неметаллическими волокнами, дисперсионно-упрочненные материалы (керметы) и керамика, упрочненная металлическими волокнами. Классификация 2. По составу твердофазные материалы достаточно разнообразны и могут быть также объединены в группы, естественно не исчерпывающие всю их полноту.
Классификация твердофазных материалов по составу Классификация 1. металлические, не металлические и композитные материалы. Композицио нный материа л (компози т, КМ) — неоднородный сплошной материал, состоящий из двух или более компонентов, среди которых можно выделить наполнитель (включения специальных компонентов), обеспечивающий необходимые механические характеристики материала, и матрицу (или пластическая основа), обеспечивающую совместную работу наполнителя. Среди многих типов композитов важнейшими являются металлы, упрочненные неметаллическими волокнами, дисперсионно-упрочненные материалы (керметы) и керамика, упрочненная металлическими волокнами. Классификация 2. По составу твердофазные материалы достаточно разнообразны и могут быть также объединены в группы, естественно не исчерпывающие всю их полноту.
 Классификация по структуре: 1. Кристаллические – характеризуются наличием дальнего порядка в расположении атомов, ионов или молекул 2. Не кристаллические (аморфные или стекла) – отсутствует дальний порядок в расположении атомов, ионов или молекул Стекла специального назначения в последнее время создаются на основе фосфатов, боратов, германатов, титанатов и оксидов РЗЭ. Халькогенидные стекла, содержащие мышьяк и сурьму, широко используются в полупроводниковой технике и квантовой электроники. Стекла из кварца повышенной чистоты – основа волоконной оптики. Исследования по кристаллизации стекла привели к созданию новых стеклокристаллических материалов – ситаллов, обладающих высочайшей прочностью и используемых в ракетной технике и приборостроении. На их основе изготавливаются износостойкие шары для помола в мельницах, защитные покрытия для металлических сплавов и электроизоляторы.
Классификация по структуре: 1. Кристаллические – характеризуются наличием дальнего порядка в расположении атомов, ионов или молекул 2. Не кристаллические (аморфные или стекла) – отсутствует дальний порядок в расположении атомов, ионов или молекул Стекла специального назначения в последнее время создаются на основе фосфатов, боратов, германатов, титанатов и оксидов РЗЭ. Халькогенидные стекла, содержащие мышьяк и сурьму, широко используются в полупроводниковой технике и квантовой электроники. Стекла из кварца повышенной чистоты – основа волоконной оптики. Исследования по кристаллизации стекла привели к созданию новых стеклокристаллических материалов – ситаллов, обладающих высочайшей прочностью и используемых в ракетной технике и приборостроении. На их основе изготавливаются износостойкие шары для помола в мельницах, защитные покрытия для металлических сплавов и электроизоляторы.
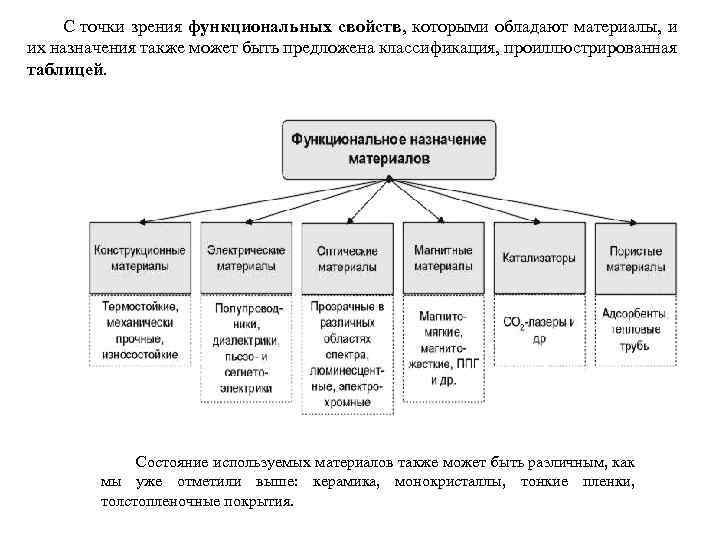 С точки зрения функциональных свойств, которыми обладают материалы, и их назначения также может быть предложена классификация, проиллюстрированная таблицей. Состояние используемых материалов также может быть различным, как мы уже отметили выше: керамика, монокристаллы, тонкие пленки, толстопленочные покрытия.
С точки зрения функциональных свойств, которыми обладают материалы, и их назначения также может быть предложена классификация, проиллюстрированная таблицей. Состояние используемых материалов также может быть различным, как мы уже отметили выше: керамика, монокристаллы, тонкие пленки, толстопленочные покрытия.
 Оптические материалы используются для передачи и преобразования световых сигналов В основе лежат следующие свойства: 1. прозрачность или светопропускание в ультрафиолетовой, визуальной или инфракрасной области спектра, 2. устойчивость к воздействию световых потоков (в светофильтрах, делителях, поляризаторах, различного рода оптических затворах и модуляторах). Особую группу оптических материалов представляют люминофоры, которые обеспечивают визуализацию изображения в электронно-лучевых трубках, они различаются по спектру, длительности и интенсивности люминесценции, способам и энергии её возбуждения и т. д. Магнитные материалы характеризуются в первую очередь параметрами кривой намагничивания. Кривая намагниченности и расположение магнитных доменов в зависимости от напряженности внешнего магнитного поля Н.
Оптические материалы используются для передачи и преобразования световых сигналов В основе лежат следующие свойства: 1. прозрачность или светопропускание в ультрафиолетовой, визуальной или инфракрасной области спектра, 2. устойчивость к воздействию световых потоков (в светофильтрах, делителях, поляризаторах, различного рода оптических затворах и модуляторах). Особую группу оптических материалов представляют люминофоры, которые обеспечивают визуализацию изображения в электронно-лучевых трубках, они различаются по спектру, длительности и интенсивности люминесценции, способам и энергии её возбуждения и т. д. Магнитные материалы характеризуются в первую очередь параметрами кривой намагничивания. Кривая намагниченности и расположение магнитных доменов в зависимости от напряженности внешнего магнитного поля Н.
 Магнитомягкие материалы - имеют достаточно узкую петлю гистерезиса, они могут быть использованы в устройствах где требуется быстрое управление сигналом при минимальных затратах энергии. Магнитожесткие материалы, для перемагничивания которых требуется очень значительная энергия, применяются в качестве постоянных магнитов в различных устройствах. К ним относятся интерметаллиды типа Sm. Co 5 или на основе соединений в системе неодим-бор-железо, ферриты со структурой типа магнетоплюмбита Ba 1 -x. Srx. Fe 12 O 19 и пр. Природа магнетизма твердых тел заключается во взаимодействии между собой спиновых моментов электронов ферромагнитных ионов и атомов в структуре материалов. В случае совпадающих по направлению спиновых моментов - материал обладает ферромагнитными свойствами (FM), при полной взаимной компенсации таких моментов образуется антиферромагнетик (AFM), а частичная компенсация приводит к получению ферримагнитных материалов (феррит), к которым часто относятся используемые на практике ферриты: например, шпинели АВ 2 О 4 или феррогранаты с общей формулой М 3 Fe 5 O 12. Важнейшая характеристика магнитных материалов - температура Кюри, при которой за счет теплового движения происходит разрушение ориентации магнитных доменов и вещество практически теряет свою намагниченность. Преимущество имеют материалы с достаточно высокой температурой Кюри и слабой температурной зависимостью намагниченности в Схематическое взаимодействие между собой спиновых эксплуатационных интервалах. моментов электронов ферромагнитных ионов и атомов в структуре материалов
Магнитомягкие материалы - имеют достаточно узкую петлю гистерезиса, они могут быть использованы в устройствах где требуется быстрое управление сигналом при минимальных затратах энергии. Магнитожесткие материалы, для перемагничивания которых требуется очень значительная энергия, применяются в качестве постоянных магнитов в различных устройствах. К ним относятся интерметаллиды типа Sm. Co 5 или на основе соединений в системе неодим-бор-железо, ферриты со структурой типа магнетоплюмбита Ba 1 -x. Srx. Fe 12 O 19 и пр. Природа магнетизма твердых тел заключается во взаимодействии между собой спиновых моментов электронов ферромагнитных ионов и атомов в структуре материалов. В случае совпадающих по направлению спиновых моментов - материал обладает ферромагнитными свойствами (FM), при полной взаимной компенсации таких моментов образуется антиферромагнетик (AFM), а частичная компенсация приводит к получению ферримагнитных материалов (феррит), к которым часто относятся используемые на практике ферриты: например, шпинели АВ 2 О 4 или феррогранаты с общей формулой М 3 Fe 5 O 12. Важнейшая характеристика магнитных материалов - температура Кюри, при которой за счет теплового движения происходит разрушение ориентации магнитных доменов и вещество практически теряет свою намагниченность. Преимущество имеют материалы с достаточно высокой температурой Кюри и слабой температурной зависимостью намагниченности в Схематическое взаимодействие между собой спиновых эксплуатационных интервалах. моментов электронов ферромагнитных ионов и атомов в структуре материалов
 Электрические материалы Спектр используемых материалов, обладающих специфическими электрическими свойствами достаточно широк. При образовании кристаллической решетки твердого тела все электронные уровни у данного типа атомов смещаются из-за действия соседних атомов друг на друга, и из отдельных энергетических уровней уединенных атомов в твердом теле образуется их целая полоса — зона энергетических уровней. То есть при обменном взаимодействии электронов энергетические уровни расщепляются. Самая верхняя из заполненных электронами зон называют валентной. Ближайшая к ней незаполненная электронами зона — зона проводимости. Эти зоны отделены друг от друга запрещенной зоной, в которой электроны находиться не могут. Схема расположения энергетических уровней свободного атома (а) и неметаллического твердого тела (б): 1 и 2 – уровни энергии атома в нормальном и возбужденном состоянии, соответственно; 1' и 2' – орбитали электронов атомов в нормальном и возбужденном состоянии, соответственно; 3 – валентная зона; 4 – зона проводимости; 5 – запрещенная зона
Электрические материалы Спектр используемых материалов, обладающих специфическими электрическими свойствами достаточно широк. При образовании кристаллической решетки твердого тела все электронные уровни у данного типа атомов смещаются из-за действия соседних атомов друг на друга, и из отдельных энергетических уровней уединенных атомов в твердом теле образуется их целая полоса — зона энергетических уровней. То есть при обменном взаимодействии электронов энергетические уровни расщепляются. Самая верхняя из заполненных электронами зон называют валентной. Ближайшая к ней незаполненная электронами зона — зона проводимости. Эти зоны отделены друг от друга запрещенной зоной, в которой электроны находиться не могут. Схема расположения энергетических уровней свободного атома (а) и неметаллического твердого тела (б): 1 и 2 – уровни энергии атома в нормальном и возбужденном состоянии, соответственно; 1' и 2' – орбитали электронов атомов в нормальном и возбужденном состоянии, соответственно; 3 – валентная зона; 4 – зона проводимости; 5 – запрещенная зона
 Классификация веществ по ширине запрещенной зоны: а, б – проводники; в – полупроводники; г – диэлектрики Проводники (а, б) — у этих материалов запрещенная зона практически отсутствует. Валентная зона вплотную прилегает к зоне проводимости или даже перекрывается ею, вследствие чего электроны в металле свободны и под влиянием слабых напряженностей приложенного электрического поля могут переходить из валентной (заполненной) зоны в зону проводимости. Отличительное свойство проводников — сильно выраженная электропроводность. Полупроводники (в) — вещества с шириной запрещенной зоной < 3 э. В. Отличительное свойство полупроводников — сильная зависимость удельной проводимости от концентрации и вида примесей и дефектов в материале, а также от внешних воздействий (температуры, света, электрических и магнитных полей). Диэлектрики (г)- вещества, имеющие самую широкую запрещенную зону (более 3 э. В) и большое удельное электрическое сопротивление (rv > 108 Ом • м). У некоторых диэлектриков запрещенная зона может быть настолько велика, что электронная электропроводность не играет определяющей роли. Отличительное свойство — способность к поляризации и возможность существования в этих материалах электростатического поля.
Классификация веществ по ширине запрещенной зоны: а, б – проводники; в – полупроводники; г – диэлектрики Проводники (а, б) — у этих материалов запрещенная зона практически отсутствует. Валентная зона вплотную прилегает к зоне проводимости или даже перекрывается ею, вследствие чего электроны в металле свободны и под влиянием слабых напряженностей приложенного электрического поля могут переходить из валентной (заполненной) зоны в зону проводимости. Отличительное свойство проводников — сильно выраженная электропроводность. Полупроводники (в) — вещества с шириной запрещенной зоной < 3 э. В. Отличительное свойство полупроводников — сильная зависимость удельной проводимости от концентрации и вида примесей и дефектов в материале, а также от внешних воздействий (температуры, света, электрических и магнитных полей). Диэлектрики (г)- вещества, имеющие самую широкую запрещенную зону (более 3 э. В) и большое удельное электрическое сопротивление (rv > 108 Ом • м). У некоторых диэлектриков запрещенная зона может быть настолько велика, что электронная электропроводность не играет определяющей роли. Отличительное свойство — способность к поляризации и возможность существования в этих материалах электростатического поля.
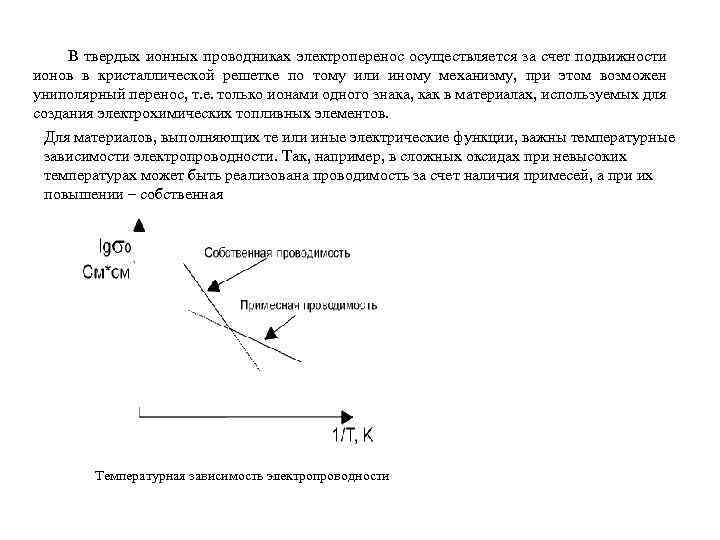 В твердых ионных проводниках электроперенос осуществляется за счет подвижности ионов в кристаллической решетке по тому или иному механизму, при этом возможен униполярный перенос, т. е. только ионами одного знака, как в материалах, используемых для создания электрохимических топливных элементов. Для материалов, выполняющих те или иные электрические функции, важны температурные зависимости электропроводности. Так, например, в сложных оксидах при невысоких температурах может быть реализована проводимость за счет наличия примесей, а при их повышении – собственная Температурная зависимость электропроводности
В твердых ионных проводниках электроперенос осуществляется за счет подвижности ионов в кристаллической решетке по тому или иному механизму, при этом возможен униполярный перенос, т. е. только ионами одного знака, как в материалах, используемых для создания электрохимических топливных элементов. Для материалов, выполняющих те или иные электрические функции, важны температурные зависимости электропроводности. Так, например, в сложных оксидах при невысоких температурах может быть реализована проводимость за счет наличия примесей, а при их повышении – собственная Температурная зависимость электропроводности
 МАТЕРИАЛ УСТРОЙСТВО Материалы с электрическими функциями (полупроводники, диэлектрики, пьезо- и сегнетоэлектрики, электролиты, сверхпроводники). Al 2 O 3·Cr 2 O 3; Fe 3 O 4·Mn 2 O 3·Ni. O; Ba. Ti. O 3, Sr. Ti. O 3; Co. O-Mn. OO 2 Терморезисторы, (с положительным и отрицательным температурным коэффициентом). Оксиды переходных металлов (Mn, Co, Ni, Fe, Cr) Терморезисторы, термометры сопротивления La. Cr. O 3, Si. C, BN, Mo. Si 2, Zr. O 2 (Y 2 O 3) Нагревательные элементы Zn. O, Cd. Se Варисторы Al 2 O 3, Be. O, Si. C, BN, Si 3 N 4 Подложки интегральных схем, изоляторы. Pb. Zr. O 3 -Pb. Ti. O 3; Ba. Ti. O 3, Ca. Ti. O 3, Ti. O 2, Si. O 2 Конденсаторы, линии задержки, фильтры, вибраторы, генераторы, зуммеры Ba. Ti. O 3 -Co. Fe 2 O 4 Магнитострикционные пьезопреобразователи. Вольфрамовые и ванадиевые бронзы, Ba. O-Sr. O- Na 2 O-Nb 2 O 5 Электрохимические устройсва радио и электротехнического назначения Li. Ta. O 3, Zn. Se Тепловые и ИК-датчики Zr. O 2(Ca. O), Zr. O 2(Y 2 O 3), Ag. I, Na-b. Al 2 O 3; Rb. Ag 4 I 5; La. Cr. O 3, YCr. O 3, La. Co. O 3 -Sr. O, Ba. Ce. O 3 Твердотельные химические источники тока, электролизеры, системы вентиляции, электроды для высокотемпературного электролиза Mg. Cr 2 O 4 -Ti. O 2, Sn. O, Ti. O 2, Fe 3 O 4, Cr 2 O 3, Ba. Ti. O 3, Ag. I, Ag 2 S, Zr. O 2(Ca. O), Me-b. Al 2 O 3 Датчики состава газов, жидких металлов, системы регистрации утечки газов, таймеры, увлажнители, средства технологической диагностики. Li. Ti 2 O 4, Li. Ti 2 S 4, Pb 3 Mo 6 S 8, Sr. Ti. O 3, Ba(Pb, Bi)O 3 Сверхпроводная передача энергии
МАТЕРИАЛ УСТРОЙСТВО Материалы с электрическими функциями (полупроводники, диэлектрики, пьезо- и сегнетоэлектрики, электролиты, сверхпроводники). Al 2 O 3·Cr 2 O 3; Fe 3 O 4·Mn 2 O 3·Ni. O; Ba. Ti. O 3, Sr. Ti. O 3; Co. O-Mn. OO 2 Терморезисторы, (с положительным и отрицательным температурным коэффициентом). Оксиды переходных металлов (Mn, Co, Ni, Fe, Cr) Терморезисторы, термометры сопротивления La. Cr. O 3, Si. C, BN, Mo. Si 2, Zr. O 2 (Y 2 O 3) Нагревательные элементы Zn. O, Cd. Se Варисторы Al 2 O 3, Be. O, Si. C, BN, Si 3 N 4 Подложки интегральных схем, изоляторы. Pb. Zr. O 3 -Pb. Ti. O 3; Ba. Ti. O 3, Ca. Ti. O 3, Ti. O 2, Si. O 2 Конденсаторы, линии задержки, фильтры, вибраторы, генераторы, зуммеры Ba. Ti. O 3 -Co. Fe 2 O 4 Магнитострикционные пьезопреобразователи. Вольфрамовые и ванадиевые бронзы, Ba. O-Sr. O- Na 2 O-Nb 2 O 5 Электрохимические устройсва радио и электротехнического назначения Li. Ta. O 3, Zn. Se Тепловые и ИК-датчики Zr. O 2(Ca. O), Zr. O 2(Y 2 O 3), Ag. I, Na-b. Al 2 O 3; Rb. Ag 4 I 5; La. Cr. O 3, YCr. O 3, La. Co. O 3 -Sr. O, Ba. Ce. O 3 Твердотельные химические источники тока, электролизеры, системы вентиляции, электроды для высокотемпературного электролиза Mg. Cr 2 O 4 -Ti. O 2, Sn. O, Ti. O 2, Fe 3 O 4, Cr 2 O 3, Ba. Ti. O 3, Ag. I, Ag 2 S, Zr. O 2(Ca. O), Me-b. Al 2 O 3 Датчики состава газов, жидких металлов, системы регистрации утечки газов, таймеры, увлажнители, средства технологической диагностики. Li. Ti 2 O 4, Li. Ti 2 S 4, Pb 3 Mo 6 S 8, Sr. Ti. O 3, Ba(Pb, Bi)O 3 Сверхпроводная передача энергии
 Материалы с оптическими функциями (оптически прозрачные, люминесцентные, электрохромные или светочвуствительные) Pb. Zr. O 3 -Pb. Ti. O 3 -La 2 O 3; Li. Nb. O 3, Ba. Ti. O 3, Ba 2 Na. Nb 5 O 15 Оптические устройства записи информации, видеодисплеи, фотопреобразователи, переключатели Si. O 2: Ge, волокна Al 2 O 3, муллит, халькогенидныесистемы, образующие стекла Волноводы, линии оптической связи, оболочки ламп накаливания, ИК-прозрачные стекла. Al 2 O 3: Cr; Y 2 Al 5 O 15, Ca. WO 4, оксиды редкоземельных элементов Оптические квантовые генераторы Li. Nb. O 3, Li. Ta. O 3; Pb. Zr. O 3 -Pb. Ti. O 3 -La 2 O 3 Электрооптические модуляторы света Zn. S: Cu. Cl; Zn 2 Si. O 4: Mn; Cs. J: Na, WO 3; Nb 2 O 5: Ag. J, Y 2 O 3 S: Eu Индуцирующие устройства, оптические устройства отражения Ga. As 1 -x. Px. Ga. P: N; Zn. S: Pb, Cu и другие халькогениды Устройства дистанционного управления, фототиристоы, детекторы света
Материалы с оптическими функциями (оптически прозрачные, люминесцентные, электрохромные или светочвуствительные) Pb. Zr. O 3 -Pb. Ti. O 3 -La 2 O 3; Li. Nb. O 3, Ba. Ti. O 3, Ba 2 Na. Nb 5 O 15 Оптические устройства записи информации, видеодисплеи, фотопреобразователи, переключатели Si. O 2: Ge, волокна Al 2 O 3, муллит, халькогенидныесистемы, образующие стекла Волноводы, линии оптической связи, оболочки ламп накаливания, ИК-прозрачные стекла. Al 2 O 3: Cr; Y 2 Al 5 O 15, Ca. WO 4, оксиды редкоземельных элементов Оптические квантовые генераторы Li. Nb. O 3, Li. Ta. O 3; Pb. Zr. O 3 -Pb. Ti. O 3 -La 2 O 3 Электрооптические модуляторы света Zn. S: Cu. Cl; Zn 2 Si. O 4: Mn; Cs. J: Na, WO 3; Nb 2 O 5: Ag. J, Y 2 O 3 S: Eu Индуцирующие устройства, оптические устройства отражения Ga. As 1 -x. Px. Ga. P: N; Zn. S: Pb, Cu и другие халькогениды Устройства дистанционного управления, фототиристоы, детекторы света
 Материалы с магнитными функциями (магнитомягкие, магнитожесткие и аморфные магнитные) Mn-Zn-ферриты, г-Fe 2 O 3, Cr. O 2 Головки и ленты для звуко- и видеозаписи. Mn-Zn- и Ni-Zn-ферриты Детали трансформаторов Li-Mn-ферриты, R 3 Fe 5 O 12 Элементы памяти ЭВМ Ni-Zn-ферриты Магнитострикционные фильтры и вибраторы (Mn 1 -x. Znx)Fe 2 O 4 Магнитопроводы Y 2 Fe 5 O 12, Li-Zn-Ti-ферриты Антенны дальней связи (СВЧ) Ba. Fe 12 O 19, Sr. Fe 12 O 19 Радиопоглощающие покрытия, постоянные магниты для статоров Конструкционные материалы (термостойкие, механостойкие, износостойкие) Al 2 O 3, Zr. O 2, Si 3 N 4, Th. O 2, , сиалоны, керамические пены и волокна из Al 2 O 3, K 2 O·Ti. O 2, Ca. O·Si. O 2 и др. Лопатки турбин. ракетные сопла, керамические двигатели, теплообменники, теплоизоляторы высокотемпературных печей. Al 2 O 3, Ti. C, Ti. N, B 4 C Режущий инструмент, подшипники, резьбовые соединения , полировальные и шлифовальные круги, абразивы. Материалы с биологическими функциями (устойчивые в физиологических средах) Al 2 O 3, Гидроксоапатитовые и фосфатные Искусственные зубы, кости, суставы, имплантируемые стекла микроэлектронные устройства, сердечные клапаны
Материалы с магнитными функциями (магнитомягкие, магнитожесткие и аморфные магнитные) Mn-Zn-ферриты, г-Fe 2 O 3, Cr. O 2 Головки и ленты для звуко- и видеозаписи. Mn-Zn- и Ni-Zn-ферриты Детали трансформаторов Li-Mn-ферриты, R 3 Fe 5 O 12 Элементы памяти ЭВМ Ni-Zn-ферриты Магнитострикционные фильтры и вибраторы (Mn 1 -x. Znx)Fe 2 O 4 Магнитопроводы Y 2 Fe 5 O 12, Li-Zn-Ti-ферриты Антенны дальней связи (СВЧ) Ba. Fe 12 O 19, Sr. Fe 12 O 19 Радиопоглощающие покрытия, постоянные магниты для статоров Конструкционные материалы (термостойкие, механостойкие, износостойкие) Al 2 O 3, Zr. O 2, Si 3 N 4, Th. O 2, , сиалоны, керамические пены и волокна из Al 2 O 3, K 2 O·Ti. O 2, Ca. O·Si. O 2 и др. Лопатки турбин. ракетные сопла, керамические двигатели, теплообменники, теплоизоляторы высокотемпературных печей. Al 2 O 3, Ti. C, Ti. N, B 4 C Режущий инструмент, подшипники, резьбовые соединения , полировальные и шлифовальные круги, абразивы. Материалы с биологическими функциями (устойчивые в физиологических средах) Al 2 O 3, Гидроксоапатитовые и фосфатные Искусственные зубы, кости, суставы, имплантируемые стекла микроэлектронные устройства, сердечные клапаны


