Химия полимеров без серной вул.pptx
- Количество слайдов: 68
 Химия и физика полимеров основной курс Химия полимеров
Химия и физика полимеров основной курс Химия полимеров
 Различают следующие типы химических реакций полимеров: 1. Реакции деструкции; 2. Реакции сшивания; 3. Полимераналогичные реакции; 4. Реакции, сопровождающиеся внутримолекулярными перегруппировками. На практике часто эти реакции протекают одновременно под влиянием комплекса факторов. Особенности химических реакций полимеров. На скорость и глубину химических реакций в полимерах оказывают влияние следующие факторы: 1. Длина макромолекул. С увеличением длины химическая реакционноспособность ограничивается скоростью диффузии или растворения реагирующих веществ, что проявляется в снижении скорости протекания реакций.
Различают следующие типы химических реакций полимеров: 1. Реакции деструкции; 2. Реакции сшивания; 3. Полимераналогичные реакции; 4. Реакции, сопровождающиеся внутримолекулярными перегруппировками. На практике часто эти реакции протекают одновременно под влиянием комплекса факторов. Особенности химических реакций полимеров. На скорость и глубину химических реакций в полимерах оказывают влияние следующие факторы: 1. Длина макромолекул. С увеличением длины химическая реакционноспособность ограничивается скоростью диффузии или растворения реагирующих веществ, что проявляется в снижении скорости протекания реакций.
 2. Конфигурационные эффекты. Реакционная способность функциональной группы может изменяться в зависимости от того в какую пространственную последовательность звеньев она входит (изо- или синдиотактическую), вследствие этого механизм и скорость химической реакции изменяются. 3. Конформационные эффекты. По ходу химической реакции изменяется химический состав макромолекул, характер внутри- и межмолекулярного взаимодействия, потенциальные барьеры вращения и т. д. , и как следствие, конформация цепи. Это влияет на степень свернутости клубка и доступность функциональных групп для реагента. Изменение конформации может привести как к ускорению, так и замедлению скорости химической реакции. 4. Надмолекулярные эффекты. Различная доступность для реагентов функциональных групп, расположенных в аморфных и кристаллических областях, а также надмолекулярных образованиях с различной плотностью упаковки, является одной из причин неоднородности продуктов реакций в полимерах, модифицируемых в стеклообразном или кристаллическом состоянии.
2. Конфигурационные эффекты. Реакционная способность функциональной группы может изменяться в зависимости от того в какую пространственную последовательность звеньев она входит (изо- или синдиотактическую), вследствие этого механизм и скорость химической реакции изменяются. 3. Конформационные эффекты. По ходу химической реакции изменяется химический состав макромолекул, характер внутри- и межмолекулярного взаимодействия, потенциальные барьеры вращения и т. д. , и как следствие, конформация цепи. Это влияет на степень свернутости клубка и доступность функциональных групп для реагента. Изменение конформации может привести как к ускорению, так и замедлению скорости химической реакции. 4. Надмолекулярные эффекты. Различная доступность для реагентов функциональных групп, расположенных в аморфных и кристаллических областях, а также надмолекулярных образованиях с различной плотностью упаковки, является одной из причин неоднородности продуктов реакций в полимерах, модифицируемых в стеклообразном или кристаллическом состоянии.
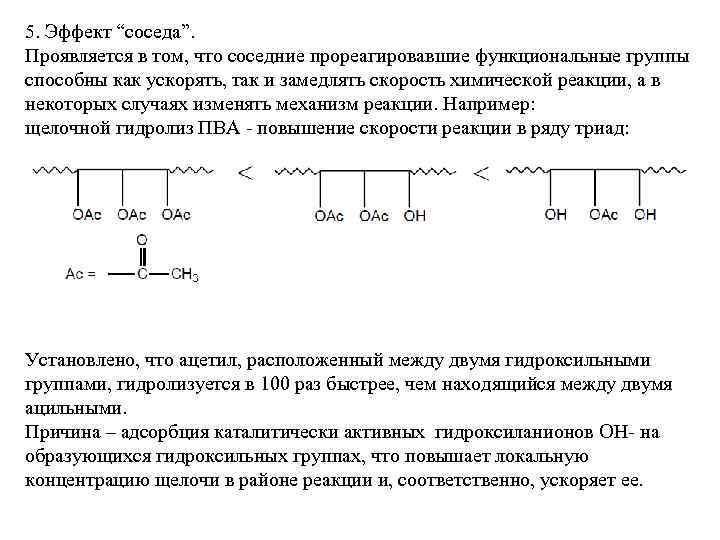 5. Эффект “соседа”. Проявляется в том, что соседние прореагировавшие функциональные группы способны как ускорять, так и замедлять скорость химической реакции, а в некоторых случаях изменять механизм реакции. Например: щелочной гидролиз ПВА - повышение скорости реакции в ряду триад: Установлено, что ацетил, расположенный между двумя гидроксильными группами, гидролизуется в 100 раз быстрее, чем находящийся между двумя ацильными. Причина – адсорбция каталитически активных гидроксиланионов ОН- на образующихся гидроксильных группах, что повышает локальную концентрацию щелочи в районе реакции и, соответственно, ускоряет ее.
5. Эффект “соседа”. Проявляется в том, что соседние прореагировавшие функциональные группы способны как ускорять, так и замедлять скорость химической реакции, а в некоторых случаях изменять механизм реакции. Например: щелочной гидролиз ПВА - повышение скорости реакции в ряду триад: Установлено, что ацетил, расположенный между двумя гидроксильными группами, гидролизуется в 100 раз быстрее, чем находящийся между двумя ацильными. Причина – адсорбция каталитически активных гидроксиланионов ОН- на образующихся гидроксильных группах, что повышает локальную концентрацию щелочи в районе реакции и, соответственно, ускоряет ее.
 Примером замедляющего влияния соседней группы служит гидролиз ПМАА в сильноосновных средах: Появление рядом с амидной группой одной и, тем более, двух карбоксилатанионов препятствует подходу к ней гидроксиланиона, поэтому степень превращения амидных групп не превышает 70 %. В результате действия различных факторов макромолекулы после участия в химических реакциях характеризуются композиционной неоднородностью двух видов: а) неоднородностью по химическому составу, так как в реакциях принимают участие только часть функциональных групп, вследствие пространственной недоступности участков макромолекул, находящихся внутри клубка или надмолекулярной структуры. б) неоднородностью распределения прореагировавших функциональных групп по длине макромолекулы.
Примером замедляющего влияния соседней группы служит гидролиз ПМАА в сильноосновных средах: Появление рядом с амидной группой одной и, тем более, двух карбоксилатанионов препятствует подходу к ней гидроксиланиона, поэтому степень превращения амидных групп не превышает 70 %. В результате действия различных факторов макромолекулы после участия в химических реакциях характеризуются композиционной неоднородностью двух видов: а) неоднородностью по химическому составу, так как в реакциях принимают участие только часть функциональных групп, вследствие пространственной недоступности участков макромолекул, находящихся внутри клубка или надмолекулярной структуры. б) неоднородностью распределения прореагировавших функциональных групп по длине макромолекулы.
 Реакции деструкции – это реакции, протекающие с разрывом химических связей в основной цепи; сопровождаются изменением ММ полимеров. В процессе переработки полимеров и эксплуатации изделий на их основе деструкция обычно проходит под одновременным действием ряда факторов: термоокислительная деструкция, фотоокислительная деструкция и т. д.
Реакции деструкции – это реакции, протекающие с разрывом химических связей в основной цепи; сопровождаются изменением ММ полимеров. В процессе переработки полимеров и эксплуатации изделий на их основе деструкция обычно проходит под одновременным действием ряда факторов: термоокислительная деструкция, фотоокислительная деструкция и т. д.
 Различают два направления деструкции: 1. Случайный разрыв связей, лежащих внутри макромолекул – образуются продукты меньшей молекулярной массы; 2. Специфический разрыв связей у концов макромолекул (деполимеризация) – образуются мономеры или продукты, близкие по ММ к мономерам, при этом ММ и другие свойства полимеров изменяются значительно медленнее, чем при деструкции по закону случая. Термодеструкция (без окисления) протекает при эксплуатации полимерного изделия в условиях высоких температурах в инертной среде или в вакууме (например в аппаратах, без доступа воздуха). Механизм термодеструкции, как правило, свободно-радикальный. Установлена закономерность, связывающая характер продуктов деструкции полимеров с теплотой полимеризации: - полимеры, содержащие четвертичные атомы углерода в цепи и имеющих низкое значение теплот полимеризации деструктируются по механизму деполимеризации, т. е. продукт деструкции – мономер; - полимеры, содержащие в цепях вторичные и третичные атомы углерода и имеющие высокое значение теплоты полимеризации деструктируются по закону случая, т. е. продуктом деструкции являются устойчивые макромолекулы меньшей молекулярной массы.
Различают два направления деструкции: 1. Случайный разрыв связей, лежащих внутри макромолекул – образуются продукты меньшей молекулярной массы; 2. Специфический разрыв связей у концов макромолекул (деполимеризация) – образуются мономеры или продукты, близкие по ММ к мономерам, при этом ММ и другие свойства полимеров изменяются значительно медленнее, чем при деструкции по закону случая. Термодеструкция (без окисления) протекает при эксплуатации полимерного изделия в условиях высоких температурах в инертной среде или в вакууме (например в аппаратах, без доступа воздуха). Механизм термодеструкции, как правило, свободно-радикальный. Установлена закономерность, связывающая характер продуктов деструкции полимеров с теплотой полимеризации: - полимеры, содержащие четвертичные атомы углерода в цепи и имеющих низкое значение теплот полимеризации деструктируются по механизму деполимеризации, т. е. продукт деструкции – мономер; - полимеры, содержащие в цепях вторичные и третичные атомы углерода и имеющие высокое значение теплоты полимеризации деструктируются по закону случая, т. е. продуктом деструкции являются устойчивые макромолекулы меньшей молекулярной массы.

 Для ПЭ характерны случайные разрывы связей в основной цепи, что сопровождается образованием двух макрорадикалов, стабилизирующихся по механизму диспропорционирования , при этом ММ ПЭ быстро уменьшается: Для ПММА, поли- -метилстирола характерна деструкция по механизму деполимеризации. Эти полимеры характеризуются низкой теплотой полимеризации (табл. ) и содержат на концах двойные связи: последовательное отщепление звеньев вдоль цепи
Для ПЭ характерны случайные разрывы связей в основной цепи, что сопровождается образованием двух макрорадикалов, стабилизирующихся по механизму диспропорционирования , при этом ММ ПЭ быстро уменьшается: Для ПММА, поли- -метилстирола характерна деструкция по механизму деполимеризации. Эти полимеры характеризуются низкой теплотой полимеризации (табл. ) и содержат на концах двойные связи: последовательное отщепление звеньев вдоль цепи
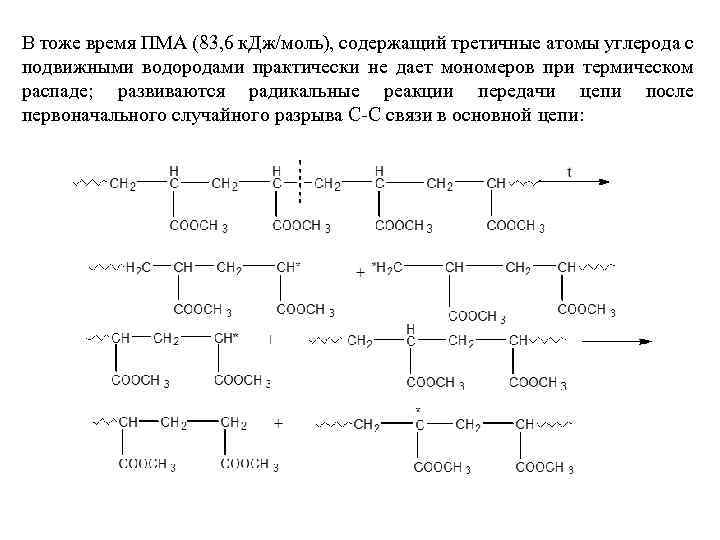 В тоже время ПМА (83, 6 к. Дж/моль), содержащий третичные атомы углерода с подвижными водородами практически не дает мономеров при термическом распаде; развиваются радикальные реакции передачи цепи после первоначального случайного разрыва С-С связи в основной цепи:
В тоже время ПМА (83, 6 к. Дж/моль), содержащий третичные атомы углерода с подвижными водородами практически не дает мономеров при термическом распаде; развиваются радикальные реакции передачи цепи после первоначального случайного разрыва С-С связи в основной цепи:
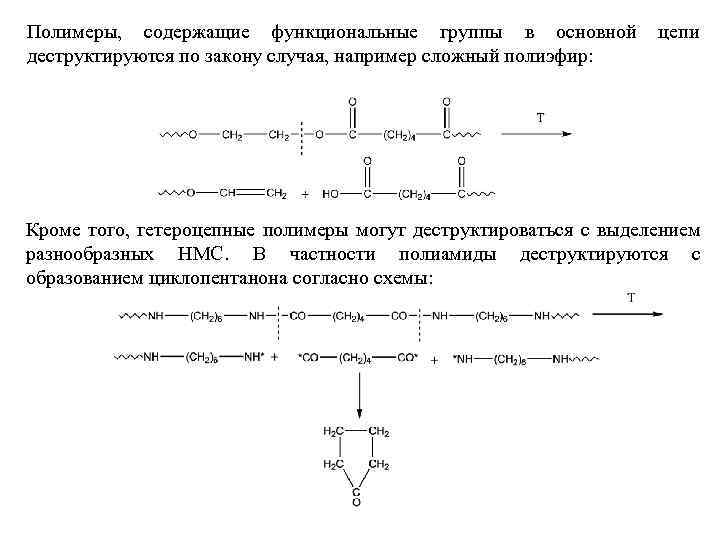 Полимеры, содержащие функциональные группы в основной деструктируются по закону случая, например сложный полиэфир: цепи Кроме того, гетероцепные полимеры могут деструктироваться с выделением разнообразных НМС. В частности полиамиды деструктируются с образованием циклопентанона согласно схемы:
Полимеры, содержащие функциональные группы в основной деструктируются по закону случая, например сложный полиэфир: цепи Кроме того, гетероцепные полимеры могут деструктироваться с выделением разнообразных НМС. В частности полиамиды деструктируются с образованием циклопентанона согласно схемы:
 Термостойкость полимеров - способность сохранять химическое строение и свойства при высоких температурах. Имеет значение как при переработке, так и при эксплуатации. Факторы, влияющие на термостойкость карбоцепных полимеров: - степень разветвленности. Разветвленные полимеры всегда менее термостойкие, чем неразветвленные; - количество заместителей. По мере увеличения числа заместителей в цепи энергия связи С-С уменьшается, поэтому ПЭ является более стойким материалом по сравнению с полипропиленом и полиизобутиленом; - микроструктура полимеров. Изотактические полимеры более термостойки, чем атактические; По величине температуры начала разложения (°С) наиболее чувствительны к термическому распаду: ПВХ (150), ПВА (170), ПММА (220). Высокой термостойкостью обладают лестничные полимеры, особенно с сопряженными двойными связями, сетчатые полимеры с ароматическими звеньями, элементорганические полимеры с высокой степенью поляризации ковалентных связей вдоль основной цепи. Например, полидиметилсилоксан (300), полиимид (450).
Термостойкость полимеров - способность сохранять химическое строение и свойства при высоких температурах. Имеет значение как при переработке, так и при эксплуатации. Факторы, влияющие на термостойкость карбоцепных полимеров: - степень разветвленности. Разветвленные полимеры всегда менее термостойкие, чем неразветвленные; - количество заместителей. По мере увеличения числа заместителей в цепи энергия связи С-С уменьшается, поэтому ПЭ является более стойким материалом по сравнению с полипропиленом и полиизобутиленом; - микроструктура полимеров. Изотактические полимеры более термостойки, чем атактические; По величине температуры начала разложения (°С) наиболее чувствительны к термическому распаду: ПВХ (150), ПВА (170), ПММА (220). Высокой термостойкостью обладают лестничные полимеры, особенно с сопряженными двойными связями, сетчатые полимеры с ароматическими звеньями, элементорганические полимеры с высокой степенью поляризации ковалентных связей вдоль основной цепи. Например, полидиметилсилоксан (300), полиимид (450).
 Фотодеструкция (фотолиз) Фотолиз протекает в полимерах под действием света с длиной волны l = 180 – 800 нм (УФ и видимая часть спектра электромагнитного излучения), наибольшее действие оказывает свет с длиной волны менее 400 нм. Фотолиз характерен для полимеров, содержащих группировки, способные поглощать свет из УФ и видимой областей электромагнитного спектра сопряженные двойные С=С связи в основной цепи и боковые хромофорные группы (бензольные ядра, ненасыщенные функциональные группы). При поглощении света происходит разрыв связей в основной или боковой цепях с образованием макрорадикалов, которые вызывают вторичные реакции распада, изомеризации, передачи цепи, сшивания. Преимущественное протекание одной из них предопределяется строением полимера и условиями. Поскольку группировки, способные к поглощению света могут содержаться не только в макромолекулах, но и в составе пластификаторов, стабилизаторов и т. п. то, под действием естественного освещения практически все полимеры подвергаются фотостарению в той или иной степени.
Фотодеструкция (фотолиз) Фотолиз протекает в полимерах под действием света с длиной волны l = 180 – 800 нм (УФ и видимая часть спектра электромагнитного излучения), наибольшее действие оказывает свет с длиной волны менее 400 нм. Фотолиз характерен для полимеров, содержащих группировки, способные поглощать свет из УФ и видимой областей электромагнитного спектра сопряженные двойные С=С связи в основной цепи и боковые хромофорные группы (бензольные ядра, ненасыщенные функциональные группы). При поглощении света происходит разрыв связей в основной или боковой цепях с образованием макрорадикалов, которые вызывают вторичные реакции распада, изомеризации, передачи цепи, сшивания. Преимущественное протекание одной из них предопределяется строением полимера и условиями. Поскольку группировки, способные к поглощению света могут содержаться не только в макромолекулах, но и в составе пластификаторов, стабилизаторов и т. п. то, под действием естественного освещения практически все полимеры подвергаются фотостарению в той или иной степени.
 В карбоцепных полимерах под действием света отщепляются боковые группы, чаще всего, водород, например в случае полиизопрена летучие продукты на 80 % содержат молекулярный водород: Последующие реакции макрорадикалов ведут к изменению строения, ММ и ММР полимеров. В разбавленных растворах полиизопрена образующийся макрорадикал аллильного типа может изомеризоваться, вызывая деструкцию макромолекулы: В концентрированных растворах или в массе протекают реакции сшивания:
В карбоцепных полимерах под действием света отщепляются боковые группы, чаще всего, водород, например в случае полиизопрена летучие продукты на 80 % содержат молекулярный водород: Последующие реакции макрорадикалов ведут к изменению строения, ММ и ММР полимеров. В разбавленных растворах полиизопрена образующийся макрорадикал аллильного типа может изомеризоваться, вызывая деструкцию макромолекулы: В концентрированных растворах или в массе протекают реакции сшивания:
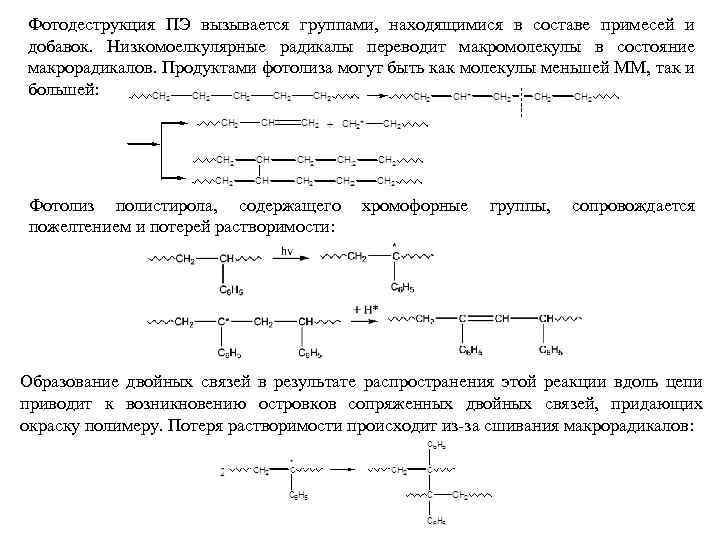 Фотодеструкция ПЭ вызывается группами, находящимися в составе примесей и добавок. Низкомоелкулярные радикалы переводит макромолекулы в состояние макрорадикалов. Продуктами фотолиза могут быть как молекулы меньшей ММ, так и большей: Фотолиз полистирола, содержащего пожелтением и потерей растворимости: хромофорные группы, сопровождается Образование двойных связей в результате распространения этой реакции вдоль цепи приводит к возникновению островков сопряженных двойных связей, придающих окраску полимеру. Потеря растворимости происходит из-за сшивания макрорадикалов:
Фотодеструкция ПЭ вызывается группами, находящимися в составе примесей и добавок. Низкомоелкулярные радикалы переводит макромолекулы в состояние макрорадикалов. Продуктами фотолиза могут быть как молекулы меньшей ММ, так и большей: Фотолиз полистирола, содержащего пожелтением и потерей растворимости: хромофорные группы, сопровождается Образование двойных связей в результате распространения этой реакции вдоль цепи приводит к возникновению островков сопряженных двойных связей, придающих окраску полимеру. Потеря растворимости происходит из-за сшивания макрорадикалов:
 Радиолиз протекает под действием излучений с высокой энергией: рентгеновские лучи, g-лучи, потоки заряженных частиц, энергия этих частиц составляет порядка 9 – 10 э. В. При поглощении энергии излучения в качестве первичных продуктов образуются макроионы, свободные электроны и возбужденные частицы, которые вызывают различные радиационно-химические превращения в полимерах: 1) разрыв связей в главных цепях и образование молекул меньшей длины; 2) образование химических связей между макромолекулами; 3) изменение числа и расположения двойных связей; Кроме того, в ходе радиационно-химических превращений выделяются низкомолекулярные соединения. Основными летучими продуктами являются: ПЭ, ПП, ПС, полибутадиен – молекулярный водород; сложные полиэфиры – оксид и диоксид углерода; ПВХ и поливинилиденхлорид – хлороводород и молекулярный хлор.
Радиолиз протекает под действием излучений с высокой энергией: рентгеновские лучи, g-лучи, потоки заряженных частиц, энергия этих частиц составляет порядка 9 – 10 э. В. При поглощении энергии излучения в качестве первичных продуктов образуются макроионы, свободные электроны и возбужденные частицы, которые вызывают различные радиационно-химические превращения в полимерах: 1) разрыв связей в главных цепях и образование молекул меньшей длины; 2) образование химических связей между макромолекулами; 3) изменение числа и расположения двойных связей; Кроме того, в ходе радиационно-химических превращений выделяются низкомолекулярные соединения. Основными летучими продуктами являются: ПЭ, ПП, ПС, полибутадиен – молекулярный водород; сложные полиэфиры – оксид и диоксид углерода; ПВХ и поливинилиденхлорид – хлороводород и молекулярный хлор.
 Под действием излучения макромолекулы ионизируются и возбуждаются: g П ® П+ + 1 е. П+ + е- ® П*, где П* - возбужденная макромолекула (молекула с избыточной энергией). Возбужденная макромолекула может распадаться на два радикала, что является актом деструкции: П* ® R 1 * + R 2 * Кроме того, возможно увеличение ненасыщенности цепей, сшивание макромолекул. Например радиолиз ПЭ:
Под действием излучения макромолекулы ионизируются и возбуждаются: g П ® П+ + 1 е. П+ + е- ® П*, где П* - возбужденная макромолекула (молекула с избыточной энергией). Возбужденная макромолекула может распадаться на два радикала, что является актом деструкции: П* ® R 1 * + R 2 * Кроме того, возможно увеличение ненасыщенности цепей, сшивание макромолекул. Например радиолиз ПЭ:
 Реакции деструкции и сшивания протекают одновременно, но в зависимости от химического строения полимера одна из них преобладает. Предпочтительной деструкции подвергаются: - полимеры, характеризующиеся низкими теплотами полимеризации, содержащие в основной цепи чередующиеся четвертичные атомы углерода: ПММА, полиизобутилен, поли- -метилстирол; - галогенсодержащие полимеры: ПВХ, поливинилиденхлорид, политетрафторэтилен, а также целлюлоза. Предпочтительному сшиванию подвергаются: - полимеры с высокой теплотой полимеризации, не имеющие четвертичных атомов углерода: ПЭ, СКИ, полибутадиен, ПМА, полиамиды, полиэфиры. Устойчивы к радиолизу полимеры на основе ароматических углеводородов, так как бензольные кольца способны поглощать значительную часть радиоизлучения. Деструкция полимеров с ароматическими заместителями протекает медленно. Стойкость ПС в 80 – 100 раз выше, чем у ПЭ.
Реакции деструкции и сшивания протекают одновременно, но в зависимости от химического строения полимера одна из них преобладает. Предпочтительной деструкции подвергаются: - полимеры, характеризующиеся низкими теплотами полимеризации, содержащие в основной цепи чередующиеся четвертичные атомы углерода: ПММА, полиизобутилен, поли- -метилстирол; - галогенсодержащие полимеры: ПВХ, поливинилиденхлорид, политетрафторэтилен, а также целлюлоза. Предпочтительному сшиванию подвергаются: - полимеры с высокой теплотой полимеризации, не имеющие четвертичных атомов углерода: ПЭ, СКИ, полибутадиен, ПМА, полиамиды, полиэфиры. Устойчивы к радиолизу полимеры на основе ароматических углеводородов, так как бензольные кольца способны поглощать значительную часть радиоизлучения. Деструкция полимеров с ароматическими заместителями протекает медленно. Стойкость ПС в 80 – 100 раз выше, чем у ПЭ.
 Механодеструкция (пластикация) протекает в условиях переработки полимеров на вальцах, в смесителях, в экструдерах; это явление характерно только для высокомолекулярных соединений. Почему? Потому что макромолекулы достаточно длинные и суммарная энергия межмолекулярного взаимодействия превышает энергию химической связи в основной цепи (например С-С связи). Поэтому сдвиговые деформации при перемешивании вызывают не нарушение межмолекулярного взаимодействия (как при перемешивании НМС), а разрывы химических связей в цепи. Механодеструкция протекает до тех пор, пока суммарная энергия физических межмолекулярных взаимодействий не станет равной энергии химической связи. Тогда под действием механического напряжения макромолекулы начнут смещаться относительно друга. Таким образом, механодеструкция способствует усреднению ММ и сужению ММР. Величина механодеструкции сильно зависит от температуры; имеет отрицательный температурный коэффициент - с понижением температуры возрастает число актов разрыва цепей, тогда как с повышением – возрастает скольжение макромолекул относительно друга.
Механодеструкция (пластикация) протекает в условиях переработки полимеров на вальцах, в смесителях, в экструдерах; это явление характерно только для высокомолекулярных соединений. Почему? Потому что макромолекулы достаточно длинные и суммарная энергия межмолекулярного взаимодействия превышает энергию химической связи в основной цепи (например С-С связи). Поэтому сдвиговые деформации при перемешивании вызывают не нарушение межмолекулярного взаимодействия (как при перемешивании НМС), а разрывы химических связей в цепи. Механодеструкция протекает до тех пор, пока суммарная энергия физических межмолекулярных взаимодействий не станет равной энергии химической связи. Тогда под действием механического напряжения макромолекулы начнут смещаться относительно друга. Таким образом, механодеструкция способствует усреднению ММ и сужению ММР. Величина механодеструкции сильно зависит от температуры; имеет отрицательный температурный коэффициент - с понижением температуры возрастает число актов разрыва цепей, тогда как с повышением – возрастает скольжение макромолекул относительно друга.
 В процессе механодеструкции происходят разрывы связей в макромолекулах и инициируются различные химические реакции. Образовавшиеся при механодеструкции активные макрорадикалы стабилизируются путем взаимодействия с активными центрами других макромолекул ( -СН 2 двойные связи, трет. атом углерода), взаимодействия между собой и с НМС. На примере полибутадиена: взаимодействие с -СН 2
В процессе механодеструкции происходят разрывы связей в макромолекулах и инициируются различные химические реакции. Образовавшиеся при механодеструкции активные макрорадикалы стабилизируются путем взаимодействия с активными центрами других макромолекул ( -СН 2 двойные связи, трет. атом углерода), взаимодействия между собой и с НМС. На примере полибутадиена: взаимодействие с -СН 2
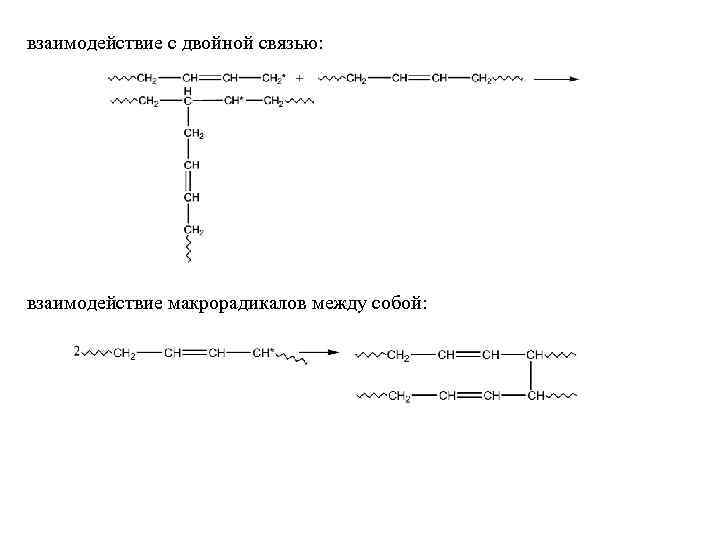 взаимодействие с двойной связью: взаимодействие макрорадикалов между собой:
взаимодействие с двойной связью: взаимодействие макрорадикалов между собой:
 Окисление полимеров Химическое взаимодействие полимеров с кислородом воздуха лежит в основе реакций, ведущих к быстрому выходу полимерных изделий из строя в результате окислительного старения. Процесс окисления активируется под действием: тепла, механических нагрузок, ультрафиолета, радиационного излучения, химических веществ (агрессивных сред, солей металлов переменной валентности). В реальных условиях чаще всего наблюдается совместное действие перечисленных факторов. Механизм окисления полимеров – свободно-радикальный цепной с вырожденным разветвлением. Характеризуется наличием трех стадий: инициирования, роста и обрыва цепи.
Окисление полимеров Химическое взаимодействие полимеров с кислородом воздуха лежит в основе реакций, ведущих к быстрому выходу полимерных изделий из строя в результате окислительного старения. Процесс окисления активируется под действием: тепла, механических нагрузок, ультрафиолета, радиационного излучения, химических веществ (агрессивных сред, солей металлов переменной валентности). В реальных условиях чаще всего наблюдается совместное действие перечисленных факторов. Механизм окисления полимеров – свободно-радикальный цепной с вырожденным разветвлением. Характеризуется наличием трех стадий: инициирования, роста и обрыва цепи.
 Механизм окисления полимеров в общем виде Инициирование сводится к образованию свободных радикалов в результате: а) «чистого» окисления связей С-Н кислородом воздуха, при этом реакционным центром становятся -метиленовое звено или третичный атом углерода, содержащие подвижный атом водорода: RH + O 2 ® R* + HOO* 2 RH + O 2 ® 2 R* + H 2 O 2 Однако эта реакция протекает с низкой скоростью. б) гомолитического распада тех же связей С-Н под действием различных видов энергии (тепловой, световой, механической): RH ® R* + Н* R* + О 2 ® ROO*
Механизм окисления полимеров в общем виде Инициирование сводится к образованию свободных радикалов в результате: а) «чистого» окисления связей С-Н кислородом воздуха, при этом реакционным центром становятся -метиленовое звено или третичный атом углерода, содержащие подвижный атом водорода: RH + O 2 ® R* + HOO* 2 RH + O 2 ® 2 R* + H 2 O 2 Однако эта реакция протекает с низкой скоростью. б) гомолитического распада тех же связей С-Н под действием различных видов энергии (тепловой, световой, механической): RH ® R* + Н* R* + О 2 ® ROO*
 Рост цепи: ROO* + Образующиеся окисления. гидроперекиси RH ® ROOH + R* называются первичными продуктами Вырожденное разветвление цепи происходит в результате распада чрезвычайно неустойчивых гидроперекисей с образованием новых радикалов (окисных, углеводородных): ROOH ® RO* + OH* RO* + RH ® ROH + R* OH* + RH ® R* + H 2 O Обрыв цепи: происходит в результате рекомбинации радикалов: 2 R* ® R-R R* + ROO* ® ROOR 2 ROO* ® O 2 + ROOR RO* + R* ® ROR
Рост цепи: ROO* + Образующиеся окисления. гидроперекиси RH ® ROOH + R* называются первичными продуктами Вырожденное разветвление цепи происходит в результате распада чрезвычайно неустойчивых гидроперекисей с образованием новых радикалов (окисных, углеводородных): ROOH ® RO* + OH* RO* + RH ® ROH + R* OH* + RH ® R* + H 2 O Обрыв цепи: происходит в результате рекомбинации радикалов: 2 R* ® R-R R* + ROO* ® ROOR 2 ROO* ® O 2 + ROOR RO* + R* ® ROR
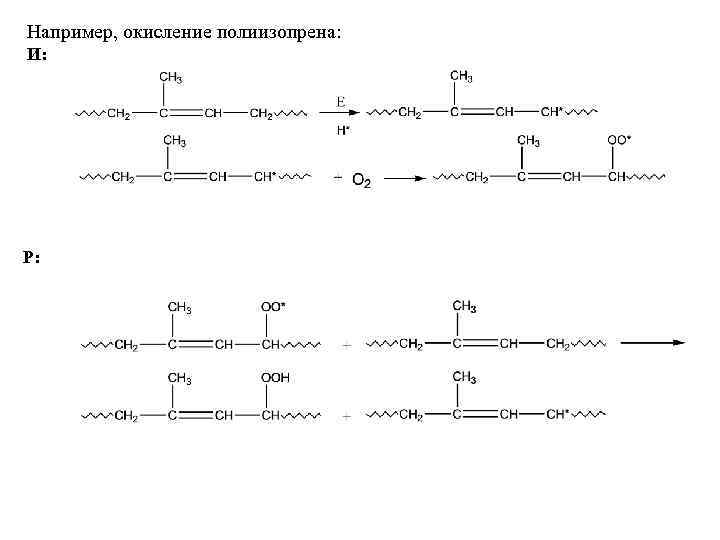 Например, окисление полиизопрена: И: Р:
Например, окисление полиизопрена: И: Р:
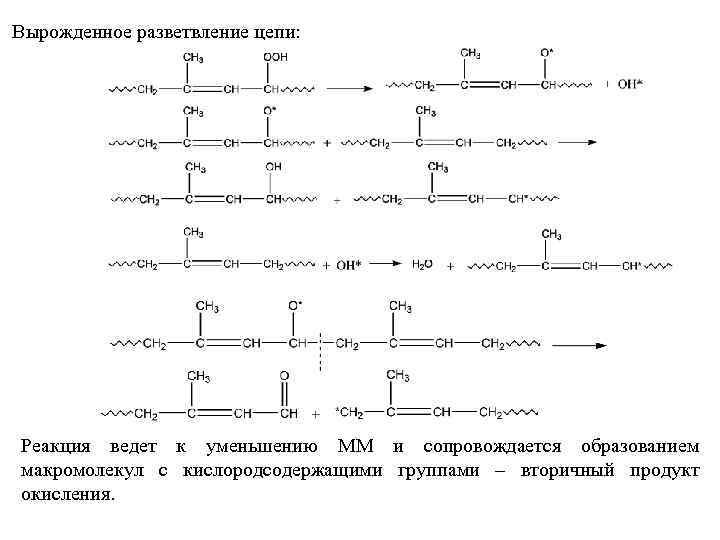 Вырожденное разветвление цепи: Реакция ведет к уменьшению ММ и сопровождается образованием макромолекул с кислородсодержащими группами – вторичный продукт окисления.
Вырожденное разветвление цепи: Реакция ведет к уменьшению ММ и сопровождается образованием макромолекул с кислородсодержащими группами – вторичный продукт окисления.
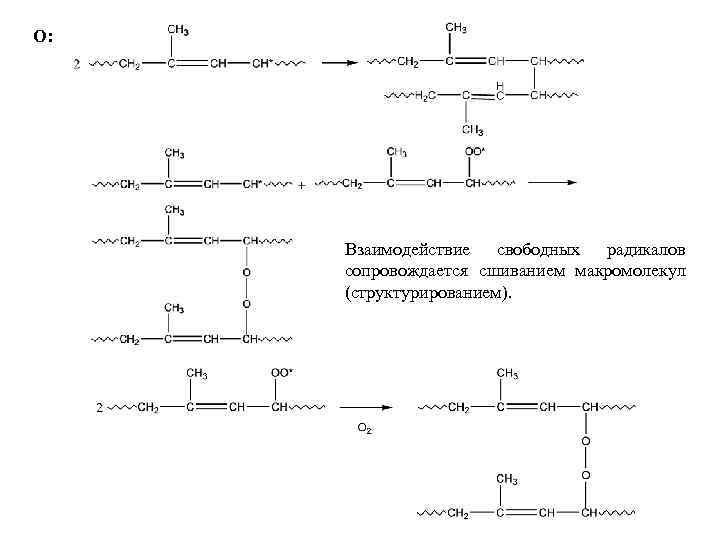 О: Взаимодействие свободных радикалов сопровождается сшиванием макромолекул (структурированием).
О: Взаимодействие свободных радикалов сопровождается сшиванием макромолекул (структурированием).
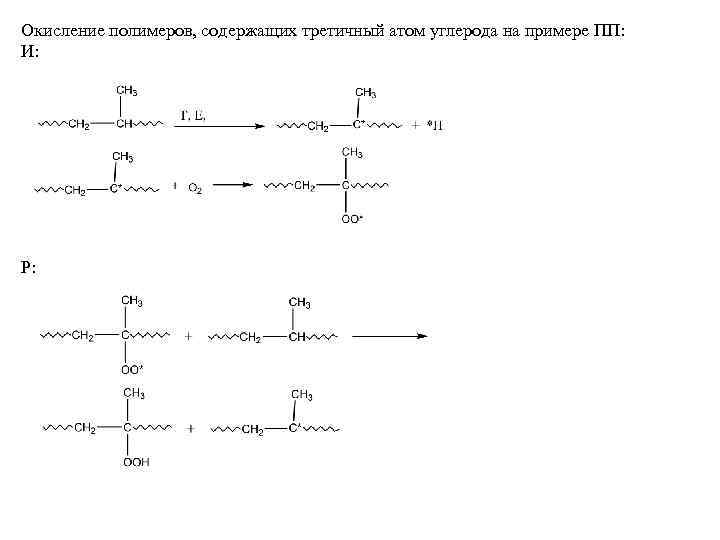 Окисление полимеров, содержащих третичный атом углерода на примере ПП: И: Р:
Окисление полимеров, содержащих третичный атом углерода на примере ПП: И: Р:
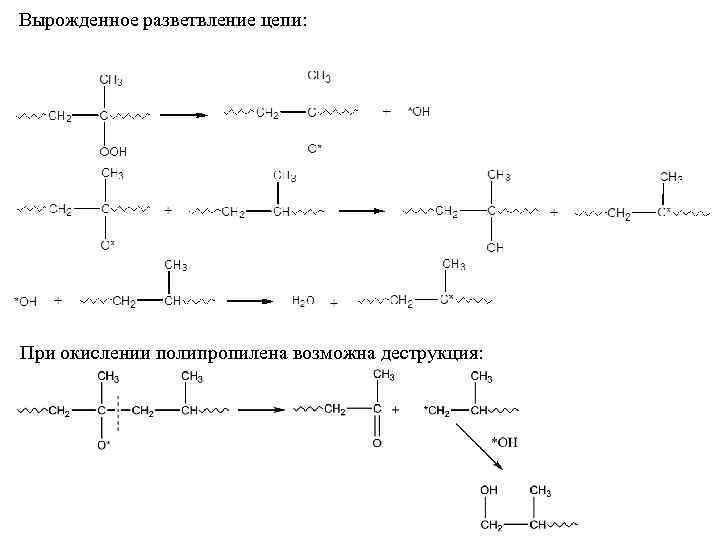 Вырожденное разветвление цепи: При окислении полипропилена возможна деструкция:
Вырожденное разветвление цепи: При окислении полипропилена возможна деструкция:
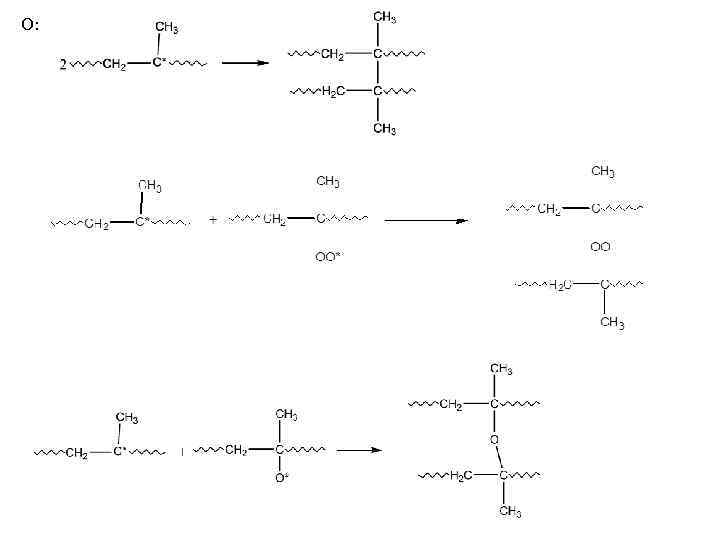 О:
О:
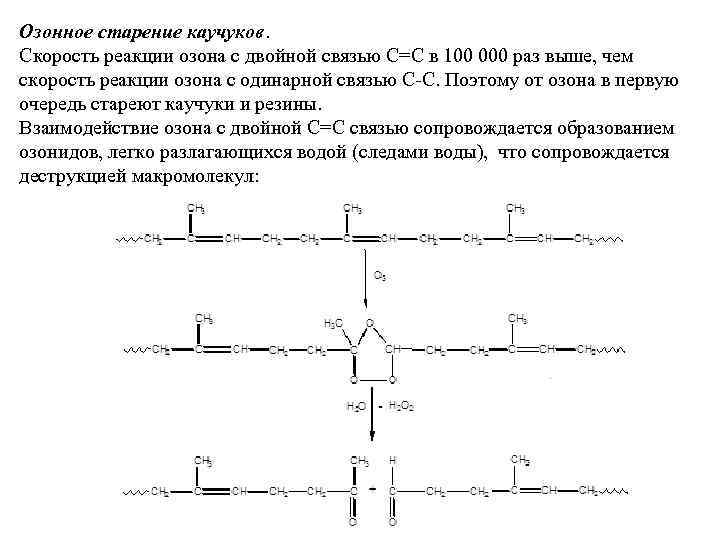 Озонное старение каучуков. Скорость реакции озона с двойной связью С=С в 100 000 раз выше, чем скорость реакции озона с одинарной связью С-С. Поэтому от озона в первую очередь стареют каучуки и резины. Взаимодействие озона с двойной С=С связью сопровождается образованием озонидов, легко разлагающихся водой (следами воды), что сопровождается деструкцией макромолекул:
Озонное старение каучуков. Скорость реакции озона с двойной связью С=С в 100 000 раз выше, чем скорость реакции озона с одинарной связью С-С. Поэтому от озона в первую очередь стареют каучуки и резины. Взаимодействие озона с двойной С=С связью сопровождается образованием озонидов, легко разлагающихся водой (следами воды), что сопровождается деструкцией макромолекул:
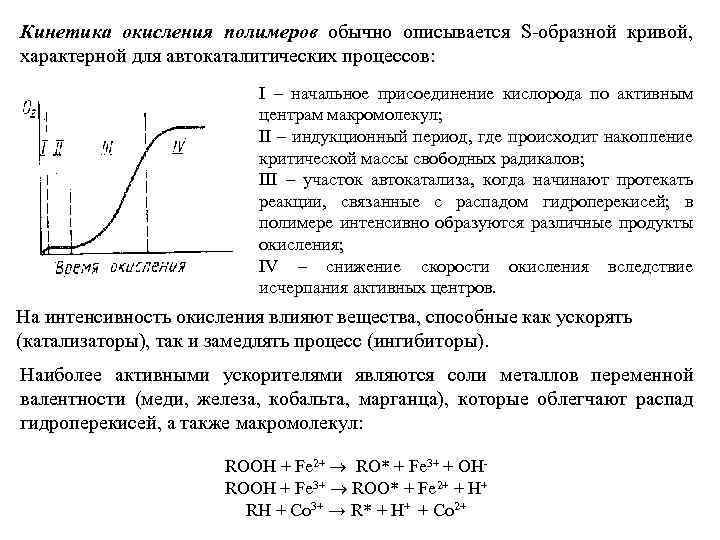 Кинетика окисления полимеров обычно описывается S-образной кривой, характерной для автокаталитических процессов: I – начальное присоединение кислорода по активным центрам макромолекул; II – индукционный период, где происходит накопление критической массы свободных радикалов; III – участок автокатализа, когда начинают протекать реакции, связанные с распадом гидроперекисей; в полимере интенсивно образуются различные продукты окисления; IV – снижение скорости окисления вследствие исчерпания активных центров. На интенсивность окисления влияют вещества, способные как ускорять (катализаторы), так и замедлять процесс (ингибиторы). Наиболее активными ускорителями являются соли металлов переменной валентности (меди, железа, кобальта, марганца), которые облегчают распад гидроперекисей, а также макромолекул: ROOH + Fe 2+ ® RO* + Fe 3+ + OHROOH + Fe 3+ ® ROO* + Fe 2+ + H+ RH + Co 3+ → R* + H+ + Co 2+
Кинетика окисления полимеров обычно описывается S-образной кривой, характерной для автокаталитических процессов: I – начальное присоединение кислорода по активным центрам макромолекул; II – индукционный период, где происходит накопление критической массы свободных радикалов; III – участок автокатализа, когда начинают протекать реакции, связанные с распадом гидроперекисей; в полимере интенсивно образуются различные продукты окисления; IV – снижение скорости окисления вследствие исчерпания активных центров. На интенсивность окисления влияют вещества, способные как ускорять (катализаторы), так и замедлять процесс (ингибиторы). Наиболее активными ускорителями являются соли металлов переменной валентности (меди, железа, кобальта, марганца), которые облегчают распад гидроперекисей, а также макромолекул: ROOH + Fe 2+ ® RO* + Fe 3+ + OHROOH + Fe 3+ ® ROO* + Fe 2+ + H+ RH + Co 3+ → R* + H+ + Co 2+
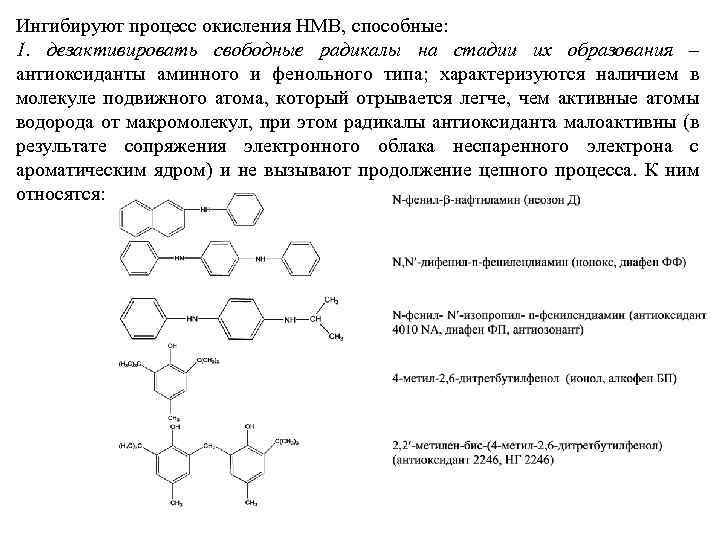 Ингибируют процесс окисления НМВ, способные: 1. дезактивировать свободные радикалы на стадии их образования – антиоксиданты аминного и фенольного типа; характеризуются наличием в молекуле подвижного атома, который отрывается легче, чем активные атомы водорода от макромолекул, при этом радикалы антиоксиданта малоактивны (в результате сопряжения электронного облака неспаренного электрона с ароматическим ядром) и не вызывают продолжение цепного процесса. К ним относятся:
Ингибируют процесс окисления НМВ, способные: 1. дезактивировать свободные радикалы на стадии их образования – антиоксиданты аминного и фенольного типа; характеризуются наличием в молекуле подвижного атома, который отрывается легче, чем активные атомы водорода от макромолекул, при этом радикалы антиоксиданта малоактивны (в результате сопряжения электронного облака неспаренного электрона с ароматическим ядром) и не вызывают продолжение цепного процесса. К ним относятся:
 Ингибирование протекает согласно следующих уравнений: R* + Ing. H ® RH + Ing* ROO* + Ing. H ® ROOH + Ing* ROO* + Ing* ® ROOIng R* + Ing*® RIng 2 Ing*® Ing-Ing В процессе окисления антиоксидант расходуется, при этом часть его присоединяется к полимеру. Т. о. действие антиоксидантов первой группы заключается во взаимодействии со свободными радикалами и обрыве цепи. На кинетике это отражается увеличением длительности индукционного периода. Однако полностью окисление не прекращается, поскольку в полимере образуются легко разлагающиеся гидроперекиси, после исчерпания антиоксиданта процесс окисления продолжается.
Ингибирование протекает согласно следующих уравнений: R* + Ing. H ® RH + Ing* ROO* + Ing. H ® ROOH + Ing* ROO* + Ing* ® ROOIng R* + Ing*® RIng 2 Ing*® Ing-Ing В процессе окисления антиоксидант расходуется, при этом часть его присоединяется к полимеру. Т. о. действие антиоксидантов первой группы заключается во взаимодействии со свободными радикалами и обрыве цепи. На кинетике это отражается увеличением длительности индукционного периода. Однако полностью окисление не прекращается, поскольку в полимере образуются легко разлагающиеся гидроперекиси, после исчерпания антиоксиданта процесс окисления продолжается.
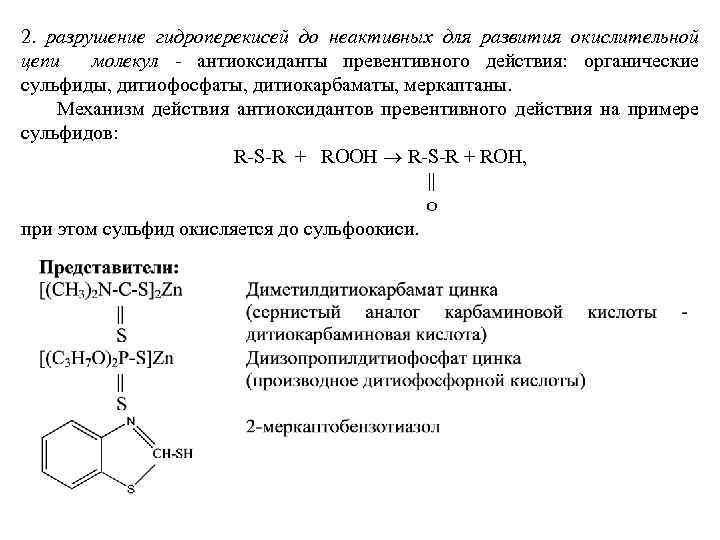 2. разрушение гидроперекисей до неактивных для развития окислительной цепи молекул - антиоксиданты превентивного действия: органические сульфиды, дитиофосфаты, дитиокарбаматы, меркаптаны. Механизм действия антиоксидантов превентивного действия на примере сульфидов: R-S-R + ROOH ® R-S-R + ROH, O при этом сульфид окисляется до сульфоокиси.
2. разрушение гидроперекисей до неактивных для развития окислительной цепи молекул - антиоксиданты превентивного действия: органические сульфиды, дитиофосфаты, дитиокарбаматы, меркаптаны. Механизм действия антиоксидантов превентивного действия на примере сульфидов: R-S-R + ROOH ® R-S-R + ROH, O при этом сульфид окисляется до сульфоокиси.
 Антиоксиданты второй группы не влияют на величину индукционного периода, но сильно снижают скорость окисления на втором участке; кроме того, способны дезактивировать соли металлов переменной валентности, образуя с ними неактивные комплексы. Для усиления защиты от окисления в полимерные системы вводят антиоксиданты первой и второй групп, которые при совместном присутствии обладают синергизмом. Это приводит к резкому увеличению индукционного периода и снижению скорости окисления во втором периоде. В литературе имеются данные о антиоксидантах молекулы которых содержат два антиокислительных центра: фенольный фрагмент и серу, причем количество обоих центров в молекуле должно быть равным. Они гораздо лучше тормозят окисление, чем обычные антиоксиданты и антиоксиданты, в которых на один атом серы приходится два фенольных фрагмента – антиоксиданты третьего поколения.
Антиоксиданты второй группы не влияют на величину индукционного периода, но сильно снижают скорость окисления на втором участке; кроме того, способны дезактивировать соли металлов переменной валентности, образуя с ними неактивные комплексы. Для усиления защиты от окисления в полимерные системы вводят антиоксиданты первой и второй групп, которые при совместном присутствии обладают синергизмом. Это приводит к резкому увеличению индукционного периода и снижению скорости окисления во втором периоде. В литературе имеются данные о антиоксидантах молекулы которых содержат два антиокислительных центра: фенольный фрагмент и серу, причем количество обоих центров в молекуле должно быть равным. Они гораздо лучше тормозят окисление, чем обычные антиоксиданты и антиоксиданты, в которых на один атом серы приходится два фенольных фрагмента – антиоксиданты третьего поколения.
 Скорость окисления полимеров зависит от наличия в цепях активных центров: - -метиленовых звеньев; - третичных атомов углерода. По способности к окислению полимеры располагаются в ряд: полидиметилсилоксан < полиэфиры < БК < СКН < полихлоропрен < СКС < СКД < СКИ В целом, ненасыщенные полимеры окисляются с большей скоростью, чем насыщенные. На скорость окисления влияет положение двойных связей и наличие заместителей у двойных связей: - звенья 1, 4 окисляются быстрее, чем 1, 2; - электронодонорные заместители (СН 3, ОСН 3) ускоряют окисление, электроноакцепторные – замедляют (хлор, нитрильная группа). Поэтому скорость окисления изопренового каучука выше, чем бутадиеннитрильного или хлоропренового, которые заметно окисляются только при повышенных температурах (300 С).
Скорость окисления полимеров зависит от наличия в цепях активных центров: - -метиленовых звеньев; - третичных атомов углерода. По способности к окислению полимеры располагаются в ряд: полидиметилсилоксан < полиэфиры < БК < СКН < полихлоропрен < СКС < СКД < СКИ В целом, ненасыщенные полимеры окисляются с большей скоростью, чем насыщенные. На скорость окисления влияет положение двойных связей и наличие заместителей у двойных связей: - звенья 1, 4 окисляются быстрее, чем 1, 2; - электронодонорные заместители (СН 3, ОСН 3) ускоряют окисление, электроноакцепторные – замедляют (хлор, нитрильная группа). Поэтому скорость окисления изопренового каучука выше, чем бутадиеннитрильного или хлоропренового, которые заметно окисляются только при повышенных температурах (300 С).
 Основная причина изменений в полимерах в процессе окисления – это протекание реакций деструкции и сшивания. В первом случае образуются молекулы меньшей ММ с концевыми кислородсодержащими функциональными группами, во втором – макромолекулы с повышенной ММ. Соотношение между актами распада и сшивания зависит от структуры полимера и температуры окисления. В случае эластомеров, построенных из звеньев 1, 4 с электронодонорными заместителями, преобладает деструкция, полимеры становятся мягкими и липкими. Для полибутадиена и его сополимеров – сшивание, полимеры становятся хрупкими и твердыми.
Основная причина изменений в полимерах в процессе окисления – это протекание реакций деструкции и сшивания. В первом случае образуются молекулы меньшей ММ с концевыми кислородсодержащими функциональными группами, во втором – макромолекулы с повышенной ММ. Соотношение между актами распада и сшивания зависит от структуры полимера и температуры окисления. В случае эластомеров, построенных из звеньев 1, 4 с электронодонорными заместителями, преобладает деструкция, полимеры становятся мягкими и липкими. Для полибутадиена и его сополимеров – сшивание, полимеры становятся хрупкими и твердыми.
 Реакции сшивания (структурирования) – это реакции, протекающие с образованием поперечных связей между макромолекулами, сопровождаются образованием полимеров сетчатого строения. Реакции сшивания протекают как в процессе синтеза полимеров, так и при переработке в полимерные изделия: реакции вулканизации (при изготовлении резин) и отверждения (при изготовлении пластмасс). Сшивание может быть осуществлено в результате: 1. Взаимодействия функциональных групп разных полимеров; 2. Взаимодействия функциональных групп одного и того же полимера; 3. Взаимодействия функциональных групп или активных центров макромолекул с полифункциональным НМС. Для осуществления сшивания требуется внешнее воздействие – нагревание, использование катализаторов, УФ- или радиационного облучения.
Реакции сшивания (структурирования) – это реакции, протекающие с образованием поперечных связей между макромолекулами, сопровождаются образованием полимеров сетчатого строения. Реакции сшивания протекают как в процессе синтеза полимеров, так и при переработке в полимерные изделия: реакции вулканизации (при изготовлении резин) и отверждения (при изготовлении пластмасс). Сшивание может быть осуществлено в результате: 1. Взаимодействия функциональных групп разных полимеров; 2. Взаимодействия функциональных групп одного и того же полимера; 3. Взаимодействия функциональных групп или активных центров макромолекул с полифункциональным НМС. Для осуществления сшивания требуется внешнее воздействие – нагревание, использование катализаторов, УФ- или радиационного облучения.
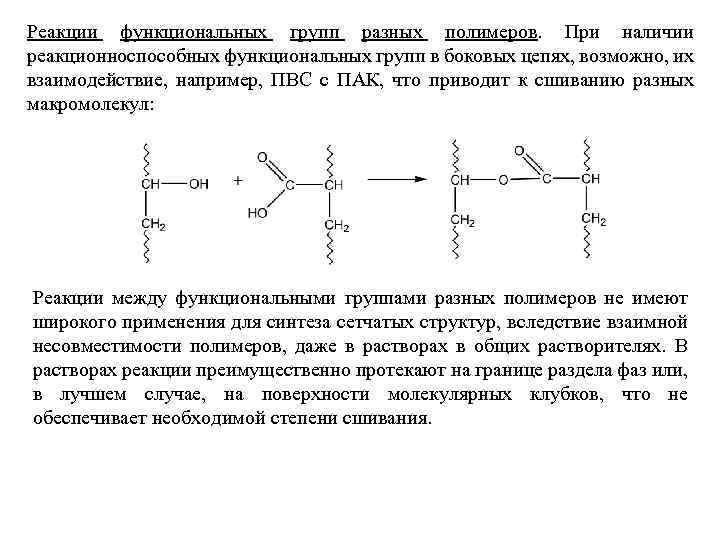 Реакции функциональных групп разных полимеров. При наличии реакционноспособных функциональных групп в боковых цепях, возможно, их взаимодействие, например, ПВС с ПАК, что приводит к сшиванию разных макромолекул: Реакции между функциональными группами разных полимеров не имеют широкого применения для синтеза сетчатых структур, вследствие взаимной несовместимости полимеров, даже в растворах в общих растворителях. В растворах реакции преимущественно протекают на границе раздела фаз или, в лучшем случае, на поверхности молекулярных клубков, что не обеспечивает необходимой степени сшивания.
Реакции функциональных групп разных полимеров. При наличии реакционноспособных функциональных групп в боковых цепях, возможно, их взаимодействие, например, ПВС с ПАК, что приводит к сшиванию разных макромолекул: Реакции между функциональными группами разных полимеров не имеют широкого применения для синтеза сетчатых структур, вследствие взаимной несовместимости полимеров, даже в растворах в общих растворителях. В растворах реакции преимущественно протекают на границе раздела фаз или, в лучшем случае, на поверхности молекулярных клубков, что не обеспечивает необходимой степени сшивания.
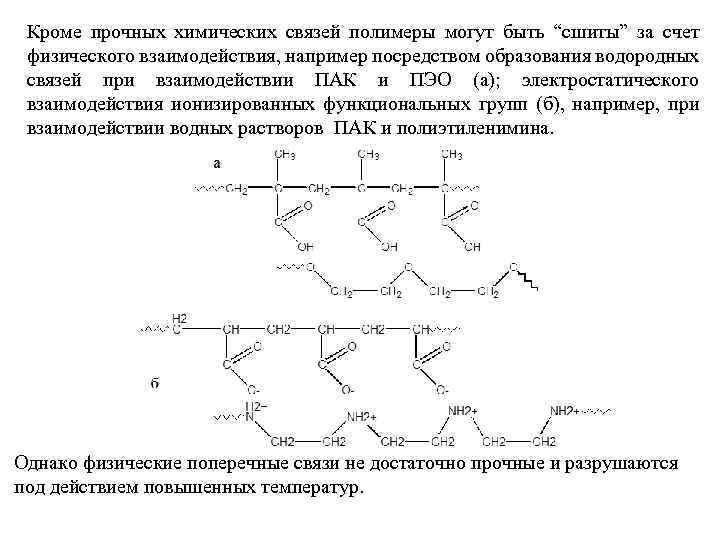 Кроме прочных химических связей полимеры могут быть “сшиты” за счет физического взаимодействия, например посредством образования водородных связей при взаимодействии ПАК и ПЭО (а); электростатического взаимодействия ионизированных функциональных групп (б), например, при взаимодействии водных растворов ПАК и полиэтиленимина. Однако физические поперечные связи не достаточно прочные и разрушаются под действием повышенных температур.
Кроме прочных химических связей полимеры могут быть “сшиты” за счет физического взаимодействия, например посредством образования водородных связей при взаимодействии ПАК и ПЭО (а); электростатического взаимодействия ионизированных функциональных групп (б), например, при взаимодействии водных растворов ПАК и полиэтиленимина. Однако физические поперечные связи не достаточно прочные и разрушаются под действием повышенных температур.
 Реакции функциональных групп одного и того же полимера протекают при наличии в полимере разных по природе функциональных групп. Например, реакции полиорганосилоксанов, содержащих винильные радикалы, а также гидридные связи Si – Н легко протекают в присутствии катализаторов с образованием поперечных связей между силоксановыми цепями: Особенностью таких реакций является возможность их внутримолекулярного протекания, что будет приводить к образованию циклов вместо поперечных связей.
Реакции функциональных групп одного и того же полимера протекают при наличии в полимере разных по природе функциональных групп. Например, реакции полиорганосилоксанов, содержащих винильные радикалы, а также гидридные связи Si – Н легко протекают в присутствии катализаторов с образованием поперечных связей между силоксановыми цепями: Особенностью таких реакций является возможность их внутримолекулярного протекания, что будет приводить к образованию циклов вместо поперечных связей.
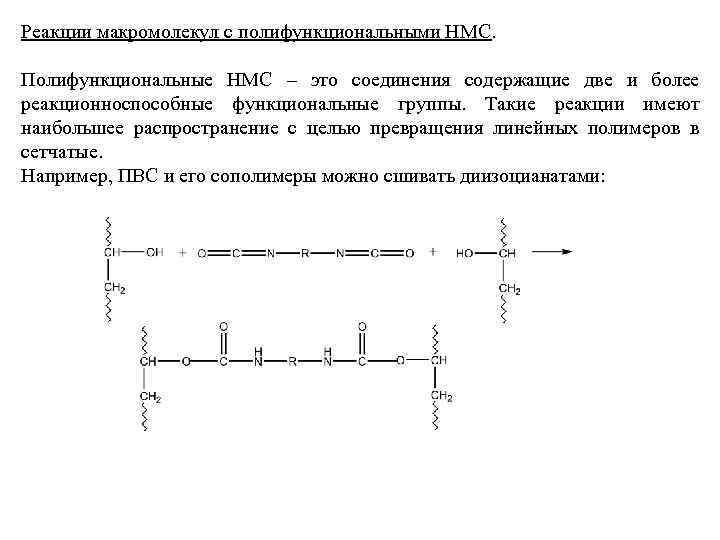 Реакции макромолекул с полифункциональными НМС. Полифункциональные НМС – это соединения содержащие две и более реакционноспособные функциональные группы. Такие реакции имеют наибольшее распространение с целью превращения линейных полимеров в сетчатые. Например, ПВС и его сополимеры можно сшивать диизоцианатами:
Реакции макромолекул с полифункциональными НМС. Полифункциональные НМС – это соединения содержащие две и более реакционноспособные функциональные группы. Такие реакции имеют наибольшее распространение с целью превращения линейных полимеров в сетчатые. Например, ПВС и его сополимеры можно сшивать диизоцианатами:
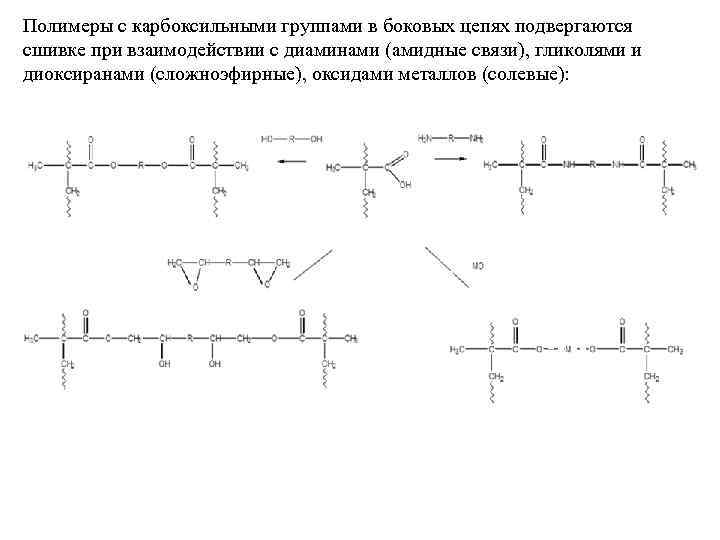 Полимеры с карбоксильными группами в боковых цепях подвергаются сшивке при взаимодействии с диаминами (амидные связи), гликолями и диоксиранами (сложноэфирные), оксидами металлов (солевые):
Полимеры с карбоксильными группами в боковых цепях подвергаются сшивке при взаимодействии с диаминами (амидные связи), гликолями и диоксиранами (сложноэфирные), оксидами металлов (солевые):
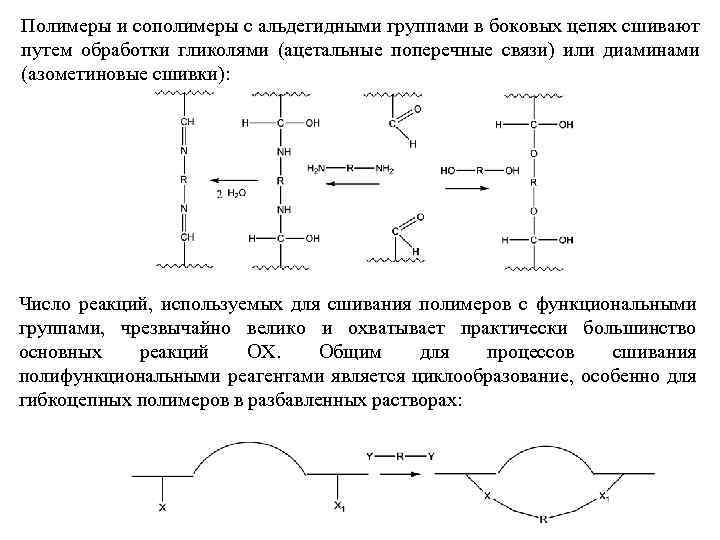 Полимеры и сополимеры с альдегидными группами в боковых цепях сшивают путем обработки гликолями (ацетальные поперечные связи) или диаминами (азометиновые сшивки): Число реакций, используемых для сшивания полимеров с функциональными группами, чрезвычайно велико и охватывает практически большинство основных реакций ОХ. Общим для процессов сшивания полифункциональными реагентами является циклообразование, особенно для гибкоцепных полимеров в разбавленных растворах:
Полимеры и сополимеры с альдегидными группами в боковых цепях сшивают путем обработки гликолями (ацетальные поперечные связи) или диаминами (азометиновые сшивки): Число реакций, используемых для сшивания полимеров с функциональными группами, чрезвычайно велико и охватывает практически большинство основных реакций ОХ. Общим для процессов сшивания полифункциональными реагентами является циклообразование, особенно для гибкоцепных полимеров в разбавленных растворах:
 Вулканизация эластомеров С химической точки зрения: вулканизация – это процесс образования редкой сетки поперечных связей между макромолекулами. С технологической точки зрения: вулканизация – это процесс превращения сырого каучука в резину, материал, обладающий в широком температурном интервале необходимыми эксплуатационными свойствами (прочностью, высокоэластичностью, твердостью, сопротивлением раздиру и т. д. ). Вулканизация может происходить под действием: физических факторов - повышенных температур (термовулканизация), радиации (радиационная вулканизация); химических факторов - вулканизующего агента (сера, перекиси, ди- и полисульфиды, оксиды металлов, азо- и диазосоединения, би-, трифункциональные соединения). Способ вулканизации предопределяется строением каучука и условиями эксплуатации резиновых изделий. При переходе от одного метода вулканизации к другому можно в широких пределах менять свойства резин на основе одного и того же каучука.
Вулканизация эластомеров С химической точки зрения: вулканизация – это процесс образования редкой сетки поперечных связей между макромолекулами. С технологической точки зрения: вулканизация – это процесс превращения сырого каучука в резину, материал, обладающий в широком температурном интервале необходимыми эксплуатационными свойствами (прочностью, высокоэластичностью, твердостью, сопротивлением раздиру и т. д. ). Вулканизация может происходить под действием: физических факторов - повышенных температур (термовулканизация), радиации (радиационная вулканизация); химических факторов - вулканизующего агента (сера, перекиси, ди- и полисульфиды, оксиды металлов, азо- и диазосоединения, би-, трифункциональные соединения). Способ вулканизации предопределяется строением каучука и условиями эксплуатации резиновых изделий. При переходе от одного метода вулканизации к другому можно в широких пределах менять свойства резин на основе одного и того же каучука.
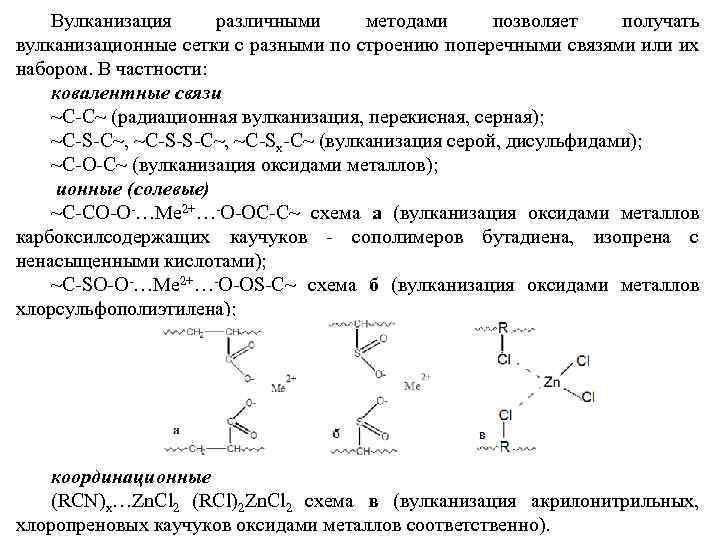 Вулканизация различными методами позволяет получать вулканизационные сетки с разными по строению поперечными связями или их набором. В частности: ковалентные связи ~С-С~ (радиационная вулканизация, перекисная, серная); ~С-S-С~, ~С-Sх-С~ (вулканизация серой, дисульфидами); ~С-О-С~ (вулканизация оксидами металлов); ионные (солевые) ~С-СО-О-…Ме 2+…-О-ОС-С~ схема а (вулканизация оксидами металлов карбоксилсодержащих каучуков - сополимеров бутадиена, изопрена с ненасыщенными кислотами); ~С-SО-О-…Ме 2+…-О-ОS-С~ схема б (вулканизация оксидами металлов хлорсульфополиэтилена); координационные (RCN)x…Zn. Cl 2 (RCl)2 Zn. Cl 2 схема в (вулканизация акрилонитрильных, хлоропреновых каучуков оксидами металлов соответственно).
Вулканизация различными методами позволяет получать вулканизационные сетки с разными по строению поперечными связями или их набором. В частности: ковалентные связи ~С-С~ (радиационная вулканизация, перекисная, серная); ~С-S-С~, ~С-Sх-С~ (вулканизация серой, дисульфидами); ~С-О-С~ (вулканизация оксидами металлов); ионные (солевые) ~С-СО-О-…Ме 2+…-О-ОС-С~ схема а (вулканизация оксидами металлов карбоксилсодержащих каучуков - сополимеров бутадиена, изопрена с ненасыщенными кислотами); ~С-SО-О-…Ме 2+…-О-ОS-С~ схема б (вулканизация оксидами металлов хлорсульфополиэтилена); координационные (RCN)x…Zn. Cl 2 (RCl)2 Zn. Cl 2 схема в (вулканизация акрилонитрильных, хлоропреновых каучуков оксидами металлов соответственно).
 Свойства резин изменяются в зависимости от типа поперечных связей: серная вулканизация позволяет получать резины с хорошими динамическими свойствами; перекисная – резины с повышенной теплостойкостью; радиационная – резины с улучшенными диэлектрическими характеристиками. При этом методы вулканизации, разработанные для каучуков общего назначения, как правило не приемлемы для каучуков специального назначения. Технические способы проведения вулканизации: - вулканизация в горячем воздухе; в основном используется для вулканизации изделий из резин на основе насыщенных каучуков в термостатах при 150 – 250 С; - вулканизация в поле токов высокой частоты; используется для вулканизации полярных каучуков (хлоропреновый, бутадиен-нитрильные и др. ), обогрев осуществляется тепловой энергией генерируемой переменным электрическим полем сверхвысокой частоты; - вулканизация в псевдоожиженном слое; используется для вулканизации полых и пористых резиновых профилей в среде стеклянных шариков или кварцевого песка, поддерживаемых во взвешенном состоянии горячим воздухом 150 – 250 С, продуваемом с определенной скоростью; - вулканизация в расплаве солей; используются расплавы солей, температуры расплава которых 170 – 300 С.
Свойства резин изменяются в зависимости от типа поперечных связей: серная вулканизация позволяет получать резины с хорошими динамическими свойствами; перекисная – резины с повышенной теплостойкостью; радиационная – резины с улучшенными диэлектрическими характеристиками. При этом методы вулканизации, разработанные для каучуков общего назначения, как правило не приемлемы для каучуков специального назначения. Технические способы проведения вулканизации: - вулканизация в горячем воздухе; в основном используется для вулканизации изделий из резин на основе насыщенных каучуков в термостатах при 150 – 250 С; - вулканизация в поле токов высокой частоты; используется для вулканизации полярных каучуков (хлоропреновый, бутадиен-нитрильные и др. ), обогрев осуществляется тепловой энергией генерируемой переменным электрическим полем сверхвысокой частоты; - вулканизация в псевдоожиженном слое; используется для вулканизации полых и пористых резиновых профилей в среде стеклянных шариков или кварцевого песка, поддерживаемых во взвешенном состоянии горячим воздухом 150 – 250 С, продуваемом с определенной скоростью; - вулканизация в расплаве солей; используются расплавы солей, температуры расплава которых 170 – 300 С.
 Изменение свойств каучука при вулканизации. Наиболее характерными являются: 1. Вулканизаты обладают высокой эластичностью, не способны к пластической (необратимой) деформации в отличие от сырых резиновых смесей. 2. Вулканизат теряет способность растворяться даже в термодинамически “хороших” растворителях: он лишь ограниченно набухает в них. 3. Резко повышается прочность при растяжении: резиновая смесь на основе НК (после обработки на вальцах) имеет прочность при растяжении 1 – 1, 5 МПа, после вулканизации до 35 МПа. Однако прочность в зависимости от степени вулканизации изменяется экстремально (рис. ). 4. Повышается твердость материала и улучшаются его динамические свойства (при многократных циклических деформациях). 5. Повышается стойкость к старению. 6. Уменьшается влаго- и газопроницаемость, т. к. сшивание макромолекул уменьшает диффузию газов и паров. Рис. Зависимость прочности вулканизатов при одноосном растяжении от степени вулканизации
Изменение свойств каучука при вулканизации. Наиболее характерными являются: 1. Вулканизаты обладают высокой эластичностью, не способны к пластической (необратимой) деформации в отличие от сырых резиновых смесей. 2. Вулканизат теряет способность растворяться даже в термодинамически “хороших” растворителях: он лишь ограниченно набухает в них. 3. Резко повышается прочность при растяжении: резиновая смесь на основе НК (после обработки на вальцах) имеет прочность при растяжении 1 – 1, 5 МПа, после вулканизации до 35 МПа. Однако прочность в зависимости от степени вулканизации изменяется экстремально (рис. ). 4. Повышается твердость материала и улучшаются его динамические свойства (при многократных циклических деформациях). 5. Повышается стойкость к старению. 6. Уменьшается влаго- и газопроницаемость, т. к. сшивание макромолекул уменьшает диффузию газов и паров. Рис. Зависимость прочности вулканизатов при одноосном растяжении от степени вулканизации
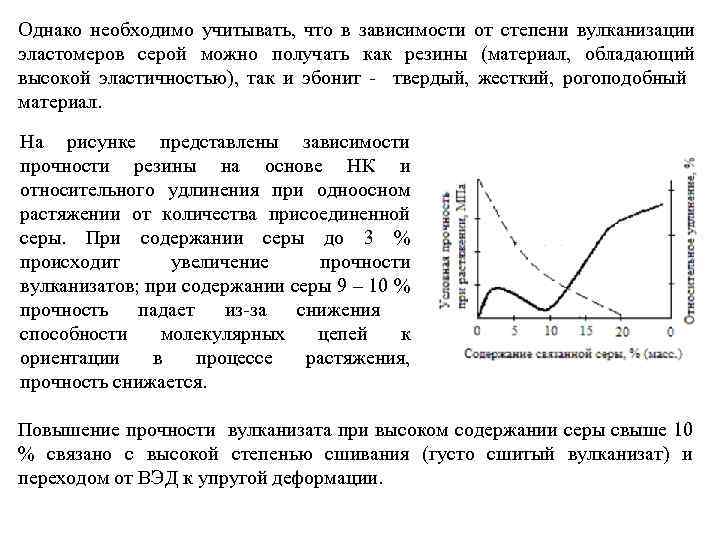 Однако необходимо учитывать, что в зависимости от степени вулканизации эластомеров серой можно получать как резины (материал, обладающий высокой эластичностью), так и эбонит - твердый, жесткий, рогоподобный материал. На рисунке представлены зависимости прочности резины на основе НК и относительного удлинения при одноосном растяжении от количества присоединенной серы. При содержании серы до 3 % происходит увеличение прочности вулканизатов; при содержании серы 9 – 10 % прочность падает из-за снижения способности молекулярных цепей к ориентации в процессе растяжения, прочность снижается. Повышение прочности вулканизата при высоком содержании серы свыше 10 % связано с высокой степенью сшивания (густо сшитый вулканизат) и переходом от ВЭД к упругой деформации.
Однако необходимо учитывать, что в зависимости от степени вулканизации эластомеров серой можно получать как резины (материал, обладающий высокой эластичностью), так и эбонит - твердый, жесткий, рогоподобный материал. На рисунке представлены зависимости прочности резины на основе НК и относительного удлинения при одноосном растяжении от количества присоединенной серы. При содержании серы до 3 % происходит увеличение прочности вулканизатов; при содержании серы 9 – 10 % прочность падает из-за снижения способности молекулярных цепей к ориентации в процессе растяжения, прочность снижается. Повышение прочности вулканизата при высоком содержании серы свыше 10 % связано с высокой степенью сшивания (густо сшитый вулканизат) и переходом от ВЭД к упругой деформации.
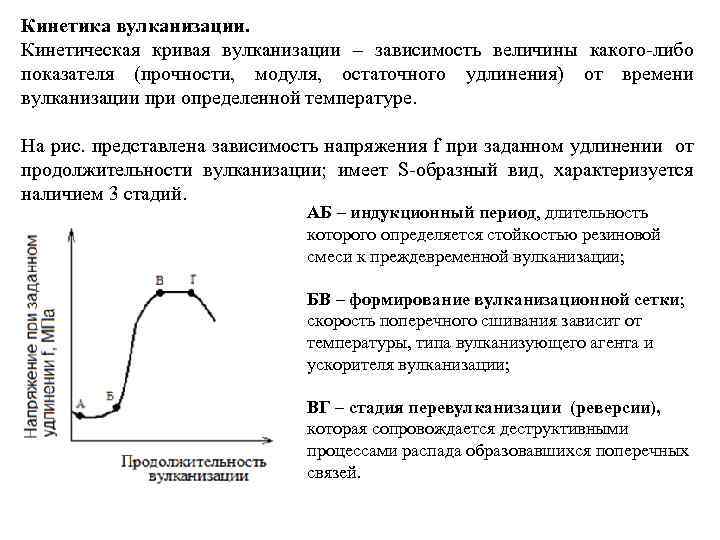 Кинетика вулканизации. Кинетическая кривая вулканизации – зависимость величины какого-либо показателя (прочности, модуля, остаточного удлинения) от времени вулканизации при определенной температуре. На рис. представлена зависимость напряжения f при заданном удлинении от продолжительности вулканизации; имеет S-образный вид, характеризуется наличием 3 стадий. АБ – индукционный период, длительность которого определяется стойкостью резиновой смеси к преждевременной вулканизации; БВ – формирование вулканизационной сетки; скорость поперечного сшивания зависит от температуры, типа вулканизующего агента и ускорителя вулканизации; ВГ – стадия перевулканизации (реверсии), которая сопровождается деструктивными процессами распада образовавшихся поперечных связей.
Кинетика вулканизации. Кинетическая кривая вулканизации – зависимость величины какого-либо показателя (прочности, модуля, остаточного удлинения) от времени вулканизации при определенной температуре. На рис. представлена зависимость напряжения f при заданном удлинении от продолжительности вулканизации; имеет S-образный вид, характеризуется наличием 3 стадий. АБ – индукционный период, длительность которого определяется стойкостью резиновой смеси к преждевременной вулканизации; БВ – формирование вулканизационной сетки; скорость поперечного сшивания зависит от температуры, типа вулканизующего агента и ускорителя вулканизации; ВГ – стадия перевулканизации (реверсии), которая сопровождается деструктивными процессами распада образовавшихся поперечных связей.
 Подвулканизация (или преждевременная вулканизация, скорчинг) – необратимое изменение свойств резиновой смеси при изготовлении, переработке и хранении (т. е. на стадиях, предшествующих вулканизации), сопровождается повышением вязкости и снижением перерабатываемости. С технологической точки зрения – нежелательный процесс. Длительность индукционного периода определяется длительностью нахождения резиновой смеси в вязкотекучем состоянии от начала нагрева резиновой смеси до момента, когда скорость вулканизации становится заметной. На участке БВ (главный период вулканизации) интенсивно образуются поперечные связи и, кроме того, происходит созревание вулканизационной сетки, суть которого заключается в перегруппировке полисульфидных связей в моно- и дисульфидные (при серной вулканизации). Завершению процесса формирования вулканизационной сетки соответствует оптимум вулканизации (точка В).
Подвулканизация (или преждевременная вулканизация, скорчинг) – необратимое изменение свойств резиновой смеси при изготовлении, переработке и хранении (т. е. на стадиях, предшествующих вулканизации), сопровождается повышением вязкости и снижением перерабатываемости. С технологической точки зрения – нежелательный процесс. Длительность индукционного периода определяется длительностью нахождения резиновой смеси в вязкотекучем состоянии от начала нагрева резиновой смеси до момента, когда скорость вулканизации становится заметной. На участке БВ (главный период вулканизации) интенсивно образуются поперечные связи и, кроме того, происходит созревание вулканизационной сетки, суть которого заключается в перегруппировке полисульфидных связей в моно- и дисульфидные (при серной вулканизации). Завершению процесса формирования вулканизационной сетки соответствует оптимум вулканизации (точка В).
 Оптимум вулканизации - время вулканизации в течение которого получают вулканизаты с наилучшим комплексом свойств. Вулканизаты с меньшим временем вулканизации называются недовулканизованными, с большим – перевулканизованными. Плато вулканизации – это отрезок времени (ВГ), в течение которого значения измеряемых параметров близки к оптимальным и меняются относительно мало. В соответствии с этим различают широкое и узкое плато вулканизации. С технологической точки зрения предпочтительно широкое плато вулканизации. Реверсия обусловлена наложением двух процессов: образования поперечных связей и реакций деструкции (распада поперечных связей). С технической точки зрения реверсия – нежелательный процесс, резины характеризуются меньшей прочностью, имеют низкое сопротивление старению.
Оптимум вулканизации - время вулканизации в течение которого получают вулканизаты с наилучшим комплексом свойств. Вулканизаты с меньшим временем вулканизации называются недовулканизованными, с большим – перевулканизованными. Плато вулканизации – это отрезок времени (ВГ), в течение которого значения измеряемых параметров близки к оптимальным и меняются относительно мало. В соответствии с этим различают широкое и узкое плато вулканизации. С технологической точки зрения предпочтительно широкое плато вулканизации. Реверсия обусловлена наложением двух процессов: образования поперечных связей и реакций деструкции (распада поперечных связей). С технической точки зрения реверсия – нежелательный процесс, резины характеризуются меньшей прочностью, имеют низкое сопротивление старению.
 Методы определения скорости вулканизации. Скорость вулканизации определяется: - физическими; - химическими методами. Химические методы позволяют определить расход агента вулканизации в образцах вулканизатов с различным временем вулканизации, например определение содержания свободной и связанной серы. К физическим относится метод определения количества поеперечных связей методом равновесного набухания, при этом исследуются вулканизаты с разным временем вулканизации. Кинетическую кривую вулканизации с использованием одного образца, возможно, получить с помощью реометров. В этом методе в образец резиновой смеси запрессовывается ротор, который, находясь при повышенной температуре периодически поворачивается на небольшой угол. По мере вулканизации возрастает упругость смеси и увеличивается усилие, необходимое для поворота ротора, что позволяет оценить изменение модуля сдвига в ходе вулканизации. Полученные с помощью различных методов кинетические кривые используют для расчета таких параметров, как скорость вулканизации, константа скорости, температурный коэффициент и энергия активации процесса в соответствии с уравнениями формальной кинетики химических реакций.
Методы определения скорости вулканизации. Скорость вулканизации определяется: - физическими; - химическими методами. Химические методы позволяют определить расход агента вулканизации в образцах вулканизатов с различным временем вулканизации, например определение содержания свободной и связанной серы. К физическим относится метод определения количества поеперечных связей методом равновесного набухания, при этом исследуются вулканизаты с разным временем вулканизации. Кинетическую кривую вулканизации с использованием одного образца, возможно, получить с помощью реометров. В этом методе в образец резиновой смеси запрессовывается ротор, который, находясь при повышенной температуре периодически поворачивается на небольшой угол. По мере вулканизации возрастает упругость смеси и увеличивается усилие, необходимое для поворота ротора, что позволяет оценить изменение модуля сдвига в ходе вулканизации. Полученные с помощью различных методов кинетические кривые используют для расчета таких параметров, как скорость вулканизации, константа скорости, температурный коэффициент и энергия активации процесса в соответствии с уравнениями формальной кинетики химических реакций.
 Перекисная вулканизация применяется для получения резин с повышенной теплостойкостью из таких каучуков как СКН, СКЭП, СКИ, полисилоксановые каучуки и т. д. Для вулканизации используются органические перекиси и гидроперекиси, особенностью строения которых является наличие –О-О-, которая легко распадается гомолитически. Отдельные представители: Основные требования, предъявляемые к перекисям: - нетоксичность; - нелетучесть при температурах приготовления резиновых смесей; - хорошая совместимость с каучуком (для равномерного распределения в объеме резиновой смеси) ; - высокая скорость разложения на свободные радикалы при температуре вулканизации (но не при температурах других технологических стадий, иначе это приведет к преждевременной вулканизации); - высокая эффективность сшивания.
Перекисная вулканизация применяется для получения резин с повышенной теплостойкостью из таких каучуков как СКН, СКЭП, СКИ, полисилоксановые каучуки и т. д. Для вулканизации используются органические перекиси и гидроперекиси, особенностью строения которых является наличие –О-О-, которая легко распадается гомолитически. Отдельные представители: Основные требования, предъявляемые к перекисям: - нетоксичность; - нелетучесть при температурах приготовления резиновых смесей; - хорошая совместимость с каучуком (для равномерного распределения в объеме резиновой смеси) ; - высокая скорость разложения на свободные радикалы при температуре вулканизации (но не при температурах других технологических стадий, иначе это приведет к преждевременной вулканизации); - высокая эффективность сшивания.
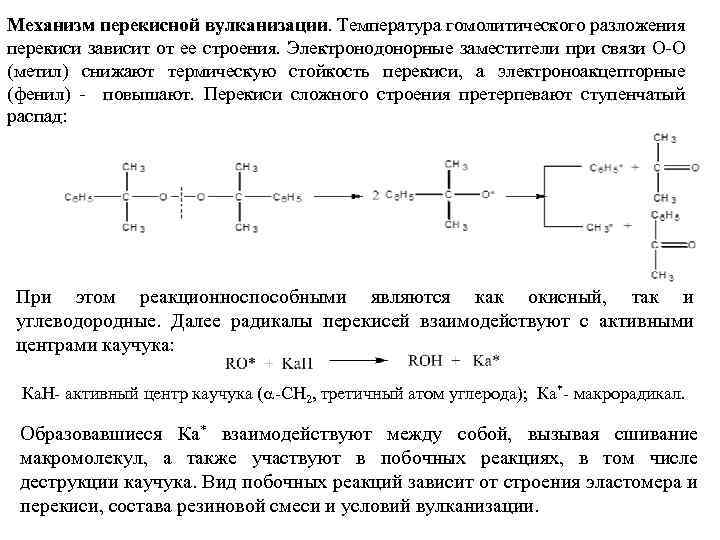 Механизм перекисной вулканизации. Температура гомолитического разложения перекиси зависит от ее строения. Электронодонорные заместители при связи О-О (метил) снижают термическую стойкость перекиси, а электроноакцепторные (фенил) - повышают. Перекиси сложного строения претерпевают ступенчатый распад: При этом реакционноспособными являются как окисный, так и углеводородные. Далее радикалы перекисей взаимодействуют с активными центрами каучука: Ка. Н- активный центр каучука ( -СН 2, третичный атом углерода); Ка*- макрорадикал. Образовавшиеся Ка* взаимодействуют между собой, вызывая сшивание макромолекул, а также участвуют в побочных реакциях, в том числе деструкции каучука. Вид побочных реакций зависит от строения эластомера и перекиси, состава резиновой смеси и условий вулканизации.
Механизм перекисной вулканизации. Температура гомолитического разложения перекиси зависит от ее строения. Электронодонорные заместители при связи О-О (метил) снижают термическую стойкость перекиси, а электроноакцепторные (фенил) - повышают. Перекиси сложного строения претерпевают ступенчатый распад: При этом реакционноспособными являются как окисный, так и углеводородные. Далее радикалы перекисей взаимодействуют с активными центрами каучука: Ка. Н- активный центр каучука ( -СН 2, третичный атом углерода); Ка*- макрорадикал. Образовавшиеся Ка* взаимодействуют между собой, вызывая сшивание макромолекул, а также участвуют в побочных реакциях, в том числе деструкции каучука. Вид побочных реакций зависит от строения эластомера и перекиси, состава резиновой смеси и условий вулканизации.
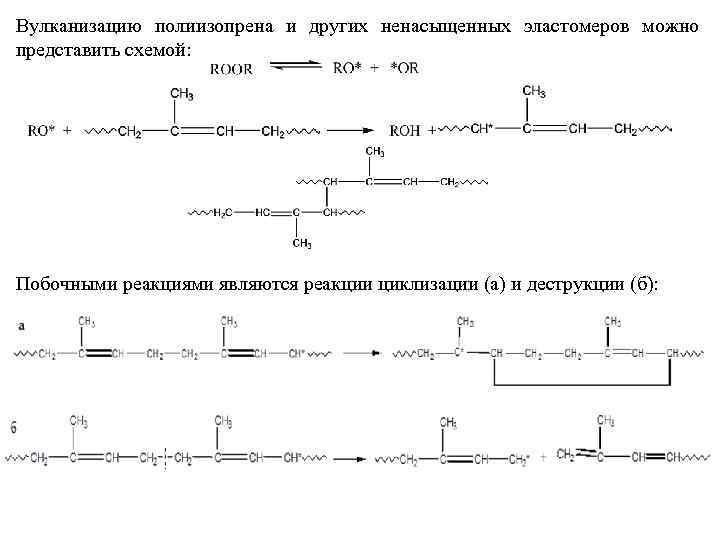 Вулканизацию полиизопрена и других ненасыщенных эластомеров можно представить схемой: Побочными реакциями являются реакции циклизации (а) и деструкции (б):
Вулканизацию полиизопрена и других ненасыщенных эластомеров можно представить схемой: Побочными реакциями являются реакции циклизации (а) и деструкции (б):
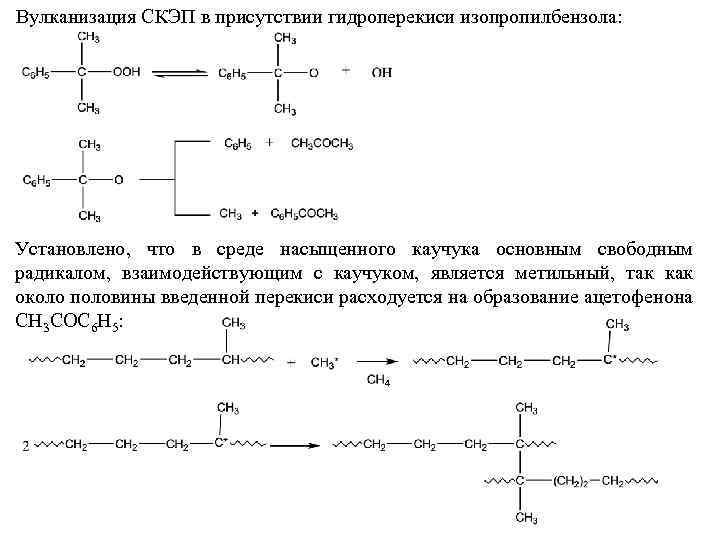 Вулканизация СКЭП в присутствии гидроперекиси изопропилбензола: Установлено, что в среде насыщенного каучука основным свободным радикалом, взаимодействующим с каучуком, является метильный, так как около половины введенной перекиси расходуется на образование ацетофенона СН 3 СОС 6 Н 5:
Вулканизация СКЭП в присутствии гидроперекиси изопропилбензола: Установлено, что в среде насыщенного каучука основным свободным радикалом, взаимодействующим с каучуком, является метильный, так как около половины введенной перекиси расходуется на образование ацетофенона СН 3 СОС 6 Н 5:
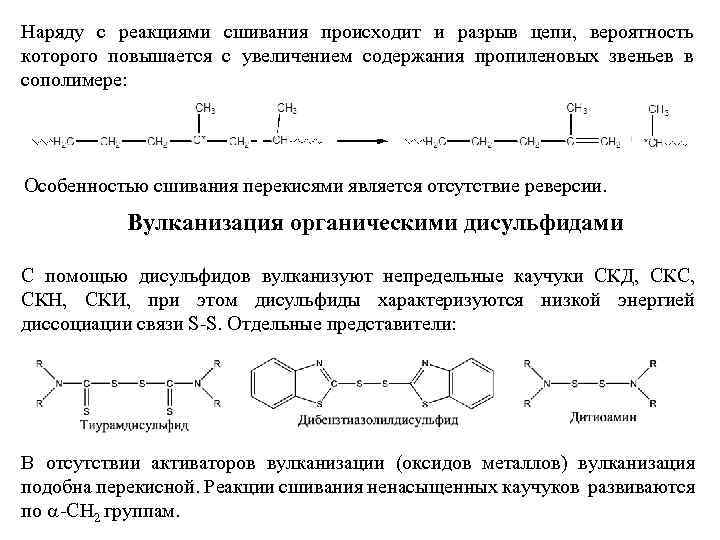 Наряду с реакциями сшивания происходит и разрыв цепи, вероятность которого повышается с увеличением содержания пропиленовых звеньев в сополимере: Особенностью сшивания перекисями является отсутствие реверсии. Вулканизация органическими дисульфидами С помощью дисульфидов вулканизуют непредельные каучуки СКД, СКС, СКН, СКИ, при этом дисульфиды характеризуются низкой энергией диссоциации связи S-S. Отдельные представители: В отсутствии активаторов вулканизации (оксидов металлов) вулканизация подобна перекисной. Реакции сшивания ненасыщенных каучуков развиваются по -СН 2 группам.
Наряду с реакциями сшивания происходит и разрыв цепи, вероятность которого повышается с увеличением содержания пропиленовых звеньев в сополимере: Особенностью сшивания перекисями является отсутствие реверсии. Вулканизация органическими дисульфидами С помощью дисульфидов вулканизуют непредельные каучуки СКД, СКС, СКН, СКИ, при этом дисульфиды характеризуются низкой энергией диссоциации связи S-S. Отдельные представители: В отсутствии активаторов вулканизации (оксидов металлов) вулканизация подобна перекисной. Реакции сшивания ненасыщенных каучуков развиваются по -СН 2 группам.
 Механизм вулканизации в общем виде: RSSR ® 2 RS* (распад при температуре вулканизации) Ka. H + RS* ® RSH + Ka* 2 Ka* ® Ka-Ka (С-С связь) Связей С-С образуется мало, т. к. отличительной чертой вулканизации дисульфидами является активное взаимодействие радикалов RS* и непрореагировавших молекул дисульфида RSSR с макрорадикалами, приводящее к их дезактивации (образованию неактивных продуктов присоединения): Ка* + RS* ® Ka-S-R Ka* + RSSR ® Ka. SR + RS* Для подавления реакций дезактивации и получения сшитых продуктов в резиновые смеси вводится более 5 масс. ч. дисульфида, где наряду с неактивными продуктами присоединения (Ка. SR) образуются активные типа Kа. SSR, которые впоследствии приводят к образованию моносульфидных связей: RS* + R-SSR ® RSR + RSS* Ka* + RSS* ® Ka. SSR активный продукт присоединения Ka. H Ka. S-SR ® Ka. S* + *SR ® Ka. S* + Ka* ® Ka-S-Ka моносульфидная связь - RSH
Механизм вулканизации в общем виде: RSSR ® 2 RS* (распад при температуре вулканизации) Ka. H + RS* ® RSH + Ka* 2 Ka* ® Ka-Ka (С-С связь) Связей С-С образуется мало, т. к. отличительной чертой вулканизации дисульфидами является активное взаимодействие радикалов RS* и непрореагировавших молекул дисульфида RSSR с макрорадикалами, приводящее к их дезактивации (образованию неактивных продуктов присоединения): Ка* + RS* ® Ka-S-R Ka* + RSSR ® Ka. SR + RS* Для подавления реакций дезактивации и получения сшитых продуктов в резиновые смеси вводится более 5 масс. ч. дисульфида, где наряду с неактивными продуктами присоединения (Ка. SR) образуются активные типа Kа. SSR, которые впоследствии приводят к образованию моносульфидных связей: RS* + R-SSR ® RSR + RSS* Ka* + RSS* ® Ka. SSR активный продукт присоединения Ka. H Ka. S-SR ® Ka. S* + *SR ® Ka. S* + Ka* ® Ka-S-Ka моносульфидная связь - RSH
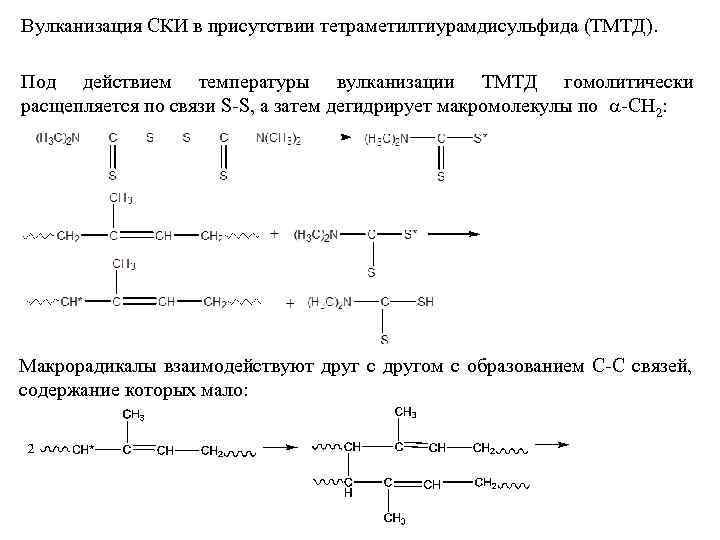 Вулканизация СКИ в присутствии тетраметилтиурамдисульфида (ТМТД). Под действием температуры вулканизации ТМТД гомолитически расщепляется по связи S-S, а затем дегидрирует макромолекулы по -СН 2: Макрорадикалы взаимодействуют друг с другом с образованием С-С связей, содержание которых мало:
Вулканизация СКИ в присутствии тетраметилтиурамдисульфида (ТМТД). Под действием температуры вулканизации ТМТД гомолитически расщепляется по связи S-S, а затем дегидрирует макромолекулы по -СН 2: Макрорадикалы взаимодействуют друг с другом с образованием С-С связей, содержание которых мало:
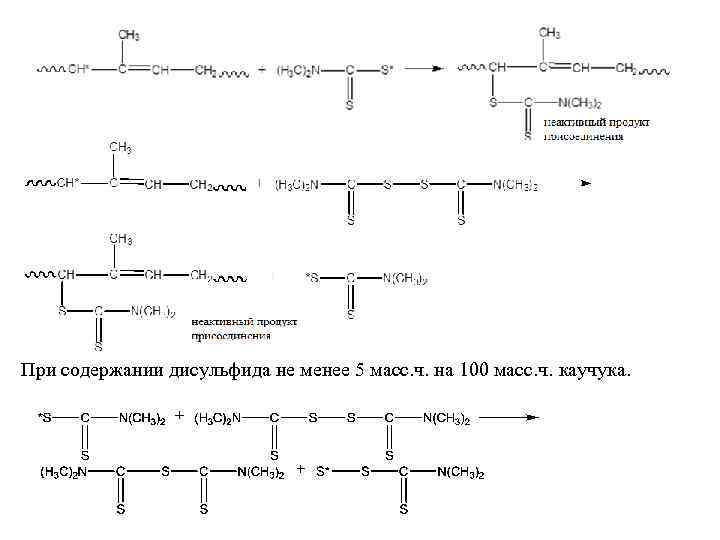 При содержании дисульфида не менее 5 масс. ч. на 100 масс. ч. каучука.
При содержании дисульфида не менее 5 масс. ч. на 100 масс. ч. каучука.
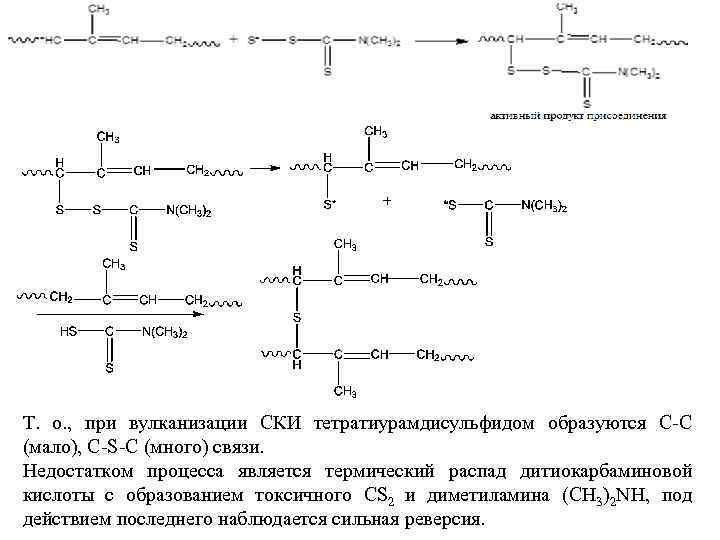 Т. о. , при вулканизации СКИ тетратиурамдисульфидом образуются С-С (мало), С-S-С (много) связи. Недостатком процесса является термический распад дитиокарбаминовой кислоты с образованием токсичного СS 2 и диметиламина (СН 3)2 NH, под действием последнего наблюдается сильная реверсия.
Т. о. , при вулканизации СКИ тетратиурамдисульфидом образуются С-С (мало), С-S-С (много) связи. Недостатком процесса является термический распад дитиокарбаминовой кислоты с образованием токсичного СS 2 и диметиламина (СН 3)2 NH, под действием последнего наблюдается сильная реверсия.
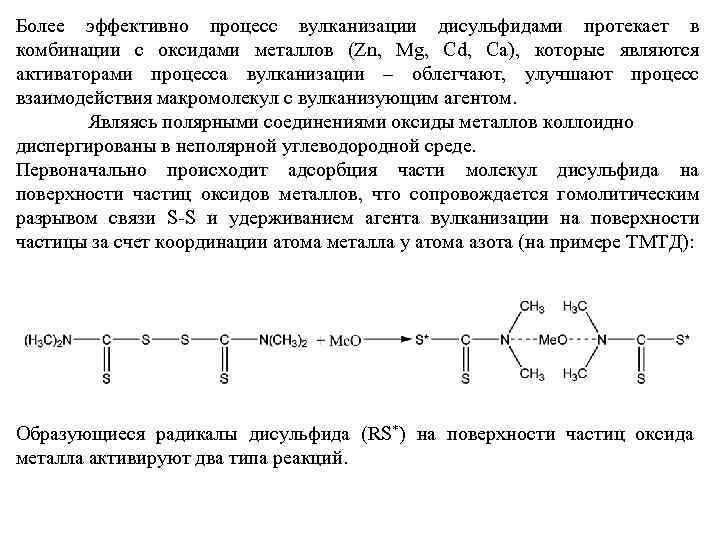 Более эффективно процесс вулканизации дисульфидами протекает в комбинации с оксидами металлов (Zn, Mg, Cd, Ca), которые являются активаторами процесса вулканизации – облегчают, улучшают процесс взаимодействия макромолекул с вулканизующим агентом. Являясь полярными соединениями оксиды металлов коллоидно диспергированы в неполярной углеводородной среде. Первоначально происходит адсорбция части молекул дисульфида на поверхности частиц оксидов металлов, что сопровождается гомолитическим разрывом связи S-S и удерживанием агента вулканизации на поверхности частицы за счет координации атома металла у атома азота (на примере ТМТД): Образующиеся радикалы дисульфида (RS*) на поверхности частиц оксида металла активируют два типа реакций.
Более эффективно процесс вулканизации дисульфидами протекает в комбинации с оксидами металлов (Zn, Mg, Cd, Ca), которые являются активаторами процесса вулканизации – облегчают, улучшают процесс взаимодействия макромолекул с вулканизующим агентом. Являясь полярными соединениями оксиды металлов коллоидно диспергированы в неполярной углеводородной среде. Первоначально происходит адсорбция части молекул дисульфида на поверхности частиц оксидов металлов, что сопровождается гомолитическим разрывом связи S-S и удерживанием агента вулканизации на поверхности частицы за счет координации атома металла у атома азота (на примере ТМТД): Образующиеся радикалы дисульфида (RS*) на поверхности частиц оксида металла активируют два типа реакций.
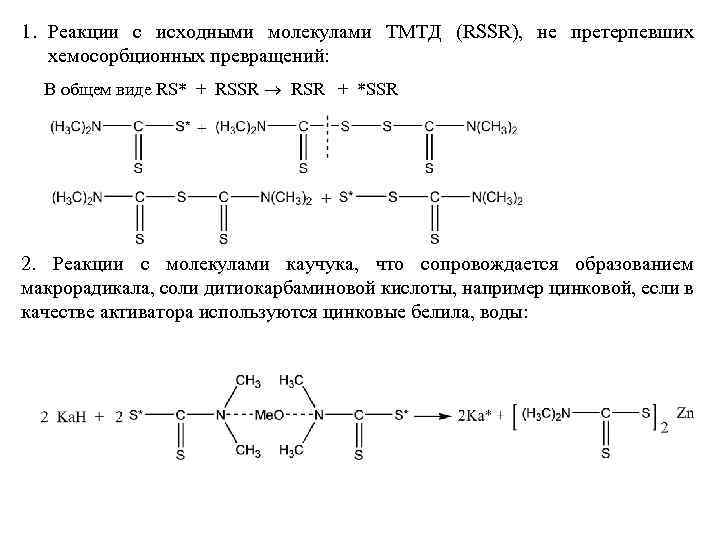 1. Реакции с исходными молекулами ТМТД (RSSR), не претерпевших хемосорбционных превращений: В общем виде RS* + RSSR ® RSR + *SSR 2. Реакции с молекулами каучука, что сопровождается образованием макрорадикала, соли дитиокарбаминовой кислоты, например цинковой, если в качестве активатора используются цинковые белила, воды:
1. Реакции с исходными молекулами ТМТД (RSSR), не претерпевших хемосорбционных превращений: В общем виде RS* + RSSR ® RSR + *SSR 2. Реакции с молекулами каучука, что сопровождается образованием макрорадикала, соли дитиокарбаминовой кислоты, например цинковой, если в качестве активатора используются цинковые белила, воды:
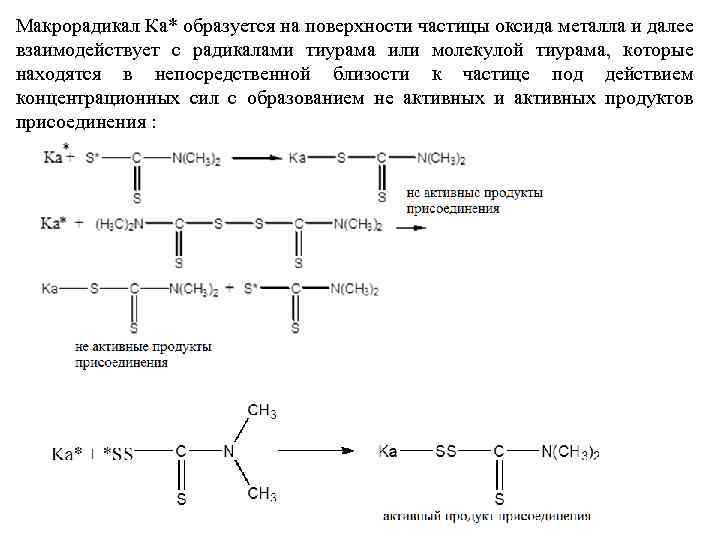 Макрорадикал Ка* образуется на поверхности частицы оксида металла и далее взаимодействует с радикалами тиурама или молекулой тиурама, которые находятся в непосредственной близости к частице под действием концентрационных сил с образованием не активных и активных продуктов присоединения :
Макрорадикал Ка* образуется на поверхности частицы оксида металла и далее взаимодействует с радикалами тиурама или молекулой тиурама, которые находятся в непосредственной близости к частице под действием концентрационных сил с образованием не активных и активных продуктов присоединения :
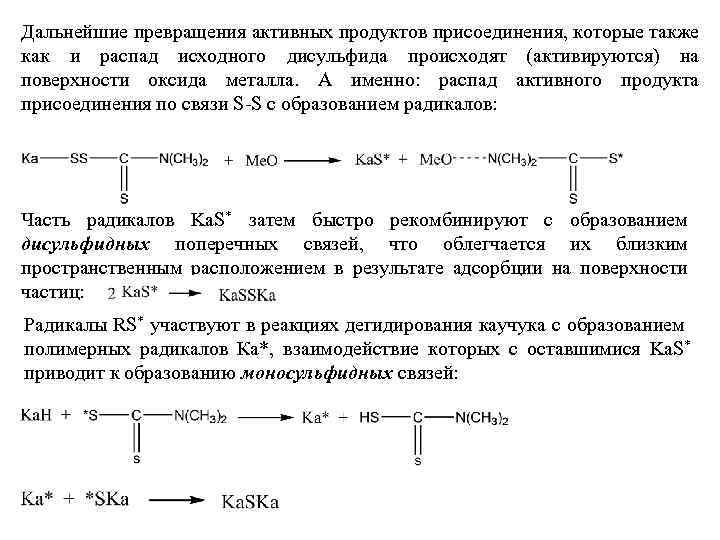 Дальнейшие превращения активных продуктов присоединения, которые также как и распад исходного дисульфида происходят (активируются) на поверхности оксида металла. А именно: распад активного продукта присоединения по связи S-S с образованием радикалов: Часть радикалов Ka. S* затем быстро рекомбинируют с образованием дисульфидных поперечных связей, что облегчается их близким пространственным расположением в результате адсорбции на поверхности частиц: Радикалы RS* участвуют в реакциях дегидирования каучука с образованием полимерных радикалов Ка*, взаимодействие которых с оставшимися Ka. S* приводит к образованию моносульфидных связей:
Дальнейшие превращения активных продуктов присоединения, которые также как и распад исходного дисульфида происходят (активируются) на поверхности оксида металла. А именно: распад активного продукта присоединения по связи S-S с образованием радикалов: Часть радикалов Ka. S* затем быстро рекомбинируют с образованием дисульфидных поперечных связей, что облегчается их близким пространственным расположением в результате адсорбции на поверхности частиц: Радикалы RS* участвуют в реакциях дегидирования каучука с образованием полимерных радикалов Ка*, взаимодействие которых с оставшимися Ka. S* приводит к образованию моносульфидных связей:
 Т. о. в присутствии активаторов вулканизации образуются моно- и дисульфидные поперечные связи. Сшивание происходит на поверхности частиц, затем сшитые участки под влиянием теплового движения десорбируются и перераспределяются в объем каучука. Преимуществом является и то, что вместо дитиокарбаминовой кислоты образуется дитиокарбомат цинка, являющийся эффективным антиоксидантом: Серная вулканизация Применяется для получения резиновых изделий (автопокрышки и камеры, РТИ, резиновая обувь) из ненасыщенных каучуков. Вулканизующая группа состоит из серы, ускорителя (или комплекса ускорителей), активатора. Ускоритель – это вещество, с помощью которого можно влиять на кинетику вулканизации (скорость, оптимум и плато вулканизации), характер вулканизационной сетки и, соответственно, свойства вулканизатов.
Т. о. в присутствии активаторов вулканизации образуются моно- и дисульфидные поперечные связи. Сшивание происходит на поверхности частиц, затем сшитые участки под влиянием теплового движения десорбируются и перераспределяются в объем каучука. Преимуществом является и то, что вместо дитиокарбаминовой кислоты образуется дитиокарбомат цинка, являющийся эффективным антиоксидантом: Серная вулканизация Применяется для получения резиновых изделий (автопокрышки и камеры, РТИ, резиновая обувь) из ненасыщенных каучуков. Вулканизующая группа состоит из серы, ускорителя (или комплекса ускорителей), активатора. Ускоритель – это вещество, с помощью которого можно влиять на кинетику вулканизации (скорость, оптимум и плато вулканизации), характер вулканизационной сетки и, соответственно, свойства вулканизатов.


