lekt_3_B_Al[1].ppt
- Количество слайдов: 30

Химия элементов. Лекция 3 Общая характеристика элементов IIIA -группы. Бор. Алюминий
![Элементы IIIА-группы • Общая электронная формула: […] ns 2 (n – 1)d 10 np Элементы IIIА-группы • Общая электронная формула: […] ns 2 (n – 1)d 10 np](https://present5.com/presentation/54107950_159336321/image-2.jpg)
Элементы IIIА-группы • Общая электронная формула: […] ns 2 (n – 1)d 10 np 1 nd 0 ns 2 np 1 Валентные возможности: B 3, 4; Al, Ga, In, Tl 3 6 Степени окисления: 0, +III (Tl. III – с. ок-ль)
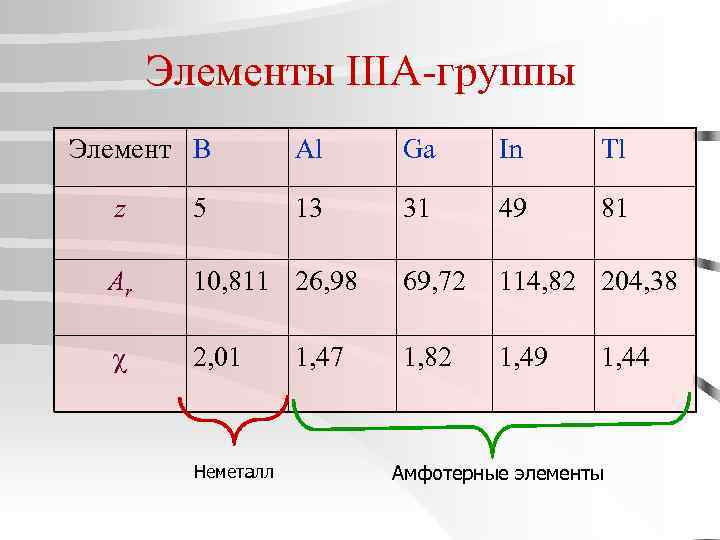
Элементы IIIA-группы Элемент B Al Ga In Tl 13 31 49 81 z 5 Ar 10, 811 26, 98 69, 72 114, 82 204, 38 2, 01 1, 82 1, 49 Неметалл 1, 47 1, 44 Амфотерные элементы
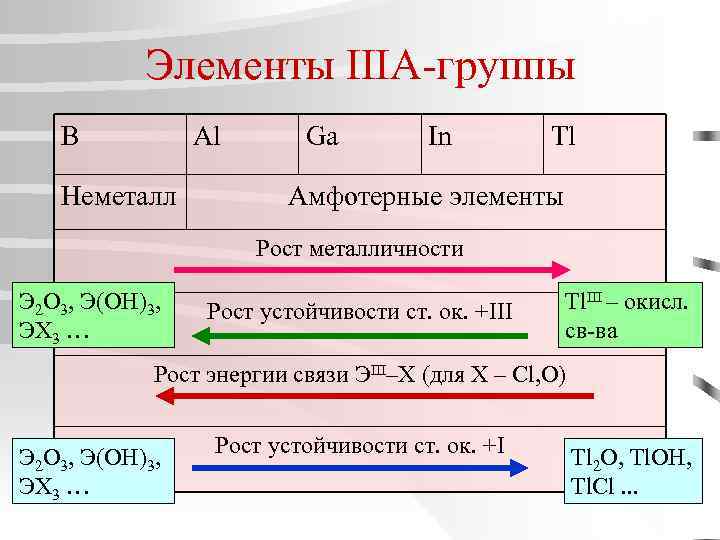
Элементы IIIA-группы B Al Неметалл Ga In Tl Амфотерные элементы Рост металличности Э 2 O 3, Э(OH)3, ЭХ 3 … Рост устойчивости ст. ок. +III Tl. III – окисл. св-ва Рост энергии связи ЭIII–X (для X – Cl, O) Э 2 O 3, Э(OH)3, ЭХ 3 … Рост устойчивости ст. ок. +I Tl 2 O, Tl. OH, Tl. Cl. . .
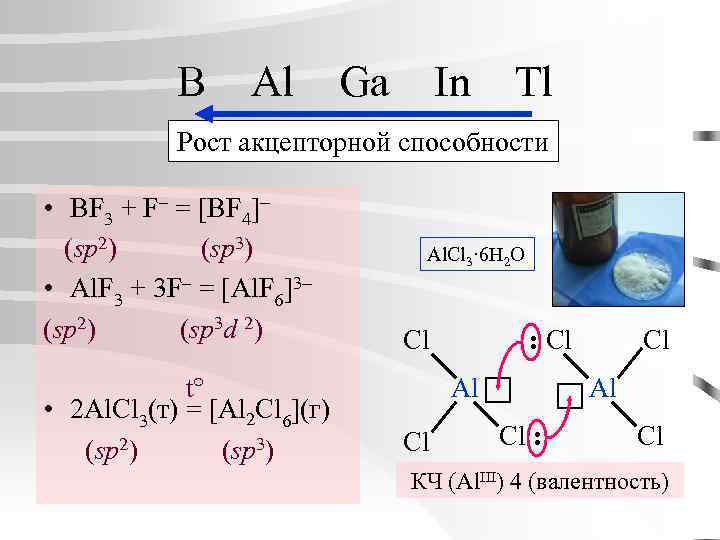
B Al Ga In Tl Рост акцепторной способности • BF 3 + F– = [BF 4] (sp 2) (sp 3) • Al. F 3 + 3 F– = [Al. F 6]3 (sp 2) (sp 3 d 2) t° • 2 Al. Cl 3(т) = [Al 2 Cl 6](г) (sp 2) (sp 3) Al. Cl 3· 6 H 2 O Cl : Cl Al Cl : Cl КЧ (Al. III) 4 (валентность)

Кислородные соединения Э 2 О 3 кислотный амфотерные B Al Ga In Tl Оксид алюминия кислотность увеличивается • Э 2 O 3(т) + 2 Na. OH (т) = 2 Na. ЭO 2(т) + H 2 O(г) (Э = B Tl, сплавление) • Э 2 O 3(т) + 6 H 3 O+(р) = 2 Э 3+(р) + 9 H 2 O (Э = Al Tl) Tl 2 O – основный оксид, Tl. OH – сильное основание
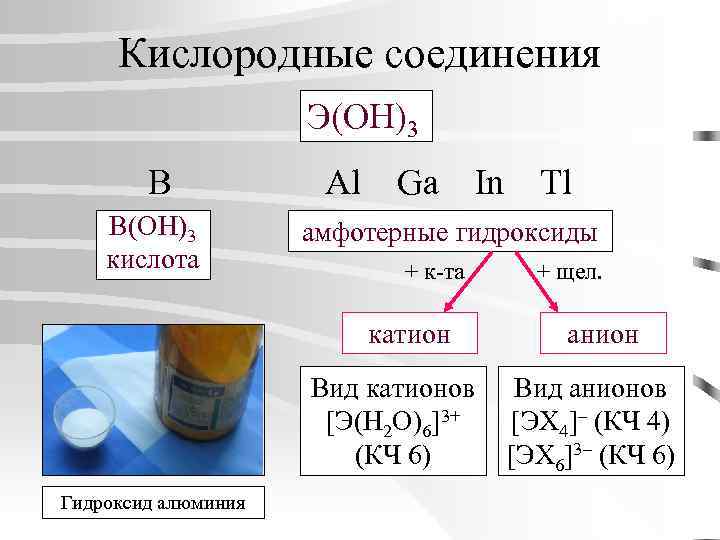
Кислородные соединения Э(OH)3 B Al Ga In Tl B(OH)3 кислота амфотерные гидроксиды + к-та катион + щел. анион Вид катионов Вид анионов [Э(H 2 O)6]3+ [ЭХ 4]– (КЧ 4) (КЧ 6) [ЭХ 6]3– (КЧ 6) Гидроксид алюминия
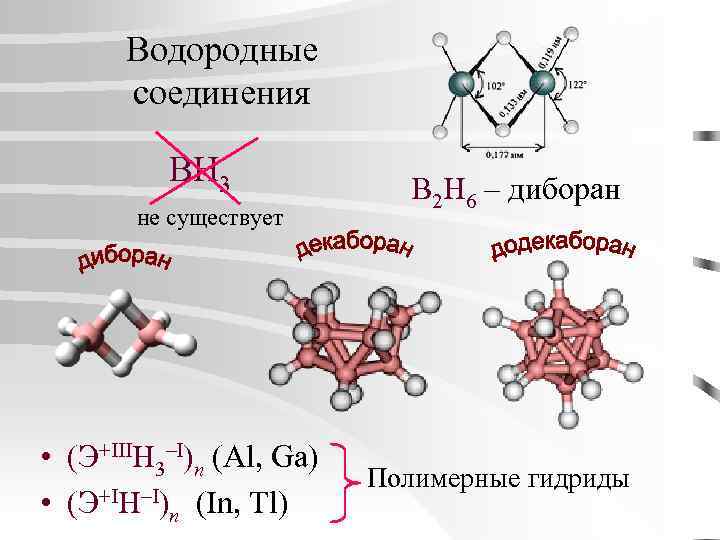
Водородные соединения BH 3 не существует B 2 H 6 – диборан • (Э+IIIН 3–I)n (Al, Ga) Полимерные гидриды • (Э+IН–I)n (In, Tl)
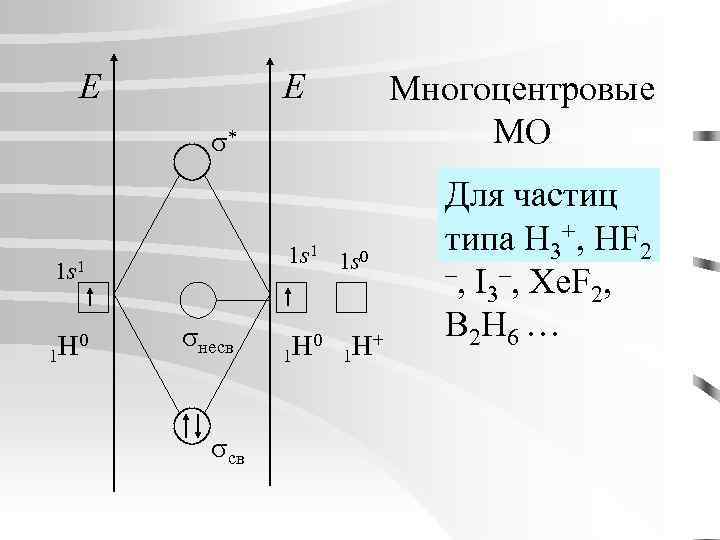
E E Многоцентровые МО * 1 s 1 1 s 0 1 s 1 H 0 1 несв H 0 1 H+ 1 Для частиц типа H 3+, HF 2 –, I –, Xe. F , 3 2 B 2 H 6 …
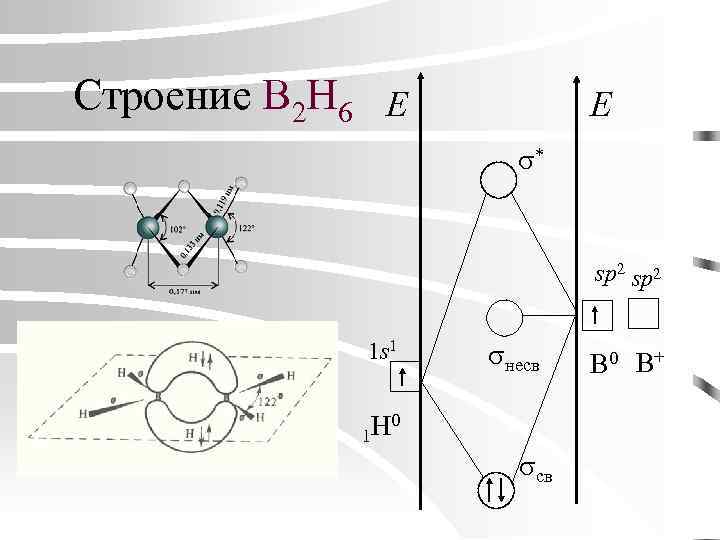
Строение B 2 H 6 E E * sp 2 1 s 1 несв H 0 1 св B 0 B+
![Гидридные комплексы ЭН 3 + H– = [ЭH 4] B Al Ga In Tl Гидридные комплексы ЭН 3 + H– = [ЭH 4] B Al Ga In Tl](https://present5.com/presentation/54107950_159336321/image-11.jpg)
Гидридные комплексы ЭН 3 + H– = [ЭH 4] B Al Ga In Tl Рост устойчивости комплексов • Na[BH 4] – тетрагидридоборат натрия • Li[Al. H 4] – тетрагидридоалюминат лития Восстановительные свойства • [Al. H 4] + 4 H 2 O = [Al(OH)4] + 4 H 2 • Li[Al. H 4] + RCHO = RCH 2 OH + Li. OH + Al(OH)3
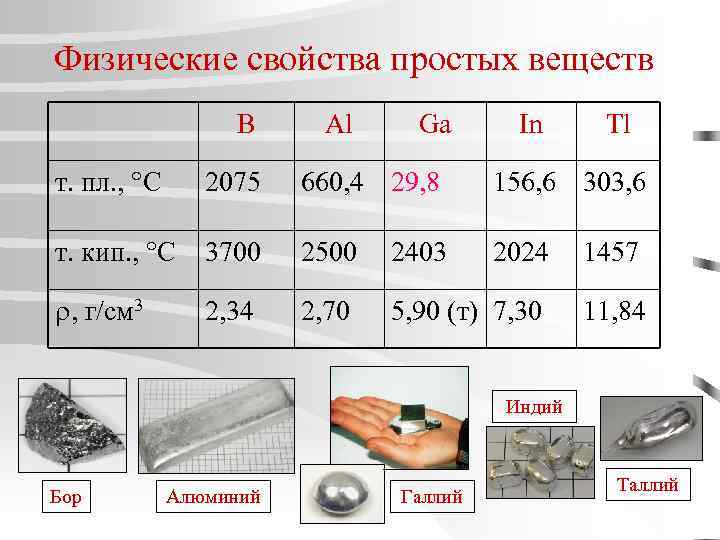
Физические свойства простых веществ B Al Ga In Tl т. пл. , С 2075 660, 4 29, 8 156, 6 303, 6 т. кип. , С 3700 2500 2403 2024 1457 , г/см 3 2, 34 2, 70 5, 90 (т) 7, 30 11, 84 Индий Бор Алюминий Галлий Таллий
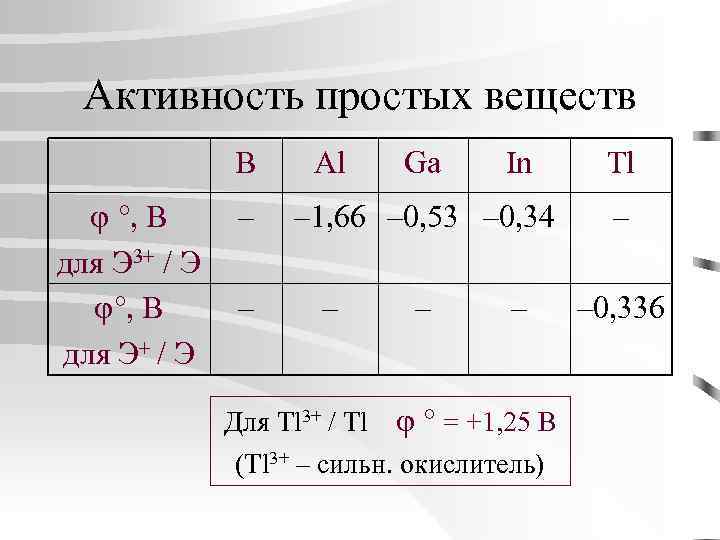
Активность простых веществ B , В для Э 3+ / Э , В для Э+ / Э – – Al Ga In – 1, 66 – 0, 53 – 0, 34 – – – Для Tl 3+ / Tl = +1, 25 В (Tl 3+ – сильн. окислитель) Tl – – 0, 336

Химические свойства простых веществ • B + 3 HNO 3 = B(OH)3 + 3 NO 2 • 4 B + 4 Na. OH(т) + 3 O 2 = 4 Na. BO 2 + 2 H 2 O (сплавление) • 2 Ga + 6 H 3 O+ + 6 H 2 O = = 2[Ga(H 2 O)6]3+ + 3 H 2 • 2 Ga + 2 OH + 6 H 2 O = = 2[Ga(OH)4] + 3 H 2
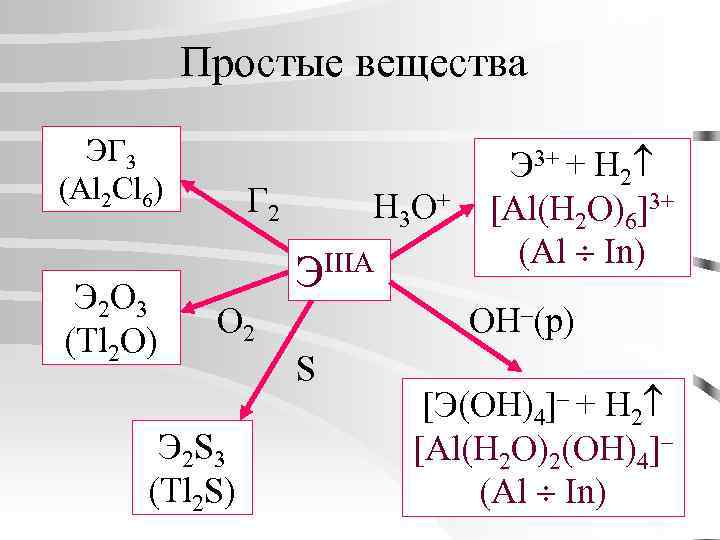
Простые вещества ЭГ 3 (Al 2 Cl 6) Э 2 О 3 (Tl 2 O) Г 2 H 3 O+ ЭIIIA O 2 Э 2 S 3 (Tl 2 S) Э 3+ + H 2 [Al(H 2 O)6]3+ (Al In) OH–(р) S [Э(OH)4]– + H 2 [Al(H 2 O)2(OH)4]– (Al In)

Распространение в природе. Минералы 3. Al 7, 57 % масс. 37. B 2· 10– 3 %. масс. 38. Ga Редкие 65. Tl рассеянные элементы 68. In Боксит Al: боксит Al. O(OH) каолин Al 4(Si 4 O 10)(OH)8 корунд Al 2 O 3 (рубин и сапфир) криолит Na 3[Al. F 6] алунит (K, Na)Al 3(SO 4)2(OH)6 полевые шпаты – ортоклаз K(Al. Si 3 O 8) нефелин K, Na(Al. Si. O 4) Нефелин Алунит Каолин Криолит

B: Корунд бура Na 2 B 4 O 7. 10 H 2 O кернит Na 2 B 4 O 7. 4 H 2 O борацит Mg 3(B 7 O 13)Cl сассолин B(OH)3 Сапфиры и рубины Кернит Бура (тинкал) Сассолин
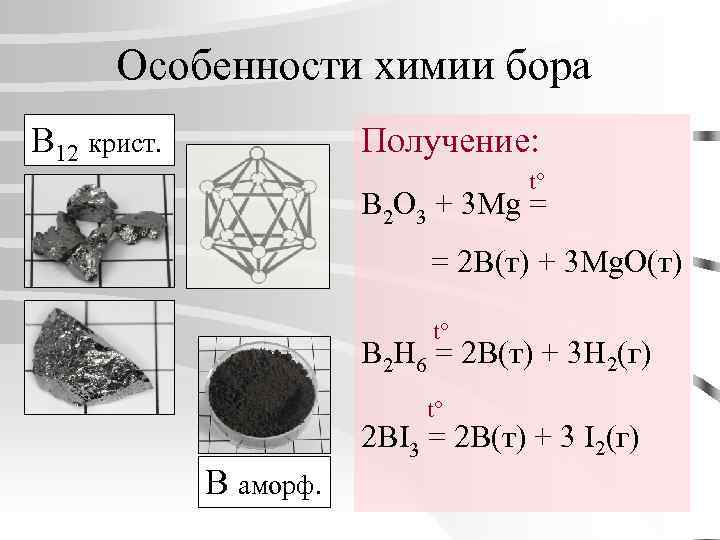
Особенности химии бора B 12 крист. Получение: t° B 2 O 3 + 3 Mg = = 2 B(т) + 3 Mg. O(т) t° B 2 H 6 = 2 B(т) + 3 H 2(г) t° 2 BI 3 = 2 B(т) + 3 I 2(г) B аморф.

Кислородные соединения бора • B 2 O 3 – кислотный оксид B 2 O 3 + 3 H 2 O = 2 B(OH)3 • Гидроксид бора B(OH)3 (борная кислота) I. Растворение и гидратация: B(OH)3(т) + H 2 O = [B(H 2 O)(OH)3](р) II. Протолиз [B(H 2 O)(OH)3] + H 2 O [B(OH)4] + H 3 O+; KK = 5, 75 · 10– 10
![Строение B(OH)3 и [B(H 2 O)(OH)3] OH OH B B HO OH sp 2 Строение B(OH)3 и [B(H 2 O)(OH)3] OH OH B B HO OH sp 2](https://present5.com/presentation/54107950_159336321/image-20.jpg)
Строение B(OH)3 и [B(H 2 O)(OH)3] OH OH B B HO OH sp 2 -гибр. HO OH : OH 2 sp 3 -гибр. t° B(OH)3 (HBO 2)n B 2 O 3 –H 2 O
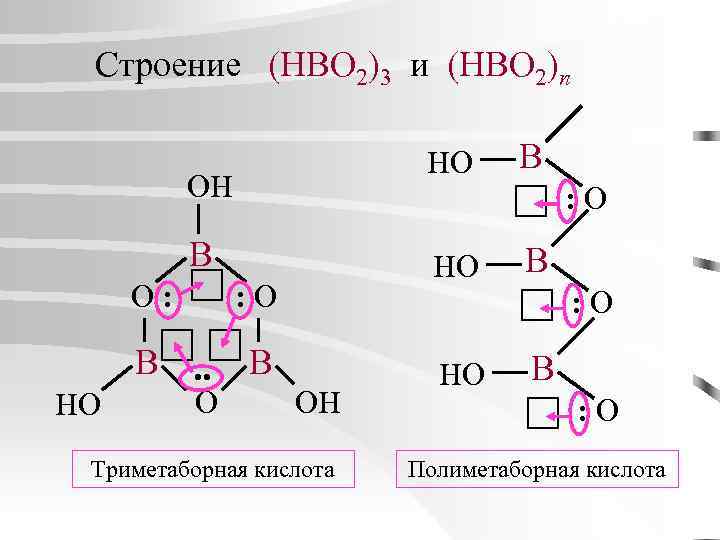
Строение (HBO 2)3 и (HBO 2)n HO OH : O B O : HO HO : O B. . O B B : O B OH Триметаборная кислота HO B : O Полиметаборная кислота
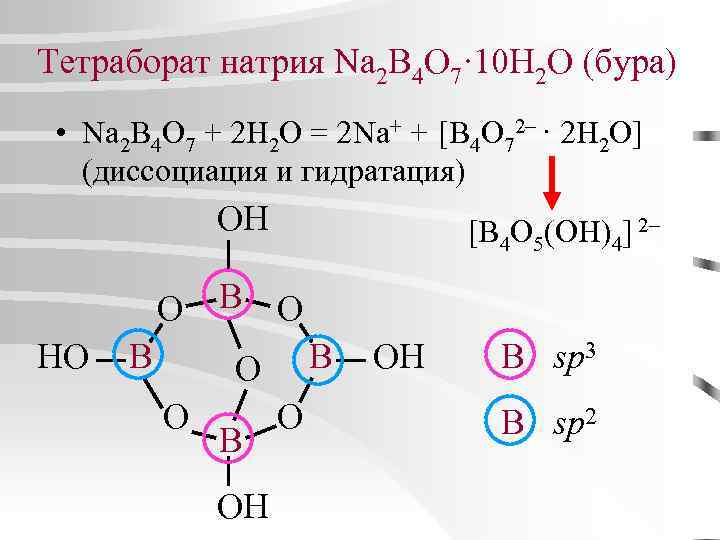
Тетраборат натрия Na 2 B 4 O 7· 10 H 2 O (бура) • Na 2 B 4 O 7 + 2 H 2 O = 2 Na+ + [B 4 O 72– · 2 H 2 O] (диссоциация и гидратация) OH [B 4 O 5(OH)4] 2 O B O HO B B O O B OH O OH B sp 3 B sp 2
![Гидролиз тетрабората натрия [B 4 O 5(OH)4] 2 + 2 H 2 O 4 Гидролиз тетрабората натрия [B 4 O 5(OH)4] 2 + 2 H 2 O 4](https://present5.com/presentation/54107950_159336321/image-23.jpg)
Гидролиз тетрабората натрия [B 4 O 5(OH)4] 2 + 2 H 2 O 4 B(OH)3 ·H 2 O + 2 OH– p. H > 7 B(OH)3 +Na. OH Na 3 BO 3 H 2 B 4 O 7 HBO 2 +HCl Na 2 B 4 O 7 Na. BO 2 (t) Na[B(OH)4]

Получение B(OH)3 • BCl 3 + 3 H 2 O = B(OH)3 + 3 HCl (лаб. ) • Na 2 B 4 O 7 + H 2 SO 4 + 5 H 2 O = = 4 B(OH)3 + Na 2 SO 4 (лаб. , пром. )

Обнаружение соединений бора Na 2 B 4 O 7 + 12 C 2 H 5 OH + 2 H 2 SO 4 = = 4 B(OC 2 H 5)3 + 7 H 2 O + 2 Na. HSO 4 2 B(OC 2 H 5)3 + 18 O 2 = B 2 O 3 + 15 H 2 O + 12 CO 2 Получение и горение борноэтилового эфира. Видео
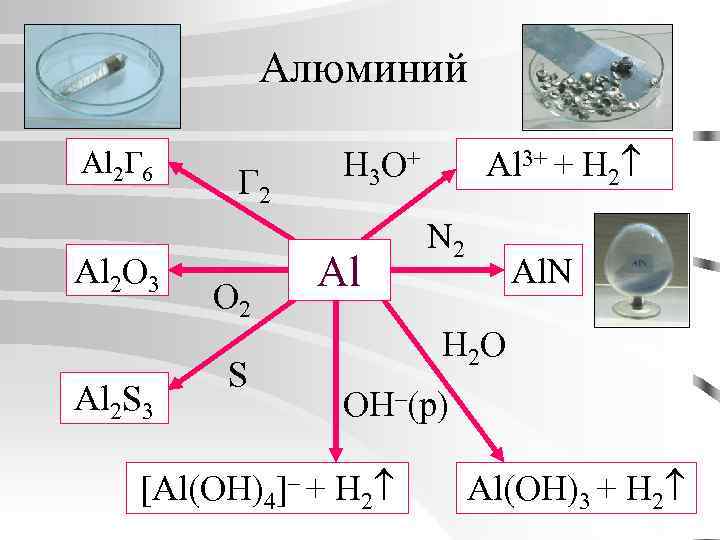
Алюминий Al 2 Г 6 Al 2 О 3 Al 2 S 3 Г 2 O 2 S Al 3+ + H 2 H 3 O+ Al N 2 Al. N H 2 O OH–(р) [Al(OH)4]– + H 2 Al(OH)3 + H 2

Окисление амальгамированного алюминия • Алюминиевая ложка, погруженная в раствор Hg(NO 3)2, покрывается амальгамой – сплавом алюминия и ртути. • Алюминий теряет защитную оксидную плёнку и окисляется, превращаясь в белые хлопья Al(OH)3. Термитная сварка Самолеты Изделия из алюминия в быту

• 2 Al + 6 H 3 O+ + 6 H 2 O = 2[Al(H 2 O)6]3+ + 3 H 2 Al 3+/Al = – 1, 70 B • 2 Al + 2 OH + 6 H 2 O = 2[Al(OH)4] + 3 H 2 [Al(OH)4]–/Al = – 2, 34 B • 2 Al + 6 H 2 O = 2 Al(OH)3 + 3 H 2 Al(OH)3 /Al = – 1, 54 B В щелочной среде восст. св-ва сильнее: • 8 Al + 30 HNO 3(оч. разб. ) = = 8 Al(NO 3)3 + 3 NH 4 NO 3 + 9 H 2 O • 8 Al + 18 H 2 O + 5 KOH + 3 KNO 3 = = 8 K[Al(OH)4] + 3 NH 3
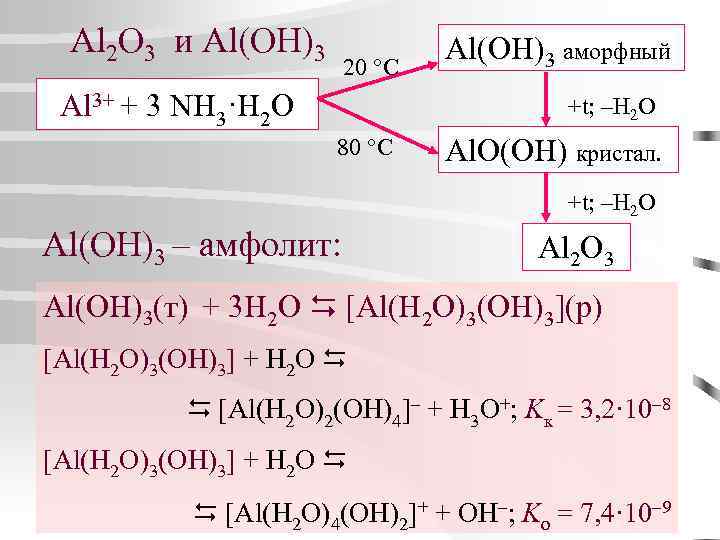
Al 2 O 3 и Al(OH)3 20 °C Al 3+ + 3 NH 3·H 2 O Al(OH)3 аморфный +t; –H 2 O 80 °C Al. O(OH) кристал. +t; –H 2 O Al(OH)3 – амфолит: Al 2 O 3 Al(OH)3(т) + 3 H 2 O [Al(H 2 O)3(OH)3](р) [Al(H 2 O)3(OH)3] + H 2 O [Al(H 2 O)2(OH)4]– + H 3 O+; Kк = 3, 2· 10– 8 [Al(H 2 O)3(OH)3] + H 2 O [Al(H 2 O)4(OH)2]+ + OH–; Kо = 7, 4· 10– 9

Формы существования Al. III в растворах р. Н < 4 (изб. к-ты): [Al(H 2 O)6]3+ sp 3 d 2 (октаэдр) р. Н > 4 (гидролиз): [Al(H 2 O)6]3+ + H 2 O [Al(H 2 O)5 OH]2+ + H 3 O+ Kк = 9, 55· 10– 5 р. Н > 7: [Al(H 2 O)2(OH)4 ] sp 3 d 2 (искаж. октаэдр) р. Н > 7 (изб. щелочи): [Al(OH)4 ] sp 3(тетраэдр)
lekt_3_B_Al[1].ppt