Лекция 1 Галогены.ppt
- Количество слайдов: 53
 Химия элементов Галогены
Химия элементов Галогены
 В 7 группу периодической системы подгруппу 7 А входят элементы F Cl Br J At Галоген происходит от греч. “галс”- соль и “ген”- образование, рост, т. е. “солеобразующий”.
В 7 группу периодической системы подгруппу 7 А входят элементы F Cl Br J At Галоген происходит от греч. “галс”- соль и “ген”- образование, рост, т. е. “солеобразующий”.
 Электронная конфигурация и структура атомов Х : F, Cl, Br, J, At ns 2 np 5 -7 е- на внешней оболочке - : F-, Cl-, Br-, J-, At- Х ns 2 np 6 -устойчивый октет
Электронная конфигурация и структура атомов Х : F, Cl, Br, J, At ns 2 np 5 -7 е- на внешней оболочке - : F-, Cl-, Br-, J-, At- Х ns 2 np 6 -устойчивый октет
 В свободном виде существуют в форме двухатомных молекул, формула . . Льюиса для них : Х: Х: , атомы . . соединены одинарной ковалентной связью: Cl 2 J 2 Br 2 F 2 At 2
В свободном виде существуют в форме двухатомных молекул, формула . . Льюиса для них : Х: Х: , атомы . . соединены одинарной ковалентной связью: Cl 2 J 2 Br 2 F 2 At 2
 Элементы были открыты: Хлор - К. Шееле 1774 г. Фтор - Б. Куртуа 1811 г. Бром - А. Болер 1826 г. Йод - А. Муассак 1886 г. Астат - Э. Сегре 1940 г.
Элементы были открыты: Хлор - К. Шееле 1774 г. Фтор - Б. Куртуа 1811 г. Бром - А. Болер 1826 г. Йод - А. Муассак 1886 г. Астат - Э. Сегре 1940 г.
 Галогены простые вещества, имеющие состав Х 2. Очень реакционноспособны и в свободном виде в природе не встречаются. Источником галогенов являются их соли - галогениды Ме. Х.
Галогены простые вещества, имеющие состав Х 2. Очень реакционноспособны и в свободном виде в природе не встречаются. Источником галогенов являются их соли - галогениды Ме. Х.
 ХЛОР Желто-зеленый газ. Ядовит. В природе встречается в виде Na. Cl, KCl, Mg. Cl 2, Ca. Cl 2 и в виде НCl в желудочном соке.
ХЛОР Желто-зеленый газ. Ядовит. В природе встречается в виде Na. Cl, KCl, Mg. Cl 2, Ca. Cl 2 и в виде НCl в желудочном соке.
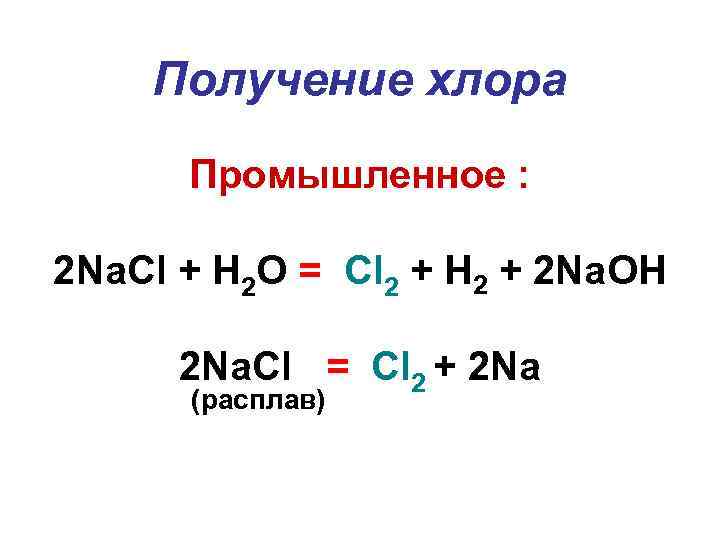 Получение хлора Промышленное : 2 Na. Cl + H 2 O = Cl 2 + H 2 + 2 Na. OH 2 Na. Cl = Cl 2 + 2 Na (расплав)
Получение хлора Промышленное : 2 Na. Cl + H 2 O = Cl 2 + H 2 + 2 Na. OH 2 Na. Cl = Cl 2 + 2 Na (расплав)
 Лабораторное: • 2 KMn. O 4 + 16 HCl = 2 Mn. Cl 2 + 5 Cl 2 + 2 KCl + 8 H 2 O • Ca(OCl)2 + 4 HCl = 2 Cl 2 + Ca. Cl 2 + 2 H 2 O • Mn. O 2 + 4 HCl = 2 Cl 2 + Mn. Cl 2 + 2 H 2 O
Лабораторное: • 2 KMn. O 4 + 16 HCl = 2 Mn. Cl 2 + 5 Cl 2 + 2 KCl + 8 H 2 O • Ca(OCl)2 + 4 HCl = 2 Cl 2 + Ca. Cl 2 + 2 H 2 O • Mn. O 2 + 4 HCl = 2 Cl 2 + Mn. Cl 2 + 2 H 2 O
 Бром Темно-коричневая летучая жидкость. Ядовит. В природе встречается в виде Na. Br, KBr, Mg. Br 2, Ca. Br 2.
Бром Темно-коричневая летучая жидкость. Ядовит. В природе встречается в виде Na. Br, KBr, Mg. Br 2, Ca. Br 2.
 Получение брома Промышленное : 2 KBr + Cl 2 = 2 KCl + Br 2 Бром выделяют из солей морской воды
Получение брома Промышленное : 2 KBr + Cl 2 = 2 KCl + Br 2 Бром выделяют из солей морской воды
 Лабораторное: KBr + H 2 SO 4(конц) = KHSO 4 + HBr(газ) 4 HBr + Mn. O 2 = Mn. Br 2 + 2 H 2 O
Лабораторное: KBr + H 2 SO 4(конц) = KHSO 4 + HBr(газ) 4 HBr + Mn. O 2 = Mn. Br 2 + 2 H 2 O
 Йод Темно-фиолетовое кристаллическое вещество. Имеет металлический блеск, легко возгоняется. В природе встречается: 1) Na. NO 3 - чилийская селитра содержит примеси Na. JO 3, 2)содержится в гормоне тироксин. Йод используется как антисептическое средство.
Йод Темно-фиолетовое кристаллическое вещество. Имеет металлический блеск, легко возгоняется. В природе встречается: 1) Na. NO 3 - чилийская селитра содержит примеси Na. JO 3, 2)содержится в гормоне тироксин. Йод используется как антисептическое средство.
 Получение йода Промышленное 2 KJ + Cl 2 = 2 KCl + J 2 Na. JO 3 + 5 Na. HSO 3 = 3 Na. HSO 4 + 2 Na 2 SO 4 + H 2 O+ J 2 Также йод выделяют из водорослей.
Получение йода Промышленное 2 KJ + Cl 2 = 2 KCl + J 2 Na. JO 3 + 5 Na. HSO 3 = 3 Na. HSO 4 + 2 Na 2 SO 4 + H 2 O+ J 2 Также йод выделяют из водорослей.
 Фтор В 1986 году Карл Кристье открыл, что сильные Льюисовые кислоты (Sb. F 5) могут вытеснять более слабую Льюисовую кислоту Mn. F 4 из [Mn. F 6]2 - иона. Mn. F 4 термодинамически нестабилен и разлагается на Mn. F 3 и F 2. Кристье нагревал Sb. F 5 и К 2 Mn. F 6 до 1500 С в течение 4 часов. Выход F 2 более 40%. KMn. F 6 + 4 Sb. F 5 = 4 KSb. F 6 + 2 Mn. F 3 + F 2
Фтор В 1986 году Карл Кристье открыл, что сильные Льюисовые кислоты (Sb. F 5) могут вытеснять более слабую Льюисовую кислоту Mn. F 4 из [Mn. F 6]2 - иона. Mn. F 4 термодинамически нестабилен и разлагается на Mn. F 3 и F 2. Кристье нагревал Sb. F 5 и К 2 Mn. F 6 до 1500 С в течение 4 часов. Выход F 2 более 40%. KMn. F 6 + 4 Sb. F 5 = 4 KSb. F 6 + 2 Mn. F 3 + F 2
 Получение фтора Промышленное: Электролиз гидрофторидов калия. 2 KHF 2(расплав) = 2 KF(тв) + H 2(газ) + F 2 (газ) 2 KH 2 F 3(расплав) = 2 KНF 2(тв) + H 2(газ) + F 2 (газ) Лабораторное: KMn. F 6 + 4 Sb. F 5 = 4 KSb. F 6 + 2 Mn. F 3 + F 2
Получение фтора Промышленное: Электролиз гидрофторидов калия. 2 KHF 2(расплав) = 2 KF(тв) + H 2(газ) + F 2 (газ) 2 KH 2 F 3(расплав) = 2 KНF 2(тв) + H 2(газ) + F 2 (газ) Лабораторное: KMn. F 6 + 4 Sb. F 5 = 4 KSb. F 6 + 2 Mn. F 3 + F 2
 Фтор в природе встречается: • в минералах - флюорит (Ca. F 2), криолит (Na 3 Al. F 6), флюороапатит (Ca 5(PO 4)3 F), • в морской воде, в крови.
Фтор в природе встречается: • в минералах - флюорит (Ca. F 2), криолит (Na 3 Al. F 6), флюороапатит (Ca 5(PO 4)3 F), • в морской воде, в крови.
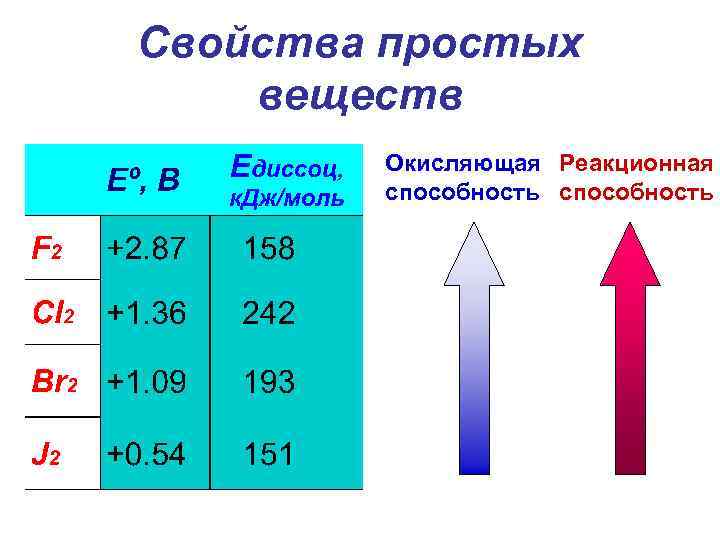 Свойства простых веществ Окисляющая Реакционная способность
Свойства простых веществ Окисляющая Реакционная способность
 Некоторые общие реакции галогенов § § § § n. X 2 + 2 M = 2 MXn Все X 2 с больш. мет. Все X 2 + H 2 = 2 HX 3 X 2+ 2 P = 2 PX 3 Все X 2, и с As, Sb, Bi вместо P 5 X 2+ 2 P = 2 PX 5 Х=F, Cl, Br Все X 2 + H 2 S = S + 2 HX В соотв. с Е° X'2 + 2 X- = 2 X'- + X 2 Х= Cl, Br X 2 + Cn. H 2 n+2 = Cn. H 2 n+1 X + HX Х= Cl, Br X 2 + Cn. H 2 n = Cn. H 2 n. X 2
Некоторые общие реакции галогенов § § § § n. X 2 + 2 M = 2 MXn Все X 2 с больш. мет. Все X 2 + H 2 = 2 HX 3 X 2+ 2 P = 2 PX 3 Все X 2, и с As, Sb, Bi вместо P 5 X 2+ 2 P = 2 PX 5 Х=F, Cl, Br Все X 2 + H 2 S = S + 2 HX В соотв. с Е° X'2 + 2 X- = 2 X'- + X 2 Х= Cl, Br X 2 + Cn. H 2 n+2 = Cn. H 2 n+1 X + HX Х= Cl, Br X 2 + Cn. H 2 n = Cn. H 2 n. X 2
 Реакции с водой 2 F 2 + H 2 O = O 2 + 4 HF X 2 + H 2 O = HX + HXO Х= Cl, Br, J
Реакции с водой 2 F 2 + H 2 O = O 2 + 4 HF X 2 + H 2 O = HX + HXO Х= Cl, Br, J
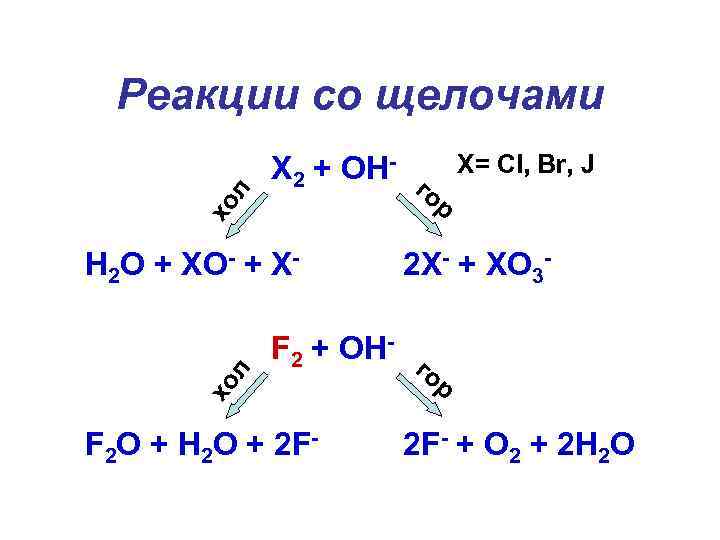 хо л Реакции со щелочами X 2 + OH- г Х= Cl, Br, J ор хо л H 2 O + XO- + X- 2 X- + XO 3 - F 2 + OH- г ор F 2 O + H 2 O + 2 F- + O 2 + 2 H 2 O
хо л Реакции со щелочами X 2 + OH- г Х= Cl, Br, J ор хо л H 2 O + XO- + X- 2 X- + XO 3 - F 2 + OH- г ор F 2 O + H 2 O + 2 F- + O 2 + 2 H 2 O
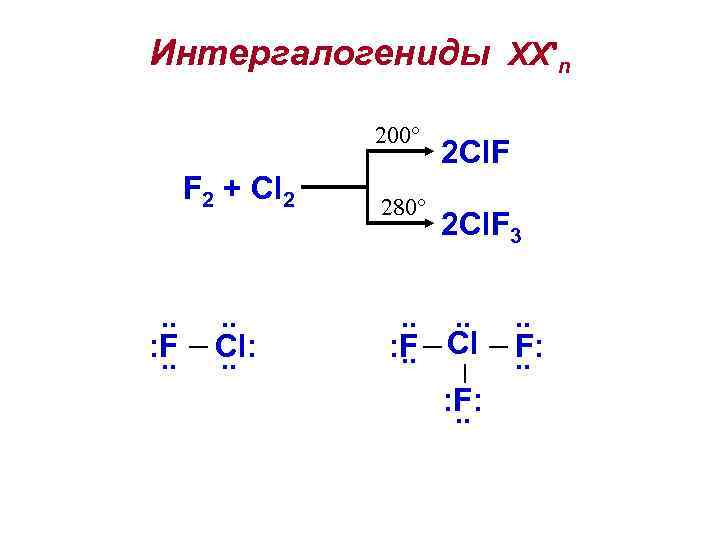 Интергалогениды ХХ'n 200° F 2 + Cl 2 . . : F. . Cl: . . 280° 2 Cl. F 3 . . . : F Cl F: . . : F: . .
Интергалогениды ХХ'n 200° F 2 + Cl 2 . . : F. . Cl: . . 280° 2 Cl. F 3 . . . : F Cl F: . . : F: . .
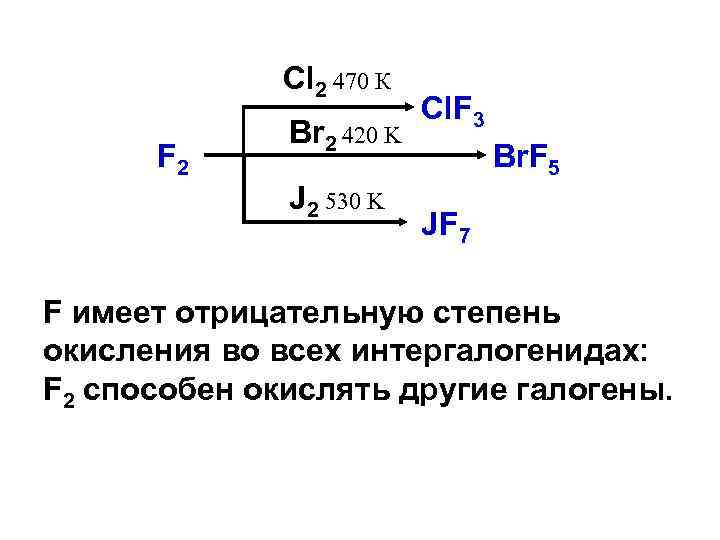 Cl 2 470 К F 2 Br 2 420 K J 2 530 K Cl. F 3 Br. F 5 JF 7 F имеет отрицательную степень окисления во всех интергалогенидах: F 2 способен окислять другие галогены.
Cl 2 470 К F 2 Br 2 420 K J 2 530 K Cl. F 3 Br. F 5 JF 7 F имеет отрицательную степень окисления во всех интергалогенидах: F 2 способен окислять другие галогены.
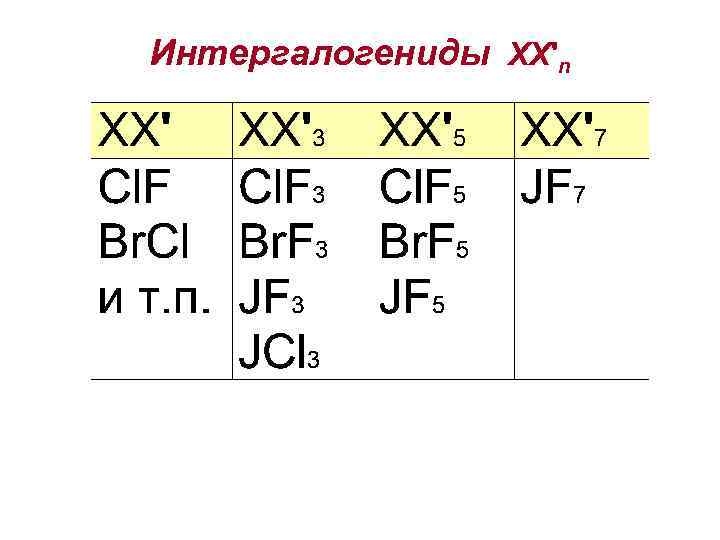 Интергалогениды ХХ'n
Интергалогениды ХХ'n
 Галогенводороды НХ Получение 1) Прямой синтез H 2 + X 2 = 2 HX Со фтором - взрывоопасно, С йодом - медленно даже на свету,
Галогенводороды НХ Получение 1) Прямой синтез H 2 + X 2 = 2 HX Со фтором - взрывоопасно, С йодом - медленно даже на свету,
 C Cl 2, Br 2 реакция протекает фотохимически по радикальному механизму : а- инициирование цепи б- продолжение цепи в- стадии обрыва цепи a Cl 2 = 2 Cl • + H 2 = HCl + H • б H • + Cl 2 = HCl + Cl • H • + H • = H 2 в Cl • + Cl • = Cl 2 H • + Cl • = HCl
C Cl 2, Br 2 реакция протекает фотохимически по радикальному механизму : а- инициирование цепи б- продолжение цепи в- стадии обрыва цепи a Cl 2 = 2 Cl • + H 2 = HCl + H • б H • + Cl 2 = HCl + Cl • H • + H • = H 2 в Cl • + Cl • = Cl 2 H • + Cl • = HCl
 2) Вытеснение менее летучей кислотой Na. X + H 2 SO 4 = HX + Na. HSO 4 Х= Cl, F Na. X + H 3 PO 4 = HX + Na. H 2 PO 4 Х= Br, J
2) Вытеснение менее летучей кислотой Na. X + H 2 SO 4 = HX + Na. HSO 4 Х= Cl, F Na. X + H 3 PO 4 = HX + Na. H 2 PO 4 Х= Br, J
 3) Гидролиз галогенидов неметаллов BCl 3 + 3 H 2 O = H 3 BO 3 + 3 HCl Si. Cl 4 + 2 H 2 O = Si. O 2 + 4 HCl PX 3 + 3 H 2 O = H 3 PO 4 + 3 HX Х= Cl, Br, J
3) Гидролиз галогенидов неметаллов BCl 3 + 3 H 2 O = H 3 BO 3 + 3 HCl Si. Cl 4 + 2 H 2 O = Si. O 2 + 4 HCl PX 3 + 3 H 2 O = H 3 PO 4 + 3 HX Х= Cl, Br, J
 4) Восстановление сероводородом Br 2(вод) + H 2 S(газ) = S(тв) + 2 HBr(вод)
4) Восстановление сероводородом Br 2(вод) + H 2 S(газ) = S(тв) + 2 HBr(вод)
 5) Галогенирование алканов X 2 + Cn. H 2 n+2 = Cn. H 2 n+1 X + HX Х= Cl, F, Br, J
5) Галогенирование алканов X 2 + Cn. H 2 n+2 = Cn. H 2 n+1 X + HX Х= Cl, F, Br, J
 Реакции галогенводородов 1. Изменяют синюю окраску лакмуса 2. Нейтрализуют основания Na. OH + HCl = Na. Cl + H 2 O 3. Реагируют с металлами Mg + 2 HCl = Mg. Cl 2 + H 2 4. Реагируют с карбонатами Ca. CO 3 + 2 HCl = Ca. Cl 2 + H 2 O + CO 2
Реакции галогенводородов 1. Изменяют синюю окраску лакмуса 2. Нейтрализуют основания Na. OH + HCl = Na. Cl + H 2 O 3. Реагируют с металлами Mg + 2 HCl = Mg. Cl 2 + H 2 4. Реагируют с карбонатами Ca. CO 3 + 2 HCl = Ca. Cl 2 + H 2 O + CO 2
 Сила кислот увеличивается в ряду: HF HCl HBr HJ 10% 92. 6% 93. 5% 95% Кажущаяся степень диссоциации Восстанавливающая способность
Сила кислот увеличивается в ряду: HF HCl HBr HJ 10% 92. 6% 93. 5% 95% Кажущаяся степень диссоциации Восстанавливающая способность
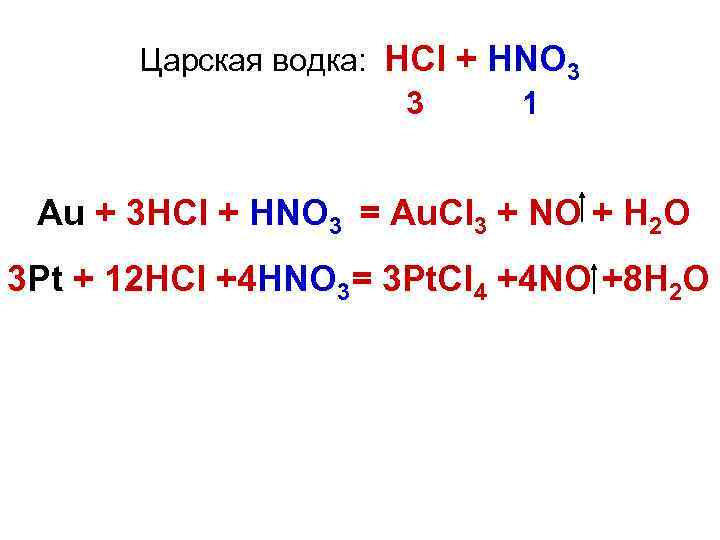 Царская водка: HCl + HNO 3 3 1 Au + 3 HCl + HNO 3 = Au. Cl 3 + NO + H 2 O 3 Pt + 12 HCl +4 HNO 3= 3 Pt. Cl 4 +4 NO +8 H 2 O
Царская водка: HCl + HNO 3 3 1 Au + 3 HCl + HNO 3 = Au. Cl 3 + NO + H 2 O 3 Pt + 12 HCl +4 HNO 3= 3 Pt. Cl 4 +4 NO +8 H 2 O
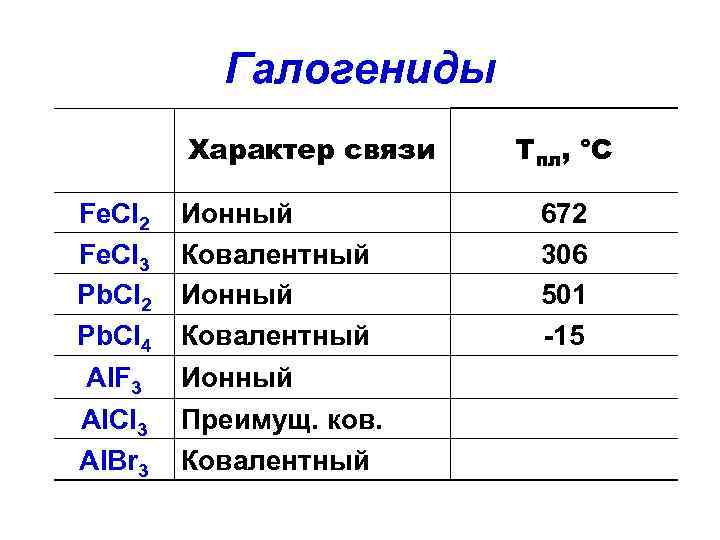 Галогениды Характер связи Fe. Cl 2 Fe. Cl 3 Pb. Cl 2 Pb. Cl 4 Al. F 3 Al. Cl 3 Al. Br 3 Ионный Ковалентный Ионный Преимущ. ков. Ковалентный Тпл, °С 672 306 501 -15
Галогениды Характер связи Fe. Cl 2 Fe. Cl 3 Pb. Cl 2 Pb. Cl 4 Al. F 3 Al. Cl 3 Al. Br 3 Ионный Ковалентный Ионный Преимущ. ков. Ковалентный Тпл, °С 672 306 501 -15
 Получение галогенидов Взаимодействие металлов или их оксидов с НХ или Х 2 Fe + 2 HCl = Fe. Cl 2 + H 2 2 Fe + Cl 2 = 2 Fe. Cl 3 Fe 2 О 3 + 2 HCl = Fe. Cl 2 + H 2 О 2 P + Cl 2 = 2 PCl 3 + 3 Cl 2 = 2 PCl 5
Получение галогенидов Взаимодействие металлов или их оксидов с НХ или Х 2 Fe + 2 HCl = Fe. Cl 2 + H 2 2 Fe + Cl 2 = 2 Fe. Cl 3 Fe 2 О 3 + 2 HCl = Fe. Cl 2 + H 2 О 2 P + Cl 2 = 2 PCl 3 + 3 Cl 2 = 2 PCl 5
 Важнейшие реакции галогенидов 1. Вытеснение - = 2 Cl- + J Сl 2 + 2 J 2 Cl 2. С конц. серной кислотой (тв) + H 2 SO 4 = HCl + HSO 4 (тв) 3. С ионами свинца 2++ 2 XPb = Pb. X 2 4. С ионами серебрa (качественная реакция на галогениды) ++ XAg = Ag. X
Важнейшие реакции галогенидов 1. Вытеснение - = 2 Cl- + J Сl 2 + 2 J 2 Cl 2. С конц. серной кислотой (тв) + H 2 SO 4 = HCl + HSO 4 (тв) 3. С ионами свинца 2++ 2 XPb = Pb. X 2 4. С ионами серебрa (качественная реакция на галогениды) ++ XAg = Ag. X
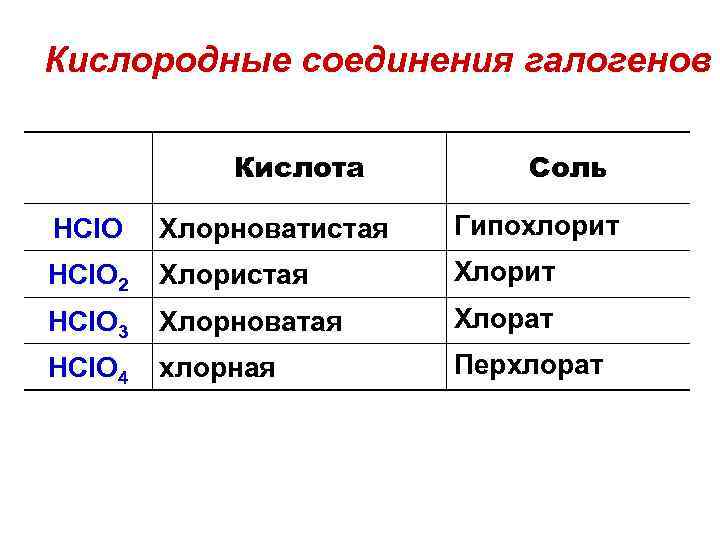 Кислородные соединения галогенов Кислота Соль HCl. O Хлорноватистая Гипохлорит HCl. O 2 Хлористая Хлорит HCl. O 3 Хлорноватая Хлорат HCl. O 4 хлорная Перхлорат
Кислородные соединения галогенов Кислота Соль HCl. O Хлорноватистая Гипохлорит HCl. O 2 Хлористая Хлорит HCl. O 3 Хлорноватая Хлорат HCl. O 4 хлорная Перхлорат
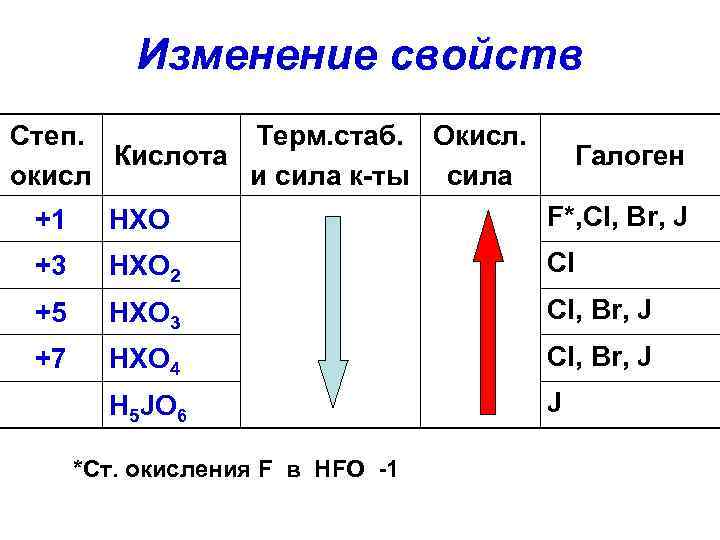 Изменение свойств Степ. Терм. стаб. Окисл. Кислота окисл и сила к-ты сила Галоген +1 HXO F*, Cl, Br, J +3 HXO 2 Cl +5 HXO 3 Cl, Br, J +7 HXO 4 Cl, Br, J H 5 JO 6 J *Cт. окисления F в HFO -1
Изменение свойств Степ. Терм. стаб. Окисл. Кислота окисл и сила к-ты сила Галоген +1 HXO F*, Cl, Br, J +3 HXO 2 Cl +5 HXO 3 Cl, Br, J +7 HXO 4 Cl, Br, J H 5 JO 6 J *Cт. окисления F в HFO -1
 Получение кислородсодержащих кислот галогенов • Оксокислоты НХО для хлора, брома и йода не получены и известны только в растворах. Исключение – НFO. • НFO – бесцв. тв. вещество, получение: F 2 + H 2 O = НFO + HF • НFO быстро реагирует с водой: 4 НFO + 2 H 2 O = 4 HF + 2 Н 2 О 2 + О 2
Получение кислородсодержащих кислот галогенов • Оксокислоты НХО для хлора, брома и йода не получены и известны только в растворах. Исключение – НFO. • НFO – бесцв. тв. вещество, получение: F 2 + H 2 O = НFO + HF • НFO быстро реагирует с водой: 4 НFO + 2 H 2 O = 4 HF + 2 Н 2 О 2 + О 2
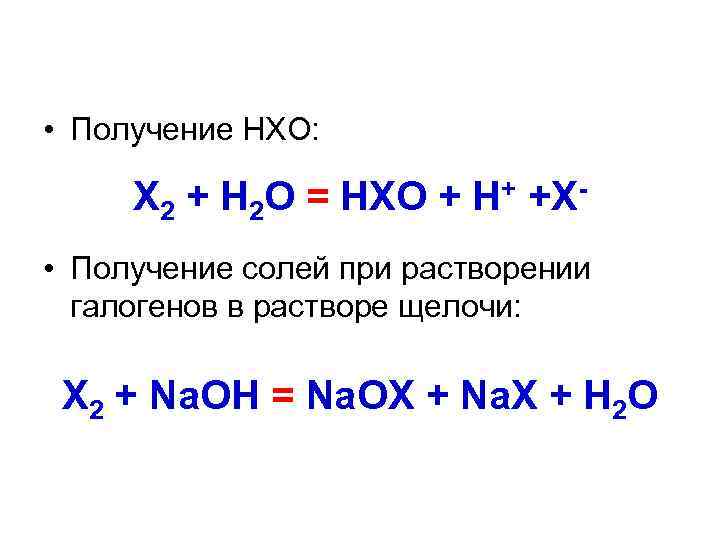 • Получение НХО: Х 2 + H 2 O = НХO + H+ +Х • Получение солей при растворении галогенов в растворе щелочи: Х 2 + Na. OH = Na. OХ + Na. Х + H 2 O
• Получение НХО: Х 2 + H 2 O = НХO + H+ +Х • Получение солей при растворении галогенов в растворе щелочи: Х 2 + Na. OH = Na. OХ + Na. Х + H 2 O
 • Кислоты НХО 2 также не удается выделить. • НCl. О 2 – хлористая кислота, получение Ba(Сl. O 2)2 + H 2 SO 4 = 2 HCl. O 2 +Ba. SO 4 • ее соли – хлориты синтезируют косвенным путем: 2 Сl. O 2 + 2 KOH = KCl. O 2 +KCl. O 3 + H 2 O
• Кислоты НХО 2 также не удается выделить. • НCl. О 2 – хлористая кислота, получение Ba(Сl. O 2)2 + H 2 SO 4 = 2 HCl. O 2 +Ba. SO 4 • ее соли – хлориты синтезируют косвенным путем: 2 Сl. O 2 + 2 KOH = KCl. O 2 +KCl. O 3 + H 2 O
 • Кислота НJО 3 единственная из кислот состава НХО 3 выделенная в твердом состоянии. • Получение солей НСl. О 3 : Химическое окисление 6 KОН +3 Сl 2 = KCl. O 3 + 5 KСl + 3 H 2 O Электрохимическое окисление KСl + 3 H 2 O = KCl. O 3 + 3 H 2
• Кислота НJО 3 единственная из кислот состава НХО 3 выделенная в твердом состоянии. • Получение солей НСl. О 3 : Химическое окисление 6 KОН +3 Сl 2 = KCl. O 3 + 5 KСl + 3 H 2 O Электрохимическое окисление KСl + 3 H 2 O = KCl. O 3 + 3 H 2
 Соли кислородсодержащих кислот галогенов более устойчивы, чем кислоты. 2 KCl. O 3 = 2 KCl + 3 O 2 при Т >370°C KCl. O 3 = KCl. O 4 + KCl при Т <370°C Бертолетовая соль
Соли кислородсодержащих кислот галогенов более устойчивы, чем кислоты. 2 KCl. O 3 = 2 KCl + 3 O 2 при Т >370°C KCl. O 3 = KCl. O 4 + KCl при Т <370°C Бертолетовая соль
 • Кислота НCl. О 4 наиболее устойчивая и частоприменяемая среди кислот состава НХО 4. Na. Cl. O 4 + НСlконц = Na. Сl + HCl. O 4 При нагревании перхлораты теряют кислород KCl. O 4 = KСl + 2 O 2
• Кислота НCl. О 4 наиболее устойчивая и частоприменяемая среди кислот состава НХО 4. Na. Cl. O 4 + НСlконц = Na. Сl + HCl. O 4 При нагревании перхлораты теряют кислород KCl. O 4 = KСl + 2 O 2
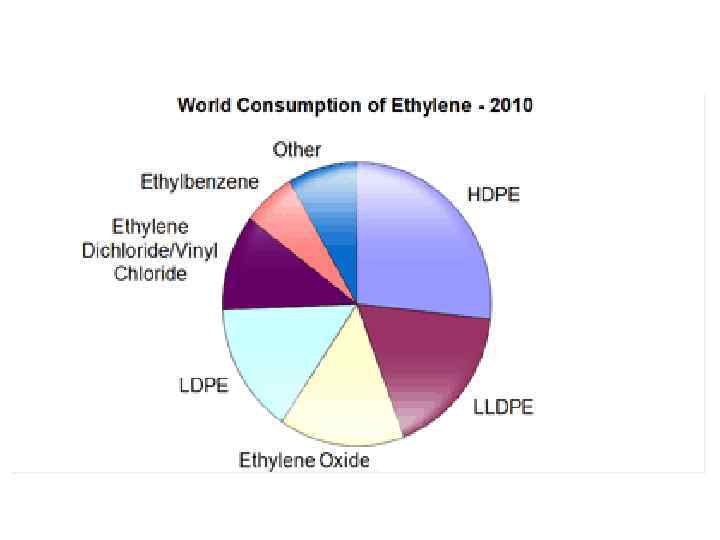
 Хлор интенсивно используется : • производсво ПВХ • производство органических химикатов • производство неорганических химикатов • дезинфекция, обеззараживание воды, отбеливание
Хлор интенсивно используется : • производсво ПВХ • производство органических химикатов • производство неорганических химикатов • дезинфекция, обеззараживание воды, отбеливание
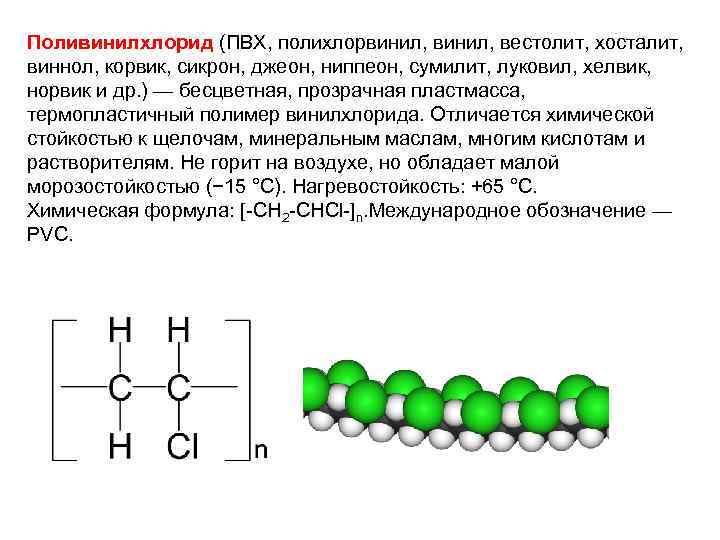 Поливинилхлорид (ПВХ, полихлорвинил, вестолит, хосталит, виннол, корвик, сикрон, джеон, ниппеон, сумилит, луковил, хелвик, норвик и др. ) — бесцветная, прозрачная пластмасса, термопластичный полимер винилхлорида. Отличается химической стойкостью к щелочам, минеральным маслам, многим кислотам и растворителям. Не горит на воздухе, но обладает малой морозостойкостью (− 15 °C). Нагревостойкость: +65 °C. Химическая формула: [-CH 2 -CHCl-]n. Международное обозначение — PVC.
Поливинилхлорид (ПВХ, полихлорвинил, вестолит, хосталит, виннол, корвик, сикрон, джеон, ниппеон, сумилит, луковил, хелвик, норвик и др. ) — бесцветная, прозрачная пластмасса, термопластичный полимер винилхлорида. Отличается химической стойкостью к щелочам, минеральным маслам, многим кислотам и растворителям. Не горит на воздухе, но обладает малой морозостойкостью (− 15 °C). Нагревостойкость: +65 °C. Химическая формула: [-CH 2 -CHCl-]n. Международное обозначение — PVC.
 ОКМ - простой путь от метана к этилену CH 4 О 2 (ПГ, ПНГ) Кат. С 2 Н 4 Созданы новые оксидно-кремниевые композитные материалы - эффективные катализаторы одностадийного превращения метана в этилен. Уровень востребованности промышленностью: - Разработана технология получения катализатора, конструкция реакторного узла и предложена технологическая схема процесса. - Подготовлены пилотные испытания. Дедов А. Г. , Локтев А. С. , Моисеев И. И. и др. (РГУ НГ, ИОНХ РАН, ИНХС РАН)
ОКМ - простой путь от метана к этилену CH 4 О 2 (ПГ, ПНГ) Кат. С 2 Н 4 Созданы новые оксидно-кремниевые композитные материалы - эффективные катализаторы одностадийного превращения метана в этилен. Уровень востребованности промышленностью: - Разработана технология получения катализатора, конструкция реакторного узла и предложена технологическая схема процесса. - Подготовлены пилотные испытания. Дедов А. Г. , Локтев А. С. , Моисеев И. И. и др. (РГУ НГ, ИОНХ РАН, ИНХС РАН)
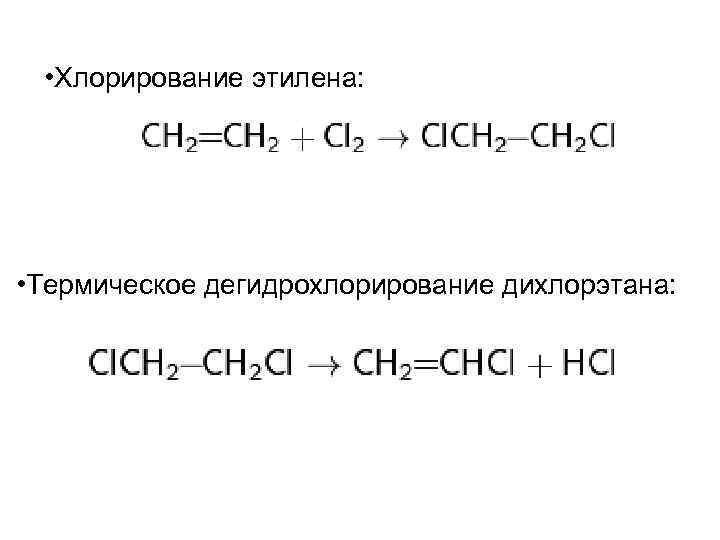 • Хлорирование этилена: • Термическое дегидрохлорирование дихлорэтана:
• Хлорирование этилена: • Термическое дегидрохлорирование дихлорэтана:
 Применение ПВХ Применяется для электроизоляции проводов и кабелей, производства листов, труб (преимущественно хлорированный поливинилхлорид), пленок для натяжных потолков, искусственных кож, поливинилхлоридного волокна, пенополивинилхлорида, линолеума, обувных пластикатов, мебельной кромки и т. д. Также применяется для производства грампластинок (т. н. виниловых), профилей для изготовления окон и дверей. Поливинилхлорид также часто используется в одежде и аксессуарах для создания подобного коже материала, отличающегося гладкостью и блеском. Поливинилхлорид используют как уплотнитель в бытовых холодильниках, вместо относительно сложных механических затворов. Это дало возможность применить магнитные затворы в виде намагниченных эластичных вставок, помещаемых в баллоне уплотнителя.
Применение ПВХ Применяется для электроизоляции проводов и кабелей, производства листов, труб (преимущественно хлорированный поливинилхлорид), пленок для натяжных потолков, искусственных кож, поливинилхлоридного волокна, пенополивинилхлорида, линолеума, обувных пластикатов, мебельной кромки и т. д. Также применяется для производства грампластинок (т. н. виниловых), профилей для изготовления окон и дверей. Поливинилхлорид также часто используется в одежде и аксессуарах для создания подобного коже материала, отличающегося гладкостью и блеском. Поливинилхлорид используют как уплотнитель в бытовых холодильниках, вместо относительно сложных механических затворов. Это дало возможность применить магнитные затворы в виде намагниченных эластичных вставок, помещаемых в баллоне уплотнителя.
 Бром используется : • для получения 1, 2 -дибромэтана - компонента бензина • для получения Ag. Br - светочувствительного компонента фотографических материалов • в огнестойких материалах, красках
Бром используется : • для получения 1, 2 -дибромэтана - компонента бензина • для получения Ag. Br - светочувствительного компонента фотографических материалов • в огнестойких материалах, красках
 Фтор используется : • фторирующий агент для получения фтор- и перфторуглеводородов и др. , • для получения фторсодержащих полимеров, химически инертных, (-СF 2 -CF 2 -) - тефлон, • для получения КF 6, который используется для разделения стабильных и нестабильных изотопов, • Ca 5(PC 4)2 F - используется в зубной пасте • используется для получения гексафторида урана в процессах обогащения ядерного топлив
Фтор используется : • фторирующий агент для получения фтор- и перфторуглеводородов и др. , • для получения фторсодержащих полимеров, химически инертных, (-СF 2 -CF 2 -) - тефлон, • для получения КF 6, который используется для разделения стабильных и нестабильных изотопов, • Ca 5(PC 4)2 F - используется в зубной пасте • используется для получения гексафторида урана в процессах обогащения ядерного топлив
 Использование Иода В медицине: 5 -процентный спиртовой раствор иода используется для дезинфекцииткожи вокруг повреждения (рваной, резаной или иной раны). В рентгенологических и томографических исследованиях широко применяются йодсодержащие контрастные препараты. В технике: Источники света (галогеновая лампа, металлогалогеновая лампа) Производство аккумуляторов (Иод используется в качестве компонента положительного электрода (окислителя) в литиево-иодных аккумуляторах для электромобилей. ) Лазерный термоядерный синтез (Некоторые иодорганические соединения применяются для производства сверхмощных газовых лазеров на возбужденных атомах иода (исследования в области лазерного термоядерного синтеза и промышленность). Радиоэлектронная промышленность (В последние годы резко повысился спрос на иод со стороны производителей жидкокристаллических дисплеев).
Использование Иода В медицине: 5 -процентный спиртовой раствор иода используется для дезинфекцииткожи вокруг повреждения (рваной, резаной или иной раны). В рентгенологических и томографических исследованиях широко применяются йодсодержащие контрастные препараты. В технике: Источники света (галогеновая лампа, металлогалогеновая лампа) Производство аккумуляторов (Иод используется в качестве компонента положительного электрода (окислителя) в литиево-иодных аккумуляторах для электромобилей. ) Лазерный термоядерный синтез (Некоторые иодорганические соединения применяются для производства сверхмощных газовых лазеров на возбужденных атомах иода (исследования в области лазерного термоядерного синтеза и промышленность). Радиоэлектронная промышленность (В последние годы резко повысился спрос на иод со стороны производителей жидкокристаллических дисплеев).


