2016_HetБАВ_6.ppt
- Количество слайдов: 31

Химия биологически активных веществ Лекция 6 ХИНОЛИН, ИЗОХИНОЛИН, АКРИДИН 1

1. ХИНОЛИН Строение хинолина 2 3
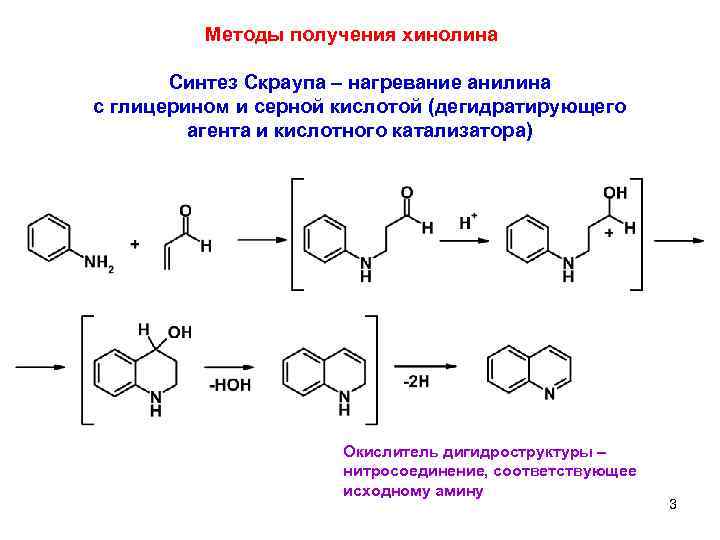
Методы получения хинолина Синтез Скраупа – нагревание анилина с глицерином и серной кислотой (дегидратирующего агента и кислотного катализатора) Окислитель дигидроструктуры – нитросоединение, соответствующее исходному амину 3 4
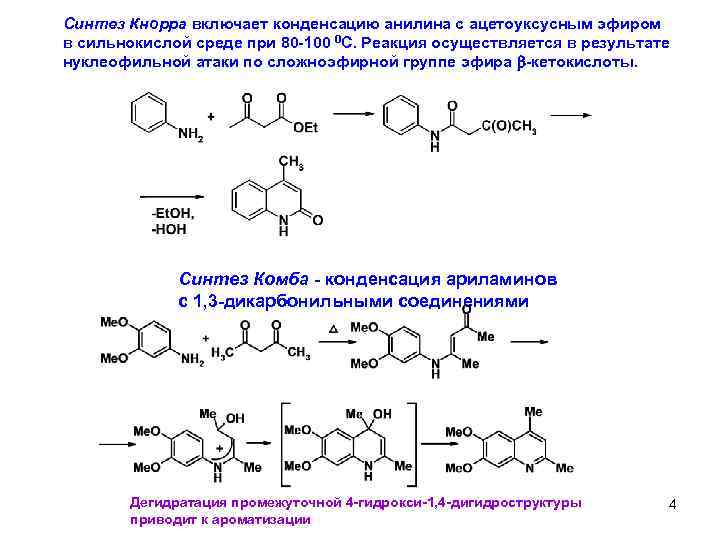
Синтез Кнорра включает конденсацию анилина с ацетоуксусным эфиром в сильнокислой среде при 80 -100 0 С. Реакция осуществляется в результате нуклеофильной атаки по сложноэфирной группе эфира b-кетокислоты. Синтез Комба - конденсация ариламинов с 1, 3 -дикарбонильными соединениями Дегидратация промежуточной 4 -гидрокси-1, 4 -дигидроструктуры приводит к ароматизации 46
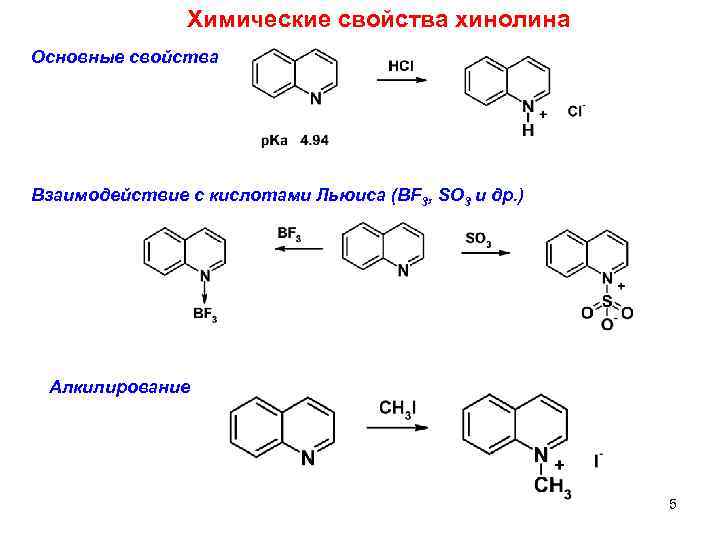
Химические свойства хинолина Основные свойства Взаимодействие с кислотами Льюиса (BF 3, SO 3 и др. ) Алкилирование 5
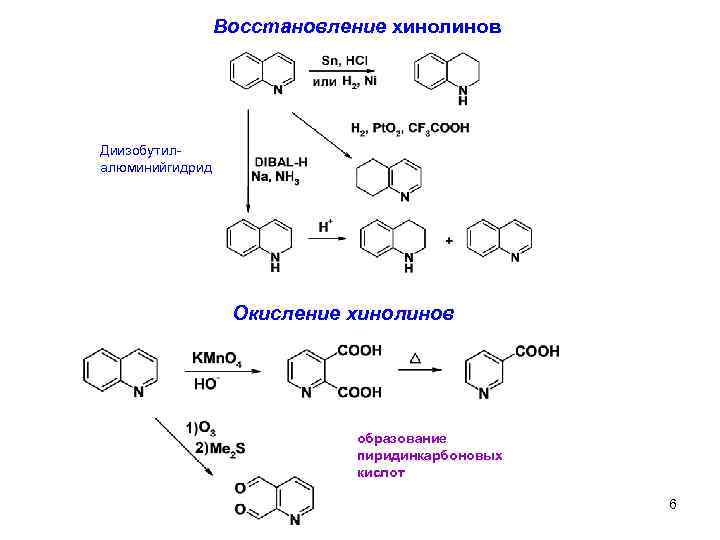
Восстановление хинолинов Диизобутилалюминийгидрид Окисление хинолинов образование пиридинкарбоновых кислот 69
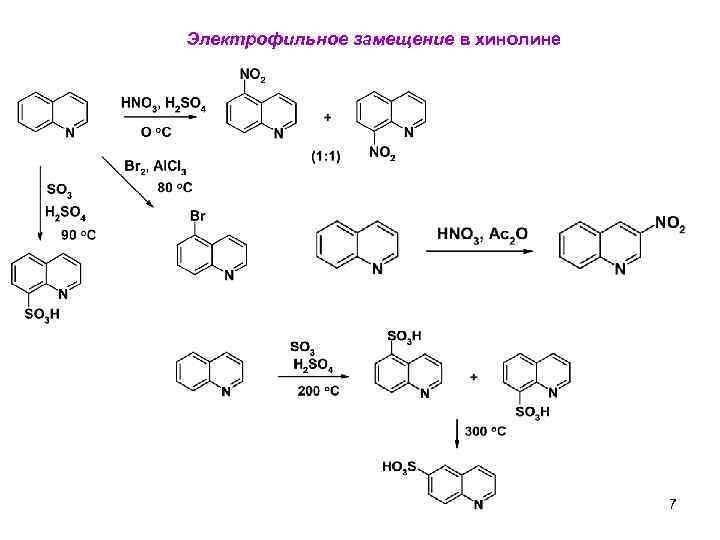
Электрофильное замещение в хинолине 7 12
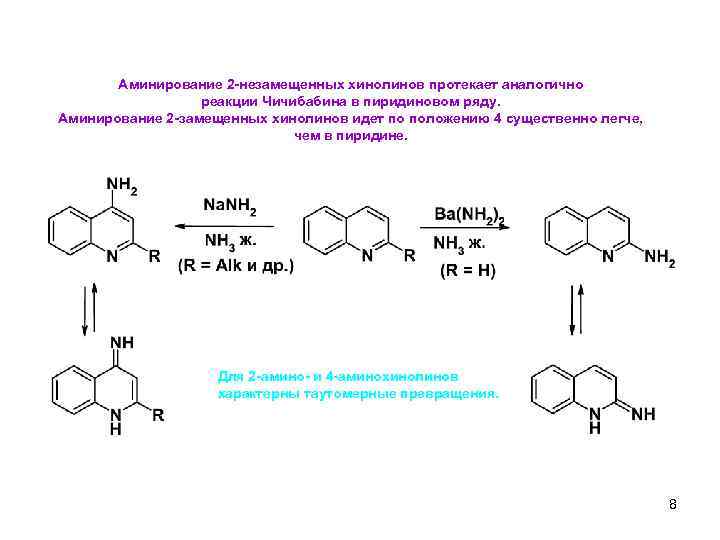
Аминирование 2 -незамещенных хинолинов протекает аналогично реакции Чичибабина в пиридиновом ряду. Аминирование 2 -замещенных хинолинов идет по положению 4 существенно легче, чем в пиридине. Для 2 -амино- и 4 -аминохинолинов характерны таутомерные превращения. 8 13
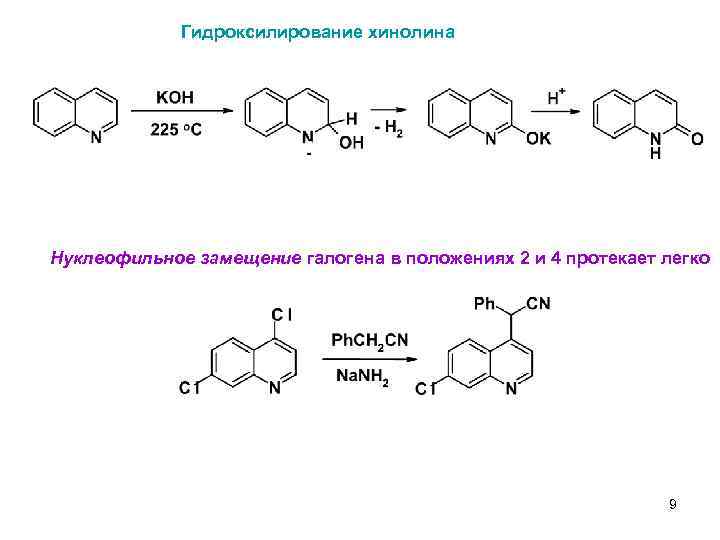
Гидроксилирование хинолина Нуклеофильное замещение галогена в положениях 2 и 4 протекает легко 9 14
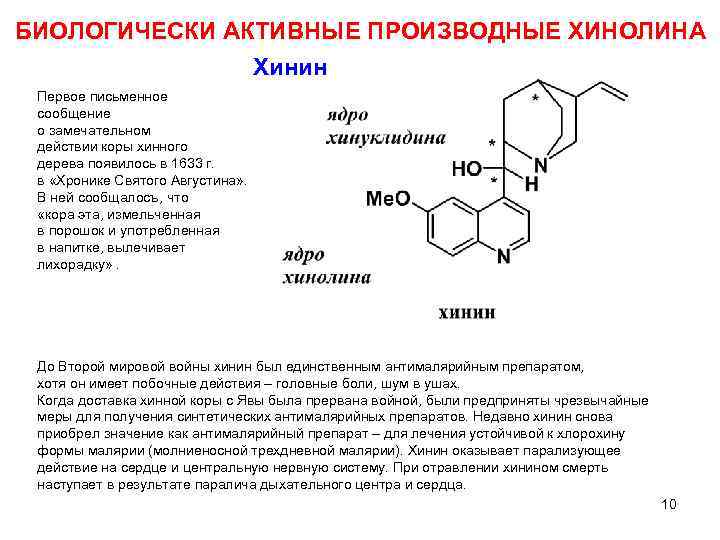
БИОЛОГИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ ХИНОЛИНА Хинин Первое письменное сообщение о замечательном действии коры хинного дерева появилось в 1633 г. в «Хронике Святого Августина» . В ней сообщалосъ, что «кора эта, измельченная в порошок и употребленная в напитке, вылечивает лихорадку» . До Второй мировой войны хинин был единственным антималярийным препаратом, хотя он имеет побочные действия – головные боли, шум в ушах. Когда доставка хинной коры с Явы была прервана войной, были предприняты чрезвычайные меры для получения синтетических антималярийных препаратов. Недавно хинин снова приобрел значение как антималярийный препарат – для лечения устойчивой к хлорохину формы малярии (молниеносной трехдневной малярии). Хинин оказывает парализующее действие на сердце и центральную нервную систему. При отравлении хинином смерть наступает в результате паралича дыхательного центра и сердца. 10 3
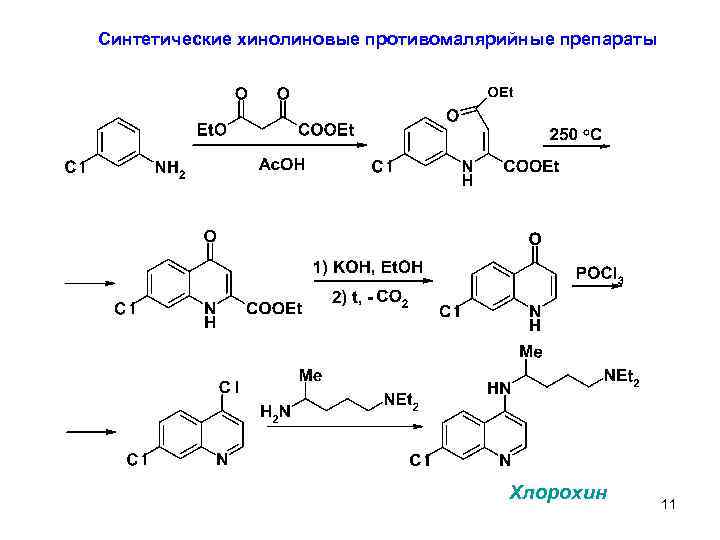
Синтетические хинолиновые противомалярийные препараты Хлорохин 11
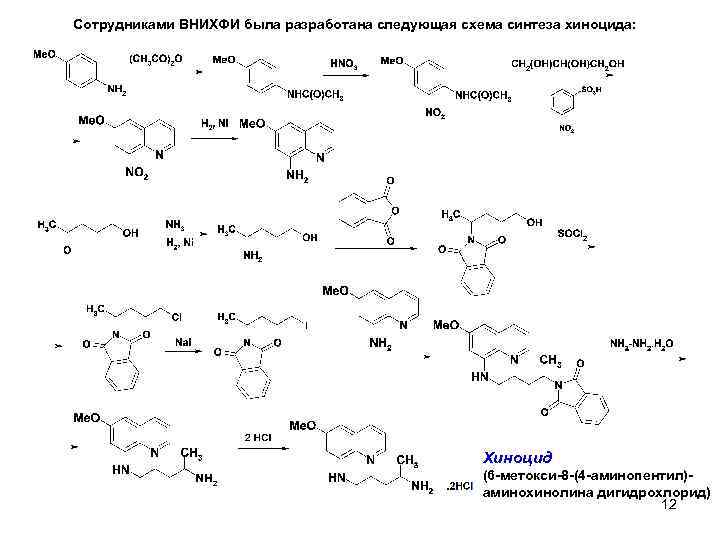
Сотрудниками ВНИХФИ была разработана следующая схема синтеза хиноцида: Хиноцид (6 -метокси-8 -(4 -аминопентил)аминохинолина дигидрохлорид) 12
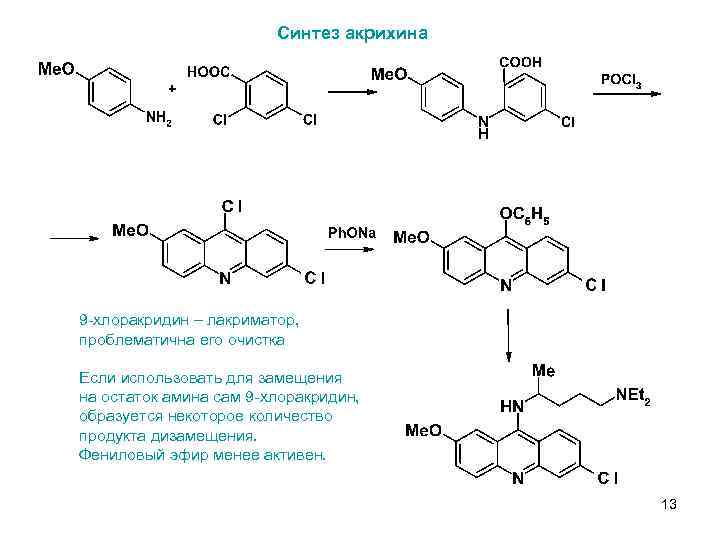
Синтез акрихина 9 -хлоракридин – лакриматор, проблематична его очистка Если использовать для замещения на остаток амина сам 9 -хлоракридин, образуется некоторое количество продукта дизамещения. Фениловый эфир менее активен. 13
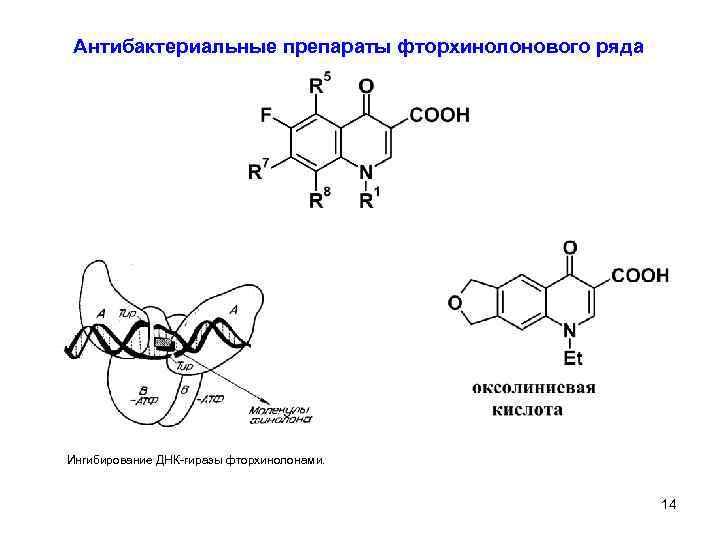
Антибактериальные препараты фторхинолонового ряда Ингибирование ДНК-гиразы фторхинолонами. 14 5
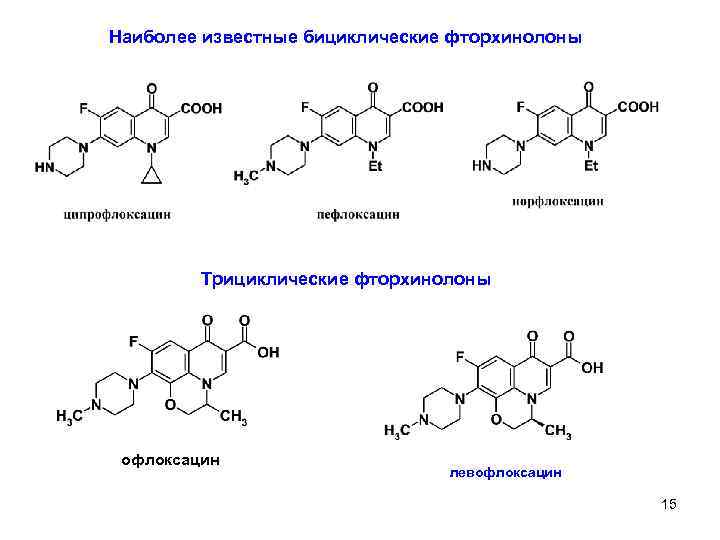
Наиболее известные бициклические фторхинолоны Трициклические фторхинолоны офлоксацин левофлоксацин 15 7
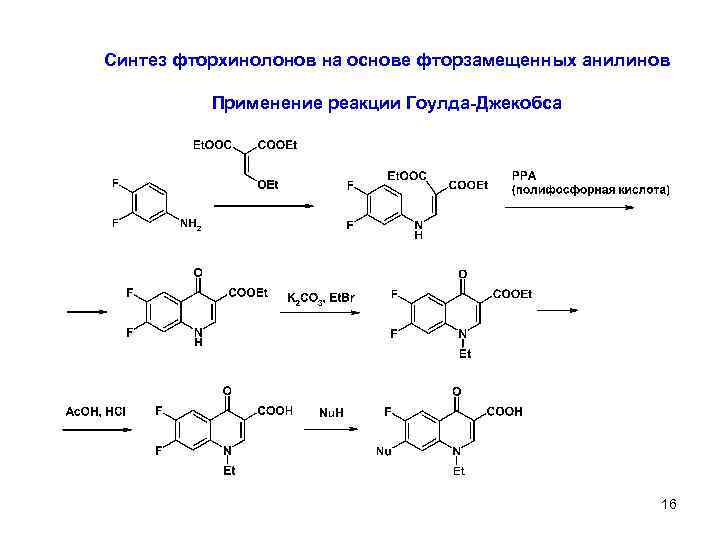
Синтез фторхинолонов на основе фторзамещенных анилинов Применение реакции Гоулда-Джекобса 16 8
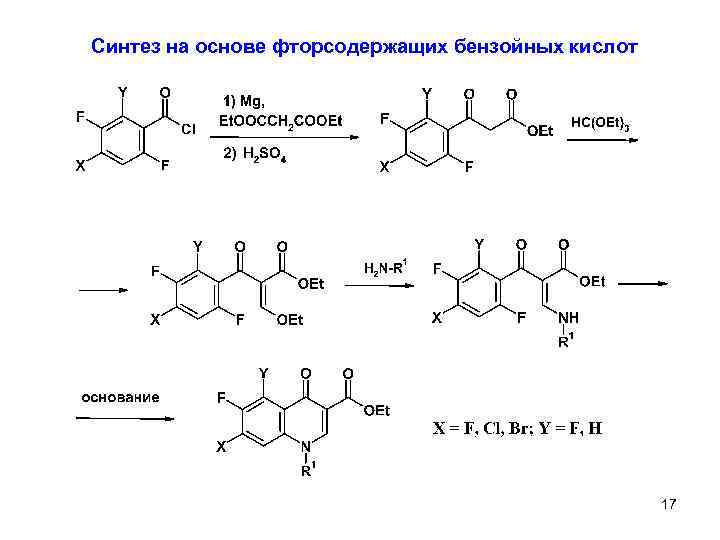
Синтез на основе фторсодержащих бензойных кислот 17 9
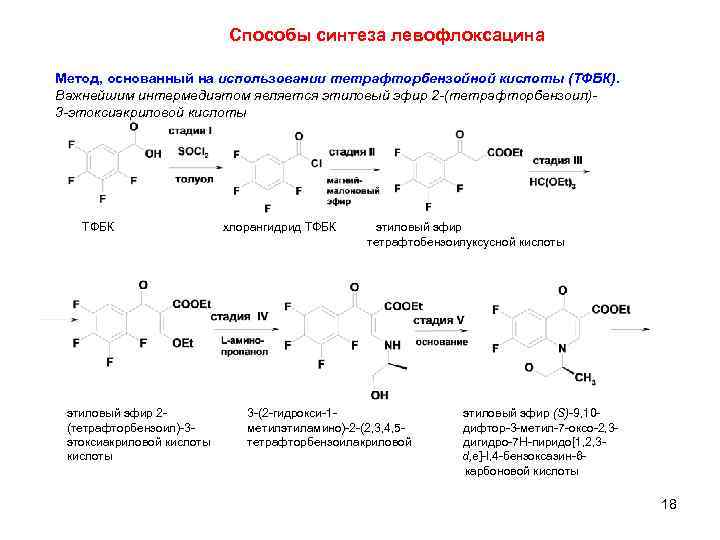
Способы синтеза левофлоксацина Метод, основанный на использовании тетрафторбензойной кислоты (ТФБК). Важнейшим интермедиатом является этиловый эфир 2 -(тетрафторбензоил)3 -этоксиакриловой кислоты ТФБК этиловый эфир 2(тетрафторбензоил)-3 этоксиакриловой кислоты хлорангидрид ТФБК этиловый эфир тетрафтобензоилуксусной кислоты 3 -(2 -гидрокси-1 метилэтиламино)-2 -(2, 3, 4, 5 тетрафторбензоилакриловой этиловый эфир (S)-9, 10 дифтор-3 -метил-7 -оксо-2, 3 дигидро-7 H-пиридо[1, 2, 3 d, e]-l, 4 -бензоксазин-6 карбоновой кислоты 18
![(S)-9, 10 -дифтор-3 -метил-7 -оксо-2, 3 дигидро-7 H-пиридо[1, 2, 3 -d, e]-l, 4 бензоксазин-6 (S)-9, 10 -дифтор-3 -метил-7 -оксо-2, 3 дигидро-7 H-пиридо[1, 2, 3 -d, e]-l, 4 бензоксазин-6](https://present5.com/presentation/183500408_443894058/image-19.jpg)
(S)-9, 10 -дифтор-3 -метил-7 -оксо-2, 3 дигидро-7 H-пиридо[1, 2, 3 -d, e]-l, 4 бензоксазин-6 -карбоновая кислота (S)-9 -фтор-2, 3 -дигидро-3 -метил-10 -(4 метил-1 -пиперазинил)-7 -оксо-7 Нпиридо[1, 2, 3 -d, e]-1, 4 -бензоксазин-6 карбоновая кислота, полугидрат В зависимости от условий циклизация (стадия V) протекает в один или 2 этапа, во втором случае выделяют промежуточный продукт – бициклический хинолон. 19
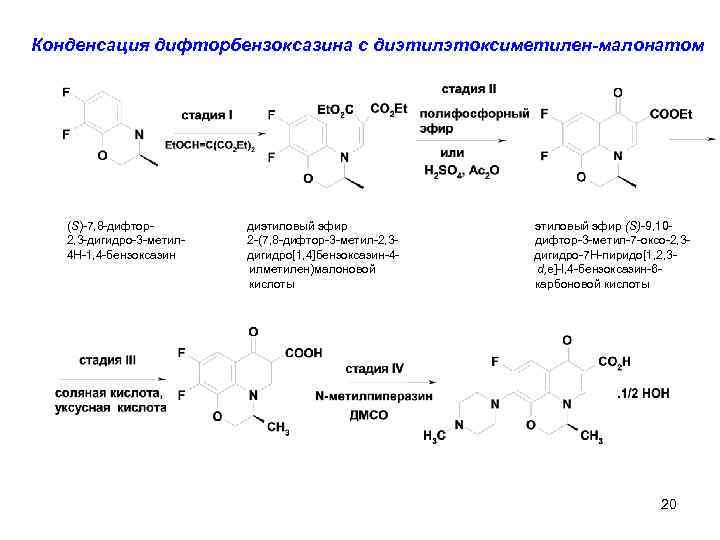
Конденсация дифторбензоксазина с диэтилэтоксиметилен-малонатом (S)-7, 8 -дифтор2, 3 -дигидро-3 -метил 4 H-1, 4 -бензоксазин диэтиловый эфир 2 -(7, 8 -дифтор-3 -метил-2, 3 дигидро[1, 4]бензоксазин-4 илметилен)малоновой кислоты этиловый эфир (S)-9, 10 дифтор-3 -метил-7 -оксо-2, 3 дигидро-7 H-пиридо[1, 2, 3 d, e]-l, 4 -бензоксазин-6 карбоновой кислоты 20
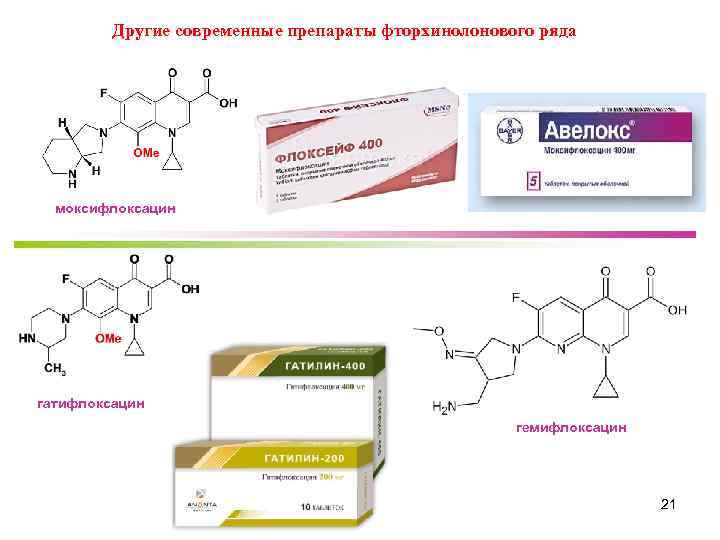
Другие современные препараты фторхинолонового ряда моксифлоксацин гатифлоксацин гемифлоксацин 21
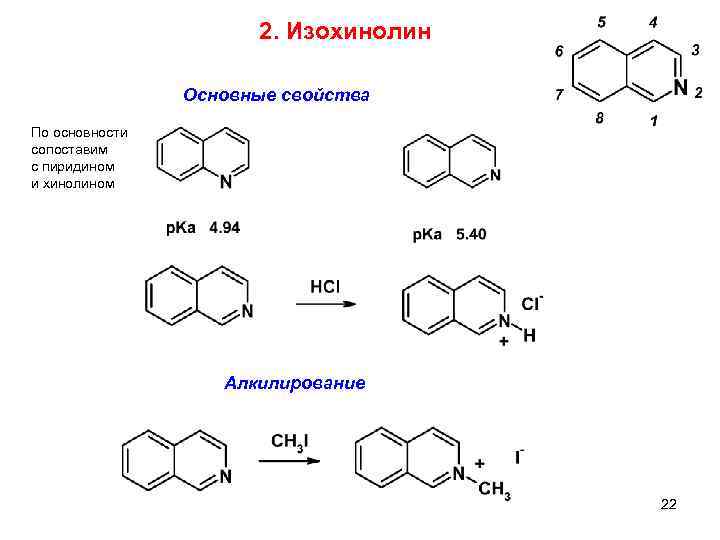
2. Изохинолин Основные свойства По основности сопоставим с пиридином и хинолином Алкилирование 22 3
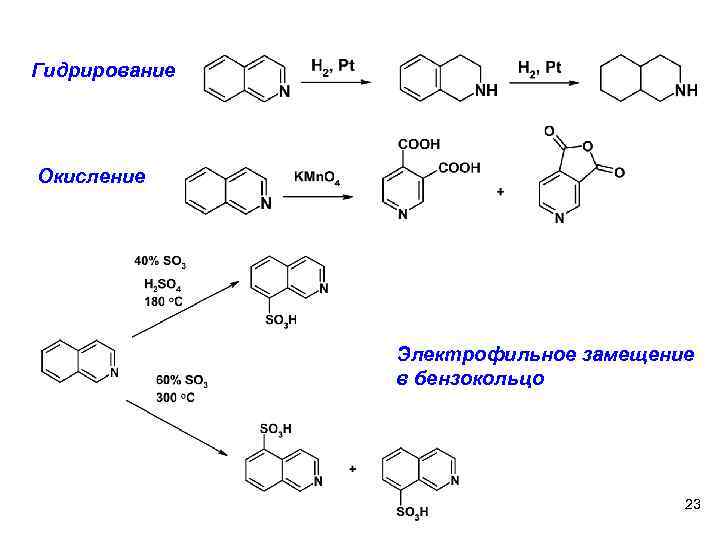
Гидрирование Окисление Электрофильное замещение в бензокольцо 23
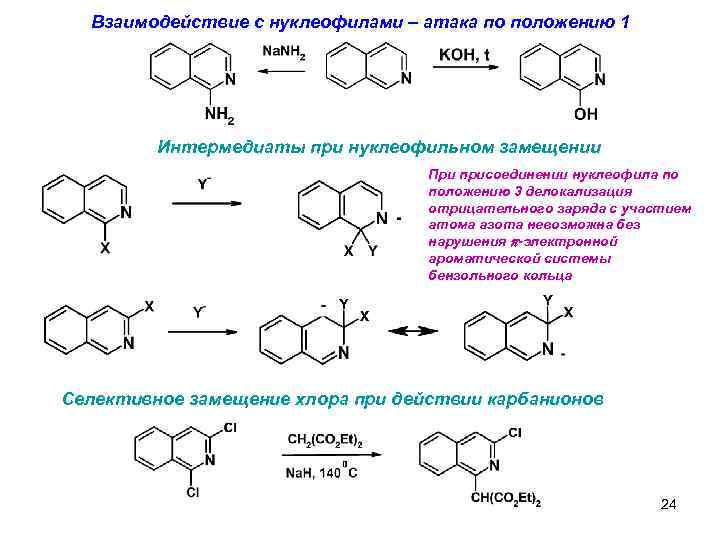
Взаимодействие с нуклеофилами – атака по положению 1 Интермедиаты при нуклеофильном замещении При присоединении нуклеофила по положению 3 делокализация отрицательного заряда с участием атома азота невозможна без нарушения p-электронной ароматической системы бензольного кольца Селективное замещение хлора при действии карбанионов 24
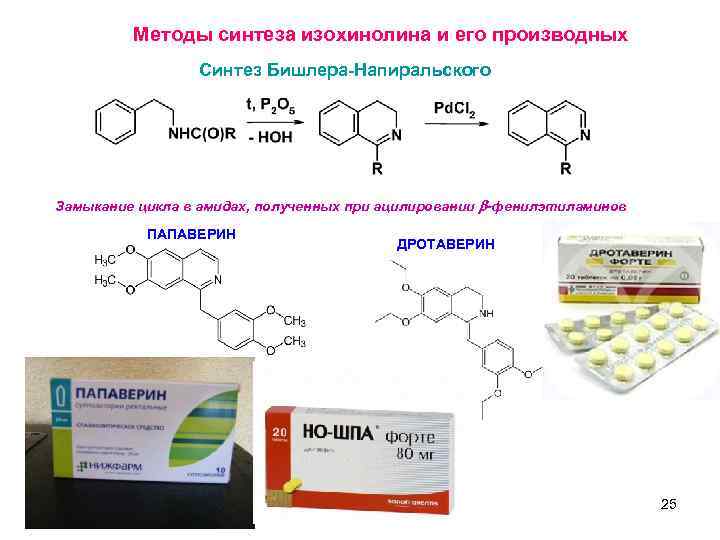
Методы синтеза изохинолина и его производных Синтез Бишлера-Напиральского Замыкание цикла в амидах, полученных при ацилировании b-фенилэтиламинов ПАПАВЕРИН ДРОТАВЕРИН 25 7
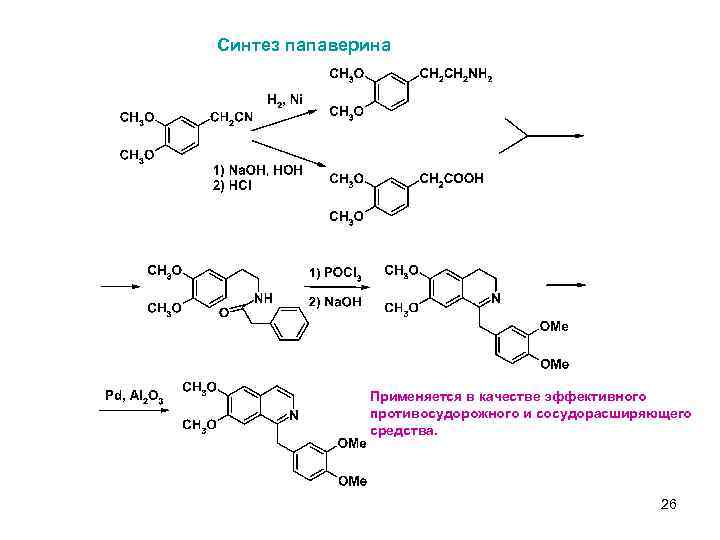
Синтез папаверина Применяется в качестве эффективного противосудорожного и сосудорасширяющего средства. 26
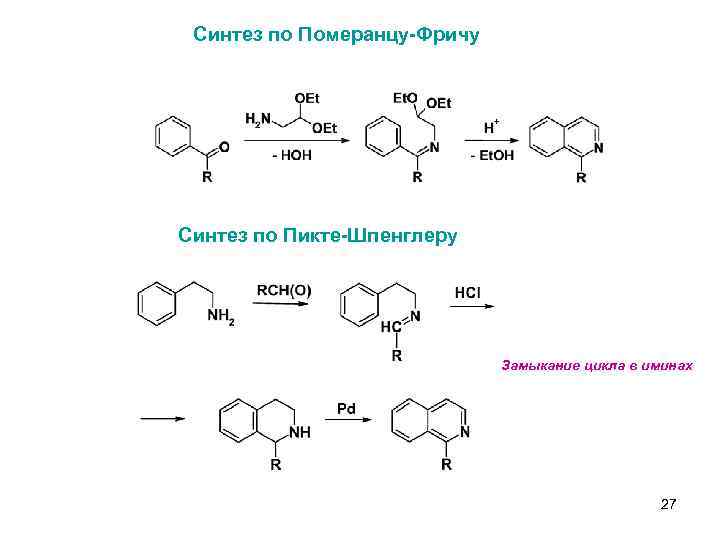
Синтез по Померанцу-Фричу Синтез по Пикте-Шпенглеру Замыкание цикла в иминах 27
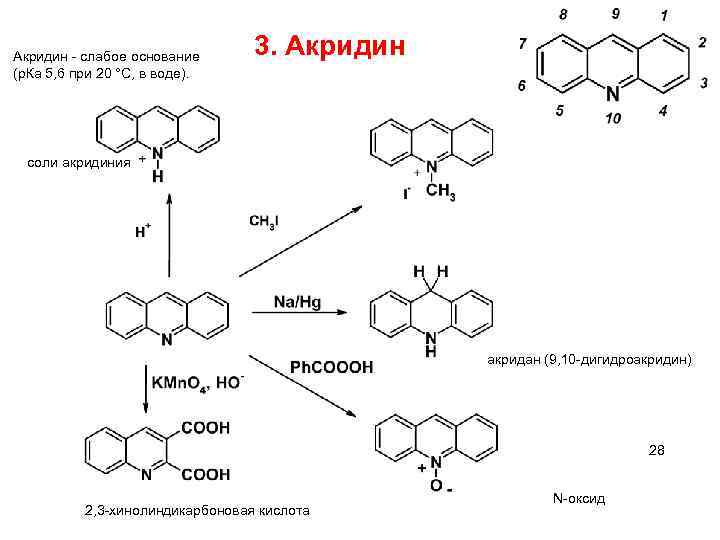
Акридин - слабое основание (р. Ка 5, 6 при 20 °С, в воде). 3. Акридин соли акридиния акридан (9, 10 -дигидроакридин) 28 2, 3 -хинолиндикарбоновая кислота N-оксид
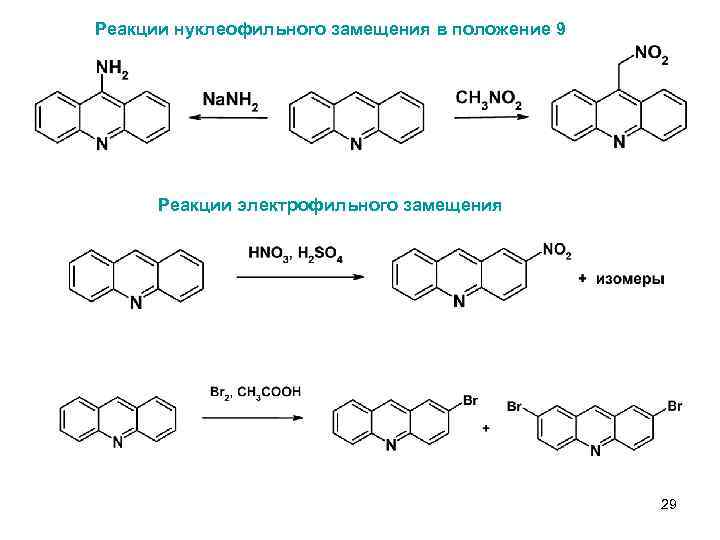
Реакции нуклеофильного замещения в положение 9 5 Реакции электрофильного замещения 29
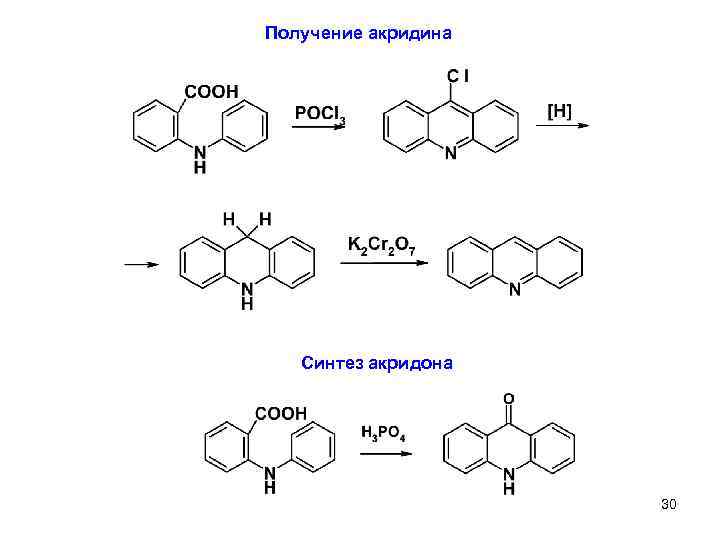
Получение акридина Синтез акридона 30 6

Курс лекций является частью учебно-методического комплекса «Химия биологически активных веществ» автор: • Носова Эмилия Владимировна, д. х. н. , доцент кафедры органической и биомолекулярной химии Ур. ФУ Учебно-методический комплекс подготовлен на кафедре органической химии химико-технологического института Ур. ФУ Никакая часть презентации не может быть воспроизведена в какой бы то ни было форме без письменного разрешения авторов 31 18
2016_HetБАВ_6.ppt