МИКРА 7.ppt
- Количество слайдов: 42

ХИМИОТЕРАПИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ

КРАТКАЯ ИСТОРИЧЕСКАЯ СПРАВКА 1. 1890 г. - Д. Л. Романовский указал, что для каждой инфекции должно быть найдено «вещество, которое при введении в заболевший организм окажет наименьший вред последнему и вызовет наибольшее деструктивное действие в патогенном агенте» . 2. Конец XIX века – открытия Пауля Эрлиха – начало истории современной антимикробной терапии. а) открытие способности анилиновых красителей убивать трипаносомы, б) успех применения производного мышьяка (сальварсан) при лечении сифилиса, в) постулат о «волшебной пуле» – веществе с минимальной органотропностью и максимальной паразитотропностью. 3. 1928 г. – А. Флеминг открыл пенициллин. 4. 1932 г. – Г. Домагк синтезировал «пронтозил» или «красный стрептоцид» . 5. 1940 г. - Х. Флори и Э. Чейн получили чистый пенициллин. 6. 1942 г. - З. В. Ермольева получила первый отечественный пенициллин (крустозин). 7. 1944 г. - З. Ваксман открыл стрептомицин.

ПРИНЦИПЫ ХИМИОТЕРАПИИ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ 1. ПРИНЦИП ФИЗИОЛОГИЧЕСКОЙ ИМИТАЦИИ - действие любого препарата на патоген обусловлено соответствием конфигурации молекул этого вещества или его частей с конфигурацией молекул соединений, участвующих в физиологической регуляции процессов, специфичных для возбудителя. 2. ВЫСОКАЯ ЭФФЕКТИВНОСТЬ - спектр активности , достигаемая концентрация, терапевтический индекс. 3. СООТВЕТСТВУЮЩИЙ АНТИМИКРОБНЫЙ ЭФФЕКТ

Критерии эффективности химиотерапии • Терапевтический индекс — частное от деления минимальной токсической дозы соединения на минимальную дозу, проявляющую антимикробную активность. Более высокие значения терапевтического индекса соответствуют большей эффективности препарата. • Достижимая концентрация в сыворотке крови зависит от массы тела пациента, дозы препарата, пути и схемы введения, а также скорости его выведения из организма. В настоящее время этот критерий не считают абсолютным, так как содержание ряда препаратов в тканях может намного превышать их концентрацию в сыворотке крови.

По механизму действия антибиотики разделяют на три основные группы: • ингибиторы синтеза клеточной стенки микроорганизма (пенициллины, цефалоспорины, ванкомицин, тейкопланин и др. ); • антибиотики, нарушающие молекулярную организацию, функции клеточных мембран (полимиксин, нистатин, леворин, амфотерицин и др. ); • антибиотики, подавляющие синтез белка и нуклеиновых кислот, в частности, ингибиторы синтеза белка на уровне рибосом (хлорамфеникол, тетрациклины, макролиды, линкомицин, аминогликозиды) и ингибиторы РНК-полимеразы (рифампицин) и др.

По спектру противомикробного действия антибиотики разделяют на группы: • 1) Препараты, действующие преимущественно на грамположительные и грамотрицательные кокки (стафилококки, стрептококки, менингококки, гонококки), некоторые грамположительные палочки (коринебактерии, клостридии). К этим препаратам относятся бензилпенициллин, бициллины, феноксиметилпенициллин, пенициллиназоустойчивые пенициллины (оксациллин, метициллин), цефалоспорины 1 -го поколения, макролиды, ванкомицин, линкомицин. • 2) Антибиотики широкого спектра действия, активные в отношении грамположительных и грамотрицательных палочек: хлорамфеникол, тетрациклины, аминогликозиды, полусинтетические пенициллины широкого спектра действия (ампициллин, азлоциллин и др. ) и цефалоспорины 2 -го поколения. • 3) Антибиотики с преимущественной активностью в отношении грамотрицательных палочек (полимиксины, цефалоспорины 3 -го поколения). • 4) Противотуберкулезные антибиотики (стрептомицин, рифампицин, флоримицин). • 5) Противогрибковые антимикотики (нистатин, леворин, гризеофульвин, амфотерицин В, кетоконазол, анкотил, дифлюкан и др. ).

• Минимальная бактерицидная концентрация (МБК) Наименьшая концентрация антибиотика, которая при исследовании in vitro вызывает гибель 99, 9% микроорганизмов от исходного уровня в течение определенного периода времени, бактерицидные (МБК) в отношении популяции микроорганизмов в целом. Измеряется в мкг/мл или мг/л. • Минимальная подавляющая концентрация (МПК) Наименьшая концентрация антибиотика, способная подавить видимый рост микроорганизма in vitro. Измеряется в мкг/мл или мг/л. • МПК 50 Минимальная подавляющая концентрация антибиотика для 50% исследованных штаммов. Измеряется в мкг/мл или мг/л. • МПК 90 Минимальная подавляющая концентрация антибиотика для 90% исследованных штаммов. Измеряется в мкг/мл или мг/л.

АНТИБИОТИКИ (anti - против; biosis – жизнь) КЛАССИФИКАЦИЯ 1. Способ получения - Биосинтетические (природные) (их продуцентами выступают специальные штаммы микроорганизмов) - Полусинтетические (химическое соединение природного антибиотика (его «ядра» ), с различными химическими радикалами) - Синтетические (источник получения – химический синтез) 2. Тип продуцента - Грибы (пенициллин, гризеофульвин, цефалоспорины) - Актиномицеты (стрептомицин, эритромицин) - Бактерии (полимиксин) 3. Механизм действия Подавляют - синтез компонентов клеточной стенки, функции ЦПМ, синтез белка, транскрипцию и синтез нуклеиновых кислот.
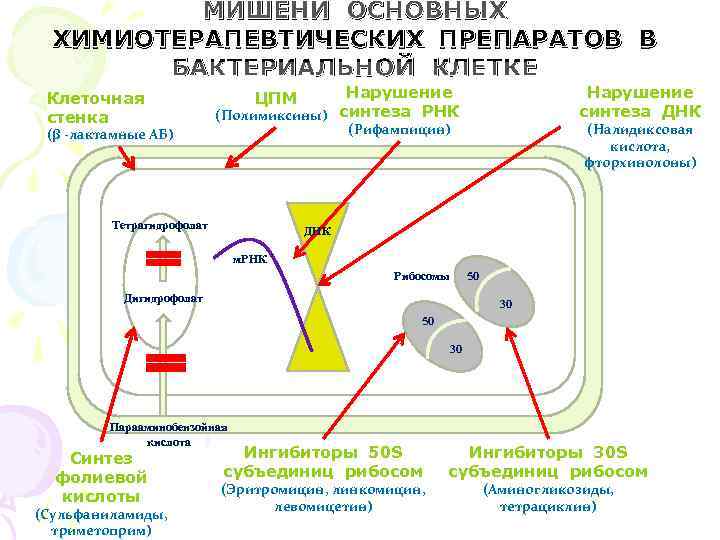
МИШЕНИ ОСНОВНЫХ ХИМИОТЕРАПЕВТИЧЕСКИХ ПРЕПАРАТОВ В БАКТЕРИАЛЬНОЙ КЛЕТКЕ Клеточная ЦПМ Нарушение Нарушение стенка (Полимиксины) синтеза РНК синтеза ДНК (β -лактамные АБ) (Рифампицин) (Налидиксовая кислота, фторхинолоны) Тетрагидрофолат ДНК м. РНК Рибосомы 50 Дигидрофолат 30 50 30 Парааминобензойная кислота Синтез Ингибиторы 50 S Ингибиторы 30 S фолиевой субъединиц рибосом (Эритромицин, линкомицин, (Аминогликозиды, кислоты левомицетин) тетрациклин) (Сульфаниламиды, триметоприм)

ИНГИБИТОРЫ СИНТЕЗА КОМПОНЕНТОВ КЛЕТОЧНОЙ СТЕНКИ Влияют на синтез пептидогликана клеточной стенки бактерий. 1. β – Лактамные антибиотики 2. Бацитрацины 3. Ванкомицин
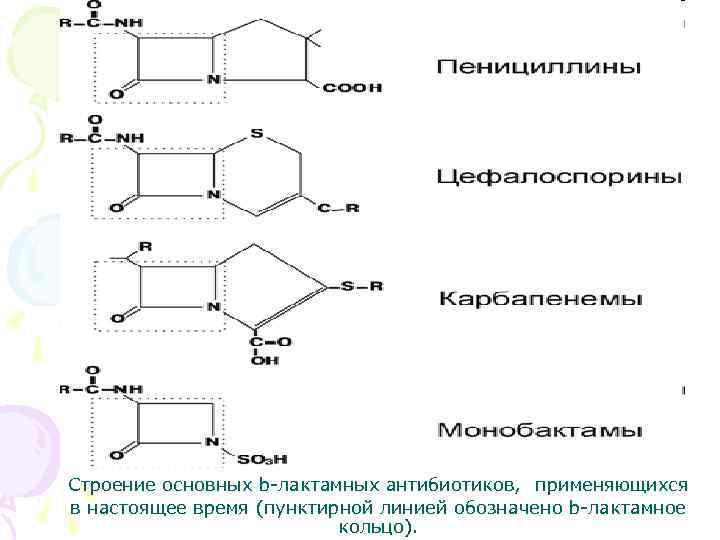
Строение основных b-лактамных антибиотиков, применяющихся в настоящее время (пунктирной линией обозначено b-лактамное кольцо).
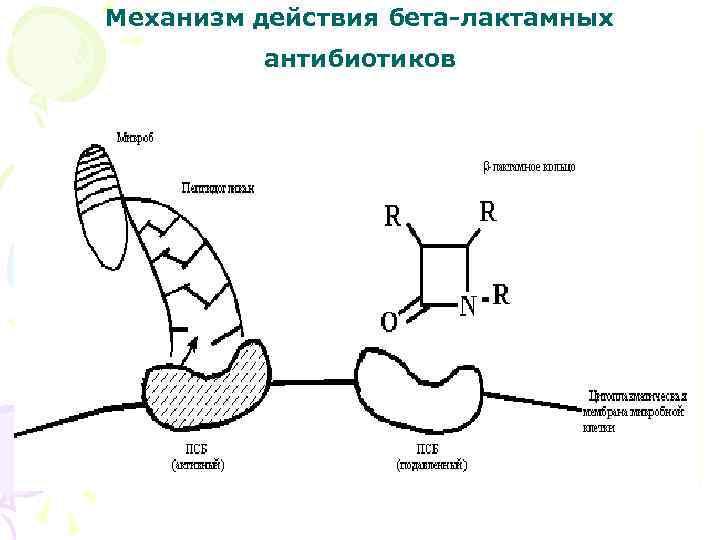
Механизм действия бета-лактамных антибиотиков

Индивидуальные свойства отдельных БЛА • аффинность к ПСБ, (сродство к пенициллинсвязывающим белкам (ферментам) микроба) • способностью проникать через внешние структуры микроорганизмов • устойчивостью к гидролизу бета-лактамазами.

Механизмы приобретенной резистентности к БЛА • Снижение аффинности ПСБ к антибиотикам. • Снижение проницаемости внешних структур микроорганизма. • Появление новых бета-лактамаз или изменение характера экспрессии имеющихся.

К практически важным свойствам бета-лактамаз относятся: • Субстратный профиль (способность к преимущественному гидролизу тех или иных БЛА, например пенициллинов или цефалоспоринов или тех и других в равной степени). • Локализация кодирующих генов (плазмидная или хромосомная). При плазмидной локализации генов происходит быстрое внутри- и межвидовое распространение резистентности, при хромосомной наблюдают распространение резистентного клона. • Тип экспрессии (конститутивный или индуцибельный). При конститутивном типе микроорганизмы синтезируют бета-лактамазы с постоянной скоростью, при индуцибельном количество синтезируемого фермента резко возрастает после контакта с антибиотиком (индукции). • Чувствительность к ингибиторам. К ингибиторам относятся вещества бета-лактамной природы, обладающие минимальной антибактериальной активностью, но способные необратимо связываться с бета-лактамазами и, таким образом, ингибировать их активность (суицидное ингибирование). В результате при одновременном применении БЛА и ингибиторов бета-лактамаз последние защищают антибиотики от гидролиза.

Характеристика основных бета-лактамаз Ферменты Характеристика Стафилококковые бета-лактамазы, Гидролизуют природные и полусинтетические плазмидные, класс А пенициллины, кроме метициллина и оксациллина. Чувствительны к ингибиторам. Плазмидные бета-лактамазы Гидролизуют природные и полусинтетические грамоотрицательных бактерий широкого пенициллины, цефалоспорины I поколения. спектра, класс А Чувствительны к ингибиторам. Плазмидные бета-лактамазы Гидролизуют природные и полусинтетические грамоотрицательных бактерий расширенного пенициллины, цефалоспорины I - IV спектра, класс А поколений. Чувствительны к ингибиторам. Хромосомные бета-лактамазы Гидролизуют природные и полусинтетические грамоотрицательных бактерий, класс С пенициллины, цефалоспорины I - III поколений. Хромосомные бета-лактамазы Гидролизуют природные и полусинтетические грамоотрицательных бактерий, класс А пенициллины цефалоспорины I - II поколений. Чувствительны к ингибиторам. Хромосомные бета-лактамазы Эффективно гидролизуют практически все грамоотрицательных бактерий, класс В бета-лактамы, включая карбапенемы. Не чувствительны к ингибиторам.
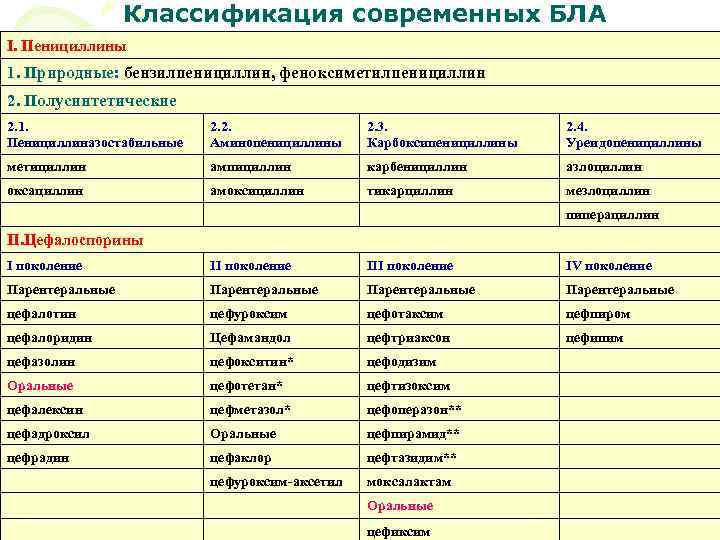
Классификация современных БЛА I. Пенициллины 1. Природные: бензилпенициллин, феноксиметилпенициллин 2. Полусинтетические 2. 1. 2. 2. 3. 2. 4. Пенициллиназостабильные Аминопенициллины Карбоксипенициллины Уреидопенициллины метициллин ампициллин карбенициллин азлоциллин оксациллин амоксициллин тикарциллин мезлоциллин пиперациллин II. Цефалоспорины I поколение II поколение IV поколение Парентеральные цефалотин цефуроксим цефотаксим цефпиром цефалоридин Цефамандол цефтриаксон цефипим цефазолин цефокситин* цефодизим Оральные цефотетан* цефтизоксим цефалексин цефметазол* цефоперазон** цефадроксил Оральные цефпирамид** цефрадин цефаклор цефтазидим** цефуроксим-аксетил моксалактам Оральные цефиксим
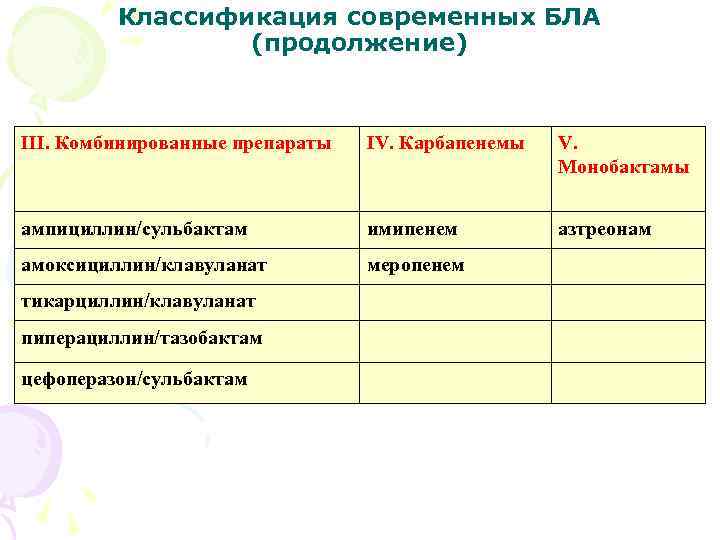
Классификация современных БЛА (продолжение) III. Комбинированные препараты IV. Карбапенемы V. Монобактамы ампициллин/сульбактам имипенем азтреонам амоксициллин/клавуланат меропенем тикарциллин/клавуланат пиперациллин/тазобактам цефоперазон/сульбактам

ПЕНИЦИЛЛИНЫ Самая низкая токсичность в ряду антибиотиков. 1. Биосинтетические пенициллины Бензилпенициллин, феноксиметилпенициллин Оказывают действие на грам+ и ограниченное число грам- бактерий. Инактивируются бактериальными β -лактамазами (пенициллиназами). 2. Полусинтетические пенициллины I поколение (оксациллин, клоксациллин, флуксоциллин и др. ) Узкий спектр действия (грам+). II и III поколения (ампициллин, амоксициллин, азлоциллин, пиперациллин и др. ) Широкий спектр, но инактивируются β - лактамазами. 3. Потенцированные антибиотики Содержат дополнительное β -лактамное кольцо, что защищает молекулу антибиотика от инактивации ферментами бактерий. (Клавулановая кислота, сульбактам)

Цефалоспорины Занимают первое место среди всех антимикробных препаратов по частоте применения. Популярность этих антибиотиков объясняется наличием у них многих положительных качеств, в их числе: • широкий спектр антимикробного действия с учетом всех препаратов этого класса, охватывающий практически все микроорганизмы, за исключением энтерококков, хламидий и микоплазм; • бактерицидный механизм действия; • устойчивость к бета-лактамазам стафилококков у препаратов I и II поколений и грамотрицательных бактерий у препаратов III и IV поколений; • хорошая переносимость и небольшая частота побочных проявлений; • простота и удобство дозирования.

ЦЕФАЛОСПОРИНЫ 1. I поколение Цефазолин, цефалексин и др. 2. II поколение Цефуроксим, цефамандол и др. 3. III поколение Цефотаксим, цефтриаксон, цефоперазон, цефтазидим и др. 4. IV поколение Цефепим, цефпиром

МОНОБАКТАМЫ И КАРБАПЕНЕМЫ 1. Монобактамы Азтреонам Устойчивы к β -лактамазам и активны в отношении узкого спектра грам- бактерий ( Pseudomonas, Serratia), проявляющих множественную антибиотикорезистентность. 2. Карбапенемы Имипенем Самый широкий спектр действия среди всех β- лактамных антибиотиков.

Классификация хинолонов I поколение: • Налидиксовая кислота • Оксолиновая кислота • Пипемидовая (пипемидиевая) кислота II поколение: • Ломефлоксацин • Норфлоксацин • Офлоксацин • Пефлоксацин • Ципрофлоксацин III поколение: • Левофлоксацин • Спарфлоксацин IV поколение: • Моксифлоксацин
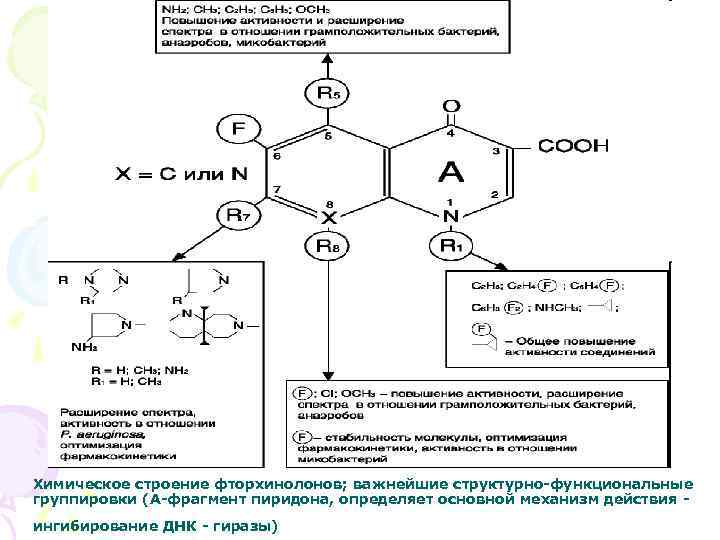
Химическое строение фторхинолонов; важнейшие структурно-функциональные группировки (А-фрагмент пиридона, определяет основной механизм действия - ингибирование ДНК - гиразы)

АМИНОГЛИКОЗИДЫ I поколение Стрептомицин, канамицин и др. II поколение Гентамицин, сизомицин, тобромицин III поколение Амикацин Быстрое достижение бактериоцидного эффекта, показаны при резистентности к другим препаратам

ТЕТРАЦИКЛИНЫ, ХЛОРАМФЕНИКОЛ 1. Биосинтетические Окситетрациклин, тетрациклин (вытеснены полусинтетическими) 2. Полусинтетические Доксициклин, миноциклин Активны в отношении грам+ и грам- бактерий, а также микоплазм и внутриклеточных паразитов. Имеют большое значение в качестве средств лечения холеры, туляремии, бруцеллёза. ХЛОРАМФЕНИКОЛ (левомицетин) Препарат действует на многие грам+ и грам- бактерий, внутриклеточных паразитов. Эффективен в отношении грамотрицательных анаэробов.
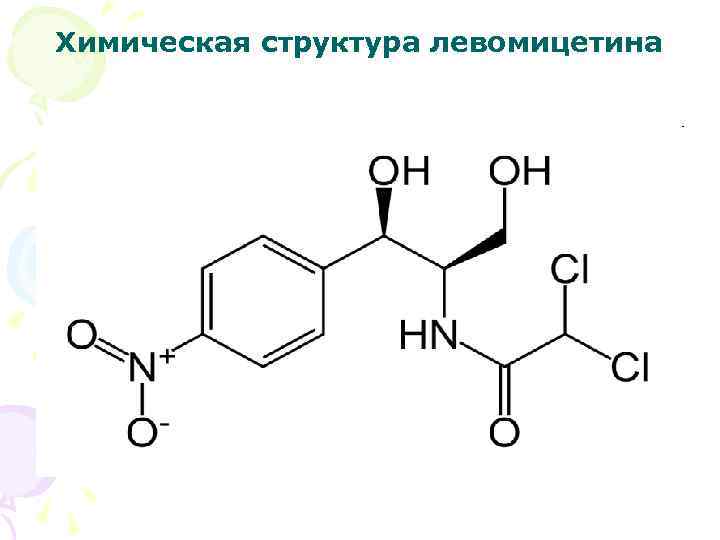
Химическая структура левомицетина

ПОЛИМИКСИНЫ, ПОЛИЕНОВЫЕ АНТИБИОТИКИ, ГРАМИЦИДИНЫ 1. Полимиксины Полимиксин В и Е (колистин) Препараты токсичны, применяют местно. Действуют на грам - (бактерицидный эффект) флору (протеи, клебсиеллы, эшерихии, псевдомонады и др. ) 2. Полиеновые антибиотики Нистатин, леворин и амфотерицин В Самый широкий спектр действия среди всех β-лактамных антибиотиков. 3. Грамицидины Бактериостатические препараты, применение ограничено.

МАКРОЛИДЫ, АЗАЛИДЫ Спектр действия несколько шире, чем у бензилпенициллина. 1. Биосинтетические Эритромицин, олеандомицин, спирамицин 2. Полусинтетические Рокситромицин, кларитромицин Активны в отношении пенициллин- и тетрациклинрезистентных штаммов бактерий, а также внутриклеточных паразитов – риккетсий, хламидий и др. АЗАЛИДЫ Азитромицин Механизм активности аналогичен макролидам, депонируется в фагоцитах.
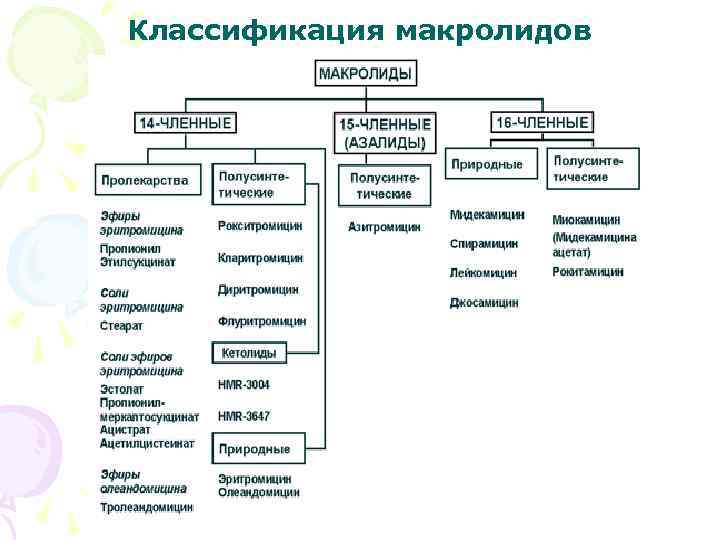
Классификация макролидов

ИНГИБИТОРЫ ФУНКЦИИ ЦИТОПЛАЗМАТИЧЕСКОЙ МЕМБРАНЫ Нарушают проницаемость ЦПМ, приводят к активному выходу белков из бактериальной клетки. 1. Полимиксины 2. Полиеновые антибиотики 3. Грамицидины

ИНГИБИТОРЫ СИНТЕЗА БЕЛКА Подавляют синтез белка на бактериальных рибосомах. Аминогликозиды 1. Тетрациклины 2. Хлорамфеникол 3. Макролиды 4. Азалиды 5. Линкозамиды

ЛИНКОЗАМИДЫ ЛИНКОМИЦИН синтетический аналог КЛИНДАМИЦИН Спектр антибактериального действия сходен с макролидами, однако все штаммы кишечной палочки устойчивы к препаратам.

ИНГИБИТОРЫ ТРАНСКРИПЦИИ И СИНТЕЗА НУКЛЕИНОВЫХ КИСЛОТ Рифампицин Основное показание к применению – лечение туберкулёза. Устойчивость к рифампицину развивается довольно быстро.
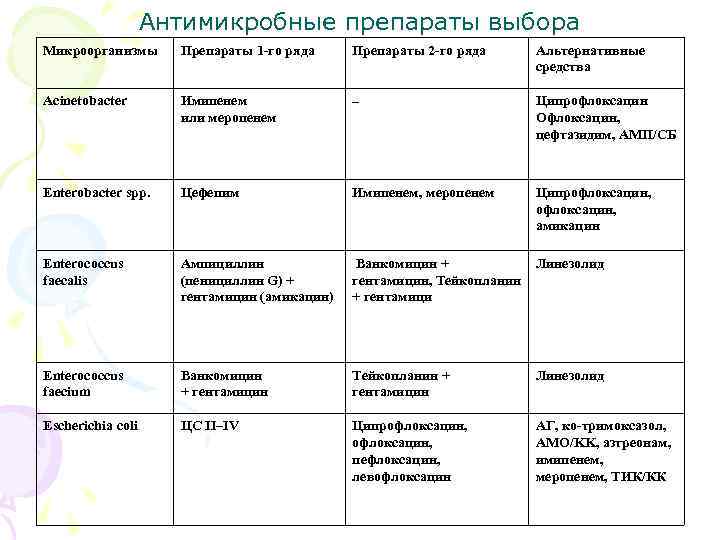
Антимикробные препараты выбора Микроорганизмы Препараты 1 -го ряда Препараты 2 -го ряда Альтернативные средства Acinetobacter Имипенем – Ципрофлоксацин или меропенем Офлоксацин, цефтазидим, АМП/СБ Enterobacter spp. Цефепим Имипенем, меропенем Ципрофлоксацин, амикацин Enterococcus Ампициллин Ванкомицин + Линезолид faecalis (пенициллин G) + гентамицин, Тейкопланин гентамицин (амикацин) + гентамици Enterococcus Ванкомицин Тейкопланин + Линезолид faecium + гентамицин Escherichia coli ЦС II–IV Ципрофлоксацин, АГ, ко-тримоксазол, офлоксацин, АМО/KK, азтреонам, пефлоксацин, имипенем, левофлоксацин меропенем, ТИК/КК
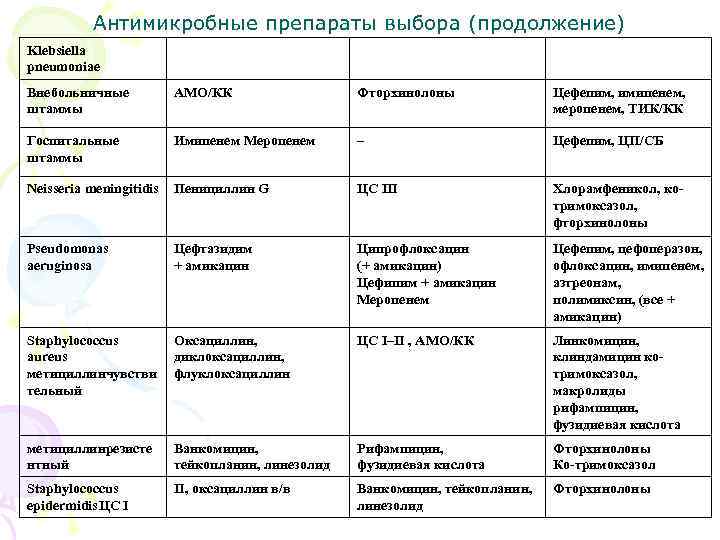
Антимикробные препараты выбора (продолжение) Klebsiella pneumoniae Внебольничные АМО/КК Фторхинолоны Цефепим, имипенем, штаммы меропенем, ТИК/КК Госпитальные Имипенем Меропенем – Цефепим, ЦП/СБ штаммы Neisseria meningitidis Пенициллин G ЦС III Хлорамфеникол, ко- тримоксазол, фторхинолоны Pseudomonas Цефтазидим Ципрофлоксацин Цефепим, цефоперазон, aeruginosa + амикацин (+ амикацин) офлоксацин, имипенем, Цефипим + амикацин азтреонам, Меропенем полимиксин, (все + амикацин) Staphylococcus Оксациллин, ЦС I–II , АМО/КК Линкомицин, aureus диклоксациллин, клиндамицин ко- метициллинчувстви флуклоксациллин тримоксазол, тельный макролиды рифампицин, фузидиевая кислота метициллинрезисте Ванкомицин, Рифампицин, Фторхинолоны нтный тейкопланин, линезолид фузидиевая кислота Ко-тримоксазол Staphylococcus II, оксациллин в/в Ванкомицин, тейкопланин, Фторхинолоны epidermidis. ЦС I линезолид
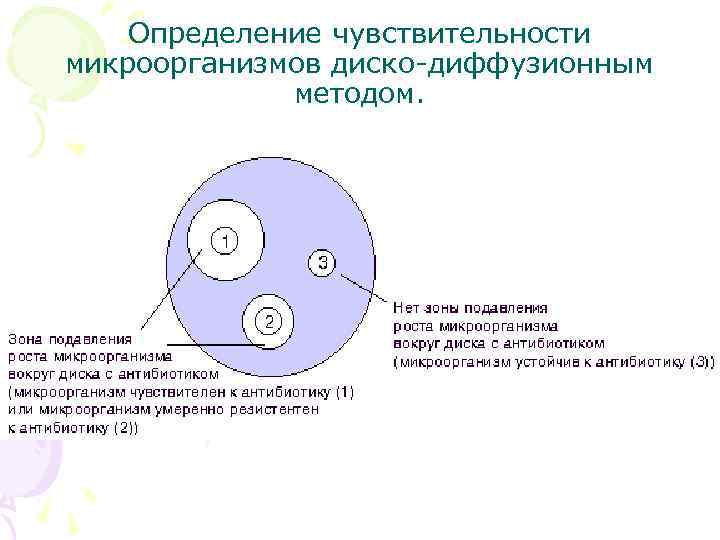
Определение чувствительности микроорганизмов диско-диффузионным методом.
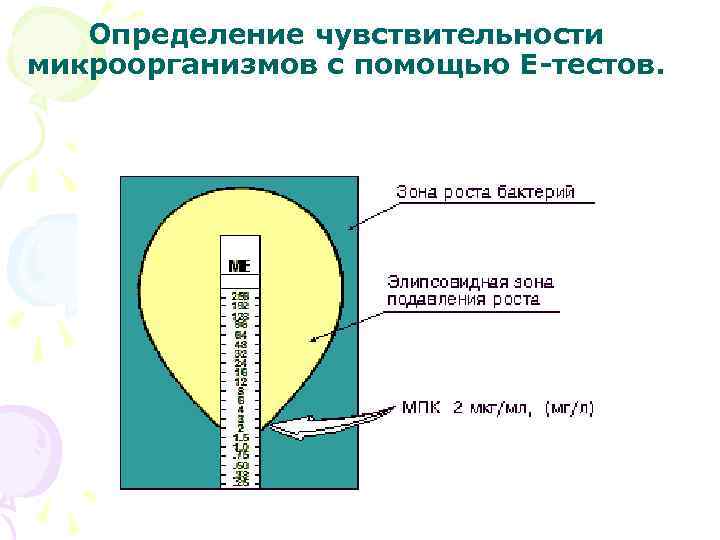
Определение чувствительности микроорганизмов с помощью Е-тестов.
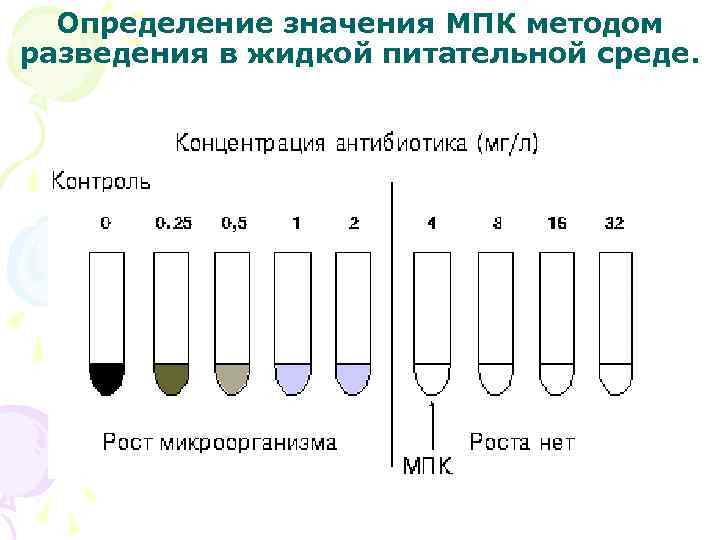
Определение значения МПК методом разведения в жидкой питательной среде.
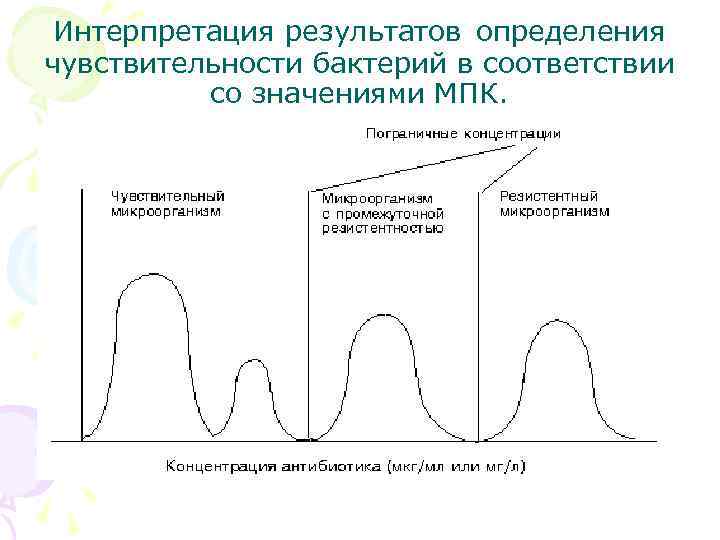
Интерпретация результатов определения чувствительности бактерий в соответствии со значениями МПК.
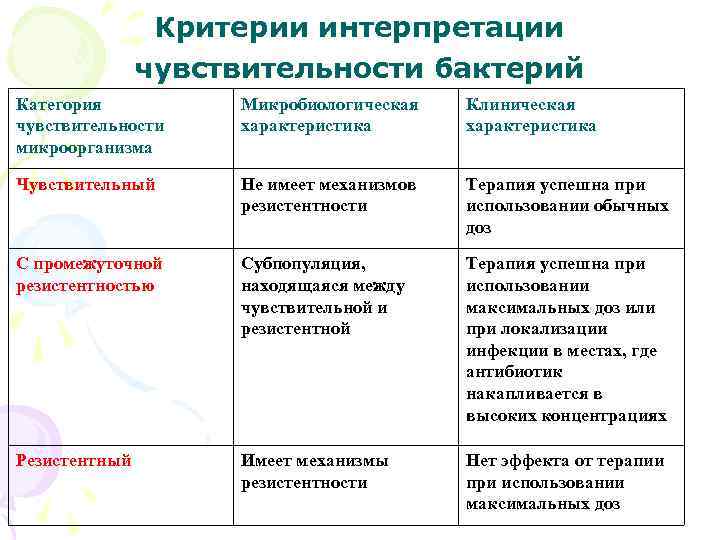
Критерии интерпретации чувствительности бактерий Категория Микробиологическая Клиническая чувствительности характеристика микроорганизма Чувствительный Не имеет механизмов Терапия успешна при резистентности использовании обычных доз С промежуточной Субпопуляция, Терапия успешна при резистентностью находящаяся между использовании чувствительной и максимальных доз или резистентной при локализации инфекции в местах, где антибиотик накапливается в высоких концентрациях Резистентный Имеет механизмы Нет эффекта от терапии резистентности при использовании максимальных доз

Диспенсер дисков с антибиотиками
МИКРА 7.ppt