Химико-токсикологический анализ веществ, изолируемых дистилляцией (перегонкой





























ХТА летучих ядов (вечерники).ppt
- Количество слайдов: 43
 Химико-токсикологический анализ веществ, изолируемых дистилляцией (перегонкой с водяным паром) – «летучих ядов» Петухов Алексей Евгеньевич к. ф. н. , старший преподаватель кафедры фармацевтической и токсикологической химии
Химико-токсикологический анализ веществ, изолируемых дистилляцией (перегонкой с водяным паром) – «летучих ядов» Петухов Алексей Евгеньевич к. ф. н. , старший преподаватель кафедры фармацевтической и токсикологической химии
 Приказ МЗ СССР от 25. 12. 73 г. № 1021 В первый раздел Перечня включены: n синильная кислота; n спирты (метиловый, этиловый, пропиловый, бутиловый и амиловый); n формальдегид; n хлороформ, хлоралгидрат, четыреххлористый углерод, дихлорэтан; n фенол, крезолы. Во второй раздел Перечня включены: этиленгликоль, ацетон, бензол, толуол, ксилол и др.
Приказ МЗ СССР от 25. 12. 73 г. № 1021 В первый раздел Перечня включены: n синильная кислота; n спирты (метиловый, этиловый, пропиловый, бутиловый и амиловый); n формальдегид; n хлороформ, хлоралгидрат, четыреххлористый углерод, дихлорэтан; n фенол, крезолы. Во второй раздел Перечня включены: этиленгликоль, ацетон, бензол, толуол, ксилол и др.
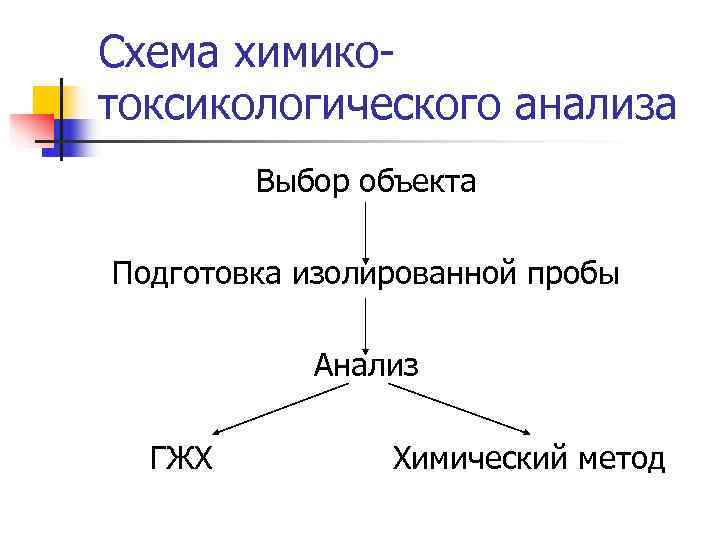
 Схема химико- токсикологического анализа Выбор объекта Подготовка изолированной пробы Анализ ГЖХ Химический метод
Схема химико- токсикологического анализа Выбор объекта Подготовка изолированной пробы Анализ ГЖХ Химический метод
 Объекты исследования Отбор проб регламентирован приказом МЗ РФ от 24. 04. 11 г. № 346 н n. Желудок и кишечник (их содержимое); n Кровь n Легкие n Органы, осуществляющие элиминацию ксенобиотиков (печень, почки) n Селезенку n Мозг n Моча n Жировая ткань
Объекты исследования Отбор проб регламентирован приказом МЗ РФ от 24. 04. 11 г. № 346 н n. Желудок и кишечник (их содержимое); n Кровь n Легкие n Органы, осуществляющие элиминацию ксенобиотиков (печень, почки) n Селезенку n Мозг n Моча n Жировая ткань
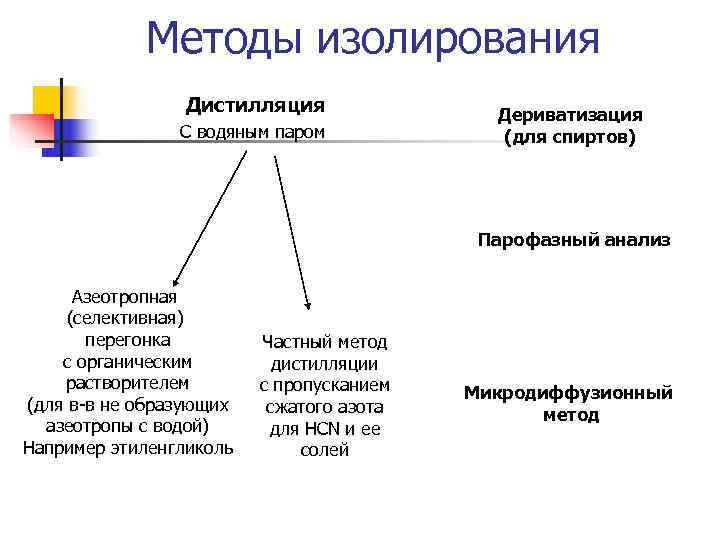
 Методы изолирования Дистилляция Дериватизация С водяным паром (для спиртов) Парофазный анализ Азеотропная (селективная) перегонка Частный метод с органическим дистилляции растворителем с пропусканием Микродиффузионный (для в-в не образующих сжатого азота метод азеотропы с водой) для HCN и ее Например этиленгликоль солей
Методы изолирования Дистилляция Дериватизация С водяным паром (для спиртов) Парофазный анализ Азеотропная (селективная) перегонка Частный метод с органическим дистилляции растворителем с пропусканием Микродиффузионный (для в-в не образующих сжатого азота метод азеотропы с водой) для HCN и ее Например этиленгликоль солей
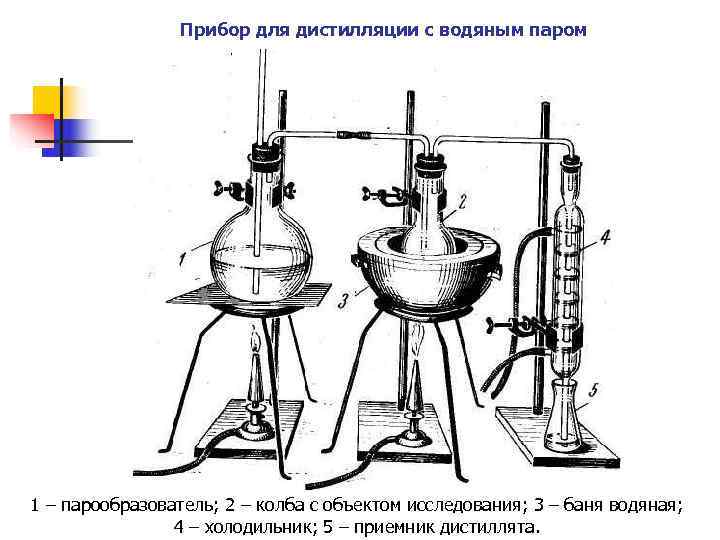
 Прибор для дистилляции с водяным паром 1 – парообразователь; 2 – колба с объектом исследования; 3 – баня водяная; 4 – холодильник; 5 – приемник дистиллята.
Прибор для дистилляции с водяным паром 1 – парообразователь; 2 – колба с объектом исследования; 3 – баня водяная; 4 – холодильник; 5 – приемник дистиллята.
 Перегонка с водяным паром. Схема прибора n Паро-образователь (нагрев на открытом пламени выше 100 о. С) n Колба с анализируемым образцом (нагрев на водяной бане до 60 -70 о. С) n Холодильник n Приемник
Перегонка с водяным паром. Схема прибора n Паро-образователь (нагрев на открытом пламени выше 100 о. С) n Колба с анализируемым образцом (нагрев на водяной бане до 60 -70 о. С) n Холодильник n Приемник
 Схема общего анализа группы веществ, изолируемых перегонкой с водяным паром 100 г биологического материала р. Н 2 -3, щавелевая кислота n 1) 5 мл - первая фракция собирается в приемник с 5 мл 0, 1 н Na. OH n 2) 300 мл – вторая фракция
Схема общего анализа группы веществ, изолируемых перегонкой с водяным паром 100 г биологического материала р. Н 2 -3, щавелевая кислота n 1) 5 мл - первая фракция собирается в приемник с 5 мл 0, 1 н Na. OH n 2) 300 мл – вторая фракция
 Основы метода n В основе метода лежит закон парциальных давлений; n Смеси взаимно нерастворимых жидкостей кипят при температуре более низкой, чем температура кипения каждого из компонентов (азеотроп); n Суммарное давление паров компонентов над системой Р, равное сумме давлений р1 + р2 всегда выше давления пара каждого компонента в отдельности
Основы метода n В основе метода лежит закон парциальных давлений; n Смеси взаимно нерастворимых жидкостей кипят при температуре более низкой, чем температура кипения каждого из компонентов (азеотроп); n Суммарное давление паров компонентов над системой Р, равное сумме давлений р1 + р2 всегда выше давления пара каждого компонента в отдельности
 Основы метода n Давление при котором начинается кипение, достигается при температурах, меньших температур кипения отдельных компонентов; n В отдельных случаях, если вещество с водой не дает азеотропа, в реакционную смесь дополнительно вводят вещество, образующее с токсичным веществом азеотроп (пример – этиленгликоль)
Основы метода n Давление при котором начинается кипение, достигается при температурах, меньших температур кипения отдельных компонентов; n В отдельных случаях, если вещество с водой не дает азеотропа, в реакционную смесь дополнительно вводят вещество, образующее с токсичным веществом азеотроп (пример – этиленгликоль)
 Пример n бензол (Ткип. 80, 2 о. С при 760 мм рт. ст. ) перегоняется с водой (Ткип. 100 о. С при 760 мм рт. ст. ) при температуре 69 о. С. При этом количественное соотношение в дистилляте (в граммах) m 1 M 1 P 1 ------- = ------- , m 2 M 2 P 2 где m 1 и m 2 - массы данных веществ в дистилляте, M 1 и M 2 – их молекулярные массы, P 1 и P 2 – парциальные давления их паров.
Пример n бензол (Ткип. 80, 2 о. С при 760 мм рт. ст. ) перегоняется с водой (Ткип. 100 о. С при 760 мм рт. ст. ) при температуре 69 о. С. При этом количественное соотношение в дистилляте (в граммах) m 1 M 1 P 1 ------- = ------- , m 2 M 2 P 2 где m 1 и m 2 - массы данных веществ в дистилляте, M 1 и M 2 – их молекулярные массы, P 1 и P 2 – парциальные давления их паров.
 Химико-токсикологический анализ синильной кислоты n 1) К 1 мл дистиллята + 1 мл 10% ТХУ + 0, 5 мл бромной воды + 0, 3 мл 0, 5% гидразин сульфата сине-фиолетовый цвет n 2) 2 -3 капли дистиллята высушивают на предметном стекле + 1 к 1% Ag. NO 3 в 50% азотной кислоте, нагрев на пламени горелки, + 1 к 1% метиленовой сини темно-зеленые игольчатые кристаллы n 3) 1 мл дистиллята + 3 к 40% Fe. Cl 3/Fe. Cl 2, нагрев до кипения, охлаждают, + 10% HCl до кислой среды по лакмусовой бумаге берлинская лазурь
Химико-токсикологический анализ синильной кислоты n 1) К 1 мл дистиллята + 1 мл 10% ТХУ + 0, 5 мл бромной воды + 0, 3 мл 0, 5% гидразин сульфата сине-фиолетовый цвет n 2) 2 -3 капли дистиллята высушивают на предметном стекле + 1 к 1% Ag. NO 3 в 50% азотной кислоте, нагрев на пламени горелки, + 1 к 1% метиленовой сини темно-зеленые игольчатые кристаллы n 3) 1 мл дистиллята + 3 к 40% Fe. Cl 3/Fe. Cl 2, нагрев до кипения, охлаждают, + 10% HCl до кислой среды по лакмусовой бумаге берлинская лазурь
 Образование берлинской лазури Na. OH+HCN = Na. CN + H 2 O Fe. SO 4 + 2 Na. CN = Fe(CN)2 + Na 2 SO 4 Fe(CN)2 + Na. CN = Na 4[Fe(CN)6] 3 Na 4[Fe(CN)6] + 2 Fe 2(SO 4)3 = Fe 4[Fe(CN)6]3 + 6 Na 2 SO 4 синее окрашивание Заключение о качественном обнаружении (если синий осадок не выпадает тотчас) или необнаружении HCN дается лишь по истечении 24 -48 час, т. к. при следовых количествах HCN в присутствии органических веществ осадок Берлинской лазури может выпадать медленно. Чувствительность реакции 20 мкг HCN в 1 мл раствора
Образование берлинской лазури Na. OH+HCN = Na. CN + H 2 O Fe. SO 4 + 2 Na. CN = Fe(CN)2 + Na 2 SO 4 Fe(CN)2 + Na. CN = Na 4[Fe(CN)6] 3 Na 4[Fe(CN)6] + 2 Fe 2(SO 4)3 = Fe 4[Fe(CN)6]3 + 6 Na 2 SO 4 синее окрашивание Заключение о качественном обнаружении (если синий осадок не выпадает тотчас) или необнаружении HCN дается лишь по истечении 24 -48 час, т. к. при следовых количествах HCN в присутствии органических веществ осадок Берлинской лазури может выпадать медленно. Чувствительность реакции 20 мкг HCN в 1 мл раствора
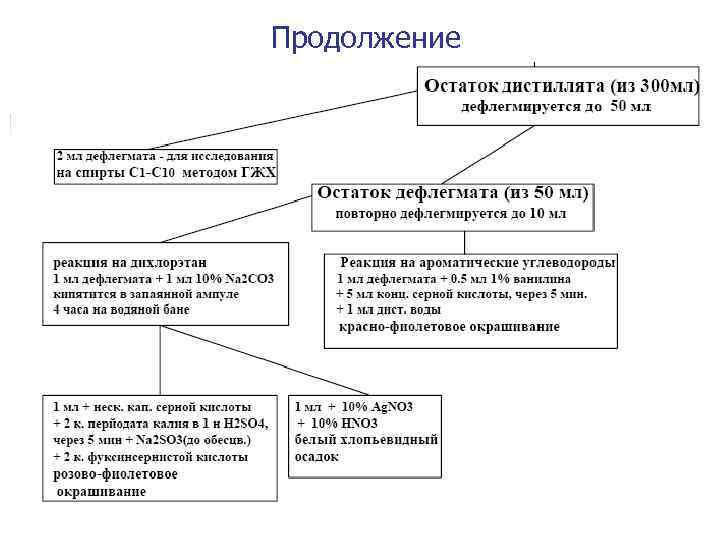
 Продолжение
Продолжение
 Химико-токсикологический анализ хлорсодержащих растворителей (хлороформ, четыреххлористый углерод и т. д. ) Вторая порция дистиллята (300 мл) качественные реакции n Реакция отщепления атома хлора n Реакция образования изонитрила n Реакция с резорцином
Химико-токсикологический анализ хлорсодержащих растворителей (хлороформ, четыреххлористый углерод и т. д. ) Вторая порция дистиллята (300 мл) качественные реакции n Реакция отщепления атома хлора n Реакция образования изонитрила n Реакция с резорцином
 Реакции на органически связанный хлор 1. Общей реакцией на галогенопроизводные является реакция отщепления галоида, что достигается при нагревании части дистиллята со спиртовым раствором Na. OH: + Ag. NO 3 в HNO 3 2. В случае отсутствия осадка или мути проводят реакцию получения изонитрила CHCl 3 + C 6 H 5 NH 2 + 3 KOH C 6 H 5 CN + 3 KCl + 3 H 20 Отрицательный результат этой реакции позволяет судить о ненахождении в исследуемом объекте галогенорганических веществ.
Реакции на органически связанный хлор 1. Общей реакцией на галогенопроизводные является реакция отщепления галоида, что достигается при нагревании части дистиллята со спиртовым раствором Na. OH: + Ag. NO 3 в HNO 3 2. В случае отсутствия осадка или мути проводят реакцию получения изонитрила CHCl 3 + C 6 H 5 NH 2 + 3 KOH C 6 H 5 CN + 3 KCl + 3 H 20 Отрицательный результат этой реакции позволяет судить о ненахождении в исследуемом объекте галогенорганических веществ.
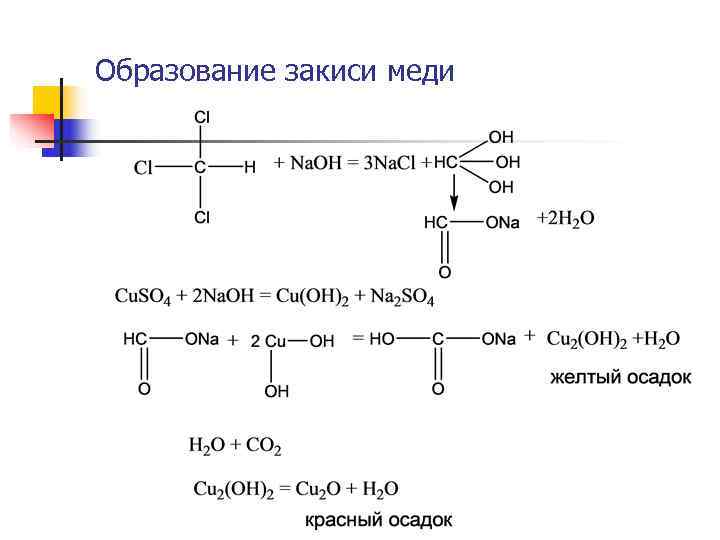
 Продолжение 3. Реакция дистиллята с 1% свежеприготовленным р-ром резорцина (м -диоксибензол) в 10% р-ре Na. OH при нагревании: Появление розового (красного) окрашивания может указывать на наличие Хлороформа, 4 -хлористого углерода, хлоралгидрата. 4. При значительных количествах ССl 3 и хлоралгидрата проводят реакцию восстановления Cu(OH)2 в Cu 2(OH), пере ходящую далее в Cu 2 O при кипячении с р-ром Феллинга. При наличии хлороформа, хлоралгидрата и летучих с водяным паром альдегидов (формальдегид, уксусный альдегид) образуется желтый осадок гидрата закиси меди, переходящий Почти тотчас в красный осадок закиси меди. Альдегиды исключаются в ходе анализа соответствующими реакциями.
Продолжение 3. Реакция дистиллята с 1% свежеприготовленным р-ром резорцина (м -диоксибензол) в 10% р-ре Na. OH при нагревании: Появление розового (красного) окрашивания может указывать на наличие Хлороформа, 4 -хлористого углерода, хлоралгидрата. 4. При значительных количествах ССl 3 и хлоралгидрата проводят реакцию восстановления Cu(OH)2 в Cu 2(OH), пере ходящую далее в Cu 2 O при кипячении с р-ром Феллинга. При наличии хлороформа, хлоралгидрата и летучих с водяным паром альдегидов (формальдегид, уксусный альдегид) образуется желтый осадок гидрата закиси меди, переходящий Почти тотчас в красный осадок закиси меди. Альдегиды исключаются в ходе анализа соответствующими реакциями.
 Образование закиси меди
Образование закиси меди
 Продолжение Для отличия хлоралгидрата от хлороформа используют реакцию с реактивом Несслера: CCl 3 CHO + K 2[Hg. J 4] + 3 KOH Hg + CCl 3 CHOK + 4 KJ + 2 H 2 O При наличии хлоралгидрата в исследуемом растворе образуется кирпично- красный осадок, который затем становится грязно-зеленым Такую же реакцию дают альдегиды и некоторые другие восстанавливающие вещества
Продолжение Для отличия хлоралгидрата от хлороформа используют реакцию с реактивом Несслера: CCl 3 CHO + K 2[Hg. J 4] + 3 KOH Hg + CCl 3 CHOK + 4 KJ + 2 H 2 O При наличии хлоралгидрата в исследуемом растворе образуется кирпично- красный осадок, который затем становится грязно-зеленым Такую же реакцию дают альдегиды и некоторые другие восстанавливающие вещества
 Продолжение Для отличия дихлорэтана от хлороформа и др. используют реакции: 1) образования этиленгликоля и обнаружение его после переведения в формальдегид: При нагревании 1, 2 -дихлорэтана с раствором карбоната натрия в запаянной ампуле образуется этиленгликоль. При взаимодействии этиленгликоля с периодатом калия образуется формальдегид Формальдегид подтверждают реакциями с хромотроповой и фуксинсернистой кислотой Такую же реакцию дают альдегиды и некоторые другие восстанавливающие вещества
Продолжение Для отличия дихлорэтана от хлороформа и др. используют реакции: 1) образования этиленгликоля и обнаружение его после переведения в формальдегид: При нагревании 1, 2 -дихлорэтана с раствором карбоната натрия в запаянной ампуле образуется этиленгликоль. При взаимодействии этиленгликоля с периодатом калия образуется формальдегид Формальдегид подтверждают реакциями с хромотроповой и фуксинсернистой кислотой Такую же реакцию дают альдегиды и некоторые другие восстанавливающие вещества
 Продолжение 2) образования ацетиленида меди: При нагревании 1, 2 -дихлорэтана с раствором гидроксида натрия запаянной ампуле образуется ацетилен, который при взаимодействии с солями меди (I) дает ацетиленид меди, имеющий розовую или вишневую окраску
Продолжение 2) образования ацетиленида меди: При нагревании 1, 2 -дихлорэтана с раствором гидроксида натрия запаянной ампуле образуется ацетилен, который при взаимодействии с солями меди (I) дает ацетиленид меди, имеющий розовую или вишневую окраску
 Химико-токсикологический анализ формальдегида 1. Реакция с резорцином в щелочной среде. Чувствительность - 0, 03 мкг в пробе. Реакция не является специфичной и имеет только отрицательное значение. Белки и продукты их разложения мешают реакции, поэтому ее нельзя проводить (например, для установления факта консервирования формалином) непосредственно с жидкостью, которой залиты внутренние органы трупа. 2. Дистиллят смешивают с 5 -кратным объемом конц. H 2 SO 4. После охлаждения смеси вносят 0, 02 -0, 03 г кодеина (морфина) – сразу или через несколько минут появляется красно- или сине-фиолетовое окрашивание. Чувствительность - 0, 02 мкг в пробе. 3. Дистиллят смешивают с 2 -3 каплями конц. H 2 SO 4 или HCl и р-ром фуксинсернистой кислоты – через несколько минут появляется синее или сине-фиолетовое окрашивание. Чувствительность - 0, 03 мкг в пробе. Реакцию дают все альдегиды. Ацетон также дает сине-фиолетовое окрашивание.
Химико-токсикологический анализ формальдегида 1. Реакция с резорцином в щелочной среде. Чувствительность - 0, 03 мкг в пробе. Реакция не является специфичной и имеет только отрицательное значение. Белки и продукты их разложения мешают реакции, поэтому ее нельзя проводить (например, для установления факта консервирования формалином) непосредственно с жидкостью, которой залиты внутренние органы трупа. 2. Дистиллят смешивают с 5 -кратным объемом конц. H 2 SO 4. После охлаждения смеси вносят 0, 02 -0, 03 г кодеина (морфина) – сразу или через несколько минут появляется красно- или сине-фиолетовое окрашивание. Чувствительность - 0, 02 мкг в пробе. 3. Дистиллят смешивают с 2 -3 каплями конц. H 2 SO 4 или HCl и р-ром фуксинсернистой кислоты – через несколько минут появляется синее или сине-фиолетовое окрашивание. Чувствительность - 0, 03 мкг в пробе. Реакцию дают все альдегиды. Ацетон также дает сине-фиолетовое окрашивание.
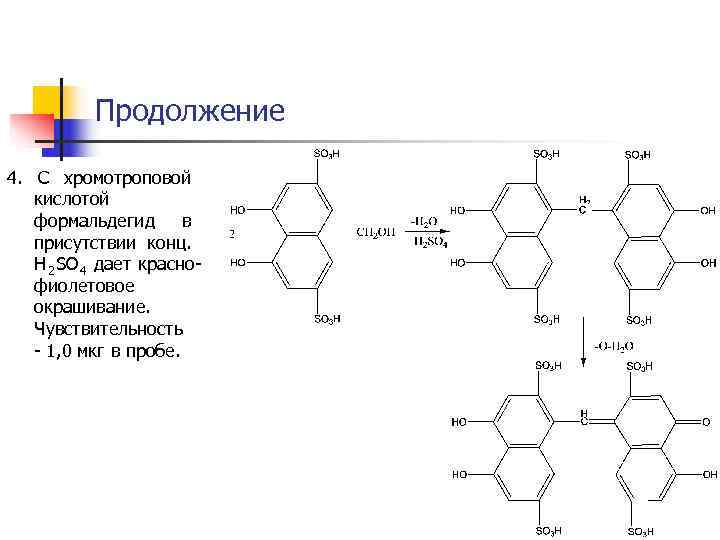
 Продолжение 4. С хромотроповой кислотой формальдегид в присутствии конц. H 2 SO 4 дает красно- фиолетовое окрашивание. Чувствительность - 1, 0 мкг в пробе.
Продолжение 4. С хромотроповой кислотой формальдегид в присутствии конц. H 2 SO 4 дает красно- фиолетовое окрашивание. Чувствительность - 1, 0 мкг в пробе.
 Продолжение 5. При нагревании дистиллята с Ag. NO 3 в аммиачной среде восстанавливается металлическое серебро: Ag. NO 3 + NH 4 OH = Ag. OH + NH 4 NO 3; 2 Ag. OH = Ag 2 O + H 2 O; Чувствительность – 0, 02 мкг в пробе. Заключение о нахождении формальдегида в биоматериале дается, как правило, при условии получения положительных результатов второй и третьей реакций.
Продолжение 5. При нагревании дистиллята с Ag. NO 3 в аммиачной среде восстанавливается металлическое серебро: Ag. NO 3 + NH 4 OH = Ag. OH + NH 4 NO 3; 2 Ag. OH = Ag 2 O + H 2 O; Чувствительность – 0, 02 мкг в пробе. Заключение о нахождении формальдегида в биоматериале дается, как правило, при условии получения положительных результатов второй и третьей реакций.
 Химико-токсикологический анализ ацетона 1. 1 мл дистиллята или исследуемой жидкости с несколькими каплями 1% свежеприготовленного нитропруссида натрия [Na 2 Fe(CN) 5 NO] • 2 H 2 O дает оранжево-красное окрашивание, переходящее при добавлении CH 3 COOH до кислой реакции в красно- фиолетовой или вишнево-красное окрашивание. 2. С р-ром йода в KI в присутствии 10% водного р-ра NH 4 OH образуется йодоформ (характерный запах) и выпадает желтый кристаллический осадок. Чувствительность реакции – 0, 1 мг/мл.
Химико-токсикологический анализ ацетона 1. 1 мл дистиллята или исследуемой жидкости с несколькими каплями 1% свежеприготовленного нитропруссида натрия [Na 2 Fe(CN) 5 NO] • 2 H 2 O дает оранжево-красное окрашивание, переходящее при добавлении CH 3 COOH до кислой реакции в красно- фиолетовой или вишнево-красное окрашивание. 2. С р-ром йода в KI в присутствии 10% водного р-ра NH 4 OH образуется йодоформ (характерный запах) и выпадает желтый кристаллический осадок. Чувствительность реакции – 0, 1 мг/мл.
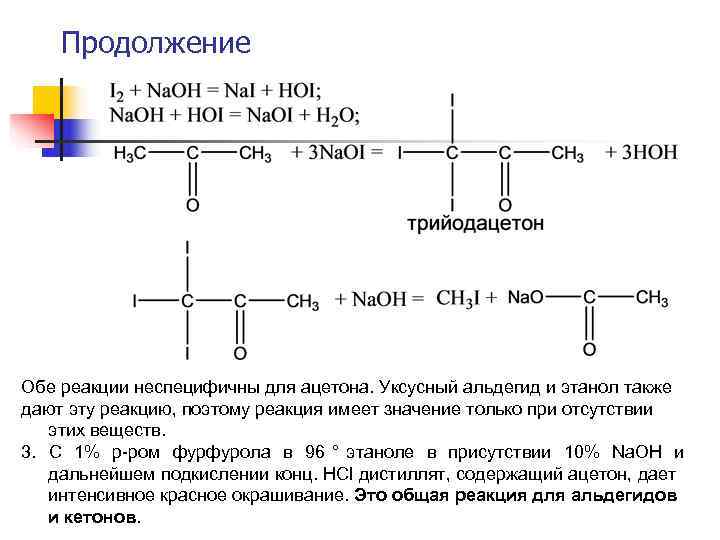
 Продолжение Обе реакции неспецифичны для ацетона. Уксусный альдегид и этанол также дают эту реакцию, поэтому реакция имеет значение только при отсутствии этих веществ. 3. С 1% р-ром фурфурола в 96 ° этаноле в присутствии 10% Na. OH и дальнейшем подкислении конц. HCl дистиллят, содержащий ацетон, дает интенсивное красное окрашивание. Это общая реакция для альдегидов и кетонов.
Продолжение Обе реакции неспецифичны для ацетона. Уксусный альдегид и этанол также дают эту реакцию, поэтому реакция имеет значение только при отсутствии этих веществ. 3. С 1% р-ром фурфурола в 96 ° этаноле в присутствии 10% Na. OH и дальнейшем подкислении конц. HCl дистиллят, содержащий ацетон, дает интенсивное красное окрашивание. Это общая реакция для альдегидов и кетонов.
 Химико-токсикологический анализ метанола Наиболее характерными и чувствительными реакциями доказательства метанола являются реакции, основанные на окислении его в формальдегид. Поэтому необходимо убедиться в отсутствии формальдегида. 1. Окисление метанола в дистилляте проводят 2%р-ром KMn. O 4 в кислой среде (10% H 2 SO 4 ) при охлаждении холодной водой, добиваясь возможно большей полноты окисления метанола до формальдегида. CH 3 OH + 2 KMn. O 4 +3 H 2 SO 4= 5 H 2 CO + 2 Mn. SO 4 + K 2 SO 4 + 8 H 2 O Для уничтожения избытка KMn. O 4 к исследуемой жидкости по каплям прибавляют до обесцвечивания 15% р-р бисульфита натрия или щавелевой кислоты: 2 KMn. O 4 + 5 Na 2 SO 3 + 3 H 2 SO 4= 2 Mn. SO 4+ 5 Na 2 SO 4 + K 2 SO 4 + 3 H 2 O 2 KMn. O 4 + 5 H 2 C 2 O 4 + 3 H 2 SO 4 = 2 Mn. SO 4+ K 2 SO 4 + 10 CO 2 + 8 H 2 O
Химико-токсикологический анализ метанола Наиболее характерными и чувствительными реакциями доказательства метанола являются реакции, основанные на окислении его в формальдегид. Поэтому необходимо убедиться в отсутствии формальдегида. 1. Окисление метанола в дистилляте проводят 2%р-ром KMn. O 4 в кислой среде (10% H 2 SO 4 ) при охлаждении холодной водой, добиваясь возможно большей полноты окисления метанола до формальдегида. CH 3 OH + 2 KMn. O 4 +3 H 2 SO 4= 5 H 2 CO + 2 Mn. SO 4 + K 2 SO 4 + 8 H 2 O Для уничтожения избытка KMn. O 4 к исследуемой жидкости по каплям прибавляют до обесцвечивания 15% р-р бисульфита натрия или щавелевой кислоты: 2 KMn. O 4 + 5 Na 2 SO 3 + 3 H 2 SO 4= 2 Mn. SO 4+ 5 Na 2 SO 4 + K 2 SO 4 + 3 H 2 O 2 KMn. O 4 + 5 H 2 C 2 O 4 + 3 H 2 SO 4 = 2 Mn. SO 4+ K 2 SO 4 + 10 CO 2 + 8 H 2 O
 Продолжение Раствор, содержащий, окисленный до формальдегида, метанол, делят на 2 части и исследуют: А) с р-ром кодеина или морфина в конц. H 2 SO 4 – при наличии H 2 CO появляется красно-фиолетовое (сине-фиолетовое) окрашивание. Б) с р-ром фуксинсернистой кислоты в присутствии 1 мл конц. HCl - появляется синее или сине-фиолетовое окрашивание. Чувствительность реакции – 0, 1 мг в пробе. 2. Реакция образования метилового эфира салициловой кислоты. Характерный запах. Чувствительность реакции – 0, 3 мг в пробе.
Продолжение Раствор, содержащий, окисленный до формальдегида, метанол, делят на 2 части и исследуют: А) с р-ром кодеина или морфина в конц. H 2 SO 4 – при наличии H 2 CO появляется красно-фиолетовое (сине-фиолетовое) окрашивание. Б) с р-ром фуксинсернистой кислоты в присутствии 1 мл конц. HCl - появляется синее или сине-фиолетовое окрашивание. Чувствительность реакции – 0, 1 мг в пробе. 2. Реакция образования метилового эфира салициловой кислоты. Характерный запах. Чувствительность реакции – 0, 3 мг в пробе.
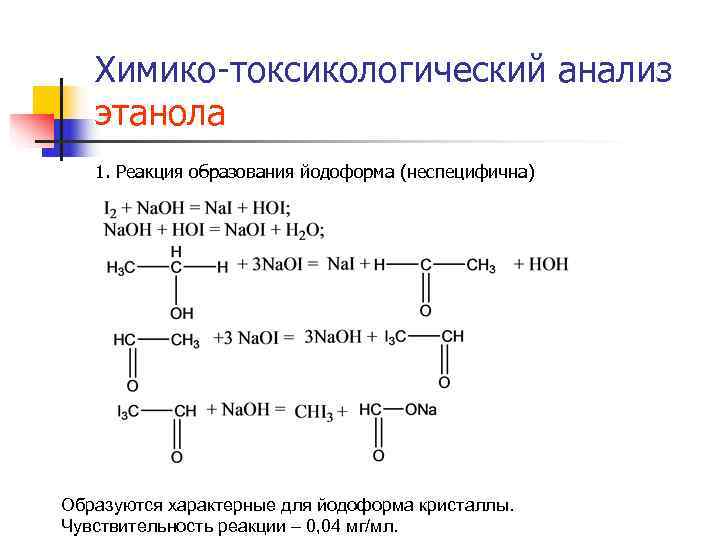
 Химико-токсикологический анализ этанола 1. Реакция образования йодоформа (неспецифична) Образуются характерные для йодоформа кристаллы. Чувствительность реакции – 0, 04 мг/мл.
Химико-токсикологический анализ этанола 1. Реакция образования йодоформа (неспецифична) Образуются характерные для йодоформа кристаллы. Чувствительность реакции – 0, 04 мг/мл.
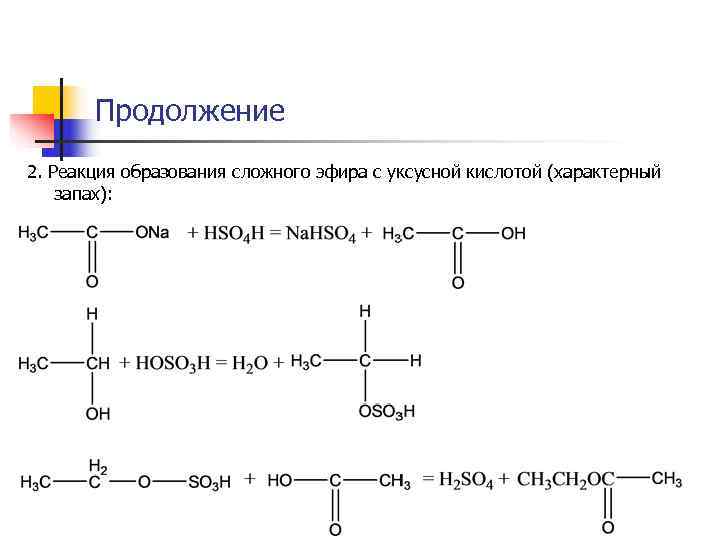
 Продолжение 2. Реакция образования сложного эфира с уксусной кислотой (характерный запах):
Продолжение 2. Реакция образования сложного эфира с уксусной кислотой (характерный запах):
 Продолжение 3. Реакция окисления этанола 5% р-ром бихромата калия в сернокислой среде до уксусного альдегида – специфический запах: Чувствительность реакции не превышает 3 мг в 1 мл дистиллята.
Продолжение 3. Реакция окисления этанола 5% р-ром бихромата калия в сернокислой среде до уксусного альдегида – специфический запах: Чувствительность реакции не превышает 3 мг в 1 мл дистиллята.
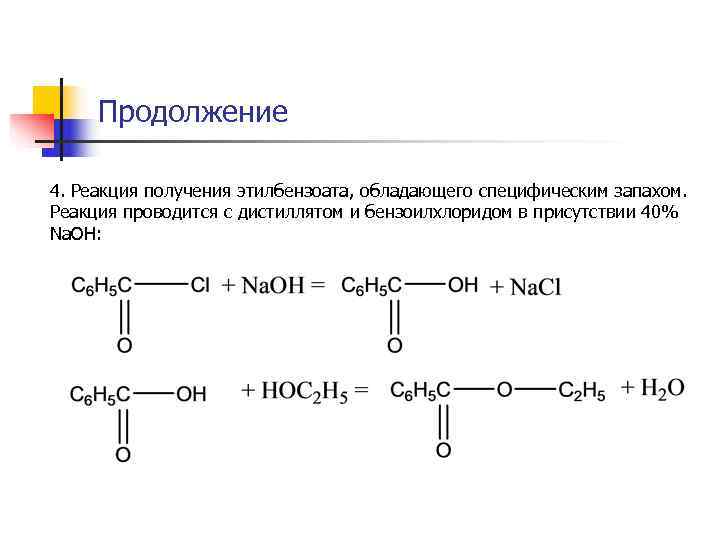
 Продолжение 4. Реакция получения этилбензоата, обладающего специфическим запахом. Реакция проводится с дистиллятом и бензоилхлоридом в присутствии 40% Na. OH:
Продолжение 4. Реакция получения этилбензоата, обладающего специфическим запахом. Реакция проводится с дистиллятом и бензоилхлоридом в присутствии 40% Na. OH:
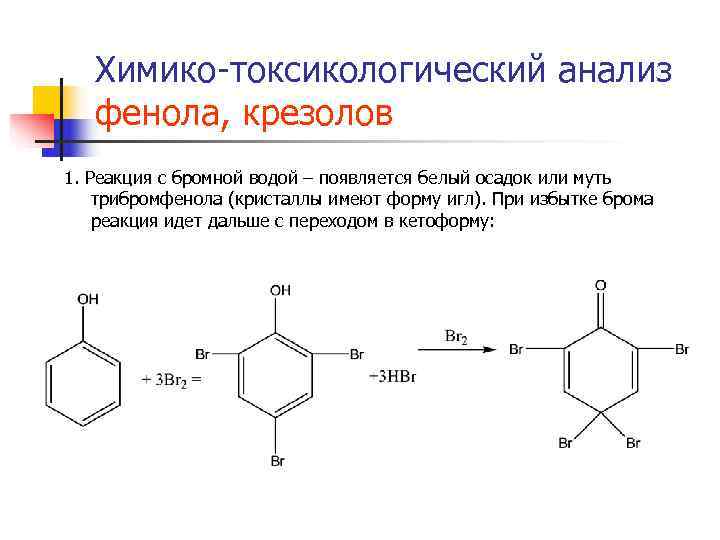
 Химико-токсикологический анализ фенола, крезолов 1. Реакция с бромной водой – появляется белый осадок или муть трибромфенола (кристаллы имеют форму игл). При избытке брома реакция идет дальше с переходом в кетоформу:
Химико-токсикологический анализ фенола, крезолов 1. Реакция с бромной водой – появляется белый осадок или муть трибромфенола (кристаллы имеют форму игл). При избытке брома реакция идет дальше с переходом в кетоформу:
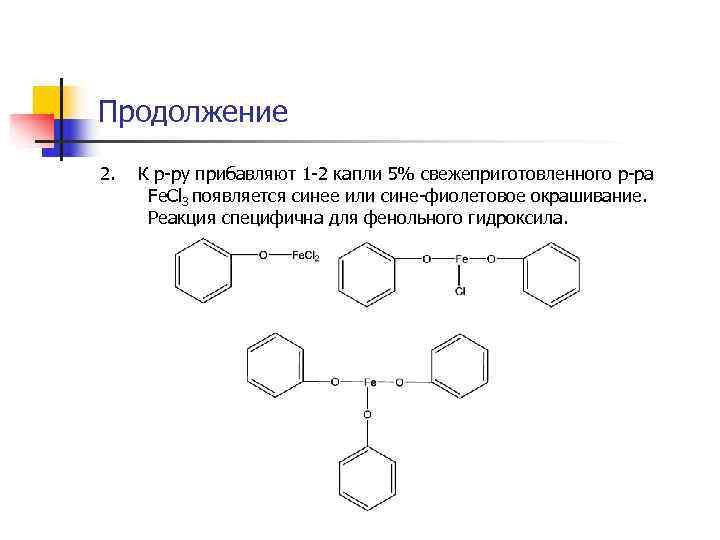
 Продолжение 2. К р-ру прибавляют 1 -2 капли 5% свежеприготовленного р-ра Fe. Cl 3 появляется синее или сине-фиолетовое окрашивание. Реакция специфична для фенольного гидроксила.
Продолжение 2. К р-ру прибавляют 1 -2 капли 5% свежеприготовленного р-ра Fe. Cl 3 появляется синее или сине-фиолетовое окрашивание. Реакция специфична для фенольного гидроксила.
 Химико-токсикологическое значение этиленгликоля (т. кип. 195 о. С – перегонка с бензолом) Метаболизм –летальный синтез 1. Окисление перманганатом калия в щелочной среде до щавелевой кислоты, подкисление и образование оксалатов калия при добавлении хлорида кальция – помутнение 2. С сульфатом меди в щелочной среде – синяя окраска Cu. SO 4 + 2 Na. OH Na 2 SO 4 + Cu(OH)2 HOCH 2 OH + Cu(OH)2 (-OCH 2 O-)Cu + 2 H 2 O 3. Окисление до формальдегида и обнаружение с реакцией фуксинсернистой кислотой– сине-фиолетовое окрашивание HOCH 2 OH + KJO 4 2 HCHO + KJO 3 + H 2 O
Химико-токсикологическое значение этиленгликоля (т. кип. 195 о. С – перегонка с бензолом) Метаболизм –летальный синтез 1. Окисление перманганатом калия в щелочной среде до щавелевой кислоты, подкисление и образование оксалатов калия при добавлении хлорида кальция – помутнение 2. С сульфатом меди в щелочной среде – синяя окраска Cu. SO 4 + 2 Na. OH Na 2 SO 4 + Cu(OH)2 HOCH 2 OH + Cu(OH)2 (-OCH 2 O-)Cu + 2 H 2 O 3. Окисление до формальдегида и обнаружение с реакцией фуксинсернистой кислотой– сине-фиолетовое окрашивание HOCH 2 OH + KJO 4 2 HCHO + KJO 3 + H 2 O
 Химико-токсикологическое значение амилового спирта качественные реакции n С ванилином (или салициловым альдегидом) в кислой среде – красная окраска
Химико-токсикологическое значение амилового спирта качественные реакции n С ванилином (или салициловым альдегидом) в кислой среде – красная окраска
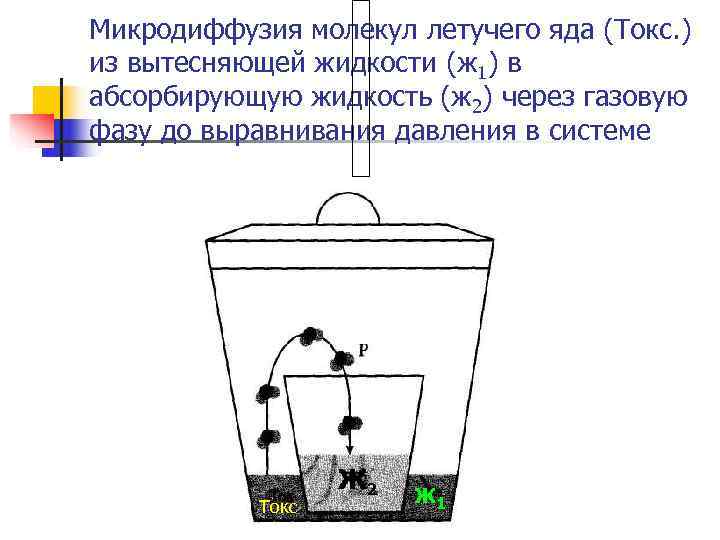
 Микродиффузия молекул летучего яда (Токс. ) из вытесняющей жидкости (ж 1) в абсорбирующую жидкость (ж 2) через газовую фазу до выравнивания давления в системе Ж 2 Токс Ж 1
Микродиффузия молекул летучего яда (Токс. ) из вытесняющей жидкости (ж 1) в абсорбирующую жидкость (ж 2) через газовую фазу до выравнивания давления в системе Ж 2 Токс Ж 1
 Подготовка пробы к ГЖХ анализу n Прямой парофазный анализ n Пробоподготовка, основанная на дериватизации анализируемых соединений
Подготовка пробы к ГЖХ анализу n Прямой парофазный анализ n Пробоподготовка, основанная на дериватизации анализируемых соединений
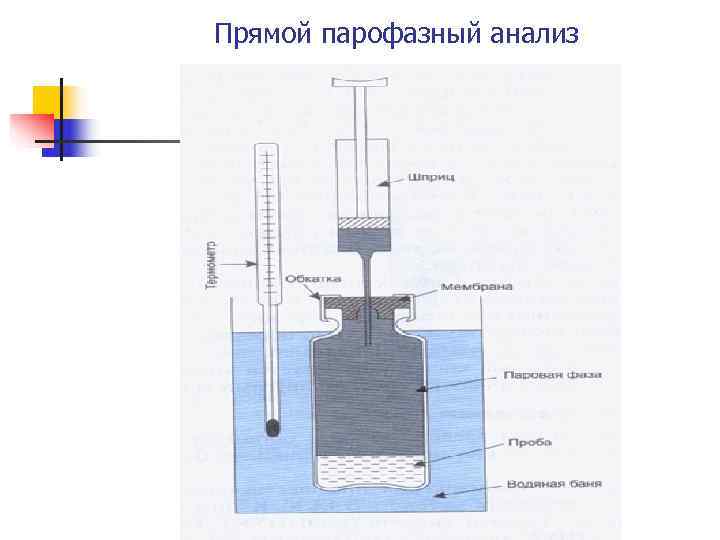
 Прямой парофазный анализ
Прямой парофазный анализ
 Алкилнитрильный метод Качественное и количественное определение С 1 -С 5 спиртов ROH + Na. NO 2 + CCl 3 COOH RONO + CCl 3 COONa + H 2 O
Алкилнитрильный метод Качественное и количественное определение С 1 -С 5 спиртов ROH + Na. NO 2 + CCl 3 COOH RONO + CCl 3 COONa + H 2 O
 Методика n 0, 5 мл 50% трихлоруксусной кислоты n 0, 5 мл дефлегмата n Закрывается пробкой и закатывается n 0, 5 мл 30% нитрита натрия n Взбалтывается и через 1 мин шприцом отбирается 0, 3 мл парогазовой пробы и вводится в испаритель хроматографа
Методика n 0, 5 мл 50% трихлоруксусной кислоты n 0, 5 мл дефлегмата n Закрывается пробкой и закатывается n 0, 5 мл 30% нитрита натрия n Взбалтывается и через 1 мин шприцом отбирается 0, 3 мл парогазовой пробы и вводится в испаритель хроматографа
 Методика n При проведении количественного определения в качестве внутреннего стандарта в пробу добавляется 0, 5 мл 0, 1% н-пропанола
Методика n При проведении количественного определения в качестве внутреннего стандарта в пробу добавляется 0, 5 мл 0, 1% н-пропанола
 Спасибо за внимание!
Спасибо за внимание!

