5.3 Электрохимия Кулонометрия, Кондуктометрия.ppt
- Количество слайдов: 51
 ХИМИКО-АНАЛИТИЧЕСКИЙ КОНТРОЛЬ Электрохимические методы. Электрогравиметрия. Кулонометрия. Кондуктометрия. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 1
ХИМИКО-АНАЛИТИЧЕСКИЙ КОНТРОЛЬ Электрохимические методы. Электрогравиметрия. Кулонометрия. Кондуктометрия. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 1
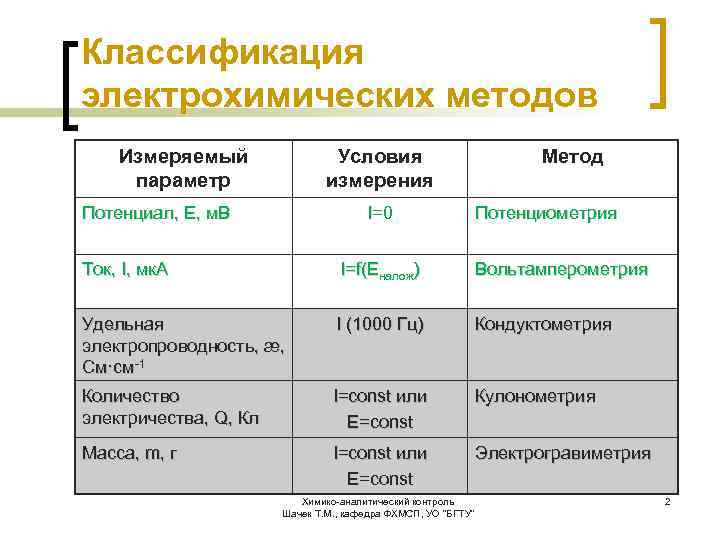 Классификация электрохимических методов Измеряемый параметр Условия измерения Потенциал, Е, м. В I=0 Метод Потенциометрия Ток, I, мк. А I=f(Eналож) Вольтамперометрия Удельная электропроводность, æ, См·см-1 I (1000 Гц) Кондуктометрия Количество электричества, Q, Кл I=const или E=const Кулонометрия Масса, m, г I=const или E=const Электрогравиметрия Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 2
Классификация электрохимических методов Измеряемый параметр Условия измерения Потенциал, Е, м. В I=0 Метод Потенциометрия Ток, I, мк. А I=f(Eналож) Вольтамперометрия Удельная электропроводность, æ, См·см-1 I (1000 Гц) Кондуктометрия Количество электричества, Q, Кл I=const или E=const Кулонометрия Масса, m, г I=const или E=const Электрогравиметрия Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 2
 Электрохимические методы 1. 2. 3. Кулонометрия. Характеристика метода. Применение для контроля качества продукции; Электрогравиметрия. Характеристика метода. Применение для контроля качества продукции; Кондуктометрия. Характеристика метода. Применение для контроля качества продукции. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 3
Электрохимические методы 1. 2. 3. Кулонометрия. Характеристика метода. Применение для контроля качества продукции; Электрогравиметрия. Характеристика метода. Применение для контроля качества продукции; Кондуктометрия. Характеристика метода. Применение для контроля качества продукции. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 3
 Кулонометрия Сущность метода Измерение количества электричества, прошедшего через электролизер при электрохимическом окислении или восстановлении вещества на рабочем электроде Условие: полнота электрохимического превращения определяемого вещества. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 4
Кулонометрия Сущность метода Измерение количества электричества, прошедшего через электролизер при электрохимическом окислении или восстановлении вещества на рабочем электроде Условие: полнота электрохимического превращения определяемого вещества. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 4
 Кулонометрия Объединенный закон Фарадея связывающий в общей форме заряд и массу продукта электролиза Q = I t = (m/M) · z · F Кулон (Кл) – количество электричества, протекающее через поперечное сечение проводника в течение 1 секунды при силе тока 1 А. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 5
Кулонометрия Объединенный закон Фарадея связывающий в общей форме заряд и массу продукта электролиза Q = I t = (m/M) · z · F Кулон (Кл) – количество электричества, протекающее через поперечное сечение проводника в течение 1 секунды при силе тока 1 А. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 5
 Кулонометрия Сущность метода Измерение количества электричества, прошедшего через электролизер при электрохимическом окислении или восстановлении вещества на рабочем электроде Классификация: v Прямая и косвенная кулонометрия; v Потенциостатическая и гальваностатическая кулонометрия. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 6
Кулонометрия Сущность метода Измерение количества электричества, прошедшего через электролизер при электрохимическом окислении или восстановлении вещества на рабочем электроде Классификация: v Прямая и косвенная кулонометрия; v Потенциостатическая и гальваностатическая кулонометрия. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 6
 Кулонометрия Прямая кулонометрия Аналит электрохимически активное вещество, которое осаждают (или переводят в новую степень окисления) на электроде при заданном потенциале электролиза. Затраченное количество электричества пропорционально количеству прореагировавшего вещества Q~m Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 7
Кулонометрия Прямая кулонометрия Аналит электрохимически активное вещество, которое осаждают (или переводят в новую степень окисления) на электроде при заданном потенциале электролиза. Затраченное количество электричества пропорционально количеству прореагировавшего вещества Q~m Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 7
 Гальваностатическая кулонометрия Электрохимическая ячейка рабочий, вспомогательный и электрод сравнения; Условия: постоянный ток, протекающий через ячейку; вспомогательный электрод отделяют от рабочего диафрагмой. v v Аналитический сигнал v v сила постоянного тока; время прохождения тока через ячейку. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 8
Гальваностатическая кулонометрия Электрохимическая ячейка рабочий, вспомогательный и электрод сравнения; Условия: постоянный ток, протекающий через ячейку; вспомогательный электрод отделяют от рабочего диафрагмой. v v Аналитический сигнал v v сила постоянного тока; время прохождения тока через ячейку. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 8
 Гальваностатическая кулонометрия Недостатки метода v v для проведения количественной реакции требуется длительное время; потребляемый ток (особенно по мере завершения электролиза) может частично расходоваться на прохождение не представляющей интереса побочной реакции. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 9
Гальваностатическая кулонометрия Недостатки метода v v для проведения количественной реакции требуется длительное время; потребляемый ток (особенно по мере завершения электролиза) может частично расходоваться на прохождение не представляющей интереса побочной реакции. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 9
 Потенциостатическая кулонометрия Электрохимическая ячейка рабочий, вспомогательный и электрод сравнения; Условия: постоянный потенциал рабочего электрода; вспомогательный электрод отделяют от рабочего диафрагмой. v v Аналитический сигнал v v значения мгновенного тока; время прохождения тока через ячейку. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 10
Потенциостатическая кулонометрия Электрохимическая ячейка рабочий, вспомогательный и электрод сравнения; Условия: постоянный потенциал рабочего электрода; вспомогательный электрод отделяют от рабочего диафрагмой. v v Аналитический сигнал v v значения мгновенного тока; время прохождения тока через ячейку. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 10
 Потенциостатическая кулонометрия v Зависимость силы тока от времени электролиза при постоянном потенциале выражается экспоненциальной функцией: v Константа K зависит от коэффициента диффузии электроактивного вещества D, объема раствора V, толщины диффузионного слоя и площади поверхности электрода A: Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 11
Потенциостатическая кулонометрия v Зависимость силы тока от времени электролиза при постоянном потенциале выражается экспоненциальной функцией: v Константа K зависит от коэффициента диффузии электроактивного вещества D, объема раствора V, толщины диффузионного слоя и площади поверхности электрода A: Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 11
 Потенциостатическая кулонометрия Определение общего количества электричества Интегрирование по времени измеряемых значений мгновенного тока Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 12
Потенциостатическая кулонометрия Определение общего количества электричества Интегрирование по времени измеряемых значений мгновенного тока Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 12
 Потенциостатическая кулонометрия Определение общего количества электричества Способы интегрирования: с помощью кулонометра (химического, механического или электронного); расчетный (компьютерная обработка данных с помощью аналого-цифрового преобразования измеряемого тока). Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 13
Потенциостатическая кулонометрия Определение общего количества электричества Способы интегрирования: с помощью кулонометра (химического, механического или электронного); расчетный (компьютерная обработка данных с помощью аналого-цифрового преобразования измеряемого тока). Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 13
 Потенциостатическая кулонометрия Определение общего количества электричества Способы интегрирования: Химический кулонометр Электролитическая ячейка, в которой при замыкании цепи со 100 %-ым выходом по току протекает электрохимическая реакция известной стехиометрии. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 14
Потенциостатическая кулонометрия Определение общего количества электричества Способы интегрирования: Химический кулонометр Электролитическая ячейка, в которой при замыкании цепи со 100 %-ым выходом по току протекает электрохимическая реакция известной стехиометрии. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 14
 Потенциостатическая кулонометрия Электрохимическая ячейка рабочий, вспомогательный и электрод сравнения; Условия: v постоянный потенциал рабочего электрода; v вспомогательный электрод отделяют от рабочего диафрагмой; v электролиз проводят как на катоде – Bi (III), Co (II), Cu (II), Pb (II), Ni (II) – путем восстановления до металла или до низших степеней окисления – Cr (VI) до Cr (III), Fe (III) до Fe (II); так и на аноде – Cl-, SCN-, окисление Cr (II) до Cr (III), As (III) до As (V). Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 15
Потенциостатическая кулонометрия Электрохимическая ячейка рабочий, вспомогательный и электрод сравнения; Условия: v постоянный потенциал рабочего электрода; v вспомогательный электрод отделяют от рабочего диафрагмой; v электролиз проводят как на катоде – Bi (III), Co (II), Cu (II), Pb (II), Ni (II) – путем восстановления до металла или до низших степеней окисления – Cr (VI) до Cr (III), Fe (III) до Fe (II); так и на аноде – Cl-, SCN-, окисление Cr (II) до Cr (III), As (III) до As (V). Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 15
 Кулонометрическое титрование Сущность – при постоянной силе тока электрохимическим путем генерируют вещество, служащее титрантом для определяемого вещества. Индикация конечной точки титрования: v v v визуальная; фотометрическая; электрохимическая. Условия: I = const Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 16
Кулонометрическое титрование Сущность – при постоянной силе тока электрохимическим путем генерируют вещество, служащее титрантом для определяемого вещества. Индикация конечной точки титрования: v v v визуальная; фотометрическая; электрохимическая. Условия: I = const Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 16
 Кулонометрическое титрование Метод незаменим при использовании неустойчивых титрантов I 2; v CI 2; v Br 2; v Ag(II); v Ti (II). Определение аскорбиновой кислоты v окисление электрохимически генерированным иодидом до дегидроаскорбиновой кислоты. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 17
Кулонометрическое титрование Метод незаменим при использовании неустойчивых титрантов I 2; v CI 2; v Br 2; v Ag(II); v Ti (II). Определение аскорбиновой кислоты v окисление электрохимически генерированным иодидом до дегидроаскорбиновой кислоты. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 17
 Кулонометрическое титрование Преимущества перед другими методами титрования v v v Не требуется готовить стандартные растворы; Простота точного измерения небольших количеств электричества, вплоть до 1 м. Кл; Реагенты, которые трудно хранить или стандартизировать, могут быть получены in situ и стандартизованы кулонометрическим способом. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 18
Кулонометрическое титрование Преимущества перед другими методами титрования v v v Не требуется готовить стандартные растворы; Простота точного измерения небольших количеств электричества, вплоть до 1 м. Кл; Реагенты, которые трудно хранить или стандартизировать, могут быть получены in situ и стандартизованы кулонометрическим способом. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 18
 Кулонометрическое титрование Требование Стехиометрическое и быстрое взаимодействие титранта с определяемым веществом. Способы v Кислотно-основное титрование; v Осадительное титрование; v Redox-титрование; v Комплексометрическое титрование. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 19
Кулонометрическое титрование Требование Стехиометрическое и быстрое взаимодействие титранта с определяемым веществом. Способы v Кислотно-основное титрование; v Осадительное титрование; v Redox-титрование; v Комплексометрическое титрование. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 19
 Кулонометрическое титрование Определение кислот Основано на титровании ионов водорода ионами ОН-, генерируемыми при восстановлении воды на платиновом электроде. Избыток ОН- после ТЭ обнаруживают с помощью р. Нметра. Применение: v Кислотность хлебопекарных дрожжей; v Лимонная кислота в техническом препарате; v Кислотность зерна; v Кислотность пива; v Кислотность молока. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 20
Кулонометрическое титрование Определение кислот Основано на титровании ионов водорода ионами ОН-, генерируемыми при восстановлении воды на платиновом электроде. Избыток ОН- после ТЭ обнаруживают с помощью р. Нметра. Применение: v Кислотность хлебопекарных дрожжей; v Лимонная кислота в техническом препарате; v Кислотность зерна; v Кислотность пива; v Кислотность молока. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 20
 Кулонометрическое титрование Определение хлорид-ионов Реакция титрования хлорид-ионов электрохимически регенирируемыми ионами серебра. Точку эквивалентности определяют амперометрически. Применение: v определение хлоридов в сточных водах; v определение хлорида натрия в сыре; v определение хлорида натрия в мясных продуктах. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 21
Кулонометрическое титрование Определение хлорид-ионов Реакция титрования хлорид-ионов электрохимически регенирируемыми ионами серебра. Точку эквивалентности определяют амперометрически. Применение: v определение хлоридов в сточных водах; v определение хлорида натрия в сыре; v определение хлорида натрия в мясных продуктах. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 21
 Кулонометрическое титрование Определение тиосульфат –ионов v v v Через раствор, содержащий избыток KI и крахмал, пропускают ток; I- электрохимически окисляются до I 2, который немедленно реагирует с тиосульфат-ионами; точку эквивалентности определяют визуально по первому появлению слабо-фиолетового окрашивания раствора; Измеряют секундомером время; Q = I · ; по закону Фарадея определяют массу вещества. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 22
Кулонометрическое титрование Определение тиосульфат –ионов v v v Через раствор, содержащий избыток KI и крахмал, пропускают ток; I- электрохимически окисляются до I 2, который немедленно реагирует с тиосульфат-ионами; точку эквивалентности определяют визуально по первому появлению слабо-фиолетового окрашивания раствора; Измеряют секундомером время; Q = I · ; по закону Фарадея определяют массу вещества. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 22
 Кулонометрия Особенности и преимущества v v v высокие метрологические характеристики, рекордные для электрохимического метода анализа; автоматизация процесса; возможность определения основного компонента и примесей без предварительного отделения; отсутствие применения стандартных растворов и предварительной градуировки по стандартам; сокращение затрат и времени на подготовительные операции перед измерением. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 23
Кулонометрия Особенности и преимущества v v v высокие метрологические характеристики, рекордные для электрохимического метода анализа; автоматизация процесса; возможность определения основного компонента и примесей без предварительного отделения; отсутствие применения стандартных растворов и предварительной градуировки по стандартам; сокращение затрат и времени на подготовительные операции перед измерением. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 23
 Кулонометрия Анализатор кулонометрический "Эксперт-006" Прибор для определения кислотности, антиоксидантной, активности, кислотно -основного титрования, измерения диоксида серы и решения широкого круга химико-аналитических задач: по определению массы вещества, содержащегося в растворе в форме ионов, комплексных соединений, нейтральных молекул и других электроактивных соединений. Комплектуется различными рабочими электродами и электрохимическими ячейками. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 24
Кулонометрия Анализатор кулонометрический "Эксперт-006" Прибор для определения кислотности, антиоксидантной, активности, кислотно -основного титрования, измерения диоксида серы и решения широкого круга химико-аналитических задач: по определению массы вещества, содержащегося в растворе в форме ионов, комплексных соединений, нейтральных молекул и других электроактивных соединений. Комплектуется различными рабочими электродами и электрохимическими ячейками. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 24
 Кулонометрия Аналитические комплексы: Комплекс "Эксперт-006" - базовый - кулонометр для титрования электрогеннерированными галогенидами; Комплекс "Эксперт-006" - р. Н - кулонометрический титратор для кислотноосновного титрования; Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 25
Кулонометрия Аналитические комплексы: Комплекс "Эксперт-006" - базовый - кулонометр для титрования электрогеннерированными галогенидами; Комплекс "Эксперт-006" - р. Н - кулонометрический титратор для кислотноосновного титрования; Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 25
 Кулонометрия Аналитические комплексы: Комплекс "Эксперт-006" - антиоксиданты - кулонометрический титратор для измерения антиоксидантной активности; Комплекс "Эксперт-006" - универсальный кулонометрический титратор (кулонометр). Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 26
Кулонометрия Аналитические комплексы: Комплекс "Эксперт-006" - антиоксиданты - кулонометрический титратор для измерения антиоксидантной активности; Комплекс "Эксперт-006" - универсальный кулонометрический титратор (кулонометр). Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 26
 Электрогравиметрия Метод основан на полном электрохимическом превращении определяемого вещества и взвешивании продуктов реакции: v v Определяют массу электрода; Определяемый ион выделяют путем электролиза в виде металла на электроде; Определяют массу электрода с выделившимся металлом; Рассчитывают содержание иона в растворе. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 27
Электрогравиметрия Метод основан на полном электрохимическом превращении определяемого вещества и взвешивании продуктов реакции: v v Определяют массу электрода; Определяемый ион выделяют путем электролиза в виде металла на электроде; Определяют массу электрода с выделившимся металлом; Рассчитывают содержание иона в растворе. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 27
 Электрогравиметрия Метод основан на полном электрохимическом превращении определяемого вещества и взвешивании продуктов реакции v v Безэталонный метод; Простейший вариант кулонометрии. Способы анализа v v v при постоянном напряжении между электродами; при постоянной силе тока; при контролируемом потенциале рабочего электрода. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 28
Электрогравиметрия Метод основан на полном электрохимическом превращении определяемого вещества и взвешивании продуктов реакции v v Безэталонный метод; Простейший вариант кулонометрии. Способы анализа v v v при постоянном напряжении между электродами; при постоянной силе тока; при контролируемом потенциале рабочего электрода. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 28
 Электрогравиметрия Требования v v Осадки д. б. мелкокристаллические, свободные от примесей, хорошо удерживающиеся на электроде; Отсутствие концентрационной поляризации. Условия v v v Электролиз проводят при невысоких плотностях тока от 0, 01 до 0, 1 А см-2; Раствор перемешивают; Возможно нагревание раствора. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 29
Электрогравиметрия Требования v v Осадки д. б. мелкокристаллические, свободные от примесей, хорошо удерживающиеся на электроде; Отсутствие концентрационной поляризации. Условия v v v Электролиз проводят при невысоких плотностях тока от 0, 01 до 0, 1 А см-2; Раствор перемешивают; Возможно нагревание раствора. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 29
 Электрогравиметрия Метод внутреннего (самопроизвольного) электролиза Реакция в ячейке (гальваническом элементе) протекает самопроизвольно без приложения внешнего напряжения. Катод инертный металлический электрод (обычно платиновая сетка); Анод электрохимически активный электрод. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 30
Электрогравиметрия Метод внутреннего (самопроизвольного) электролиза Реакция в ячейке (гальваническом элементе) протекает самопроизвольно без приложения внешнего напряжения. Катод инертный металлический электрод (обычно платиновая сетка); Анод электрохимически активный электрод. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 30
 Электрогравиметрия Характеристики метода Селективность раздельное выделение на электроде при разности их E: v 0, 3 В (для однозарядных ионов); v 0, 1 В (для двухзарядных ионов). Точность и воспроизводимость Лучшие из всех методов определения Сu, Sn, Pb, Cd, Zn. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 31
Электрогравиметрия Характеристики метода Селективность раздельное выделение на электроде при разности их E: v 0, 3 В (для однозарядных ионов); v 0, 1 В (для двухзарядных ионов). Точность и воспроизводимость Лучшие из всех методов определения Сu, Sn, Pb, Cd, Zn. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 31
 Кулонометрия. Задачи 1. 2. 3. Определить содержание (%) меди в сплаве, если для выделения всей меди из 25, 0 мл раствора, отобранного из общего объема раствора 200, 0 мл, в котором растворено 0, 56 г сплава, потребовалось 3 мин 20 с при силе тока 100, 0 м. А. Выход меди по току равен 90%. В сплаве содержится 20, 0 мас. % свинца. Навеску сплава массой 0, 6 г растворили в 20, 0 мл раствора. Для кулонометрического определения было взято 30, 0 мл этого раствора. Сколько времени необходимо проводить электролиз током 50, 0 м. А для полного выделения свинца, если выход по току равен 0, 6? Химическое соединение содержит 25, 0 мас. % кобальта. Из 250, 0 мол раствора этого соединения для кулонометрического анализа было взято 20, 0 мл раствора Электролиз проводили током 70, 0 м. А в течение 30 мин 40 с, выход по току составлял 35%. Какая масса соединения растворена в 250, 0 мл? Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 32
Кулонометрия. Задачи 1. 2. 3. Определить содержание (%) меди в сплаве, если для выделения всей меди из 25, 0 мл раствора, отобранного из общего объема раствора 200, 0 мл, в котором растворено 0, 56 г сплава, потребовалось 3 мин 20 с при силе тока 100, 0 м. А. Выход меди по току равен 90%. В сплаве содержится 20, 0 мас. % свинца. Навеску сплава массой 0, 6 г растворили в 20, 0 мл раствора. Для кулонометрического определения было взято 30, 0 мл этого раствора. Сколько времени необходимо проводить электролиз током 50, 0 м. А для полного выделения свинца, если выход по току равен 0, 6? Химическое соединение содержит 25, 0 мас. % кобальта. Из 250, 0 мол раствора этого соединения для кулонометрического анализа было взято 20, 0 мл раствора Электролиз проводили током 70, 0 м. А в течение 30 мин 40 с, выход по току составлял 35%. Какая масса соединения растворена в 250, 0 мл? Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 32
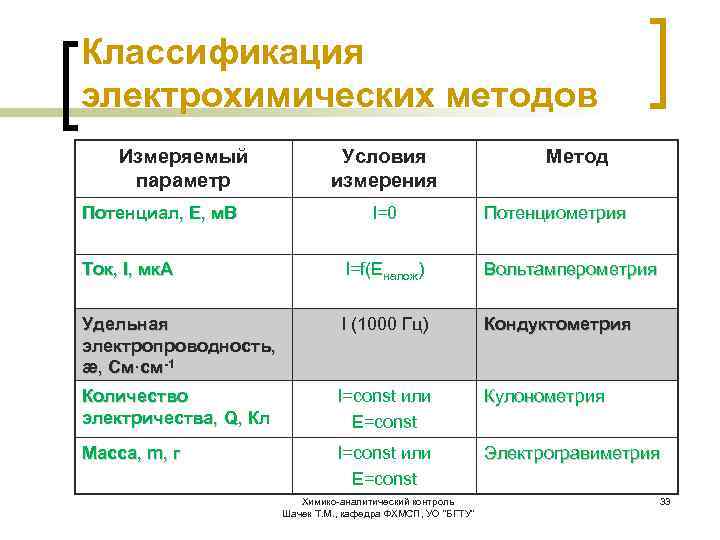 Классификация электрохимических методов Измеряемый параметр Потенциал, Е, м. В Условия измерения I=0 Метод Потенциометрия Ток, I, мк. А I=f(Eналож) Вольтамперометрия Удельная электропроводность, æ, См·см-1 I (1000 Гц) Кондуктометрия Количество электричества, Q, Кл I=const или E=const Кулонометрия Масса, m, г I=const или E=const Электрогравиметрия Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 33
Классификация электрохимических методов Измеряемый параметр Потенциал, Е, м. В Условия измерения I=0 Метод Потенциометрия Ток, I, мк. А I=f(Eналож) Вольтамперометрия Удельная электропроводность, æ, См·см-1 I (1000 Гц) Кондуктометрия Количество электричества, Q, Кл I=const или E=const Кулонометрия Масса, m, г I=const или E=const Электрогравиметрия Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 33
 Кондуктометрия Основана на измерении электропроводности анализируемого раствора. Электрическая проводимость – способность вещества проводить электрический ток под действием внешнего электрического поля. Электролиты -? Истинные электролиты – электролиты, состоящие из ионов изначально. Потенциальные электролиты – ионы образуются в результате растворения электролита вследствие электролитической диссоциации. КА ↔ К+ + А-, Кс =[К+][А-]/[КА], R=U/I, ρ = A·R/L (Ом·см) k = 1/ρ (Ом-1·см-1) Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 34
Кондуктометрия Основана на измерении электропроводности анализируемого раствора. Электрическая проводимость – способность вещества проводить электрический ток под действием внешнего электрического поля. Электролиты -? Истинные электролиты – электролиты, состоящие из ионов изначально. Потенциальные электролиты – ионы образуются в результате растворения электролита вследствие электролитической диссоциации. КА ↔ К+ + А-, Кс =[К+][А-]/[КА], R=U/I, ρ = A·R/L (Ом·см) k = 1/ρ (Ом-1·см-1) Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 34
 Кондуктометрия k – удельная электропроводность, См/м, λ = k/c – эквивалентная электропроводность. cev = z+v+c = |z- |v-c – эквивалентная концентрация. λ m и λ определяется величинами подвижностей ионов электролита: λ = zеc F (u++ u-) Сильные электролиты λ∞ λ = λ∞ - k √ с 140 130 Слабые электролиты 120 -lg c 3, 0 2, 0 1, 0 λ = λ∞ - k' √ с Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 35
Кондуктометрия k – удельная электропроводность, См/м, λ = k/c – эквивалентная электропроводность. cev = z+v+c = |z- |v-c – эквивалентная концентрация. λ m и λ определяется величинами подвижностей ионов электролита: λ = zеc F (u++ u-) Сильные электролиты λ∞ λ = λ∞ - k √ с 140 130 Слабые электролиты 120 -lg c 3, 0 2, 0 1, 0 λ = λ∞ - k' √ с Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 35
 Кондуктометрия λm = k/c – мольная электропроводность; λ = k/cev – эквивалентная электропроводность. cev = z+v+c = |z- |v-c – эквивалентная концентрация. λ m и λ определяется величинами подвижностей ионов электролита: λ = zеc F (u++ u-) Сильные электролиты λ∞ λ = λ∞ - k √ с 140 130 Слабые электролиты 120 -lg c 3, 0 2, 0 1, 0 λ = λ∞ - k' √ с Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 36
Кондуктометрия λm = k/c – мольная электропроводность; λ = k/cev – эквивалентная электропроводность. cev = z+v+c = |z- |v-c – эквивалентная концентрация. λ m и λ определяется величинами подвижностей ионов электролита: λ = zеc F (u++ u-) Сильные электролиты λ∞ λ = λ∞ - k √ с 140 130 Слабые электролиты 120 -lg c 3, 0 2, 0 1, 0 λ = λ∞ - k' √ с Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 36
 Кондуктометрия v v В очень разбавленных растворах (предельно разбавленных) эквивалентная электропроводность (λ 0) является постоянной характеристикой раствора, не зависящей от изменения концентрации электролита. Предельная эквивалентная электропроводность раствора электролита равна сумме эквивалентных электропроводностей катиона и аниона: λ 0 = λ 0+ + λ 0 -. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 37
Кондуктометрия v v В очень разбавленных растворах (предельно разбавленных) эквивалентная электропроводность (λ 0) является постоянной характеристикой раствора, не зависящей от изменения концентрации электролита. Предельная эквивалентная электропроводность раствора электролита равна сумме эквивалентных электропроводностей катиона и аниона: λ 0 = λ 0+ + λ 0 -. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 37
 Кондуктометрия v v Эквивалентные электропроводности подавляющего числа ионов близки друг к другу по величине. Исключение составляют ионы H+, OH-, Fe(CN)63 -, Fe(CN)64 -. Температура анализируемого раствора оказывает существенное влияние на измеряемые величины удельной электропроводности. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 38
Кондуктометрия v v Эквивалентные электропроводности подавляющего числа ионов близки друг к другу по величине. Исключение составляют ионы H+, OH-, Fe(CN)63 -, Fe(CN)64 -. Температура анализируемого раствора оказывает существенное влияние на измеряемые величины удельной электропроводности. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 38
 Кондуктометрия 1. 2. 3. Электрохимическая ячейка; Измеряют сопротивление; Рассчитывают удельное сопротивление: k=(1/R)·(L/A)=G·C, G = 1/R – электропроводность раствора, Ом-1; С – постоянная ячейки, см-1. С – определяют экспериментально путем градуировки. К электродам прилагают переменное напряжение – для исключения явлений электролиза и поляризации. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 39
Кондуктометрия 1. 2. 3. Электрохимическая ячейка; Измеряют сопротивление; Рассчитывают удельное сопротивление: k=(1/R)·(L/A)=G·C, G = 1/R – электропроводность раствора, Ом-1; С – постоянная ячейки, см-1. С – определяют экспериментально путем градуировки. К электродам прилагают переменное напряжение – для исключения явлений электролиза и поляризации. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 39
 Кондуктометрия Прямая кондуктометрия установление концентрации электролита и электропроводности раствора v v Контроль производственных процессов, например, в гальваническом производстве, при производстве бумаги. Способ детектирования в жидкостной и газовой хроматографии. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 40
Кондуктометрия Прямая кондуктометрия установление концентрации электролита и электропроводности раствора v v Контроль производственных процессов, например, в гальваническом производстве, при производстве бумаги. Способ детектирования в жидкостной и газовой хроматографии. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 40
 Кондуктометрия Кондуктометрическое титрование основано на химической реакции, сопровождающейся изменением электропроводности раствора. Кривые титрования – электрическая проводимость (сопротивление) – объем титранта; Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 41
Кондуктометрия Кондуктометрическое титрование основано на химической реакции, сопровождающейся изменением электропроводности раствора. Кривые титрования – электрическая проводимость (сопротивление) – объем титранта; Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 41
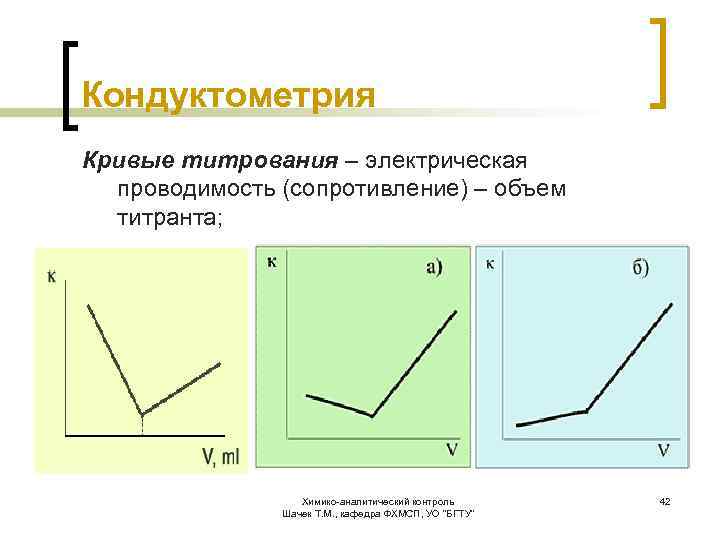 Кондуктометрия Кривые титрования – электрическая проводимость (сопротивление) – объем титранта; Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 42
Кондуктометрия Кривые титрования – электрическая проводимость (сопротивление) – объем титранта; Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 42
 Кондуктометрия Кондуктометрическое титрование Классификация: q Постояннотоковые; q Переменнотоковые низкочастотные (частота тока <105 Гц) или высокочастотные (>105 Гц). Ø Контактные; Ø Безконтактные. v Кислотно-основное; v Осадительное; v Комплексонометрическое. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 43
Кондуктометрия Кондуктометрическое титрование Классификация: q Постояннотоковые; q Переменнотоковые низкочастотные (частота тока <105 Гц) или высокочастотные (>105 Гц). Ø Контактные; Ø Безконтактные. v Кислотно-основное; v Осадительное; v Комплексонометрическое. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 43
 Кондуктометрическое титрование Определение кислотности яичного порошка Кондуктометрическое титрование водного раствора яичного порошка раствором щелочи К= V 1· 250· 100/m·V· 10 Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 44
Кондуктометрическое титрование Определение кислотности яичного порошка Кондуктометрическое титрование водного раствора яичного порошка раствором щелочи К= V 1· 250· 100/m·V· 10 Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 44
 Кондуктометрическое титрование Определение активного хлора в дезинфицирующем средстве Методика основана на взаимодействии хлора с иодидом калия, сопровождающемся образованием эквивалентного количества иода. Иод определяют кондуктометрическим титрованием раствором тиосульфата натрия w= 0, 00355· 100·V· 100·К / m· 10 Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 45
Кондуктометрическое титрование Определение активного хлора в дезинфицирующем средстве Методика основана на взаимодействии хлора с иодидом калия, сопровождающемся образованием эквивалентного количества иода. Иод определяют кондуктометрическим титрованием раствором тиосульфата натрия w= 0, 00355· 100·V· 100·К / m· 10 Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 45
 Кондуктометрическое титрование Определение общей жесткости воды Методика основана на образовании комплексонатов кальция и магния при взаимодействии соответствующих катионов с комплексоном III. Титрование проводят в среде аммонийного буферного раствора (р. Н≈10) Ж = 0, 05·V 1·К· 1000 /V 2 Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 46
Кондуктометрическое титрование Определение общей жесткости воды Методика основана на образовании комплексонатов кальция и магния при взаимодействии соответствующих катионов с комплексоном III. Титрование проводят в среде аммонийного буферного раствора (р. Н≈10) Ж = 0, 05·V 1·К· 1000 /V 2 Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 46
 Кондуктометрия Кондуктометр КП-202 Чувствительный элемент трехэлектродный, проточнопогружного типа, с двумя геометрическими постоянными: С 1=0, 01 см-1 ± 20%, С 2=0, 5 см-1 ± 20%. Предназначен для непрерывного измерения характеристик водных и неводных растворов диссоциирующих химических веществ: v удельная электрическая проводимость (УЭП); v удельное электрическое сопротивление (УЭС); v температура. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 47
Кондуктометрия Кондуктометр КП-202 Чувствительный элемент трехэлектродный, проточнопогружного типа, с двумя геометрическими постоянными: С 1=0, 01 см-1 ± 20%, С 2=0, 5 см-1 ± 20%. Предназначен для непрерывного измерения характеристик водных и неводных растворов диссоциирующих химических веществ: v удельная электрическая проводимость (УЭП); v удельное электрическое сопротивление (УЭС); v температура. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 47
 Кондуктометрия Кондуктометр КП-202 Диапазоны измерений: v v v УЭП от 2 х10 -6 до 1 х10 -1 См/м; УЭС от 10 до 5 х105 Ом м; t от 0 до 99 °С. Основная приведенная погрешность измерений температуры и УЭП (УЭС) ± 2, 5%. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 48
Кондуктометрия Кондуктометр КП-202 Диапазоны измерений: v v v УЭП от 2 х10 -6 до 1 х10 -1 См/м; УЭС от 10 до 5 х105 Ом м; t от 0 до 99 °С. Основная приведенная погрешность измерений температуры и УЭП (УЭС) ± 2, 5%. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 48
 Кондуктометрия Кондуктометр HI 8733 Предназначен для измерения удельной электропроводности в следующих условиях эксплуатации прибора: v температура окружающей среды от 0 до 50ºС; v относительная влажность воздуха – 100%. Диапазон измеряемых величин от 0, 0 до 199, 0 м. См/см. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 49
Кондуктометрия Кондуктометр HI 8733 Предназначен для измерения удельной электропроводности в следующих условиях эксплуатации прибора: v температура окружающей среды от 0 до 50ºС; v относительная влажность воздуха – 100%. Диапазон измеряемых величин от 0, 0 до 199, 0 м. См/см. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 49
 Кондуктометрия Преимущества v v v высокая чувствительность (нижняя граница определяемых концентраций ~10 -4 -10 -5 М); достаточно высокая точность (относит, погрешность определения 0, 1– 2%); простота методик; доступность аппаратуры; возможность исследования окрашенных и мутных растворов, последовательного определения компонентов смеси, а также автоматизации анализа. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 50
Кондуктометрия Преимущества v v v высокая чувствительность (нижняя граница определяемых концентраций ~10 -4 -10 -5 М); достаточно высокая точность (относит, погрешность определения 0, 1– 2%); простота методик; доступность аппаратуры; возможность исследования окрашенных и мутных растворов, последовательного определения компонентов смеси, а также автоматизации анализа. Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 50
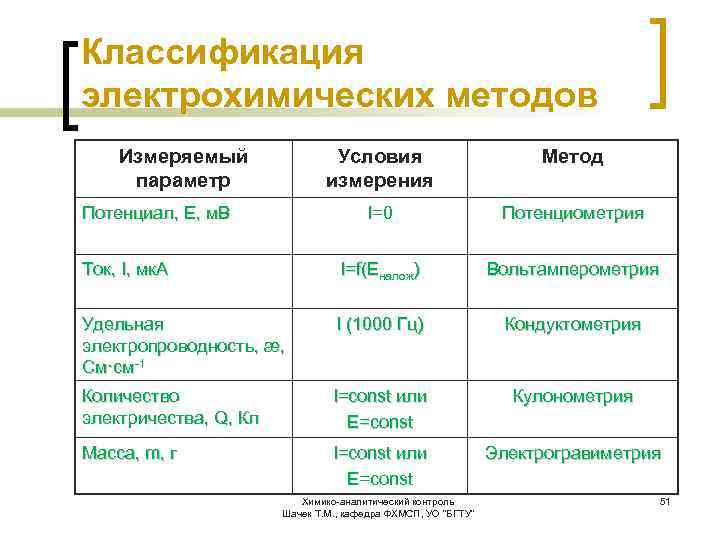 Классификация электрохимических методов Измеряемый параметр Условия измерения Метод I=0 Потенциометрия Ток, I, мк. А I=f(Eналож) Вольтамперометрия Удельная электропроводность, æ, См·см-1 I (1000 Гц) Кондуктометрия Количество электричества, Q, Кл I=const или E=const Кулонометрия Масса, m, г I=const или E=const Электрогравиметрия Потенциал, Е, м. В Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 51
Классификация электрохимических методов Измеряемый параметр Условия измерения Метод I=0 Потенциометрия Ток, I, мк. А I=f(Eналож) Вольтамперометрия Удельная электропроводность, æ, См·см-1 I (1000 Гц) Кондуктометрия Количество электричества, Q, Кл I=const или E=const Кулонометрия Масса, m, г I=const или E=const Электрогравиметрия Потенциал, Е, м. В Химико-аналитический контроль Шачек Т. М. , кафедра ФХМСП, УО "БГТУ" 51


