Lecture2.ppt
- Количество слайдов: 22
 Хімічний склад підземних вод
Хімічний склад підземних вод
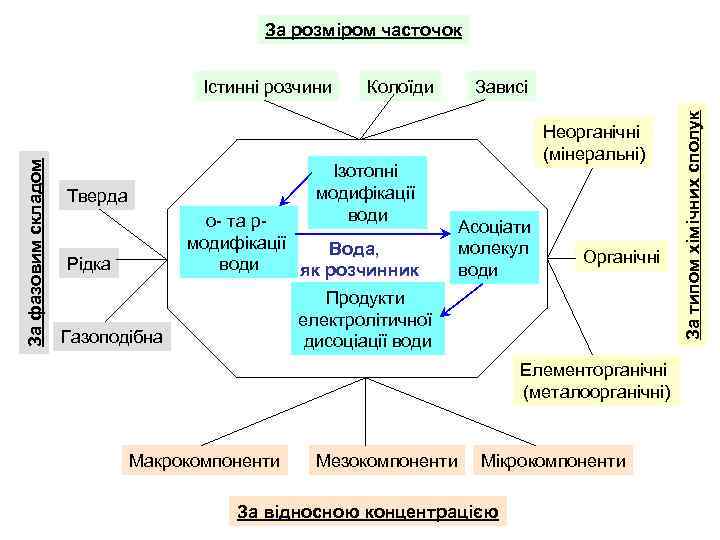 За розміром часточок Колоїди Ізотопні модифікації води Тверда о- та р- модифікації Вода, води як розчинник Рідка Зависі Неорганічні (мінеральні) Асоціати молекул води Органічні Продукти електролітичної дисоціації води Газоподібна Елементорганічні (металоорганічні) Макрокомпоненти Мезокомпоненти Мікрокомпоненти За відносною концентрацією За типом хімічних сполук За фазовим складом Істинні розчини
За розміром часточок Колоїди Ізотопні модифікації води Тверда о- та р- модифікації Вода, води як розчинник Рідка Зависі Неорганічні (мінеральні) Асоціати молекул води Органічні Продукти електролітичної дисоціації води Газоподібна Елементорганічні (металоорганічні) Макрокомпоненти Мезокомпоненти Мікрокомпоненти За відносною концентрацією За типом хімічних сполук За фазовим складом Істинні розчини
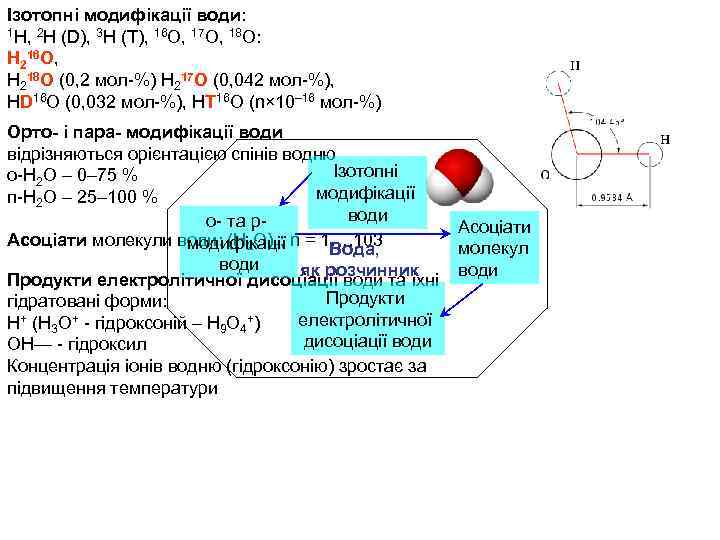 Ізотопні модифікації води: 1 Н, 2 Н (D), 3 H (T), 16 O, 17 O, 18 O: H 216 O, H 218 O (0, 2 мол-%) H 217 O (0, 042 мол-%), HD 16 O (0, 032 мол-%), HT 16 O (n× 10– 16 мол-%) Орто- і пара- модифікації води відрізняються орієнтацією спінів водню Ізотопні о-Н 2 О – 0– 75 % модифікації п-Н 2 О – 25– 100 % води о- та р- Асоціати молекули води: (Н 2 О)n; n = 1…. 103 модифікації молекул Вода, води як розчинник Продукти електролітичної дисоціації води та їхні Продукти гідратовані форми: електролітичної Н+ (Н 3 О+ - гідроксоній – Н 9 О 4+) дисоціації води ОН— - гідроксил Концентрація іонів водню (гідроксонію) зростає за підвищення температури
Ізотопні модифікації води: 1 Н, 2 Н (D), 3 H (T), 16 O, 17 O, 18 O: H 216 O, H 218 O (0, 2 мол-%) H 217 O (0, 042 мол-%), HD 16 O (0, 032 мол-%), HT 16 O (n× 10– 16 мол-%) Орто- і пара- модифікації води відрізняються орієнтацією спінів водню Ізотопні о-Н 2 О – 0– 75 % модифікації п-Н 2 О – 25– 100 % води о- та р- Асоціати молекули води: (Н 2 О)n; n = 1…. 103 модифікації молекул Вода, води як розчинник Продукти електролітичної дисоціації води та їхні Продукти гідратовані форми: електролітичної Н+ (Н 3 О+ - гідроксоній – Н 9 О 4+) дисоціації води ОН— - гідроксил Концентрація іонів водню (гідроксонію) зростає за підвищення температури
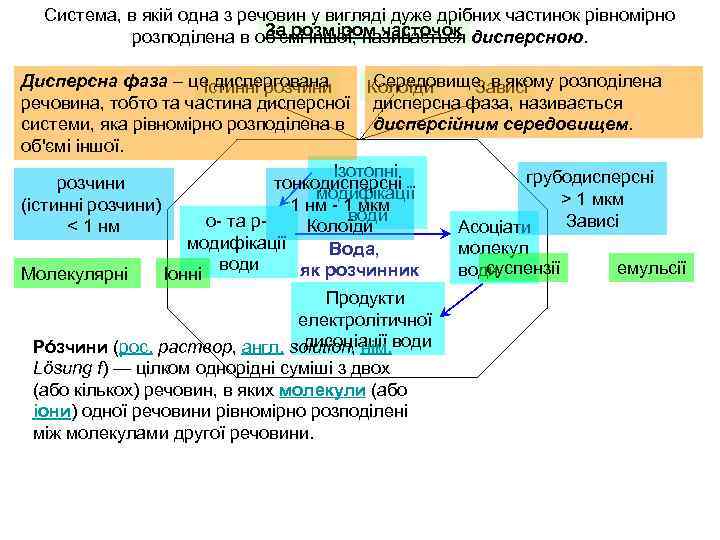 Система, в якій одна з речовин у вигляді дуже дрібних частинок рівномірно За розміром часточок розподілена в об'ємі іншої, називається дисперсною. Дисперсна фаза – це диспергована Середовище, в якому розподілена Істинні розчини Колоїди Зависі речовина, тобто та частина дисперсної дисперсна фаза, називається системи, яка рівномірно розподілена в дисперсійним середовищем. об'ємі іншої. Ізотопні грубодисперсні розчини тонкодисперсні модифікації > 1 мкм (істинні розчини) 1 нм - 1 мкм води Зависі о- та р- < 1 нм Колоїди Асоціати модифікації молекул Вода, води суспензії емульсії води як розчинник Молекулярні Іонні Продукти електролітичної дисоціації води Рóзчини (рос. раствор, англ. solution, нім. Lösung f) — цілком однорідні суміші з двох (або кількох) речовин, в яких молекули (або іони) одної речовини рівномірно розподілені між молекулами другої речовини.
Система, в якій одна з речовин у вигляді дуже дрібних частинок рівномірно За розміром часточок розподілена в об'ємі іншої, називається дисперсною. Дисперсна фаза – це диспергована Середовище, в якому розподілена Істинні розчини Колоїди Зависі речовина, тобто та частина дисперсної дисперсна фаза, називається системи, яка рівномірно розподілена в дисперсійним середовищем. об'ємі іншої. Ізотопні грубодисперсні розчини тонкодисперсні модифікації > 1 мкм (істинні розчини) 1 нм - 1 мкм води Зависі о- та р- < 1 нм Колоїди Асоціати модифікації молекул Вода, води суспензії емульсії води як розчинник Молекулярні Іонні Продукти електролітичної дисоціації води Рóзчини (рос. раствор, англ. solution, нім. Lösung f) — цілком однорідні суміші з двох (або кількох) речовин, в яких молекули (або іони) одної речовини рівномірно розподілені між молекулами другої речовини.
 Розчини Рідкі розчини утворюються при розчиненні газоподібних, рідких або твердих речовин в рідкому дисперсійному середовищі (розчиннику). Фізична теорія розчинів (Я. Вант. Гоф, С. Арреніус) розглядає процес розчинення як простий розподіл (діспергування) однієї речовини у всьому об'ємі іншої. Властивості розчинів повинні залежати тільки від концентрації розчиненої речовини. Розчинник – це індіферентне середовище, в якому хаотично розподілені частинки розчиненої речовини Д. І. Менделєєв показав, що в розчині є сполуки, які утворюються завдяки взаємодії молекул розчиненої речовини і розчинника. Такі сполуки називаються сольватами (гідратами), а процес їх утворення в результаті взаємодії компонентів розчину – сольватацією (гідратацією). Термін “гідрати” і “гідратація” застосовують, коли розчинником є вода.
Розчини Рідкі розчини утворюються при розчиненні газоподібних, рідких або твердих речовин в рідкому дисперсійному середовищі (розчиннику). Фізична теорія розчинів (Я. Вант. Гоф, С. Арреніус) розглядає процес розчинення як простий розподіл (діспергування) однієї речовини у всьому об'ємі іншої. Властивості розчинів повинні залежати тільки від концентрації розчиненої речовини. Розчинник – це індіферентне середовище, в якому хаотично розподілені частинки розчиненої речовини Д. І. Менделєєв показав, що в розчині є сполуки, які утворюються завдяки взаємодії молекул розчиненої речовини і розчинника. Такі сполуки називаються сольватами (гідратами), а процес їх утворення в результаті взаємодії компонентів розчину – сольватацією (гідратацією). Термін “гідрати” і “гідратація” застосовують, коли розчинником є вода.
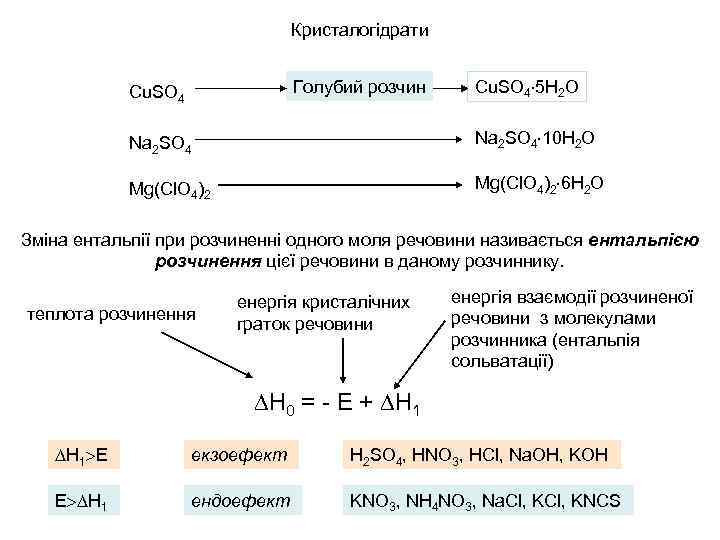 Кристалогідрати Голубий розчин Cu. SO 4 5 H 2 O Na 2 SO 4 10 H 2 O Mg(Cl. O 4)2 6 H 2 O Зміна ентальпії при розчиненні одного моля речовини називається ентальпією розчинення цієї речовини в даному розчиннику. теплота розчинення енергія кристалічних граток речовини енергія взаємодії розчиненої речовини з молекулами розчинника (ентальпія сольватації) Н 0 = - Е + Н 1 Е екзоефект H 2 SO 4, HNO 3, HCl, Na. OH, KOH Е Н 1 ендоефект KNO 3, NH 4 NO 3, Na. Cl, KNCS
Кристалогідрати Голубий розчин Cu. SO 4 5 H 2 O Na 2 SO 4 10 H 2 O Mg(Cl. O 4)2 6 H 2 O Зміна ентальпії при розчиненні одного моля речовини називається ентальпією розчинення цієї речовини в даному розчиннику. теплота розчинення енергія кристалічних граток речовини енергія взаємодії розчиненої речовини з молекулами розчинника (ентальпія сольватації) Н 0 = - Е + Н 1 Е екзоефект H 2 SO 4, HNO 3, HCl, Na. OH, KOH Е Н 1 ендоефект KNO 3, NH 4 NO 3, Na. Cl, KNCS
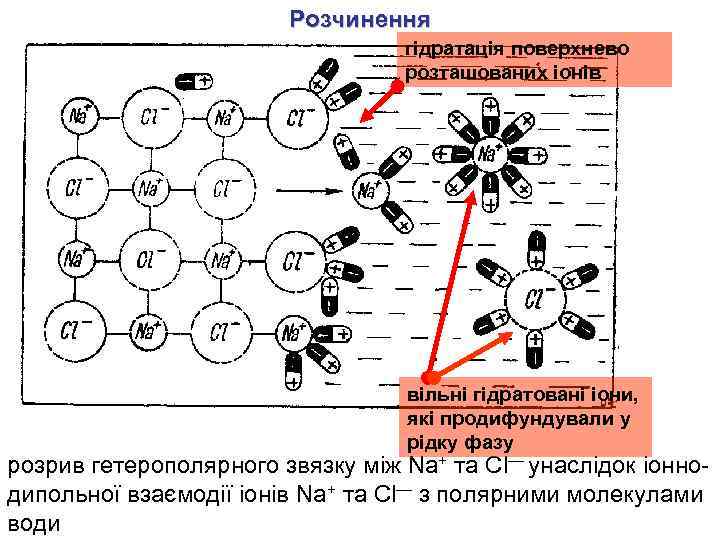 Розчинення гідратація поверхнево розташованих іонів вільні гідратовані іони, які продифундували у рідку фазу розрив гетерополярного звязку між Na+ та Cl— унаслідок іоннодипольної взаємодії іонів Na+ та Cl— з полярними молекулами води
Розчинення гідратація поверхнево розташованих іонів вільні гідратовані іони, які продифундували у рідку фазу розрив гетерополярного звязку між Na+ та Cl— унаслідок іоннодипольної взаємодії іонів Na+ та Cl— з полярними молекулами води
 Розчинність Насиченим розчином називається такий розчин, який знаходиться в рівновазі з твердою фазою розчиненої речовини і містить максимально можливу за даних умов кількість цієї речовини . Залежність розчинності газу від тиску виражається законом ГенріДальтона: розчинність газу при постійній температурі в рідині прямо пропорційна його парціальному тиску. m = kp,
Розчинність Насиченим розчином називається такий розчин, який знаходиться в рівновазі з твердою фазою розчиненої речовини і містить максимально можливу за даних умов кількість цієї речовини . Залежність розчинності газу від тиску виражається законом ГенріДальтона: розчинність газу при постійній температурі в рідині прямо пропорційна його парціальному тиску. m = kp,
![Способи вираження концентрації розчинів Масова концентрація або масова частка розчиненої речовини [%, г/100 г] Способи вираження концентрації розчинів Масова концентрація або масова частка розчиненої речовини [%, г/100 г]](https://present5.com/presentation/-46204815_156756462/image-9.jpg) Способи вираження концентрації розчинів Масова концентрація або масова частка розчиненої речовини [%, г/100 г] Молярна концентрація (молярність) [моль·дм-3] Моляльна концентрація (моляльність) [моль·кг-1] Молярна концентрація еквівалентів (нормальна концентрація, нормальність) [моль-екв·дм-3] У відповідності із законом еквівалентів, розчини взаємодіють між собою в кількостях, пропорційних їх еквівалентам
Способи вираження концентрації розчинів Масова концентрація або масова частка розчиненої речовини [%, г/100 г] Молярна концентрація (молярність) [моль·дм-3] Моляльна концентрація (моляльність) [моль·кг-1] Молярна концентрація еквівалентів (нормальна концентрація, нормальність) [моль-екв·дм-3] У відповідності із законом еквівалентів, розчини взаємодіють між собою в кількостях, пропорційних їх еквівалентам
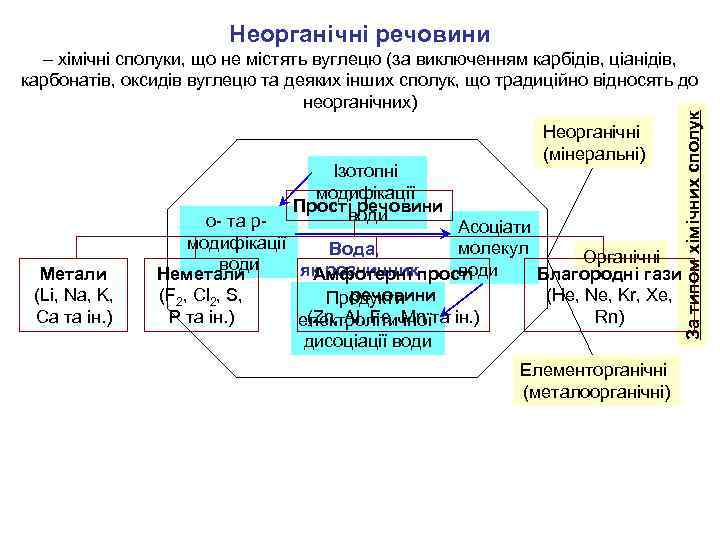 Неорганічні речовини Ізотопні модифікації Прості речовини води Метали (Li, Na, K, Ca та ін. ) Неорганічні (мінеральні) За типом хімічних сполук – хімічні сполуки, що не містять вуглецю (за виключенням карбідів, ціанідів, карбонатів, оксидів вуглецю та деяких інших сполук, що традиційно відносять до неорганічних) о- та р- Асоціати модифікації молекул Вода, Органічні води як розчинникпрості Неметали Амфотерні Благородні гази (F 2, Cl 2, S, речовини (He, Ne, Kr, Xe, Продукти P та ін. ) (Zn, Al. Fe, Mn та ін. ) Rn) електролітичної дисоціації води Елементорганічні (металоорганічні)
Неорганічні речовини Ізотопні модифікації Прості речовини води Метали (Li, Na, K, Ca та ін. ) Неорганічні (мінеральні) За типом хімічних сполук – хімічні сполуки, що не містять вуглецю (за виключенням карбідів, ціанідів, карбонатів, оксидів вуглецю та деяких інших сполук, що традиційно відносять до неорганічних) о- та р- Асоціати модифікації молекул Вода, Органічні води як розчинникпрості Неметали Амфотерні Благородні гази (F 2, Cl 2, S, речовини (He, Ne, Kr, Xe, Продукти P та ін. ) (Zn, Al. Fe, Mn та ін. ) Rn) електролітичної дисоціації води Елементорганічні (металоорганічні)
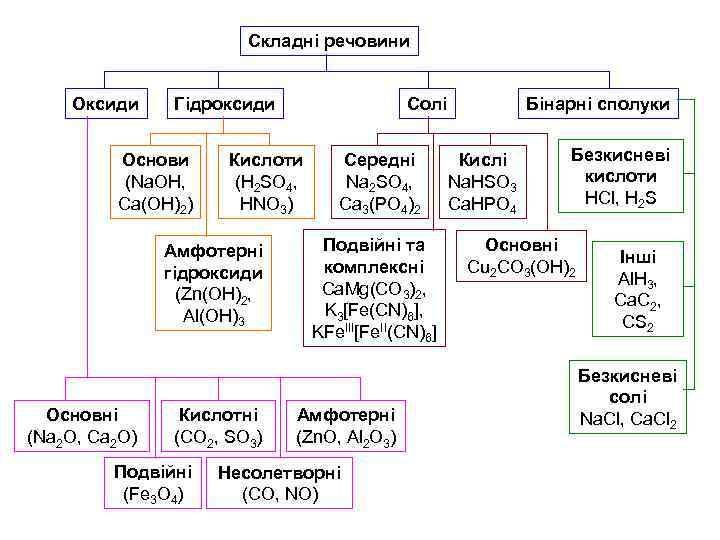 Складні речовини Оксиди Гідроксиди Основи (Na. OH, Ca(OH)2) Кислоти (H 2 SO 4, HNO 3) Амфотерні гідроксиди (Zn(OH)2, Al(OH)3 Основні (Na 2 O, Ca 2 O) Кислотні (CO 2, SO 3) Подвійні (Fe 3 O 4) Солі Середні Na 2 SO 4, Ca 3(PO 4)2 Подвійні та комплексні Ca. Mg(CO 3)2, K 3[Fe(CN)6], KFe. III[Fe. II(CN)6] Амфотерні (Zn. O, Al 2 O 3) Несолетворні (CO, NO) Бінарні сполуки Кислі Na. HSO 3 Ca. HPO 4 Безкисневі кислоти HCl, H 2 S Основні Cu 2 CO 3(OH)2 Інші Al. H 3, Ca. C 2, CS 2 Безкисневі солі Na. Cl, Ca. Cl 2
Складні речовини Оксиди Гідроксиди Основи (Na. OH, Ca(OH)2) Кислоти (H 2 SO 4, HNO 3) Амфотерні гідроксиди (Zn(OH)2, Al(OH)3 Основні (Na 2 O, Ca 2 O) Кислотні (CO 2, SO 3) Подвійні (Fe 3 O 4) Солі Середні Na 2 SO 4, Ca 3(PO 4)2 Подвійні та комплексні Ca. Mg(CO 3)2, K 3[Fe(CN)6], KFe. III[Fe. II(CN)6] Амфотерні (Zn. O, Al 2 O 3) Несолетворні (CO, NO) Бінарні сполуки Кислі Na. HSO 3 Ca. HPO 4 Безкисневі кислоти HCl, H 2 S Основні Cu 2 CO 3(OH)2 Інші Al. H 3, Ca. C 2, CS 2 Безкисневі солі Na. Cl, Ca. Cl 2
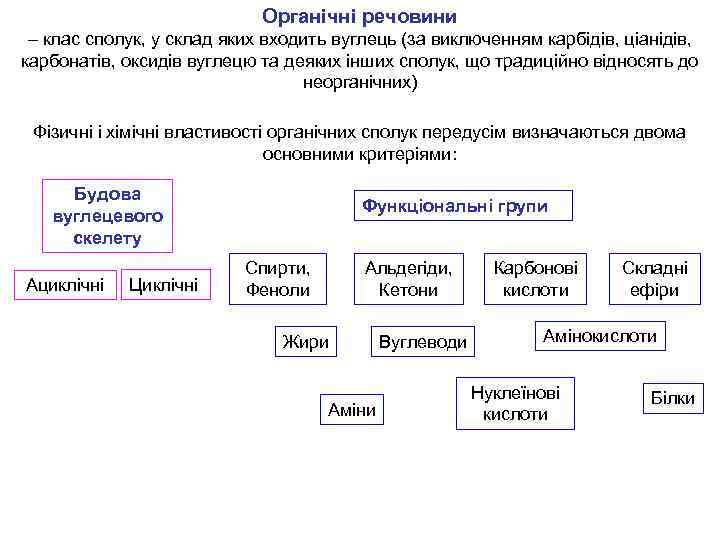 Органічні речовини – клас сполук, у склад яких входить вуглець (за виключенням карбідів, ціанідів, карбонатів, оксидів вуглецю та деяких інших сполук, що традиційно відносять до неорганічних) Фізичні і хімічні властивості органічних сполук передусім визначаються двома основними критеріями: Будова вуглецевого скелету Ациклічні Циклічні Функціональні групи Спирти, Феноли Альдегіди, Кетони Жири Аміни Вуглеводи Карбонові кислоти Складні ефіри Амінокислоти Нуклеїнові кислоти Білки
Органічні речовини – клас сполук, у склад яких входить вуглець (за виключенням карбідів, ціанідів, карбонатів, оксидів вуглецю та деяких інших сполук, що традиційно відносять до неорганічних) Фізичні і хімічні властивості органічних сполук передусім визначаються двома основними критеріями: Будова вуглецевого скелету Ациклічні Циклічні Функціональні групи Спирти, Феноли Альдегіди, Кетони Жири Аміни Вуглеводи Карбонові кислоти Складні ефіри Амінокислоти Нуклеїнові кислоти Білки
 Гумусові речовини • Гумінові кислоти – високомолекулярна фракція гумусових речовин, розчинна в лугах та нерозчинна в кислотах • Фульвокислоти – фракція гумусових речовин, розчинна в лугах і кислотах
Гумусові речовини • Гумінові кислоти – високомолекулярна фракція гумусових речовин, розчинна в лугах та нерозчинна в кислотах • Фульвокислоти – фракція гумусових речовин, розчинна в лугах і кислотах
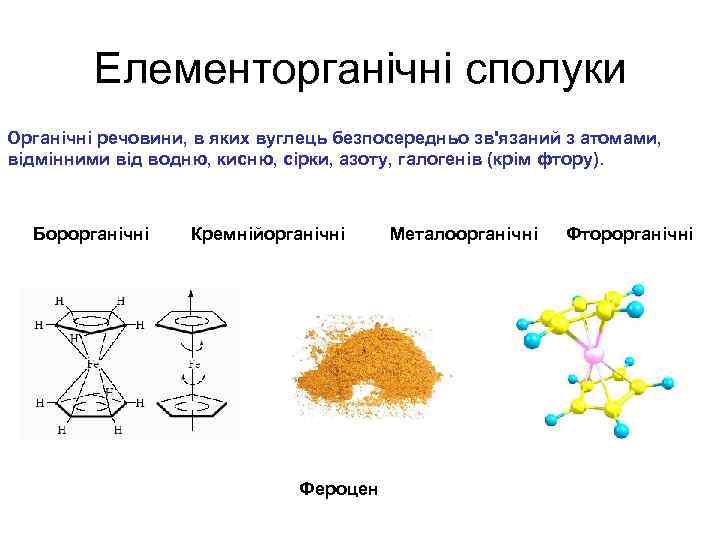 Елементорганічні сполуки Органічні речовини, в яких вуглець безпосередньо зв'язаний з атомами, відмінними від водню, кисню, сірки, азоту, галогенів (крім фтору). Борорганічні Кремнійорганічні Фероцен Металоорганічні Фторорганічні
Елементорганічні сполуки Органічні речовини, в яких вуглець безпосередньо зв'язаний з атомами, відмінними від водню, кисню, сірки, азоту, галогенів (крім фтору). Борорганічні Кремнійорганічні Фероцен Металоорганічні Фторорганічні
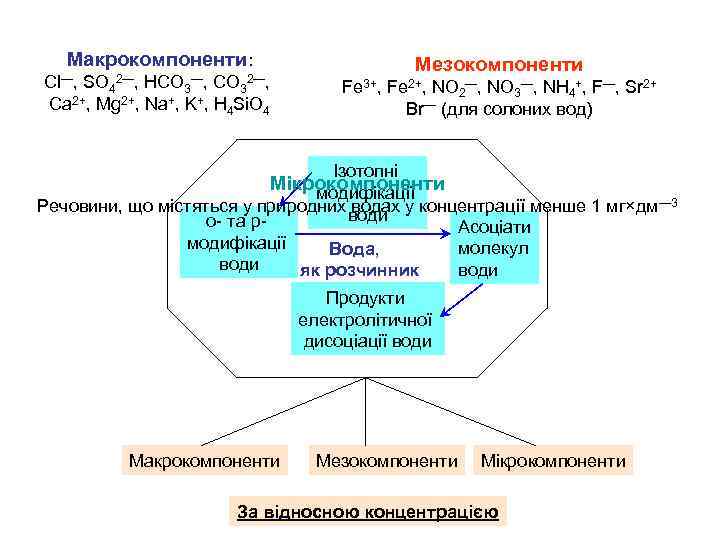 Макрокомпоненти: Cl—, SO 42—, HCO 3—, CO 32—, Ca 2+, Mg 2+, Na+, K+, H 4 Si. O 4 Мезокомпоненти Fe 3+, Fe 2+, NO 2—, NO 3—, NH 4+, F—, Sr 2+ Br— (для солоних вод) Ізотопні Мікрокомпоненти модифікації Речовини, що містяться у природних водах у концентрації менше 1 мг×дм— 3 води о- та р- Асоціати модифікації молекул Вода, води як розчинник Продукти електролітичної дисоціації води Макрокомпоненти Мезокомпоненти Мікрокомпоненти За відносною концентрацією
Макрокомпоненти: Cl—, SO 42—, HCO 3—, CO 32—, Ca 2+, Mg 2+, Na+, K+, H 4 Si. O 4 Мезокомпоненти Fe 3+, Fe 2+, NO 2—, NO 3—, NH 4+, F—, Sr 2+ Br— (для солоних вод) Ізотопні Мікрокомпоненти модифікації Речовини, що містяться у природних водах у концентрації менше 1 мг×дм— 3 води о- та р- Асоціати модифікації молекул Вода, води як розчинник Продукти електролітичної дисоціації води Макрокомпоненти Мезокомпоненти Мікрокомпоненти За відносною концентрацією
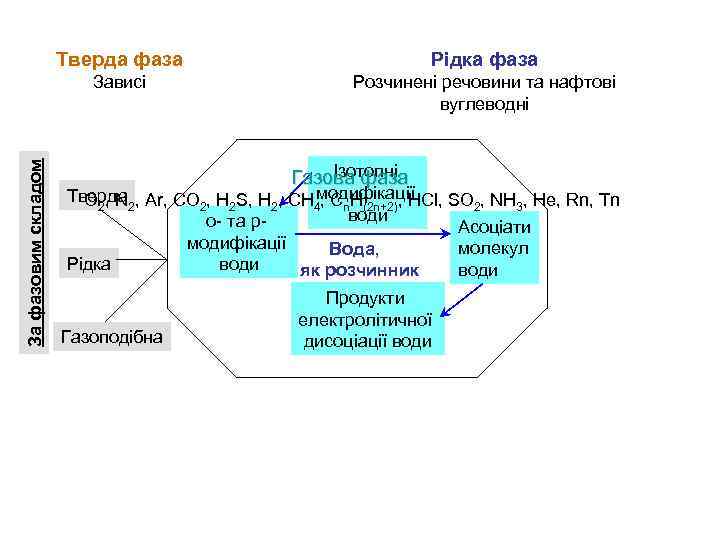 Рідка фаза Зависі За фазовим складом Тверда фаза Розчинені речовини та нафтові вуглеводні Ізотопні Газова фаза Тверда , Ar, CO , H S, H , CH модифікації O 2, N 2 2 4, Cn. H(2 n+2), HCl, SO 2, NH 3, He, Rn, Tn води о- та р- Асоціати модифікації молекул Вода, Рідка води як розчинник Газоподібна Продукти електролітичної дисоціації води
Рідка фаза Зависі За фазовим складом Тверда фаза Розчинені речовини та нафтові вуглеводні Ізотопні Газова фаза Тверда , Ar, CO , H S, H , CH модифікації O 2, N 2 2 4, Cn. H(2 n+2), HCl, SO 2, NH 3, He, Rn, Tn води о- та р- Асоціати модифікації молекул Вода, Рідка води як розчинник Газоподібна Продукти електролітичної дисоціації води
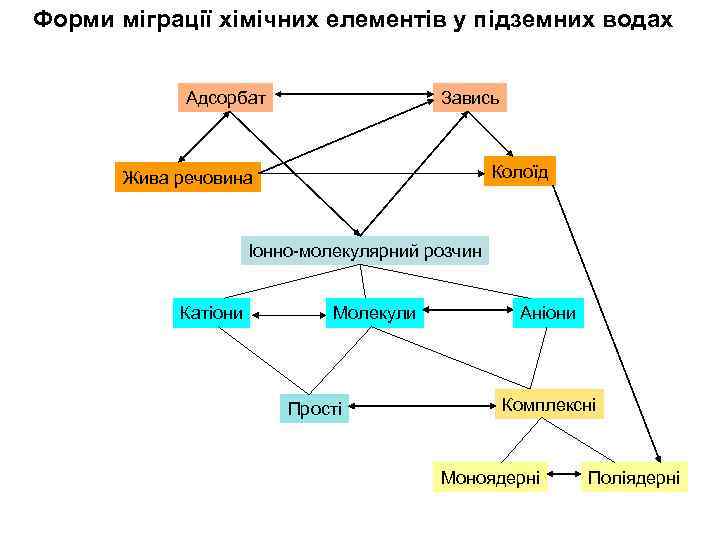 Форми міграції хімічних елементів у підземних водах Адсорбат Завись Колоїд Жива речовина Іонно-молекулярний розчин Катіони Молекули Прості Аніони Комплексні Моноядерні Поліядерні
Форми міграції хімічних елементів у підземних водах Адсорбат Завись Колоїд Жива речовина Іонно-молекулярний розчин Катіони Молекули Прості Аніони Комплексні Моноядерні Поліядерні
 Показники якості води 1 -а група: загальний вміст неорганічних речовин • Мінералізація ΣМ – загальний вміст усіх неорганічних розчинених у воді речовин [мг×дм— 3, г×кг— 1] • Сухий залишок – загальна маса речовин, отриманих після випарювання профільтрованої води та наступного висушування осаду до постійної ваги при температурі 110 о. С [мг×дм— 3, г×кг— 1] • Сума іонів – сумарна концентрація іонів, органічних і неорганічних речовин, розчинених у природних водах [мгекв. ×дм— 3, мг-екв. ×кг— 1, рідше - мг×дм— 3, г×кг— 1] • Солоність загальна – загальний вміст електролітів, розчинених у воді, за виключенням вільних кислот і лугів [мг×дм— 3, г×кг— 1] • Солоність океанологічна (S‰) – маса (г) сухого залишку 1 кг морської води за умови, що всі гідрокарбонати кальцію і магнію переведено в хлориди, органічну речовину спалено при 480 о. С, а Br— і I— заміщено еквівалентною кількістю Cl —
Показники якості води 1 -а група: загальний вміст неорганічних речовин • Мінералізація ΣМ – загальний вміст усіх неорганічних розчинених у воді речовин [мг×дм— 3, г×кг— 1] • Сухий залишок – загальна маса речовин, отриманих після випарювання профільтрованої води та наступного висушування осаду до постійної ваги при температурі 110 о. С [мг×дм— 3, г×кг— 1] • Сума іонів – сумарна концентрація іонів, органічних і неорганічних речовин, розчинених у природних водах [мгекв. ×дм— 3, мг-екв. ×кг— 1, рідше - мг×дм— 3, г×кг— 1] • Солоність загальна – загальний вміст електролітів, розчинених у воді, за виключенням вільних кислот і лугів [мг×дм— 3, г×кг— 1] • Солоність океанологічна (S‰) – маса (г) сухого залишку 1 кг морської води за умови, що всі гідрокарбонати кальцію і магнію переведено в хлориди, органічну речовину спалено при 480 о. С, а Br— і I— заміщено еквівалентною кількістю Cl —
 Показники якості води 2 -а група: лужно-кислотні властивості • Лужність загальна – сума речовин, що вступають в реакцію з катіоном водню: аніонів слабких кислот НСО 3—, CO 32—, H 2 PO 4—, HPO 42—, HSO 3—, SO 32—, HS—, S 2—, H 2 BO 32—, H 3 Si. O 4—, гумінових, фульво- та інших органічних кислот, гідроксил-іону ОН— та слабких основ (аміак, аналін, піридин та ін. ) [мг-екв. ×дм— 3] • Лужність вільна – сума карбонатів та гідроксил-іонів [мгекв. ×дм— 3] • Кислотність загальна – сума речовин, що вступають в реакцію з гідроксил-аніоном: вільних сильних HCl, H 2 SO 4, HSO 4— і слабких Н 2 CO 3, CH 3 COOH, H 2 S кислот, органічних кислот і катіонів слабких основ (NH 4+, Fe 2+, Fe 3+, Al 3+, органічних основ) [мг-екв. ×дм— 3] • Кислотність вільна – сума вільних сильних кислот [мгекв. ×дм— 3] • Водневий показник р. Н – логарифм концентрації Н+
Показники якості води 2 -а група: лужно-кислотні властивості • Лужність загальна – сума речовин, що вступають в реакцію з катіоном водню: аніонів слабких кислот НСО 3—, CO 32—, H 2 PO 4—, HPO 42—, HSO 3—, SO 32—, HS—, S 2—, H 2 BO 32—, H 3 Si. O 4—, гумінових, фульво- та інших органічних кислот, гідроксил-іону ОН— та слабких основ (аміак, аналін, піридин та ін. ) [мг-екв. ×дм— 3] • Лужність вільна – сума карбонатів та гідроксил-іонів [мгекв. ×дм— 3] • Кислотність загальна – сума речовин, що вступають в реакцію з гідроксил-аніоном: вільних сильних HCl, H 2 SO 4, HSO 4— і слабких Н 2 CO 3, CH 3 COOH, H 2 S кислот, органічних кислот і катіонів слабких основ (NH 4+, Fe 2+, Fe 3+, Al 3+, органічних основ) [мг-екв. ×дм— 3] • Кислотність вільна – сума вільних сильних кислот [мгекв. ×дм— 3] • Водневий показник р. Н – логарифм концентрації Н+
 Показники якості води 3 -а група: жорсткість води (вміст лужноземельних металів) • Загальна жорсткість – сумарна концентрація катіонів двовалентних лужноземельних металів Ca 2+, Mg 2+, а також Sr 2+, Ba 2+ [мг-екв. ×дм— 3] • Карбонатна жорсткість – кількість катіонів лужноземельних металів, еквівалентна кількості СО 32— та НСО 3— [мгекв. ×дм— 3] • Некарбонатна жорсткість – кількість катіонів лужноземельних металів, еквівалентна аніонам усіх кислот, окрім вугільної [мг-екв. ×дм— 3] • Усувна жорсткість – експериментально визначувана величина зменшення жорсткості після тривалого кипіння води [мг-екв. ×дм— 3] • Неусувна жорсткість – різниця між загальною і усувною жорсткістю [мг-екв. ×дм— 3]
Показники якості води 3 -а група: жорсткість води (вміст лужноземельних металів) • Загальна жорсткість – сумарна концентрація катіонів двовалентних лужноземельних металів Ca 2+, Mg 2+, а також Sr 2+, Ba 2+ [мг-екв. ×дм— 3] • Карбонатна жорсткість – кількість катіонів лужноземельних металів, еквівалентна кількості СО 32— та НСО 3— [мгекв. ×дм— 3] • Некарбонатна жорсткість – кількість катіонів лужноземельних металів, еквівалентна аніонам усіх кислот, окрім вугільної [мг-екв. ×дм— 3] • Усувна жорсткість – експериментально визначувана величина зменшення жорсткості після тривалого кипіння води [мг-екв. ×дм— 3] • Неусувна жорсткість – різниця між загальною і усувною жорсткістю [мг-екв. ×дм— 3]
 Показники якості води 4 -а група: вміст органічних речовин • Загальна окиснюваність – загальний вміст всіх речовин, що окиснюються при кип’ятінні в середовищі K 2 Cr 2 O 7+50% H 2 SO 4 [мг О 2×дм— 3] • Хімічне поглинання кисню (ХПК) або біхроматна окиснюваність – кисневий еквівалент тільки органічних речовин, що окиснюються в тих же умовах • Перманганатна окиснюваність – загальний вміст всіх органічних речовин, що окиснюються при кип’ятінні з 0, 01 н розчином KMn. O 4 [мг О 2×дм— 3] • Органічний вуглець Сорг. – кількість вуглецю, що міститься у розчиненій органічній речовині [мг×дм— 3] • Біохімічне споживання кисню (БСК) – повне – відображає вміст у воді органічних речовин, що піддаються біохімічному розкладенню в аеробних умовах [мг О 2×дм— 3] • БСКn - те ж саме, де n – кількість діб.
Показники якості води 4 -а група: вміст органічних речовин • Загальна окиснюваність – загальний вміст всіх речовин, що окиснюються при кип’ятінні в середовищі K 2 Cr 2 O 7+50% H 2 SO 4 [мг О 2×дм— 3] • Хімічне поглинання кисню (ХПК) або біхроматна окиснюваність – кисневий еквівалент тільки органічних речовин, що окиснюються в тих же умовах • Перманганатна окиснюваність – загальний вміст всіх органічних речовин, що окиснюються при кип’ятінні з 0, 01 н розчином KMn. O 4 [мг О 2×дм— 3] • Органічний вуглець Сорг. – кількість вуглецю, що міститься у розчиненій органічній речовині [мг×дм— 3] • Біохімічне споживання кисню (БСК) – повне – відображає вміст у воді органічних речовин, що піддаються біохімічному розкладенню в аеробних умовах [мг О 2×дм— 3] • БСКn - те ж саме, де n – кількість діб.
 Показники якості води 5 -а група: інші показники • Окиснювально-відновний потенціал Eh – характеризує потужність і спрямованість окиснювально-відновних процесів, виражається потенціалом (м. В) вимірювального електроду відносно нормального водневого електроду. • Важкі метали, розташовані в таблиці Мендєлєєва після заліза, - для екологічних завдань та при пошуках родовищ (сума Zn, Cu, Pb – індикатор сульфідних родовищ) [мкг×дм— 3] • Загальна газонасиченість – сумарний вміст усіх газоподібних компонентів, розчинених у воді [мг×дм— 3]
Показники якості води 5 -а група: інші показники • Окиснювально-відновний потенціал Eh – характеризує потужність і спрямованість окиснювально-відновних процесів, виражається потенціалом (м. В) вимірювального електроду відносно нормального водневого електроду. • Важкі метали, розташовані в таблиці Мендєлєєва після заліза, - для екологічних завдань та при пошуках родовищ (сума Zn, Cu, Pb – індикатор сульфідних родовищ) [мкг×дм— 3] • Загальна газонасиченість – сумарний вміст усіх газоподібних компонентів, розчинених у воді [мг×дм— 3]


