1227080.ppt
- Количество слайдов: 21

Хімічні властивості алканів Розробила вчитель хімії Тетерівської ЗОШ І-ІІІ ст. ім. Ніни Сосніної Кисіль Юлія Вячеславівна

Мета уроку: Ознайомитись з хімічними властивостями метану та його гомологів; n навчитись складати відповідні рівняння реакцій; n установити залежність між будовою алканів та їхніми хімічними властивостями. n

Експрес-контроль 1. 2. 3. 4. 5. 6. 7. 8. Найпростіша органічна речовина – це… Загальна формула алканів – … Гомологи – це речовини, які … Ізомери – це речовини, які … Гомологічна різниця – це група атомів … За кімнатної температури газуватими є тільки алкани з числом атомів Карбону … Молекула метану має форму … Третім членом гомологічного ряду алканів є …

Відповіді на завдання: 1. 2. 3. 4. 5. 6. 7. 8. …метан. …Сn. H 2 n+2. …мають подібну будову, але різняться за складом на одну або декілька груп СН 2. … мають однакову молекулярну формулу, але різну просторову будову. …CH 2. … від 1 до 4. …СН 4. …пропан.

Хімічні властивості алканів n Алкани хімічно неактивні речовини, завдяки цьому їх називають парафінами. n Алкани не взаємодіють із розчинами кислот і лугів. n Алкани не окиснюються розчином калій перманганату.

Алкани – неактивні речовини

Взаємодія з киснем n Алкани дуже добре взаємодіють з киснем. n Метан при підпалюванні згоряє блідосинім полум'ям, погано помітним на яскравому сонячному світлі: СН 4 + 2 О 2 → CO 2 +2 H 2 O n При цьому виділяється велика кількість теплоти – близько 50 к. Дж на 1 г вуглеводню.

Небезпечна суміш Суміші метану з повітрям (10% метану) – вибухонебезпечні. n При використанні газових плит необхідно постійно стежити за тим, щоб полум'я не згасло. n У побутовий газ додають невелику кількість меркаптану – речовини з огидним запахом. n

Окиснення гомологів метану n Повне окиснення до вуглекислого газу відбувається тільки при горінні в надлишку кисню: 2 С 6 Н 14 + 19 О 2 → 12 CO 2 + 14 H 2 O n При нестачі кисню утворюється надзвичайно отруйний чадний газ: 2 С 6 Н 14 + 13 О 2 → 12 CO + 14 H 2 O

Горіння вищих алканів Алкани з високим числом атомів Карбону при горінні можуть утворювати вуглець. n Побутові свічки, що складаються із суміші твердих алканів, при горінні утворюють полум'я, що утворює кіптяву. n Кіптява – це частинки сажі (вуглецю), які не встигають згоріти: n 2 С 20 Н 42 + 21 О 2 → 40 C + 42 H 2 O

Горіння парафіну, визначення якісного складу продуктів горіння

Взаємодія з галогенами Реакція заміщення з галогенами називається галогенуванням. n Взаємодія алканів із хлором або бромом відбувається тільки при освітленні або нагріванні: n

Взаємодія з галогенами n У випадку надлишку галогену можуть заміщуватися декілька атомів Гідрогену: СН 4 + 3 Cl 2 → CHCl 3 + 3 HCl n При достатній кількості галогену можуть заміщуватися усі атоми Гідрогену: CH 4 + 4 Cl 2 → CCl 4 + 4 HCl

Назви утворених продуктів n Назви утворених продуктів походять від назв алканів. n CH 3 Cl – хлорметан. n CHCl 3 – трихлорметан (хлороформ). n ССl 4 – тетрахлорметан.

Термічний розклад n При сильному нагріванні (понад 1000 о. С) алкани розкладаються з утворенням вуглецю і водню:
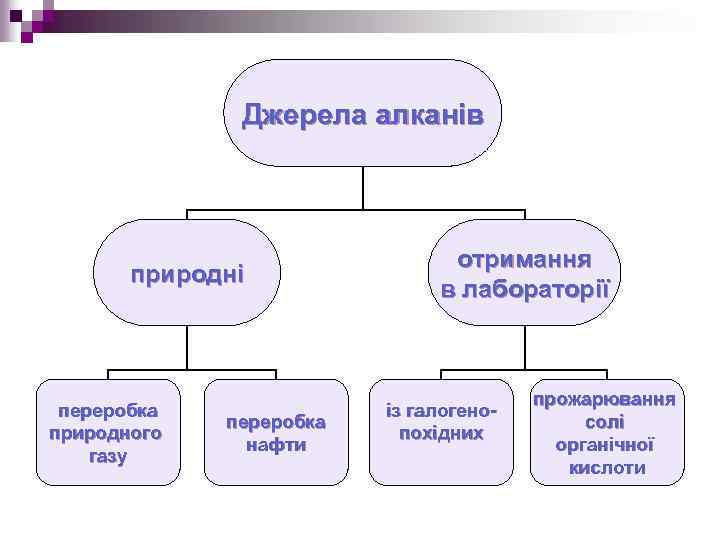
Джерела алканів природні переробка природного газу переробка нафти отримання в лабораторії із галогенопохідних прожарювання солі органічної кислоти
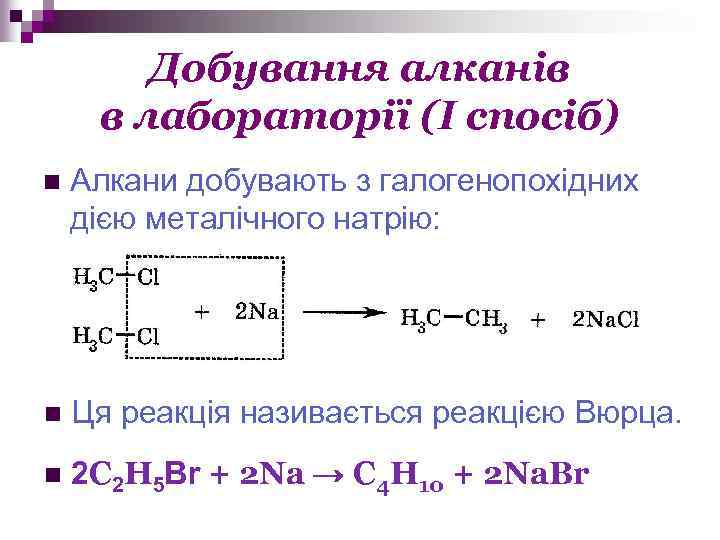
Добування алканів в лабораторії (І спосіб) n Алкани добувають з галогенопохідних дією металічного натрію: n Ця реакція називається реакцією Вюрца. n 2 C 2 H 5 Br + 2 Na → C 4 H 10 + 2 Na. Br

Добування алканів в лабораторії (ІІ спосіб) n Алкани добувають прожарюванням солі органічної (карбонової) кислоти у присутності лугів: n Ця реакція називається методом Дюма.

Завдання на закріплення знань: 1. Напишіть рівняння реакції горіння а) пропану; б) пентану. 2. Напишіть рівняння реакції одержання дихлоретану з етану. 3. Напишіть рівняння термічного розкладу пропану. 4. Складіть рівняння реакцій за такою схемою: СН 4 → CH 3 Br → C 2 H 6 → CO 2

Відповіді на завдання: 1. а) C 3 H 8 + 5 O 2 → 3 CO 2 + 4 H 2 O б) C 5 H 12 + 8 O 2 → 5 CO 2 + 6 H 2 O 2. C 2 H 6 + 2 Cl 2 → C 2 H 4 Cl 2 + 2 HCl 3. C 3 H 8 → 3 C +4 H 2 4. 1) CH 4 +Br 2 → CH 3 Br + HBr 2) 2 CH 3 Br + 2 Na → C 2 H 6 + 2 Na. Br 3) 2 C 2 H 6 + 7 O 2 → 4 CO 2 + 6 H 2 O

Домашнє завдання n Вивчити § 20, стор. 128 -131, § 21, стор. 137 -139, n виконати завдання № 7, 8, стор. 133, № 11, 12 стор. 141, n додаткове завдання № 14, 15 стор. 133, № 16 стор. 141.
1227080.ppt