07 Гидрофобные вещества.ppt
- Количество слайдов: 17
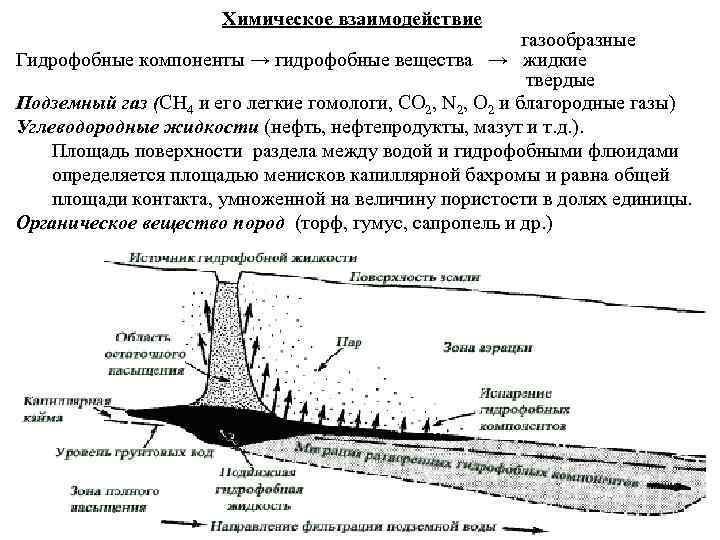
Химическое взаимодействие газообразные Гидрофобные компоненты → гидрофобные вещества → жидкие твердые Подземный газ (CH 4 и его легкие гомологи, CO 2, N 2, O 2 и благородные газы) Углеводородные жидкости (нефть, нефтепродукты, мазут и т. д. ). Площадь поверхности раздела между водой и гидрофобными флюидами определяется площадью менисков капиллярной бахромы и равна общей площади контакта, умноженной на величину пористости в долях единицы. Органическое вещество пород (торф, гумус, сапропель и др. )

Массообмен с подземным газом Подземный газ – газовый раствор в условиях геологической среды. 1. Обмен газовыми компонентами, для которых . и ai = fi = Pi 2. Смешиваются между собой в любых пропорциях. 3. Концентрации в объемных и мольных долях имеют одинаковые значения, т. е. Co, i= Ci и 4. В подземном газе объем и давление связаны уравнением: PV = NRTZ , N –число молей, Z- коэффициент сжимаемости, который в случае идеального газа равен 1. При низких давлениях парциальное давление:

Лекция 6 Пример 1: Определить парциальное давление компонентов в подземном газе зоны аэрации, если его состав, как в атмосфере: N 2 78, 09%, O 2 20, 9%, Ar 0, 93% и CO 2 0, 03%. Так как давление газа в зоне аэрации P ≈ 101 к. Па, а Pi = 0, 01 PCi парциальные давления имеют следующие значения: N 2 - 78, 9 к. Па, O 2 - 21, 1 к. Па, Ar - 0, 94 к. Па, CO 2 - 0, 03 к. Па. Пример 2: В газах зоны аэрации обнаружен бензол с концентрацией 503 мкг∙л-1. Необходимо определить его парциальное давление. Молекулярный вес бензола 78, 11 г∙моль-1. Так как R=0, 082054 л∙атм∙град-1 моль-1, T=293 K. Свb=503 мкг∙л-1× 10 -6 г∙ мкг-1 =0, 503∙ 10 -3 г∙л-1.

Параметры равновесия подземного газа с водой Если снижать давление на воду, то в конце концов появятся пузырьки газа. Давление выделения первого бесконечно малого пузырька – давление насыщения. Давление насыщения Pн ≤ P Коэффициент насыщения Pн/P <1 Коэффициенты растворимости и распределения Коэффициенты растворимости: Коэффициент растворимости Генри: Hi –коэффициентом растворимости в атм·м 3·моль-1) Коэффициентом растворимости Бунзена: Bi- коэффициентом растворимости в см 3·л-1· атм-1
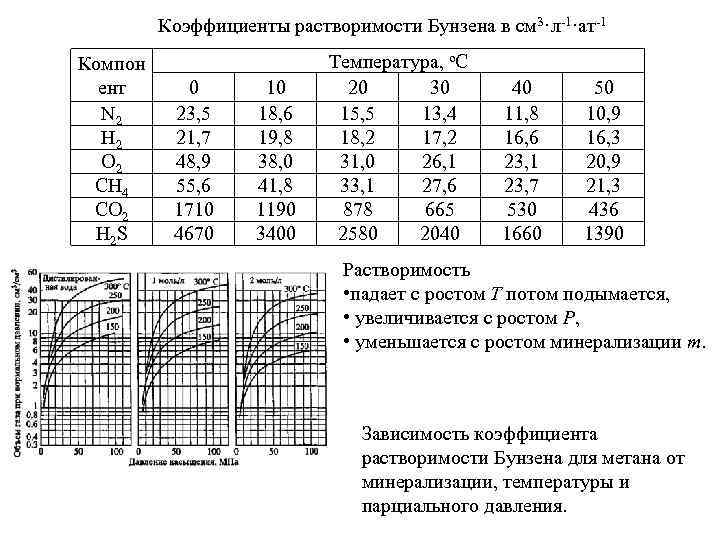
Коэффициенты растворимости Бунзена в см 3·л-1·ат-1 Компон ент N 2 H 2 O 2 CH 4 CO 2 H 2 S 0 23, 5 21, 7 48, 9 55, 6 1710 4670 10 18, 6 19, 8 38, 0 41, 8 1190 3400 Температура, o. C 20 30 15, 5 13, 4 18, 2 17, 2 31, 0 26, 1 33, 1 27, 6 878 665 2580 2040 40 11, 8 16, 6 23, 1 23, 7 530 1660 50 10, 9 16, 3 20, 9 21, 3 436 1390 Растворимость • падает с ростом T потом подымается, • увеличивается с ростом P, • уменьшается с ростом минерализации m. Зависимость коэффициента растворимости Бунзена для метана от минерализации, температуры и парциального давления.
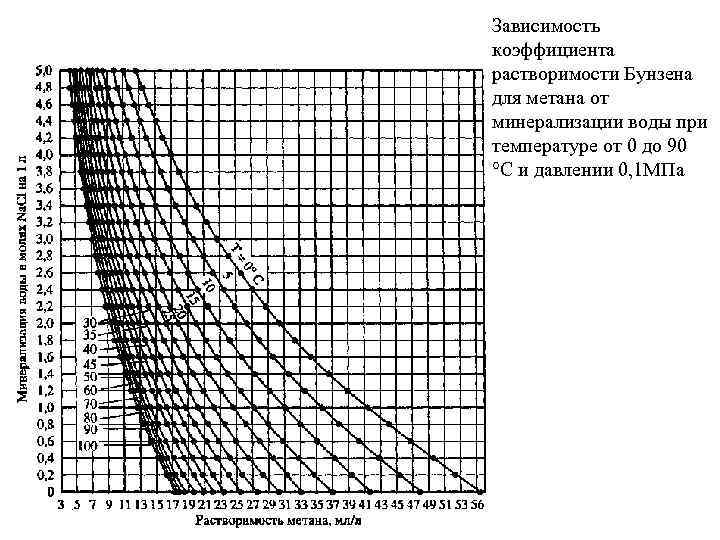
Зависимость коэффициента растворимости Бунзена для метана от минерализации воды при температуре от 0 до 90 °С и давлении 0, 1 МПа

Коэффициент распределения Определение парциального давления: Учет минерализации воды: Коэфициент Сеченова - Si m - минерализация воды /58 Показатели равновесия: или

Массообмен с гидрофобными жидкостями. Подвижные гидрофобные жидкости и неподвижное органическое вещество. 1. При Ci =1 давление насыщенного пара <1 атм (760 мм рт. ст. ), и 2. Закон Рауля: 3. Концентрации: средняя молекулярная масса –Mср. (кг/моль), средняя плотность гидрофобной жидкости - ρср (мг/см 3) средний молекулярный объем – νср. (м 3/моль)

Параметры равновесия с подземным газом, водой и породой С подземным газом: С подземной водой: Растворимость в воде – максимальное содержание в чистой воде в стандартных условиях Св, max, i , т. е. при pi= Коэффициент растворимости Генри в воде: • • Классификация (Дональд Маккей и Янг Шу, 1981) по летучести (атм·м 3/моль): Высоко летучие: испарение быстрое, если Hi более 10 -3 Летучие: испарение значительное, если Hi от 10 -3 до 10 -5 Полулетучие: испарение медленное, если Hi от10 -5 до 3× 10 -7 Нелетучие: испарение не значительное, если Hi менее 3× 10 -7 атм·м 3/мол
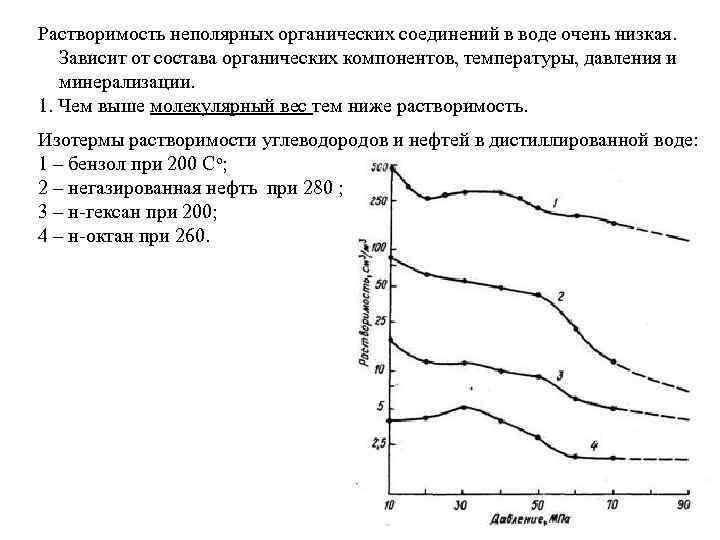
Растворимость неполярных органических соединений в воде очень низкая. Зависит от состава органических компонентов, температуры, давления и минерализации. 1. Чем выше молекулярный вес тем ниже растворимость. Изотермы растворимости углеводородов и нефтей в дистиллированной воде: 1 – бензол при 200 Co; 2 – негазированная нефть при 280 ; 3 – н-гексан при 200; 4 – н-октан при 260.
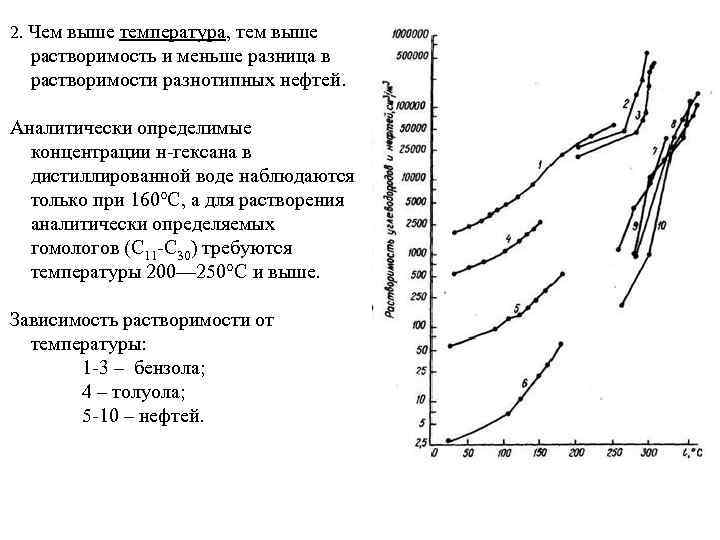
2. Чем выше температура, тем выше растворимость и меньше разница в растворимости разнотипных нефтей. Аналитически определимые концентрации н-гексана в дистиллированной воде наблюдаются только при 160°С, а для растворения аналитически определяемых гомологов (C 11 -C 30) требуются температуры 200— 250°С и выше. Зависимость растворимости от температуры: 1 -3 – бензола; 4 – толуола; 5 -10 – нефтей.
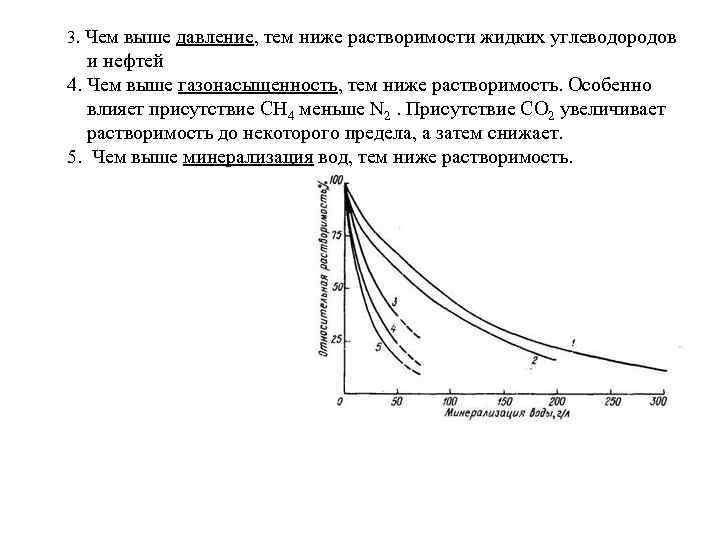
3. Чем выше давление, тем ниже растворимости жидких углеводородов и нефтей 4. Чем выше газонасыщенность, тем ниже растворимость. Особенно влияет присутствие CH 4 меньше N 2. Присутствие CO 2 увеличивает растворимость до некоторого предела, а затем снижает. 5. Чем выше минерализация вод, тем ниже растворимость.

Коэффициент распределения: Для чистых растворителей: ; по октанолу (CH 3(CH 2)6 CH 2 OH): безразмерная величина Для сложных растворов: на грамм ОВ (мл/г): на грамм Cорг (см 3 г-1): средний молекулярный объем – νср. (м 3/моль)
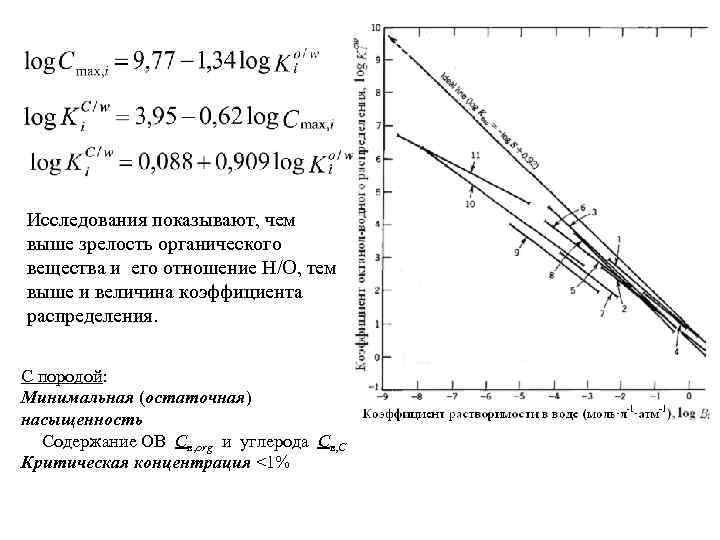
Исследования показывают, чем выше зрелость органического вещества и его отношение H/O, тем выше и величина коэффициента распределения. С породой: Минимальная (остаточная) насыщенность Содержание ОВ Cв, org и углерода Cв, C Критическая концентрация <1%
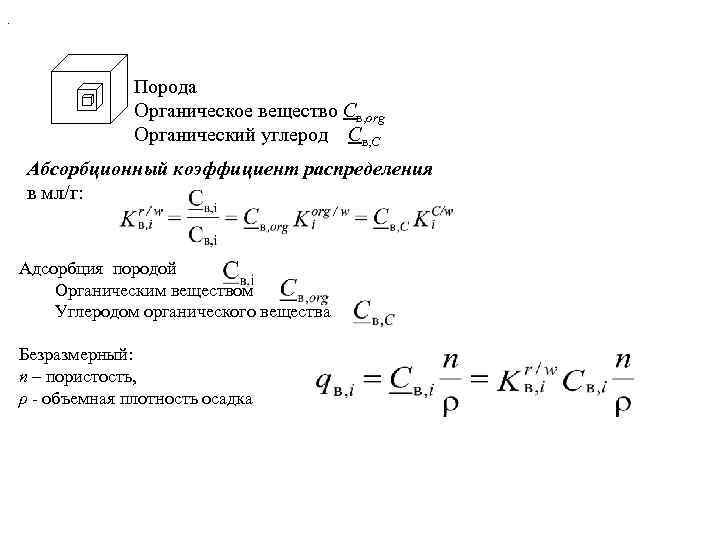
. Порода Органическое вещество Cв, org Органический углерод Cв, C Абсорбционный коэффициент распределения в мл/г: Адсорбция породой Органическим веществом Углеродом органического вещества Безразмерный: n – пористость, ρ - объемная плотность осадка

Распределение гидрофобных компонентов Morg - органическим веществом вмещающего их грунта с массой Подземный газ Нефть Порода

Подземная вода Подземный газ Нефть Порода
07 Гидрофобные вещества.ppt