Lecture_3_Khim_ravnovesie.ppt
- Количество слайдов: 44

ХИМИЧЕСКОЕ РАВНОВЕСИЕ

УРАВНЕНИЯ ОБЪЕДИНЕННОГО ПЕРВОГО И ВТОРОГО ЗАКОНОВ ТЕРМОДИНАМИКИ d. U = Td. S – pd. V + А max d. H = Td. S + Vdp + А max d. F = – Sd. T – pd. V + А max d. G = – Sd. T + Vdp + А max U(S, V), U(S, p), F(T, V), G(T, p) – термодинамические потенциалы 2

ВЗАИМОСВЯЗЬ МЕЖДУ ТЕРМОДИНАМИЧЕСКИМИ ФУНКЦИЯМИ H = U + p. V F = U – TS G = H – TS = = U + p. V – TS = = F + p. V 3

ХИМИЧЕСКИЙ ПОТЕНЦИАЛ d. U = Td. S – pd. V + Величина ( U/ ni)S, V, n, т. е. приращение внутренней энергии данной фазы системы при увеличении массы данного вещества на единицу, если объем, энтропия и массы всех остальных веществ остаются постоянными, называется химическим потенциалом і i-го компонента. 4

5

УСЛОВИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ Изменение энергии Гиббса системы, в которой протекает химическая реакция, определяется уравнением d. G = – Sd. T + Vdp + іdnі 6

ХИМИЧЕСКАЯ ПЕРЕМЕННАЯ - химическая переменная, или число пробегов химической реакции (степень продвижения реакции) 7

Выразив dnі через d , получим для изменения энергии Гиббса реакции: d. G = – Sd. T + Vdp + і іd Если при p, T = const реакция протекает самопроизвольно, то d. G < 0 и, следовательно, і і < 0 8

Условия химического равновесия в общей форме Если реакция протекает при постоянных температуре и объеме, условие равновесия имеет вид: 9

ЗАКОН ДЕЙСТВИЯ МАСС Рассмотрим реакцию, протекающую в газовой фазе 10

В состоянии равновесия 11

КОНСТАНТА ХИМИЧЕСКОГО РАВНОВЕСИЯ 1 Отсюда 12

КОНСТАНТА ХИМИЧЕСКОГО РАВНОВЕСИЯ 2 или 13

Константу равновесия можно также выражать через числа молей nі, молярные концентрации сі или мольные доли хі (Р – общее давление, V – общий объем системы) 14

где – разность между суммарным числом молей продуктов реакции и исходных веществ 15

В общем случае численные значения констант равновесия Kp, Kn, Kс и Kх не совпадают и лишь при = 0, т. е. когда реакция протекает без изменения числа молей, константы равновесия имеют одинаковое значение, независимо от способа выражения состава 16

17

Величина константы равновесия зависит от способа записи уравнения химической реакции. 3 H 2 + N 2 = 2 NH 3 3/2 Н 2 + 1/2 N 2 = NH 3 18

Для обратной реакции разложения аммиака 2 NH 3 = 3 H 2 + N 2 19

УРАВНЕНИЕ ИЗОТЕРМЫ ХИМИЧЕСКОЙ РЕАКЦИИ 20
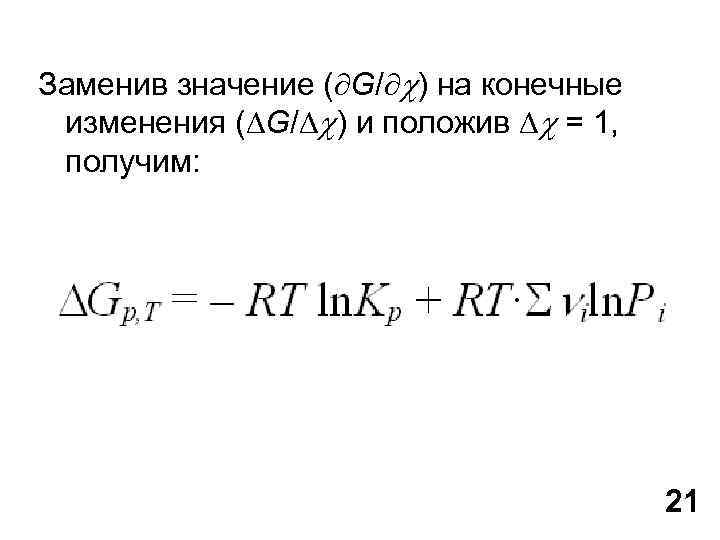
Заменив значение ( G/ ) на конечные изменения ( G/ ) и положив = 1, получим: 21

22

23

24

25

26

27

Если парциальные давления всех участников реакции в неравновесной смеси равны единице (Рі = 1), то где - изменение стандартной энергии Гиббса реакции 28

Величины Gp, T и Gop, T являются количественной мерой химического сродства (стандартного химического сродства) реагирующих веществ, т. е. способности веществ вступать в химическое взаимодействие друг с другом 29

ВЛИЯНИЕ ВНЕШНИХ УСЛОВИЙ НА ПОЛОЖЕНИЕ РАВНОВЕСИЯ Принцип подвижного равновесия (принцип Ле-Шателье): При внешнем воздействии на систему, находящуюся в равновесии, в ней происходят изменения, направленные против этих внешних воздействий 30

Повышение внешнего давления 1 смещает равновесие в сторону уменьшения числа молей реагирующих веществ. Kp, зависит только от температуры, но не зависит от общего давления: 31

Повышение внешнего давления 2 При < 0 величина ( ln. Kх/ Р)T > 0, т. е. равновесие смещается в сторону уменьшения числа молей реагирующих веществ. 32

Введение какого-либо из реагирующих веществ смещает равновесие в сторону поглощения этого вещества. Если в равновесную газовую смесь вводить инертный газ при постоянном объеме, то общее давление будет возрастать, т. е. инертная добавка влияет на смещение равновесия так же, как повышение давления. 33

• Введение инертной добавки при постоянном давлении смещает равновесие в сторону увеличения числа молей реагирующих веществ. • Повышение температуры смещает равновесие в сторону эндотермической реакции. 34

35

36

37

ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА ХИМИЧЕСКОЕ РАВНОВЕСИЕ 1 38

ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА ХИМИЧЕСКОЕ РАВНОВЕСИЕ 2 39

УРАВНЕНИЕ ИЗОБАРЫ ВАНТ-ГОФФА УРАВНЕНИЕ ИЗОХОРЫ ВАНТ-ГОФФА 40

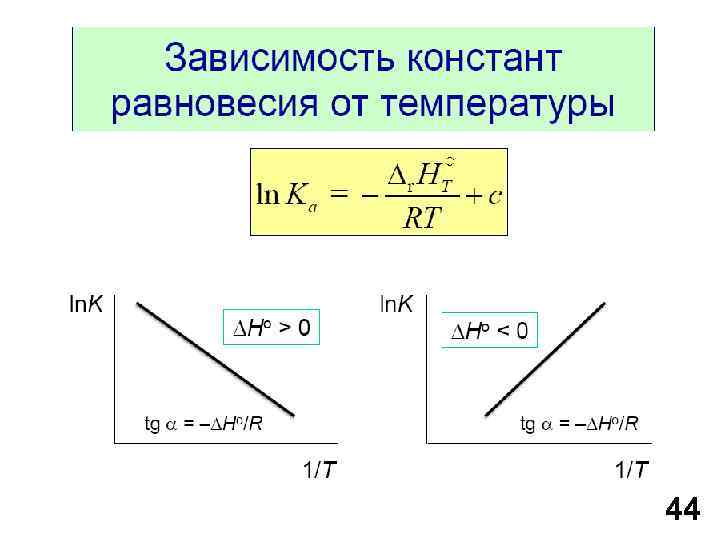
Для эндотермических реакций ( H > 0 или U > 0) величина dln. Kр/d. T > 0, т. е. при повышении температуры возрастает константа равновесия для эндотермической реакции, что согласуется с принципом подвижного равновесия. 41

ИНТЕГРАЛЬНАЯ ФОРМА ИЗОБАРЫ ВАНТ-ГОФФА 1 K 1 и K 2 – константы равновесия при температурах T 1 и T 2 соответственно. 42

ИНТЕГРАЛЬНАЯ ФОРМА ИЗОБАРЫ ВАНТ-ГОФФА 2 В небольшом температурном интервале можно считать величину Н постоянной, тогда 43
44
Lecture_3_Khim_ravnovesie.ppt