6-РАВНОВЕСИЕ.ppt
- Количество слайдов: 26
 Химическое равновесие Термодинамические параметры: T; P; i; Сi – const 1. Термодинамическое условие равновесия - r. G = 0 2. Кинетическое условие равновесия реакция а. A + b. B с. C + d. D Константа равновесия[f(T)] (кинетические условия)
Химическое равновесие Термодинамические параметры: T; P; i; Сi – const 1. Термодинамическое условие равновесия - r. G = 0 2. Кинетическое условие равновесия реакция а. A + b. B с. C + d. D Константа равновесия[f(T)] (кинетические условия)
 Энергия Гиббса реакции в нестандартных условиях реакция а. A + b. B = с. C + d. D r. G 0 = ( c f. G 0 C + d f. G 0 D ) – ( a f. G 0 A + b f. G 0 B ) С 0 =1 моль/л С С 0 r. Gi = r. G 0 i + R T ln. Ci – безразмерная концентрация – мольная доля; Сi – [ моль/л ] – относительное парциальное давление [атм], p 0 =1, 013. 105 Па r. G = ( c f. G 0 C+ d f. G 0 D ) – ( a f. G 0 A+ b f. G 0 B) + R T ( c ln. СC+ d ln. CD– a ln. CA– b ln. CB)
Энергия Гиббса реакции в нестандартных условиях реакция а. A + b. B = с. C + d. D r. G 0 = ( c f. G 0 C + d f. G 0 D ) – ( a f. G 0 A + b f. G 0 B ) С 0 =1 моль/л С С 0 r. Gi = r. G 0 i + R T ln. Ci – безразмерная концентрация – мольная доля; Сi – [ моль/л ] – относительное парциальное давление [атм], p 0 =1, 013. 105 Па r. G = ( c f. G 0 C+ d f. G 0 D ) – ( a f. G 0 A+ b f. G 0 B) + R T ( c ln. СC+ d ln. CD– a ln. CA– b ln. CB)
 4. 7 Равновесие – термодинамические условия ( r. G = 0) Равновесные концентрации (пост. ) Стандартная(термодинамическая) константа равнов. хим. реакции. Т/д условие равновесия (Зависит от Т и т/д функций) r. G 0 T + R T ln. K 0 = 0 r. G 0 T = r. Н 0 T – Т r. S 0 T
4. 7 Равновесие – термодинамические условия ( r. G = 0) Равновесные концентрации (пост. ) Стандартная(термодинамическая) константа равнов. хим. реакции. Т/д условие равновесия (Зависит от Т и т/д функций) r. G 0 T + R T ln. K 0 = 0 r. G 0 T = r. Н 0 T – Т r. S 0 T
 Константа равновесия К, её размерность. Связь между К (кинетич. ) и стандартной К 0 (термодинам. ) К≡KX - концентрации задаются мольными долями [безразмерная величина] К≡Kp - концентрации задаются парциальными давлениями - [(Па) ] = ( c+ d) - ( a+ b) К≡KC – концентрации задаются молярной концентрацией - [(моль/л) ] р0 = 1, 013 105 Па стандарт. давление
Константа равновесия К, её размерность. Связь между К (кинетич. ) и стандартной К 0 (термодинам. ) К≡KX - концентрации задаются мольными долями [безразмерная величина] К≡Kp - концентрации задаются парциальными давлениями - [(Па) ] = ( c+ d) - ( a+ b) К≡KC – концентрации задаются молярной концентрацией - [(моль/л) ] р0 = 1, 013 105 Па стандарт. давление
 Сдвиг равновесия. Определение направления сдвига. Правило Ле шателье Изобара реакции Р-const r. Н 0 0 (экзотерм. реакция) – K 0(T) убывающая функция(↑Т, К 0↓) r. Н 0 0 (эндотерм. реакция) – K 0(T) возрастающая функция(↑Т, К 0↑) Изотерма реакции T-const r. G 0 T = – R T ln. K 0 r. G<0 r. G>0 r. G=0
Сдвиг равновесия. Определение направления сдвига. Правило Ле шателье Изобара реакции Р-const r. Н 0 0 (экзотерм. реакция) – K 0(T) убывающая функция(↑Т, К 0↓) r. Н 0 0 (эндотерм. реакция) – K 0(T) возрастающая функция(↑Т, К 0↑) Изотерма реакции T-const r. G 0 T = – R T ln. K 0 r. G<0 r. G>0 r. G=0
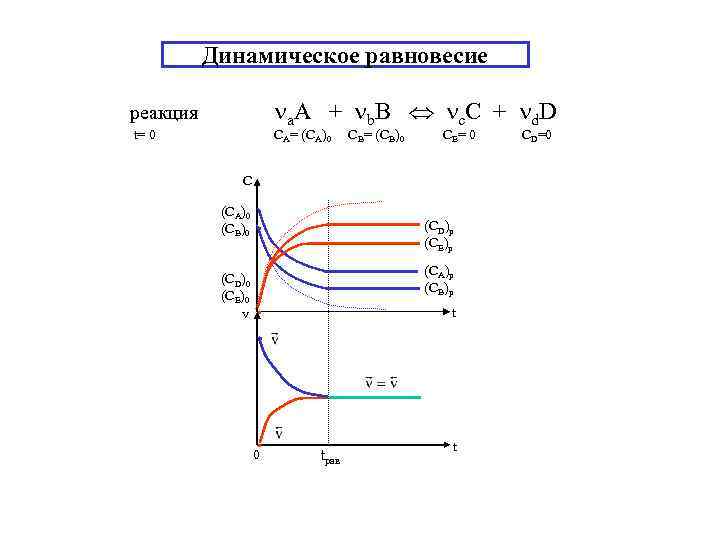 Динамическое равновесие а. A + b. B с. C + d. D реакция t= 0 CA= (CA)0 CB= (CB)0 CE= 0 С (CA)0 • (CB)0 • (CD)p (CE)p (CA)p (CB)p (CD)0 (CE)0 v • t • • 0 tрав t CD=0
Динамическое равновесие а. A + b. B с. C + d. D реакция t= 0 CA= (CA)0 CB= (CB)0 CE= 0 С (CA)0 • (CB)0 • (CD)p (CE)p (CA)p (CB)p (CD)0 (CE)0 v • t • • 0 tрав t CD=0
 Расчет равновесного состава(концентраций) газовой смеси 1. Расчет К 0(Т) Для определенной Т рассчитывают r. G 0(T)= r. H 0(T) –Т· r. S 0(T). Затем 2. Расчет КX или Кр КX Xi при Р –const (р0 = 1, 013 105 Па-стандартн. давление) Кр рi - при V - const
Расчет равновесного состава(концентраций) газовой смеси 1. Расчет К 0(Т) Для определенной Т рассчитывают r. G 0(T)= r. H 0(T) –Т· r. S 0(T). Затем 2. Расчет КX или Кр КX Xi при Р –const (р0 = 1, 013 105 Па-стандартн. давление) Кр рi - при V - const
 Пример. Диссоциация АВ при Р -const и температуре Т АВ = А + В t=0 ni равновесие САВ 0 САВ-z Xi z z
Пример. Диссоциация АВ при Р -const и температуре Т АВ = А + В t=0 ni равновесие САВ 0 САВ-z Xi z z
 Равновесие в растворах(дисперсных системах) Раствор - гомогенная однофазная многокомпонентная система, образованная двумя или более веществами. По агрегатному состоянию - газовые, жидкие и твёрдые растворы. Основн. способ получения жидк. р-ров - растворение А - растворенное вещество-твёрдое, жидкое, газ (дисперсная фаза) А+В В – растворитель (дисперсионная среда) А+В – раствор (дисперсная система) Концентрация раствора – важная характеристика раствора (относительное соотношение количеств растворенного вещества и растворителя) • массовая доля • молярная концентрация • нормальная концентр. • моляльная концентрация • массовая конц. (г/л), процент. конц. • мольная доля
Равновесие в растворах(дисперсных системах) Раствор - гомогенная однофазная многокомпонентная система, образованная двумя или более веществами. По агрегатному состоянию - газовые, жидкие и твёрдые растворы. Основн. способ получения жидк. р-ров - растворение А - растворенное вещество-твёрдое, жидкое, газ (дисперсная фаза) А+В В – растворитель (дисперсионная среда) А+В – раствор (дисперсная система) Концентрация раствора – важная характеристика раствора (относительное соотношение количеств растворенного вещества и растворителя) • массовая доля • молярная концентрация • нормальная концентр. • моляльная концентрация • массовая конц. (г/л), процент. конц. • мольная доля
 Электролитическая диссоциация АВ A+ + B- AB АВ A+ + B- С 0 - общая концентрация СД - конц. молекул в виде ионов СД = [A+]=[B-]=αС 0 [AB]=С 0 -αС 0 Степень диссоциации α>50%, <5%, 5<α<50% Сильные, слабые, средней силы электролиты Константа диссоциации(равновесия) – Вместо [Ai] = ai = γi Ci , где ai – активность, γi – коэфф. активности 1 0 К д = α 2 С 0 КД
Электролитическая диссоциация АВ A+ + B- AB АВ A+ + B- С 0 - общая концентрация СД - конц. молекул в виде ионов СД = [A+]=[B-]=αС 0 [AB]=С 0 -αС 0 Степень диссоциации α>50%, <5%, 5<α<50% Сильные, слабые, средней силы электролиты Константа диссоциации(равновесия) – Вместо [Ai] = ai = γi Ci , где ai – активность, γi – коэфф. активности 1 0 К д = α 2 С 0 КД
![Ионное произведение воды H 2 O H+ + OHKw = [H+] [OH–] = 1. Ионное произведение воды H 2 O H+ + OHKw = [H+] [OH–] = 1.](https://present5.com/presentation/114931184_450311035/image-11.jpg) Ионное произведение воды H 2 O H+ + OHKw = [H+] [OH–] = 1. 0 10 -14 [(моль/л)2] 0 [H 2 O]-const [H 2 O]=1000/18 [моль/л] Kw = КД [H 2 O] = [H+] [OH–] - ионное КД = 1. 8 10 -16 произведение воды Нейтральная среда [H+] = [OH–] = 10 -7 [моль/л] Кислая среда [H+] > 10 -7(10 -6, -5, -4 …); [OH–] < 10 -7(10 -8, -9, -10 …) [моль/л] Щелочн. среда [H+] < 10 -7(10 -8, -9, -10 …); [OH–] > 10 -7(10 -6, -5, -4 …) [моль/л]
Ионное произведение воды H 2 O H+ + OHKw = [H+] [OH–] = 1. 0 10 -14 [(моль/л)2] 0 [H 2 O]-const [H 2 O]=1000/18 [моль/л] Kw = КД [H 2 O] = [H+] [OH–] - ионное КД = 1. 8 10 -16 произведение воды Нейтральная среда [H+] = [OH–] = 10 -7 [моль/л] Кислая среда [H+] > 10 -7(10 -6, -5, -4 …); [OH–] < 10 -7(10 -8, -9, -10 …) [моль/л] Щелочн. среда [H+] < 10 -7(10 -8, -9, -10 …); [OH–] > 10 -7(10 -6, -5, -4 …) [моль/л]
![Водородный показатель p. H = –lg[H+] Нейтральная среда p. H = 7 Кислая среда Водородный показатель p. H = –lg[H+] Нейтральная среда p. H = 7 Кислая среда](https://present5.com/presentation/114931184_450311035/image-12.jpg) Водородный показатель p. H = –lg[H+] Нейтральная среда p. H = 7 Кислая среда p. H < 7 Щелочная среда p. H > 7 p. ОH = –lg[ОH–] p. H + p. ОH = 14
Водородный показатель p. H = –lg[H+] Нейтральная среда p. H = 7 Кислая среда p. H < 7 Щелочная среда p. H > 7 p. ОH = –lg[ОH–] p. H + p. ОH = 14
 Растворы кислот и оснований HAn H+ + An- Ме. OH Ме+ + OH- Слабые электролиты 0 Сильные электролиты 1 р. Н = –lg[ Скисл] p. H = 14 + lg[ Cосн]
Растворы кислот и оснований HAn H+ + An- Ме. OH Ме+ + OH- Слабые электролиты 0 Сильные электролиты 1 р. Н = –lg[ Скисл] p. H = 14 + lg[ Cосн]
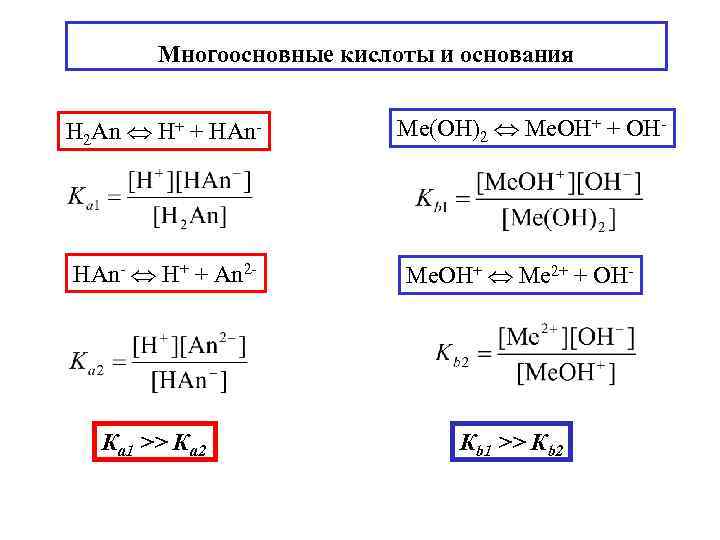 Многоосновные кислоты и основания H 2 An H+ + НAn- HAn- H+ + An 2 - Ка 1 >> Ка 2 Ме(OH)2 Ме. OH+ + OH- Ме. OH+ Ме 2+ + OH- Кb 1 >> Кb 2
Многоосновные кислоты и основания H 2 An H+ + НAn- HAn- H+ + An 2 - Ка 1 >> Ка 2 Ме(OH)2 Ме. OH+ + OH- Ме. OH+ Ме 2+ + OH- Кb 1 >> Кb 2
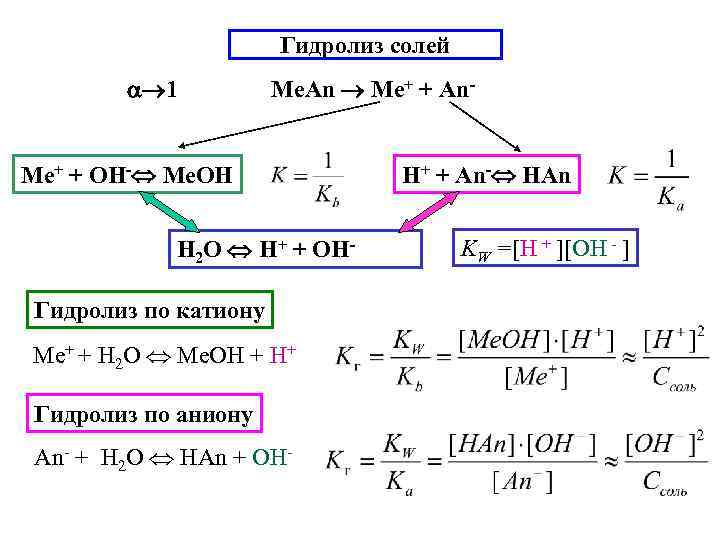 Гидролиз солей 1 Ме. An Ме+ + An- Ме+ + OH- Ме. OH H 2 O H+ + OHГидролиз по катиону Ме+ + H 2 O Ме. OH + H+ Гидролиз по аниону An- + H 2 O HAn + OH- H+ + An- HАn KW =[H + ][OH - ]
Гидролиз солей 1 Ме. An Ме+ + An- Ме+ + OH- Ме. OH H 2 O H+ + OHГидролиз по катиону Ме+ + H 2 O Ме. OH + H+ Гидролиз по аниону An- + H 2 O HAn + OH- H+ + An- HАn KW =[H + ][OH - ]
 Примеры гидролиза солей Cu. SO 4 Cu 2+ + SO 42 - 1) Kb 0; Ka Cu 2+ + H 2 O Cu. OH+ + H+ p. H <7 2 Cu. SO 4+ 2 H 2 O [Cu. OH]2 SO 4 + H 2 SO 4 2) Ka 0; Kb Na 3 РO 4 3 Na+ + РO 43 p. H >7 РO 43 - + H 2 O HРO 42 -+ OHNa 3 РO 4+ H 2 O Na 2 HРO 4+ Na. OH NH 4 NO 2 NH 4+ + NO 23) Ka 0; Kb 0 NH 4+ + H 2 O NH 4 OH + H+ p. H 7 NO 2 - + H 2 O НNO 2 + OH 4) Ka ; Kb Гидролиза нет (Na++Cl-) p. H=7
Примеры гидролиза солей Cu. SO 4 Cu 2+ + SO 42 - 1) Kb 0; Ka Cu 2+ + H 2 O Cu. OH+ + H+ p. H <7 2 Cu. SO 4+ 2 H 2 O [Cu. OH]2 SO 4 + H 2 SO 4 2) Ka 0; Kb Na 3 РO 4 3 Na+ + РO 43 p. H >7 РO 43 - + H 2 O HРO 42 -+ OHNa 3 РO 4+ H 2 O Na 2 HРO 4+ Na. OH NH 4 NO 2 NH 4+ + NO 23) Ka 0; Kb 0 NH 4+ + H 2 O NH 4 OH + H+ p. H 7 NO 2 - + H 2 O НNO 2 + OH 4) Ka ; Kb Гидролиза нет (Na++Cl-) p. H=7
![Произведение растворимости - ПР S [моль/л] - растворимость осадка Katx. Any осадок Kat+ An- Произведение растворимости - ПР S [моль/л] - растворимость осадка Katx. Any осадок Kat+ An-](https://present5.com/presentation/114931184_450311035/image-17.jpg) Произведение растворимости - ПР S [моль/л] - растворимость осадка Katx. Any осадок Kat+ An- Katx. Any S-растворимость осадка[моль/л] [Kat+] = x·S [моль/л] x. Kat+ + y. Anраствор
Произведение растворимости - ПР S [моль/л] - растворимость осадка Katx. Any осадок Kat+ An- Katx. Any S-растворимость осадка[моль/л] [Kat+] = x·S [моль/л] x. Kat+ + y. Anраствор
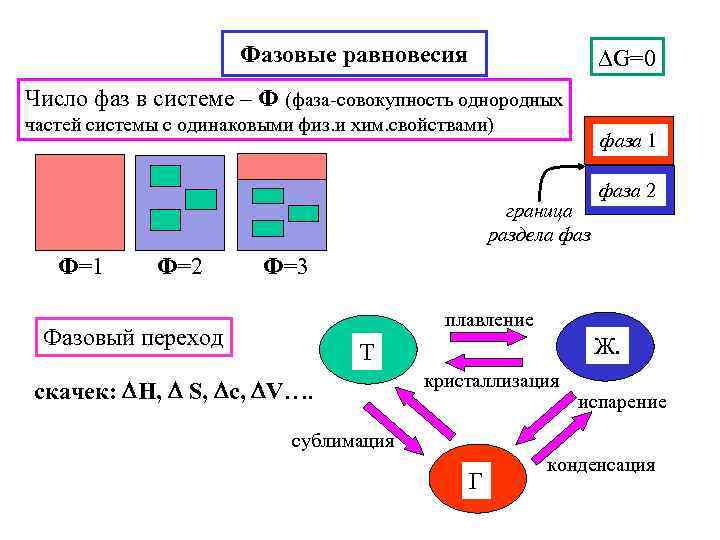 Фазовые равновесия G=0 Число фаз в системе – Ф (фаза-совокупность однородных частей системы с одинаковыми физ. и хим. свойствами) фаза 1 граница раздела фаз Ф=1 Ф=2 фаза 2 Ф=3 плавление Фазовый переход Ж. Т скачек: H, S, c, V…. кристаллизация испарение сублимация Г конденсация
Фазовые равновесия G=0 Число фаз в системе – Ф (фаза-совокупность однородных частей системы с одинаковыми физ. и хим. свойствами) фаза 1 граница раздела фаз Ф=1 Ф=2 фаза 2 Ф=3 плавление Фазовый переход Ж. Т скачек: H, S, c, V…. кристаллизация испарение сублимация Г конденсация
 Число компонентов – К (независимые составные части системы) Число видов молекул, необходимое и достаточное для образования всех фаз системы, за вычетом числа независимых реакций в системе N 2, Н 2 O, He N 2, Н 2, NН 3 К=3 N 2+3 H 2 2 NH 3 К=3– 1=2 Число термодинамических степеней свободы - С Число независимых параметров равновесия (p, T, C), которые могут произвольно изменяться (в определенном интервале) и при этом не изменяется число фаз в системе и ее строение Правило фаз Гиббса - С = К + 2 – Ф
Число компонентов – К (независимые составные части системы) Число видов молекул, необходимое и достаточное для образования всех фаз системы, за вычетом числа независимых реакций в системе N 2, Н 2 O, He N 2, Н 2, NН 3 К=3 N 2+3 H 2 2 NH 3 К=3– 1=2 Число термодинамических степеней свободы - С Число независимых параметров равновесия (p, T, C), которые могут произвольно изменяться (в определенном интервале) и при этом не изменяется число фаз в системе и ее строение Правило фаз Гиббса - С = К + 2 – Ф
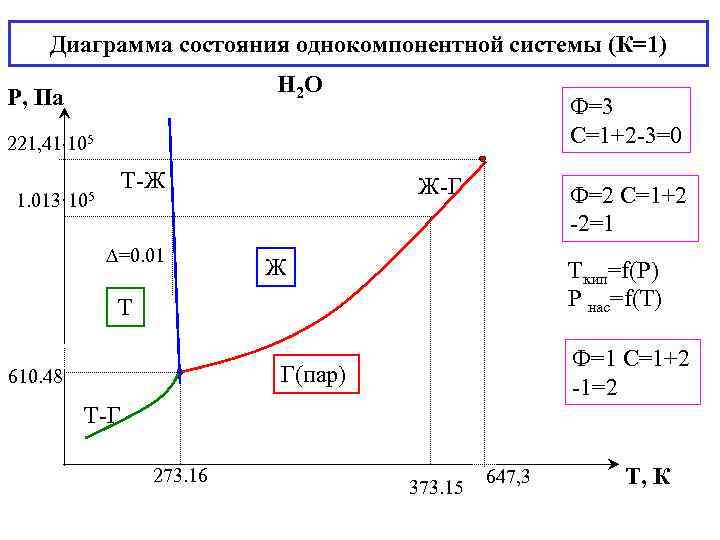 Диаграмма состояния однокомпонентной системы (К=1) Н 2 О Р, Па Ф=3 С=1+2 -3=0 221, 41 105 Т-Ж 1. 013· 105 =0. 01 Ж-Г Ф=2 С=1+2 -2=1 Ж Tкип=f(Р) Р нас=f(T) Т Ф=1 С=1+2 -1=2 Г(пар) 610. 48 Т-Г 273. 16 373. 15 647, 3 Т, К
Диаграмма состояния однокомпонентной системы (К=1) Н 2 О Р, Па Ф=3 С=1+2 -3=0 221, 41 105 Т-Ж 1. 013· 105 =0. 01 Ж-Г Ф=2 С=1+2 -2=1 Ж Tкип=f(Р) Р нас=f(T) Т Ф=1 С=1+2 -1=2 Г(пар) 610. 48 Т-Г 273. 16 373. 15 647, 3 Т, К
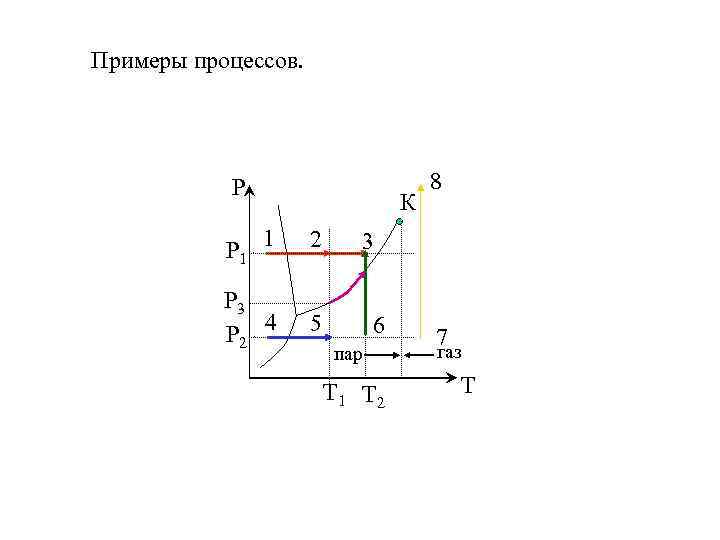 Примеры процессов. Р К Р 1 1 2 Р 3 Р 2 4 5 8 3 6 пар Т 1 Т 2 7 газ Т
Примеры процессов. Р К Р 1 1 2 Р 3 Р 2 4 5 8 3 6 пар Т 1 Т 2 7 газ Т
![Двухкомпонентная система [К=2(вода+ растворенное вeщество А)], молекулярный раствор. 0 p 0 –давление насыщенного пара Двухкомпонентная система [К=2(вода+ растворенное вeщество А)], молекулярный раствор. 0 p 0 –давление насыщенного пара](https://present5.com/presentation/114931184_450311035/image-22.jpg) Двухкомпонентная система [К=2(вода+ растворенное вeщество А)], молекулярный раствор. 0 p 0 –давление насыщенного пара (Н 2 Опар ) над растворителем Н 2 О р. А –давление (Н 2 Опар ) над раствором(Н 2 О+А) Н 2 Опар Н 2 О + А Закон Рауля Двухфазное равновесие 1) Т Ж; Ж Г С = 2 + 2 – 2 = 2 Tпл=f(р, СА) Tкип=f(р, СА) 2) Т Г Ф=3 С = 2 + 2 – 3 = 1
Двухкомпонентная система [К=2(вода+ растворенное вeщество А)], молекулярный раствор. 0 p 0 –давление насыщенного пара (Н 2 Опар ) над растворителем Н 2 О р. А –давление (Н 2 Опар ) над раствором(Н 2 О+А) Н 2 Опар Н 2 О + А Закон Рауля Двухфазное равновесие 1) Т Ж; Ж Г С = 2 + 2 – 2 = 2 Tпл=f(р, СА) Tкип=f(р, СА) 2) Т Г Ф=3 С = 2 + 2 – 3 = 1
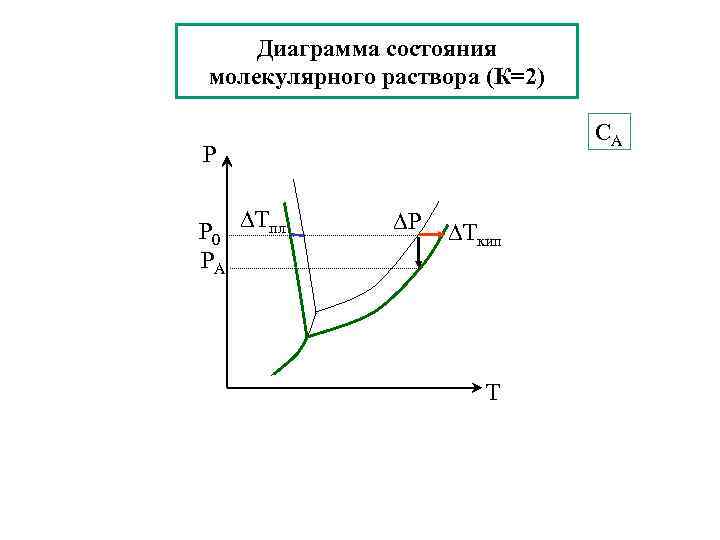 Диаграмма состояния молекулярного раствора (К=2) СА Р Р 0 РА Тпл P Ткип Т
Диаграмма состояния молекулярного раствора (К=2) СА Р Р 0 РА Тпл P Ткип Т
 Кипение и кристаллизация растворов • Повышение температуры кипения раствора по сравнению с чистым растворителем ( Ткип) прямо пропорционально концентрации растворенного вещества Ткип = Kэб См См [моль/кг] – моляльная концентрация Kэб [К кг/моль]– эбуллиоскопическая постоянная растворителя • Понижение температуры кристаллизации раствора по сравнению с чистым растворителем прямо пропорционально концентрации растворенного вещества Ткр = Kкр См Kкр [К кг/моль]– криоскопическая постоянная растворителя v. H - [Дж /кг] m. H
Кипение и кристаллизация растворов • Повышение температуры кипения раствора по сравнению с чистым растворителем ( Ткип) прямо пропорционально концентрации растворенного вещества Ткип = Kэб См См [моль/кг] – моляльная концентрация Kэб [К кг/моль]– эбуллиоскопическая постоянная растворителя • Понижение температуры кристаллизации раствора по сравнению с чистым растворителем прямо пропорционально концентрации растворенного вещества Ткр = Kкр См Kкр [К кг/моль]– криоскопическая постоянная растворителя v. H - [Дж /кг] m. H
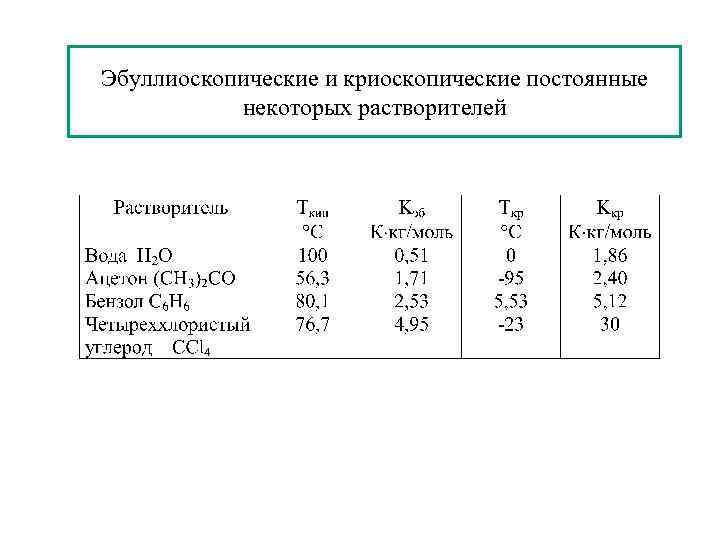 Эбуллиоскопические и криоскопические постоянные некоторых растворителей
Эбуллиоскопические и криоскопические постоянные некоторых растворителей
 Изотонический коэффициент – i (растворы электролитов) - показывает увеличение числа частиц в растворе электролита по сравнению с раствором не электролита той же концентрации(изменение коллигативных свойств) А x. В y x А + + y В - N 0 - число молекул растворенного вещества; N 0 (x + y )+(N 0 - N 0 ) - суммарное число частиц (ионов и недиссоциированных молекул) - степень диссоциации m=x+y 1 i=m Ткип = i Kэб См Ткр = i Kкр См
Изотонический коэффициент – i (растворы электролитов) - показывает увеличение числа частиц в растворе электролита по сравнению с раствором не электролита той же концентрации(изменение коллигативных свойств) А x. В y x А + + y В - N 0 - число молекул растворенного вещества; N 0 (x + y )+(N 0 - N 0 ) - суммарное число частиц (ионов и недиссоциированных молекул) - степень диссоциации m=x+y 1 i=m Ткип = i Kэб См Ткр = i Kкр См


