Химический состав живого-14.ppt
- Количество слайдов: 77
 Химический состав живого
Химический состав живого
 Единство химического состава С, Н, О, N – 99% состава живых организмов (органогены) Р, S, Na, K, Ca, Cl, Mg обязательны (макроэлементы) ü ü ü Mn, Fe, Co, Cu, Zn обязательны в микродозах (микроэлементы) Белки (структурные элементы и БАВ, в частности, ферменты) – 50 -70% смт Нуклеиновые кислоты (ДНК, РНК) Углеводы (структурные и энергетические компоненты) Липиды (структурные и энергетические компоненты) Липоиды (БАВ, например, стероидные гормоны) • Вода – среда для органических и неорганических веществ – 60 -80%, до 98% состава клетки
Единство химического состава С, Н, О, N – 99% состава живых организмов (органогены) Р, S, Na, K, Ca, Cl, Mg обязательны (макроэлементы) ü ü ü Mn, Fe, Co, Cu, Zn обязательны в микродозах (микроэлементы) Белки (структурные элементы и БАВ, в частности, ферменты) – 50 -70% смт Нуклеиновые кислоты (ДНК, РНК) Углеводы (структурные и энергетические компоненты) Липиды (структурные и энергетические компоненты) Липоиды (БАВ, например, стероидные гормоны) • Вода – среда для органических и неорганических веществ – 60 -80%, до 98% состава клетки
 Н 2 О участвует в реакциях метаболизма служит средой, в которой происходит распространение гамет и оплодотворение выполняет функции: опорную, защитную, транспортную поддерживает структуру клеток (компонент цитоплазмы) и многоклеточных тел (гидроскелет)
Н 2 О участвует в реакциях метаболизма служит средой, в которой происходит распространение гамет и оплодотворение выполняет функции: опорную, защитную, транспортную поддерживает структуру клеток (компонент цитоплазмы) и многоклеточных тел (гидроскелет)
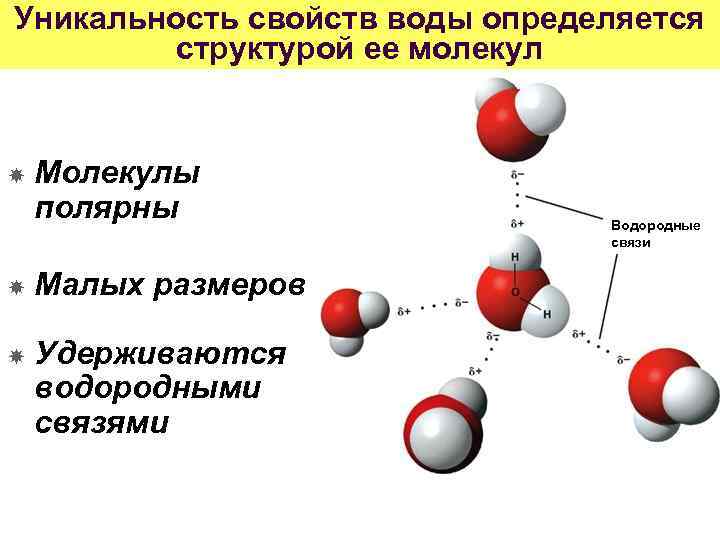 Уникальность свойств воды определяется структурой ее молекул Молекулы полярны Малых размеров σσ+ σ+ Удерживаются водородными связями Водородные связи
Уникальность свойств воды определяется структурой ее молекул Молекулы полярны Малых размеров σσ+ σ+ Удерживаются водородными связями Водородные связи
 Свойства воды Вода –растворитель для полярных веществ · - солей; сахаров и простых спиртов - Неполярные молекулы в воде гидрофобны Вода – среда для транспорта различных веществ · Вода как реагент и продукт реакций · - вода - источника водорода для синтеза органических соединений в процессе фотосинтеза - вода участвует в реакциях гидролиза • Несжимаемость воды (в жидком состоянии) -Тургор клеток, тканей; основа гидроскелета • Аномалия изменения плотности воды разных агрегатных состояний (максимальная плотность Н 2 О при Т= +4 о. С, при >/< ρ уменьшается) · Большое поверхностное натяжение и капиллярность -Когезия – сцепление молекул физического тела друг с другом под действием сил притяжения. · Большая удельная теплоемкость (4, 2 к. Дж/кг·К) · Вода и процесс эволюции
Свойства воды Вода –растворитель для полярных веществ · - солей; сахаров и простых спиртов - Неполярные молекулы в воде гидрофобны Вода – среда для транспорта различных веществ · Вода как реагент и продукт реакций · - вода - источника водорода для синтеза органических соединений в процессе фотосинтеза - вода участвует в реакциях гидролиза • Несжимаемость воды (в жидком состоянии) -Тургор клеток, тканей; основа гидроскелета • Аномалия изменения плотности воды разных агрегатных состояний (максимальная плотность Н 2 О при Т= +4 о. С, при >/< ρ уменьшается) · Большое поверхностное натяжение и капиллярность -Когезия – сцепление молекул физического тела друг с другом под действием сил притяжения. · Большая удельная теплоемкость (4, 2 к. Дж/кг·К) · Вода и процесс эволюции
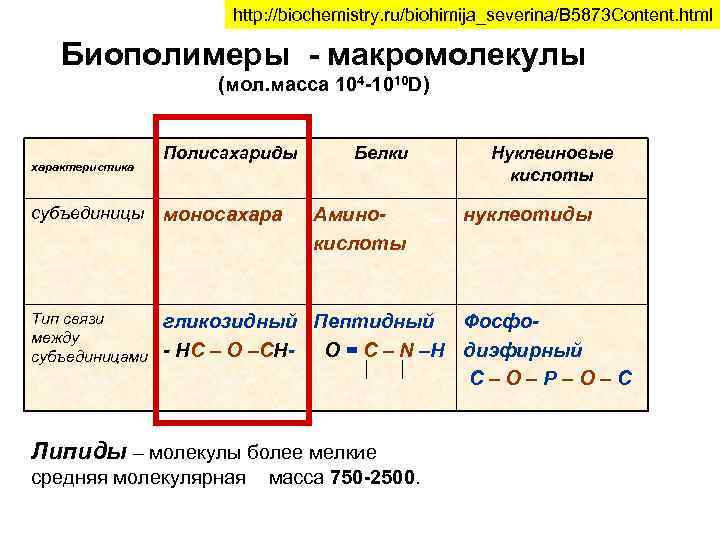 http: //biochemistry. ru/biohimija_severina/B 5873 Content. html Биополимеры - макромолекулы (мол. масса 104 -1010 D) характеристика Полисахариды Белки Нуклеиновые кислоты субъединицы моносахара Тип связи между субъединицами гликозидный Пептидный Фосфо- НС – О –СН- О = С – N –Н диэфирный С – О – Р – О – С Аминокислоты Липиды – молекулы более мелкие средняя молекулярная масса 750 -2500. нуклеотиды
http: //biochemistry. ru/biohimija_severina/B 5873 Content. html Биополимеры - макромолекулы (мол. масса 104 -1010 D) характеристика Полисахариды Белки Нуклеиновые кислоты субъединицы моносахара Тип связи между субъединицами гликозидный Пептидный Фосфо- НС – О –СН- О = С – N –Н диэфирный С – О – Р – О – С Аминокислоты Липиды – молекулы более мелкие средняя молекулярная масса 750 -2500. нуклеотиды
 Углеводы Сх(Н 20)х 3 С-9 С – углеводы, чаще пентозы (5 С) и гексозы (6 С) Глюкоза Галактоза Фруктоза Аномерная ОН-группа при Iат. С аномеры
Углеводы Сх(Н 20)х 3 С-9 С – углеводы, чаще пентозы (5 С) и гексозы (6 С) Глюкоза Галактоза Фруктоза Аномерная ОН-группа при Iат. С аномеры
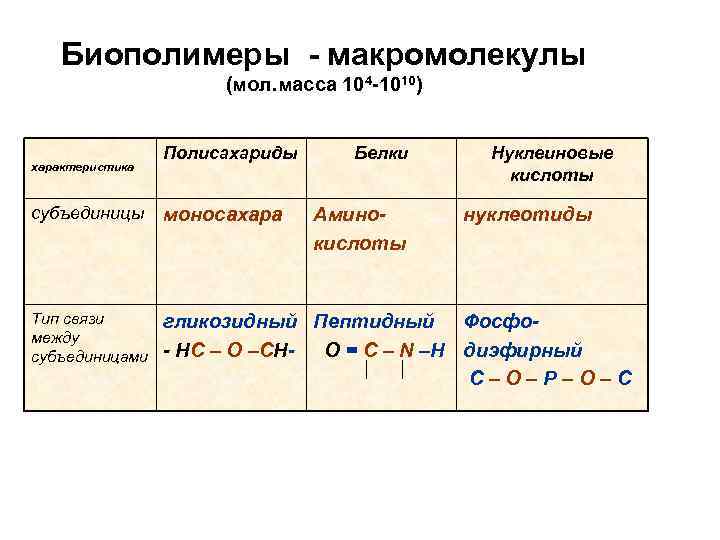 Биополимеры - макромолекулы (мол. масса 104 -1010) характеристика Полисахариды Белки Нуклеиновые кислоты субъединицы моносахара Тип связи между субъединицами гликозидный Пептидный Фосфо- НС – О –СН- О = С – N –Н диэфирный С – О – Р – О – С Аминокислоты нуклеотиды
Биополимеры - макромолекулы (мол. масса 104 -1010) характеристика Полисахариды Белки Нуклеиновые кислоты субъединицы моносахара Тип связи между субъединицами гликозидный Пептидный Фосфо- НС – О –СН- О = С – N –Н диэфирный С – О – Р – О – С Аминокислоты нуклеотиды
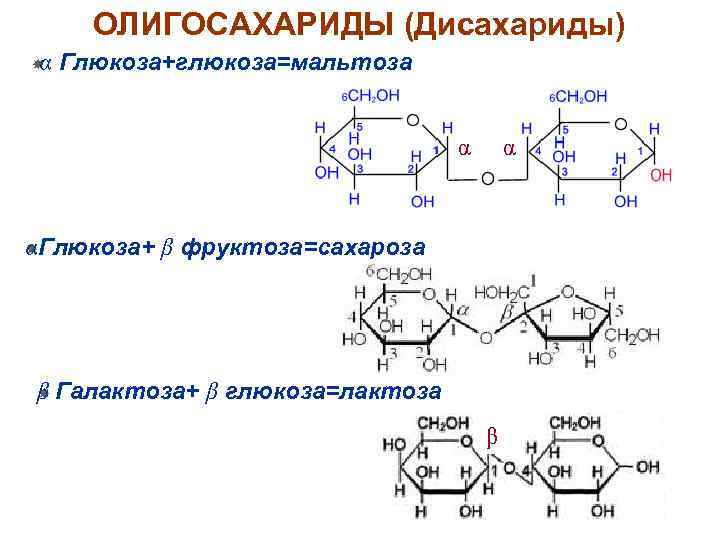 ОЛИГОСАХАРИДЫ (Дисахариды) α Глюкоза+глюкоза=мальтоза α α α Глюкоза+ β фруктоза=сахароза β Галактоза+ β глюкоза=лактоза β
ОЛИГОСАХАРИДЫ (Дисахариды) α Глюкоза+глюкоза=мальтоза α α α Глюкоза+ β фруктоза=сахароза β Галактоза+ β глюкоза=лактоза β
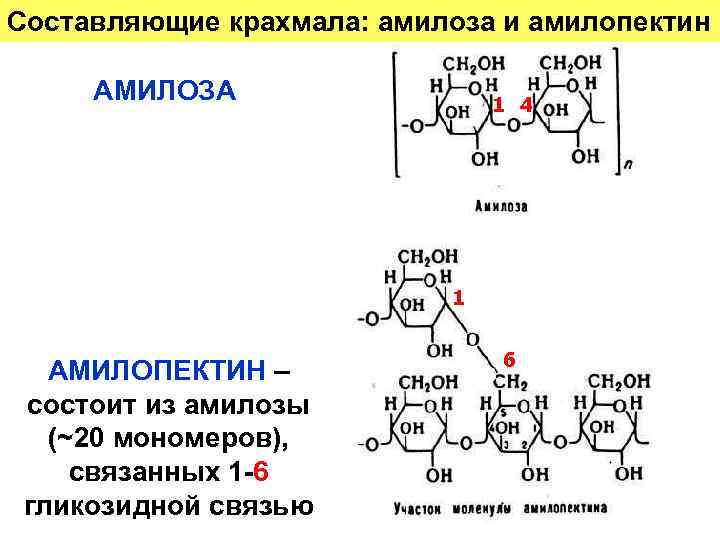 Составляющие крахмала: амилоза и амилопектин АМИЛОЗА 1 4 1 АМИЛОПЕКТИН – состоит из амилозы (~20 мономеров), связанных 1 -6 гликозидной связью 6
Составляющие крахмала: амилоза и амилопектин АМИЛОЗА 1 4 1 АМИЛОПЕКТИН – состоит из амилозы (~20 мономеров), связанных 1 -6 гликозидной связью 6
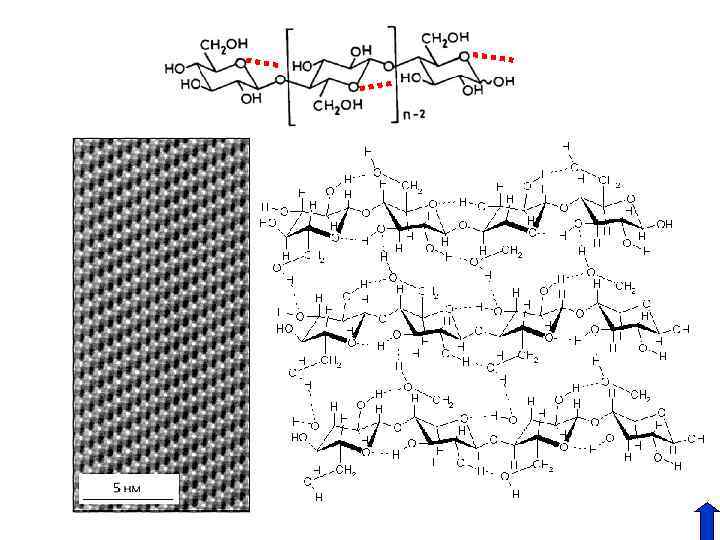
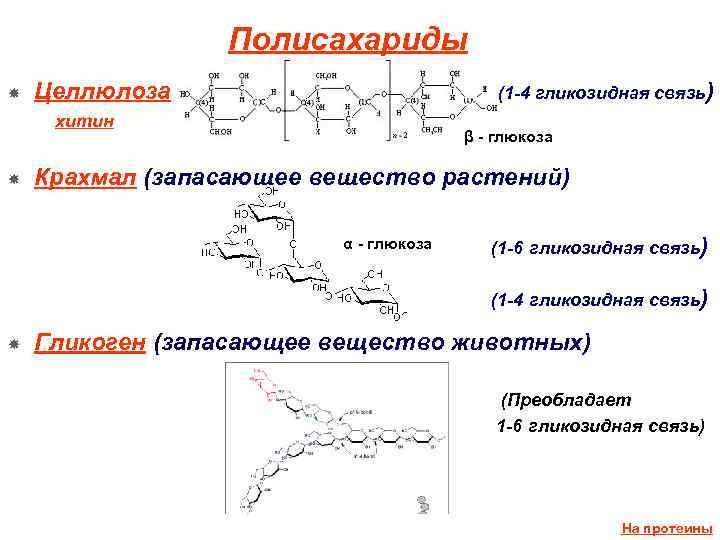 Полисахариды Целлюлоза (1 -4 гликозидная связь) хитин β - глюкоза Крахмал (запасающее вещество растений) α - глюкоза (1 -6 гликозидная связь) (1 -4 гликозидная связь) Гликоген (запасающее вещество животных) (Преобладает 1 -6 гликозидная связь) На протеины
Полисахариды Целлюлоза (1 -4 гликозидная связь) хитин β - глюкоза Крахмал (запасающее вещество растений) α - глюкоза (1 -6 гликозидная связь) (1 -4 гликозидная связь) Гликоген (запасающее вещество животных) (Преобладает 1 -6 гликозидная связь) На протеины
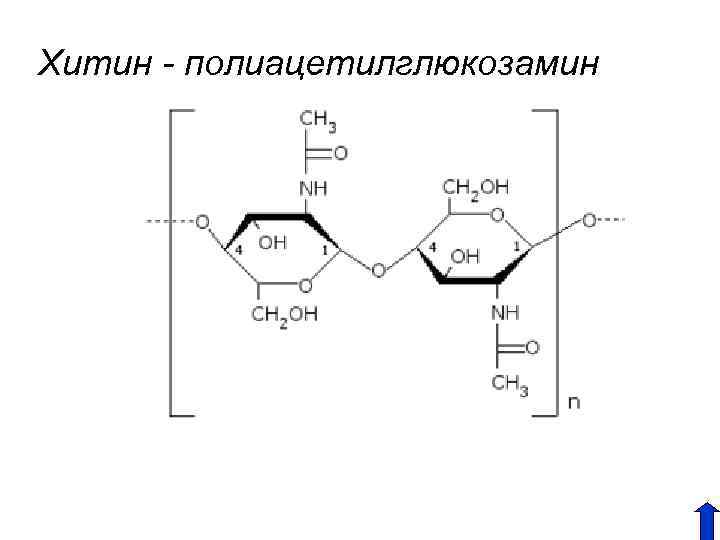 Хитин - полиацетилглюкозамин
Хитин - полиацетилглюкозамин
 1871 г. – Н. Н. Любавин – Белки состоят из аминокислот ПРОТЕИНЫ H NН 2 ---СООН Н 2 N ---С----СООН Н R глицин схема аминокислоты
1871 г. – Н. Н. Любавин – Белки состоят из аминокислот ПРОТЕИНЫ H NН 2 ---СООН Н 2 N ---С----СООН Н R глицин схема аминокислоты
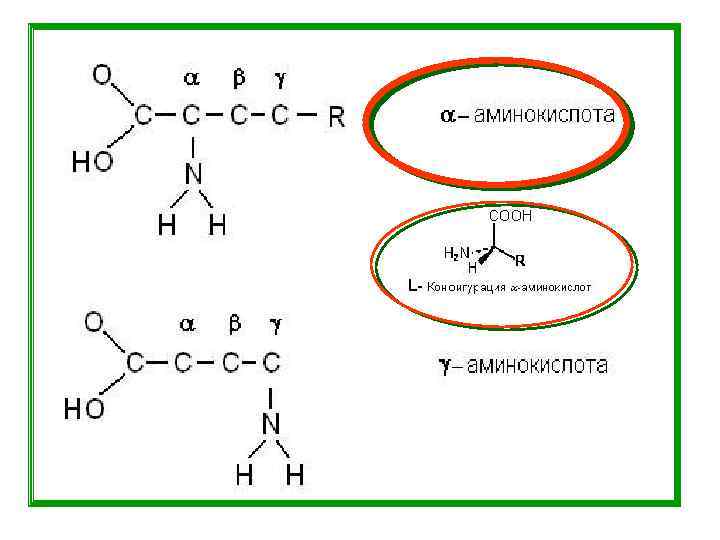
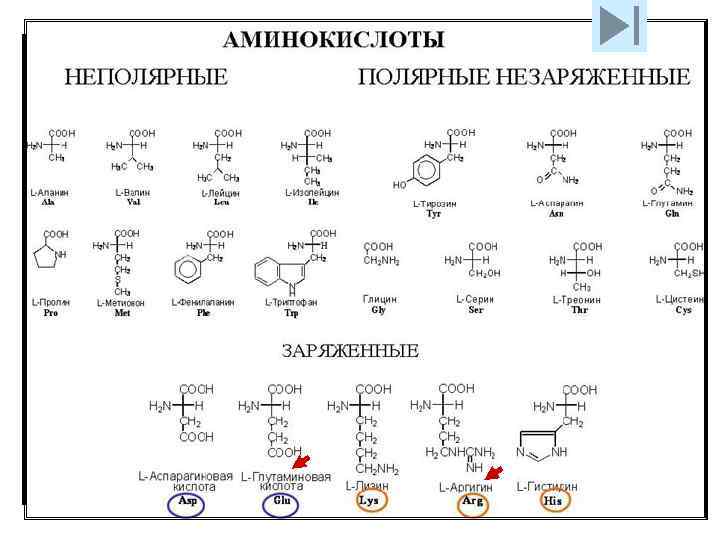
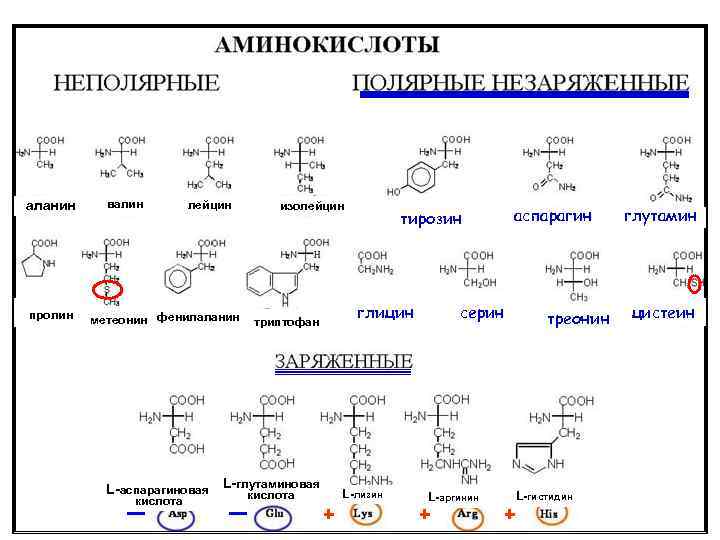 аланин пролин валин лейцин метеонин фенилаланин изолейцин глицин триптофан L-аспарагиновая L-глутаминовая кислота тирозин L-лизин + аспарагин серин L-аргинин + треонин L-гистидин + глутамин цистеин
аланин пролин валин лейцин метеонин фенилаланин изолейцин глицин триптофан L-аспарагиновая L-глутаминовая кислота тирозин L-лизин + аспарагин серин L-аргинин + треонин L-гистидин + глутамин цистеин
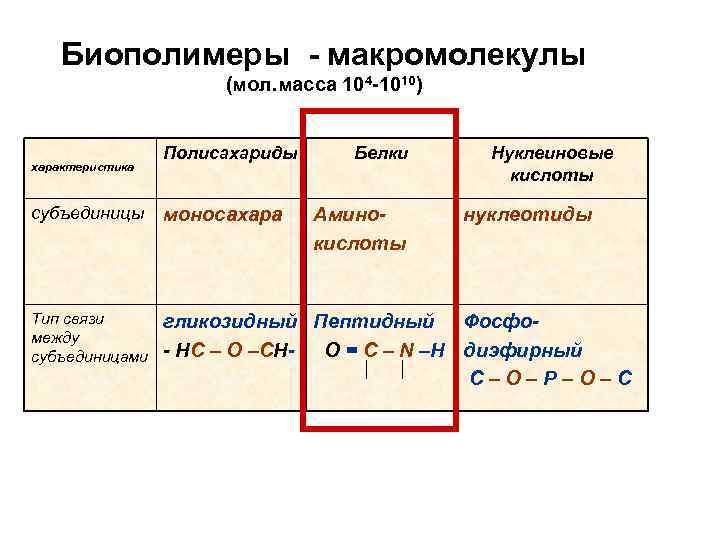 Биополимеры - макромолекулы (мол. масса 104 -1010) характеристика Полисахариды Белки Нуклеиновые кислоты субъединицы моносахара Тип связи между субъединицами гликозидный Пептидный Фосфо- НС – О –СН- О = С – N –Н диэфирный С – О – Р – О – С Аминокислоты нуклеотиды
Биополимеры - макромолекулы (мол. масса 104 -1010) характеристика Полисахариды Белки Нуклеиновые кислоты субъединицы моносахара Тип связи между субъединицами гликозидный Пептидный Фосфо- НС – О –СН- О = С – N –Н диэфирный С – О – Р – О – С Аминокислоты нуклеотиды
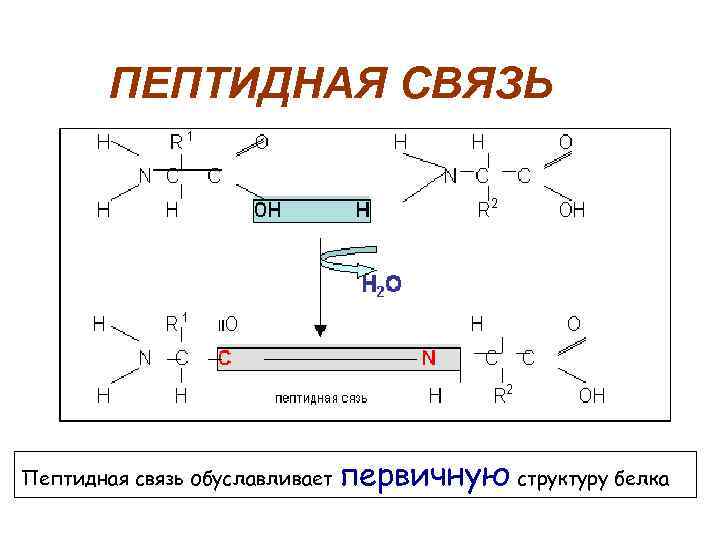 ПЕПТИДНАЯ СВЯЗЬ Пептидная связь обуславливает первичную структуру белка
ПЕПТИДНАЯ СВЯЗЬ Пептидная связь обуславливает первичную структуру белка
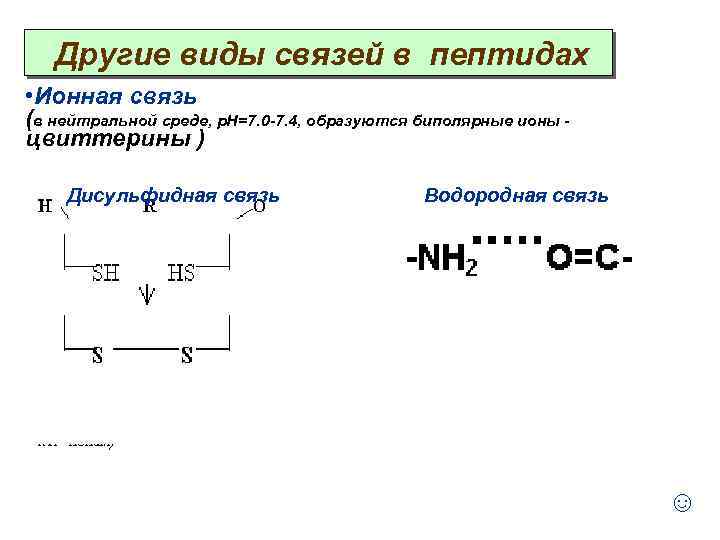 Другие виды связей в пептидах • Ионная связь (в нейтральной среде, р. Н=7. 0 -7. 4, образуются биполярные ионы цвиттерины ) Дисульфидная связь Водородная связь ☺
Другие виды связей в пептидах • Ионная связь (в нейтральной среде, р. Н=7. 0 -7. 4, образуются биполярные ионы цвиттерины ) Дисульфидная связь Водородная связь ☺
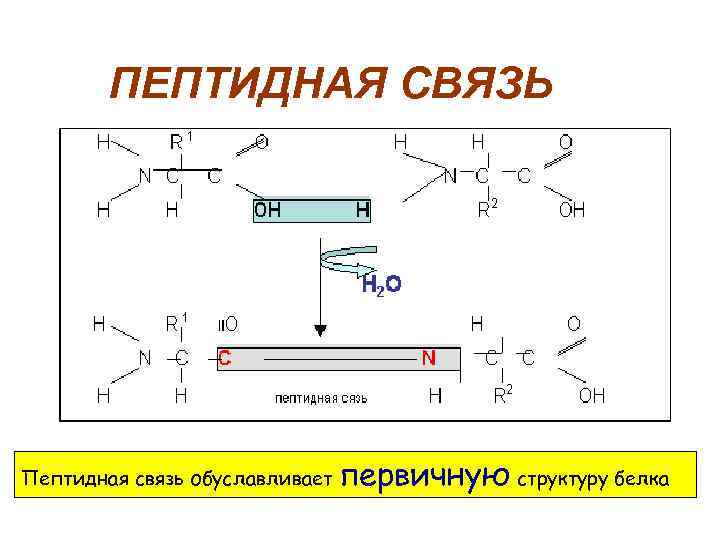 ПЕПТИДНАЯ СВЯЗЬ Пептидная связь обуславливает первичную структуру белка
ПЕПТИДНАЯ СВЯЗЬ Пептидная связь обуславливает первичную структуру белка
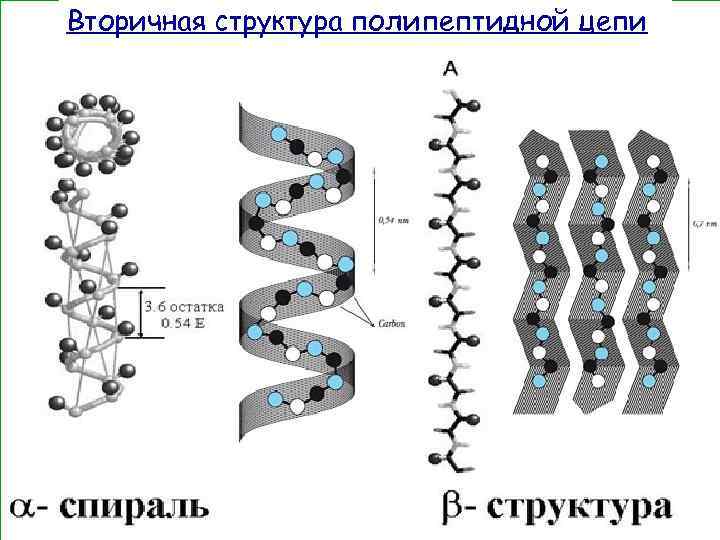 Вторичная структура полипептидной цепи
Вторичная структура полипептидной цепи
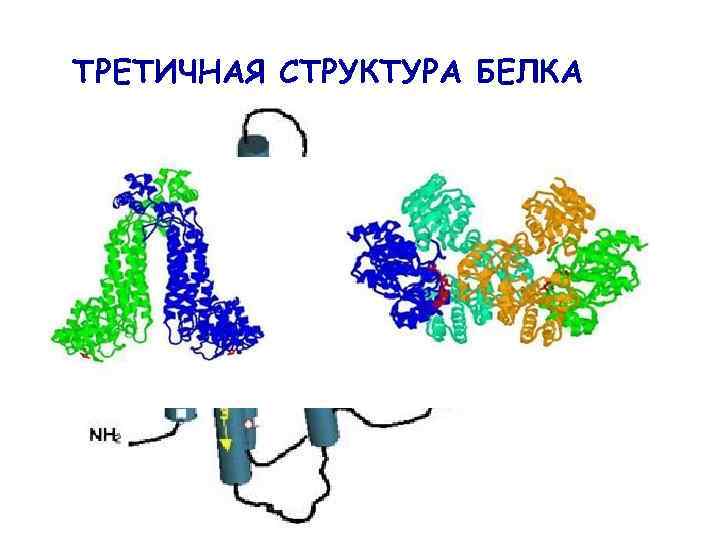 ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА
ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА
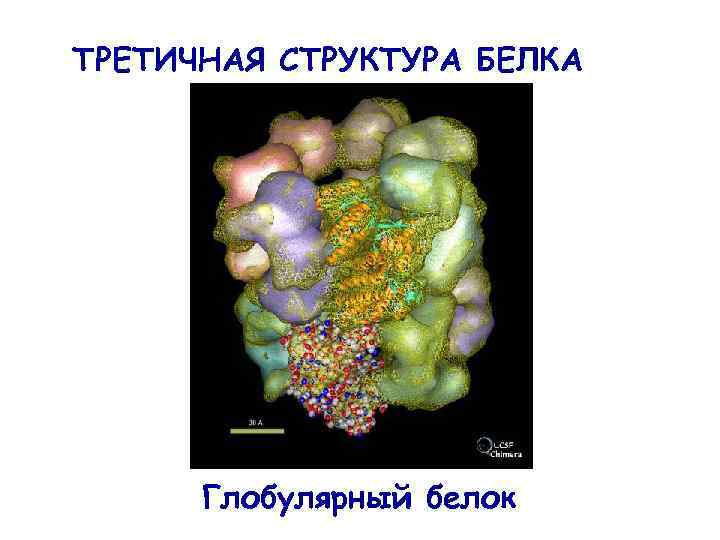 ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА Глобулярный белок
ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА Глобулярный белок
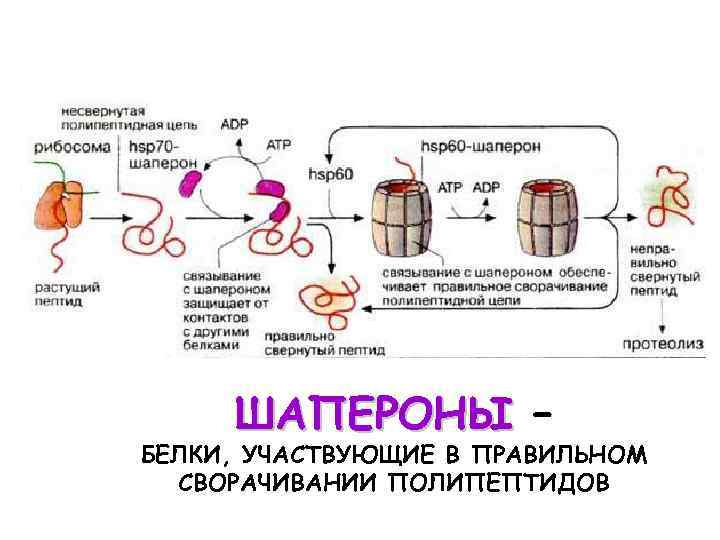 ШАПЕРОНЫ – БЕЛКИ, УЧАСТВУЮЩИЕ В ПРАВИЛЬНОМ СВОРАЧИВАНИИ ПОЛИПЕПТИДОВ
ШАПЕРОНЫ – БЕЛКИ, УЧАСТВУЮЩИЕ В ПРАВИЛЬНОМ СВОРАЧИВАНИИ ПОЛИПЕПТИДОВ
 Альцгеймера)
Альцгеймера)
 Химический состав живых систем
Химический состав живых систем
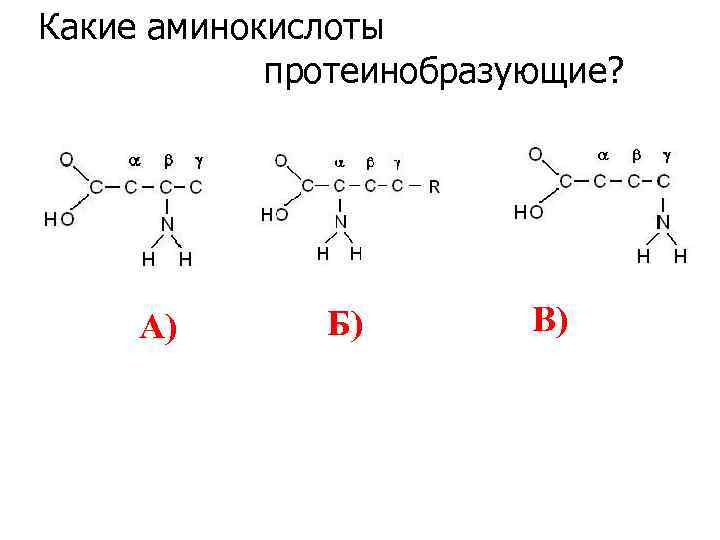 Какие аминокислоты протеинобразующие? A) Б) В)
Какие аминокислоты протеинобразующие? A) Б) В)
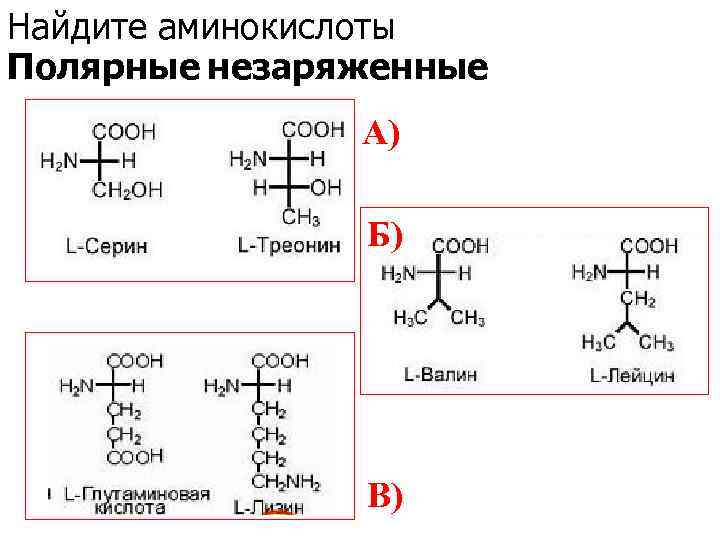 Найдите аминокислоты Полярные незаряженные A) Б) В)
Найдите аминокислоты Полярные незаряженные A) Б) В)
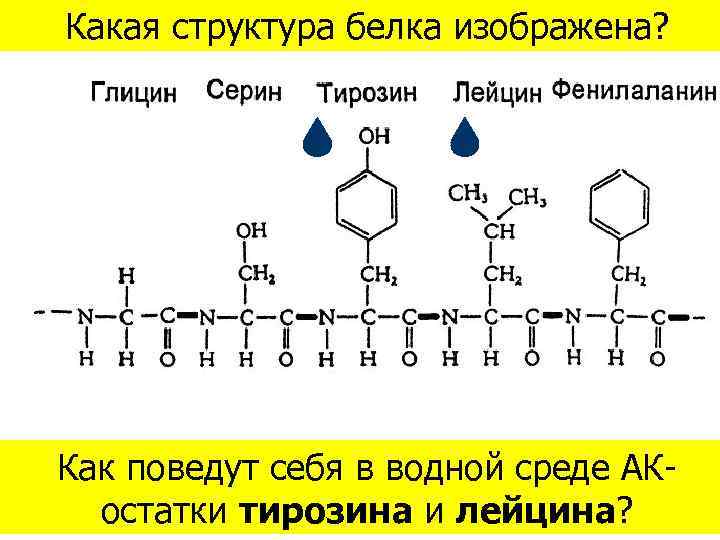 Какая структура белка изображена? Как поведут себя в водной среде АКостатки тирозина и лейцина?
Какая структура белка изображена? Как поведут себя в водной среде АКостатки тирозина и лейцина?
 Функции протеинов: • Структурная • Защитная • Глобулярные белки • Биокатализаторы • Регуляторная • Строго специфичны • Транспортная • Акт-ть ферментов зависит от T˚, р. Н, p, conc. • Двигательная • Рецепторная • Трофическая • Запасающая • Апоферменты активны при кофакторах – (не белкú!) • Аллостерические ферменты- их активность регулируется аллостерическими эффекторами • Ферментативная липиды
Функции протеинов: • Структурная • Защитная • Глобулярные белки • Биокатализаторы • Регуляторная • Строго специфичны • Транспортная • Акт-ть ферментов зависит от T˚, р. Н, p, conc. • Двигательная • Рецепторная • Трофическая • Запасающая • Апоферменты активны при кофакторах – (не белкú!) • Аллостерические ферменты- их активность регулируется аллостерическими эффекторами • Ферментативная липиды
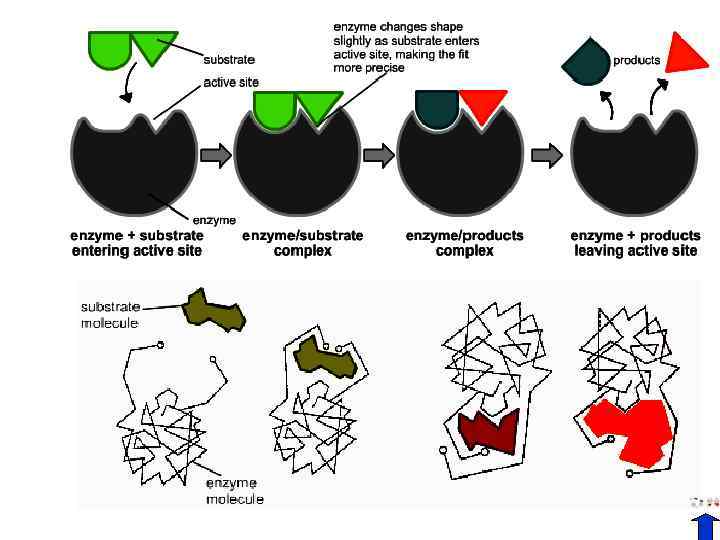
 субстрат фермент Эмиль Фишер, 1890: гипотеза «ключ-замок» Даниэль Кошланд, 1958: гипотеза «рука-перчатка» индуцированного соответствия Субстрат-ферментный комплекс Разложениение субстрата
субстрат фермент Эмиль Фишер, 1890: гипотеза «ключ-замок» Даниэль Кошланд, 1958: гипотеза «рука-перчатка» индуцированного соответствия Субстрат-ферментный комплекс Разложениение субстрата
 Денатурация белка Факторы, вызывающие нарушение пространственной конформации: ◘Высокая энергия (нагрев, облучение) → разрыв водородных и ионных связей ◘Сильные кислоты, щелочи, конц. соли → разрыв ионных связей, при длительном действии - и пептидных ◘Тяжелые металлы →разрыв ионных связей при связывании катионов с карбоксильной группой, снижение растворимости, выпадение в осадок ◘Органические растворители и детергенты → нарушают гидрофобные взаимодействия, образуя связи с неполярными группами Слайд 23
Денатурация белка Факторы, вызывающие нарушение пространственной конформации: ◘Высокая энергия (нагрев, облучение) → разрыв водородных и ионных связей ◘Сильные кислоты, щелочи, конц. соли → разрыв ионных связей, при длительном действии - и пептидных ◘Тяжелые металлы →разрыв ионных связей при связывании катионов с карбоксильной группой, снижение растворимости, выпадение в осадок ◘Органические растворители и детергенты → нарушают гидрофобные взаимодействия, образуя связи с неполярными группами Слайд 23
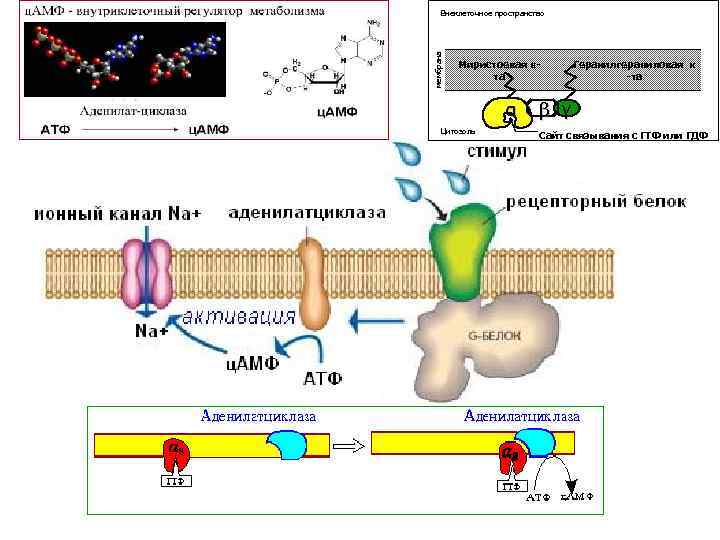 мембрана Внеклеточное пространство Миристоевая кта Геранилгераниловая к -та Инактивация рецепторной молекулы α (при фосфорилировании) β γ Цитозоль S S E E Р Р Сайт связывания с ГТФ или ГДФ
мембрана Внеклеточное пространство Миристоевая кта Геранилгераниловая к -та Инактивация рецепторной молекулы α (при фосфорилировании) β γ Цитозоль S S E E Р Р Сайт связывания с ГТФ или ГДФ
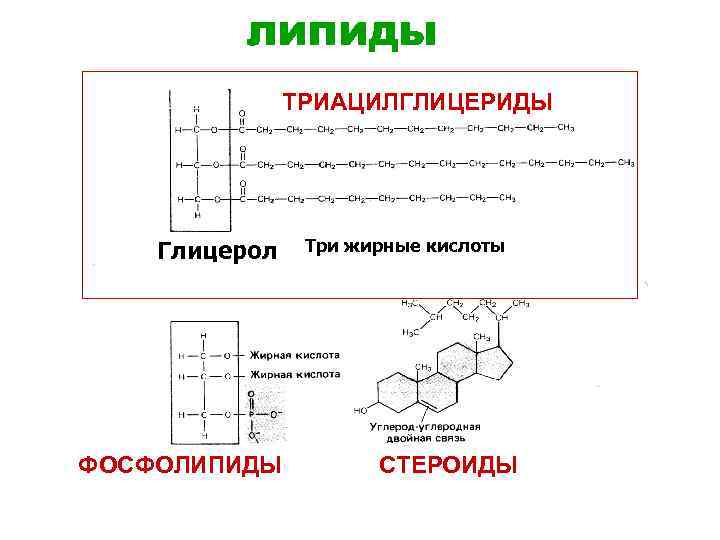 липиды ТРИАЦИЛГЛИЦЕРИДЫ Глицерол ФОСФОЛИПИДЫ Три жирные кислоты СТЕРОИДЫ
липиды ТРИАЦИЛГЛИЦЕРИДЫ Глицерол ФОСФОЛИПИДЫ Три жирные кислоты СТЕРОИДЫ
 ТРИАЦИЛГЛИЦЕРИДЫ Стеариновая CH 3(CH 2)16 COOH К жирам или Предельная (НАСЫЩЕННАЯ) К-ТА маслам будут относиться (ВХОДИТ В СОСТАВ липиды, содержащие ЖИРОВ) олеиновую (С 17 Н 33 СООН), линолевую ( С 17 Н 31 СООН) и Олеиновая CH 3(CH 2)7 CH=CH (CH 2)7 COOH арахидоновую кислоты ( С 19 Н 31 СООН)? ЛИНОЛЕВАЯ (семейство ω-6)- И α-ЛИНОЛЕНОВАЯ (семейство ω-3)- незаменимые (или эссенциальные) жирные кислоты. Непредельная (НЕНАСЫЩЕННАЯ) К-ТА Основные источники полиеновых жирных кислот для человека - жидкие растительные масла и рыбий жир (ВХОДИТ В СОСТАВ МАСЕЛ) ? !
ТРИАЦИЛГЛИЦЕРИДЫ Стеариновая CH 3(CH 2)16 COOH К жирам или Предельная (НАСЫЩЕННАЯ) К-ТА маслам будут относиться (ВХОДИТ В СОСТАВ липиды, содержащие ЖИРОВ) олеиновую (С 17 Н 33 СООН), линолевую ( С 17 Н 31 СООН) и Олеиновая CH 3(CH 2)7 CH=CH (CH 2)7 COOH арахидоновую кислоты ( С 19 Н 31 СООН)? ЛИНОЛЕВАЯ (семейство ω-6)- И α-ЛИНОЛЕНОВАЯ (семейство ω-3)- незаменимые (или эссенциальные) жирные кислоты. Непредельная (НЕНАСЫЩЕННАЯ) К-ТА Основные источники полиеновых жирных кислот для человека - жидкие растительные масла и рыбий жир (ВХОДИТ В СОСТАВ МАСЕЛ) ? !
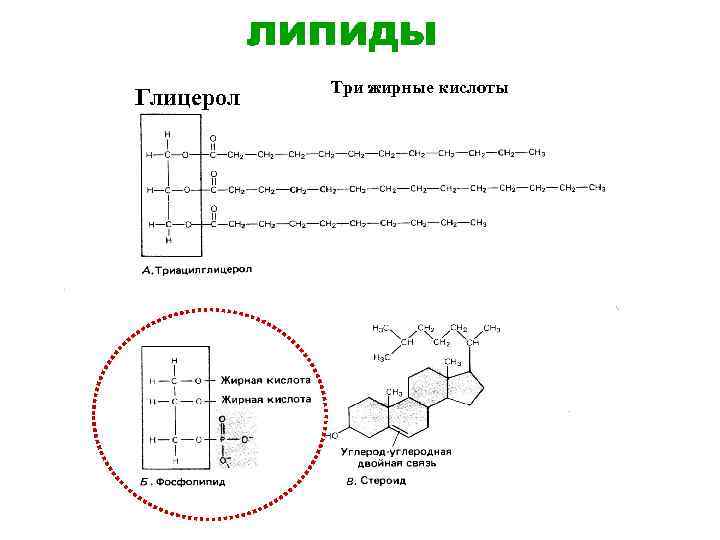 липиды Глицерол Три жирные кислоты
липиды Глицерол Три жирные кислоты
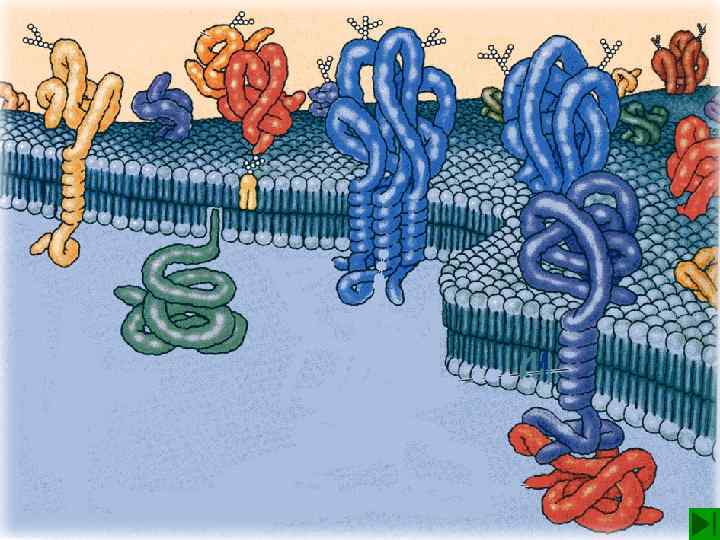
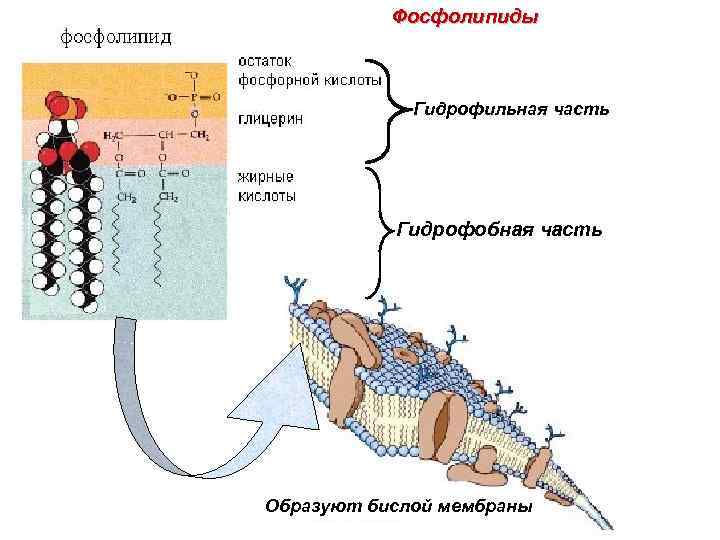 Фосфолипиды Гидрофильная часть Гидрофобная часть Образуют бислой мембраны
Фосфолипиды Гидрофильная часть Гидрофобная часть Образуют бислой мембраны
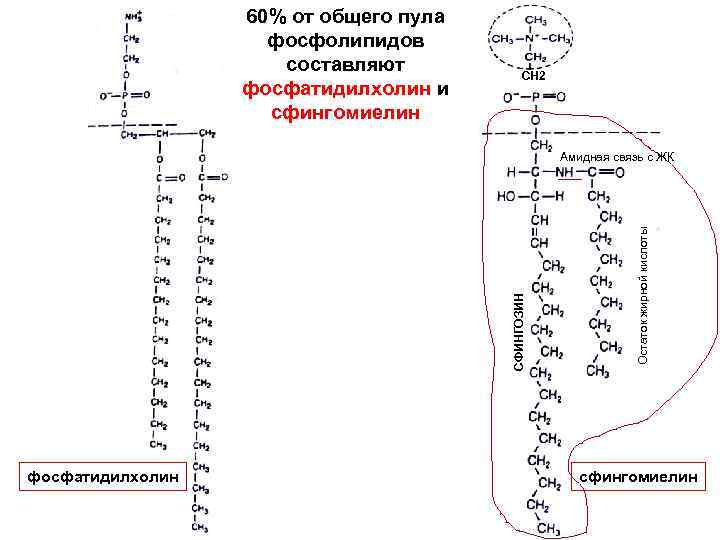 60% от общего пула фосфолипидов составляют фосфатидилхолин и сфингомиелин СН 2 фосфатидилхолин Остаток жирной кислоты СФИНГОЗИН Амидная связь с ЖК сфингомиелин
60% от общего пула фосфолипидов составляют фосфатидилхолин и сфингомиелин СН 2 фосфатидилхолин Остаток жирной кислоты СФИНГОЗИН Амидная связь с ЖК сфингомиелин
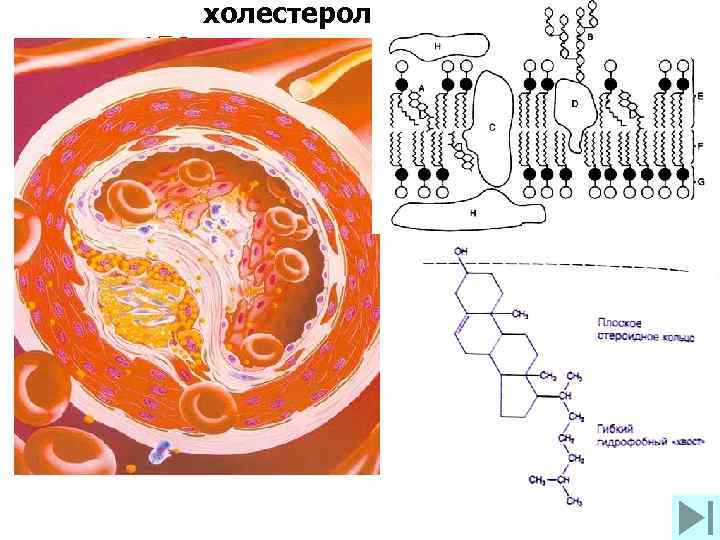 холестерол
холестерол
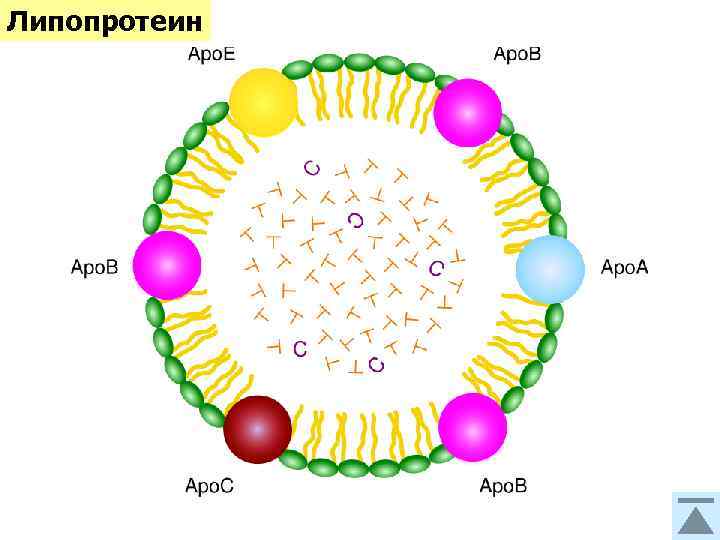 Липопротеин
Липопротеин
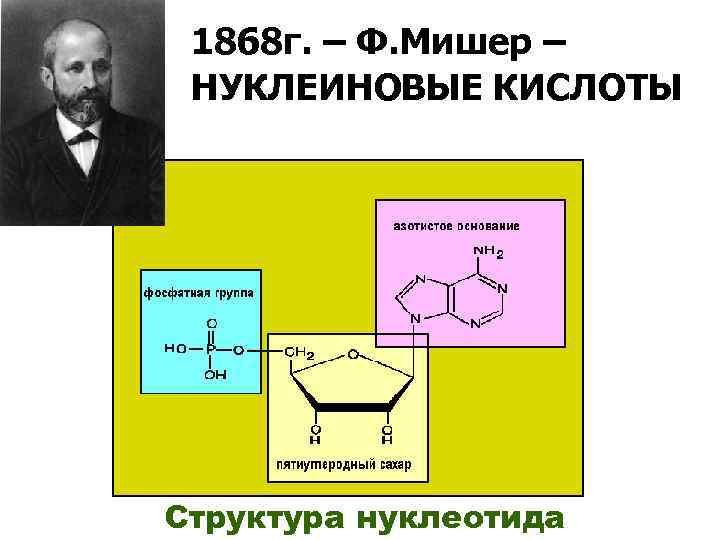 1868 г. – Ф. Мишер – НУКЛЕИНОВЫЕ КИСЛОТЫ Структура нуклеотида
1868 г. – Ф. Мишер – НУКЛЕИНОВЫЕ КИСЛОТЫ Структура нуклеотида
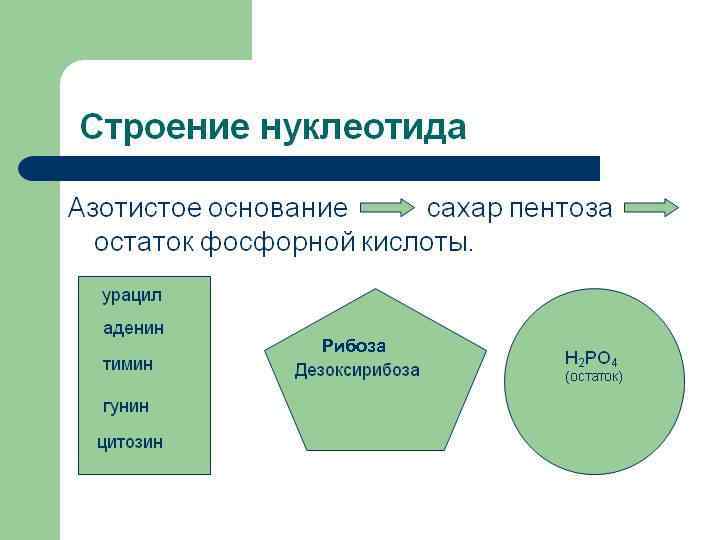 Рибоза
Рибоза
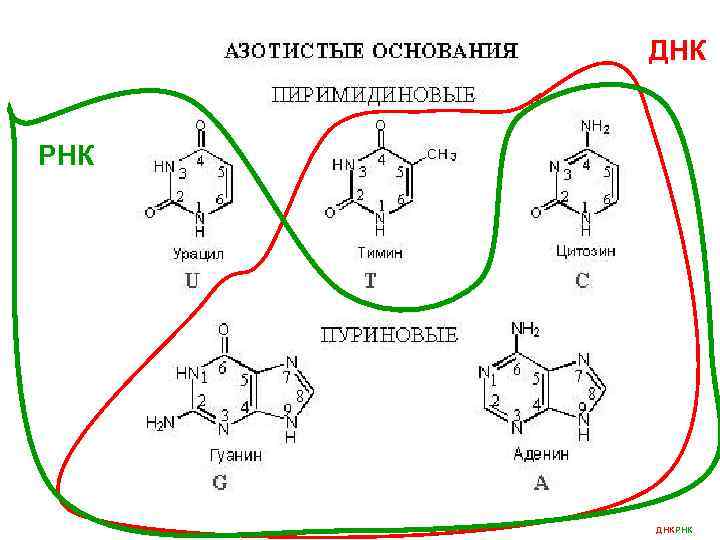 ДНК РНК ДНКРНК
ДНК РНК ДНКРНК
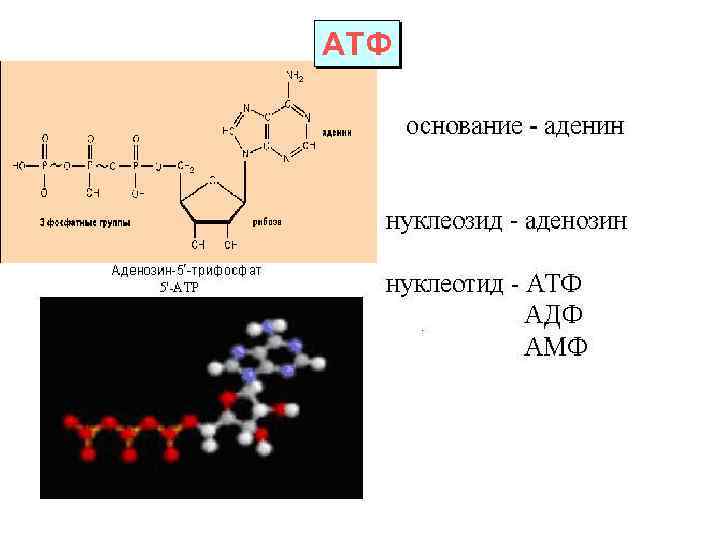 АТФ
АТФ
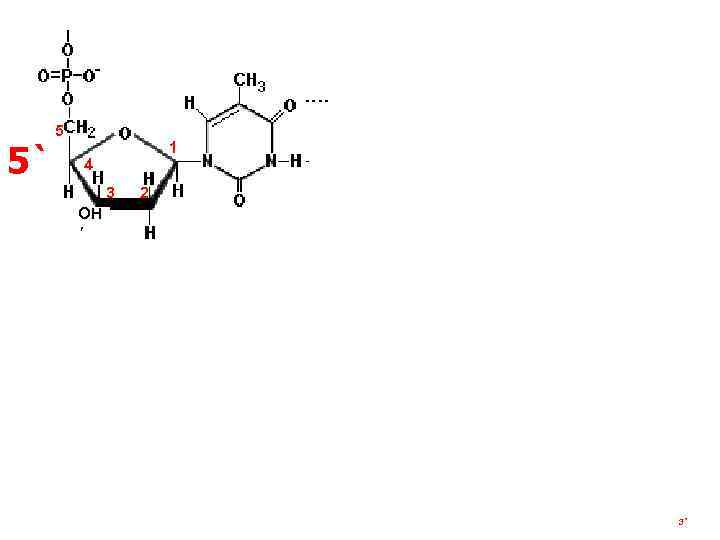 ТИМИН 3` АДЕНИН 5` 5 1 4 3 2 2 1 ОН Н 4 5 5 1 4 3 3` 3 2 2 3 1 ЦИТОЗИН ГУАНИН 4 5 5` 3`
ТИМИН 3` АДЕНИН 5` 5 1 4 3 2 2 1 ОН Н 4 5 5 1 4 3 3` 3 2 2 3 1 ЦИТОЗИН ГУАНИН 4 5 5` 3`
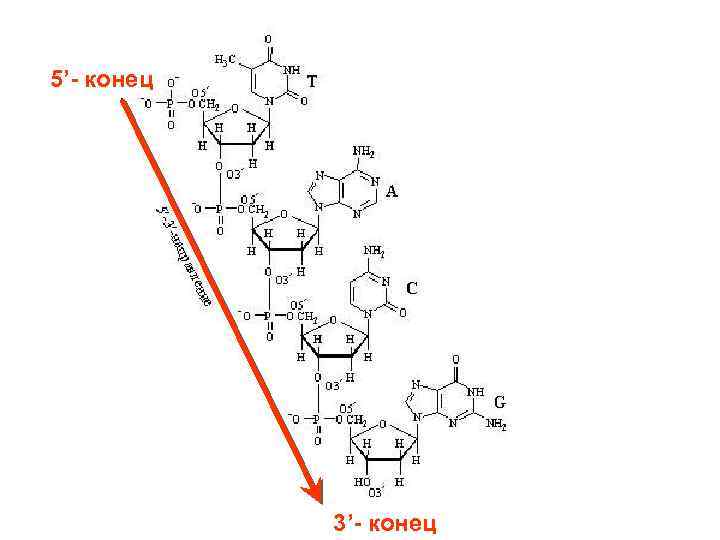 5’- конец 3’- конец
5’- конец 3’- конец
 1951 – Э. Чаргафф – выявил закономерности хим. состава ДНК %А =%Т %Г = %Ц А+Г=Т+Ц (A+Т): (Г+Ц) видоспецифично 1) Масса 1 нуклеотида = 345 А. е. м. 2) L витка ДНК=3, 4 нм 3) Нуклеотид (L) = 0, 34 нм.
1951 – Э. Чаргафф – выявил закономерности хим. состава ДНК %А =%Т %Г = %Ц А+Г=Т+Ц (A+Т): (Г+Ц) видоспецифично 1) Масса 1 нуклеотида = 345 А. е. м. 2) L витка ДНК=3, 4 нм 3) Нуклеотид (L) = 0, 34 нм.
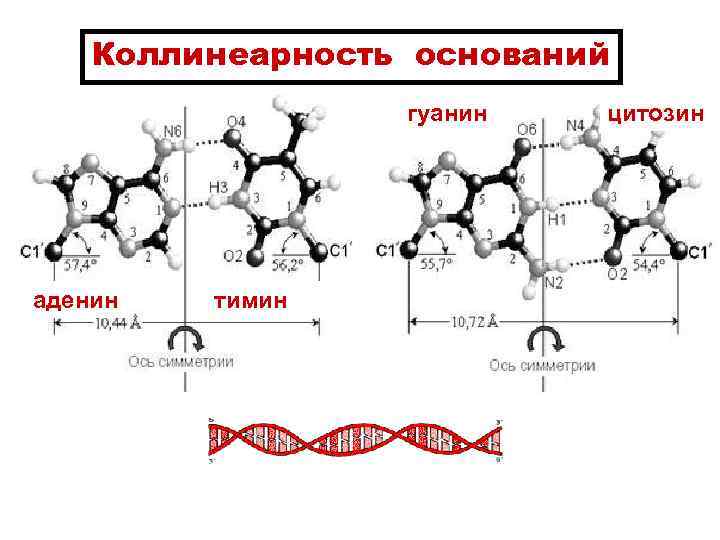 Коллинеарность оснований гуанин аденин тимин цитозин
Коллинеарность оснований гуанин аденин тимин цитозин
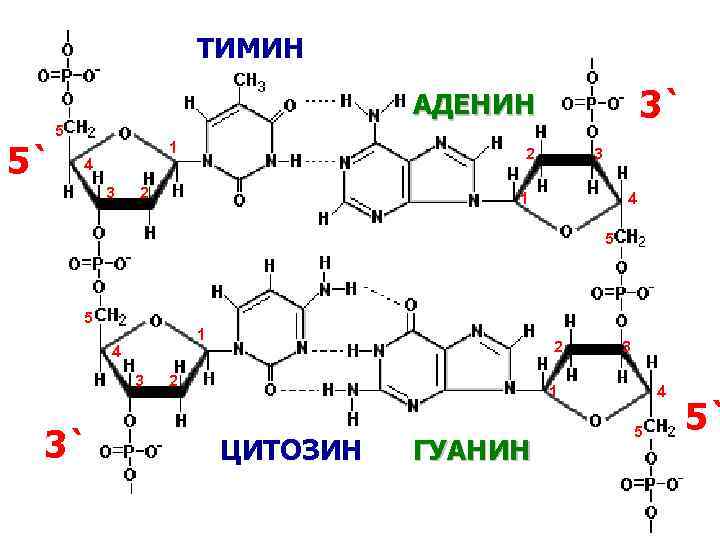 ТИМИН 3` АДЕНИН 5` 5 1 4 3 2 2 3 1 4 5 5 1 4 3 3` 2 2 3 1 ЦИТОЗИН ГУАНИН 4 5 5`
ТИМИН 3` АДЕНИН 5` 5 1 4 3 2 2 3 1 4 5 5 1 4 3 3` 2 2 3 1 ЦИТОЗИН ГУАНИН 4 5 5`
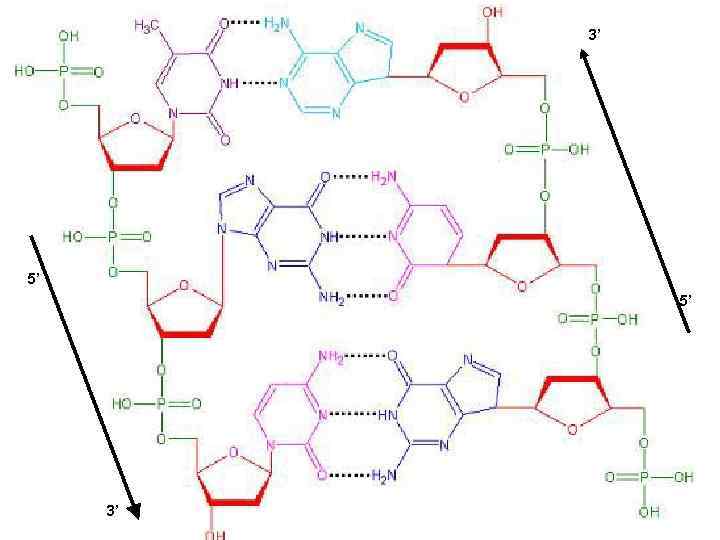 3’ 5’ 5’ 3’
3’ 5’ 5’ 3’
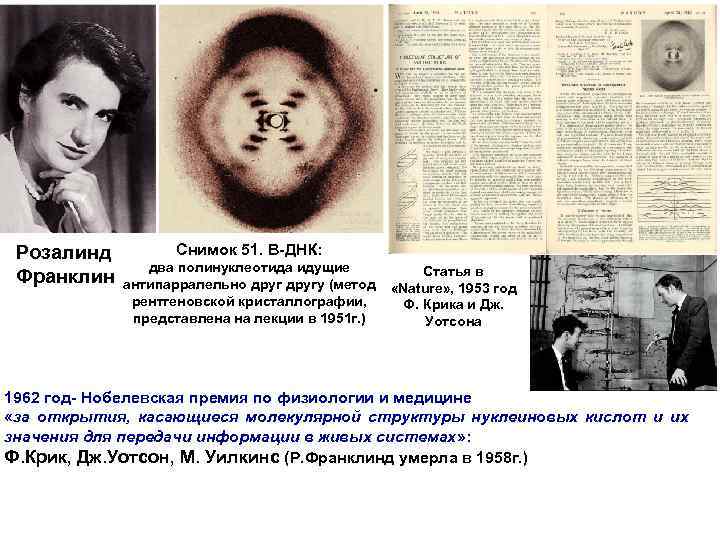 Розалинд Франклин Снимок 51. В-ДНК: два полинуклеотида идущие антипарралельно другу (метод рентгеновской кристаллографии, представлена на лекции в 1951 г. ) Статья в «Nature» , 1953 год Ф. Крика и Дж. Уотсона 1962 год- Нобелевская премия по физиологии и медицине «за открытия, касающиеся молекулярной структуры нуклеиновых кислот и их значения для передачи информации в живых системах» : Ф. Крик, Дж. Уотсон, М. Уилкинс (Р. Франклинд умерла в 1958 г. )
Розалинд Франклин Снимок 51. В-ДНК: два полинуклеотида идущие антипарралельно другу (метод рентгеновской кристаллографии, представлена на лекции в 1951 г. ) Статья в «Nature» , 1953 год Ф. Крика и Дж. Уотсона 1962 год- Нобелевская премия по физиологии и медицине «за открытия, касающиеся молекулярной структуры нуклеиновых кислот и их значения для передачи информации в живых системах» : Ф. Крик, Дж. Уотсон, М. Уилкинс (Р. Франклинд умерла в 1958 г. )
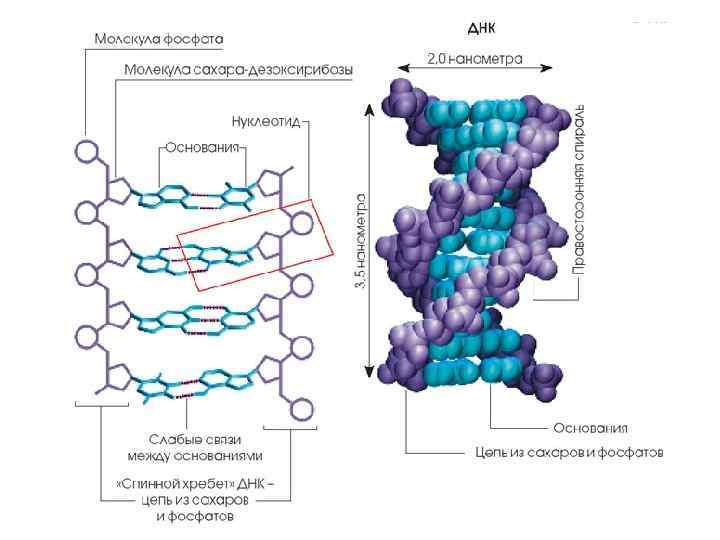
 Репликация ДНК совершается по полуконсервативному механизму Be continuities …
Репликация ДНК совершается по полуконсервативному механизму Be continuities …
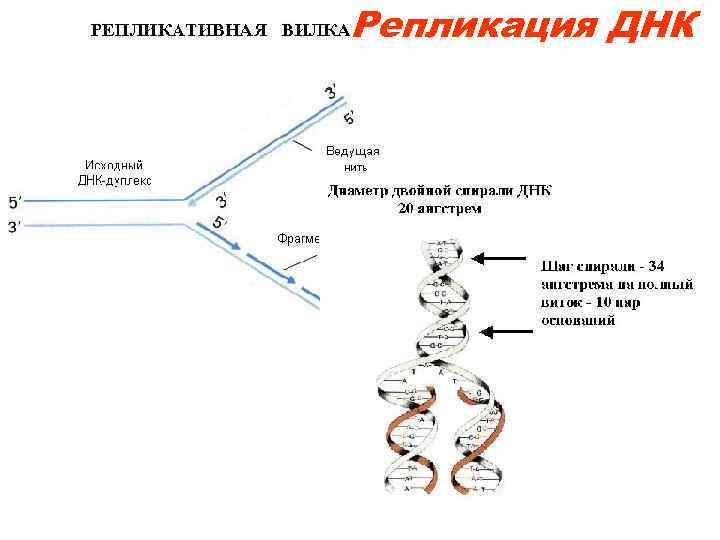 Репликация ДНК Be continuities …
Репликация ДНК Be continuities …
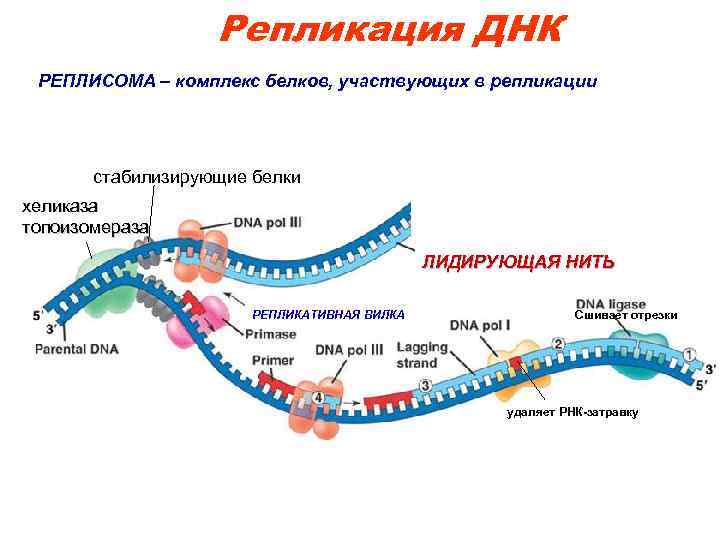 Репликация ДНК РЕПЛИСОМА – комплекс белков, участвующих в репликации стабилизирующие белки хеликаза топоизомераза ЛИДИРУЮЩАЯ НИТЬ РЕПЛИКАТИВНАЯ ВИЛКА Сшивает отрезки удаляет РНК-затравку
Репликация ДНК РЕПЛИСОМА – комплекс белков, участвующих в репликации стабилизирующие белки хеликаза топоизомераза ЛИДИРУЮЩАЯ НИТЬ РЕПЛИКАТИВНАЯ ВИЛКА Сшивает отрезки удаляет РНК-затравку
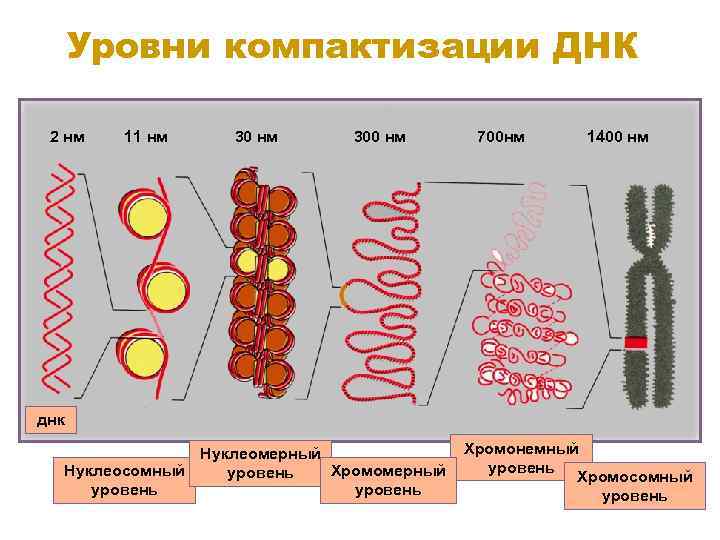 Уровни компактизации ДНК 2 нм 11 нм 300 нм 700 нм 1400 нм днк Нуклеомерный Нуклеосомный Хромомерный уровень Хромонемный уровень Хромосомный уровень
Уровни компактизации ДНК 2 нм 11 нм 300 нм 700 нм 1400 нм днк Нуклеомерный Нуклеосомный Хромомерный уровень Хромонемный уровень Хромосомный уровень
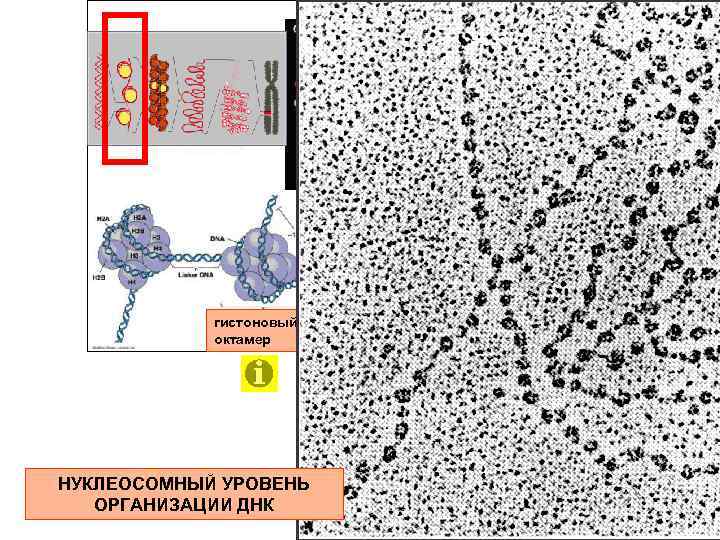 ДНК гистоновый октамер НУКЛЕОСОМНЫЙ УРОВЕНЬ ОРГАНИЗАЦИИ ДНК
ДНК гистоновый октамер НУКЛЕОСОМНЫЙ УРОВЕНЬ ОРГАНИЗАЦИИ ДНК
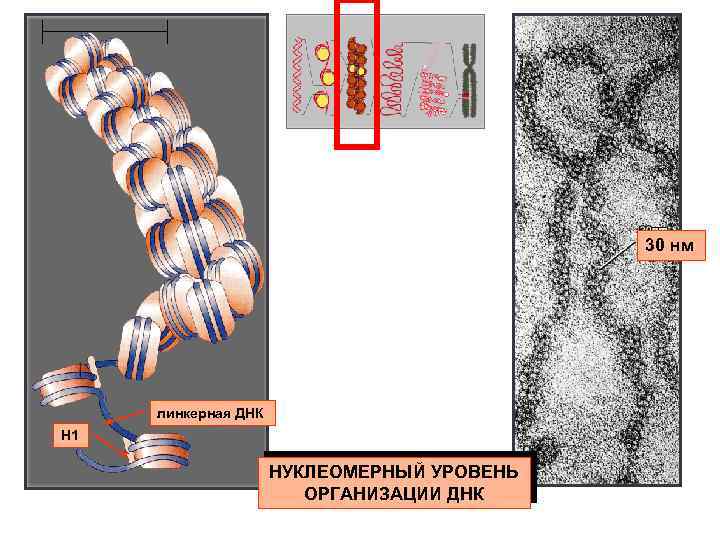 30 нм линкерная ДНК Н 1 НУКЛЕОМЕРНЫЙ УРОВЕНЬ ОРГАНИЗАЦИИ ДНК
30 нм линкерная ДНК Н 1 НУКЛЕОМЕРНЫЙ УРОВЕНЬ ОРГАНИЗАЦИИ ДНК
 Уровни компактизации ДНК 2 нм 11 нм 300 нм хромомерный уровень 700 нм Хромонемный уровень 1400 нм
Уровни компактизации ДНК 2 нм 11 нм 300 нм хромомерный уровень 700 нм Хромонемный уровень 1400 нм
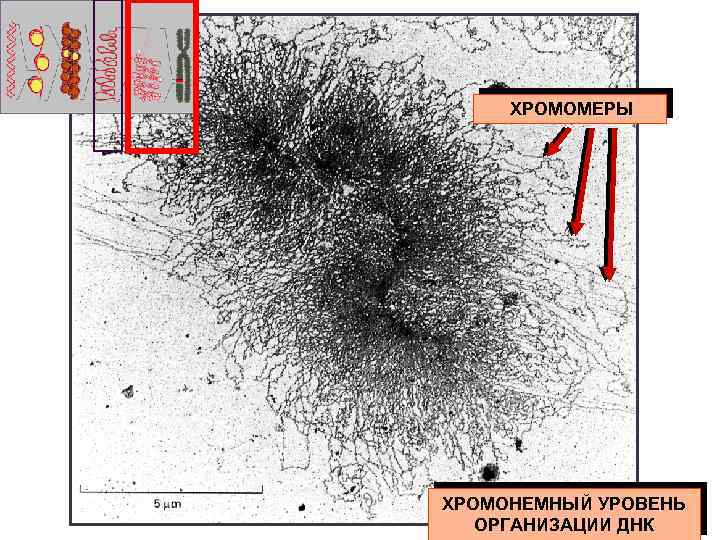 ХРОМОМЕРЫ ХРОМОНЕМНЫЙ УРОВЕНЬ ОРГАНИЗАЦИИ ДНК
ХРОМОМЕРЫ ХРОМОНЕМНЫЙ УРОВЕНЬ ОРГАНИЗАЦИИ ДНК
 1868 г. – Ф. Мишер –нуклеиновые кислоты 1871 г. – Н. Н. Любавин – Белки состоят из аминокислот 1873 г. – Ф. Шнейдер –хромосомы
1868 г. – Ф. Мишер –нуклеиновые кислоты 1871 г. – Н. Н. Любавин – Белки состоят из аминокислот 1873 г. – Ф. Шнейдер –хромосомы
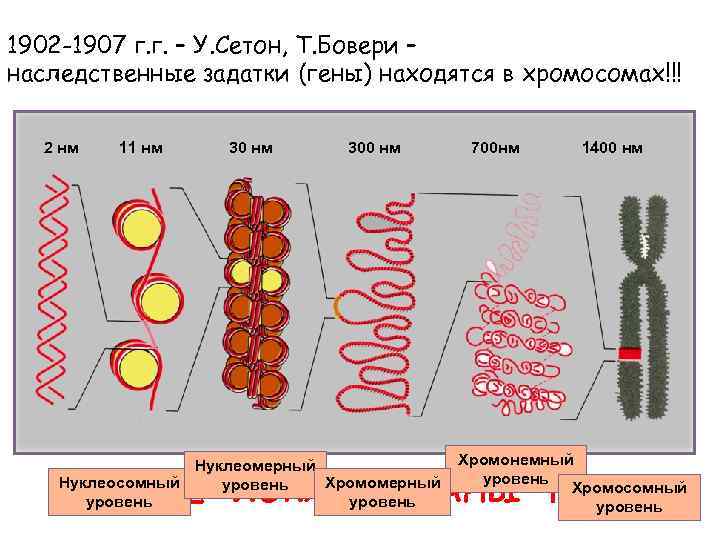 1902 -1907 г. г. – У. Сетон, Т. Бовери – наследственные задатки (гены) находятся в хромосомах!!! 2 нм 11 нм 300 нм 700 нм 1400 нм ХРОМОСОМЫ = НУКЛЕИНОВЫЕ КИСЛОТЫ + БЕЛКИ Нуклеомерный Нуклеосомный Хромомерный уровень Хромонемный уровень Хромосомный уровень ГДЕ ЖЕ ЛОКАЛИЗОВАНЫ ГЕНЫ? !
1902 -1907 г. г. – У. Сетон, Т. Бовери – наследственные задатки (гены) находятся в хромосомах!!! 2 нм 11 нм 300 нм 700 нм 1400 нм ХРОМОСОМЫ = НУКЛЕИНОВЫЕ КИСЛОТЫ + БЕЛКИ Нуклеомерный Нуклеосомный Хромомерный уровень Хромонемный уровень Хромосомный уровень ГДЕ ЖЕ ЛОКАЛИЗОВАНЫ ГЕНЫ? !
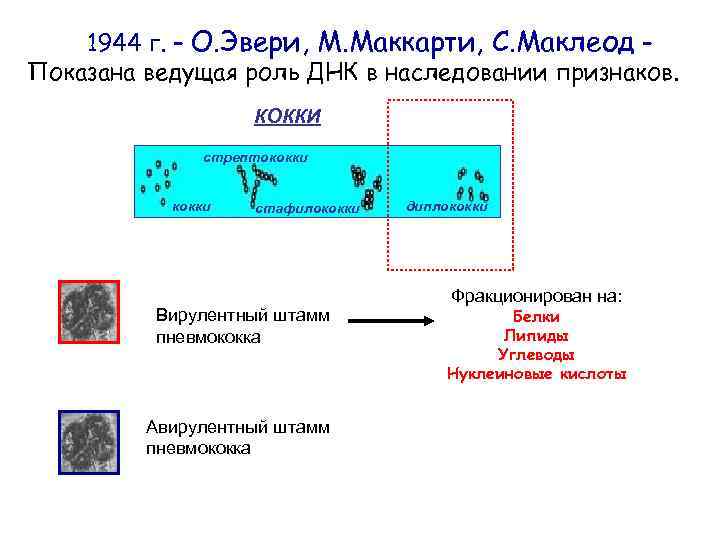 1944 г. – О. Эвери, М. Маккарти, С. Маклеод – Показана ведущая роль ДНК в наследовании признаков. КОККИ стрептококки стафилококки Вирулентный штамм пневмококка Авирулентный штамм пневмококка диплококки Фракционирован на: Белки Липиды Углеводы Нуклеиновые кислоты
1944 г. – О. Эвери, М. Маккарти, С. Маклеод – Показана ведущая роль ДНК в наследовании признаков. КОККИ стрептококки стафилококки Вирулентный штамм пневмококка Авирулентный штамм пневмококка диплококки Фракционирован на: Белки Липиды Углеводы Нуклеиновые кислоты
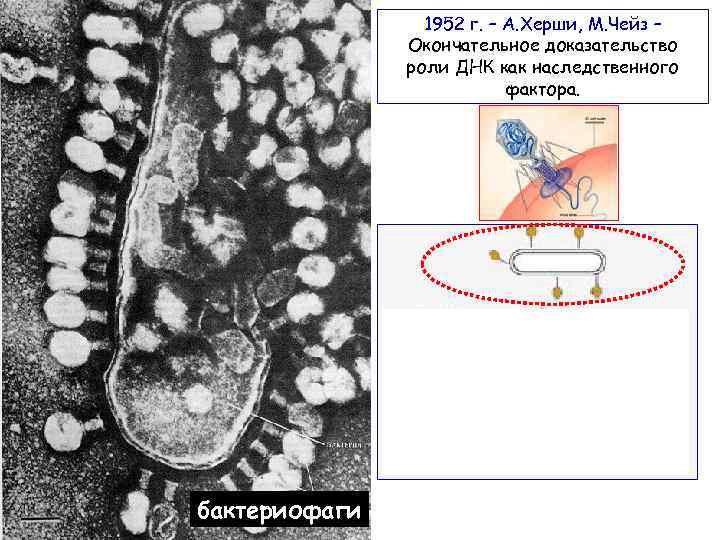 1952 г. – А. Херши, М. Чейз – Окончательное доказательство роли ДНК как наследственного фактора. бактериофаги
1952 г. – А. Херши, М. Чейз – Окончательное доказательство роли ДНК как наследственного фактора. бактериофаги
 Генетический код 1954 – Георгий Антонович Гамов – идея триплетного кодирования
Генетический код 1954 – Георгий Антонович Гамов – идея триплетного кодирования
 Свойства генетического кода • Триплетность — значащей единицей кода является триплет (= кодон) • Непрерывность —триплеты считываются непрерывно • Дискретность — триплеты считываются как целое • Специфичность — определённый кодон соответствует только одной аминокислоте • Вырожденность (=избыточность) — одной и той же аминокислоте может соответствовать несколько кодонов • Универсальность — генетический код работает одинаково в организмах разного уровня сложности • Помехоустойчивость — мутации могут быть консервативными, если замена нуклеотидов не приводит к смене класса кодируемой аминокислоты и, как следствие, не ведет к изменению конформации белка; ( в ином случае - мутации носят радикальный характер ).
Свойства генетического кода • Триплетность — значащей единицей кода является триплет (= кодон) • Непрерывность —триплеты считываются непрерывно • Дискретность — триплеты считываются как целое • Специфичность — определённый кодон соответствует только одной аминокислоте • Вырожденность (=избыточность) — одной и той же аминокислоте может соответствовать несколько кодонов • Универсальность — генетический код работает одинаково в организмах разного уровня сложности • Помехоустойчивость — мутации могут быть консервативными, если замена нуклеотидов не приводит к смене класса кодируемой аминокислоты и, как следствие, не ведет к изменению конформации белка; ( в ином случае - мутации носят радикальный характер ).
 Серповидноклеточная анемия – результат точковой мутации –замены Глутаминовой к-ты (-) на Валин (непол. )
Серповидноклеточная анемия – результат точковой мутации –замены Глутаминовой к-ты (-) на Валин (непол. )
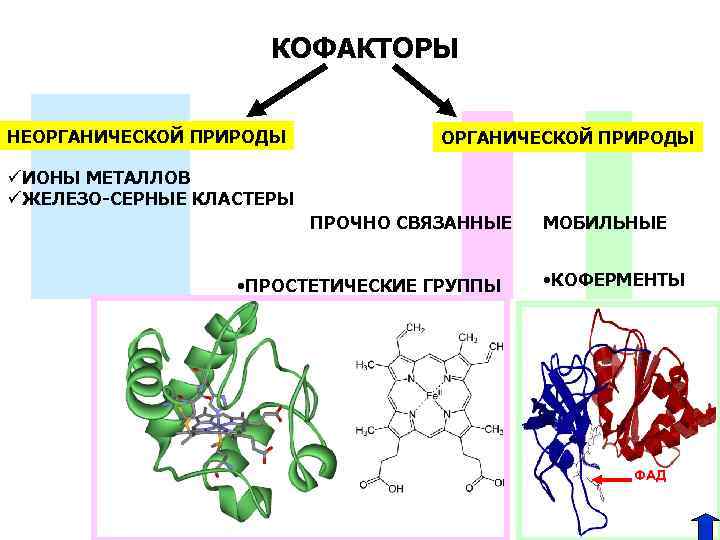 КОФАКТОРЫ НЕОРГАНИЧЕСКОЙ ПРИРОДЫ üИОНЫ МЕТАЛЛОВ üЖЕЛЕЗО-СЕРНЫЕ КЛАСТЕРЫ ПРОЧНО СВЯЗАННЫЕ • ПРОСТЕТИЧЕСКИЕ ГРУППЫ МОБИЛЬНЫЕ • КОФЕРМЕНТЫ ФАД
КОФАКТОРЫ НЕОРГАНИЧЕСКОЙ ПРИРОДЫ üИОНЫ МЕТАЛЛОВ üЖЕЛЕЗО-СЕРНЫЕ КЛАСТЕРЫ ПРОЧНО СВЯЗАННЫЕ • ПРОСТЕТИЧЕСКИЕ ГРУППЫ МОБИЛЬНЫЕ • КОФЕРМЕНТЫ ФАД
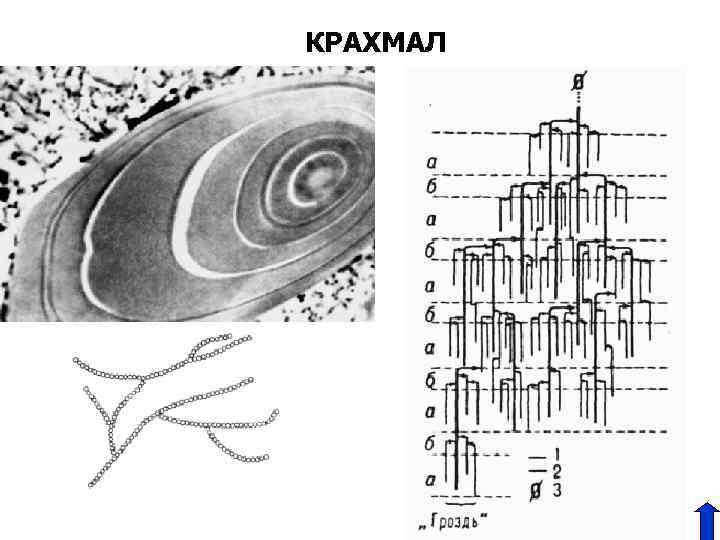 КРАХМАЛ
КРАХМАЛ
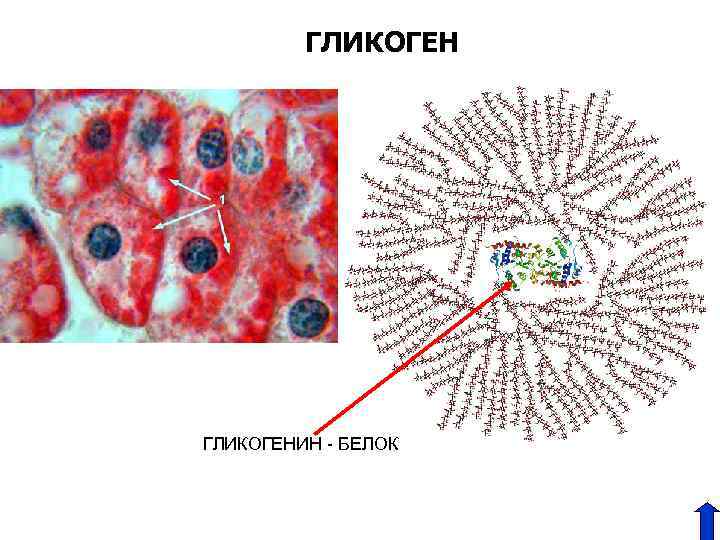 ГЛИКОГЕНИН - БЕЛОК
ГЛИКОГЕНИН - БЕЛОК
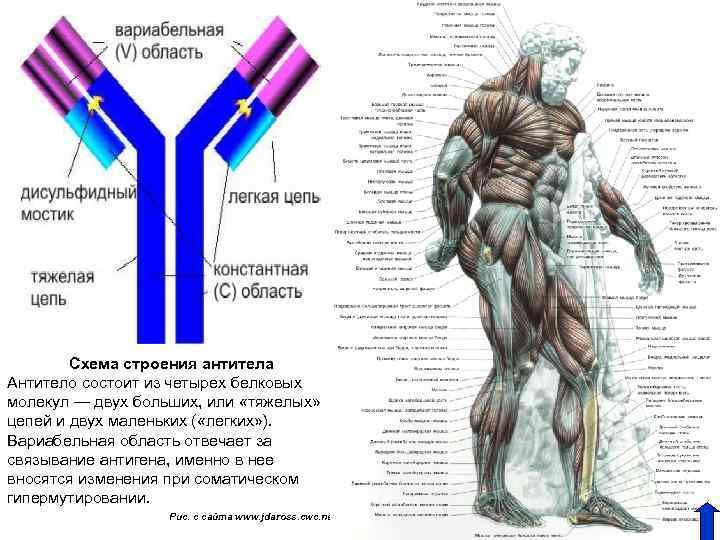 Схема строения антитела Антитело состоит из четырех белковых молекул — двух больших, или «тяжелых» цепей и двух маленьких ( «легких» ). Вариабельная область отвечает за связывание антигена, именно в нее вносятся изменения при соматическом гипермутировании. Рис. с сайта www. jdaross. cwc. net
Схема строения антитела Антитело состоит из четырех белковых молекул — двух больших, или «тяжелых» цепей и двух маленьких ( «легких» ). Вариабельная область отвечает за связывание антигена, именно в нее вносятся изменения при соматическом гипермутировании. Рис. с сайта www. jdaross. cwc. net
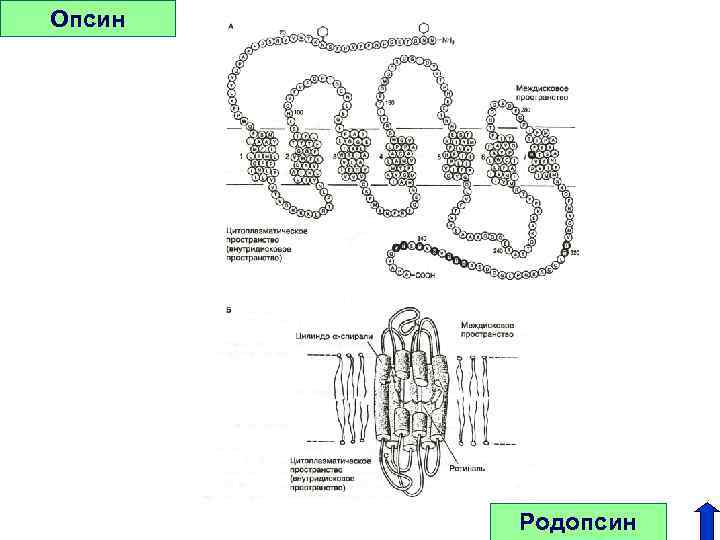 Опсин Родопсин
Опсин Родопсин
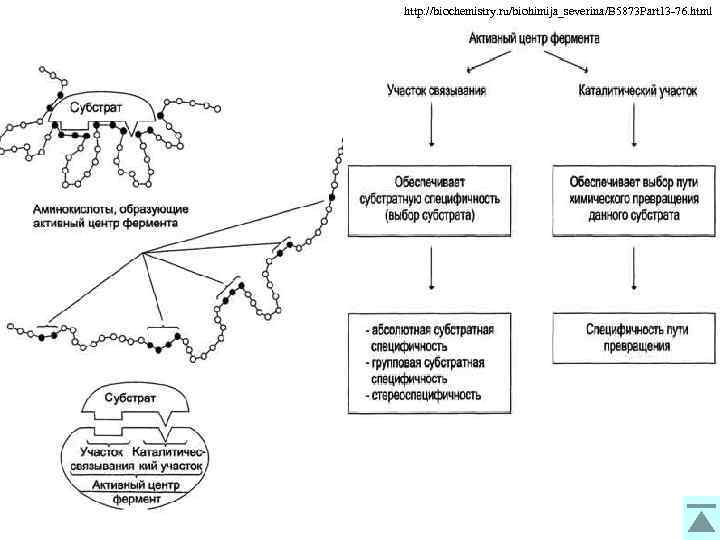 http: //biochemistry. ru/biohimija_severina/B 5873 Part 13 -76. html
http: //biochemistry. ru/biohimija_severina/B 5873 Part 13 -76. html
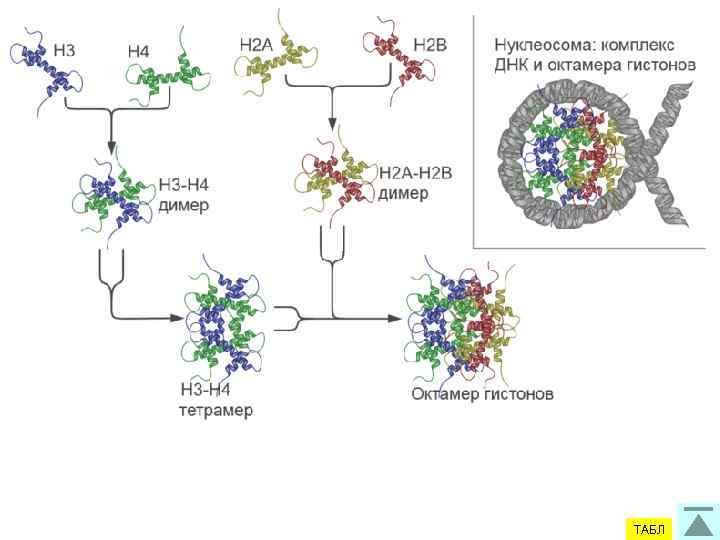 ГИСТОНЫ Любая мутация в гистоновых генах летальна ! ФРАКЦИЯ ЛИЗИН АРГИНИН Н 1 (очень богатая лизином) 1 29 % 1% Н 2 а (умеренно богатая лизином) 11% 9% Н 2 b (умеренно богатая лизином) 16% 6% Н 3 (очень богатая аргинином) 10% 13% Н 4 (богатая аргинином) 11% 14% Все гистоны, кроме Н 1, чрезвычайно консервативны в эволюционном отношении ! ТАБЛ
ГИСТОНЫ Любая мутация в гистоновых генах летальна ! ФРАКЦИЯ ЛИЗИН АРГИНИН Н 1 (очень богатая лизином) 1 29 % 1% Н 2 а (умеренно богатая лизином) 11% 9% Н 2 b (умеренно богатая лизином) 16% 6% Н 3 (очень богатая аргинином) 10% 13% Н 4 (богатая аргинином) 11% 14% Все гистоны, кроме Н 1, чрезвычайно консервативны в эволюционном отношении ! ТАБЛ


