химический состав клетки.pptx
- Количество слайдов: 36

ХИМИЧЕСКИЙ СОСТАВ КЛЕТКИ
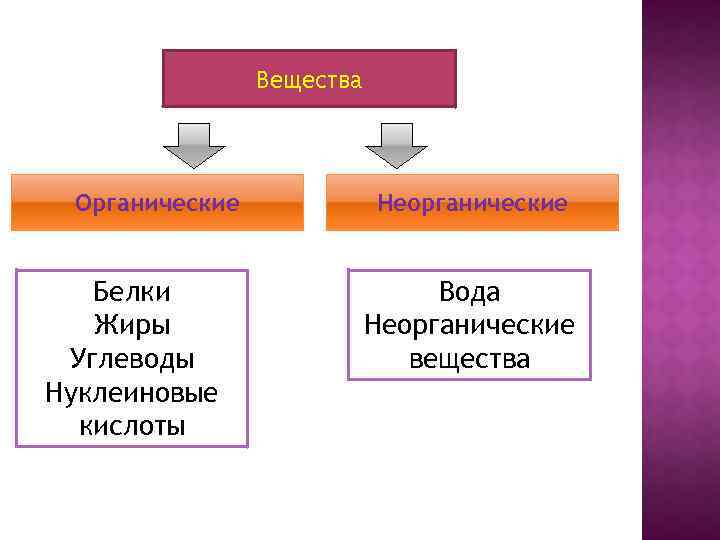
Вещества Органические Белки Жиры Углеводы Нуклеиновые кислоты Неорганические Вода Неорганические вещества
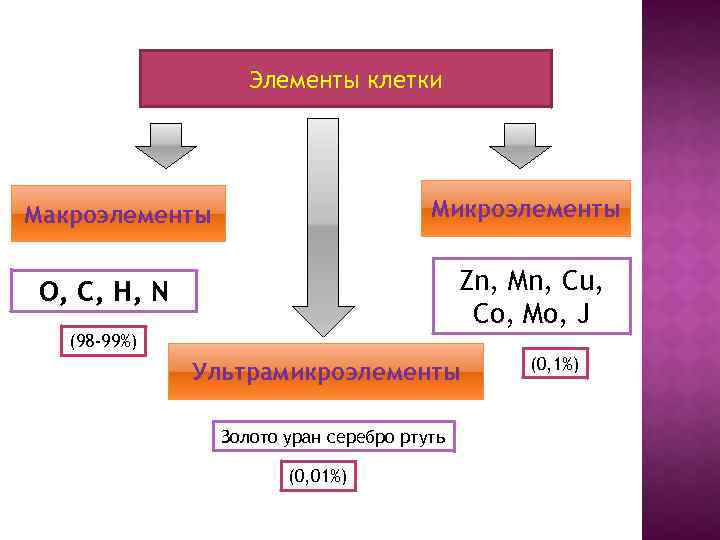
Элементы клетки Микроэлементы Макроэлементы Zn, Mn, Cu, Co, Mo, J O, C, H, N (98 -99%) Ультрамикроэлементы Золото уран серебро ртуть (0, 01%) (0, 1%)

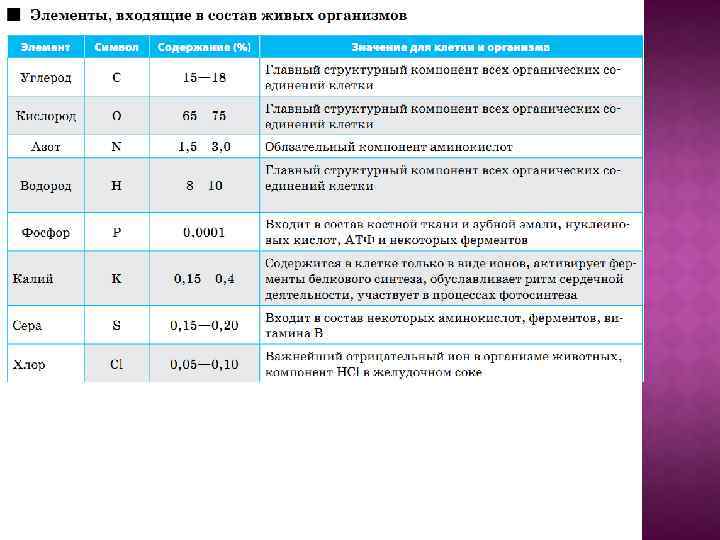
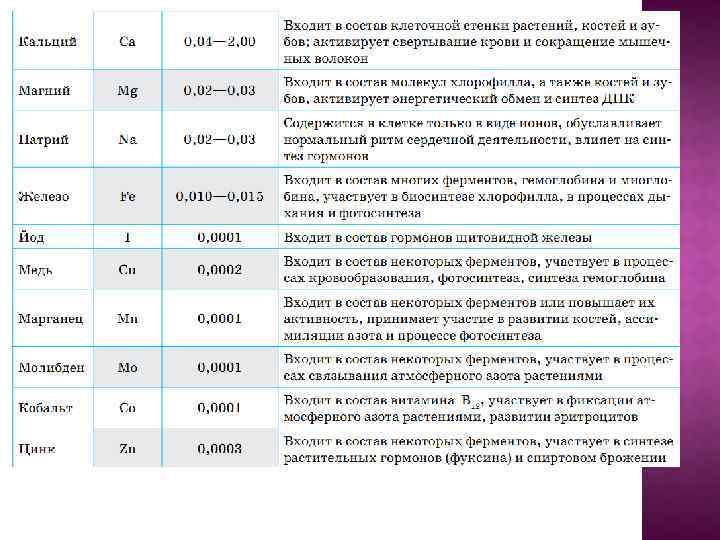
ВАЖНАЯ РОЛЬ В ОРГАНИЗМЕ: Азот – в клетках белков, нук Фосфор – ДНК, РНК, АТФ Магний – хлорофилл Железо – гемоглобин Цинк – в гормоне поджелудочной железы Йод – в щитовидной железе Кальций – в свертывание крови Калий, натрий - нервные импульсы

ВОДА Вода - преобладающий компонент всех живых организмов. Молекула воды имеет форму диполя и между ними образуются водородные связи. Среднее содержание воды в клетках около 80%. Вода присутствует в двух формах: свободной и связанной Гидрофильные вещества- вещества, растворимые в воде Гидрофобные вещества- вещества, нерастворимые в воде

ФУНКЦИИ ВОДЫ. 1. 2. 3. 4. 5. 6. Вода –универсальный растворитель. Гидрофильные (водорастворимые) и гидрофобные (нерастворимые в воде) Вода как реагент. Участвует во многих химических реакциях: гидролиз, фотосинтез Транспортная функция. Вода как термостабилизатор и терморегулятор. Свойства воды: высокая теплоемкость, высокая теплопроводность, высокая теплота испарения. Структурная функция. У растений вода поддерживает тургор, у животных служит гидростатическим скелетом (медузы). Вода- основная среда перемещения веществ в организме и клетке
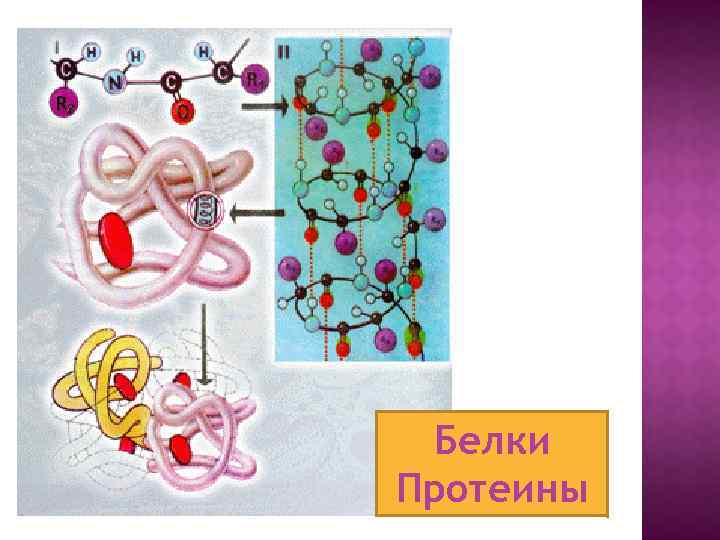
Белки Протеины
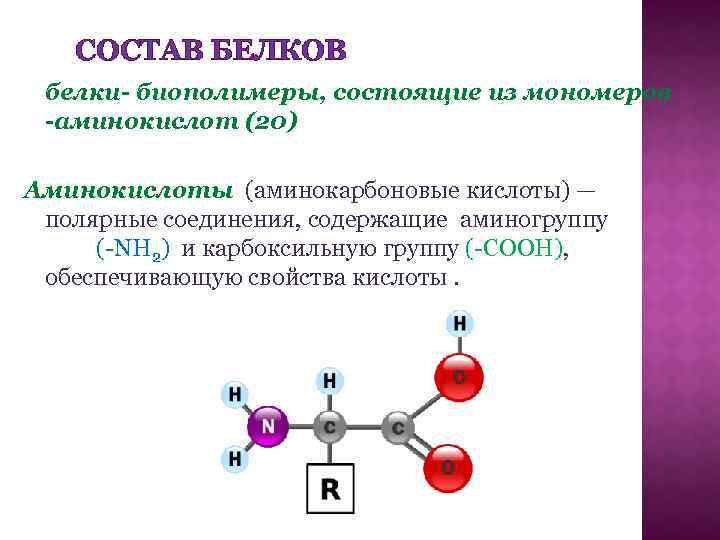
СОСТАВ БЕЛКОВ белки- биополимеры, состоящие из мономеров -аминокислот (20) Аминокислоты (аминокарбоновые кислоты) — полярные соединения, содержащие аминогруппу (-NH 2) и карбоксильную группу (-COOH), обеспечивающую свойства кислоты.
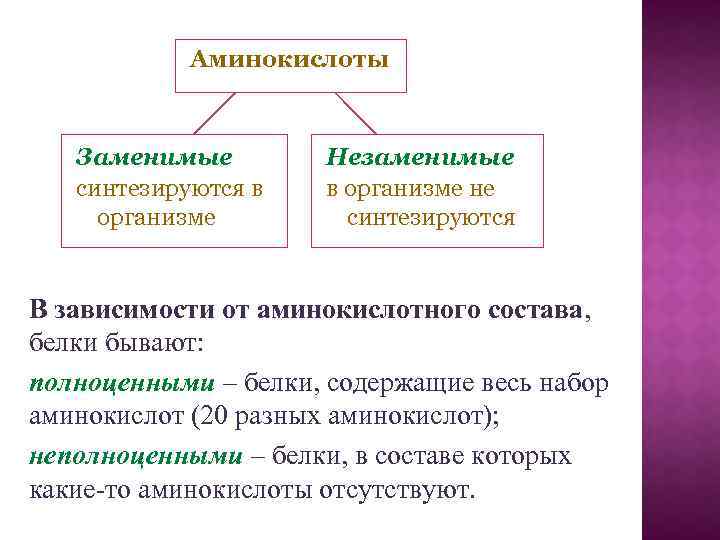
Аминокислоты Заменимые синтезируются в организме Незаменимые в организме не синтезируются В зависимости от аминокислотного состава, белки бывают: полноценными – белки, содержащие весь набор аминокислот (20 разных аминокислот); неполноценными – белки, в составе которых какие-то аминокислоты отсутствуют.

Простые белки –состоят только из аминокислот: альбумины, глобулины, гистоны Сложные белки - кроме содержат углеводы, жиры, нуклеиновые кислоты , нуклеопротеины Белки, как и антитела, защищают организм от болезнетворных бактерий и вирусов.
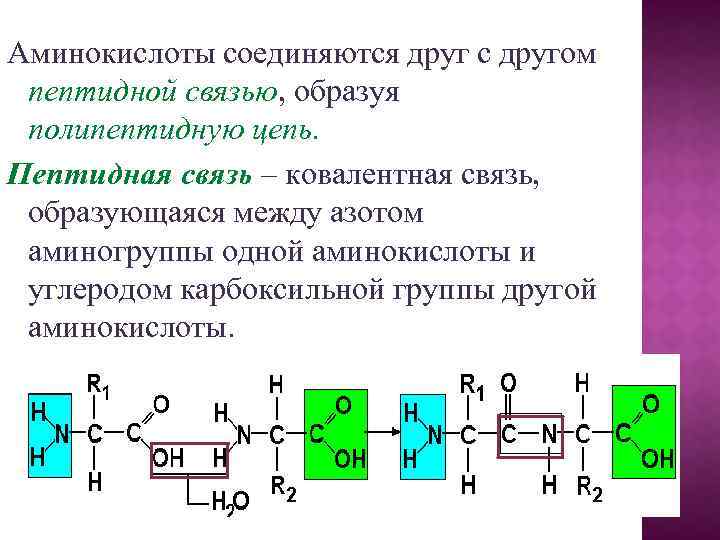
Аминокислоты соединяются друг с другом пептидной связью, образуя полипептидную цепь. Пептидная связь – ковалентная связь, образующаяся между азотом аминогруппы одной аминокислоты и углеродом карбоксильной группы другой аминокислоты.

СТРУКТУРА МОЛЕКУЛЫ БЕЛКА Выделяют 4 уровня пространственной организации белков. Первичная структура – последовательность аминокислот в полипептидной цепи. Она образуется за счет ковалентных пептидных связей между аминокислотными остатками.
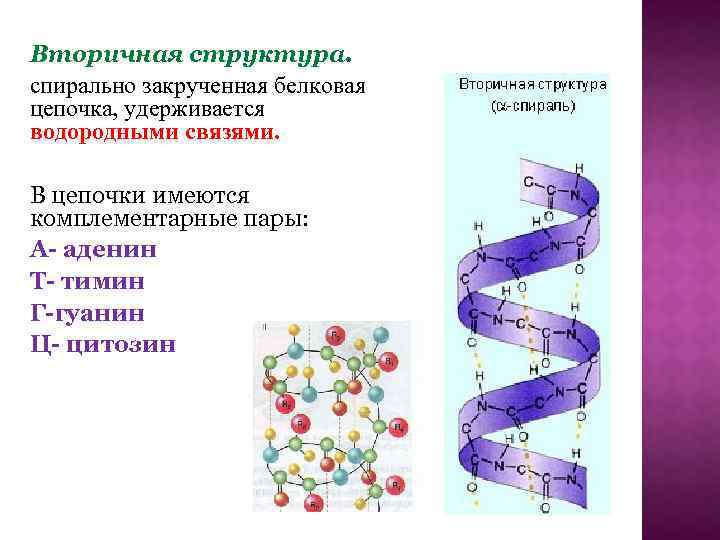
Вторичная структура. спирально закрученная белковая цепочка, удерживается водородными связями. В цепочки имеются комплементарные пары: А- аденин Т- тимин Г-гуанин Ц- цитозин
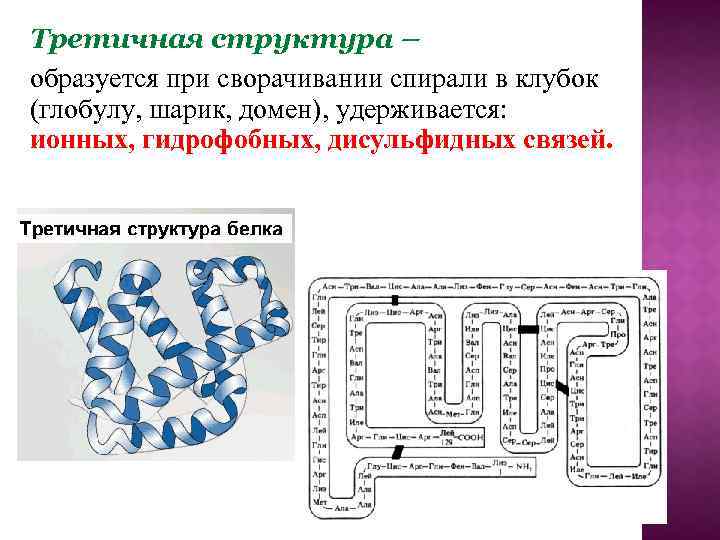
Третичная структура – образуется при сворачивании спирали в клубок (глобулу, шарик, домен), удерживается: ионных, гидрофобных, дисульфидных связей.
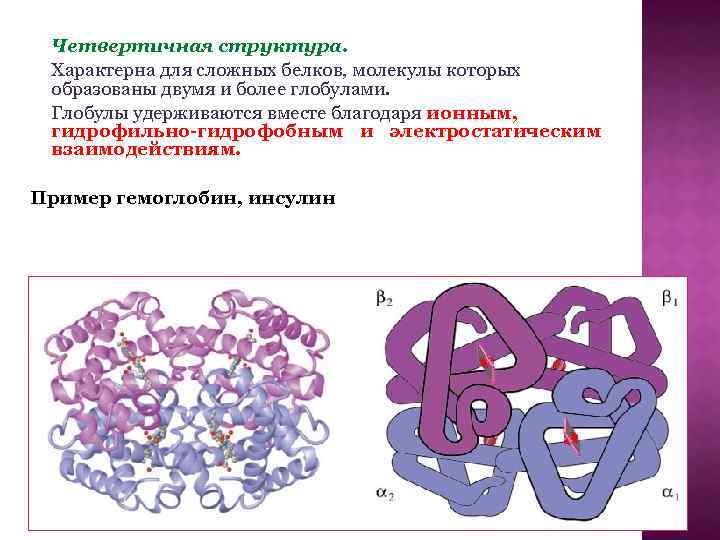
Четвертичная структура. Характерна для сложных белков, молекулы которых образованы двумя и более глобулами. Глобулы удерживаются вместе благодаря ионным, гидрофильно-гидрофобным и электростатическим взаимодействиям. Пример гемоглобин, инсулин

Денатурация – разрушение структур 3 -2 -1, нарушение структурной организации белка. Процесс обратим, если не разрушены пептидные связи. Ренатурация – восстановление нормальной структуры, сохраняется первичная. Деструкция- полное разрушение белковой молекулы.

ФУНКЦИИ БЕЛКОВ 1. Каталитическая 2. Строительная 3. Транспортная 4. Двигательная 5. Защитная 6. Гормональная 7. Запасная 8. Опорная 9. Рецепторная 10. Энергетическая

КАТАЛИТИЧЕСКАЯ ФУНКЦИЯ БЕЛКОВ Все клеточные катализаторы – белки. Их называют биокатализаторами, а чаще – ферментами. Они ускоряют реакции в десятки, сотни миллионов раз.

Защитная Предохраняют организм от вторжения чужеродных организмов и от повреждений Антитела блокируют чужеродные белки Например, фибриноген и протромбин обеспечивают свертываемость крови
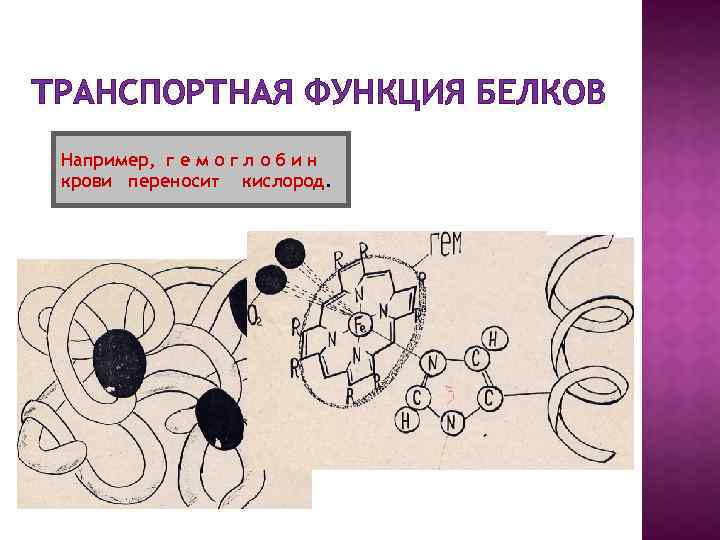
ТРАНСПОРТНАЯ ФУНКЦИЯ БЕЛКОВ Например, г е м о г л о б и н крови переносит кислород.
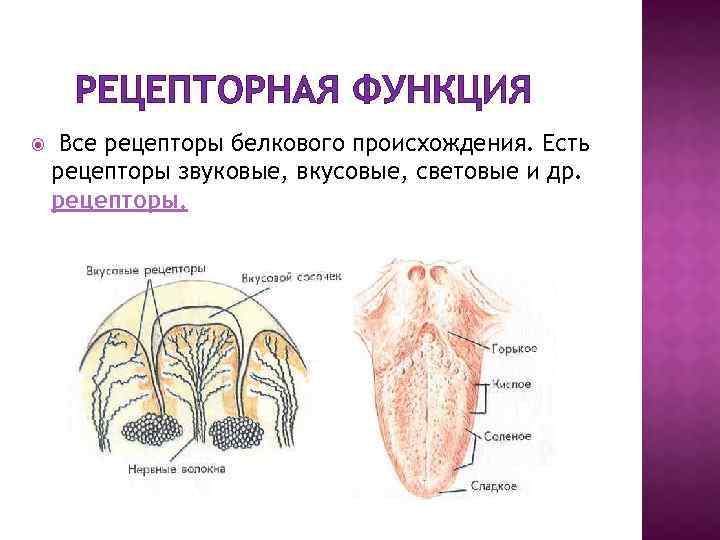
РЕЦЕПТОРНАЯ ФУНКЦИЯ Все рецепторы белкового происхождения. Есть рецепторы звуковые, вкусовые, световые и др. рецепторы.

Сократительная Белки - участвуют в сокращении мышечных волокон. Актин и миозин – белки мышц

Энергетическая 1 г белка - 17. 6 к. Дж
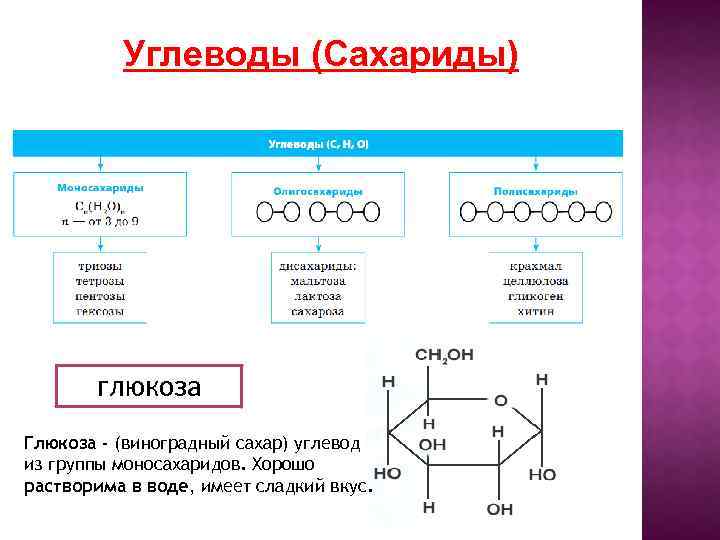
Углеводы (Сахариды) глюкоза Глюкоза - (виноградный сахар) углевод из группы моносахаридов. Хорошо растворима в воде, имеет сладкий вкус.

УГЛЕВОДЫ ДЕЛЯТСЯ: Моносахариды – глюкоза, фруктоза, рибоза, дезоксирибоза, галактоза. Бесцветные, твердые кристаллические вещества, имеющие сладкий вкус. Дисахариды –сахароза, мальтоза, лактоза (молочный сахар)Имеют сладкий вкус. Полисахариды – Крахмал (запасается в клетках растений) Гликоген (в животных клетках), Хитин - образуется у ракообразных наружный скелет(панцирь) Целлюлоза (клетчатка)- главный компонент клеточной стенки у растений

ФУНКЦИИ УГЛЕВОДОВ: 1. 2. 3. 4. энергетическая – 1 г глюкозы – 17, 6 к. Дж энергии запасающая строительная рецепторная
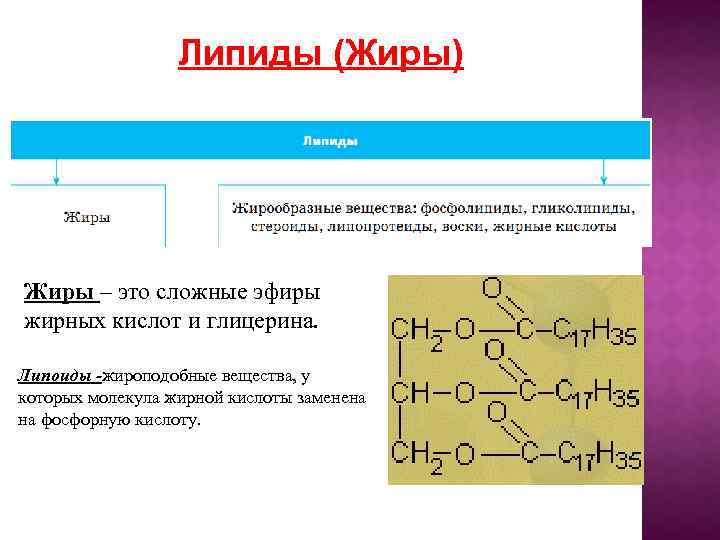
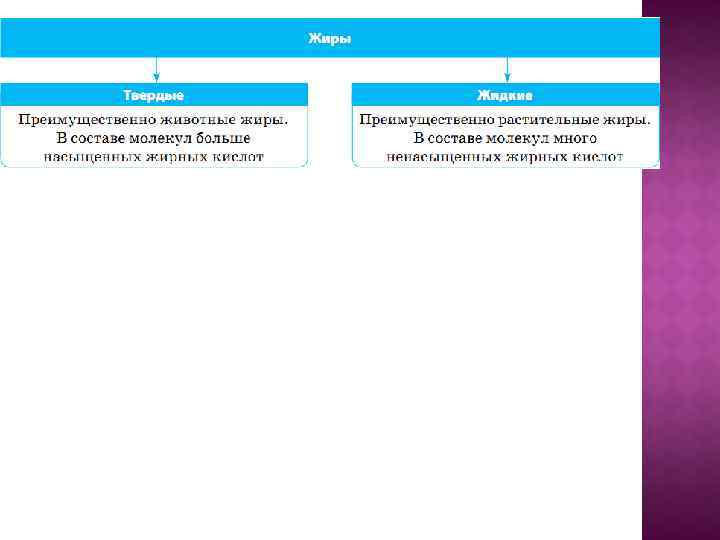
Липиды (Жиры) Жиры – это сложные эфиры жирных кислот и глицерина. Липоиды -жироподобные вещества, у которых молекула жирной кислоты заменена на фосфорную кислоту.

ФУНКЦИИ ЛИПИДОВ: 1. 2. 3. 4. 5. энергетическая – 1 г жира- 38 к. Дж строительная (структурная)- образует клеточные мембраны запасающая – защитная - подкожный жир смягчает удары терморегуляция - у кита (подкожная клетчатка)
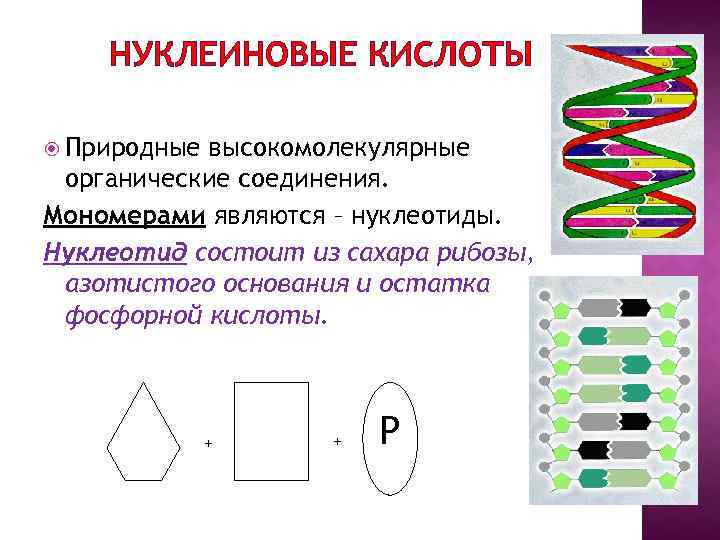
НУКЛЕИНОВЫЕ КИСЛОТЫ Природные высокомолекулярные органические соединения. Мономерами являются – нуклеотиды. Нуклеотид состоит из сахара рибозы, азотистого основания и остатка фосфорной кислоты. + + Р
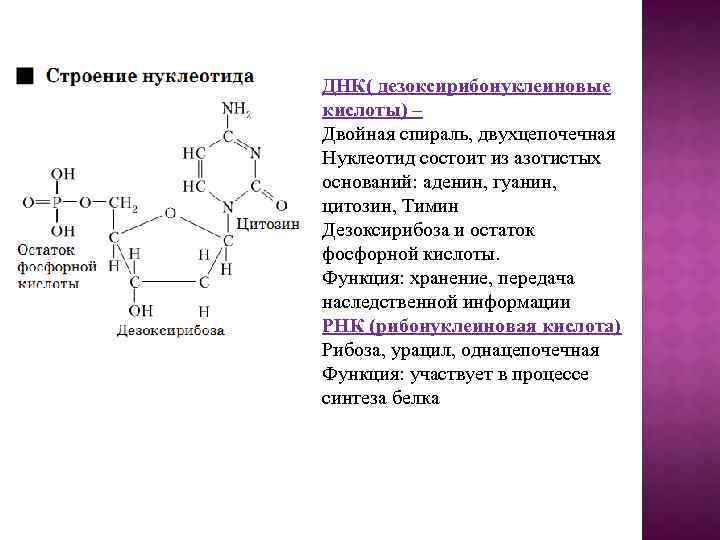
ДНК( дезоксирибонуклеиновые кислоты) – Двойная спираль, двухцепочечная Нуклеотид состоит из азотистых оснований: аденин, гуанин, цитозин, Тимин Дезоксирибоза и остаток фосфорной кислоты. Функция: хранение, передача наследственной информации РНК (рибонуклеиновая кислота) Рибоза, урацил, однацепочечная Функция: участвует в процессе синтеза белка

ВИДЫ РНК: Существует несколько разных РНК. Они носят название в зависимости от выполняемой в клетке функции или от места нахождения. Один вид РНК представлен транспортными РНК (т-РНК), так как они транспортируют аминокислоты к синтезу белка. Второй вид РНК – информационные (и-РНК): они переносят информацию о структуре белка, который должен синтезироваться. (из ядра к рибосомам) Третий вид РНК – рибосомные РНК (р-РНК): они содержатся в рибосомах. В структуре РНК нет двойной спирали, по своему строению она схожа с одной из цепей ДНК.
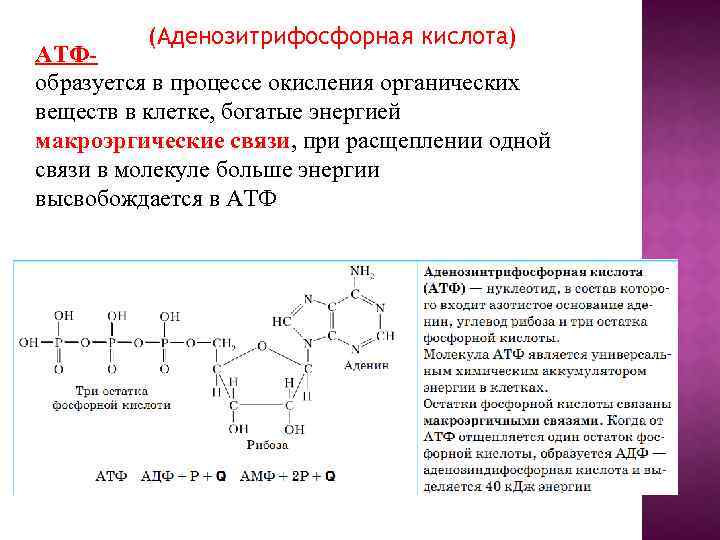
(Аденозитрифосфорная кислота) АТФобразуется в процессе окисления органических веществ в клетке, богатые энергией макроэргические связи, при расщеплении одной связи в молекуле больше энергии высвобождается в АТФ
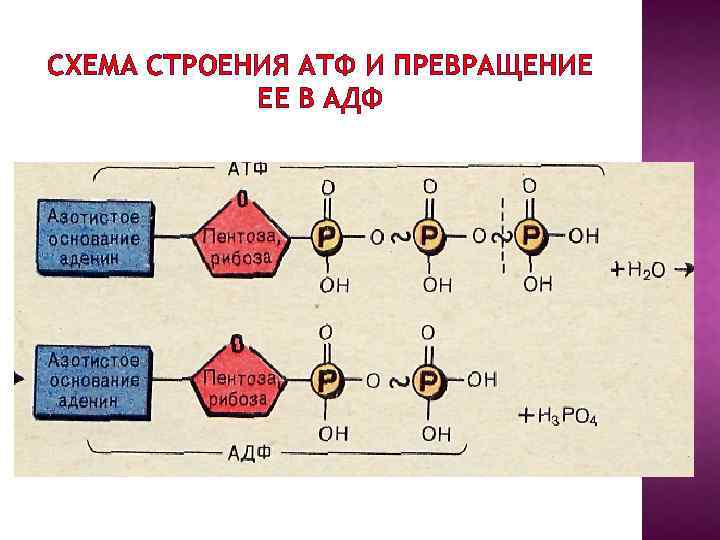
СХЕМА СТРОЕНИЯ АТФ И ПРЕВРАЩЕНИЕ ЕЕ В АДФ
химический состав клетки.pptx