Химия клетки. Подготовка к контрольной.ppt
- Количество слайдов: 66
 Химический состав клетки.
Химический состав клетки.
 Содержание. Ø Содержание химических элементов Ø Неорганические соединения. Ø Органические соединения. Ø Генетический код. Ø Задачи. выход
Содержание. Ø Содержание химических элементов Ø Неорганические соединения. Ø Органические соединения. Ø Генетический код. Ø Задачи. выход
 Неорганические соединения Ø Вода Ø Минеральные вещества
Неорганические соединения Ø Вода Ø Минеральные вещества
 Содержание воды в разных клетках организма: Ø В молодом организме человека и животного – 80 % от массы клетки; Ø В клетках старого организма – 60 %; Ø В головном мозге – 85%; Ø В клетках эмали зубов – 10 -15 %. Ø При потере 20% воды у человека наступает смерть.
Содержание воды в разных клетках организма: Ø В молодом организме человека и животного – 80 % от массы клетки; Ø В клетках старого организма – 60 %; Ø В головном мозге – 85%; Ø В клетках эмали зубов – 10 -15 %. Ø При потере 20% воды у человека наступает смерть.
 Вода. Ø Особенности строения Ø Свойства воды Ø Функции
Вода. Ø Особенности строения Ø Свойства воды Ø Функции
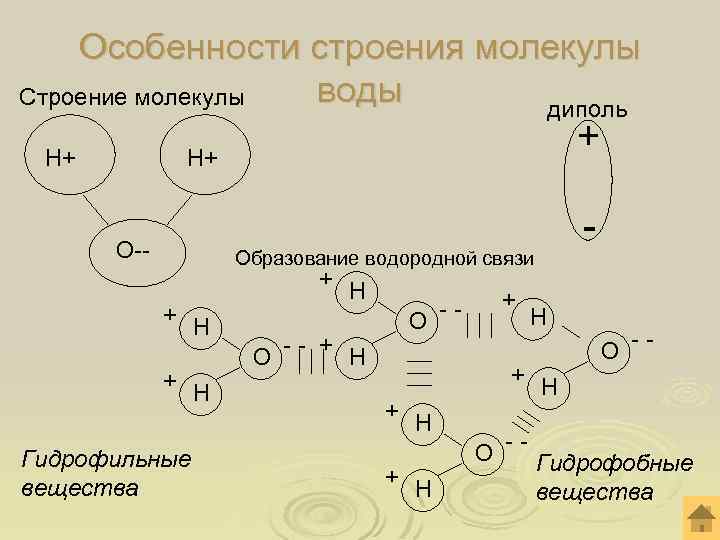 Особенности строения молекулы воды Строение молекулы диполь Н+ + Н+ О-- - Образование водородной связи + Н Гидрофильные вещества + Н О -- + + + Н Н О -- Н О - - Гидрофобные вещества
Особенности строения молекулы воды Строение молекулы диполь Н+ + Н+ О-- - Образование водородной связи + Н Гидрофильные вещества + Н О -- + + + Н Н О -- Н О - - Гидрофобные вещества
 Физические свойства воды и их значения для биологических процессов различных уровней Высокая теплоемкость и теплопроводность Ø Прозрачность в видимом участке спектра Ø Практическая полная несжимаемость Ø Подвижность молекул и вязкость Ø Хороший растворитель Ø Оптимальная для биосистем значение силы поверхностного натяжения Ø Расширение при замерзании Ø
Физические свойства воды и их значения для биологических процессов различных уровней Высокая теплоемкость и теплопроводность Ø Прозрачность в видимом участке спектра Ø Практическая полная несжимаемость Ø Подвижность молекул и вязкость Ø Хороший растворитель Ø Оптимальная для биосистем значение силы поверхностного натяжения Ø Расширение при замерзании Ø
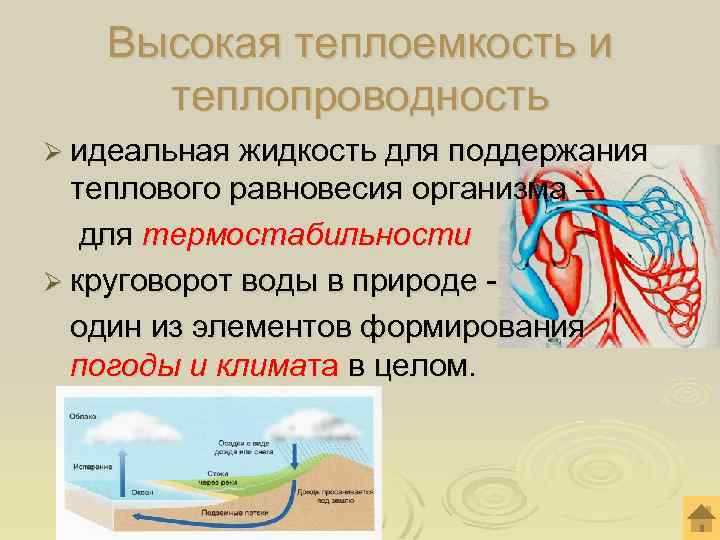 Высокая теплоемкость и теплопроводность Ø идеальная жидкость для поддержания теплового равновесия организма – для термостабильности Ø круговорот воды в природе один из элементов формирования погоды и климата в целом.
Высокая теплоемкость и теплопроводность Ø идеальная жидкость для поддержания теплового равновесия организма – для термостабильности Ø круговорот воды в природе один из элементов формирования погоды и климата в целом.
 Прозрачность в видимом участке спектра Ø возможность фотосинтеза на небольшой глубине и, следовательно, возможность существования связанных с ним пищевых цепей
Прозрачность в видимом участке спектра Ø возможность фотосинтеза на небольшой глубине и, следовательно, возможность существования связанных с ним пищевых цепей
 Практическая полная несжимаемость Ø благодаря силам межмолекулярного сцепления поддерживается форма организмов (тургорное давление, гидростатический скелет, амниотическая жидкость).
Практическая полная несжимаемость Ø благодаря силам межмолекулярного сцепления поддерживается форма организмов (тургорное давление, гидростатический скелет, амниотическая жидкость).
 Подвижность молекул Ø вследствие слабости водородных связей возможно проявление осмоса
Подвижность молекул Ø вследствие слабости водородных связей возможно проявление осмоса
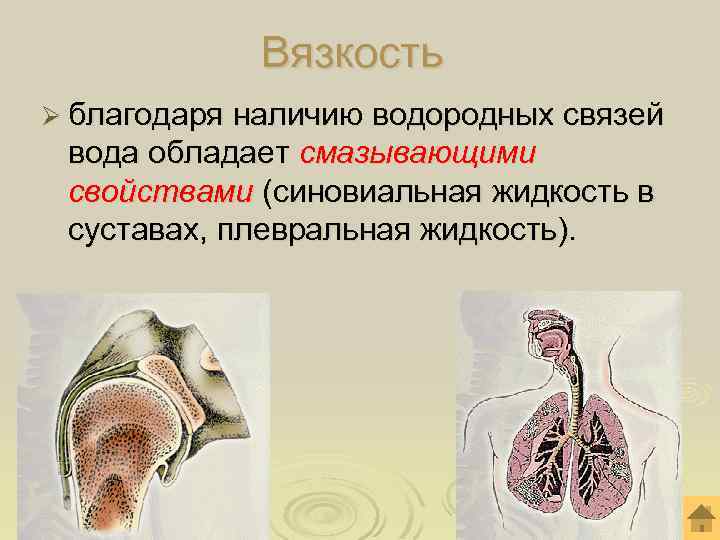 Вязкость Ø благодаря наличию водородных связей вода обладает смазывающими свойствами (синовиальная жидкость в суставах, плевральная жидкость).
Вязкость Ø благодаря наличию водородных связей вода обладает смазывающими свойствами (синовиальная жидкость в суставах, плевральная жидкость).
 Благодаря полярности молекул: самый распространенный в природе растворитель, Ø среда протекания многих химических реакций в организме, Ø образует гидратационную оболочку вокруг макромолекул (является дисперсионной средой в коллоидной системе цитоплазмы). Ø
Благодаря полярности молекул: самый распространенный в природе растворитель, Ø среда протекания многих химических реакций в организме, Ø образует гидратационную оболочку вокруг макромолекул (является дисперсионной средой в коллоидной системе цитоплазмы). Ø
 Оптимальная для биосистем значение силы поверхностного натяжения Ø водные растворы являются средством передвижения веществ в организме, которое определяется силами межмолекулярного сцепления.
Оптимальная для биосистем значение силы поверхностного натяжения Ø водные растворы являются средством передвижения веществ в организме, которое определяется силами межмолекулярного сцепления.
 Расширение при замерзании Ø лед легче воды, он образуется на поверхности водоемов и выполняет функцию теплоизоляции – защищает от холода находящиеся в воде организмы
Расширение при замерзании Ø лед легче воды, он образуется на поверхности водоемов и выполняет функцию теплоизоляции – защищает от холода находящиеся в воде организмы
 Функции воды Универсальный растворитель Ø Выполняет функцию терморегуляции в живых организмах Ø Обеспечивает гидролиз, окисление высокомолекулярных орг. соединений (белков, углеводов, жиров) Ø Является осморегулятором Ø Обеспечивает перенос и выделение определённых веществ из клетки в клетку Ø
Функции воды Универсальный растворитель Ø Выполняет функцию терморегуляции в живых организмах Ø Обеспечивает гидролиз, окисление высокомолекулярных орг. соединений (белков, углеводов, жиров) Ø Является осморегулятором Ø Обеспечивает перенос и выделение определённых веществ из клетки в клетку Ø
 Минеральные вещества. Ø Макроэлементы. Ø Микроэлементы. Ø Ультрамикроэлементы. Ø Функции. Ø Минеральные соли Ø Задания
Минеральные вещества. Ø Макроэлементы. Ø Микроэлементы. Ø Ультрамикроэлементы. Ø Функции. Ø Минеральные соли Ø Задания
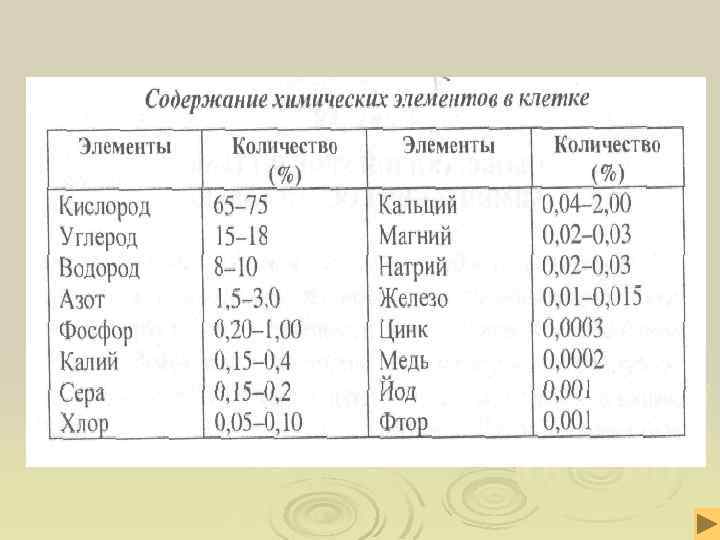
 Макроэлементы. Ø Кислород – 65 -75 %, Ø Углерод - 15 -18 %, Ø Водород - 8 -10 %, Ø Азот - 1, 5 -3 % Ø Фосфор – 0, 2 -1 % Ø Сера – 0, 15 -0, 2% Ø Хлор – 0, 05%-0, 1% Ø Калий – 0, 15 -0, 4 %, Ø Кальций -0, 04 – 2 % 98 % магний – 0, 02 - 0, 03% железо – 0, 01 -0, 015% натрий – 0, 02 -0, 03 %
Макроэлементы. Ø Кислород – 65 -75 %, Ø Углерод - 15 -18 %, Ø Водород - 8 -10 %, Ø Азот - 1, 5 -3 % Ø Фосфор – 0, 2 -1 % Ø Сера – 0, 15 -0, 2% Ø Хлор – 0, 05%-0, 1% Ø Калий – 0, 15 -0, 4 %, Ø Кальций -0, 04 – 2 % 98 % магний – 0, 02 - 0, 03% железо – 0, 01 -0, 015% натрий – 0, 02 -0, 03 %
 Биогенные элементы Ø Азот Ø Водород Ø Кислород Ø Углерод Ø Сера Ø Фосфор.
Биогенные элементы Ø Азот Ø Водород Ø Кислород Ø Углерод Ø Сера Ø Фосфор.
 Микроэлементы. Ø Медь Ø Цинк Ø Кобальт Ø Марганец Ø Йод Ø Фтор Ø Никель и др. от 0, 001 до 0, 000001 %
Микроэлементы. Ø Медь Ø Цинк Ø Кобальт Ø Марганец Ø Йод Ø Фтор Ø Никель и др. от 0, 001 до 0, 000001 %
 Ультрамикроэлементы. Ø Бор Ø Бром Ø Серебро Ø Золото Ø Селен Ø Мышьяк и др. Менее 0, 000001 %
Ультрамикроэлементы. Ø Бор Ø Бром Ø Серебро Ø Золото Ø Селен Ø Мышьяк и др. Менее 0, 000001 %
 Особенности строения минеральных солей Ø а)в диссоциированном состоянии в виде катионов: К+, Na+, Ca++, Mg++ в виде анионов: H 2 PO 4 -, Cl-, HCO 3 -, HPO 4 -Ø б) в связанном с органическими веществами состоянии обеспечивают многие функции
Особенности строения минеральных солей Ø а)в диссоциированном состоянии в виде катионов: К+, Na+, Ca++, Mg++ в виде анионов: H 2 PO 4 -, Cl-, HCO 3 -, HPO 4 -Ø б) в связанном с органическими веществами состоянии обеспечивают многие функции
 Функции минеральных солей Ø Ø Ø Ø Влияют на: Кислотно –щелочное равновесие(буферность) в организме Осмотическое давление, поступление воды в клетку. В связанном с органическими веществами состоянии обеспечивают многие функции: Железо участвует в построении молекулы гемоглобина; Магний входит в состав хлорофилла; Медь входит в состав многих окислительных ферментов; Йод содержится в составе молекул тироксина; Натрий и калий обеспечивают электрический заряд на мембранах нервных волокон; Кобальт входит в состав витамина В 12 и т. д.
Функции минеральных солей Ø Ø Ø Ø Влияют на: Кислотно –щелочное равновесие(буферность) в организме Осмотическое давление, поступление воды в клетку. В связанном с органическими веществами состоянии обеспечивают многие функции: Железо участвует в построении молекулы гемоглобина; Магний входит в состав хлорофилла; Медь входит в состав многих окислительных ферментов; Йод содержится в составе молекул тироксина; Натрий и калий обеспечивают электрический заряд на мембранах нервных волокон; Кобальт входит в состав витамина В 12 и т. д.
 Органические соединения. Ø Углеводы - 0, 2 -2, 0 % сух. вещ. кл. Ø Белки - 10 -20% сух. вещ. кл. Ø Жиры – 1 -5 % сух. вещ. кл. Ø Нуклеиновые кислоты – 1 -2 % Ø АТФ Ø Ферменты. Ø Алкалоиды Ø Низкомолекулярные органические вещества ( НМВ) - 0, 1 -0, 5 % Ø Тест.
Органические соединения. Ø Углеводы - 0, 2 -2, 0 % сух. вещ. кл. Ø Белки - 10 -20% сух. вещ. кл. Ø Жиры – 1 -5 % сух. вещ. кл. Ø Нуклеиновые кислоты – 1 -2 % Ø АТФ Ø Ферменты. Ø Алкалоиды Ø Низкомолекулярные органические вещества ( НМВ) - 0, 1 -0, 5 % Ø Тест.
 Углеводы органические вещества, состоящие из атомов углерода, водорода и кислорода (водород и кислород находятся в них, как правило, в таком же соотношении, как и в молекуле воды) С n( н 2 о)m Ø Виды углеводов Ø Сравнение классов углеводов Ø Функции Ø Задания
Углеводы органические вещества, состоящие из атомов углерода, водорода и кислорода (водород и кислород находятся в них, как правило, в таком же соотношении, как и в молекуле воды) С n( н 2 о)m Ø Виды углеводов Ø Сравнение классов углеводов Ø Функции Ø Задания
 Углеводы моносахариды Дисахаридыолигосахариды Триозы Ø Ø Тетрозы Ø (С 4 Н 8 О 4) Ø Ø Пентозы (С 5 Н 10 О 5) Ø Гексозы (С 6 Н 12 О 6) Ø Сахароза Мальтоза Лактоза полисахариды Ø Крахмал Гликоген Декстрины Целлюлоза Хитин Ø Муреин… Ø Ø
Углеводы моносахариды Дисахаридыолигосахариды Триозы Ø Ø Тетрозы Ø (С 4 Н 8 О 4) Ø Ø Пентозы (С 5 Н 10 О 5) Ø Гексозы (С 6 Н 12 О 6) Ø Сахароза Мальтоза Лактоза полисахариды Ø Крахмал Гликоген Декстрины Целлюлоза Хитин Ø Муреин… Ø Ø
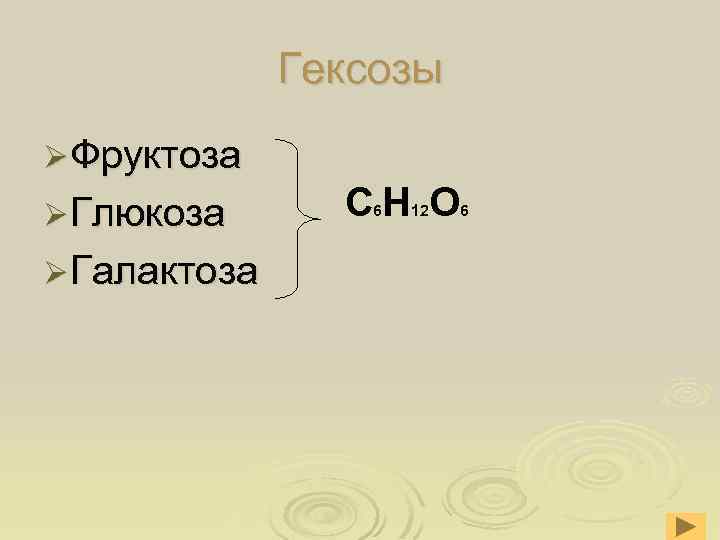 Гексозы Ø Фруктоза Ø Глюкоза Ø Галактоза СН О 6 12 6
Гексозы Ø Фруктоза Ø Глюкоза Ø Галактоза СН О 6 12 6
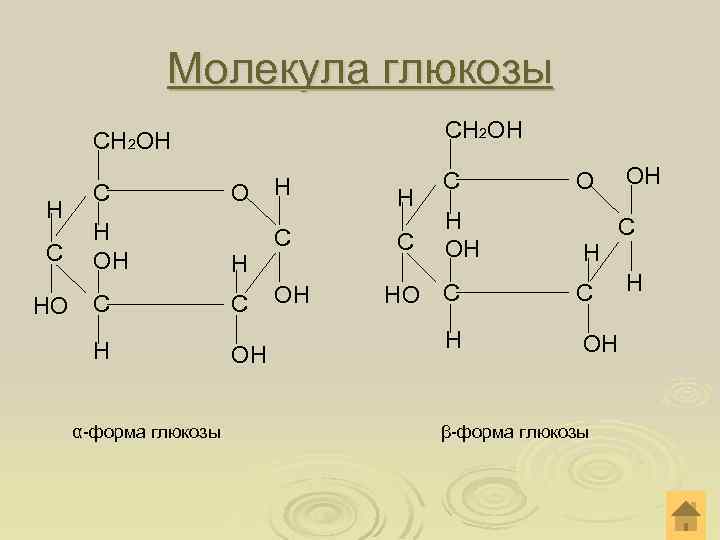 Молекула глюкозы СН 2 ОН Н С НО С Н ОН О Н С С Н ОН α-форма глюкозы Н С ОН Н С С Н ОН НО С Н ОН О Н С С ОН β-форма глюкозы Н
Молекула глюкозы СН 2 ОН Н С НО С Н ОН О Н С С Н ОН α-форма глюкозы Н С ОН Н С С Н ОН НО С Н ОН О Н С С ОН β-форма глюкозы Н
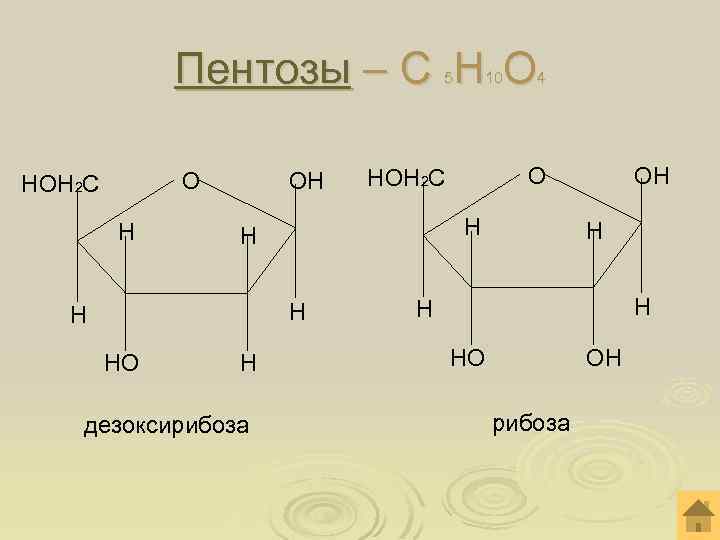 Пентозы – С Н О 5 О НОН 2 С Н ОН Н Н НО Н дезоксирибоза 4 О НОН 2 С Н Н 10 ОН Н НО ОН рибоза
Пентозы – С Н О 5 О НОН 2 С Н ОН Н Н НО Н дезоксирибоза 4 О НОН 2 С Н Н 10 ОН Н НО ОН рибоза
 Олигосахариды Сложные углеводы, содержащие от 2 до 10 моносахаридных остатков. Мальтоза. Солодовый сахар. Состоит из двух молекул глюкозы. Сахароза. Свекловичный сахар. Состоит из глюкозы и фруктозы Лактоза. Молочный сахар. Состоит из глюкозы и галактозы
Олигосахариды Сложные углеводы, содержащие от 2 до 10 моносахаридных остатков. Мальтоза. Солодовый сахар. Состоит из двух молекул глюкозы. Сахароза. Свекловичный сахар. Состоит из глюкозы и фруктозы Лактоза. Молочный сахар. Состоит из глюкозы и галактозы
 Гликоген (С Н О ) 6 10 5 n
Гликоген (С Н О ) 6 10 5 n
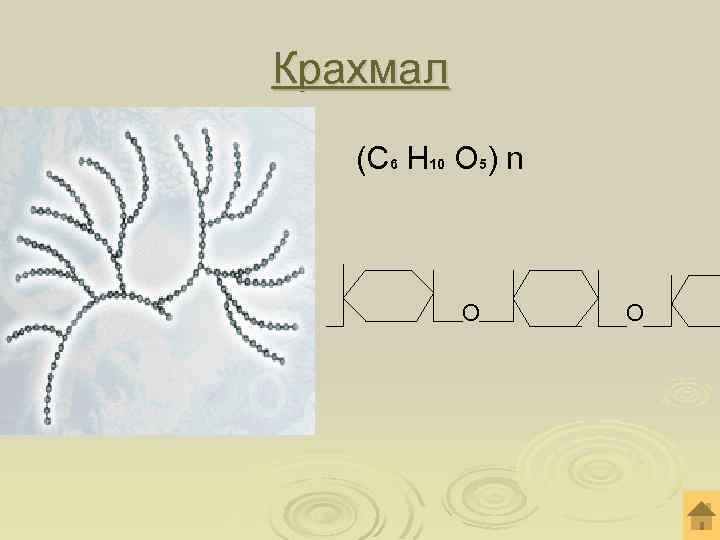 Крахмал (С 6 Н 10 О 5) n О О
Крахмал (С 6 Н 10 О 5) n О О
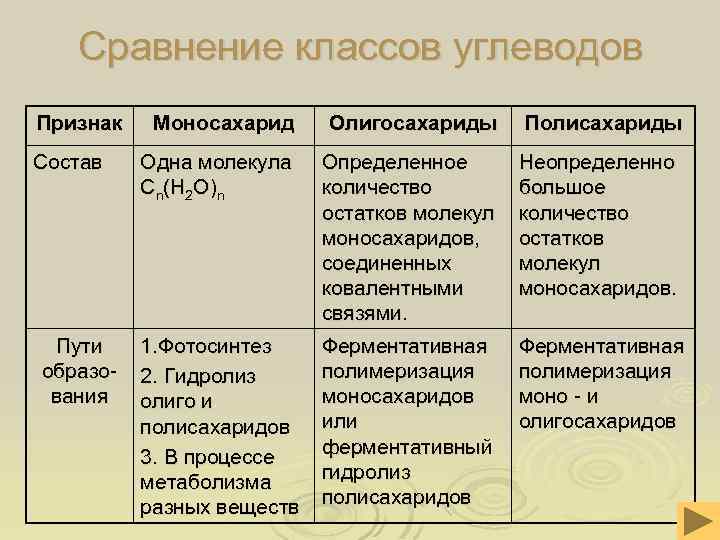 Сравнение классов углеводов Признак Состав Пути образования Моносахарид Олигосахариды Полисахариды Одна молекула Сn(H 2 O)n Определенное количество остатков молекул моносахаридов, соединенных ковалентными связями. Неопределенно большое количество остатков молекул моносахаридов. 1. Фотосинтез 2. Гидролиз олиго и полисахаридов 3. В процессе метаболизма разных веществ Ферментативная полимеризация моносахаридов или ферментативный гидролиз полисахаридов Ферментативная полимеризация моно - и олигосахаридов
Сравнение классов углеводов Признак Состав Пути образования Моносахарид Олигосахариды Полисахариды Одна молекула Сn(H 2 O)n Определенное количество остатков молекул моносахаридов, соединенных ковалентными связями. Неопределенно большое количество остатков молекул моносахаридов. 1. Фотосинтез 2. Гидролиз олиго и полисахаридов 3. В процессе метаболизма разных веществ Ферментативная полимеризация моносахаридов или ферментативный гидролиз полисахаридов Ферментативная полимеризация моно - и олигосахаридов
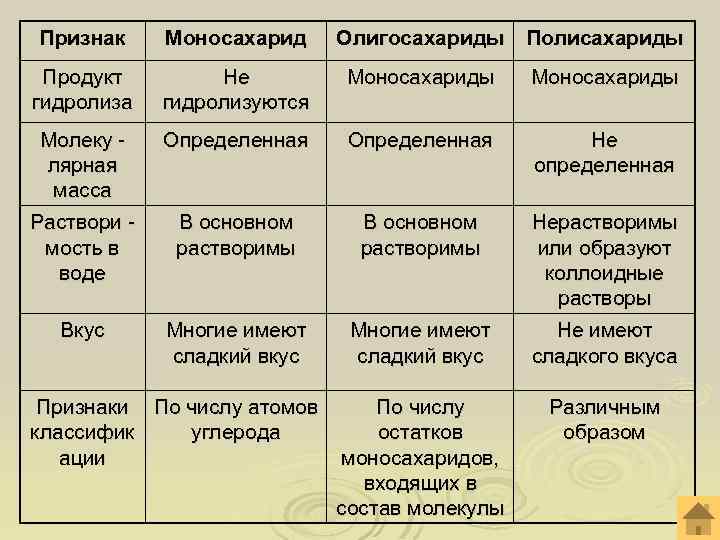 Признак Моносахарид Продукт гидролиза Не гидролизуются Моносахариды Молеку лярная масса Определенная Не определенная Раствори мость в воде В основном растворимы Нерастворимы или образуют коллоидные растворы Вкус Многие имеют сладкий вкус Не имеют сладкого вкуса По числу остатков моносахаридов, входящих в состав молекулы Различным образом Признаки По числу атомов классифик углерода ации Олигосахариды Полисахариды
Признак Моносахарид Продукт гидролиза Не гидролизуются Моносахариды Молеку лярная масса Определенная Не определенная Раствори мость в воде В основном растворимы Нерастворимы или образуют коллоидные растворы Вкус Многие имеют сладкий вкус Не имеют сладкого вкуса По числу остатков моносахаридов, входящих в состав молекулы Различным образом Признаки По числу атомов классифик углерода ации Олигосахариды Полисахариды
 Функции углеводов Ø Энергетическая. Окисление 1 г. = 17, 6 к. Дж. Ø Структурная. Целлюлоза образует стенки растительных клеток, хитин- скелет членистоногих, муреин – стенки клеток бактерии. Ø Запасающая. Гликоген резервный полисахарид у человека, грибов. Крахмал – у растений. Ø Защитная. Моносахара входят в состав витаминов, нуклеиновых кислот, ферментов. Ø Метаболическая. Глюкоза, крахмал, гликоген участвуют в процессах метаболизма клетки.
Функции углеводов Ø Энергетическая. Окисление 1 г. = 17, 6 к. Дж. Ø Структурная. Целлюлоза образует стенки растительных клеток, хитин- скелет членистоногих, муреин – стенки клеток бактерии. Ø Запасающая. Гликоген резервный полисахарид у человека, грибов. Крахмал – у растений. Ø Защитная. Моносахара входят в состав витаминов, нуклеиновых кислот, ферментов. Ø Метаболическая. Глюкоза, крахмал, гликоген участвуют в процессах метаболизма клетки.
 Жиры R CООН Ø Химическое строение Ø Классификация липидов Ø Функции Ø Задания
Жиры R CООН Ø Химическое строение Ø Классификация липидов Ø Функции Ø Задания
 Химическое строение жиров Трёхатомный спирт (глицерин) ВЖК
Химическое строение жиров Трёхатомный спирт (глицерин) ВЖК
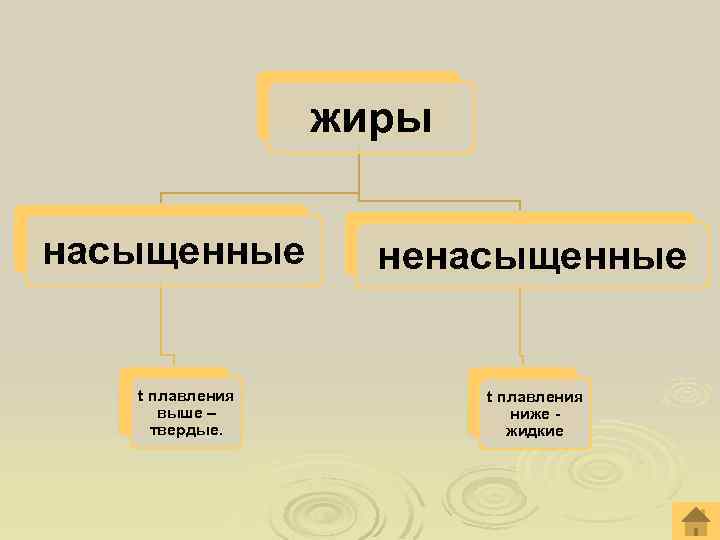 жиры насыщенные t плавления выше – твердые. ненасыщенные t плавления ниже жидкие
жиры насыщенные t плавления выше – твердые. ненасыщенные t плавления ниже жидкие
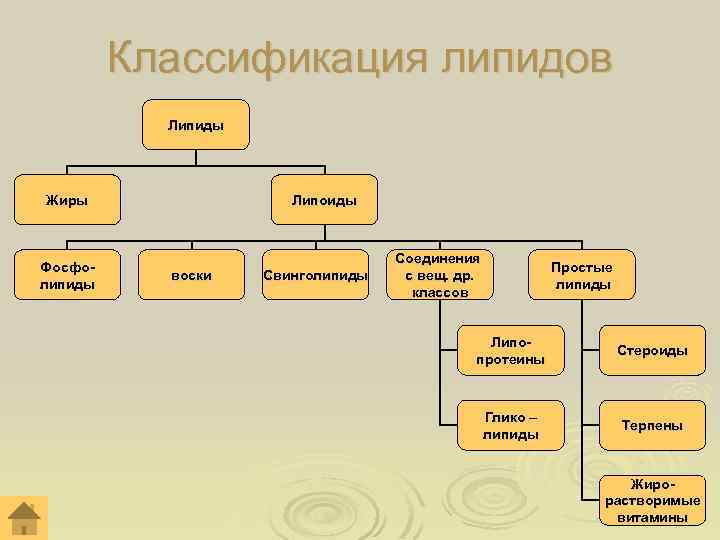 Классификация липидов Липиды Жиры Фосфолипиды Липоиды воски Свинголипиды Соединения с вещ. др. классов Простые липиды Липопротеины Стероиды Глико – липиды Терпены Жирорастворимые витамины
Классификация липидов Липиды Жиры Фосфолипиды Липоиды воски Свинголипиды Соединения с вещ. др. классов Простые липиды Липопротеины Стероиды Глико – липиды Терпены Жирорастворимые витамины
 Функции жиров Ø Энергетическая. 1 г. даёт 38, 9 к. Дж Ø Резервная - источник метаболической воды (1 г жира даёт 105 г воды) Ø Строительная Ø Регуляторная Ø Защитная
Функции жиров Ø Энергетическая. 1 г. даёт 38, 9 к. Дж Ø Резервная - источник метаболической воды (1 г жира даёт 105 г воды) Ø Строительная Ø Регуляторная Ø Защитная
 Проверочный тест. В каких клетках содержится больше углеводов? а)в растительных; б) в животных; г) одинаково. 2. Какими свойствами обладают полисахариды? а) хорошо растворимы в воде, сладкие на вкус; б) плохо растворимы в воде, сладкие на вкус; в) теряют сладкий вкус и способность растворяться в воде. 3. Основные биологические функции углеводов: а) защитная; б) энергетическая и строительная; в) энергетическая и защитная. 4. Какое свойство липидов лежит в основе энергетической функции? а) гидрофобность; б) плохая теплопроводность; в)окисление жиров. 5. Как точно можно узнать глюкозу и крахмал? а) по запаху; б) по растворимости в воде; в) по цвету. 1.
Проверочный тест. В каких клетках содержится больше углеводов? а)в растительных; б) в животных; г) одинаково. 2. Какими свойствами обладают полисахариды? а) хорошо растворимы в воде, сладкие на вкус; б) плохо растворимы в воде, сладкие на вкус; в) теряют сладкий вкус и способность растворяться в воде. 3. Основные биологические функции углеводов: а) защитная; б) энергетическая и строительная; в) энергетическая и защитная. 4. Какое свойство липидов лежит в основе энергетической функции? а) гидрофобность; б) плохая теплопроводность; в)окисление жиров. 5. Как точно можно узнать глюкозу и крахмал? а) по запаху; б) по растворимости в воде; в) по цвету. 1.
 Ø Жизнь – есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой… причем при прекращении обмена веществ прекращается и сама жизнь, что приводит к разложению белка…» Ф. Энгельс.
Ø Жизнь – есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой… причем при прекращении обмена веществ прекращается и сама жизнь, что приводит к разложению белка…» Ф. Энгельс.
 Белки Азотсодержащие орг. соединения, состоящие из аминокислот, соединённых с помощью пептидных связей и имеющие сложную структурную организацию. Ø Химический состав Ø Строение Ø Свойства белков Ø Функции
Белки Азотсодержащие орг. соединения, состоящие из аминокислот, соединённых с помощью пептидных связей и имеющие сложную структурную организацию. Ø Химический состав Ø Строение Ø Свойства белков Ø Функции
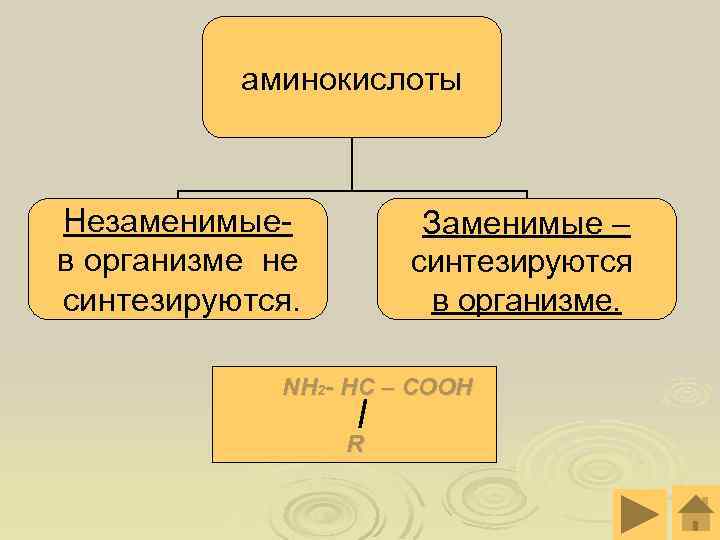 аминокислоты Незаменимыев организме не синтезируются. Заменимые – синтезируются в организме. NH 2 - HC – COOH R
аминокислоты Незаменимыев организме не синтезируются. Заменимые – синтезируются в организме. NH 2 - HC – COOH R
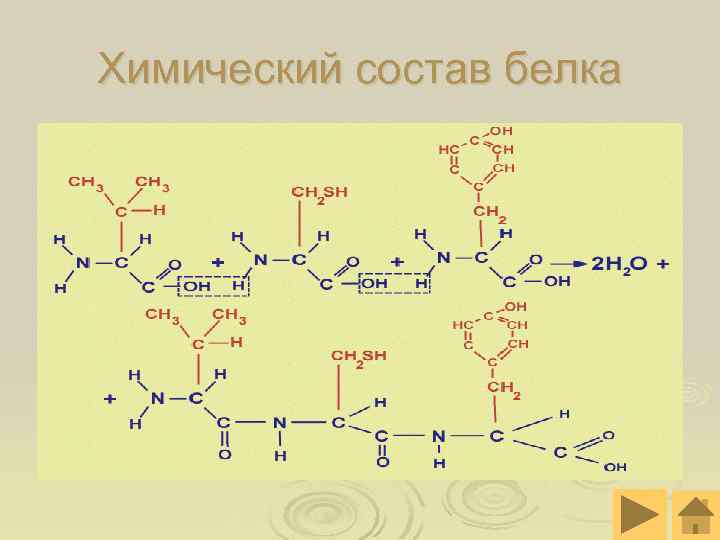 Химический состав белка
Химический состав белка
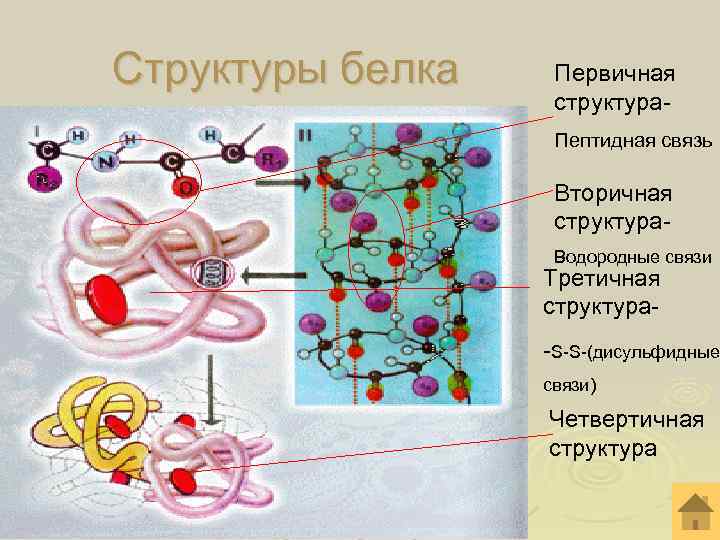 Структуры белка Первичная структура. Пептидная связь Вторичная структура. Водородные связи Третичная структура- -S-S-(дисульфидные связи) Четвертичная структура
Структуры белка Первичная структура. Пептидная связь Вторичная структура. Водородные связи Третичная структура- -S-S-(дисульфидные связи) Четвертичная структура
 Свойства белков: Ø Денатурация. Ø Ренатурация. Ø Видовая специфичность. Ø Белковая индивидуальность организма.
Свойства белков: Ø Денатурация. Ø Ренатурация. Ø Видовая специфичность. Ø Белковая индивидуальность организма.
 Денатурация белка
Денатурация белка
 Функции белков Защитная (антитела, глобулины) Ø Строительная. Входят в состав всех клеточных мембран. Ø Транспортная (гемоглобин). Ø Каталитическая (ферменты). Ø Двигательная (коллаген, актин, миозин). Ø Регуляторная ( инсулин, гормон роста). Ø Запасная или питательная ( казеин, альбумин, ). Ø Энергетическая ( источник энергии = 17, 6 кдж. Ø Токсическая ( яд змей, грибов, насекомых, ). Ø Сигнальная (молекулы белков, встроенных в мембрану). Ø
Функции белков Защитная (антитела, глобулины) Ø Строительная. Входят в состав всех клеточных мембран. Ø Транспортная (гемоглобин). Ø Каталитическая (ферменты). Ø Двигательная (коллаген, актин, миозин). Ø Регуляторная ( инсулин, гормон роста). Ø Запасная или питательная ( казеин, альбумин, ). Ø Энергетическая ( источник энергии = 17, 6 кдж. Ø Токсическая ( яд змей, грибов, насекомых, ). Ø Сигнальная (молекулы белков, встроенных в мембрану). Ø
 Нуклеиновые кислоты от латинского "nucleus" - ядро природные высокомолекулярные соединения, обеспечивающие хранение и передачу наследственной (генетической) информации в живых организмах. Нуклеиновые кислоты ДНК РНК
Нуклеиновые кислоты от латинского "nucleus" - ядро природные высокомолекулярные соединения, обеспечивающие хранение и передачу наследственной (генетической) информации в живых организмах. Нуклеиновые кислоты ДНК РНК
 Молекула ДНК
Молекула ДНК
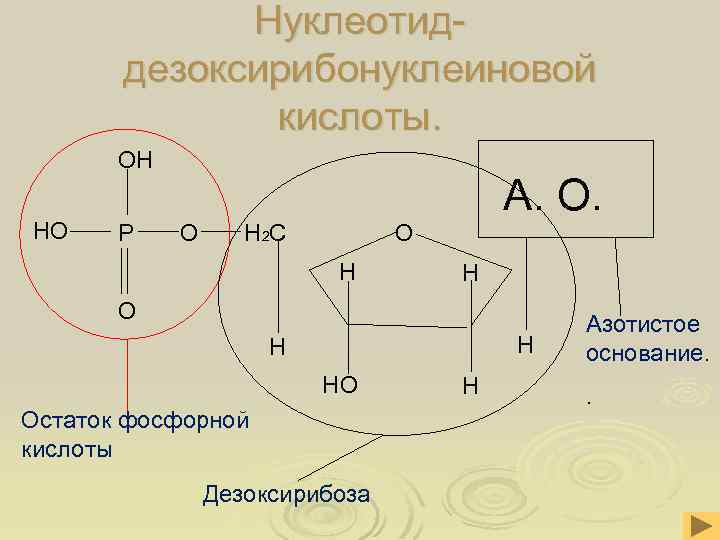 Нуклеотиддезоксирибонуклеиновой кислоты. ОН НО Р О А. О. О Н 2 С Н Н О Н Н НО Остаток фосфорной кислоты Дезоксирибоза Н Азотистое основание. .
Нуклеотиддезоксирибонуклеиновой кислоты. ОН НО Р О А. О. О Н 2 С Н Н О Н Н НО Остаток фосфорной кислоты Дезоксирибоза Н Азотистое основание. .
 Комплементарность
Комплементарность
 Репликация 2 ДНК 3 1
Репликация 2 ДНК 3 1
 Рибонуклеиновая кислота. Нуклеотид. ОН НО Р А. О. О Н 2 С О Н Н НО Остаток фосфорной кислоты Рибоза ОН Азотистое основание
Рибонуклеиновая кислота. Нуклеотид. ОН НО Р А. О. О Н 2 С О Н Н НО Остаток фосфорной кислоты Рибоза ОН Азотистое основание
 Виды РНК. Рибосомная РНК ( р. РНК) –в комплексе с белками образует рибосомы, на которых происходит синтез белка. Ø Информационная ( матричная) ( и. РНК) – программирует синтез белков в клетке. Она осуществляет передачу кода ДНК к месту синтеза белка. Ø Транспортная РНК ( т. РНК) – доставляет аминокислоты к месту синтеза белка и определяет точную ориентацию аминокислоты в рибосоме. Ø
Виды РНК. Рибосомная РНК ( р. РНК) –в комплексе с белками образует рибосомы, на которых происходит синтез белка. Ø Информационная ( матричная) ( и. РНК) – программирует синтез белков в клетке. Она осуществляет передачу кода ДНК к месту синтеза белка. Ø Транспортная РНК ( т. РНК) – доставляет аминокислоты к месту синтеза белка и определяет точную ориентацию аминокислоты в рибосоме. Ø
 Молекула т-РНК 1 петля - акцепторная. Присоединяются аминокислоты. 2 петля- антикодоновая. В процессе трансляции узнает кодон в и. РНК. 3 и 4 петли – боковые.
Молекула т-РНК 1 петля - акцепторная. Присоединяются аминокислоты. 2 петля- антикодоновая. В процессе трансляции узнает кодон в и. РНК. 3 и 4 петли – боковые.
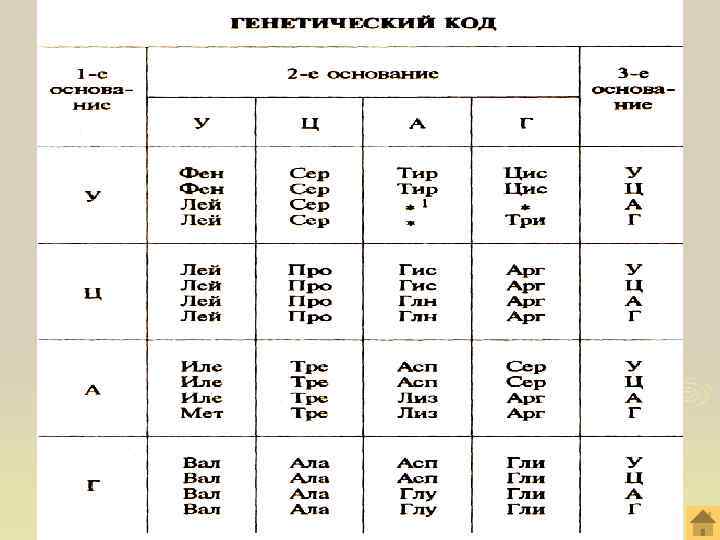
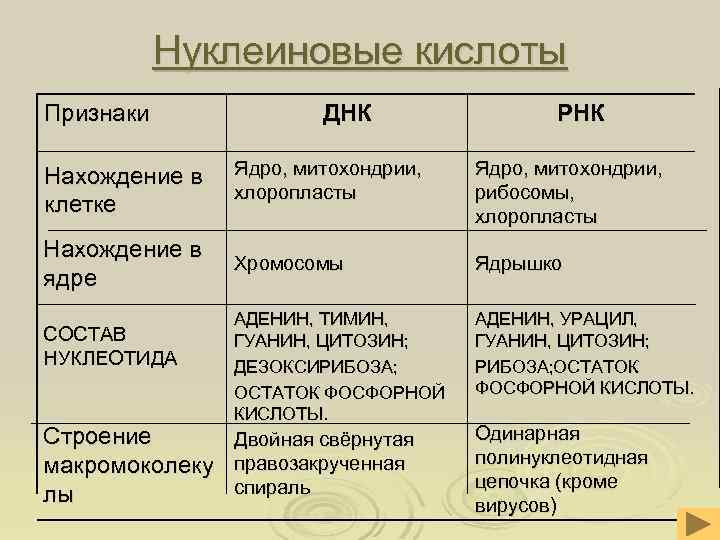 Нуклеиновые кислоты Признаки ДНК РНК Нахождение в клетке Ядро, митохондрии, хлоропласты Ядро, митохондрии, рибосомы, хлоропласты Нахождение в ядре Хромосомы Ядрышко АДЕНИН, ТИМИН, ГУАНИН, ЦИТОЗИН; ДЕЗОКСИРИБОЗА; ОСТАТОК ФОСФОРНОЙ КИСЛОТЫ. АДЕНИН, УРАЦИЛ, ГУАНИН, ЦИТОЗИН; РИБОЗА; ОСТАТОК ФОСФОРНОЙ КИСЛОТЫ. СОСТАВ НУКЛЕОТИДА Строение Двойная свёрнутая макромоколеку правозакрученная спираль лы Одинарная полинуклеотидная цепочка (кроме вирусов)
Нуклеиновые кислоты Признаки ДНК РНК Нахождение в клетке Ядро, митохондрии, хлоропласты Ядро, митохондрии, рибосомы, хлоропласты Нахождение в ядре Хромосомы Ядрышко АДЕНИН, ТИМИН, ГУАНИН, ЦИТОЗИН; ДЕЗОКСИРИБОЗА; ОСТАТОК ФОСФОРНОЙ КИСЛОТЫ. АДЕНИН, УРАЦИЛ, ГУАНИН, ЦИТОЗИН; РИБОЗА; ОСТАТОК ФОСФОРНОЙ КИСЛОТЫ. СОСТАВ НУКЛЕОТИДА Строение Двойная свёрнутая макромоколеку правозакрученная спираль лы Одинарная полинуклеотидная цепочка (кроме вирусов)
 свойства Способна к самоудвоению по принципу комплементарности: А-Т; Т-А; Г-Ц; Ц-Г. Стабильна. Не способна к самоудвоению. Лабильна. функции Химическая основа гена. Хранение и передача наследственной информации о структуре белков. и. РНК(м. РНК)определяет порядок расположения аминокислоты в белке; т. РНК –подносит аминокислоты к месту синтеза белка – рибосомам; р. РНК- определяет структуру рибосом.
свойства Способна к самоудвоению по принципу комплементарности: А-Т; Т-А; Г-Ц; Ц-Г. Стабильна. Не способна к самоудвоению. Лабильна. функции Химическая основа гена. Хранение и передача наследственной информации о структуре белков. и. РНК(м. РНК)определяет порядок расположения аминокислоты в белке; т. РНК –подносит аминокислоты к месту синтеза белка – рибосомам; р. РНК- определяет структуру рибосом.
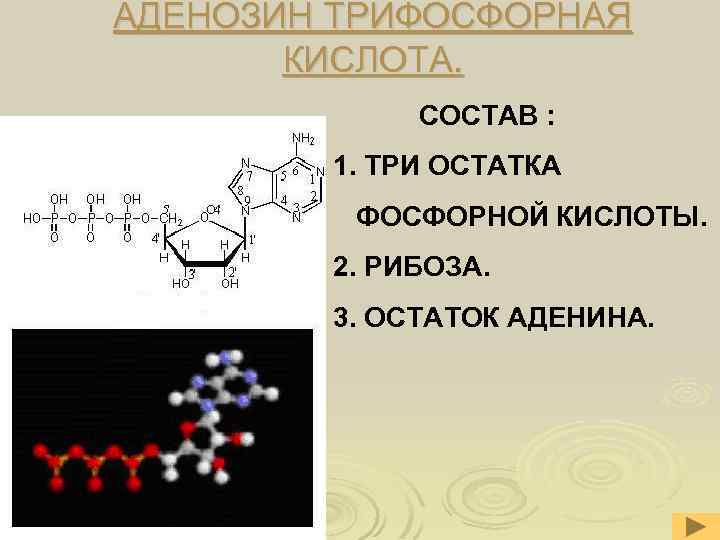 АДЕНОЗИН ТРИФОСФОРНАЯ КИСЛОТА. СОСТАВ : 1. ТРИ ОСТАТКА ФОСФОРНОЙ КИСЛОТЫ. 2. РИБОЗА. 3. ОСТАТОК АДЕНИНА.
АДЕНОЗИН ТРИФОСФОРНАЯ КИСЛОТА. СОСТАВ : 1. ТРИ ОСТАТКА ФОСФОРНОЙ КИСЛОТЫ. 2. РИБОЗА. 3. ОСТАТОК АДЕНИНА.
 ФУНКЦИЯ: l l АТФ играет центральную роль в энергетическом обмене клетки. Является непосредственным источником энергообеспечения любой клеточной функции.
ФУНКЦИЯ: l l АТФ играет центральную роль в энергетическом обмене клетки. Является непосредственным источником энергообеспечения любой клеточной функции.
 Ферменты – биологические катализаторы. ферменты Однокомпонентные (состоят только из белка) двукомпонентные (из белка и небелкового компонента) металл органического витамина
Ферменты – биологические катализаторы. ферменты Однокомпонентные (состоят только из белка) двукомпонентные (из белка и небелкового компонента) металл органического витамина
 Особенности ферментов. высокоспецифичны, связываются только со своими субстратами. Ø Форма и химическое строение активного центра таковы, что с ним могут связываться только определенные субстраты. Ø Активность фермента зависит от различных факторов: р. Н раствора, температуры. Ø
Особенности ферментов. высокоспецифичны, связываются только со своими субстратами. Ø Форма и химическое строение активного центра таковы, что с ним могут связываться только определенные субстраты. Ø Активность фермента зависит от различных факторов: р. Н раствора, температуры. Ø
 Значение ферментов. 1. Используют в медицине для обработки ран, при лечении болезни глаз, кожных заболевании, ожогов, в урологии, при истощении, ожирении; 2. При производстве антибиотиков, виноделии, хлебопечении, синтезе витаминов.
Значение ферментов. 1. Используют в медицине для обработки ран, при лечении болезни глаз, кожных заболевании, ожогов, в урологии, при истощении, ожирении; 2. При производстве антибиотиков, виноделии, хлебопечении, синтезе витаминов.


