ХИМИЧЕСКИЕ ЗНАКИ, ФОРМУЛЫ И УРАВНЕНИЯ Для












ЛЕК. 01 Химич.знаки,формулы, уравнения.ppt
- Количество слайдов: 15
 ХИМИЧЕСКИЕ ЗНАКИ, ФОРМУЛЫ И УРАВНЕНИЯ Для обозначения элементов используют химические знаки, которые состоят из первой или первой и одной из последующих букв латинских названий элементов: алюминий – Aluminium …. Al железо – Ferrum …………. . Fe водород – Hydrogenium …. H кислород – Oxygenium ……O и т. д. ЧТО ОБОЗНАЧАЕТ ХИМИЧЕСКИЙ ЗНАК?
ХИМИЧЕСКИЕ ЗНАКИ, ФОРМУЛЫ И УРАВНЕНИЯ Для обозначения элементов используют химические знаки, которые состоят из первой или первой и одной из последующих букв латинских названий элементов: алюминий – Aluminium …. Al железо – Ferrum …………. . Fe водород – Hydrogenium …. H кислород – Oxygenium ……O и т. д. ЧТО ОБОЗНАЧАЕТ ХИМИЧЕСКИЙ ЗНАК?
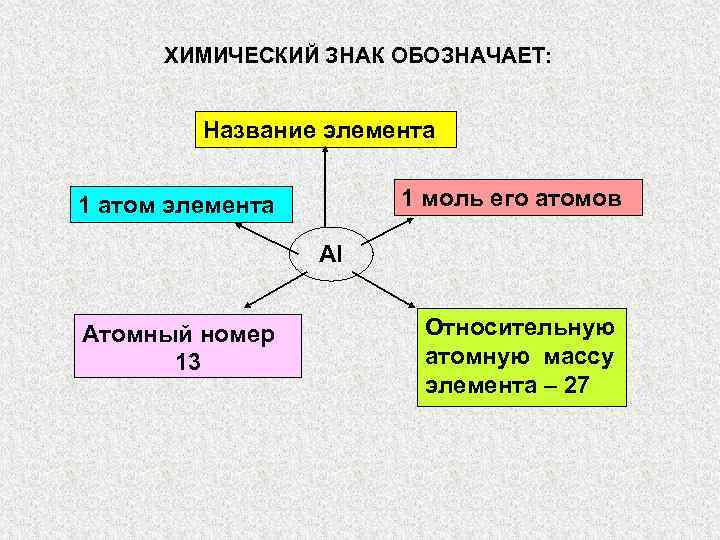
 ХИМИЧЕСКИЙ ЗНАК ОБОЗНАЧАЕТ: Название элемента 1 атом элемента 1 моль его атомов Al Атомный номер Относительную 13 атомную массу элемента – 27
ХИМИЧЕСКИЙ ЗНАК ОБОЗНАЧАЕТ: Название элемента 1 атом элемента 1 моль его атомов Al Атомный номер Относительную 13 атомную массу элемента – 27
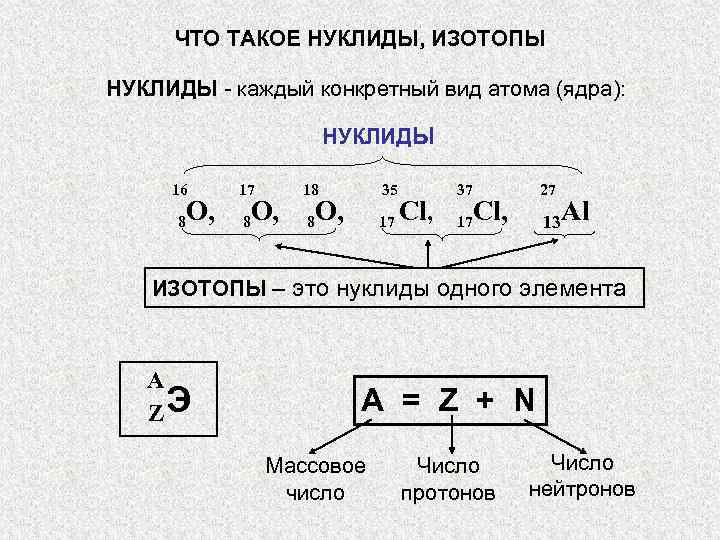
 ЧТО ТАКОЕ НУКЛИДЫ, ИЗОТОПЫ НУКЛИДЫ - каждый конкретный вид атома (ядра): НУКЛИДЫ 16 17 18 35 37 27 O, 8 8 O, O, 8 17 Cl, 17 13 Al ИЗОТОПЫ – это нуклиды одного элемента A ZЭ A = Z + N Массовое Число число протонов нейтронов
ЧТО ТАКОЕ НУКЛИДЫ, ИЗОТОПЫ НУКЛИДЫ - каждый конкретный вид атома (ядра): НУКЛИДЫ 16 17 18 35 37 27 O, 8 8 O, O, 8 17 Cl, 17 13 Al ИЗОТОПЫ – это нуклиды одного элемента A ZЭ A = Z + N Массовое Число число протонов нейтронов
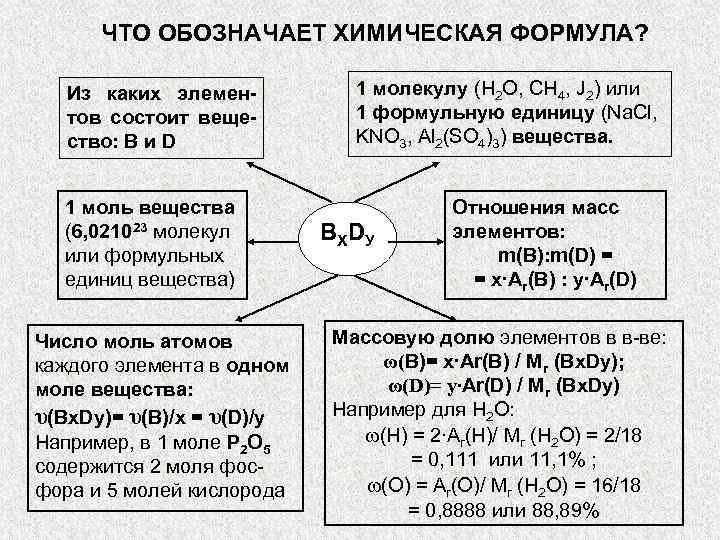
 ЧТО ОБОЗНАЧАЕТ ХИМИЧЕСКАЯ ФОРМУЛА? Из каких элемен- 1 молекулу (Н 2 О, СН 4, J 2) или тов состоит веще- 1 формульную единицу (Na. Cl, ство: В и D KNO 3, Al 2(SO 4)3) вещества. 1 моль вещества Отношения масс (6, 021023 молекул ВХ DУ элементов: или формульных m(B): m(D) = единиц вещества) = х∙Аr(B) : y∙Аr(D) Число моль атомов Массовую долю элементов в в-ве: каждого элемента в одном ω(В)= х∙Аr(B) / Mr (Bx. Dy); моле вещества: ω(D)= y∙Аr(D) / Mr (Bx. Dy) υ(Bx. Dy)= υ(B)/x = υ(D)/y Например для Н 2 О: Например, в 1 моле Р 2 О 5 ω(Н) = 2∙Аr(Н)/ Mr (Н 2 О) = 2/18 содержится 2 моля фос- = 0, 111 или 11, 1% ; фора и 5 молей кислорода ω(О) = Аr(О)/ Mr (Н 2 О) = 16/18 = 0, 8888 или 88, 89%
ЧТО ОБОЗНАЧАЕТ ХИМИЧЕСКАЯ ФОРМУЛА? Из каких элемен- 1 молекулу (Н 2 О, СН 4, J 2) или тов состоит веще- 1 формульную единицу (Na. Cl, ство: В и D KNO 3, Al 2(SO 4)3) вещества. 1 моль вещества Отношения масс (6, 021023 молекул ВХ DУ элементов: или формульных m(B): m(D) = единиц вещества) = х∙Аr(B) : y∙Аr(D) Число моль атомов Массовую долю элементов в в-ве: каждого элемента в одном ω(В)= х∙Аr(B) / Mr (Bx. Dy); моле вещества: ω(D)= y∙Аr(D) / Mr (Bx. Dy) υ(Bx. Dy)= υ(B)/x = υ(D)/y Например для Н 2 О: Например, в 1 моле Р 2 О 5 ω(Н) = 2∙Аr(Н)/ Mr (Н 2 О) = 2/18 содержится 2 моля фос- = 0, 111 или 11, 1% ; фора и 5 молей кислорода ω(О) = Аr(О)/ Mr (Н 2 О) = 16/18 = 0, 8888 или 88, 89%
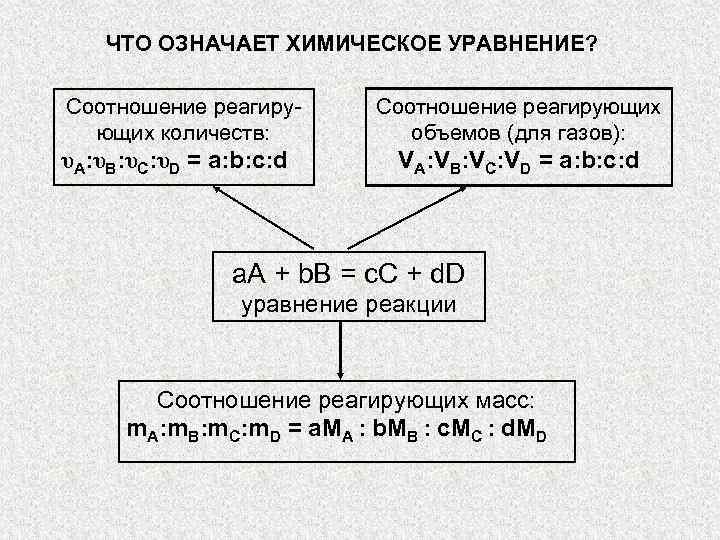
 ЧТО ОЗНАЧАЕТ ХИМИЧЕСКОЕ УРАВНЕНИЕ? Соотношение реагиру- Соотношение реагирующих количеств: объемов (для газов): υA: υB: υC: υD = a: b: c: d VA: VB: VC: VD = a: b: c: d a. А + b. B = c. C + d. D уравнение реакции Соотношение реагирующих масс: m. A: m. B: m. C: m. D = a. MA : b. MB : c. MC : d. MD
ЧТО ОЗНАЧАЕТ ХИМИЧЕСКОЕ УРАВНЕНИЕ? Соотношение реагиру- Соотношение реагирующих количеств: объемов (для газов): υA: υB: υC: υD = a: b: c: d VA: VB: VC: VD = a: b: c: d a. А + b. B = c. C + d. D уравнение реакции Соотношение реагирующих масс: m. A: m. B: m. C: m. D = a. MA : b. MB : c. MC : d. MD
 ПРИМЕР РАССЧЕТА ПО ХИМИЧЕСКОМУ УРАВНЕНИЮ Задача. Какая масса Ba. Cl 2 израсходуется при реакции с 10 г Fe 2(SO 4)3 ? Решение: Согласно уравнению реакции: Fe 2(SO 4)3 + 3 Ba. Cl 2 = 3 Ba. SO 4↓ + 2 Fe. Cl 3 1 моль 3 моля 2 моля отношение реагирующих масс: m(Fe 2(SO 4)3) : m(Ba. Cl 2) = 1 M(Fe 2(SO 4)3) : 3 M(Ba. Cl 2) отсюда находим массу хлорида бария: 3∙ 208, 24∙ 10 3 M(Ba. Cl 2) x m(Fe 2(SO 4)3) m(Ba. Cl 2) = = 15, 62 г 1 M(Fe 2(SO 4)3) 399, 88
ПРИМЕР РАССЧЕТА ПО ХИМИЧЕСКОМУ УРАВНЕНИЮ Задача. Какая масса Ba. Cl 2 израсходуется при реакции с 10 г Fe 2(SO 4)3 ? Решение: Согласно уравнению реакции: Fe 2(SO 4)3 + 3 Ba. Cl 2 = 3 Ba. SO 4↓ + 2 Fe. Cl 3 1 моль 3 моля 2 моля отношение реагирующих масс: m(Fe 2(SO 4)3) : m(Ba. Cl 2) = 1 M(Fe 2(SO 4)3) : 3 M(Ba. Cl 2) отсюда находим массу хлорида бария: 3∙ 208, 24∙ 10 3 M(Ba. Cl 2) x m(Fe 2(SO 4)3) m(Ba. Cl 2) = = 15, 62 г 1 M(Fe 2(SO 4)3) 399, 88
 ГАЗОВЫЕ ЗАКОНЫ Индивидуальное вещество в газообразном состоянии характеризуется следующими величинами: Р – давлением; Т , или t – температурой; V – объемом; m – массой всего газа; М – молярной массой. Взаимосвязь между этими величинами устанавливают газовые законы. При этом обычно используют модель идеального газа , которая основана на следующих допущениях: 1) между частицами газа отсутствуют силы взаимодействия; 2) сами частицы представляют собой материальные точки.
ГАЗОВЫЕ ЗАКОНЫ Индивидуальное вещество в газообразном состоянии характеризуется следующими величинами: Р – давлением; Т , или t – температурой; V – объемом; m – массой всего газа; М – молярной массой. Взаимосвязь между этими величинами устанавливают газовые законы. При этом обычно используют модель идеального газа , которая основана на следующих допущениях: 1) между частицами газа отсутствуют силы взаимодействия; 2) сами частицы представляют собой материальные точки.
 1. ЗАКОН БОЙЛЯ-МАРИОТТА При Т = const (изотермический процесс): PV = const или P 1 V 1 = P 2 V 2 2. ЗАКОН ГЕЙ-ЛЮССАКА При Р = const (изобарический процесс): V/Т = const или V 1/Т 1 = V 2/Т 2 3. ЗАКОН ШАРЛЯ При V = const (изохорический процесс) Р/Т = const или Р 1/Т 1 = Р 2/Т 2
1. ЗАКОН БОЙЛЯ-МАРИОТТА При Т = const (изотермический процесс): PV = const или P 1 V 1 = P 2 V 2 2. ЗАКОН ГЕЙ-ЛЮССАКА При Р = const (изобарический процесс): V/Т = const или V 1/Т 1 = V 2/Т 2 3. ЗАКОН ШАРЛЯ При V = const (изохорический процесс) Р/Т = const или Р 1/Т 1 = Р 2/Т 2
 4. УРАВНЕНИЕ КЛАПЕЙРОНА Объединенный газовый закон P 1 V 1 P 2 V 2 PV = или = const Т 1 Т 2 Т 5. УРАВНЕНИЕ КЛАПЕЙРОНА- МЕНДЕЛЕЕВА PV = n. RT, где n = m/M или PV = m. RT/М , где R = 8, 31 Дж/(моль∙К) = 0, 82 л∙атм/(моль∙К) P – давление, Па; Т – температура, К
4. УРАВНЕНИЕ КЛАПЕЙРОНА Объединенный газовый закон P 1 V 1 P 2 V 2 PV = или = const Т 1 Т 2 Т 5. УРАВНЕНИЕ КЛАПЕЙРОНА- МЕНДЕЛЕЕВА PV = n. RT, где n = m/M или PV = m. RT/М , где R = 8, 31 Дж/(моль∙К) = 0, 82 л∙атм/(моль∙К) P – давление, Па; Т – температура, К
 УРАВНЕНИЕ КЛАПЕЙРОНА- МЕНДЕЛЕЕВА (следствия) Из уравнения Клапейрона-Менделеева следуют два важных результата: Следствие 1. V = n. RT/Р = n∙(RT/Р) Отсюда, при Р = const и Т = const V 1 / n 1 = V 1 / n 1 или V ~ n Следовательно, объём газа прямо пропорционален числу молей (и числу молекул), причем коэффициент пропорциональности ( RT /Р) одинаков для всех газов и зависит только от давления и температуры. Это есть не что иное, как закон Авогадро.
УРАВНЕНИЕ КЛАПЕЙРОНА- МЕНДЕЛЕЕВА (следствия) Из уравнения Клапейрона-Менделеева следуют два важных результата: Следствие 1. V = n. RT/Р = n∙(RT/Р) Отсюда, при Р = const и Т = const V 1 / n 1 = V 1 / n 1 или V ~ n Следовательно, объём газа прямо пропорционален числу молей (и числу молекул), причем коэффициент пропорциональности ( RT /Р) одинаков для всех газов и зависит только от давления и температуры. Это есть не что иное, как закон Авогадро.
 УРАВНЕНИЕ КЛАПЕЙРОНА- МЕНДЕЛЕЕВА (следствия) Следствие 2. плотность газов прямо пропорцио- нальна их молярной массе при заданных давлении и температуре. Из уравнения Клапейрона-Менделеева найдем выражение для плотности (ρ) газа: ρ = m/ V = PМ/RT = М∙ (Р/RT) При постоянных Р и Т получим ρ1 / М 1 = ρ2 / М 2 или ρ~М
УРАВНЕНИЕ КЛАПЕЙРОНА- МЕНДЕЛЕЕВА (следствия) Следствие 2. плотность газов прямо пропорцио- нальна их молярной массе при заданных давлении и температуре. Из уравнения Клапейрона-Менделеева найдем выражение для плотности (ρ) газа: ρ = m/ V = PМ/RT = М∙ (Р/RT) При постоянных Р и Т получим ρ1 / М 1 = ρ2 / М 2 или ρ~М
 ЯДЕРНЫЕ РЕАКЦИИ Превращения атомных ядер обуславливается их взаимодействием с элементарными частицами или друг с другом. При записи уравнений ядерных реакций следует помнить, что Суммы массовых чисел и алгебраические суммы зарядов частиц левой и правой частей равенства должны быть равными, например 27 1 24 13 Al + 1 H = 12 Mg + 2 He или в сокращенной форме записи: 27 Al (p, α) 24 Mg.
ЯДЕРНЫЕ РЕАКЦИИ Превращения атомных ядер обуславливается их взаимодействием с элементарными частицами или друг с другом. При записи уравнений ядерных реакций следует помнить, что Суммы массовых чисел и алгебраические суммы зарядов частиц левой и правой частей равенства должны быть равными, например 27 1 24 13 Al + 1 H = 12 Mg + 2 He или в сокращенной форме записи: 27 Al (p, α) 24 Mg.
 ТИПЫ ЯДЕРНЫХ РЕАКЦИЙ: Альфа-распад (α) 226 222 4 88 Ra = 86 Rn + 2 He Бета-распад (β) 24 11 Na = 12 Mg + e–
ТИПЫ ЯДЕРНЫХ РЕАКЦИЙ: Альфа-распад (α) 226 222 4 88 Ra = 86 Rn + 2 He Бета-распад (β) 24 11 Na = 12 Mg + e–
 ТИПЫ ЯДЕРНЫХ РЕАКЦИЙ: Реакции под действием протонов – (p, n), (p, α) 9 1 4 Be + 1 H = 5 B + 0 n 14 1 12 4 7 N+ 1 H = 6 C + 2 He Реакции под действием α –частиц (α, р), (α, n) 27 4 30 1 13 Al + 2 He = 14 Si + 1 H 9 4 12 1 4 Be + 2 He = 6 C + 0 n
ТИПЫ ЯДЕРНЫХ РЕАКЦИЙ: Реакции под действием протонов – (p, n), (p, α) 9 1 4 Be + 1 H = 5 B + 0 n 14 1 12 4 7 N+ 1 H = 6 C + 2 He Реакции под действием α –частиц (α, р), (α, n) 27 4 30 1 13 Al + 2 He = 14 Si + 1 H 9 4 12 1 4 Be + 2 He = 6 C + 0 n
 ТИПЫ ЯДЕРНЫХ РЕАКЦИЙ: Реакции под действием нейтронов (n, р), (n, α) 14 1 14 1 7 N + 0 n = 6 C + 1 H 59 1 56 4 27 Co + 0 n = 25 Mn + 2 He
ТИПЫ ЯДЕРНЫХ РЕАКЦИЙ: Реакции под действием нейтронов (n, р), (n, α) 14 1 14 1 7 N + 0 n = 6 C + 1 H 59 1 56 4 27 Co + 0 n = 25 Mn + 2 He

