Лекция_2_3_хим_вещества_раст_клетки_2015.ppt
- Количество слайдов: 71
 Химические вещества растительной клетки 1. Первичные и вторичные метаболиты 2. Углеводы 3. Липиды 4. Нуклеиновые кислоты 5. Белки. 6. Системы регуляции. Ферменты.
Химические вещества растительной клетки 1. Первичные и вторичные метаболиты 2. Углеводы 3. Липиды 4. Нуклеиновые кислоты 5. Белки. 6. Системы регуляции. Ферменты.
 Аннотация Химические вещества растительной клетки. Различия и сходство в химическом составе животных и растений. Первичные и вторичные метаболиты. Белки, жиры, углеводы. Особенности строения, классификация, взаимосвязь между их структурой и физиологической ролью. Нуклеиновые кислоты. Структура ДНК и РНК. Уровни организации ДНК эукариот. Обмен веществ. Особенности обмена веществ растительной клетки. Уровни регуляции метаболизма клетки (генетический, мембранный, трофический). Окислительновосстановительные процессы, их роль в обмене веществ. Ферменты, их основные свойства и физиологическое значение. Особенности работы ферментов в живой клетке. Распределение ферментов в растительной клетке. Регуляция работы ферментов. Термины 1. Первичные и вторичные метаболиты растений. 2. Углевод, моносахарид, полисахарид, гликозидная связь, инулин, крахмал, целлюлоза, каллоза, сахароза, мальтоза, фруктоза, глюкоза, слизи, гемицеллюлозы, пектиновые вещества 3. Липиды, триглицериды, фосфолипиды, гликолипиды, воска 4. Белок, аминокислота, белки простые и сложные, изоэлектрическая точка, гидролазы, синтетазы, изомеразы, трансферазы, гистоны, уровни организации белковой молекулы, 5. Нуклеиновые кислоты, ДНК, РНК (матричная, транспортная, рибосомальная), нуклеотид, ген, генетический код, антикодон, репликация, транскрипция, трансляция, 6. Фермент, апофермент, кофактор, кофермент, простетическая группа, энергия активации, активный центр, аллостерический центр, изоферменты, регуляция изостерическая, регуляция аллостерическая, эффектор, специфичность работы фермента, стереоспецифичность, субстрат,
Аннотация Химические вещества растительной клетки. Различия и сходство в химическом составе животных и растений. Первичные и вторичные метаболиты. Белки, жиры, углеводы. Особенности строения, классификация, взаимосвязь между их структурой и физиологической ролью. Нуклеиновые кислоты. Структура ДНК и РНК. Уровни организации ДНК эукариот. Обмен веществ. Особенности обмена веществ растительной клетки. Уровни регуляции метаболизма клетки (генетический, мембранный, трофический). Окислительновосстановительные процессы, их роль в обмене веществ. Ферменты, их основные свойства и физиологическое значение. Особенности работы ферментов в живой клетке. Распределение ферментов в растительной клетке. Регуляция работы ферментов. Термины 1. Первичные и вторичные метаболиты растений. 2. Углевод, моносахарид, полисахарид, гликозидная связь, инулин, крахмал, целлюлоза, каллоза, сахароза, мальтоза, фруктоза, глюкоза, слизи, гемицеллюлозы, пектиновые вещества 3. Липиды, триглицериды, фосфолипиды, гликолипиды, воска 4. Белок, аминокислота, белки простые и сложные, изоэлектрическая точка, гидролазы, синтетазы, изомеразы, трансферазы, гистоны, уровни организации белковой молекулы, 5. Нуклеиновые кислоты, ДНК, РНК (матричная, транспортная, рибосомальная), нуклеотид, ген, генетический код, антикодон, репликация, транскрипция, трансляция, 6. Фермент, апофермент, кофактор, кофермент, простетическая группа, энергия активации, активный центр, аллостерический центр, изоферменты, регуляция изостерическая, регуляция аллостерическая, эффектор, специфичность работы фермента, стереоспецифичность, субстрат,
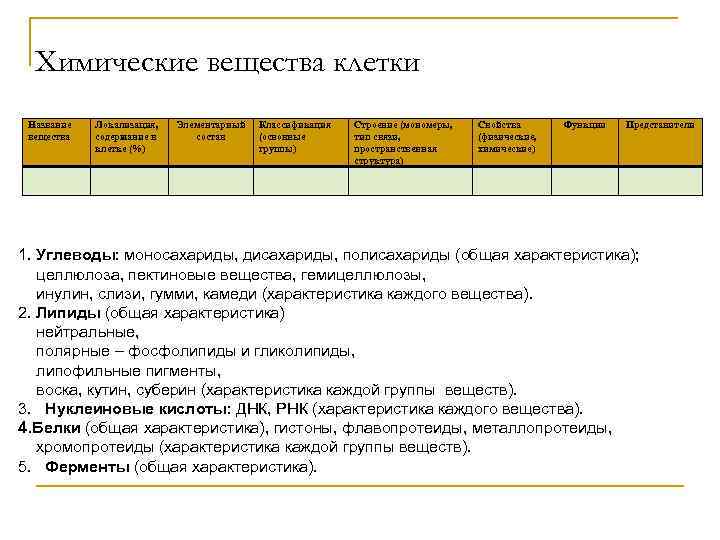 Химические вещества клетки Название вещества Локализация, содержание в клетке (%) Элементарный состав Классификация (основные группы) Строение (мономеры, тип связи, пространственная структура) Свойства (физические, химические) Функции Представители 1. Углеводы: моносахариды, дисахариды, полисахариды (общая характеристика); целлюлоза, пектиновые вещества, гемицеллюлозы, инулин, слизи, гумми, камеди (характеристика каждого вещества). 2. Липиды (общая характеристика) нейтральные, полярные – фосфолипиды и гликолипиды, липофильные пигменты, воска, кутин, суберин (характеристика каждой группы веществ). 3. Нуклеиновые кислоты: ДНК, РНК (характеристика каждого вещества). 4. Белки (общая характеристика), гистоны, флавопротеиды, металлопротеиды, хромопротеиды (характеристика каждой группы веществ). 5. Ферменты (общая характеристика).
Химические вещества клетки Название вещества Локализация, содержание в клетке (%) Элементарный состав Классификация (основные группы) Строение (мономеры, тип связи, пространственная структура) Свойства (физические, химические) Функции Представители 1. Углеводы: моносахариды, дисахариды, полисахариды (общая характеристика); целлюлоза, пектиновые вещества, гемицеллюлозы, инулин, слизи, гумми, камеди (характеристика каждого вещества). 2. Липиды (общая характеристика) нейтральные, полярные – фосфолипиды и гликолипиды, липофильные пигменты, воска, кутин, суберин (характеристика каждой группы веществ). 3. Нуклеиновые кислоты: ДНК, РНК (характеристика каждого вещества). 4. Белки (общая характеристика), гистоны, флавопротеиды, металлопротеиды, хромопротеиды (характеристика каждой группы веществ). 5. Ферменты (общая характеристика).
 Из лекции «О химическом составе клеток» немецкого биолога Альбрехта Косселя, которую он прочел для Берлинского общества физиологов 1891 году: «В то время как первичные метаболиты присутствуют в каждой растительной клетке, способной к делению, то вторичные метаболиты присутствуют в клетках только “нечаянно” и не необходимы для жизни растения. . Случайное распространение этих соединений, их нерегулярное нахождение в близких видах растений, вероятно, свидетельствует о том, что их синтез связан с процессами, не являющимися неотъемлемыми для каждой клетки, а имеющими скорее вторичный характер. . Я предлагаю называть соединения, имеющие важность для каждой клетки первичными, а соединения, не присутствующие в любой растительной клетке – вторичными» Альбрехт Коссель (1853 – 1927) Нобелевская премия 1910 г. ПЕРВИЧНЫЕ МЕТАБОЛИТЫ n n Углеводы Липиды Белки Нуклеиновые кислоты ВТОРИЧНЫЕ МЕТАБОЛИТЫ Терпены и терпеноиды 35 000 соединений Фенолы 8 000 соединений Алкалоиды 12 000 соединений Минорные группы 10 000 соединений (гликозиды, сапонины, беталаины, аллицины, )
Из лекции «О химическом составе клеток» немецкого биолога Альбрехта Косселя, которую он прочел для Берлинского общества физиологов 1891 году: «В то время как первичные метаболиты присутствуют в каждой растительной клетке, способной к делению, то вторичные метаболиты присутствуют в клетках только “нечаянно” и не необходимы для жизни растения. . Случайное распространение этих соединений, их нерегулярное нахождение в близких видах растений, вероятно, свидетельствует о том, что их синтез связан с процессами, не являющимися неотъемлемыми для каждой клетки, а имеющими скорее вторичный характер. . Я предлагаю называть соединения, имеющие важность для каждой клетки первичными, а соединения, не присутствующие в любой растительной клетке – вторичными» Альбрехт Коссель (1853 – 1927) Нобелевская премия 1910 г. ПЕРВИЧНЫЕ МЕТАБОЛИТЫ n n Углеводы Липиды Белки Нуклеиновые кислоты ВТОРИЧНЫЕ МЕТАБОЛИТЫ Терпены и терпеноиды 35 000 соединений Фенолы 8 000 соединений Алкалоиды 12 000 соединений Минорные группы 10 000 соединений (гликозиды, сапонины, беталаины, аллицины, )
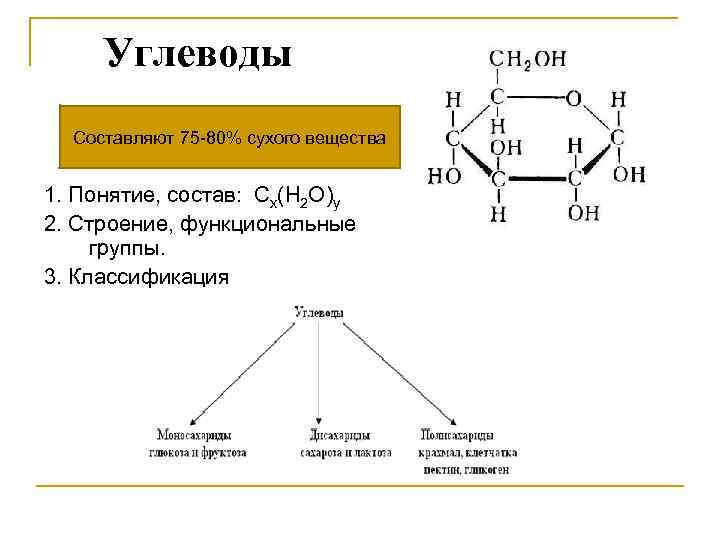 Углеводы Составляют 75 -80% сухого вещества 1. Понятие, состав: Сх(Н 2 О)у 2. Строение, функциональные группы. 3. Классификация
Углеводы Составляют 75 -80% сухого вещества 1. Понятие, состав: Сх(Н 2 О)у 2. Строение, функциональные группы. 3. Классификация
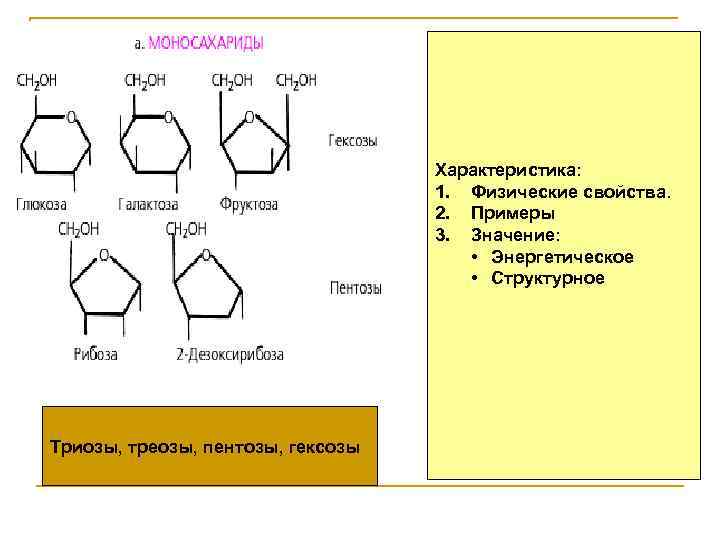 Характеристика: 1. Физические свойства. 2. Примеры 3. Значение: • Энергетическое • Структурное Триозы, треозы, пентозы, гексозы
Характеристика: 1. Физические свойства. 2. Примеры 3. Значение: • Энергетическое • Структурное Триозы, треозы, пентозы, гексозы
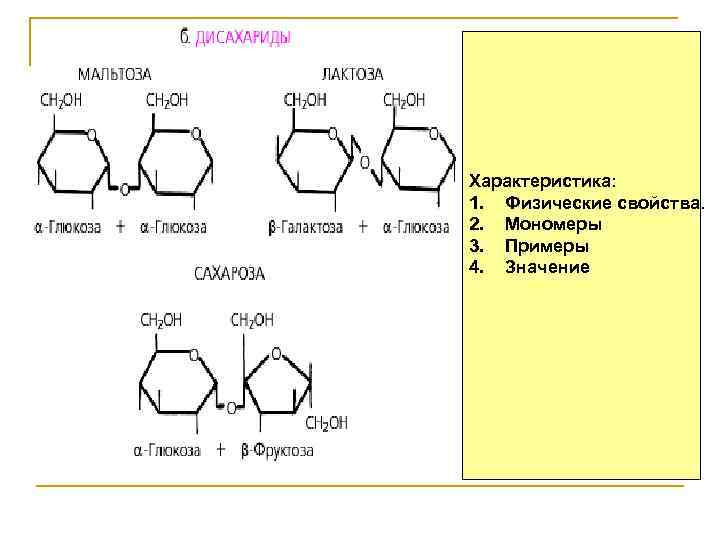 Характеристика: 1. Физические свойства. 2. Мономеры 3. Примеры 4. Значение
Характеристика: 1. Физические свойства. 2. Мономеры 3. Примеры 4. Значение
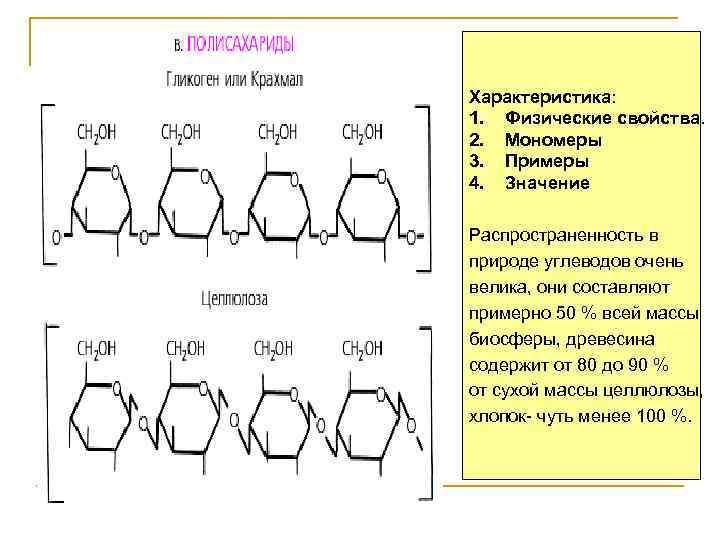 Характеристика: 1. Физические свойства. 2. Мономеры 3. Примеры 4. Значение Распространенность в природе углеводов очень велика, они составляют примерно 50 % всей массы биосферы, древесина содержит от 80 до 90 % от сухой массы целлюлозы, хлопок- чуть менее 100 %.
Характеристика: 1. Физические свойства. 2. Мономеры 3. Примеры 4. Значение Распространенность в природе углеводов очень велика, они составляют примерно 50 % всей массы биосферы, древесина содержит от 80 до 90 % от сухой массы целлюлозы, хлопок- чуть менее 100 %.
 Крахмал АМИЛОЗА- линейный полисахарид, состоящий из остатков D- глюкозы, связанных a-(1 -4)-гликозидными связями. Структурной единицей является дисахарид мальтоза. АМИЛОПЕКТИН отличается от амилозы большей молекулярной массой и наличием разветвлений в цепи, по местам (1 -6). Структурными единицами амилопектина являются мальтоза и изомальтоза. Молекулярная масса может достигать 20 000
Крахмал АМИЛОЗА- линейный полисахарид, состоящий из остатков D- глюкозы, связанных a-(1 -4)-гликозидными связями. Структурной единицей является дисахарид мальтоза. АМИЛОПЕКТИН отличается от амилозы большей молекулярной массой и наличием разветвлений в цепи, по местам (1 -6). Структурными единицами амилопектина являются мальтоза и изомальтоза. Молекулярная масса может достигать 20 000
 Физические свойства амилозы и амилопектина Амилоза растворяется в горячей воде с образованием маловязких растворов, Амилопектин способен набухать в воде при температуре ее кипения с образованием коллоидных растворов, вследствие гидратации молекулы водой. Соотношение амилозы и амилопектина в крахмале различных источников – разное. Источник крахмала Картофель, пшеница, кукуруза обычная Амилоза Амило пектин 20 -25 75 -80 Кукуруза восковидная 0 100 Рис 17 83 Яблоки (плоды) 100 0
Физические свойства амилозы и амилопектина Амилоза растворяется в горячей воде с образованием маловязких растворов, Амилопектин способен набухать в воде при температуре ее кипения с образованием коллоидных растворов, вследствие гидратации молекулы водой. Соотношение амилозы и амилопектина в крахмале различных источников – разное. Источник крахмала Картофель, пшеница, кукуруза обычная Амилоза Амило пектин 20 -25 75 -80 Кукуруза восковидная 0 100 Рис 17 83 Яблоки (плоды) 100 0
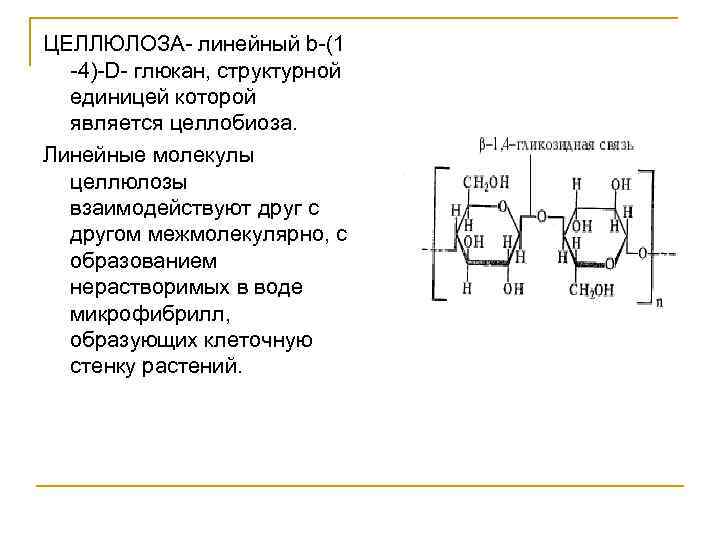 ЦЕЛЛЮЛОЗА- линейный b-(1 -4)-D- глюкан, структурной единицей которой является целлобиоза. Линейные молекулы целлюлозы взаимодействуют друг с другом межмолекулярно, с образованием нерастворимых в воде микрофибрилл, образующих клеточную стенку растений.
ЦЕЛЛЮЛОЗА- линейный b-(1 -4)-D- глюкан, структурной единицей которой является целлобиоза. Линейные молекулы целлюлозы взаимодействуют друг с другом межмолекулярно, с образованием нерастворимых в воде микрофибрилл, образующих клеточную стенку растений.
 Гемицеллюлозы (полуклетчатки) Ксилоглюкан Группа полисахаридов, не растворимых в воде, но растворяющихся в щелочах. Производные пентоз (L-ксилоза, Lарабиноза) и гексоз (D-глюкоза, D-галактоза). Молекула полимера состоит из 150 -300 молекул мономеров. Входят в состав клеточных стенок.
Гемицеллюлозы (полуклетчатки) Ксилоглюкан Группа полисахаридов, не растворимых в воде, но растворяющихся в щелочах. Производные пентоз (L-ксилоза, Lарабиноза) и гексоз (D-глюкоза, D-галактоза). Молекула полимера состоит из 150 -300 молекул мономеров. Входят в состав клеточных стенок.
 Пектиновые вещества ГК - α-D-галактуроновая кислота Р - рамноза рамногалактуронан Полимеры галактуроновой кислоты и ее метилированных производных. Содержат большое количество карбоксильных групп и могут связывать ионы двухвалентных металлов, например, Ca+2, что играет роль в объединении компонентов клеточной стенки. Обусловливают оводненность клеточной оболочки. Входят в состав клеточных стенок.
Пектиновые вещества ГК - α-D-галактуроновая кислота Р - рамноза рамногалактуронан Полимеры галактуроновой кислоты и ее метилированных производных. Содержат большое количество карбоксильных групп и могут связывать ионы двухвалентных металлов, например, Ca+2, что играет роль в объединении компонентов клеточной стенки. Обусловливают оводненность клеточной оболочки. Входят в состав клеточных стенок.
 ДРУГИЕ ПОЛИСАХАРИДЫ В клубнях и корнях георгина, нарцисса, гиацинта, туберозы, цикория, топинамбура, скорционера, овсяного корня содержание инулина достигает 10— 12 % (до 60% от содержания сухих веществ). Инулин – запасное вещество. Заменяет крахмал. Мономер – фруктоза. Характерен для растений сем. Сложноцветные, а также Колокольчиковые, Лилейные, Лобелиевые, Фиалковые
ДРУГИЕ ПОЛИСАХАРИДЫ В клубнях и корнях георгина, нарцисса, гиацинта, туберозы, цикория, топинамбура, скорционера, овсяного корня содержание инулина достигает 10— 12 % (до 60% от содержания сухих веществ). Инулин – запасное вещество. Заменяет крахмал. Мономер – фруктоза. Характерен для растений сем. Сложноцветные, а также Колокольчиковые, Лилейные, Лобелиевые, Фиалковые
 Каллоза – аморфный полимер глюкозы (1, 3 -гликозидные связи). Образуется в ответ на повреждения. Структурное значение (ситовидные трубки). Гумми (камеди) - растворимые в воде или набухающие в ней полимеры моносахаридов (глюкозы, галактозы, рамнозы, арабинозы, глюкуроновых кислот) Образуют вязкие коллоидные растворы. Защитное значение Слизи- присутствуют в семенах, корнях и коре. По химическому составу и физическим свойствам близки камедям. В состав растительной слизи входят разветвленные галактоманнаны) и линейные (глюкоманнаны) полисахариды. Способны к набуханию в воде, что способствует поглощению воды семенами и их набуханию при прорастании. Накопление слизей в тканях растений повышает их засухоустойчивость
Каллоза – аморфный полимер глюкозы (1, 3 -гликозидные связи). Образуется в ответ на повреждения. Структурное значение (ситовидные трубки). Гумми (камеди) - растворимые в воде или набухающие в ней полимеры моносахаридов (глюкозы, галактозы, рамнозы, арабинозы, глюкуроновых кислот) Образуют вязкие коллоидные растворы. Защитное значение Слизи- присутствуют в семенах, корнях и коре. По химическому составу и физическим свойствам близки камедям. В состав растительной слизи входят разветвленные галактоманнаны) и линейные (глюкоманнаны) полисахариды. Способны к набуханию в воде, что способствует поглощению воды семенами и их набуханию при прорастании. Накопление слизей в тканях растений повышает их засухоустойчивость
 Контрольные вопросы 1. Дайте общую характеристику углеводам. На чем основана их классификация? 2. Каковы функции углеводов в растениях? 3. Как классифицируются моносахариды? Каковы их свойства и значение? Приведите примеры. 4. Охарактеризуйте дисахариды. Приведите примеры. 5. Дайте характеристику полисахаридам. Каковы их общие свойства? 6. Назовите полисахариды, входящие в состав клеточной стенки, запасные полисахариды. Охарактеризуйте их строение, свойства, распространение. 7. Охарактеризуйте каллозу, гумми (камеди) и слизи, их свойства, распространение и роль в растении.
Контрольные вопросы 1. Дайте общую характеристику углеводам. На чем основана их классификация? 2. Каковы функции углеводов в растениях? 3. Как классифицируются моносахариды? Каковы их свойства и значение? Приведите примеры. 4. Охарактеризуйте дисахариды. Приведите примеры. 5. Дайте характеристику полисахаридам. Каковы их общие свойства? 6. Назовите полисахариды, входящие в состав клеточной стенки, запасные полисахариды. Охарактеризуйте их строение, свойства, распространение. 7. Охарактеризуйте каллозу, гумми (камеди) и слизи, их свойства, распространение и роль в растении.
 Липиды Жиры и жироподобные вещества. Особенности: -гидрофобность -большое количество связей С-Н Классификация: n Нейтральные липиды (триглицериды) n Полярные липиды (фосфолипиды, гликолипиды) n Воски
Липиды Жиры и жироподобные вещества. Особенности: -гидрофобность -большое количество связей С-Н Классификация: n Нейтральные липиды (триглицериды) n Полярные липиды (фосфолипиды, гликолипиды) n Воски
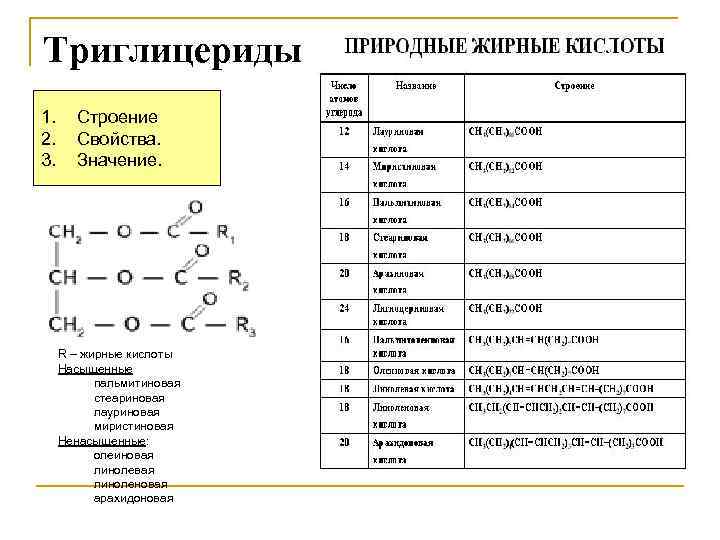 Триглицериды 1. 2. 3. Строение Свойства. Значение. R – жирные кислоты Насыщенные пальмитиновая стеариновая лауриновая миристиновая Ненасыщенные: олеиновая линоленовая арахидоновая
Триглицериды 1. 2. 3. Строение Свойства. Значение. R – жирные кислоты Насыщенные пальмитиновая стеариновая лауриновая миристиновая Ненасыщенные: олеиновая линоленовая арахидоновая
 Состав масел Хлопков ое Соево е Подсолнечное Оливковое Кукурузное Пальмитиновая 20 6 - 9 15 Стеариновая 2 4 9 2 15 Олеиновая 31 22 39 82 24 Линолевая 40 49 46 4 61 - 10 - - - Линоленовая
Состав масел Хлопков ое Соево е Подсолнечное Оливковое Кукурузное Пальмитиновая 20 6 - 9 15 Стеариновая 2 4 9 2 15 Олеиновая 31 22 39 82 24 Линолевая 40 49 46 4 61 - 10 - - - Линоленовая
 Полярные липиды: фосфолипиды и гликолипиды Х – холин, серин, глицерин, этаноламин
Полярные липиды: фосфолипиды и гликолипиды Х – холин, серин, глицерин, этаноламин

 Воска Воски — распространённые в растительном и животном мире сложные эфиры высших жирных кислот (С 24 -С 36 и С 25 -С 29) и высших высокомолекулярных спиртов (С 22 -С 32 цериловый, мирициловый) Очень устойчивы, нерастворимы в воде, но хорошо растворимы в бензине, хлороформе, эфире. Растительные воски покрывают содержатся в кутикуле, тонким слоем листья, стебли, плоды и защищают их от размачивания водой, высыхания, вредных микроорганизмов, иногда в качестве резервных липидов входят в состав семян ( «масло» жожоба). Жожоба , Хохо ба — растение вида Си ммондсия кита йская (Simmóndsia chinénsis), сильно ветвистый вечнозелёный кустарник. Масло (жидкий воск) получают методом холодного прессования из плодов и семян Карнаубский воск получают из листьев бразильской восковой пальмы, или карнаубы
Воска Воски — распространённые в растительном и животном мире сложные эфиры высших жирных кислот (С 24 -С 36 и С 25 -С 29) и высших высокомолекулярных спиртов (С 22 -С 32 цериловый, мирициловый) Очень устойчивы, нерастворимы в воде, но хорошо растворимы в бензине, хлороформе, эфире. Растительные воски покрывают содержатся в кутикуле, тонким слоем листья, стебли, плоды и защищают их от размачивания водой, высыхания, вредных микроорганизмов, иногда в качестве резервных липидов входят в состав семян ( «масло» жожоба). Жожоба , Хохо ба — растение вида Си ммондсия кита йская (Simmóndsia chinénsis), сильно ветвистый вечнозелёный кустарник. Масло (жидкий воск) получают методом холодного прессования из плодов и семян Карнаубский воск получают из листьев бразильской восковой пальмы, или карнаубы
 Кутин, суберин Суберин Мономерами являются насыщенные и ненасыщенные оксожирные кислоты. Пропитанные суберином клеточные стенки (опробковение оболочки) становятся труднопроницаемыми для воды и растворов. Кутин Состоит из оксожирных кислот и их солей, Выделяется через клеточную стенку на поверхность эпидермальной клетки Участвует в образовании кутикулы. Кутикула препятствует испарению воды, регулирует водно-тепловой режим тканей растений.
Кутин, суберин Суберин Мономерами являются насыщенные и ненасыщенные оксожирные кислоты. Пропитанные суберином клеточные стенки (опробковение оболочки) становятся труднопроницаемыми для воды и растворов. Кутин Состоит из оксожирных кислот и их солей, Выделяется через клеточную стенку на поверхность эпидермальной клетки Участвует в образовании кутикулы. Кутикула препятствует испарению воды, регулирует водно-тепловой режим тканей растений.
 Контрольные вопросы 1. Дайте общую характеристику липидам. 2. Каковы функции липидов в растениях? 3. Охарактеризуйте неполярные липиды: строение, значение, распространение. 4. Дайте характеристику фосфолипидам и гликолипидам. Какие свойства имеют? Какова их роль в растении? 5. Какова роль восков в растении? В чем особенности их строения?
Контрольные вопросы 1. Дайте общую характеристику липидам. 2. Каковы функции липидов в растениях? 3. Охарактеризуйте неполярные липиды: строение, значение, распространение. 4. Дайте характеристику фосфолипидам и гликолипидам. Какие свойства имеют? Какова их роль в растении? 5. Какова роль восков в растении? В чем особенности их строения?
 Нуклеиновые кислоты 1. Понятие. Открытие. 2. Строение нуклеотидов. 3. Типы нуклеиновых кислот. Сравнение. 4. ДНК: структура, синтез. 5. РНК: структура, синтез. 6. Значение.
Нуклеиновые кислоты 1. Понятие. Открытие. 2. Строение нуклеотидов. 3. Типы нуклеиновых кислот. Сравнение. 4. ДНК: структура, синтез. 5. РНК: структура, синтез. 6. Значение.






 Типы РНК и. РНК (м. РНК) messenger– посыльный До 5%. Ядро, цитоплазма т. РНК transfer – переносящая До 10%. Цитоплазма. р. РНК – рибосомальная 85% Рибосомы
Типы РНК и. РНК (м. РНК) messenger– посыльный До 5%. Ядро, цитоплазма т. РНК transfer – переносящая До 10%. Цитоплазма. р. РНК – рибосомальная 85% Рибосомы


 Контрольные вопросы 1. Дайте характеристику строению нуклеотида. 2. Какие главные различия в структуре и функциях ДНК и РНК? 3. Какие типы РНК вы знаете? 4. Какое значение имеют нуклеиновые кислоты? 5. Как можно доказать роль ДНК как носителя наследственной информации? 6. Дайте характеристику строению нуклеиновых кислот. Какие структурные особенности ДНК определяют ее роль? 7. Объясните термины: транскрипция, трансляция. 8. Какая часть молекулы ДНК несет информацию о: а) белке, б) аминокислоте?
Контрольные вопросы 1. Дайте характеристику строению нуклеотида. 2. Какие главные различия в структуре и функциях ДНК и РНК? 3. Какие типы РНК вы знаете? 4. Какое значение имеют нуклеиновые кислоты? 5. Как можно доказать роль ДНК как носителя наследственной информации? 6. Дайте характеристику строению нуклеиновых кислот. Какие структурные особенности ДНК определяют ее роль? 7. Объясните термины: транскрипция, трансляция. 8. Какая часть молекулы ДНК несет информацию о: а) белке, б) аминокислоте?
 Белки 1. 2. 3. 4. 5. 6. Понятие Молекулярная масса. Свойства Строение: мономеры, уровни организации. Классификация: по растворимости, простые и сложные, фибриллярные и глобулярные. Физиологическое значение.
Белки 1. 2. 3. 4. 5. 6. Понятие Молекулярная масса. Свойства Строение: мономеры, уровни организации. Классификация: по растворимости, простые и сложные, фибриллярные и глобулярные. Физиологическое значение.



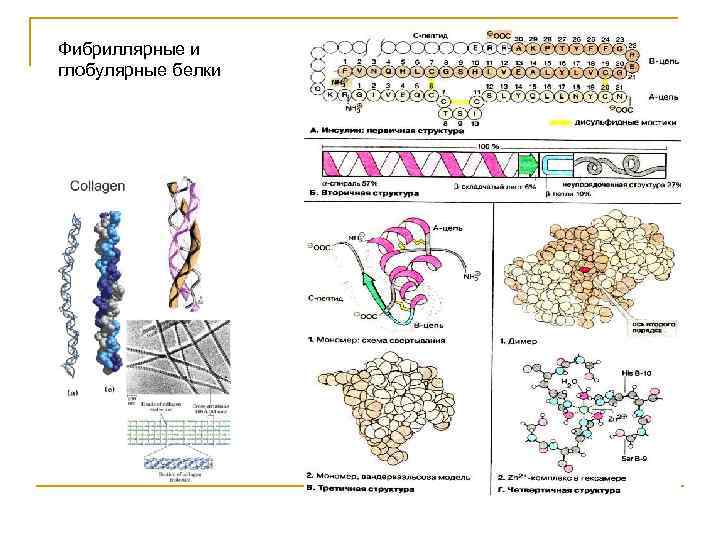 Фибриллярные и глобулярные белки
Фибриллярные и глобулярные белки
 Классификация белков по строению
Классификация белков по строению
 Классификация белков по структуре
Классификация белков по структуре
 Классификация белков по растворимости
Классификация белков по растворимости
 Классификация белков по функциям
Классификация белков по функциям

 Контрольные вопросы 1. Дайте определение белкам, каково их содержание? 2. Охарактеризуйте строение белков. 3. Какие свойства белков вам известны? 4. Охарактеризуйте фибриллярные и глобулярные белки. 5. В чем отличие простых и сложных белков? 6. Каковы функции белков в растениях?
Контрольные вопросы 1. Дайте определение белкам, каково их содержание? 2. Охарактеризуйте строение белков. 3. Какие свойства белков вам известны? 4. Охарактеризуйте фибриллярные и глобулярные белки. 5. В чем отличие простых и сложных белков? 6. Каковы функции белков в растениях?
 Системы регуляции у растений I. Внутриклеточные 1) Ферментативная 2) Генетическая 3) Мембранная II. Межклеточные 1)Трофическая 2) Гормональная 3) Электрофизиологическая III. Организменные
Системы регуляции у растений I. Внутриклеточные 1) Ферментативная 2) Генетическая 3) Мембранная II. Межклеточные 1)Трофическая 2) Гормональная 3) Электрофизиологическая III. Организменные
 Ферменты 1. Понятие, значение. 2. Особенности действия ферментов. 3. Структура ферментов. 4. Механизм действия. 5. Локализация ферментов. 6. Классификация ферментов 7. Особенности работы в живой клетке. 8. Регуляция работы ферментов.
Ферменты 1. Понятие, значение. 2. Особенности действия ферментов. 3. Структура ферментов. 4. Механизм действия. 5. Локализация ферментов. 6. Классификация ферментов 7. Особенности работы в живой клетке. 8. Регуляция работы ферментов.
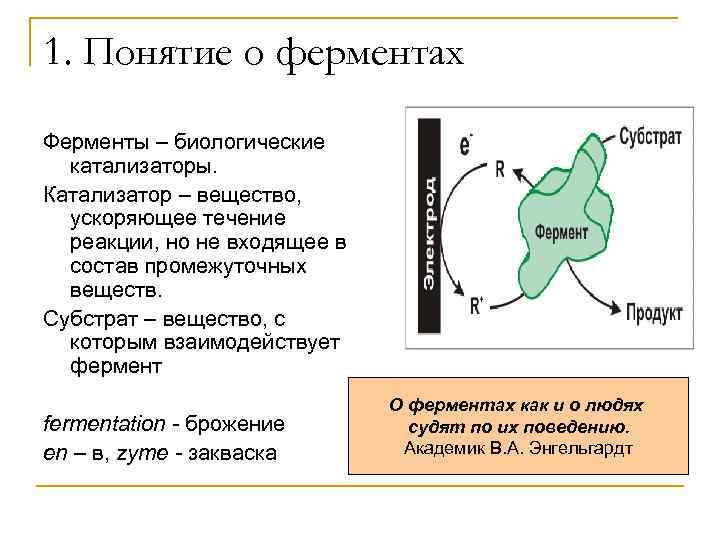 1. Понятие о ферментах Ферменты – биологические катализаторы. Катализатор – вещество, ускоряющее течение реакции, но не входящее в состав промежуточных веществ. Субстрат – вещество, с которым взаимодействует фермент fermentation - брожение en – в, zyme - закваска О ферментах как и о людях судят по их поведению. Академик В. А. Энгельгардт
1. Понятие о ферментах Ферменты – биологические катализаторы. Катализатор – вещество, ускоряющее течение реакции, но не входящее в состав промежуточных веществ. Субстрат – вещество, с которым взаимодействует фермент fermentation - брожение en – в, zyme - закваска О ферментах как и о людях судят по их поведению. Академик В. А. Энгельгардт
 Значение ферментов Ферменты играют ключевую роль в клетке: Свойства клеток определяются химизмом Химизм клеток – составом ферментов Природа фермента – спецификой РНК Специфичность РНК – ДНК 1) Участие в обмене веществ, ускорение реакций. 2) Участие в передаче наследственной информации 3) Защитная функция. 4)Приспособление к меняющимся условиям среды. Изоферменты – ферменты с одинаковой функцией.
Значение ферментов Ферменты играют ключевую роль в клетке: Свойства клеток определяются химизмом Химизм клеток – составом ферментов Природа фермента – спецификой РНК Специфичность РНК – ДНК 1) Участие в обмене веществ, ускорение реакций. 2) Участие в передаче наследственной информации 3) Защитная функция. 4)Приспособление к меняющимся условиям среды. Изоферменты – ферменты с одинаковой функцией.
 2. Особенности действия ферментов 1. Чувствительность, работают в мягких условиях. 2. Высокая скорость, ускоряют реакции (109 - 1010). 3. Специфичность (избирательность) действия. 2 Н 2 О 2 → 2 Н 2 О+О 2 Катализатор Еа, к. Дж/моль Относ. скорость реакции Без катализатора 70 1 Pt 45 (гетерогенный) 2× 103 Fe (гомогенный) 42 8× 103 Каталаза 7 9× 1010
2. Особенности действия ферментов 1. Чувствительность, работают в мягких условиях. 2. Высокая скорость, ускоряют реакции (109 - 1010). 3. Специфичность (избирательность) действия. 2 Н 2 О 2 → 2 Н 2 О+О 2 Катализатор Еа, к. Дж/моль Относ. скорость реакции Без катализатора 70 1 Pt 45 (гетерогенный) 2× 103 Fe (гомогенный) 42 8× 103 Каталаза 7 9× 1010
 Специфичность действия ферментов а) по выбору субстрата б) по типу реакции (специфичность действия). а) абсолютная (сахараза, хлорофиллаза) б) групповая (липаза, протеаза). Стереоспецифичность (фумараза не действует на малеиновую кислоту -цис-изомер).
Специфичность действия ферментов а) по выбору субстрата б) по типу реакции (специфичность действия). а) абсолютная (сахараза, хлорофиллаза) б) групповая (липаза, протеаза). Стереоспецифичность (фумараза не действует на малеиновую кислоту -цис-изомер).
 Активный центр фермента Активный (каталитический) центр – совокупность функциональных групп, принимающих непосредственное участие в ферментативной реакции. -формируется в результате специфической укладки белка. -обеспечивает соединение фермента и субстрата -дает возможность дальнейших превращений
Активный центр фермента Активный (каталитический) центр – совокупность функциональных групп, принимающих непосредственное участие в ферментативной реакции. -формируется в результате специфической укладки белка. -обеспечивает соединение фермента и субстрата -дает возможность дальнейших превращений
 Теории, объясняющие специфичность 1) «ключа и замка» Э. Фишер, 1911 г. 2) «руки и перчатки» - индуцированного соответствия Даниэля-Кошланда, 1958 г.
Теории, объясняющие специфичность 1) «ключа и замка» Э. Фишер, 1911 г. 2) «руки и перчатки» - индуцированного соответствия Даниэля-Кошланда, 1958 г.
 3. Структура ферментов Преимущественно белковой природы (рибозимы). 1) Однокомпонентные (простые) 2) Двухкомпонентные (сложные) – состоят из белковой (апофермент)и небелковой частей (кофактор). Кофактор: -прочносвязанный (простетическая группа) -слабосвязанный (кофермент)
3. Структура ферментов Преимущественно белковой природы (рибозимы). 1) Однокомпонентные (простые) 2) Двухкомпонентные (сложные) – состоят из белковой (апофермент)и небелковой частей (кофактор). Кофактор: -прочносвязанный (простетическая группа) -слабосвязанный (кофермент)
 Некоторые коферменты Кофермент Общая роль Витамин предшественник NAD+ , NADP+ Перенос водорода (электронов) Никотиновая кислота витамин РР FAD Перенос водорода (электронов) Рибофлавин - витамин В 2 Кофермент А Активация и перенос ацильных групп Пантотеновая кислота Биотин Связывание СО 2 Биотин Пиридоксальфосфат Перенос аминогрупп Пиридоксин - витамин В 6 Тетрагидрофолиевая кислота Перенос одноуглеродных фрагментов Фолиевая кислота Роль кофактора : изменение третичной структуры белка и создание комплементарности между ферментом и субстратом; непосредственное участие в реакции в качестве еще одного субстрата.
Некоторые коферменты Кофермент Общая роль Витамин предшественник NAD+ , NADP+ Перенос водорода (электронов) Никотиновая кислота витамин РР FAD Перенос водорода (электронов) Рибофлавин - витамин В 2 Кофермент А Активация и перенос ацильных групп Пантотеновая кислота Биотин Связывание СО 2 Биотин Пиридоксальфосфат Перенос аминогрупп Пиридоксин - витамин В 6 Тетрагидрофолиевая кислота Перенос одноуглеродных фрагментов Фолиевая кислота Роль кофактора : изменение третичной структуры белка и создание комплементарности между ферментом и субстратом; непосредственное участие в реакции в качестве еще одного субстрата.
 4. Механизм действия 1)Образование фермент -субстратного комплекса. 2)Преобразование промежуточного соединения в активный комплекс. 3)Выделение продуктов реакции
4. Механизм действия 1)Образование фермент -субстратного комплекса. 2)Преобразование промежуточного соединения в активный комплекс. 3)Выделение продуктов реакции


 5. Локализация ферментов 1) Эндоферменты – действуют в пределах клетки, в которой образуются. 2) Экзоферменты – выделяются из клетки и действуют вне ее.
5. Локализация ферментов 1) Эндоферменты – действуют в пределах клетки, в которой образуются. 2) Экзоферменты – выделяются из клетки и действуют вне ее.
 6. Классификация ферментов
6. Классификация ферментов
 7. Особенности работы в живой клетке. В живой клетке работа ферментов согласована, что позволяет реализовывать синтетическую функцию. n n n Топография, компартментация в клетке. Работают группами, ансамблями. Работа регулируется
7. Особенности работы в живой клетке. В живой клетке работа ферментов согласована, что позволяет реализовывать синтетическую функцию. n n n Топография, компартментация в клетке. Работают группами, ансамблями. Работа регулируется
 8. Регуляция работы ферментов 1) 2) 3) Регуляция синтеза (количества) фермента. Генный уровень (транскрипция, трансляция). Регуляция активности (качества) фермента Регуляция условиями протекания реакции.
8. Регуляция работы ферментов 1) 2) 3) Регуляция синтеза (количества) фермента. Генный уровень (транскрипция, трансляция). Регуляция активности (качества) фермента Регуляция условиями протекания реакции.
 Регуляция активности ферментов Действие на превращение предшественников ферментов в активные ферменты 2) Действие на процесс распада 3) Изменение активности фермента под действием эффекторов (малых молекул) Эффекторы могут увеличивать (активаторы) и снижать (ингибиторы) активность фермента 1)
Регуляция активности ферментов Действие на превращение предшественников ферментов в активные ферменты 2) Действие на процесс распада 3) Изменение активности фермента под действием эффекторов (малых молекул) Эффекторы могут увеличивать (активаторы) и снижать (ингибиторы) активность фермента 1)
 1) Изостерическая регуляция – эффектор связывается с активным центром (регуляция на уровне каталитических центров). Структура фермента меняется незначительно. 2) Аллостерическая регуляция – эффектор связывается с аллостерическим центром, изменяется конформация всей молекулы.
1) Изостерическая регуляция – эффектор связывается с активным центром (регуляция на уровне каталитических центров). Структура фермента меняется незначительно. 2) Аллостерическая регуляция – эффектор связывается с аллостерическим центром, изменяется конформация всей молекулы.
 Аллостерические центры – рецепторные участки, расположенные отдельно от активного центра и служащие для связывания аллостерических эффекторов.
Аллостерические центры – рецепторные участки, расположенные отдельно от активного центра и служащие для связывания аллостерических эффекторов.



 Контрольные вопросы 1. Какие системы регуляции можно выделить на внутриклеточном и межклеточном уровне? 2. Дайте определение ферментам. Какое значение они имеют? 3. Каковы особенности действия ферментов? 4. Каким образом ферменты ускоряют химические реакции? От чего зависит скорость и направленность ферментативных реакций? 5. Какое строение имеют ферменты? 6. В чем особенности работы ферментов в живой клетке? 7. Где локализованы ферменты в клетке? 8. Каковы пути регуляции биосинтеза белков ферментов? 9. Как регулируется активность ферментов? 10. Какие факторы влияют на работу ферментов? 11. Объясните термины: субстрат, активный центр, изоферменты, аллостерический центр, простетическая группа, кофермент, кофактор, аллостерическая регуляция, изостерическая регуляция.
Контрольные вопросы 1. Какие системы регуляции можно выделить на внутриклеточном и межклеточном уровне? 2. Дайте определение ферментам. Какое значение они имеют? 3. Каковы особенности действия ферментов? 4. Каким образом ферменты ускоряют химические реакции? От чего зависит скорость и направленность ферментативных реакций? 5. Какое строение имеют ферменты? 6. В чем особенности работы ферментов в живой клетке? 7. Где локализованы ферменты в клетке? 8. Каковы пути регуляции биосинтеза белков ферментов? 9. Как регулируется активность ферментов? 10. Какие факторы влияют на работу ферментов? 11. Объясните термины: субстрат, активный центр, изоферменты, аллостерический центр, простетическая группа, кофермент, кофактор, аллостерическая регуляция, изостерическая регуляция.
 Строение растительной клетки Компартмент клеточная стенка плазмалемма гиалоплазма митохондрии хлоропласты вакуоль ЭПР аппарат Гольджи лизосомы микротельца рибосомы Химический состав Особенности строения Свойства Функции
Строение растительной клетки Компартмент клеточная стенка плазмалемма гиалоплазма митохондрии хлоропласты вакуоль ЭПР аппарат Гольджи лизосомы микротельца рибосомы Химический состав Особенности строения Свойства Функции


