01 Пластовая вода.ppt
- Количество слайдов: 27
 Химические свойства в нормальных и пластовых условиях Минеральный состав Сухой остаток, минерализация Газовый состав Газонасыщенность Органический состав БПК, ХПК (окисляемость) Общие свойства Кислотность-щелочность, p. H Окислительно-восстановительный потенциал, Eh (pe) Жесткость, Агрессивность 1. Сухой остаток– минеральный остаток после выпаривания влаги. 2. Методы определения: Согласно ГОСТ’у 18164 -72 выпаривают профильтрованную воду на водяной бане, высушивают остаток при 110 o. C до постоянства массы и взвешивают его. Размерность мг/л для пресных, г/л для солоноватых и соленых вод, г/кг для рассолов.
Химические свойства в нормальных и пластовых условиях Минеральный состав Сухой остаток, минерализация Газовый состав Газонасыщенность Органический состав БПК, ХПК (окисляемость) Общие свойства Кислотность-щелочность, p. H Окислительно-восстановительный потенциал, Eh (pe) Жесткость, Агрессивность 1. Сухой остаток– минеральный остаток после выпаривания влаги. 2. Методы определения: Согласно ГОСТ’у 18164 -72 выпаривают профильтрованную воду на водяной бане, высушивают остаток при 110 o. C до постоянства массы и взвешивают его. Размерность мг/л для пресных, г/л для солоноватых и соленых вод, г/кг для рассолов.
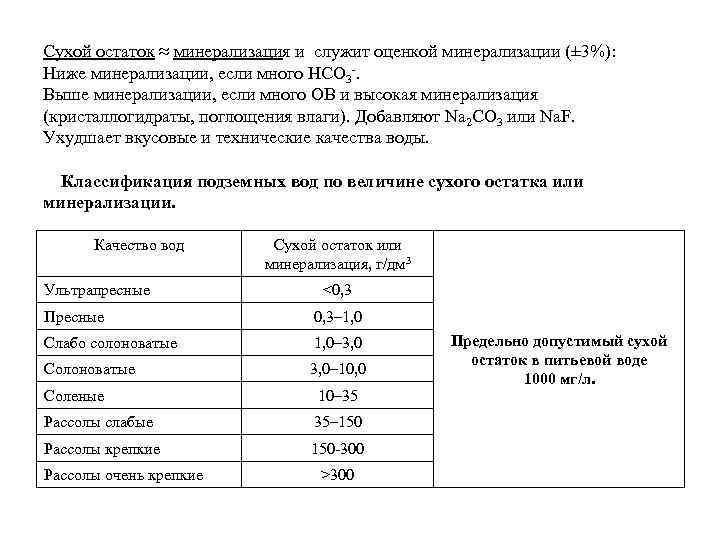 Сухой остаток ≈ минерализация и служит оценкой минерализации (± 3%): Ниже минерализации, если много HCO 3 -. Выше минерализации, если много ОВ и высокая минерализация (кристаллогидраты, поглощения влаги). Добавляют Na 2 CO 3 или Na. F. Ухудшает вкусовые и технические качества воды. Классификация подземных вод по величине сухого остатка или минерализации. Качество вод Ультрапресные Сухой остаток или минерализация, г/дм 3 <0, 3 Пресные 0, 3– 1, 0 Слабо солоноватые 1, 0– 3, 0 Солоноватые 3, 0– 10, 0 Соленые 10– 35 Рассолы слабые 35– 150 Рассолы крепкие 150 -300 Рассолы очень крепкие >300 Предельно допустимый сухой остаток в питьевой воде 1000 мг/л.
Сухой остаток ≈ минерализация и служит оценкой минерализации (± 3%): Ниже минерализации, если много HCO 3 -. Выше минерализации, если много ОВ и высокая минерализация (кристаллогидраты, поглощения влаги). Добавляют Na 2 CO 3 или Na. F. Ухудшает вкусовые и технические качества воды. Классификация подземных вод по величине сухого остатка или минерализации. Качество вод Ультрапресные Сухой остаток или минерализация, г/дм 3 <0, 3 Пресные 0, 3– 1, 0 Слабо солоноватые 1, 0– 3, 0 Солоноватые 3, 0– 10, 0 Соленые 10– 35 Рассолы слабые 35– 150 Рассолы крепкие 150 -300 Рассолы очень крепкие >300 Предельно допустимый сухой остаток в питьевой воде 1000 мг/л.
 2. Газонасыщенность – наибольший газовый фактор. Методы определения: при спонтанной или принудительной дегазации. Размерность: мл/л или см 3/л, при высоких значениях - в см 3/см 3. очень низкая < 50 мл/л, средняя – 100 -1000 мл/л, низкая - 50 -100 мл/л, высокая > 1000 мл/л. Влияет на бальнеологические свойства, агрессивность и пластовые свойства. 3. Биохимическое потребление кислорода (БПК) - количество O 2 необходимое для окисления ОВ воды аэробами (до начала нитрификации). Размерность мг. O/л. Методы определения Отбирается в стеклянную емкость на срок менее 1 суток. Определение содержания O 2 за время инкубации в герметичных условиях в темноте и при 20± 1°С. , где CO 2, нач и CO 2, кон – концентрации кислорода до и после инкубации, мг/л.
2. Газонасыщенность – наибольший газовый фактор. Методы определения: при спонтанной или принудительной дегазации. Размерность: мл/л или см 3/л, при высоких значениях - в см 3/см 3. очень низкая < 50 мл/л, средняя – 100 -1000 мл/л, низкая - 50 -100 мл/л, высокая > 1000 мл/л. Влияет на бальнеологические свойства, агрессивность и пластовые свойства. 3. Биохимическое потребление кислорода (БПК) - количество O 2 необходимое для окисления ОВ воды аэробами (до начала нитрификации). Размерность мг. O/л. Методы определения Отбирается в стеклянную емкость на срок менее 1 суток. Определение содержания O 2 за время инкубации в герметичных условиях в темноте и при 20± 1°С. , где CO 2, нач и CO 2, кон – концентрации кислорода до и после инкубации, мг/л.
 Достоверность зависит от 1 – температуры (2– 3 раза на 10 o. C), 2 – характера ОВ, 3 – количества O 2 (2 -3 мг/л), 4 –нитрификации (на 7 сутки, ингибиторы), 5 - продолжительность (БПК 5, БПК 10, БПКполн). БПК 5 ≈0, 7 БПКполн БПК 5 как показатель степени загрязненности Степень загрязнения БПК 5, мг O/л очень чистые 0, 5– 1, 0 чистые 1, 1– 1, 9 умеренно загрязненные 2, 0– 2, 9 загрязненные 3, 0– 3, 9 грязные 4, 0– 10, 0 очень грязные Более 10, 0 Предельно допустимое БПК 5 питьевых вод - 3 мг O/л, хозяйственно-бытовых - 6 мг O/л.
Достоверность зависит от 1 – температуры (2– 3 раза на 10 o. C), 2 – характера ОВ, 3 – количества O 2 (2 -3 мг/л), 4 –нитрификации (на 7 сутки, ингибиторы), 5 - продолжительность (БПК 5, БПК 10, БПКполн). БПК 5 ≈0, 7 БПКполн БПК 5 как показатель степени загрязненности Степень загрязнения БПК 5, мг O/л очень чистые 0, 5– 1, 0 чистые 1, 1– 1, 9 умеренно загрязненные 2, 0– 2, 9 загрязненные 3, 0– 3, 9 грязные 4, 0– 10, 0 очень грязные Более 10, 0 Предельно допустимое БПК 5 питьевых вод - 3 мг O/л, хозяйственно-бытовых - 6 мг O/л.
 4. Химическое потребление кислорода (ХПК) или окисляемость способность воды восстанавливать кислород сильных окислителей. – Размерность в мг O/л. – ХПКтеор. –если окисляются: C до CO 2, S до SO 3, P до P 2 O 5, N до аммонийных солей, а H до H 2 O или аммонийных солей. Замеренное ХПК< ХПКтеор. • Методы опробования – Если пробу отфильтровать, подкислить H 2 SO 4 до p. H<2 и охладить до 25°С, хранить до 5 суток. Если заморозить до минус 20°С в полимерной емкости, то хранить почти месяц. • Метод анализа – Окисляют избытком перманганата калия (KMn. O 4), бихромата калия (K 2 Cr 2 O 7), иодата калия (KIO 3) и др. при кипячении в присутствии H 2 SO 4. Остаток окислителя оттитровывают. Метод его анализа нормирован ГОСТ’ом 23268. 12 -78. Погрешность ее оценки не должна превышать ± 30%. – Достоверность зависит от характера окислителя: бихроматное ХПК – 95% ХПКтеор. , перманганатное ХПК - 25 -50% ХПКтеор. .
4. Химическое потребление кислорода (ХПК) или окисляемость способность воды восстанавливать кислород сильных окислителей. – Размерность в мг O/л. – ХПКтеор. –если окисляются: C до CO 2, S до SO 3, P до P 2 O 5, N до аммонийных солей, а H до H 2 O или аммонийных солей. Замеренное ХПК< ХПКтеор. • Методы опробования – Если пробу отфильтровать, подкислить H 2 SO 4 до p. H<2 и охладить до 25°С, хранить до 5 суток. Если заморозить до минус 20°С в полимерной емкости, то хранить почти месяц. • Метод анализа – Окисляют избытком перманганата калия (KMn. O 4), бихромата калия (K 2 Cr 2 O 7), иодата калия (KIO 3) и др. при кипячении в присутствии H 2 SO 4. Остаток окислителя оттитровывают. Метод его анализа нормирован ГОСТ’ом 23268. 12 -78. Погрешность ее оценки не должна превышать ± 30%. – Достоверность зависит от характера окислителя: бихроматное ХПК – 95% ХПКтеор. , перманганатное ХПК - 25 -50% ХПКтеор. .
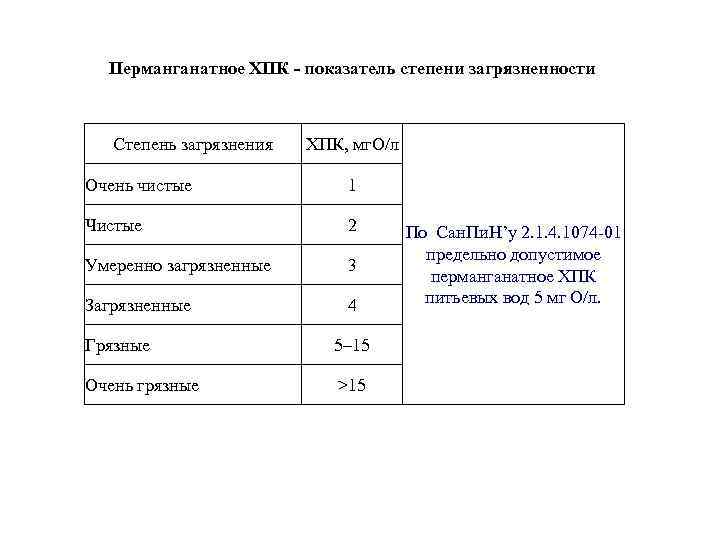 Перманганатное ХПК - показатель степени загрязненности Степень загрязнения ХПК, мг. О/л Очень чистые 1 Чистые 2 Умеренно загрязненные 3 Загрязненные 4 Грязные 5– 15 Очень грязные >15 По Сан. Пи. Н’у 2. 1. 4. 1074 -01 предельно допустимое перманганатное ХПК питьевых вод 5 мг О/л.
Перманганатное ХПК - показатель степени загрязненности Степень загрязнения ХПК, мг. О/л Очень чистые 1 Чистые 2 Умеренно загрязненные 3 Загрязненные 4 Грязные 5– 15 Очень грязные >15 По Сан. Пи. Н’у 2. 1. 4. 1074 -01 предельно допустимое перманганатное ХПК питьевых вод 5 мг О/л.
 5. Кислотность – щелочность – способность природных вод участвовать в реакциях обмена ионами H+ и OH-. Измеряется величинами p. H, щелочности и кислотности. a. p. H • Методы опробования: Непосредственно в месте залегания, или хранить пробу охлажденной, без дегазации и контакта с O 2. • Методы определения −Индикаторная бумага. Точность не более ± 1. −Визуальная колориметрия с помощью индикаторов, меняющих окраску в зависимости от концентрации водородных ионов. Точность около ± 0, 5 − р. Н-метры. Они требуют предварительную калибровку по буферным растворам. Точность достигает ± 0, 1 Свойства воды как функция р. Н. Воды сильнокислые слабокислые нейтральные слабощелочные сильнощелочные р. Н <3 3– 5 5– 6, 5– 7, 5– 8, 5– 9, 5 По Сан. Пи. Н’у 2. 1. 4. 107401 в питьевых водах допустимо p. H 6 -9.
5. Кислотность – щелочность – способность природных вод участвовать в реакциях обмена ионами H+ и OH-. Измеряется величинами p. H, щелочности и кислотности. a. p. H • Методы опробования: Непосредственно в месте залегания, или хранить пробу охлажденной, без дегазации и контакта с O 2. • Методы определения −Индикаторная бумага. Точность не более ± 1. −Визуальная колориметрия с помощью индикаторов, меняющих окраску в зависимости от концентрации водородных ионов. Точность около ± 0, 5 − р. Н-метры. Они требуют предварительную калибровку по буферным растворам. Точность достигает ± 0, 1 Свойства воды как функция р. Н. Воды сильнокислые слабокислые нейтральные слабощелочные сильнощелочные р. Н <3 3– 5 5– 6, 5– 7, 5– 8, 5– 9, 5 По Сан. Пи. Н’у 2. 1. 4. 107401 в питьевых водах допустимо p. H 6 -9.
 b. Щелочность - способность нейтрализовать сильные кислоты. Определяется прямым титрованием воды раствором сильной кислоты (HCl) Все, что выше p. H 4, 3 -общая щелочность, что выше р. Н 8, 4 - свободная щелочность. При р. Н = 4, 3 проба воды имеет нулевую щелочность. Измеряется в мг-экв/л титрующей кислоты. c. Кислотность - способность нейтрализовать сильные щелочи. Определяется прямым титрованием воды раствором сильной щелочи (КОН или Na. OH) Все, что ниже 8, 4 - общая кислотность, что ниже р. Н 4, 3 - свободная кислотность. Измеряется в мг-экв/л титрующей щелочи. При p. H < 4, 3 титруются сильные кислоты. При p. H от 4, 3 до 8, 4 титруются слабые кислоты и основания. При p. H>8, 4 титруются сильные основания.
b. Щелочность - способность нейтрализовать сильные кислоты. Определяется прямым титрованием воды раствором сильной кислоты (HCl) Все, что выше p. H 4, 3 -общая щелочность, что выше р. Н 8, 4 - свободная щелочность. При р. Н = 4, 3 проба воды имеет нулевую щелочность. Измеряется в мг-экв/л титрующей кислоты. c. Кислотность - способность нейтрализовать сильные щелочи. Определяется прямым титрованием воды раствором сильной щелочи (КОН или Na. OH) Все, что ниже 8, 4 - общая кислотность, что ниже р. Н 4, 3 - свободная кислотность. Измеряется в мг-экв/л титрующей щелочи. При p. H < 4, 3 титруются сильные кислоты. При p. H от 4, 3 до 8, 4 титруются слабые кислоты и основания. При p. H>8, 4 титруются сильные основания.
 Cэ, ксо, Cэ, аск и Cэ, ОК - суммы концентраций катионов сильных оснований, анионов сильных кислот и анионов органических кислот, соответственно, в мг-экв/л. Поэтому: Щелочность ≈ p. H + сумма слабых кислот Щелочность ≈ = карбонатная щелочность Щелочность используется для: 1 - расчета содержания карбонатов, 2 -при выборе воды для ирригации, 3 - при очистке грязных вод.
Cэ, ксо, Cэ, аск и Cэ, ОК - суммы концентраций катионов сильных оснований, анионов сильных кислот и анионов органических кислот, соответственно, в мг-экв/л. Поэтому: Щелочность ≈ p. H + сумма слабых кислот Щелочность ≈ = карбонатная щелочность Щелочность используется для: 1 - расчета содержания карбонатов, 2 -при выборе воды для ирригации, 3 - при очистке грязных вод.
 6. Окислительно-восстановительный потенциал – способность воды как окислителя – восстановителя. • Измеряется: 1 - Eh в вольтах или милливольтах При + недостаток электронов (окислитель) При – избыток электронов (восстановитель) 2 - pe в безразмерных величинах F -постоянная Фарадея (96484, 56 Кл/моль или 23, 6 ккал/В г экв); R -газовая постоянная (1, 987 10 -3 ккал/град моль), T- абсолютная температура, градусы Кельвина. При 250 С pe = 16, 9 Eh и Eh = 0, 059 pe • Методы опробования Прямо в месте залегания, или хранить пробы без дегазации и контакта с O 2. • Методы определения: – с помощью электродов (стандартного водородного, каломельного, хлорсеребряного и др. ) – Eh-метры – по родекс-парам.
6. Окислительно-восстановительный потенциал – способность воды как окислителя – восстановителя. • Измеряется: 1 - Eh в вольтах или милливольтах При + недостаток электронов (окислитель) При – избыток электронов (восстановитель) 2 - pe в безразмерных величинах F -постоянная Фарадея (96484, 56 Кл/моль или 23, 6 ккал/В г экв); R -газовая постоянная (1, 987 10 -3 ккал/град моль), T- абсолютная температура, градусы Кельвина. При 250 С pe = 16, 9 Eh и Eh = 0, 059 pe • Методы опробования Прямо в месте залегания, или хранить пробы без дегазации и контакта с O 2. • Методы определения: – с помощью электродов (стандартного водородного, каломельного, хлорсеребряного и др. ) – Eh-метры – по родекс-парам.
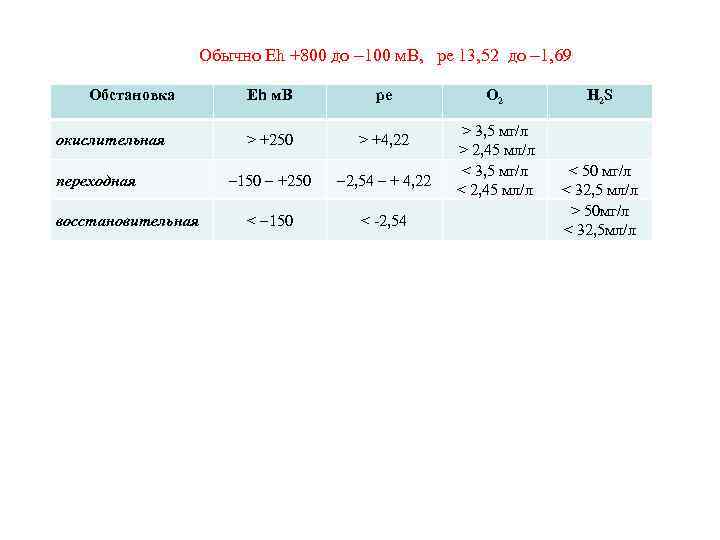 Обычно Eh +800 до 100 м. В, pe 13, 52 до 1, 69 Обстановка окислительная переходная восстановительная Eh м. В pe > +250 > +4, 22 150 +250 2, 54 + 4, 22 < 150 < -2, 54 О 2 > 3, 5 мг/л > 2, 45 мл/л < 3, 5 мг/л < 2, 45 мл/л H 2 S < 50 мг/л < 32, 5 мл/л > 50 мг/л < 32, 5 мл/л
Обычно Eh +800 до 100 м. В, pe 13, 52 до 1, 69 Обстановка окислительная переходная восстановительная Eh м. В pe > +250 > +4, 22 150 +250 2, 54 + 4, 22 < 150 < -2, 54 О 2 > 3, 5 мг/л > 2, 45 мл/л < 3, 5 мг/л < 2, 45 мл/л H 2 S < 50 мг/л < 32, 5 мл/л > 50 мг/л < 32, 5 мл/л
 7. Жесткость - способность образовывать нерастворимые соли при изменении технологических условий вследствие присутствия щелочно-земельных и поливалентных металлов. • • Измеряется в мг-экв/л. Опробуют: Хранть не более 1 суток, пресные воды 2 суток Различают: общую, устранимую и постоянную жесткость. Методы определения − Общая жесткость (ОЖ): a. - взаимодействием с жирными кислотами: 2 Na(ЖК) + Ca. SO 4 = Ca(ЖК)2 + Na 2 SO 4 b. - по ГОСТ’у 4151 -72 титрованием реактивом трилон Б (двунатриевая соль этилендиаминтетрауксусной кислоты). c. – расчетный метод, как сумма солей Ca, Mg, Ba, (Fe) − Устранимая жесткость (УЖ): a. – по изменениею ОЖ при кипячении в течение 1 часа. Ca(HCO 3)2 Ca. CO 3 + H 2 O + CO 2. b. – расчетный метод – меньшая из величин общей жесткости и карбонатной щелочности. − Постоянная жесткость (ПЖ): ПЖ= ОЖ -УЖ.
7. Жесткость - способность образовывать нерастворимые соли при изменении технологических условий вследствие присутствия щелочно-земельных и поливалентных металлов. • • Измеряется в мг-экв/л. Опробуют: Хранть не более 1 суток, пресные воды 2 суток Различают: общую, устранимую и постоянную жесткость. Методы определения − Общая жесткость (ОЖ): a. - взаимодействием с жирными кислотами: 2 Na(ЖК) + Ca. SO 4 = Ca(ЖК)2 + Na 2 SO 4 b. - по ГОСТ’у 4151 -72 титрованием реактивом трилон Б (двунатриевая соль этилендиаминтетрауксусной кислоты). c. – расчетный метод, как сумма солей Ca, Mg, Ba, (Fe) − Устранимая жесткость (УЖ): a. – по изменениею ОЖ при кипячении в течение 1 часа. Ca(HCO 3)2 Ca. CO 3 + H 2 O + CO 2. b. – расчетный метод – меньшая из величин общей жесткости и карбонатной щелочности. − Постоянная жесткость (ПЖ): ПЖ= ОЖ -УЖ.
 Качество природных вод как функция их жесткости по О. А. Алекину. Вода очень мягкая Жесткость, мг-экв/л менее 1, 5 мягкая 1, 5 -3, 0 умеренно мягкая 3, 0 -6, 0 жесткая 6, 0 -9, 0 Очень жесткая более 6, 0 По ГОСТ 2874 -82 общая жесткость питьевой воды должна быть меньше 7 мг-экв/л.
Качество природных вод как функция их жесткости по О. А. Алекину. Вода очень мягкая Жесткость, мг-экв/л менее 1, 5 мягкая 1, 5 -3, 0 умеренно мягкая 3, 0 -6, 0 жесткая 6, 0 -9, 0 Очень жесткая более 6, 0 По ГОСТ 2874 -82 общая жесткость питьевой воды должна быть меньше 7 мг-экв/л.
 8. Агрессивность - способность растворять и разрушать породы и строительные материалы вследствие физико-химического воздействия. • Различают агрессивности: кислородную, общекислотную, углекислотную, сульфатную, магнезиальную. Кислородная агрессивность вызвана присутствием в воде растворённого O 2, опасна металлическим конструкциям (металлическим сваям, водопроводным, газопроводным трубам и т. д. ). Общекислотная агрессивность связана с низкой p. H (< 6, 8), опасна к карбонат содержащим материалам. Углекислотная агрессивность определяется присутствием агрессивной CO 2, (более 3 -8 мг/л) опасна для известняков и бетона. Сульфатная агрессииность при большом содержании SO 42 - , опасна для обычных цементов при содержании > 250 мг/л, а при сульфатостойких — > 4000 мг/л Магнезиальная агрессивность возникает при высоких содержаниях Mg 2+ , до 750 мг/л и более • • Размерность – обычно содержание агрессивного агента. Методы определения: 1 - Расчетные методы. 2 - Экспериментальные.
8. Агрессивность - способность растворять и разрушать породы и строительные материалы вследствие физико-химического воздействия. • Различают агрессивности: кислородную, общекислотную, углекислотную, сульфатную, магнезиальную. Кислородная агрессивность вызвана присутствием в воде растворённого O 2, опасна металлическим конструкциям (металлическим сваям, водопроводным, газопроводным трубам и т. д. ). Общекислотная агрессивность связана с низкой p. H (< 6, 8), опасна к карбонат содержащим материалам. Углекислотная агрессивность определяется присутствием агрессивной CO 2, (более 3 -8 мг/л) опасна для известняков и бетона. Сульфатная агрессииность при большом содержании SO 42 - , опасна для обычных цементов при содержании > 250 мг/л, а при сульфатостойких — > 4000 мг/л Магнезиальная агрессивность возникает при высоких содержаниях Mg 2+ , до 750 мг/л и более • • Размерность – обычно содержание агрессивного агента. Методы определения: 1 - Расчетные методы. 2 - Экспериментальные.
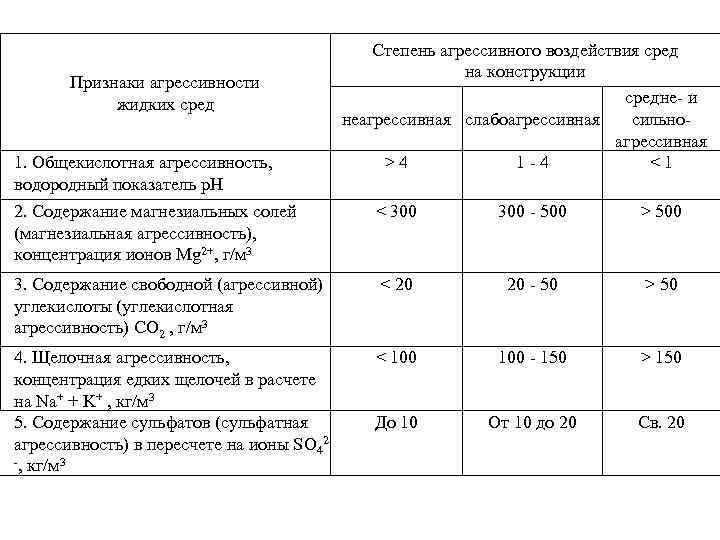 Признаки агрессивности жидких сред 1. Общекислотная агрессивность, водородный показатель р. Н Степень агрессивного воздействия сред на конструкции средне- и сильнонеагрессивная слабоагрессивная >4 1 -4 <1 2. Содержание магнезиальных солей (магнезиальная агрессивность), концентрация ионов Mg 2+, г/м 3 < 300 - 500 > 500 3. Содержание свободной (агрессивной) углекислоты (углекислотная агрессивность) СО 2 , г/м 3 < 20 20 - 50 > 50 4. Щелочная агрессивность, концентрация едких щелочей в расчете на Na+ + K+ , кг/м 3 5. Содержание сульфатов (сульфатная агрессивность) в пересчете на ионы SO 42 -, кг/м 3 < 100 - 150 > 150 До 10 От 10 до 20 Св. 20
Признаки агрессивности жидких сред 1. Общекислотная агрессивность, водородный показатель р. Н Степень агрессивного воздействия сред на конструкции средне- и сильнонеагрессивная слабоагрессивная >4 1 -4 <1 2. Содержание магнезиальных солей (магнезиальная агрессивность), концентрация ионов Mg 2+, г/м 3 < 300 - 500 > 500 3. Содержание свободной (агрессивной) углекислоты (углекислотная агрессивность) СО 2 , г/м 3 < 20 20 - 50 > 50 4. Щелочная агрессивность, концентрация едких щелочей в расчете на Na+ + K+ , кг/м 3 5. Содержание сульфатов (сульфатная агрессивность) в пересчете на ионы SO 42 -, кг/м 3 < 100 - 150 > 150 До 10 От 10 до 20 Св. 20
 Физические свойства – характеризуют свойства воды как жидкого раствора. 1. Давление - сила, уравновешивающая давление извне. • Единицы измерения: 1 МПа=1 106 Н/м 2=10, 19 ат= 9, 87 атм= 10 бар Атмосфера: техническая 1 ат=0, 980665 бар =98, 0665 к. Па физическая 1 атм=1, 01325 бар = 101, 325 к. Па • Методы определения: в месте залегания манометрами. На малых глубинах, как правило, игнорируется. Влияет на растворимость и содержание газовых компонентов. Манометр скважинный автономный МИКОН-107 для регистрации значений давления и температуры по стволу скважины и (или) в любой его точке. Диапазоны измерений избыточного давления, кгс/см 2: 0… 160; 250; 400; 600 Рабочий диапазон температур, °C 25…+100 Габаритные размеры изделия: - диаметр, не более 25 мм - длина, не более 1051 мм - масса не более 5 кг
Физические свойства – характеризуют свойства воды как жидкого раствора. 1. Давление - сила, уравновешивающая давление извне. • Единицы измерения: 1 МПа=1 106 Н/м 2=10, 19 ат= 9, 87 атм= 10 бар Атмосфера: техническая 1 ат=0, 980665 бар =98, 0665 к. Па физическая 1 атм=1, 01325 бар = 101, 325 к. Па • Методы определения: в месте залегания манометрами. На малых глубинах, как правило, игнорируется. Влияет на растворимость и содержание газовых компонентов. Манометр скважинный автономный МИКОН-107 для регистрации значений давления и температуры по стволу скважины и (или) в любой его точке. Диапазоны измерений избыточного давления, кгс/см 2: 0… 160; 250; 400; 600 Рабочий диапазон температур, °C 25…+100 Габаритные размеры изделия: - диаметр, не более 25 мм - длина, не более 1051 мм - масса не более 5 кг
 2. Температура -теплота, которую природная вода способна отдать. • Единицы измерения: o. C = 273, 16 K =5/9(o. F-32). • Методы определения: в месте залегания ленивым или максимальным термометром. Влияет на содержание минеральных компонентов Pи. T определяют фазовое состояние раствора Na. CI и др. соли критическую точку поднимают и по T и по P. CO 2 и др. газы критическую точку опускают по T и поднимает по P. Конец лекции 2 3. Сжимаемость - способность уплотнения под нагрузкой внешнего давления. • Единицы измерения: Па-1 , , ; V= PV • Методы определения: экспериментальные или рассчетные. пресной воды при 200 С равна 0, 5 ГПа-1. Зависит: от P: 100 V/V=1% при P=20 МПа, на глубине > 2 км. от T: пресной воды при P=41 МПа и T= 930 С = 0, 4 ГПа-1. от состава: минеральные увеличивают или уменьшают, газовые только увеличивают: пв. = пр. (1 -0, 0495 Q)
2. Температура -теплота, которую природная вода способна отдать. • Единицы измерения: o. C = 273, 16 K =5/9(o. F-32). • Методы определения: в месте залегания ленивым или максимальным термометром. Влияет на содержание минеральных компонентов Pи. T определяют фазовое состояние раствора Na. CI и др. соли критическую точку поднимают и по T и по P. CO 2 и др. газы критическую точку опускают по T и поднимает по P. Конец лекции 2 3. Сжимаемость - способность уплотнения под нагрузкой внешнего давления. • Единицы измерения: Па-1 , , ; V= PV • Методы определения: экспериментальные или рассчетные. пресной воды при 200 С равна 0, 5 ГПа-1. Зависит: от P: 100 V/V=1% при P=20 МПа, на глубине > 2 км. от T: пресной воды при P=41 МПа и T= 930 С = 0, 4 ГПа-1. от состава: минеральные увеличивают или уменьшают, газовые только увеличивают: пв. = пр. (1 -0, 0495 Q)
 4. Плотность - масса единицы объема воды. • Единицы измерения: г/мл, кг/л или кг/м 3. Удельный вес в Н/м 3 γ = 9, 80665ρ, в к. Г (кгс) γ = ρ • Методы определения: гравиметрически, ареометром Зависит: P увеличивает T до 40 C увеличивает, потом уменьшает Соли увеличивают (до 7 г/л - 1 кг/л, 35 г/л - 1, 021, 03 кг/л, при 100 г/л 1, 07 кг/л, а при 300 г/л - 1, 2 -1, 3 кг/л) ρ =1+ 0, 0063 m 2+ 0, 068 m, где ρ - плотность в г/мл, m- минерализация в г/кг 5. Вязкость - сила внутреннего трения воды. • Единицы измерения: динамическая вязкость Па с = Н с/м 2 =кг м-1 с-1= 10 П (пуаз), текучести φ =1/η Кинематическая вязкость ν = η/ρ, 1 мм 2/с=10 -6 м 2/с = 1 с. Ст • Методы определения: вискозиметры. Зависит от температуры, минерализации и состава
4. Плотность - масса единицы объема воды. • Единицы измерения: г/мл, кг/л или кг/м 3. Удельный вес в Н/м 3 γ = 9, 80665ρ, в к. Г (кгс) γ = ρ • Методы определения: гравиметрически, ареометром Зависит: P увеличивает T до 40 C увеличивает, потом уменьшает Соли увеличивают (до 7 г/л - 1 кг/л, 35 г/л - 1, 021, 03 кг/л, при 100 г/л 1, 07 кг/л, а при 300 г/л - 1, 2 -1, 3 кг/л) ρ =1+ 0, 0063 m 2+ 0, 068 m, где ρ - плотность в г/мл, m- минерализация в г/кг 5. Вязкость - сила внутреннего трения воды. • Единицы измерения: динамическая вязкость Па с = Н с/м 2 =кг м-1 с-1= 10 П (пуаз), текучести φ =1/η Кинематическая вязкость ν = η/ρ, 1 мм 2/с=10 -6 м 2/с = 1 с. Ст • Методы определения: вискозиметры. Зависит от температуры, минерализации и состава
 6. Электропроводимость – способность проводить электричество. G =1/R. • Единицы измерения: удельная проводимостью в См/м. 1 мо (hmo) =1 См см-1 • Методы определения: кондуктометрами или солемерами. В пресных от 3 10 -5 до 3 10 -3 См м-1, в рассолах до 5 10 -3 -1, 2 См м-1. Т увеличивает. 7. Радиоактивность – способность испускать частицы , и гамма-лучи растворенных в них нестабильных, радиоактивных изотопов (40 K, 87 Rb, продукты распада 238 U и 232 Th и др). • Единицы измерения: удельная радиоактивность в Бк/м 3. (1 эман = 10 -10 Ки/л = 3700 Бк/м 3) • Методы опробования: Пробы без консервации хранят не более 4 часов, при подкислении до р. Н < 1 и при температуре 0 -8°С - до 4 суток. • Методы определения: радиометры. Измерение общей альфа-активности в питьевой воде регламентируется ГОСТ’ом Р 51730 -2001.
6. Электропроводимость – способность проводить электричество. G =1/R. • Единицы измерения: удельная проводимостью в См/м. 1 мо (hmo) =1 См см-1 • Методы определения: кондуктометрами или солемерами. В пресных от 3 10 -5 до 3 10 -3 См м-1, в рассолах до 5 10 -3 -1, 2 См м-1. Т увеличивает. 7. Радиоактивность – способность испускать частицы , и гамма-лучи растворенных в них нестабильных, радиоактивных изотопов (40 K, 87 Rb, продукты распада 238 U и 232 Th и др). • Единицы измерения: удельная радиоактивность в Бк/м 3. (1 эман = 10 -10 Ки/л = 3700 Бк/м 3) • Методы опробования: Пробы без консервации хранят не более 4 часов, при подкислении до р. Н < 1 и при температуре 0 -8°С - до 4 суток. • Методы определения: радиометры. Измерение общей альфа-активности в питьевой воде регламентируется ГОСТ’ом Р 51730 -2001.
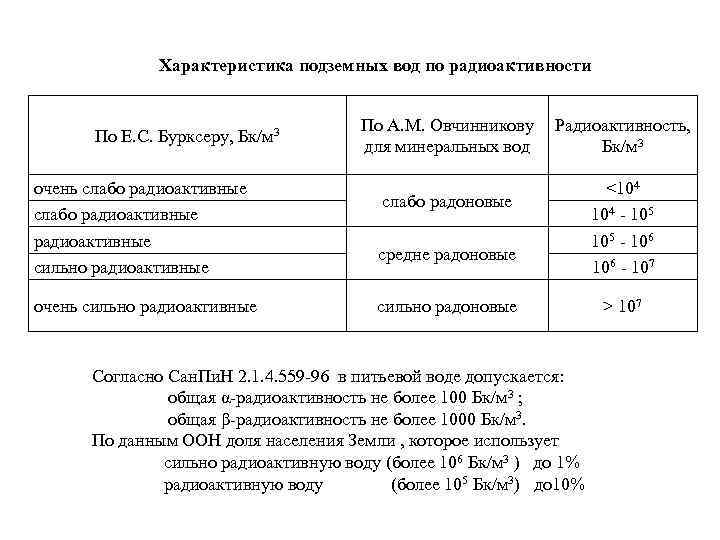 Характеристика подземных вод по радиоактивности По Е. С. Бурксеру, Бк/м 3 очень слабо радиоактивные сильно радиоактивные очень сильно радиоактивные По А. М. Овчинникову для минеральных вод Радиоактивность, Бк/м 3 слабо радоновые средне радоновые сильно радоновые Согласно Сан. Пи. Н 2. 1. 4. 559 -96 в питьевой воде допускается: общая α-радиоактивность не более 100 Бк/м 3 ; общая β-радиоактивность не более 1000 Бк/м 3. По данным ООН доля населения Земли , которое использует сильно радиоактивную воду (более 106 Бк/м 3 ) до 1% радиоактивную воду (более 105 Бк/м 3) до 10% <104 - 105 - 106 - 107 > 107
Характеристика подземных вод по радиоактивности По Е. С. Бурксеру, Бк/м 3 очень слабо радиоактивные сильно радиоактивные очень сильно радиоактивные По А. М. Овчинникову для минеральных вод Радиоактивность, Бк/м 3 слабо радоновые средне радоновые сильно радоновые Согласно Сан. Пи. Н 2. 1. 4. 559 -96 в питьевой воде допускается: общая α-радиоактивность не более 100 Бк/м 3 ; общая β-радиоактивность не более 1000 Бк/м 3. По данным ООН доля населения Земли , которое использует сильно радиоактивную воду (более 106 Бк/м 3 ) до 1% радиоактивную воду (более 105 Бк/м 3) до 10% <104 - 105 - 106 - 107 > 107
 Гидрохимические классификации природных вод По преобладанию: С. А. Щукарева (49 типов), Н. И. Толстихина (100 типов), О. С. Джикия (625 типов) и т. д. Терапевт и бальнеолог Михаил Георгиевич Курлов (1859— 1932) предложил в 1930 г. : Формула Куллова: CO 2 0, 012, M 0, 20 (>5%-экв) Классификация С. А. Щукарева предложена в 1934 г. В основе формула М. Г. Курлова. (>25 экв%. ) 49 классов. Из них главные 17, 33 и 45.
Гидрохимические классификации природных вод По преобладанию: С. А. Щукарева (49 типов), Н. И. Толстихина (100 типов), О. С. Джикия (625 типов) и т. д. Терапевт и бальнеолог Михаил Георгиевич Курлов (1859— 1932) предложил в 1930 г. : Формула Куллова: CO 2 0, 012, M 0, 20 (>5%-экв) Классификация С. А. Щукарева предложена в 1934 г. В основе формула М. Г. Курлова. (>25 экв%. ) 49 классов. Из них главные 17, 33 и 45.
 Классификация О. С. Джикии предложена в 1963 В основе формула М. Г. Курлова (более 1 экв%. ) 625 классов
Классификация О. С. Джикии предложена в 1963 В основе формула М. Г. Курлова (более 1 экв%. ) 625 классов
 По солевому составу: Ч. Пальмера 1911 г. , В. А. Сулина (1946 г. ) , О. А. Алекина (1948) и М. Г. Валяшко (1935 -1955 г), . Классификация Ч. Пальмера (1911) Сильные основания (щелочи) Na+ и K+; сильные кислоты. Cl- и SO 42 слабые кислоты – и Слабые основания Очень слабые основания (щелочные земли) (тяжелые металлы) Ca 2+ и Mg 2+ Fe 2+, Cu 2+, Al 3+ 1 -ой солености 2 -ой солености 3 -ей солености 1 -ой щелочности 2 -ой щелочности 3 -ей щелочности 1 -СК<СО, 2 - СК=СО, 3 -СК>СО, 4 - СК=СО+Сл. О, 5 - СК>СО+Сл. О Классификация В. А. Сулина (1946) Na+ > Cl. Cl- > Na+ (Na+-Cl-)>SO 42 - Гидрокарбонатно-натриевые (Na+-Cl-)
По солевому составу: Ч. Пальмера 1911 г. , В. А. Сулина (1946 г. ) , О. А. Алекина (1948) и М. Г. Валяшко (1935 -1955 г), . Классификация Ч. Пальмера (1911) Сильные основания (щелочи) Na+ и K+; сильные кислоты. Cl- и SO 42 слабые кислоты – и Слабые основания Очень слабые основания (щелочные земли) (тяжелые металлы) Ca 2+ и Mg 2+ Fe 2+, Cu 2+, Al 3+ 1 -ой солености 2 -ой солености 3 -ей солености 1 -ой щелочности 2 -ой щелочности 3 -ей щелочности 1 -СК<СО, 2 - СК=СО, 3 -СК>СО, 4 - СК=СО+Сл. О, 5 - СК>СО+Сл. О Классификация В. А. Сулина (1946) Na+ > Cl. Cl- > Na+ (Na+-Cl-)>SO 42 - Гидрокарбонатно-натриевые (Na+-Cl-)
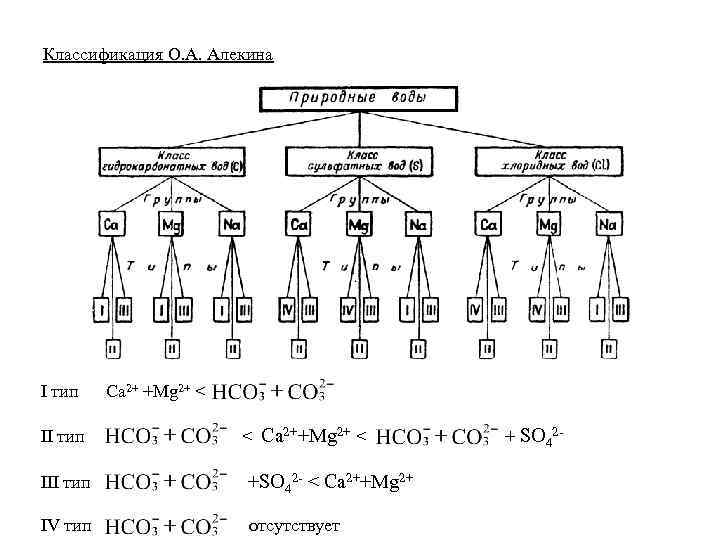 Классификация О. А. Алекина I тип II тип Ca 2+ +Mg 2+ < < Ca 2++Mg 2+ < III тип +SO 42 - < Ca 2++Mg 2+ IV тип отсутствует + SO 42 -
Классификация О. А. Алекина I тип II тип Ca 2+ +Mg 2+ < < Ca 2++Mg 2+ < III тип +SO 42 - < Ca 2++Mg 2+ IV тип отсутствует + SO 42 -
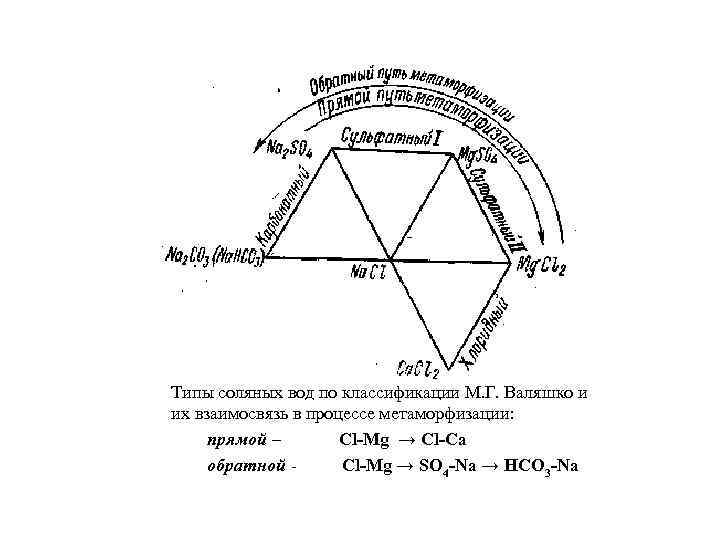 Типы соляных вод по классификации М. Г. Валяшко и их взаимосвязь в процессе метаморфизации: прямой – Cl-Mg → Cl-Ca обратной Cl-Mg → SO 4 -Na → HCO 3 -Na
Типы соляных вод по классификации М. Г. Валяшко и их взаимосвязь в процессе метаморфизации: прямой – Cl-Mg → Cl-Ca обратной Cl-Mg → SO 4 -Na → HCO 3 -Na
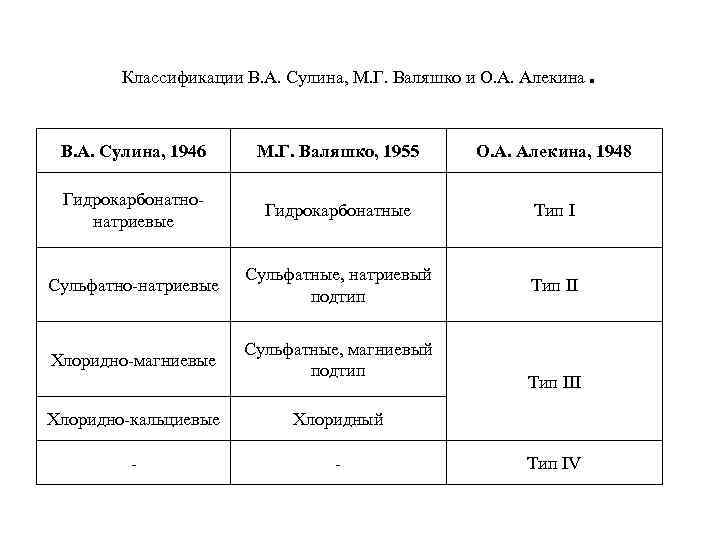 Классификации В. А. Сулина, М. Г. Валяшко и О. А. Алекина . В. А. Сулина, 1946 М. Г. Валяшко, 1955 О. А. Алекина, 1948 Гидрокарбонатнонатриевые Гидрокарбонатные Тип I Сульфатно-натриевые Сульфатные, натриевый подтип Тип II Хлоридно-магниевые Сульфатные, магниевый подтип Хлоридно-кальциевые Хлоридный - - Тип III Тип IV
Классификации В. А. Сулина, М. Г. Валяшко и О. А. Алекина . В. А. Сулина, 1946 М. Г. Валяшко, 1955 О. А. Алекина, 1948 Гидрокарбонатнонатриевые Гидрокарбонатные Тип I Сульфатно-натриевые Сульфатные, натриевый подтип Тип II Хлоридно-магниевые Сульфатные, магниевый подтип Хлоридно-кальциевые Хлоридный - - Тип III Тип IV
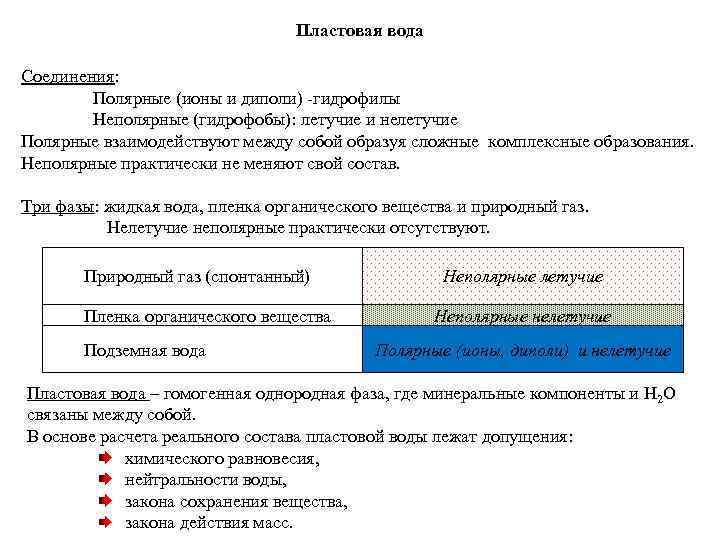 Пластовая вода Соединения: Полярные (ионы и диполи) -гидрофилы Неполярные (гидрофобы): летучие и нелетучие Полярные взаимодействуют между собой образуя сложные комплексные образования. Неполярные практически не меняют свой состав. Три фазы: жидкая вода, пленка органического вещества и природный газ. Нелетучие неполярные практически отсутствуют. Природный газ (спонтанный) Пленка органического вещества Подземная вода Неполярные летучие Неполярные нелетучие Полярные (ионы, диполи) и нелетучие Пластовая вода – гомогенная однородная фаза, где минеральные компоненты и H 2 O связаны между собой. В основе расчета реального состава пластовой воды лежат допущения: химического равновесия, нейтральности воды, закона сохранения вещества, закона действия масс.
Пластовая вода Соединения: Полярные (ионы и диполи) -гидрофилы Неполярные (гидрофобы): летучие и нелетучие Полярные взаимодействуют между собой образуя сложные комплексные образования. Неполярные практически не меняют свой состав. Три фазы: жидкая вода, пленка органического вещества и природный газ. Нелетучие неполярные практически отсутствуют. Природный газ (спонтанный) Пленка органического вещества Подземная вода Неполярные летучие Неполярные нелетучие Полярные (ионы, диполи) и нелетучие Пластовая вода – гомогенная однородная фаза, где минеральные компоненты и H 2 O связаны между собой. В основе расчета реального состава пластовой воды лежат допущения: химического равновесия, нейтральности воды, закона сохранения вещества, закона действия масс.


