oxidy_soli_osnovania_kisloty.ppt
- Количество слайдов: 17
 Химические свойства опорные конспекты Оксиды, основания, кислоты и соли
Химические свойства опорные конспекты Оксиды, основания, кислоты и соли
 КИСЛОТЫ 1 Действие кислот на индикаторы HCl → H+ + Cl- метилоранж красный H 2 SO 4→ H+ + HSO 4 - ; HSO 4 - ↔ H+ + SO 42 - универсальный красный Реакция нейтрализации 2 Н+ + ОН- = Н 2 О, ∆Н < 0 (можно увидеть только с индикатором) 2 Fe(OH)3(н) + 6 H+(сильная кислота) = 2 Fe 3+ + 3 H 2 O, ∆Н < 0 3 Соль (р, м, н) + кислота → соль + кислота (↓ или ↑) 2 H+ + Si. O 32 -→H 2 Si. O 3↓; Са. СО 3 + 2 Н+→Са 2+ + Н 2 О + СО 2↑ *С солями (н, м) реагируют только сильные кислоты 4 Кислота + основный оксид = соль + H 2 O 3 Н 2 SО 4 + Fe 2 O 3 = Fe 2(SO 4)3 + 3 Н 2 О 6 H+ + Fe 2 O 3 = 2 Fe 3+ + 3 H 2 O 5 Кислота + металл (в ряду активности до Н 2) = соль + Н 2↑, ∆Н < 0 Zn + 2 H+(кроме HNO 3) = Zn 2+ + Н 2↑, ∆Н < 0
КИСЛОТЫ 1 Действие кислот на индикаторы HCl → H+ + Cl- метилоранж красный H 2 SO 4→ H+ + HSO 4 - ; HSO 4 - ↔ H+ + SO 42 - универсальный красный Реакция нейтрализации 2 Н+ + ОН- = Н 2 О, ∆Н < 0 (можно увидеть только с индикатором) 2 Fe(OH)3(н) + 6 H+(сильная кислота) = 2 Fe 3+ + 3 H 2 O, ∆Н < 0 3 Соль (р, м, н) + кислота → соль + кислота (↓ или ↑) 2 H+ + Si. O 32 -→H 2 Si. O 3↓; Са. СО 3 + 2 Н+→Са 2+ + Н 2 О + СО 2↑ *С солями (н, м) реагируют только сильные кислоты 4 Кислота + основный оксид = соль + H 2 O 3 Н 2 SО 4 + Fe 2 O 3 = Fe 2(SO 4)3 + 3 Н 2 О 6 H+ + Fe 2 O 3 = 2 Fe 3+ + 3 H 2 O 5 Кислота + металл (в ряду активности до Н 2) = соль + Н 2↑, ∆Н < 0 Zn + 2 H+(кроме HNO 3) = Zn 2+ + Н 2↑, ∆Н < 0
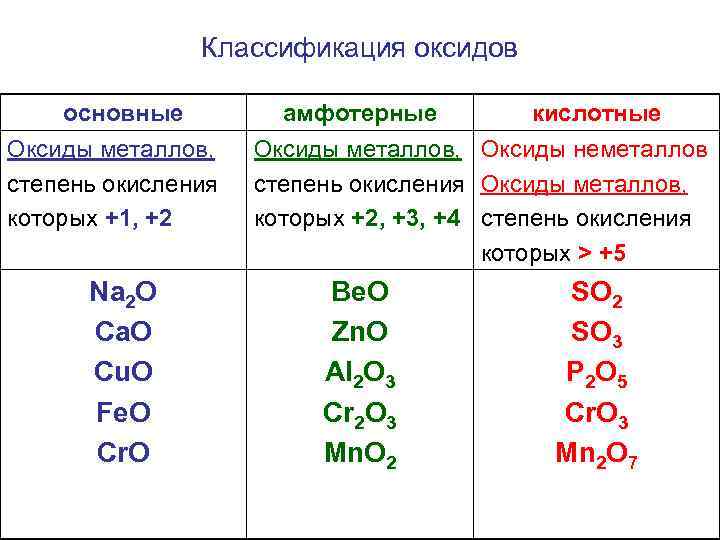 Классификация оксидов основные Оксиды металлов, степень окисления которых +1, +2 Na 2 O Ca. O Cu. O Fe. O Cr. O амфотерные кислотные Оксиды металлов, Оксиды неметаллов степень окисления Оксиды металлов, которых +2, +3, +4 степень окисления которых > +5 Be. O Zn. O Al 2 O 3 Cr 2 O 3 Mn. O 2 SO 3 P 2 O 5 Cr. O 3 Mn 2 O 7
Классификация оксидов основные Оксиды металлов, степень окисления которых +1, +2 Na 2 O Ca. O Cu. O Fe. O Cr. O амфотерные кислотные Оксиды металлов, Оксиды неметаллов степень окисления Оксиды металлов, которых +2, +3, +4 степень окисления которых > +5 Be. O Zn. O Al 2 O 3 Cr 2 O 3 Mn. O 2 SO 3 P 2 O 5 Cr. O 3 Mn 2 O 7
 1. Кислотные свойства проявляет оксид: 1) Si. O 2 2) Al 2 O 3 3) CO 4) Ba. O 2. Оксид с наиболее выраженными основными свойствами образует: 1) Be 2) Mg 3) Ba 4) Zn 3. Установите соответствие между формулой вещества и классом соединений, к которому это вещество принадлежит: А) оксид азота (II) 1) кислотный оксид Б) оксид кальция 2) основный оксид В) оксид серы (IV) 3) несолеобразующий оксид Г) оксид углерода (II) 4) амфотерный оксид
1. Кислотные свойства проявляет оксид: 1) Si. O 2 2) Al 2 O 3 3) CO 4) Ba. O 2. Оксид с наиболее выраженными основными свойствами образует: 1) Be 2) Mg 3) Ba 4) Zn 3. Установите соответствие между формулой вещества и классом соединений, к которому это вещество принадлежит: А) оксид азота (II) 1) кислотный оксид Б) оксид кальция 2) основный оксид В) оксид серы (IV) 3) несолеобразующий оксид Г) оксид углерода (II) 4) амфотерный оксид
 Опорный конспект (ОК) Основные оксиды Основный оксид+Н 2 О=щелочь ОКСИДЫ Кислотные оксиды Кислотный оксид+Н 2 О=кислота Li 2 O + H 2 O = 2 Li. OH Р 2 О 5 + 3 Н 2 О = 2 Н 3 РО 4 Основный оксид + кислотный оксид = соль Кислотный оксид + основный оксид = соль Li 2 O + N 2 O 5 = Li 3 PO 4 Р 2 О 5 + Ва. О = Ва 3(РО 4)2 Основный оксид + кислота = соль Кислотный оксид + щелочь = соль + вода Li 2 O + Н 3 РО 4 = Li 3 PO 4 + Н 2 О Р 2 О 5 + 3 Ва(ОН)2 = Ва 3(РО 4)2↓ + 3 Н 2 О **Кислотный оксид + соль = соль + кислотный оксид ↑ Na 2 CO 3 + Si. O 2 = Na 2 Si. O 3 + CO 2↑ Применяется в производстве стекла
Опорный конспект (ОК) Основные оксиды Основный оксид+Н 2 О=щелочь ОКСИДЫ Кислотные оксиды Кислотный оксид+Н 2 О=кислота Li 2 O + H 2 O = 2 Li. OH Р 2 О 5 + 3 Н 2 О = 2 Н 3 РО 4 Основный оксид + кислотный оксид = соль Кислотный оксид + основный оксид = соль Li 2 O + N 2 O 5 = Li 3 PO 4 Р 2 О 5 + Ва. О = Ва 3(РО 4)2 Основный оксид + кислота = соль Кислотный оксид + щелочь = соль + вода Li 2 O + Н 3 РО 4 = Li 3 PO 4 + Н 2 О Р 2 О 5 + 3 Ва(ОН)2 = Ва 3(РО 4)2↓ + 3 Н 2 О **Кислотный оксид + соль = соль + кислотный оксид ↑ Na 2 CO 3 + Si. O 2 = Na 2 Si. O 3 + CO 2↑ Применяется в производстве стекла
 Выберите из перечня веществ основный оксид. Напишите для него уравнения возможных реакций с перечисленными ниже веществами: вода, оксид азота (V), серная кислота, гидроксид кальция, оксид железа (II), оксид калия, карбонат натрия
Выберите из перечня веществ основный оксид. Напишите для него уравнения возможных реакций с перечисленными ниже веществами: вода, оксид азота (V), серная кислота, гидроксид кальция, оксид железа (II), оксид калия, карбонат натрия
 Выберите из перечня веществ кислотный оксид. Напишите для него уравнения возможных реакций с перечисленными ниже веществами: вода, оксид азота (V), серная кислота, гидроксид кальция, оксид железа (II), оксид калия, карбонат натрия
Выберите из перечня веществ кислотный оксид. Напишите для него уравнения возможных реакций с перечисленными ниже веществами: вода, оксид азота (V), серная кислота, гидроксид кальция, оксид железа (II), оксид калия, карбонат натрия
 ОСНОВАНИЯ Действие щелочей на индикаторы 1 Li. OH → Li+ + OH- фенолфталеиновый в щелочах малиновый Са(ОН)2→Са. ОН++ОН-; Са. ОН+ ↔Са 2++ОН- универсальный синий Реакция нейтрализации 2 Н+ + ОН- = Н 2 О, ∆Н < 0 (можно увидеть только с индикатором) 2 Fe(OH)3(н) + 6 H+(сильная кислота) = 2 Fe 3+ + 3 H 2 O, ∆Н < 0 Щелочь (р) + соль(р) = н. основание↓ + соль (р) 3 3 Na. OH + Fe. Cl 3 = Fe(OH)3↓ + 3 Na. Cl Fe 3+ + 3 OH- = Fe(OH)3↓ красно-бурый осадок, ржавчина Щелочь + кислотный оксид = соль + Н 2 О 4 3 Са(ОН)2 + Р 2 О 5 = Са 3(РО 4)2↓ + 3 Н 2 О 3 Са 2+ + 6 ОН- + Р 2 О 5 = Са 3(РО 4)2↓ + 3 Н 2 О
ОСНОВАНИЯ Действие щелочей на индикаторы 1 Li. OH → Li+ + OH- фенолфталеиновый в щелочах малиновый Са(ОН)2→Са. ОН++ОН-; Са. ОН+ ↔Са 2++ОН- универсальный синий Реакция нейтрализации 2 Н+ + ОН- = Н 2 О, ∆Н < 0 (можно увидеть только с индикатором) 2 Fe(OH)3(н) + 6 H+(сильная кислота) = 2 Fe 3+ + 3 H 2 O, ∆Н < 0 Щелочь (р) + соль(р) = н. основание↓ + соль (р) 3 3 Na. OH + Fe. Cl 3 = Fe(OH)3↓ + 3 Na. Cl Fe 3+ + 3 OH- = Fe(OH)3↓ красно-бурый осадок, ржавчина Щелочь + кислотный оксид = соль + Н 2 О 4 3 Са(ОН)2 + Р 2 О 5 = Са 3(РО 4)2↓ + 3 Н 2 О 3 Са 2+ + 6 ОН- + Р 2 О 5 = Са 3(РО 4)2↓ + 3 Н 2 О
 Выберите из перечня веществ основание (щелочь). Напишите для него уравнения возможных реакций с перечисленными ниже веществами: вода, оксид серы (VI), серная кислота, гидроксид калия, гидроксид железа (II), оксид кальция, хлорид меди (II)
Выберите из перечня веществ основание (щелочь). Напишите для него уравнения возможных реакций с перечисленными ниже веществами: вода, оксид серы (VI), серная кислота, гидроксид калия, гидроксид железа (II), оксид кальция, хлорид меди (II)
 Выберите из перечня веществ кислоту Напишите для нее уравнения возможных реакций с перечисленными ниже веществами: вода, оксид серы (VI), серная кислота, гидроксид кальция, гидроксид меди (II), оксид железа (III), силикат натрия, магний
Выберите из перечня веществ кислоту Напишите для нее уравнения возможных реакций с перечисленными ниже веществами: вода, оксид серы (VI), серная кислота, гидроксид кальция, гидроксид меди (II), оксид железа (III), силикат натрия, магний
 1. Наиболее сильные основные свойства проявляет гидроксид: 1) Li. OH 2) KOH 3) Na. OH 4) Rb. OH 2. Амфотерные свойства проявляют кислородные соединения: 1) бария 2) магния 3) кальция 4) бериллия 3. К двухосновным слабым кислородсодержащим кислотам относится: 1) HNO 3 2) H 2 S 3) H 2 CO 3 4) H 2 SO 4 4. К слабым кислородсодержащим кислотам относится: 1) HNО 3 2) HCl. O 4 3) H 2 Si. O 3 4)H 2 S
1. Наиболее сильные основные свойства проявляет гидроксид: 1) Li. OH 2) KOH 3) Na. OH 4) Rb. OH 2. Амфотерные свойства проявляют кислородные соединения: 1) бария 2) магния 3) кальция 4) бериллия 3. К двухосновным слабым кислородсодержащим кислотам относится: 1) HNO 3 2) H 2 S 3) H 2 CO 3 4) H 2 SO 4 4. К слабым кислородсодержащим кислотам относится: 1) HNО 3 2) HCl. O 4 3) H 2 Si. O 3 4)H 2 S
 СОЛИ Все соли – ионные соединения, сильные электролиты Соль (р, м, н) + кислота → соль + кислота (↓ или ↑) 1 2 H+ + Si. O 32 -→H 2 Si. O 3↓; Са. СО 3 + 2 Н+→Са 2+ + Н 2 О + СО 2↑ *С солями (н, м) реагируют только сильные кислоты Соль (р) + щелочь (р) → основание ↓ + соль (р или ↓) 2 Fe 3+ + 3 OH- → Fe(OH)3↓ Соль (р) + соль (р) → соль ↓ + соль (р) 3 Pb 2++2 I-→Pb. I 2↓(ярко-желтый осадок, не растворимый в к-тах) Соль (р) + металл → соль (р) + металл 4 Pb 2+ + Zn → Zn 2+ + Pb↓ ОВР *Металл вытесняет металлы, следующие за ним в ряду активности, из растворов их солей.
СОЛИ Все соли – ионные соединения, сильные электролиты Соль (р, м, н) + кислота → соль + кислота (↓ или ↑) 1 2 H+ + Si. O 32 -→H 2 Si. O 3↓; Са. СО 3 + 2 Н+→Са 2+ + Н 2 О + СО 2↑ *С солями (н, м) реагируют только сильные кислоты Соль (р) + щелочь (р) → основание ↓ + соль (р или ↓) 2 Fe 3+ + 3 OH- → Fe(OH)3↓ Соль (р) + соль (р) → соль ↓ + соль (р) 3 Pb 2++2 I-→Pb. I 2↓(ярко-желтый осадок, не растворимый в к-тах) Соль (р) + металл → соль (р) + металл 4 Pb 2+ + Zn → Zn 2+ + Pb↓ ОВР *Металл вытесняет металлы, следующие за ним в ряду активности, из растворов их солей.
 Выберите из перечня веществ соль Напишите для нее уравнения возможных реакций с перечисленными ниже веществами: вода, оксид серы (VI), серная кислота, гидроксид натрия, сульфат меди (II), железо, хлорид натрия, нитрат серебра
Выберите из перечня веществ соль Напишите для нее уравнения возможных реакций с перечисленными ниже веществами: вода, оксид серы (VI), серная кислота, гидроксид натрия, сульфат меди (II), железо, хлорид натрия, нитрат серебра
 Генетическая связь неорганических веществ • Металл • Неметалл • Основный оксид • Кислотный оксид • Основание • Кислота • Соль
Генетическая связь неорганических веществ • Металл • Неметалл • Основный оксид • Кислотный оксид • Основание • Кислота • Соль
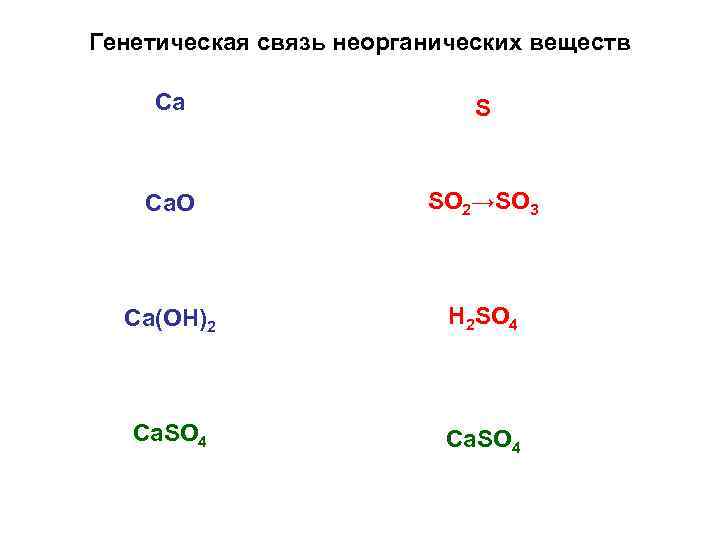 Генетическая связь неорганических веществ Са S Са. О SO 2→SO 3 Са(ОН)2 H 2 SO 4 Са. SО 4 Ca. SO 4
Генетическая связь неорганических веществ Са S Са. О SO 2→SO 3 Са(ОН)2 H 2 SO 4 Са. SО 4 Ca. SO 4
 Реакции ионного обмена идут без изменения заряда ионов В ионном виде не записывают В ионном виде записывают: • слабые электролиты: Н 2 О, Н 2 СО 3, HF, H 2 S, HNO 2, H 2 Si. O 3, СН 3 СООН, NH 4 OH • Н 2 СО 3 в продуктах записывают как Н 2 О + СО 2↑ • H 2 SO 3 в продуктах Н 2 О+SО 2↑ • NH 4 OH в продуктах NH 3↑+H 2 O • нерастворимые вещества (н) • малорастворимые вещества (м), если они – продукты, исключение Са(ОН)2 -щелочь • Оксиды – не электролиты • растворимые вещества (р) • малорастворимые вещества (м), если они – реагенты
Реакции ионного обмена идут без изменения заряда ионов В ионном виде не записывают В ионном виде записывают: • слабые электролиты: Н 2 О, Н 2 СО 3, HF, H 2 S, HNO 2, H 2 Si. O 3, СН 3 СООН, NH 4 OH • Н 2 СО 3 в продуктах записывают как Н 2 О + СО 2↑ • H 2 SO 3 в продуктах Н 2 О+SО 2↑ • NH 4 OH в продуктах NH 3↑+H 2 O • нерастворимые вещества (н) • малорастворимые вещества (м), если они – продукты, исключение Са(ОН)2 -щелочь • Оксиды – не электролиты • растворимые вещества (р) • малорастворимые вещества (м), если они – реагенты
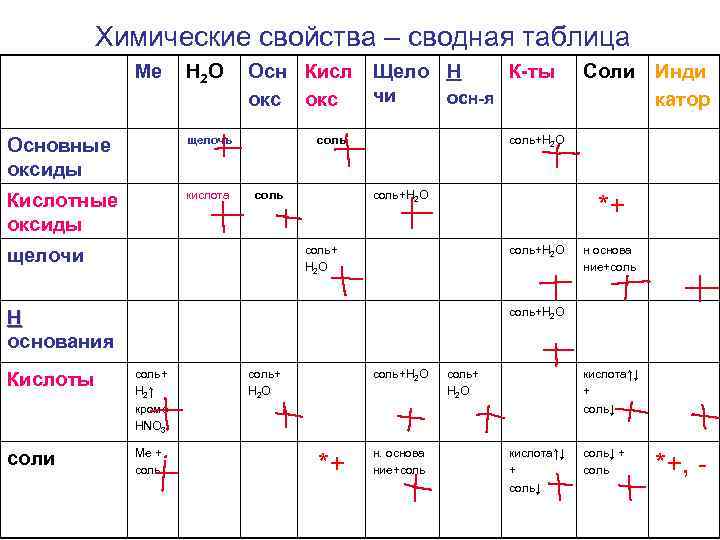 Химические свойства – сводная таблица Ме H 2 O Основные оксиды щелочь Кислотные оксиды кислота Осн Кисл Щело Н К-ты чи осн-я окс соль Инди катор соль+Н 2 О *+ соль+ Н 2 О щелочи Соли соль+Н 2 О н основа ние+соль+Н 2 О Н основания Кислоты соль+ Н 2↑ кроме HNO 3 соли Ме + соль+ Н 2 О соль+Н 2 О *+ н. основа ние+соль+ Н 2 О кислота↑↓ + соль↓ + соль *+, -
Химические свойства – сводная таблица Ме H 2 O Основные оксиды щелочь Кислотные оксиды кислота Осн Кисл Щело Н К-ты чи осн-я окс соль Инди катор соль+Н 2 О *+ соль+ Н 2 О щелочи Соли соль+Н 2 О н основа ние+соль+Н 2 О Н основания Кислоты соль+ Н 2↑ кроме HNO 3 соли Ме + соль+ Н 2 О соль+Н 2 О *+ н. основа ние+соль+ Н 2 О кислота↑↓ + соль↓ + соль *+, -


