 Химические свойства и применение оксидов
Химические свойства и применение оксидов
 Что же такое оксид? Оксиды — весьма распространённый тип соединений, содержащихся в земной коре и во вселенной вообще. Примерами таких соединений являются ржавчина, вода, песок, углекислый газ, ряд красителей. Оксидами называется класс минералов, представляющих собой соединения металла с кислородом. В зависимости от химических свойств различают: Основные оксиды Кислотные оксиды
Что же такое оксид? Оксиды — весьма распространённый тип соединений, содержащихся в земной коре и во вселенной вообще. Примерами таких соединений являются ржавчина, вода, песок, углекислый газ, ряд красителей. Оксидами называется класс минералов, представляющих собой соединения металла с кислородом. В зависимости от химических свойств различают: Основные оксиды Кислотные оксиды
 Основные оксиды реагируют с кислотами с образованием солей. Основным оксидам соответствуют основания. К основным оксидам относятся оксиды щелочных (Na 2 O, Li 2 O, K 2 O) и щелочноземельных металлов (Ca. O, Mg. O), а также оксиды переходных элементов в низших степенях окисления I и II (Cr. O, Mn. O).
Основные оксиды реагируют с кислотами с образованием солей. Основным оксидам соответствуют основания. К основным оксидам относятся оксиды щелочных (Na 2 O, Li 2 O, K 2 O) и щелочноземельных металлов (Ca. O, Mg. O), а также оксиды переходных элементов в низших степенях окисления I и II (Cr. O, Mn. O).
 Химические свойства и применение оксидов v Взаимодействие свойства основных оксидов: Na 2 O+H 2 O=2 Na. OH Ca. O+H 2 O=Ca(OH)2 v Взаимодействие основных оксидов с сильными кислотами с образованием соли и воды: Mg. O+H 2 SO 4 =Mg. SO 4 +H 2 O Ba. O+2 HCl=Ba. Cl 2 +H 2 O v Взаимодействие основных и кислотных окстдов между собой с образованием соли: Ca. O+CO 2=Ca. CO 3 Ba. O+Si. O 2=Ba. Si. O 3
Химические свойства и применение оксидов v Взаимодействие свойства основных оксидов: Na 2 O+H 2 O=2 Na. OH Ca. O+H 2 O=Ca(OH)2 v Взаимодействие основных оксидов с сильными кислотами с образованием соли и воды: Mg. O+H 2 SO 4 =Mg. SO 4 +H 2 O Ba. O+2 HCl=Ba. Cl 2 +H 2 O v Взаимодействие основных и кислотных окстдов между собой с образованием соли: Ca. O+CO 2=Ca. CO 3 Ba. O+Si. O 2=Ba. Si. O 3
 Химические свойства кислотных оксидов v Кислотные оксиды (кроме Si. O 2) взаимодействуют с водой с образованием кислот: SO 3+H 2 O=H 2 SO 4 P 2 O 5+3 H 2 O=2 H 3 PO 4 v Кислотные оксиды взаимодействующие со щелочами с образованием соли и воды: 2 Na. OH+SO 2=Na 2 SO 3+H 2 O Ca(OH)2+CO 2=Ca. CO 3+H 2 O v Кислотные оксиды взаимодействуют с основными оксидами с образованием соли: Si. O 2+Ca. O=Ca. Si. O 3
Химические свойства кислотных оксидов v Кислотные оксиды (кроме Si. O 2) взаимодействуют с водой с образованием кислот: SO 3+H 2 O=H 2 SO 4 P 2 O 5+3 H 2 O=2 H 3 PO 4 v Кислотные оксиды взаимодействующие со щелочами с образованием соли и воды: 2 Na. OH+SO 2=Na 2 SO 3+H 2 O Ca(OH)2+CO 2=Ca. CO 3+H 2 O v Кислотные оксиды взаимодействуют с основными оксидами с образованием соли: Si. O 2+Ca. O=Ca. Si. O 3
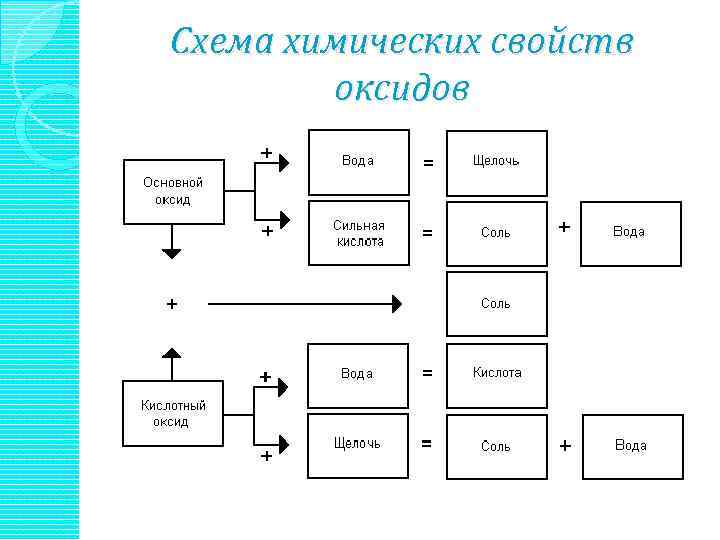 Схема химических свойств оксидов
Схема химических свойств оксидов
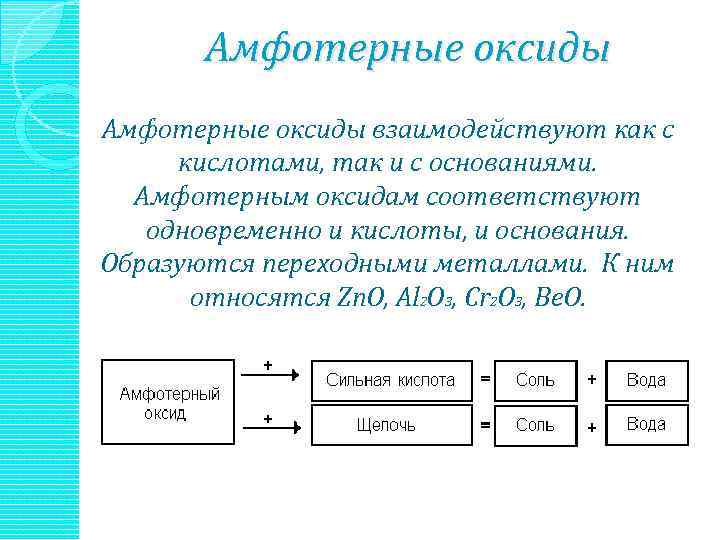 Амфотерные оксиды Aмфотерные оксиды взаимодействуют как с кислотами, так и с основаниями. Амфотерным оксидам соответствуют одновременно и кислоты, и основания. Образуются переходными металлами. К ним относятся Zn. O, Al 2 O 3, Cr 2 O 3, Be. O.
Амфотерные оксиды Aмфотерные оксиды взаимодействуют как с кислотами, так и с основаниями. Амфотерным оксидам соответствуют одновременно и кислоты, и основания. Образуются переходными металлами. К ним относятся Zn. O, Al 2 O 3, Cr 2 O 3, Be. O.
 Применение оксидов Оксиды широко применяются в различных отраслях экономики. Газообразный диоксид сер SO 2 применяется для отбеливания шерсти, шелка. В сельском хозяйстве применяется как дезинфицирующее средство для уничтожения вредителей в овощных и фруктовых хранилищах. Углекислый газ CO 2 используется в пищевой промышленности как хладагент в виде «сухого» льда, а также при тушении пожаров. Твердый оксид кремния (IV) Si. O 2 используется для получения стекла и керамики. Некоторые оксиды применяются в производстве красок: Zn. O используется для получения белой краски, а Cr 2 O 3 -зеленой. Оксид кальция используется в производстве строительных материалов.
Применение оксидов Оксиды широко применяются в различных отраслях экономики. Газообразный диоксид сер SO 2 применяется для отбеливания шерсти, шелка. В сельском хозяйстве применяется как дезинфицирующее средство для уничтожения вредителей в овощных и фруктовых хранилищах. Углекислый газ CO 2 используется в пищевой промышленности как хладагент в виде «сухого» льда, а также при тушении пожаров. Твердый оксид кремния (IV) Si. O 2 используется для получения стекла и керамики. Некоторые оксиды применяются в производстве красок: Zn. O используется для получения белой краски, а Cr 2 O 3 -зеленой. Оксид кальция используется в производстве строительных материалов.
 Спасибо за внимание! Выполнила: ученица 8 «Б» класса Тлеугазы Альфира
Спасибо за внимание! Выполнила: ученица 8 «Б» класса Тлеугазы Альфира