1.Студентам- Хим.р-ции. Кинетика-равновесие.ppt
- Количество слайдов: 11
 Химические реакции Кинетика-Равновесие- Смещение равновесия
Химические реакции Кинетика-Равновесие- Смещение равновесия
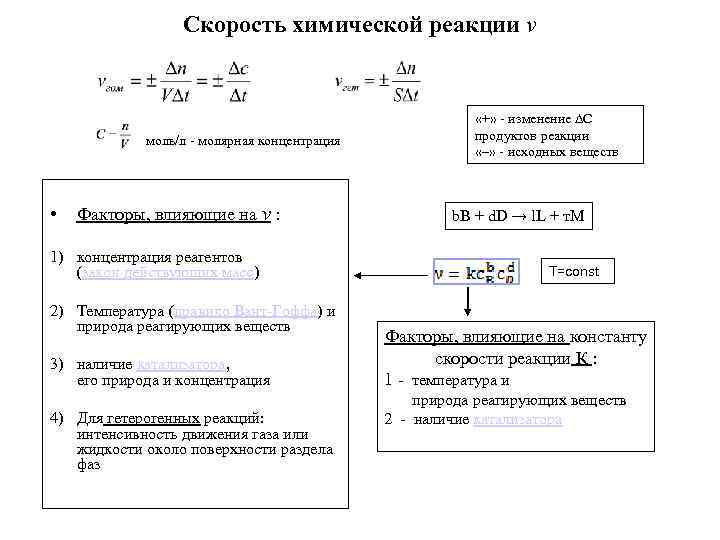 Скорость химической реакции v моль/л - молярная концентрация • Факторы, влияющие на v : 1) концентрация реагентов (закон действующих масс) b. В + d. D → l. L + т. М 2) Температура (правило Вант-Гоффа) и природа реагирующих веществ 3) наличие катализатора, его природа и концентрация 4) Для гетерогенных реакций: интенсивность движения газа или жидкости около поверхности раздела фаз «+» - изменение ∆С продуктов реакции «–» - исходных веществ Т=const Факторы, влияющие на константу скорости реакции К : 1 - температура и природа реагирующих веществ 2 - наличие катализатора
Скорость химической реакции v моль/л - молярная концентрация • Факторы, влияющие на v : 1) концентрация реагентов (закон действующих масс) b. В + d. D → l. L + т. М 2) Температура (правило Вант-Гоффа) и природа реагирующих веществ 3) наличие катализатора, его природа и концентрация 4) Для гетерогенных реакций: интенсивность движения газа или жидкости около поверхности раздела фаз «+» - изменение ∆С продуктов реакции «–» - исходных веществ Т=const Факторы, влияющие на константу скорости реакции К : 1 - температура и природа реагирующих веществ 2 - наличие катализатора
 1) Концентрация реагентов. Закон действующих масс • Кинетическое уравнение реакции b. В + d. D → l. L + т. М Т -const Для практических расчетов ур-е записывается через концентрации, соответствующие состоянию хим. равновесия [ ] : 2 NO(г) + O 2(г) = 2 NO 2(г) v=k[NO]2[O 2] Для гетерогенной реакции берутся концентрации веществ, находящихся в газообразной фазе или в растворе С(т) + О 2(г) = СО 2(г) v=k[О 2]
1) Концентрация реагентов. Закон действующих масс • Кинетическое уравнение реакции b. В + d. D → l. L + т. М Т -const Для практических расчетов ур-е записывается через концентрации, соответствующие состоянию хим. равновесия [ ] : 2 NO(г) + O 2(г) = 2 NO 2(г) v=k[NO]2[O 2] Для гетерогенной реакции берутся концентрации веществ, находящихся в газообразной фазе или в растворе С(т) + О 2(г) = СО 2(г) v=k[О 2]
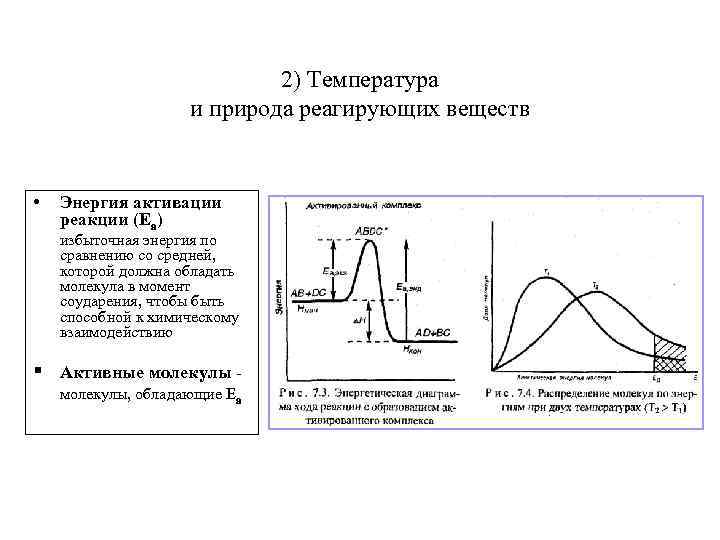 2) Температура и природа реагирующих веществ • Энергия активации реакции (Еа) избыточная энергия по сравнению со средней, которой должна обладать молекула в момент соударения, чтобы быть способной к химическому взаимодействию § Активные молекулы, обладающие Еа
2) Температура и природа реагирующих веществ • Энергия активации реакции (Еа) избыточная энергия по сравнению со средней, которой должна обладать молекула в момент соударения, чтобы быть способной к химическому взаимодействию § Активные молекулы, обладающие Еа
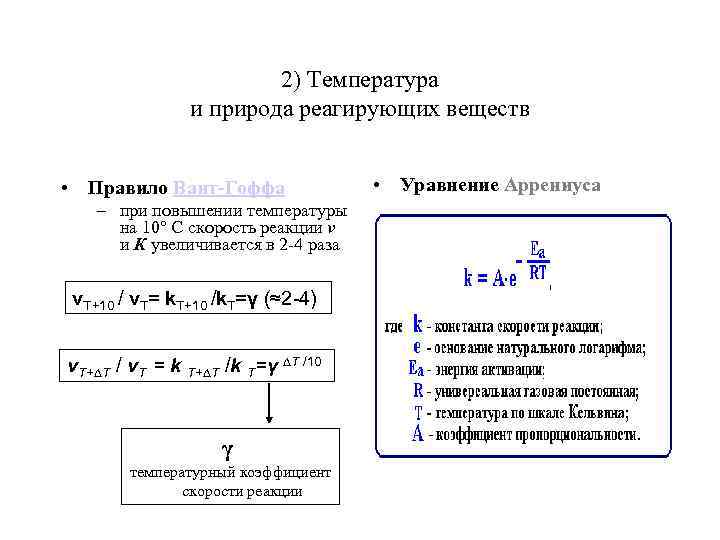 2) Температура и природа реагирующих веществ • Правило Вант-Гоффа – при повышении температуры на 10° С скорость реакции v и К увеличивается в 2 -4 раза v. Т+10 / v. Т= k. Т+10 /k. Т=γ (≈2 -4) v. Т+∆Т / v. Т = k Т+∆Т /k Т=γ ∆Т /10 γ температурный коэффициент скорости реакции • Уравнение Аррениуса
2) Температура и природа реагирующих веществ • Правило Вант-Гоффа – при повышении температуры на 10° С скорость реакции v и К увеличивается в 2 -4 раза v. Т+10 / v. Т= k. Т+10 /k. Т=γ (≈2 -4) v. Т+∆Т / v. Т = k Т+∆Т /k Т=γ ∆Т /10 γ температурный коэффициент скорости реакции • Уравнение Аррениуса
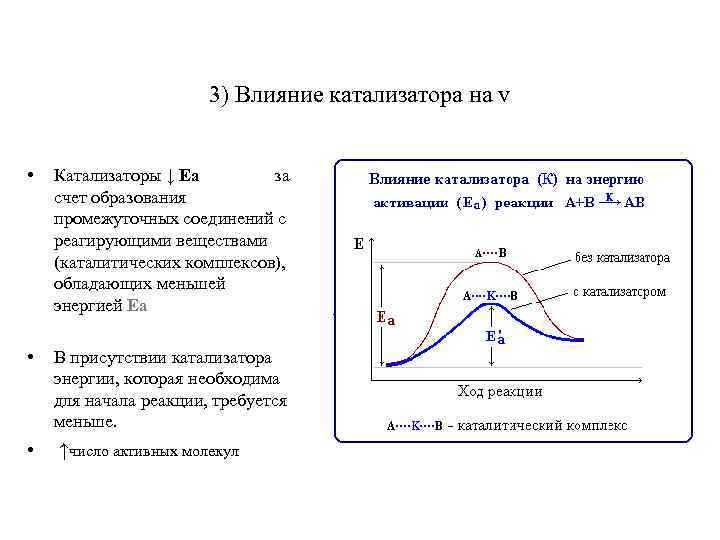 3) Влияние катализатора на v • Катализаторы ↓ Еа за счет образования промежуточных соединений с реагирующими веществами (каталитических комплексов), обладающих меньшей энергией Еа • В присутствии катализатора энергии, которая необходима для начала реакции, требуется меньше. • ↑число активных молекул
3) Влияние катализатора на v • Катализаторы ↓ Еа за счет образования промежуточных соединений с реагирующими веществами (каталитических комплексов), обладающих меньшей энергией Еа • В присутствии катализатора энергии, которая необходима для начала реакции, требуется меньше. • ↑число активных молекул
 4) Гетерогенные реакции: интенсивность движения газа или жидкости около поверхности раздела фаз • Стадии реакции: 1. Подвод реагирующих веществ к поверхности раздела фаз Химическая реакция на поверхности Отвод продуктов реакции 2. 3. • Лимитирующей стадией является самая медленная Еа мала → лимитирующие стадии 1 и 3 Еа велика → лим. стадия 2
4) Гетерогенные реакции: интенсивность движения газа или жидкости около поверхности раздела фаз • Стадии реакции: 1. Подвод реагирующих веществ к поверхности раздела фаз Химическая реакция на поверхности Отвод продуктов реакции 2. 3. • Лимитирующей стадией является самая медленная Еа мала → лимитирующие стадии 1 и 3 Еа велика → лим. стадия 2
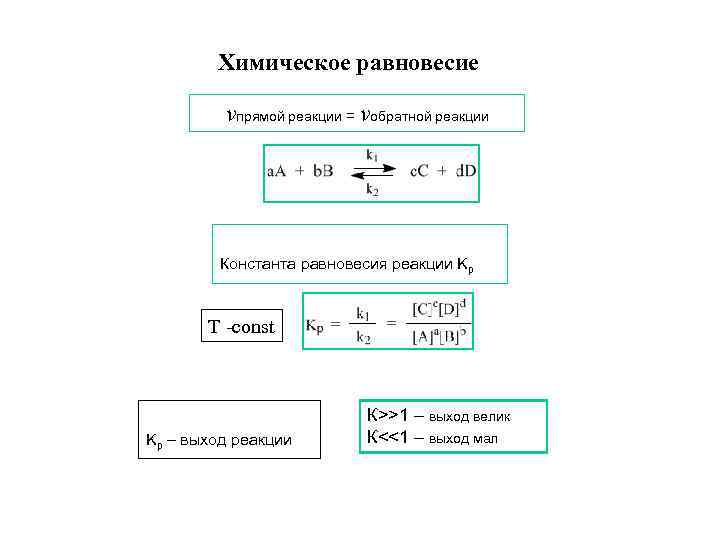 Химическое равновесие vпрямой реакции = vобратной реакции Константа равновесия реакции Kp Т -const Kp – выход реакции К>>1 – выход велик К<<1 – выход мал
Химическое равновесие vпрямой реакции = vобратной реакции Константа равновесия реакции Kp Т -const Kp – выход реакции К>>1 – выход велик К<<1 – выход мал
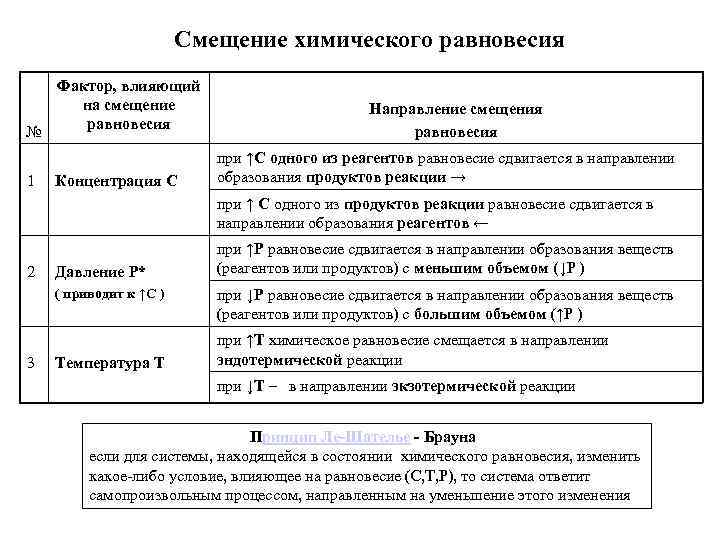 Смещение химического равновесия Фактор, влияющий на смещение равновесия № 1 Концентрация C Направление смещения равновесия при ↑С одного из реагентов равновесие сдвигается в направлении образования продуктов реакции → при ↑ С одного из продуктов реакции равновесие сдвигается в направлении образования реагентов ← 2 Давление P* ( приводит к ↑С ) 3 Температура T при ↑Р равновесие сдвигается в направлении образования веществ (реагентов или продуктов) с меньшим объемом (↓Р ) при ↓Р равновесие сдвигается в направлении образования веществ (реагентов или продуктов) с большим объемом (↑Р ) при ↑Т химическое равновесие смещается в направлении эндотермической реакции при ↓Т – в направлении экзотермической реакции Принцип Ле-Шателье - Брауна если для системы, находящейся в состоянии химического равновесия, изменить какое-либо условие, влияющее на равновесие (С, Т, Р), то система ответит самопроизвольным процессом, направленным на уменьшение этого изменения
Смещение химического равновесия Фактор, влияющий на смещение равновесия № 1 Концентрация C Направление смещения равновесия при ↑С одного из реагентов равновесие сдвигается в направлении образования продуктов реакции → при ↑ С одного из продуктов реакции равновесие сдвигается в направлении образования реагентов ← 2 Давление P* ( приводит к ↑С ) 3 Температура T при ↑Р равновесие сдвигается в направлении образования веществ (реагентов или продуктов) с меньшим объемом (↓Р ) при ↓Р равновесие сдвигается в направлении образования веществ (реагентов или продуктов) с большим объемом (↑Р ) при ↑Т химическое равновесие смещается в направлении эндотермической реакции при ↓Т – в направлении экзотермической реакции Принцип Ле-Шателье - Брауна если для системы, находящейся в состоянии химического равновесия, изменить какое-либо условие, влияющее на равновесие (С, Т, Р), то система ответит самопроизвольным процессом, направленным на уменьшение этого изменения
 Направление протекания реакции Характер изменения энергии Гиббса ΔG позволяет судить о принципиальной возможности осуществления процесса Константа равновесия реакции 1) При ΔG < 0 процесс может протекать 2) При ΔG > 0 процесс протекать не может 3) Если ΔG = 0, то система находится в состоянии химического равновесия ΔG < 0 К>1 ΔG > 0 К<1 ΔG = 0 К=1 Изменение св. энергии Гиббса G в ходе химической реакции связано с конст. равновесия К
Направление протекания реакции Характер изменения энергии Гиббса ΔG позволяет судить о принципиальной возможности осуществления процесса Константа равновесия реакции 1) При ΔG < 0 процесс может протекать 2) При ΔG > 0 процесс протекать не может 3) Если ΔG = 0, то система находится в состоянии химического равновесия ΔG < 0 К>1 ΔG > 0 К<1 ΔG = 0 К=1 Изменение св. энергии Гиббса G в ходе химической реакции связано с конст. равновесия К
 Направление протекания реакции Тепловой эфффект реакции ∆Н: (Н – энтальпия) Изменение энтропиии ∆S: ∆H = (∆Hini)прод - (∆Hjnj)исх ∆S = (∆Sini)прод - (∆Sjnj)исх ∆Нi - теплота образования вещества i; ∆ Нj – теплота образования вещества j; ni, nj– стехиометрические коэфф-ты в ур-ии р-ции
Направление протекания реакции Тепловой эфффект реакции ∆Н: (Н – энтальпия) Изменение энтропиии ∆S: ∆H = (∆Hini)прод - (∆Hjnj)исх ∆S = (∆Sini)прод - (∆Sjnj)исх ∆Нi - теплота образования вещества i; ∆ Нj – теплота образования вещества j; ni, nj– стехиометрические коэфф-ты в ур-ии р-ции


