FBB-belok2-2013.ppt
- Количество слайдов: 46

Химические основы биологических процессов Лекция 3 1. 2. 3. 4. 5. План лекции Строение и физико химические свойства аминокислот. Пептидная связь. Способы образования пептидной связи. Первичная структура белков Cпособы установления первичной структуры.
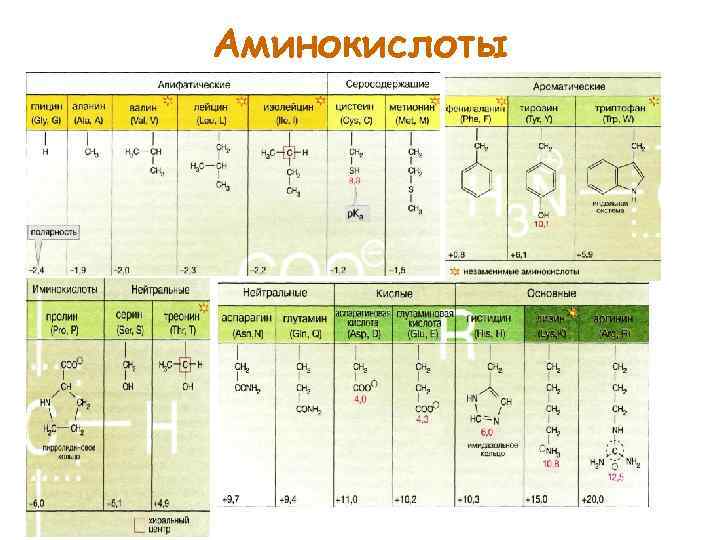
Аминокислоты

Растворимость и кислотно-основные свойства аминокислот. Z = +1 Z = 0 Z = -1 Для глицина р. К 1 = 2, 34, р. К 2 = 9, 6 • уравнение Гендерсона Хассельбаха Изоэлектрическая точка – значение р. Н, при котором общий заряд молекулы равен нулю
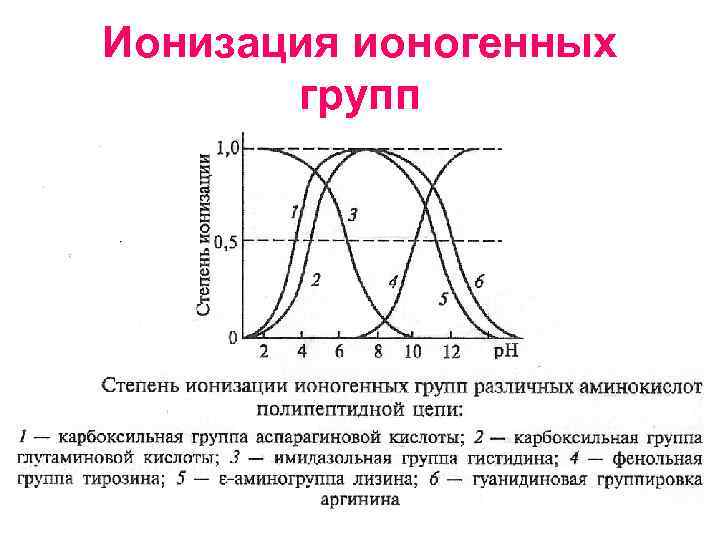
Ионизация ионогенных групп
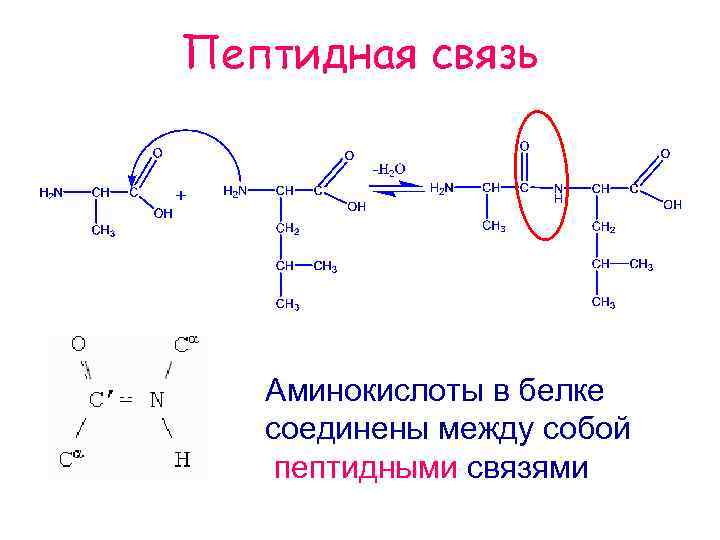
Пептидная связь Аминокислоты в белке соединены между собой пептидными связями
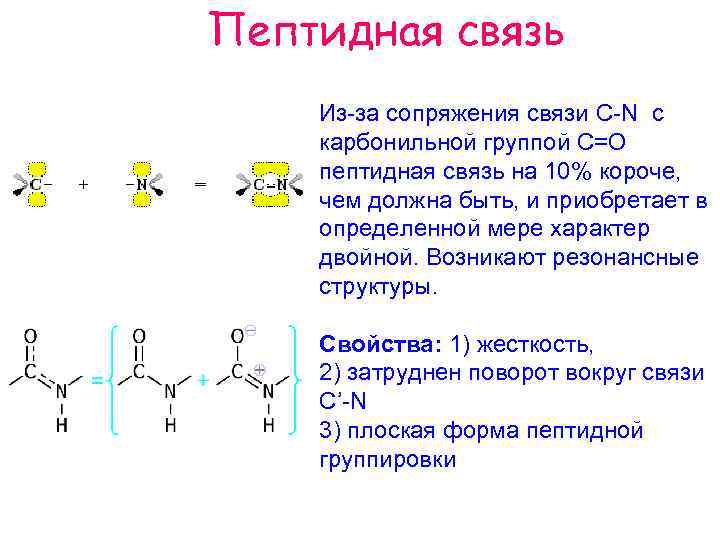
Пептидная связь Из за сопряжения связи C N с карбонильной группой C=O пептидная связь на 10% короче, чем должна быть, и приобретает в определенной мере характер двойной. Возникают резонансные структуры. Свойства: 1) жесткость, 2) затруднен поворот вокруг связи C’ N 3) плоская форма пептидной группировки
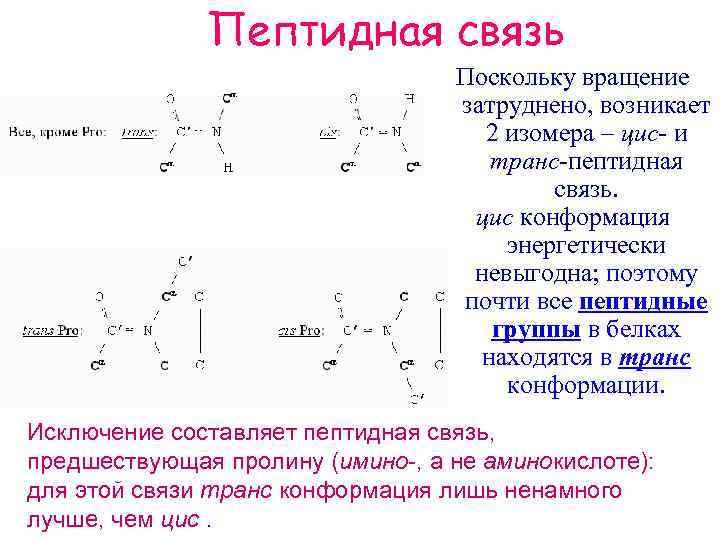
Пептидная связь Поскольку вращение затруднено, возникает 2 изомера – цис- и транс-пептидная связь. цис конформация энергетически невыгодна; поэтому почти все пептидные группы в белках находятся в транс конформации. Исключение составляет пептидная связь, предшествующая пролину (имино , а не аминокислоте): для этой связи транс конформация лишь ненамного лучше, чем цис.
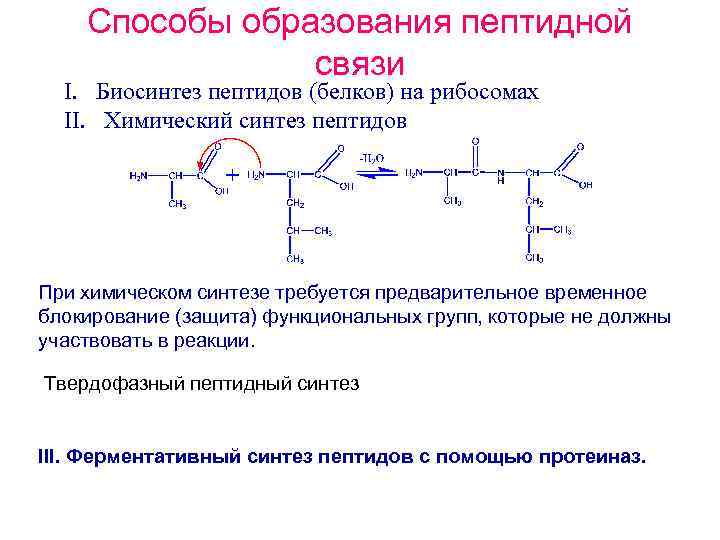
Способы образования пептидной связи I. Биосинтез пептидов (белков) на рибосомах II. Химический синтез пептидов При химическом синтезе требуется предварительное временное блокирование (защита) функциональных групп, которые не должны участвовать в реакции. Твердофазный пептидный синтез III. Ферментативный синтез пептидов с помощью протеиназ.
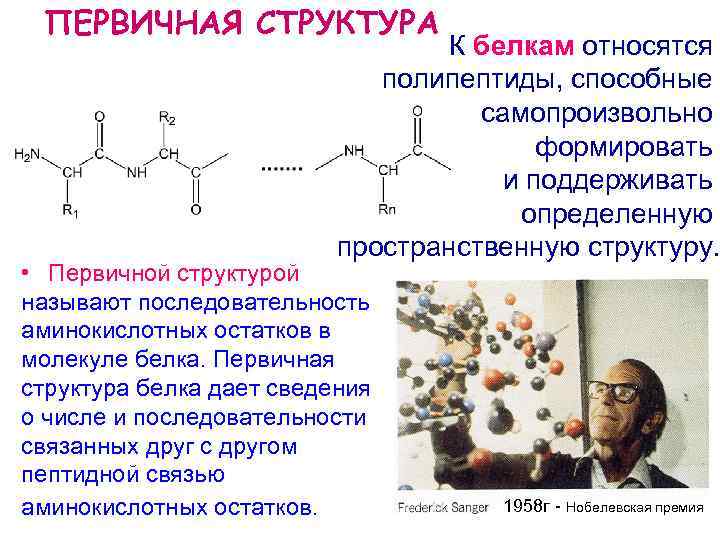
ПЕРВИЧНАЯ СТРУКТУРА К белкам относятся полипептиды, способные самопроизвольно формировать и поддерживать определенную пространственную структуру. • Первичной структурой называют последовательность аминокислотных остатков в молекуле белка. Первичная структура белка дает сведения о числе и последовательности связанных друг с другом пептидной связью аминокислотных остатков. 1958 г Нобелевская премия

Белок - линейный полимер Мономерное звено – аминокислотный остаток Тип связи – амидная (пептидная) Полярность цепи полимера: N-конец и С-конец Белок - информационная макромолекула mprrrvigqrkilpdpkfgsellakfvnilmvdgkkstaesivysaletlaqrsgksele
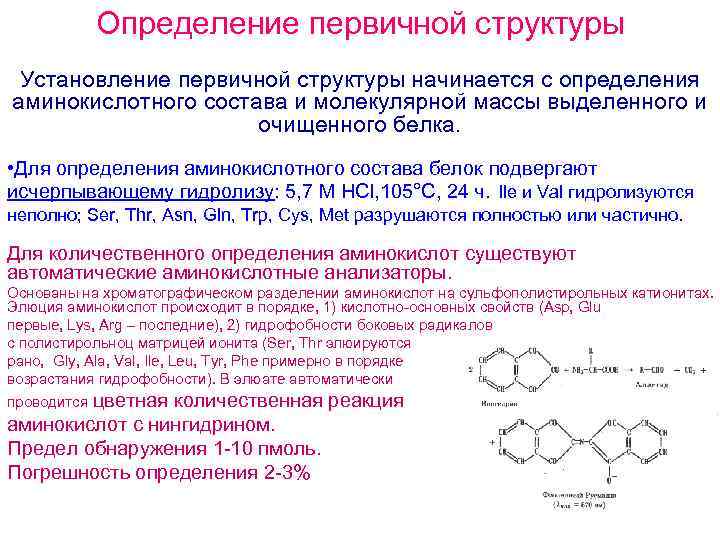
Определение первичной структуры Установление первичной структуры начинается с определения аминокислотного состава и молекулярной массы выделенного и очищенного белка. • Для определения аминокислотного состава белок подвергают исчерпывающему гидролизу: 5, 7 М HCl, 105°С, 24 ч. Ile и Val гидролизуются неполно; Ser, Thr, Asn, Gln, Trp, Cys, Met разрушаются полностью или частично. Для количественного определения аминокислот существуют автоматические аминокислотные анализаторы. Основаны на хроматографическом разделении аминокислот на сульфополистирольных катионитах. Элюция аминокислот происходит в порядке, 1) кислотно основных свойств (Asp, Glu первые, Lys, Arg – последние), 2) гидрофобности боковых радикалов с полистирольноц матрицей ионита (Ser, Thr элюируются рано, Gly, Ala, Val, Ile, Leu, Tyr, Phe примерно в порядке возрастания гидрофобности). В элюате автоматически проводится цветная количественная реакция аминокислот с нингидрином. Предел обнаружения 1 10 пмоль. Погрешность определения 2 3%
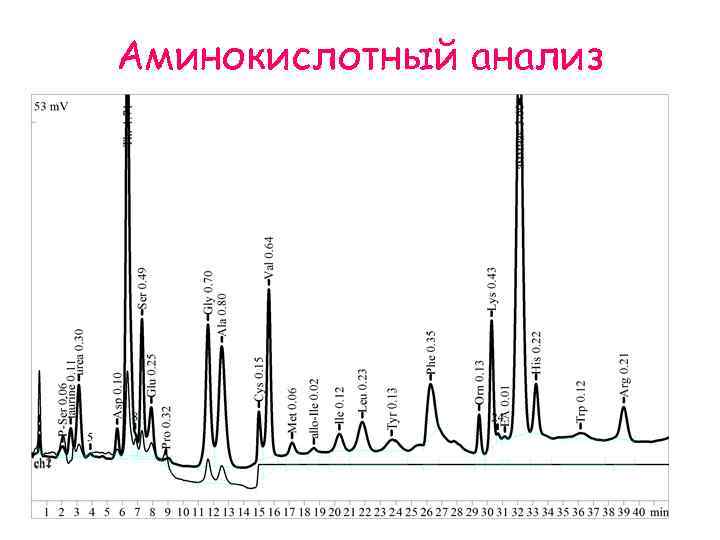
Аминокислотный анализ

Методы определения первичной структуры белка 1. Анализ последовательности нуклеотидов в соответствующем структурном гене или к. ДНК • Преимущества: быстрый, довольно точный и простой анализ • Недостатки: нужно выделить и клонировать ген, не позволяет обнаружить посттрансляционные модификации 2. Анализ самого белка. • Преимущества: нужен только сам белок, можно обнаружит все модификации • Недостатки: довольно длительные, сложные и дорогостоящие процедуры, не всегда дающие однозначные точные результаты.

Методы определения первичной структуры белка Определение аминокислотной последовательности белка сводится к следующим основным этапам: 1) Получение белка в гомогенном состоянии (индивидуальное вещество). 2) Расщепление белка на несколько фрагментов с длиной, доступной для секвенирования (определения последовательности аминокислот). 3) Секвенирование каждого из полученных фрагментов. 4) Сборка полной структуры белка из установленных структур его фрагментов.

Определение первичной структуры • Необходимо предварительно получить белок в чистом гомогенном (индивидуальном) состоянии Критерии гомогенности: • Обнаружение при электрофорезе или изоэлектрофокусировании единственной белковой полосы, проявляющей характерную активность; + данные иммуноэлектрофореза и иммуноблоттинга; • Обнаружение при SDS ПААГ электрофорезе единственной полосы, отвечающей денатуриро ванному белку, в особенности если иммуно блоттинг подтверждает, что она несет антигенные детерминанты данного белка. • • • Обнаружение единственного белкового пика, совпадающего с пиком активности при различных методах жидкостной хроматографии (аффинной, ионообменной, гидрофобной, гель хроматографии). Выявление единственной N концевой последовательности.

Методы фрагментации цепи • 1. ферментативный гидролиз. Используются протеиназы: Трипсин расщепляет связи после Lys или Arg. Химотрипсин- после ароматических аминокислот Phe, Tyr, Trp. Пепсин расщепляет связи, образованные Trp, Phe, Tyr, Met, Leu. Папаин гидролизует связи после Arg, Lys, Gly. Glu, Asp-специфичные протеиназы (эндопротеиназы Glu-C). Ферменты гидролизуют пептидные связи после Glu, Asp. В общем случае гидролиз протекает тем специфичнее, чем короче время инкубации с протеиназой. Большое значение имеет чистота выбранного фермента (протеиназы).
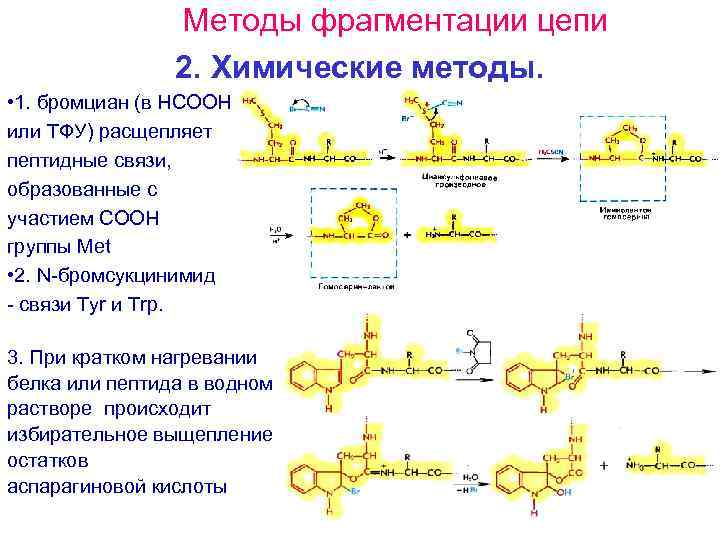
Методы фрагментации цепи 2. Химические методы. • 1. бромциан (в HCOOH или ТФУ) расщепляет пептидные связи, образованные с участием СООН группы Met • 2. N бромсукцинимид связи Tyr и Trp. 3. При кратком нагревании белка или пептида в водном растворе происходит избирательное выщепление остатков аспарагиновой кислоты

Определение концевых аминокислот • Смесь пептидов, полученных в результате различных методов расщепления сначала должна быть разделена, и каждый из пептидов очищен. • Определение С-концевых аминокислот (редко): исчерпывающий гидразинолиз пептидных связей. Получаются гидразиды всех аминокислот, кроме С концевой.

Определение концевых аминокислот Определение N-концевых аминокислот. 1. динитрофенильный метод Сенгера. пептид или белок обрабатывается 2, 4 динитрофторбензолом и образующаяся в результате гидролиза ДНФ аминокислота (желтая, 360 нм, экстинкция около 15 000) экстрагируется и идентифицируется. 2. дансильный метод N концевая аминокислота реагирует с DNS Cl и идентифицируется в виде интенсивно флуоресцирующего желтым светом пятна DNS производного. Предел обнаружения 10 14 моль.
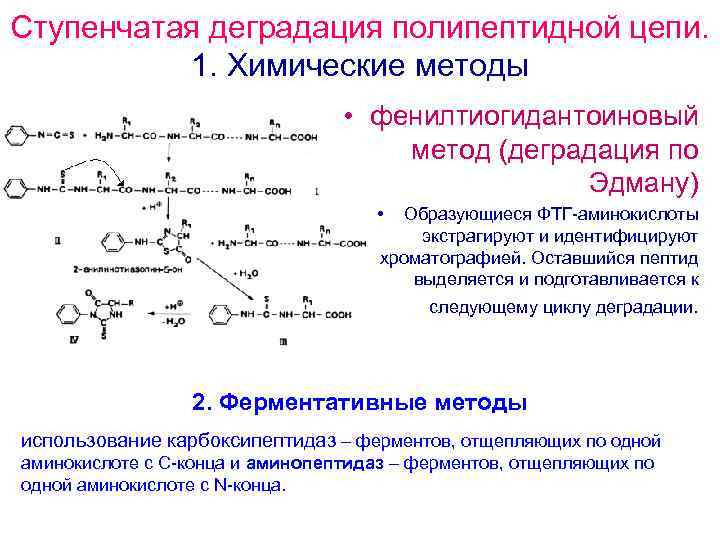
Ступенчатая деградация полипептидной цепи. 1. Химические методы • фенилтиогидантоиновый метод (деградация по Эдману) • Образующиеся ФТГ аминокислоты экстрагируют и идентифицируют хроматографией. Оставшийся пептид выделяется и подготавливается к следующему циклу деградации. 2. Ферментативные методы использование карбоксипептидаз – ферментов, отщепляющих по одной аминокислоте с С конца и аминопептидаз – ферментов, отщепляющих по одной аминокислоте с N конца.
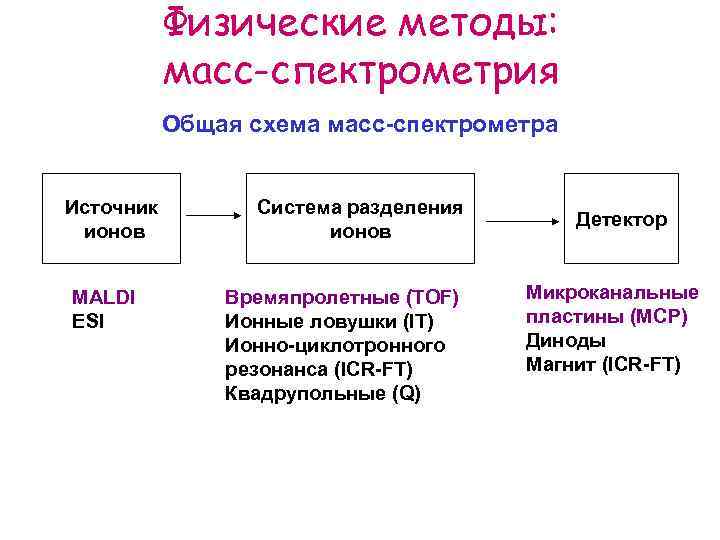
Физические методы: масс-спектрометрия Общая схема масс-спектрометра Источник ионов MALDI ESI Система разделения ионов Времяпролетные (TOF) Ионные ловушки (IT) Ионно-циклотронного резонанса (ICR-FT) Квадрупольные (Q) Детектор Микроканальные пластины (MCP) Диноды Магнит (ICR-FT)
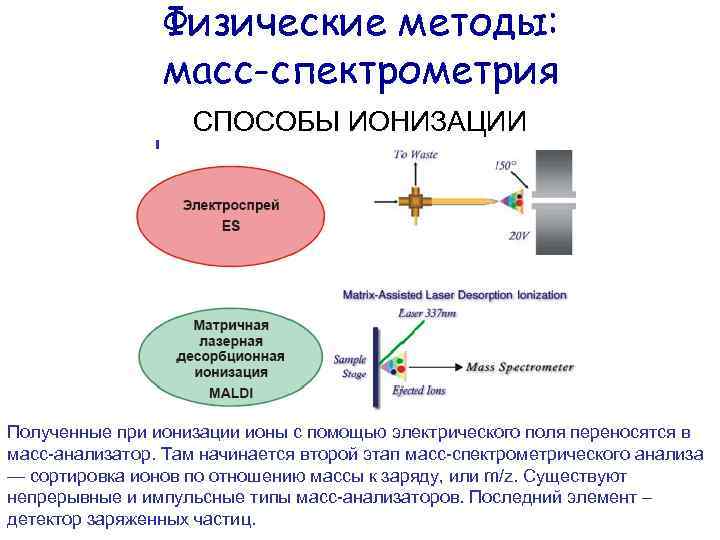
Физические методы: масс-спектрометрия СПОСОБЫ ИОНИЗАЦИИ Полученные при ионизации ионы с помощью электрического поля переносятся в масс анализатор. Там начинается второй этап масс спектрометрического анализа — сортировка ионов по отношению массы к заряду, или m/z. Существуют непрерывные и импульсные типы масс анализаторов. Последний элемент – детектор заряженных частиц.
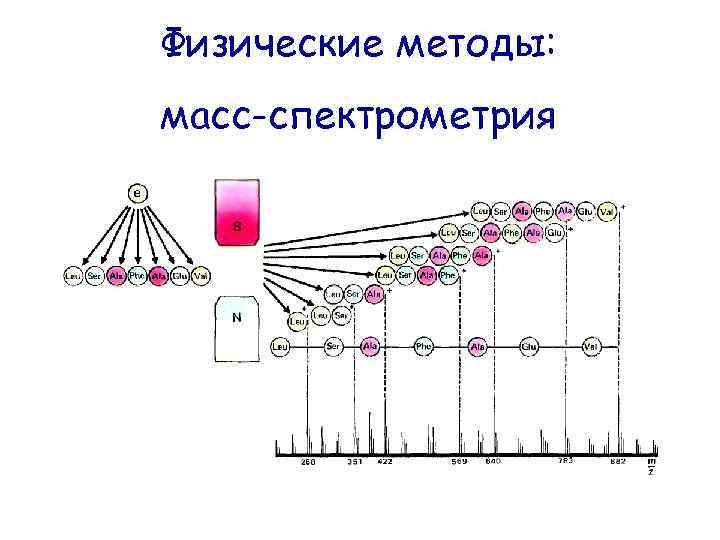
Физические методы: масс-спектрометрия
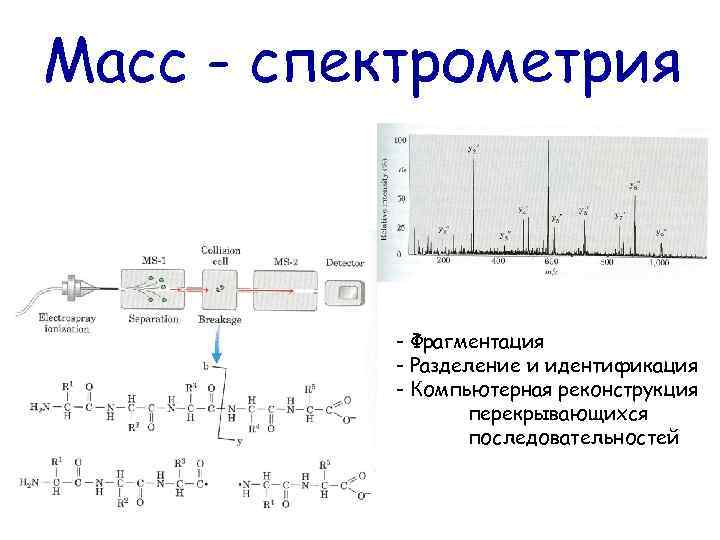
Масс - спектрометрия - Фрагментация - Разделение и идентификация - Компьютерная реконструкция перекрывающихся последовательностей

Вторичная структура белка • Вторичная структура – это пространственное расположение атомов основной цепи молекулы белка на ее отдельных участках. Локальное понятие, в соответствии с которым любой участок полипептидной цепи имеет вторичную структуру. Есть периодические и непериодические участки. • регулярные вторичные структуры белка —α спирали и β структуры
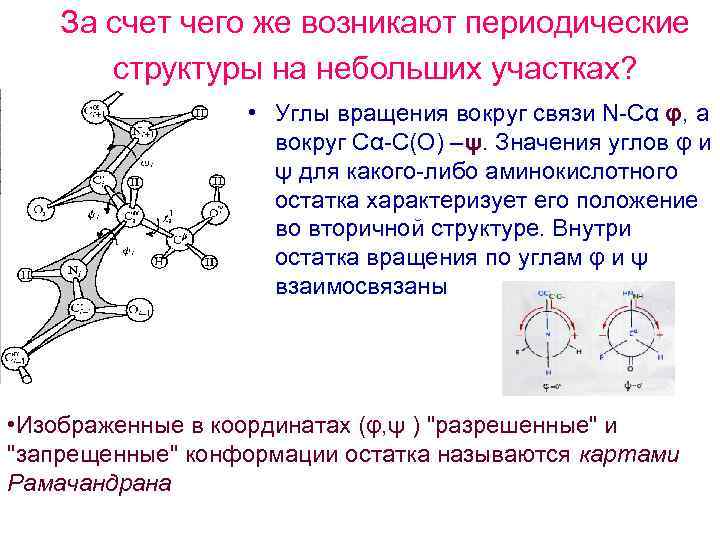
За счет чего же возникают периодические структуры на небольших участках? • Углы вращения вокруг связи N Cα φ, а вокруг Cα C(O) –ψ. Значения углов φ и ψ для какого либо аминокислотного остатка характеризует его положение во вторичной структуре. Внутри остатка вращения по углам φ и ψ взаимосвязаны • Изображенные в координатах (φ, ψ ) "разрешенные" и "запрещенные" конформации остатка называются картами Рамачандрана
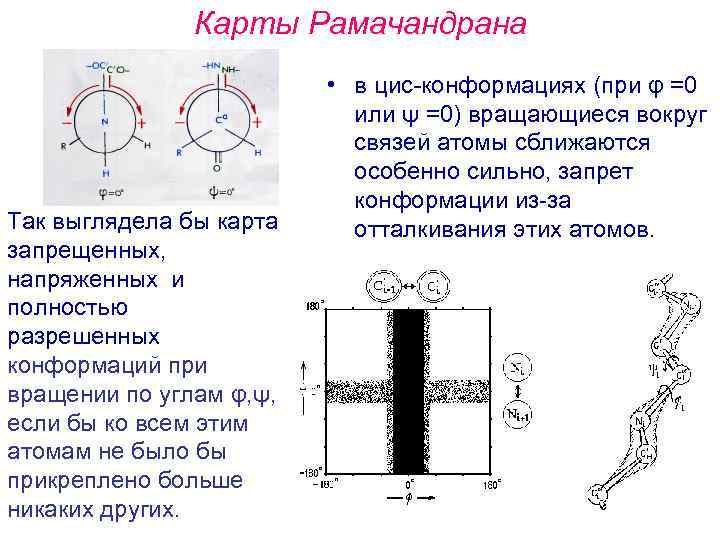
Карты Рамачандрана Так выглядела бы карта запрещенных, напряженных и полностью разрешенных конформаций при вращении по углам φ, ψ, если бы ко всем этим атомам не было бы прикреплено больше никаких других. • в цис-конформациях (при φ =0 или ψ =0) вращающиеся вокруг связей атомы сближаются особенно сильно, запрет конформации из за отталкивания этих атомов.
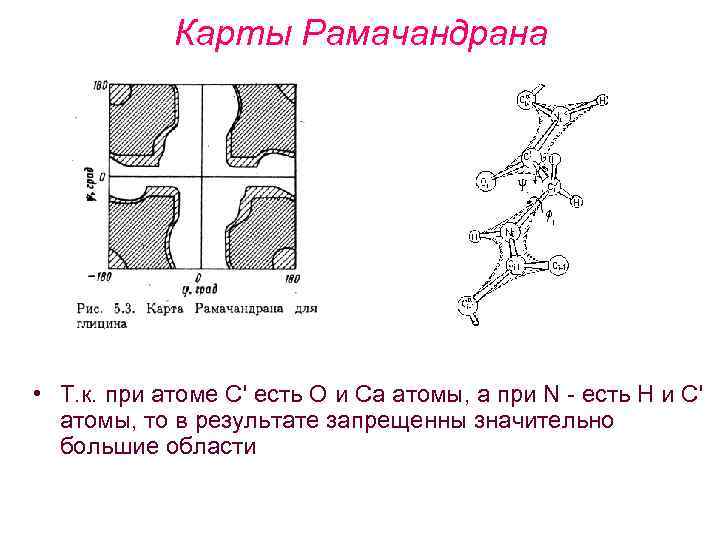
Карты Рамачандрана • Т. к. при атоме C' есть О и Ca атомы, а при N есть H и C' атомы, то в результате запрещенны значительно большие области
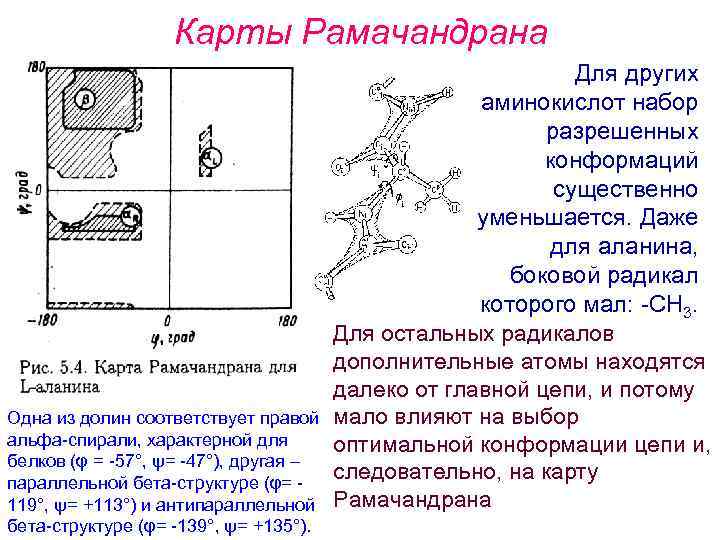
Карты Рамачандрана Одна из долин соответствует правой альфа спирали, характерной для белков (φ = 57°, ψ= 47°), другая – параллельной бета структуре (φ= 119°, ψ= +113°) и антипараллельной бета структуре (φ= 139°, ψ= +135°). Для других аминокислот набор разрешенных конформаций существенно уменьшается. Даже для аланина, боковой радикал которого мал: СН 3. Для остальных радикалов дополнительные атомы находятся далеко от главной цепи, и потому мало влияют на выбор оптимальной конформации цепи и, следовательно, на карту Рамачандрана

Карты Рамачандрана Наблюдаемые в белках конформации аминокислотных остатков (точки) для глицина (справа) и для всех остальных остатков (слева). Контур очерчивает стерически разрешенные области.
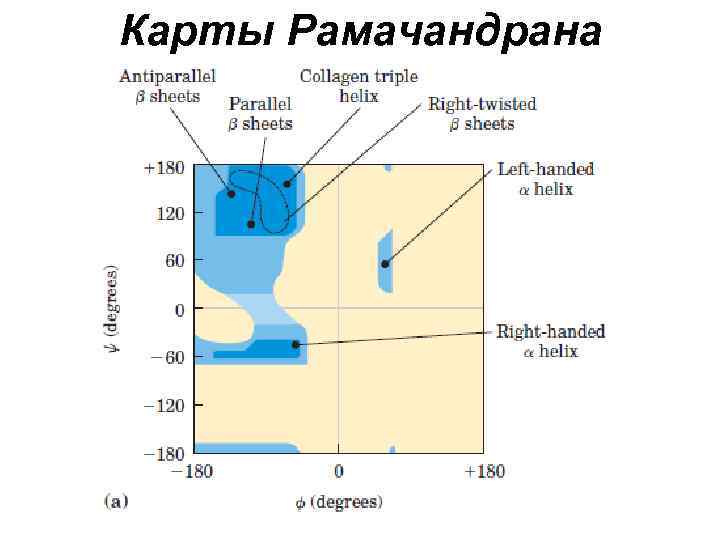
Карты Рамачандрана
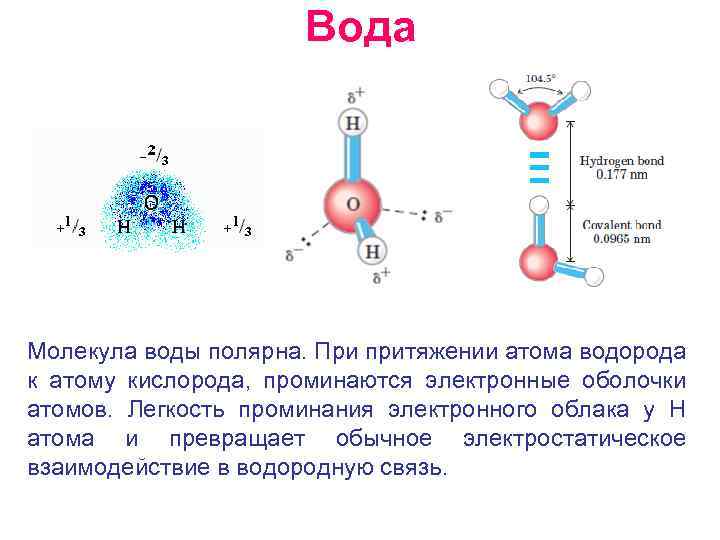
Вода Молекула воды полярна. При притяжении атома водорода к атому кислорода, проминаются электронные оболочки атомов. Легкость проминания электронного облака у Н атома и превращает обычное электростатическое взаимодействие в водородную связь.
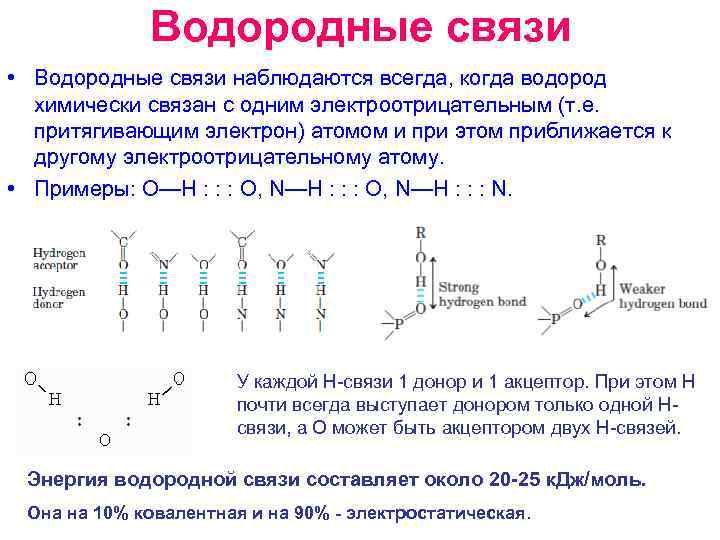
Водородные связи • Водородные связи наблюдаются всегда, когда водород химически связан с одним электроотрицательным (т. е. притягивающим электрон) атомом и при этом приближается к другому электроотрицательному атому. • Примеры: O—H : : : O, N—H : : : N. У каждой Н связи 1 донор и 1 акцептор. При этом Н почти всегда выступает донором только одной Н связи, а О может быть акцептором двух Н связей. Энергия водородной связи составляет около 20 -25 к. Дж/моль. Она на 10% ковалентная и на 90% - электростатическая.

Водородные связи • И пептидные группы главной цепи, и полярные боковые группы выступают донорами и акцепторами водородных связей. Они могут завязывать водородные связи друг с другом или с молекулами воды. Энергетический баланс близок к нулю: две Н связи было, две стало. Но энтропия воды возрастает. Вследствие роста энтропии свободная энергия системы "белок в воде" падает, — примерно на 1. 5 ккал/моль. Эта выделенная водой свободная энергия может скомпенсировать рост свободной энергии, сопровождающий падение энтропии при фиксации групп D и А связью D: : : A. В результате регулярная вторичная структура полипептидов в воде находится как раз на грани стабильности. Н связи, стабилизующие структуру белка в воде носят энтропийную, а не энтальпийную природу.
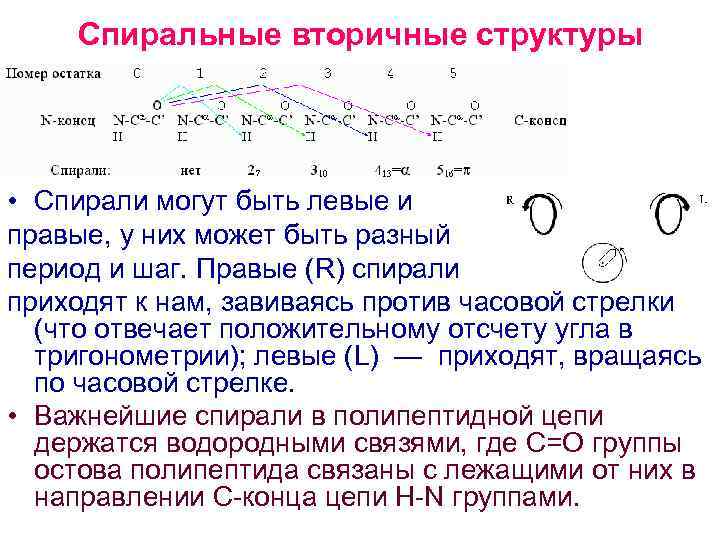
Спиральные вторичные структуры • Спирали могут быть левые и правые, у них может быть разный период и шаг. Правые (R) спирали приходят к нам, завиваясь против часовой стрелки (что отвечает положительному отсчету угла в тригонометрии); левые (L) — приходят, вращаясь по часовой стрелке. • Важнейшие спирали в полипептидной цепи держатся водородными связями, где С=О группы остова полипептида связаны с лежащими от них в направлении С конца цепи H N группами.

Альфа-спирали • В белках преобладают правые альфа спирали Конформации различных вторичных структур на фоне карты разрешенных и запрещенных конформаций аминокислотных остатков. 27 R, 27 L: правая и левая спираль 27; 310 R, 310 L: правая и левая спираль 310; αR, αL — правая и левая α спираль; πR, πL — правая и левая π спираль. β — β структура. Р — спираль Poly(Pro)II. — конформации, разрешенные для аланина (Ala); — области, разрешенные лишь для глицина, но не для аланина и других остатков; — области, запрещенные для всех остатков.
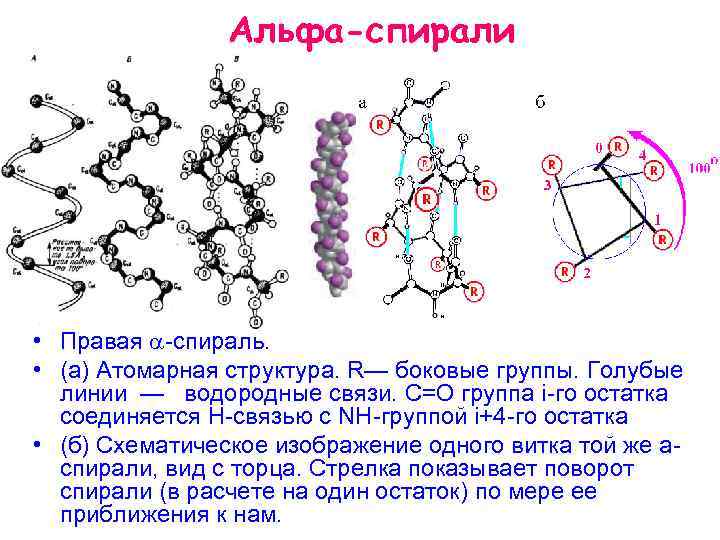
Альфа-спирали • Правая спираль. • (а) Атомарная структура. R— боковые группы. Голубые линии — водородные связи. C=O группа i го остатка соединяется H связью с NH группой i+4 го остатка • (б) Схематическое изображение одного витка той же a спирали, вид с торца. Стрелка показывает поворот спирали (в расчете на один остаток) по мере ее приближения к нам.
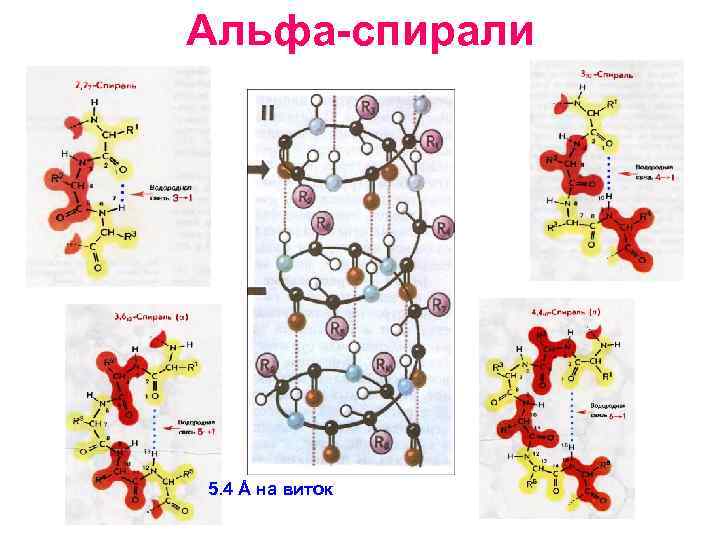
Альфа-спирали 5. 4 Å на виток

Бета-структуры • Схема хода цепи и расположения водородных связей в параллельной, антипараллельной и смешанной b b структуре. Видно, что Н связи одного остатка в b тяже направлены одну сторону, следующего — в противоположную, и т. д.
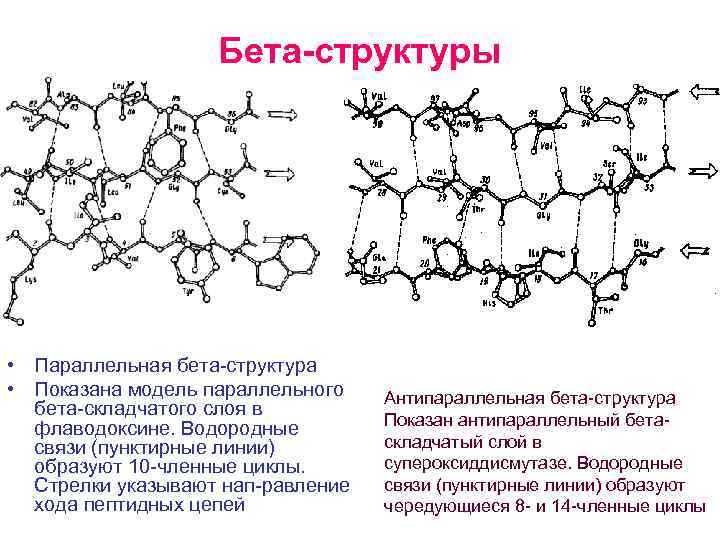
Бета-структуры • Параллельная бета структура • Показана модель параллельного бета складчатого слоя в флаводоксине. Водородные связи (пунктирные линии) образуют 10 членные циклы. Стрелки указывают нап равление хода пептидных цепей Антипараллельная бета структура Показан антипараллельный бета складчатый слой в супероксиддисмутазе. Водородные связи (пунктирные линии) образуют чередующиеся 8 и 14 членные циклы
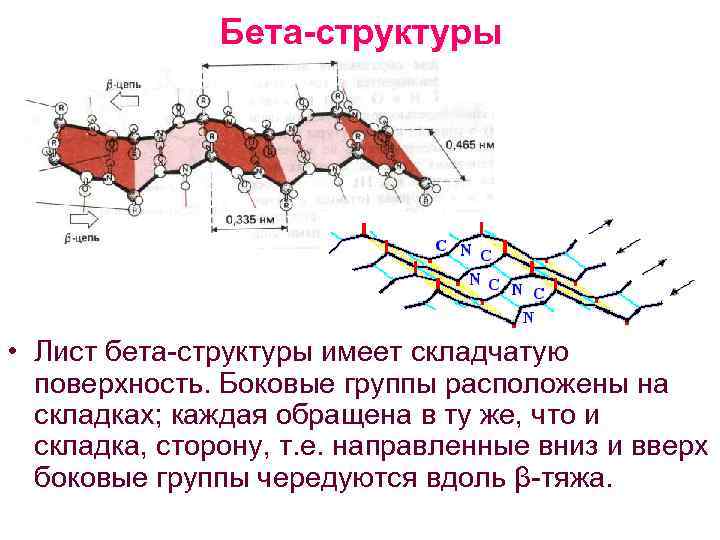
Бета-структуры • Лист бета структуры имеет складчатую поверхность. Боковые группы расположены на складках; каждая обращена в ту же, что и складка, сторону, т. е. направленные вниз и вверх боковые группы чередуются вдоль β тяжа.
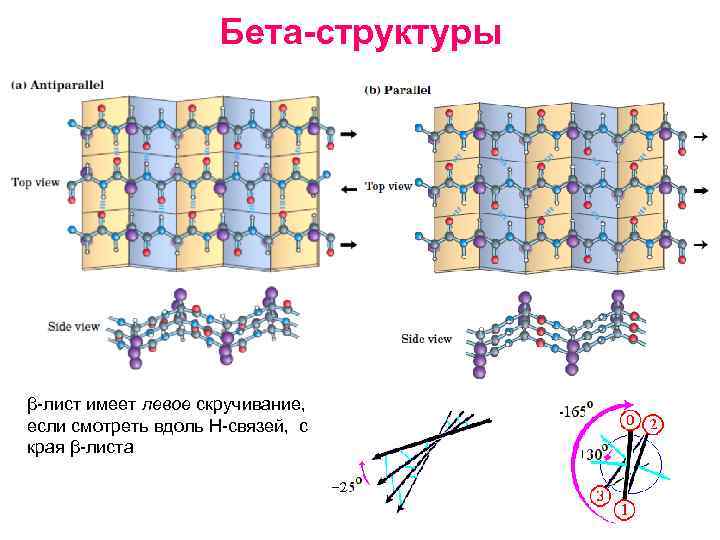
Бета-структуры β лист имеет левое скручивание, если смотреть вдоль Н связей, с края β листа
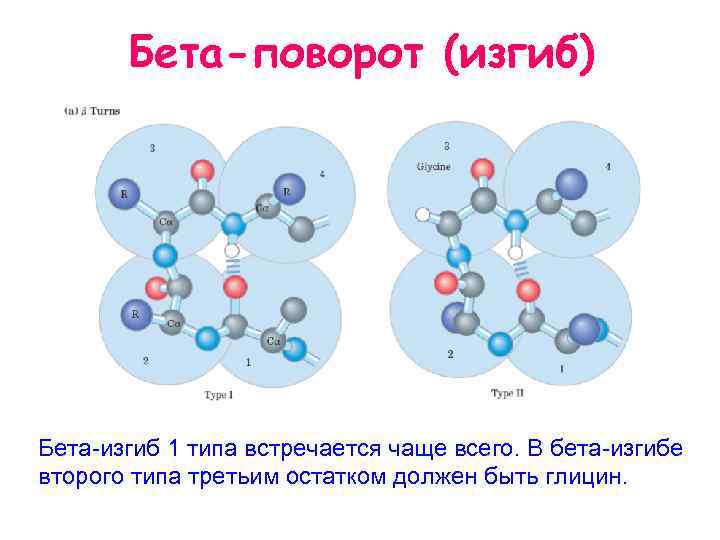
Бета-поворот (изгиб) Бета изгиб 1 типа встречается чаще всего. В бета изгибе второго типа третьим остатком должен быть глицин.
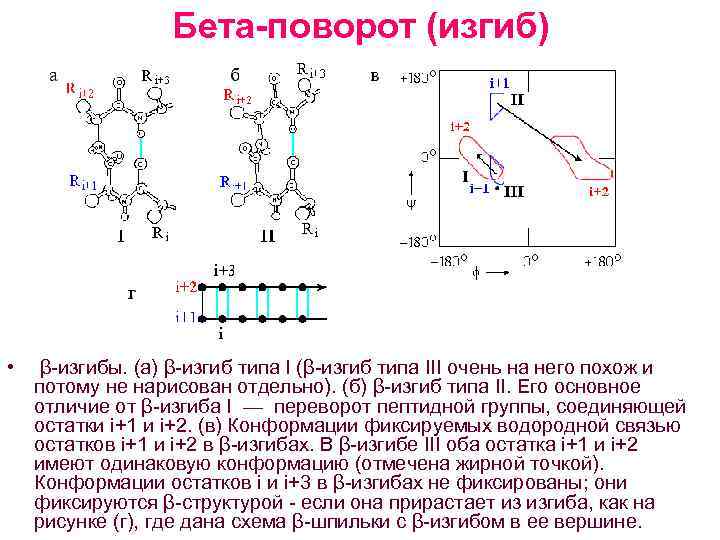
Бета-поворот (изгиб) • β изгибы. (а) β изгиб типа I (β изгиб типа III очень на него похож и потому не нарисован отдельно). (б) β изгиб типа II. Его основное отличие от β изгиба I — переворот пептидной группы, соединяющей остатки i+1 и i+2. (в) Конформации фиксируемых водородной связью остатков i+1 и i+2 в β изгибах. В β изгибе III оба остатка i+1 и i+2 имеют одинаковую конформацию (отмечена жирной точкой). Конформации остатков i и i+3 в β изгибах не фиксированы; они фиксируются β структурой если она прирастает из изгиба, как на рисунке (г), где дана схема β шпильки с β изгибом в ее вершине.

Пролин. Структурные особенности Пролин имеет ограничения для углов фи и пси из за наличия 5 членного кольца. Угол фи ограничивается 60 а угол пси группируется около значений 45 и +135 в спиральных и бета складчатых областях на карте Рамачндрана. На рисунке приведена карта, на которую нанесены данные об углах пролина взятые из примерно 160 решенных структур. Спирали. Остатки пролина часто встречаются в качестве первой аминокислоты, на N конце спирали, где потеря H связи иминогруппой пролина не оказывает значительного влияния. При анализе структур с высоким разрешением, пролин наиболее часто встречается на втором месте в спирали, и примерно 90% пролинов встречаются в первом витке спирали. Если пролин встречается после 4 го остатка, то это приводит к изгибу спирали вследствие невозможности образования Н связи внутри спирали, а также стерическими затруднениями, приводящими к неспособности принять спиральную геометрию.
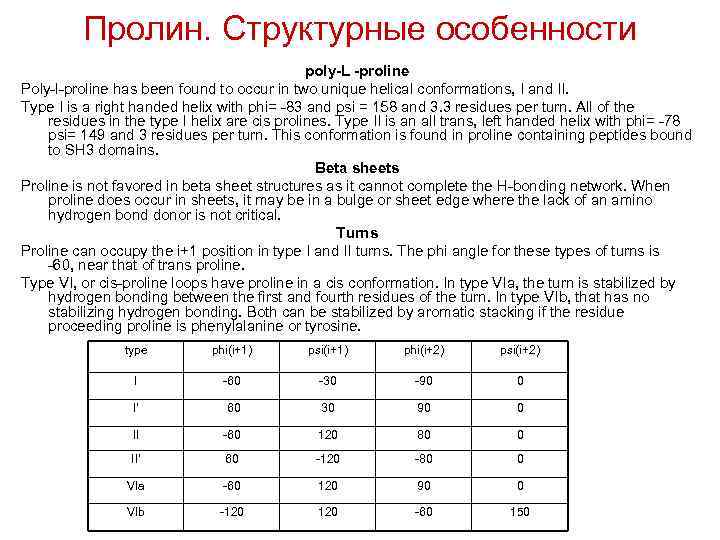
Пролин. Структурные особенности poly-L -proline Poly l proline has been found to occur in two unique helical conformations, I and II. Type I is a right handed helix with phi= 83 and psi = 158 and 3. 3 residues per turn. All of the residues in the type I helix are cis prolines. Type II is an all trans, left handed helix with phi= 78 psi= 149 and 3 residues per turn. This conformation is found in proline containing peptides bound to SH 3 domains. Beta sheets Proline is not favored in beta sheet structures as it cannot complete the H bonding network. When proline does occur in sheets, it may be in a bulge or sheet edge where the lack of an amino hydrogen bond donor is not critical. Turns Proline can occupy the i+1 position in type I and II turns. The phi angle for these types of turns is 60, near that of trans proline. Type VI, or cis proline loops have proline in a cis conformation. In type VIa, the turn is stabilized by hydrogen bonding between the first and fourth residues of the turn. In type VIb, that has no stabilizing hydrogen bonding. Both can be stabilized by aromatic stacking if the residue proceeding proline is phenylalanine or tyrosine. type phi(i+1) psi(i+1) phi(i+2) psi(i+2) I 60 30 90 0 I' 60 30 90 0 II 60 120 80 0 II' 60 120 80 0 VIa 60 120 90 0 VIb 120 60 150
FBB-belok2-2013.ppt