Химические элементы O2 и N2.pptx
- Количество слайдов: 12
 Химические элементы O 2 и N 2 Лупанова Дарья, 11 «А» класс
Химические элементы O 2 и N 2 Лупанова Дарья, 11 «А» класс
 Кислород – О 2 Кислород - элемент 16 -й группы (по устаревшей классификации — главной подгруппы VI группы), второго периода ПСХЭ, с атомным номером 8. Кислород (при нормальных условиях) — газ без цвета, вкуса и запаха, молекула которого состоит из двух атомов кислорода (формула O 2 ), в связи с чем его также называют дикислород.
Кислород – О 2 Кислород - элемент 16 -й группы (по устаревшей классификации — главной подгруппы VI группы), второго периода ПСХЭ, с атомным номером 8. Кислород (при нормальных условиях) — газ без цвета, вкуса и запаха, молекула которого состоит из двух атомов кислорода (формула O 2 ), в связи с чем его также называют дикислород.
 Получение. В промышленности кислород получают из воздуха. Основной способ получения - криогенная ректификация. Также успешно применяются в промышленности кислородные установки, работающие на основе мембранной технологии. Существуют и некоторые другие способы:
Получение. В промышленности кислород получают из воздуха. Основной способ получения - криогенная ректификация. Также успешно применяются в промышленности кислородные установки, работающие на основе мембранной технологии. Существуют и некоторые другие способы:
 Физические свойства При нормальных условиях кислород — это газ без цвета, вкуса и запаха. Немного тяжелее воздуха. 1 л его имеет массу 1, 429 г. Слабо растворяется в воде и спирте, но хорошо растворяется в расплавленном серебре. Жидкий кислород (температура кипения − 182, 98 °C) — жидкое состояние кислорода, бледно-голубая жидкость. Твёрдый кислород (температура плавления − 218, 35 °C) — твёрдое состояние кислорода, синие кристаллы.
Физические свойства При нормальных условиях кислород — это газ без цвета, вкуса и запаха. Немного тяжелее воздуха. 1 л его имеет массу 1, 429 г. Слабо растворяется в воде и спирте, но хорошо растворяется в расплавленном серебре. Жидкий кислород (температура кипения − 182, 98 °C) — жидкое состояние кислорода, бледно-голубая жидкость. Твёрдый кислород (температура плавления − 218, 35 °C) — твёрдое состояние кислорода, синие кристаллы.
 Химические свойства Сильный окислитель, самый активный неметалл после фтора, взаимодействует со всеми элементами, кроме гелия, неона, аргона и фтора, образуя оксиды. Кислород реагирует непосредственно со всеми простыми веществами, кроме Au и инертных газов (He, Ne, Ar, Kr, Xe, Rn); реакции с галогенами происходят под воздействием электрического разряда или ультрафиолета.
Химические свойства Сильный окислитель, самый активный неметалл после фтора, взаимодействует со всеми элементами, кроме гелия, неона, аргона и фтора, образуя оксиды. Кислород реагирует непосредственно со всеми простыми веществами, кроме Au и инертных газов (He, Ne, Ar, Kr, Xe, Rn); реакции с галогенами происходят под воздействием электрического разряда или ультрафиолета.
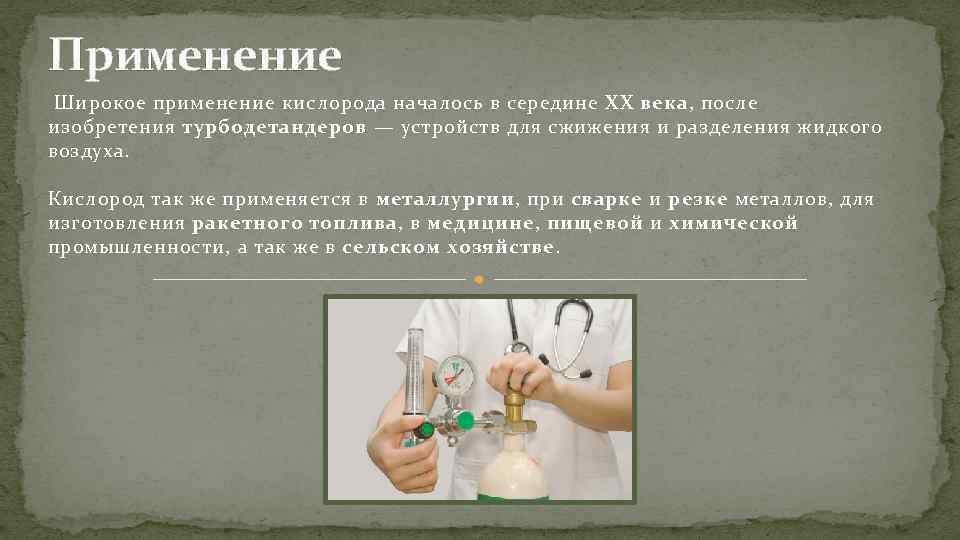 Применение Широкое применение кислорода началось в середине XX века, после изобретения турбодетандеров — устройств для сжижения и разделения жидкого воздуха. Кислород так же применяется в металлургии, при сварке и резке металлов, для изготовления ракетного топлива, в медицине, пищевой и химической промышленности, а так же в сельском хозяйстве.
Применение Широкое применение кислорода началось в середине XX века, после изобретения турбодетандеров — устройств для сжижения и разделения жидкого воздуха. Кислород так же применяется в металлургии, при сварке и резке металлов, для изготовления ракетного топлива, в медицине, пищевой и химической промышленности, а так же в сельском хозяйстве.
 Азот – N 2 Азот - элемент 15 -й группы (по устаревшей классификации — главной подгруппы V группы), второго периода ПСХЭ, с атомным номером 7. Относится к пниктогенам. Азот — двухатомный газ без цвета, вкуса и запаха. Один из самых распространённых элементов на Земле. Весьма инертен.
Азот – N 2 Азот - элемент 15 -й группы (по устаревшей классификации — главной подгруппы V группы), второго периода ПСХЭ, с атомным номером 7. Относится к пниктогенам. Азот — двухатомный газ без цвета, вкуса и запаха. Один из самых распространённых элементов на Земле. Весьма инертен.
 Получение. В лабораториях его получают по реакции разложения нитрита аммония. Наиболее чистый азот можно получить разложением азидов металлов: Ещё один лабораторный способ получения азота — нагревание смеси дихромата калия и сульфата аммония. Один из лабораторных способов — пропускание аммиака над оксидом меди (II) при температуре ~700 °C.
Получение. В лабораториях его получают по реакции разложения нитрита аммония. Наиболее чистый азот можно получить разложением азидов металлов: Ещё один лабораторный способ получения азота — нагревание смеси дихромата калия и сульфата аммония. Один из лабораторных способов — пропускание аммиака над оксидом меди (II) при температуре ~700 °C.
 Физические свойства При нормальных условиях азот — это бесцветный газ, не имеет запаха, мало растворим в воде. В жидком состоянии (темп. кипения − 195, 8 °C) — бесцветная, подвижная, как вода, жидкость. Плотность жидкого азота 808 кг/м³. При контакте с воздухом поглощает из него кислород. При − 209, 86 °C азот переходит в твёрдое состояние в виде снегоподобной массы или больших белоснежных кристаллов. При контакте с воздухом поглощает из него кислород, при этом плавится, образуя раствор кислорода в азоте.
Физические свойства При нормальных условиях азот — это бесцветный газ, не имеет запаха, мало растворим в воде. В жидком состоянии (темп. кипения − 195, 8 °C) — бесцветная, подвижная, как вода, жидкость. Плотность жидкого азота 808 кг/м³. При контакте с воздухом поглощает из него кислород. При − 209, 86 °C азот переходит в твёрдое состояние в виде снегоподобной массы или больших белоснежных кристаллов. При контакте с воздухом поглощает из него кислород, при этом плавится, образуя раствор кислорода в азоте.
 Химические свойства Азот в свободном состоянии существует в форме двухатомных молекул N 2. Молекула азота крайне прочна, способна выдержать реакцию диссоциации N 2 ↔ 2 N. Молекула азота неполярна и слабо поляризуется, силы взаимодействия между молекулами очень слабые, поэтому в обычных условиях азот газообразен. Вследствие большой прочности молекулы азота некоторые его соединения эндотермичны (многие галогениды, азиды, оксиды), соединения азота термически малоустойчивы и довольно легко разлагаются при нагревании. Именно поэтому азот на Земле находится по большей части в свободном состоянии.
Химические свойства Азот в свободном состоянии существует в форме двухатомных молекул N 2. Молекула азота крайне прочна, способна выдержать реакцию диссоциации N 2 ↔ 2 N. Молекула азота неполярна и слабо поляризуется, силы взаимодействия между молекулами очень слабые, поэтому в обычных условиях азот газообразен. Вследствие большой прочности молекулы азота некоторые его соединения эндотермичны (многие галогениды, азиды, оксиды), соединения азота термически малоустойчивы и довольно легко разлагаются при нагревании. Именно поэтому азот на Земле находится по большей части в свободном состоянии.
 Применение Жидкий азот применяется как хладагент и для криотерапии. Промышленные применения газообразного азота обусловлены его инертными свойствами. Газообразный азот пожаро- и взрывобезопасен, препятствует окислению, гниению. Важной областью применения азота является его использование для дальнейшего синтеза самых разнообразных азотосодержащих соединений.
Применение Жидкий азот применяется как хладагент и для криотерапии. Промышленные применения газообразного азота обусловлены его инертными свойствами. Газообразный азот пожаро- и взрывобезопасен, препятствует окислению, гниению. Важной областью применения азота является его использование для дальнейшего синтеза самых разнообразных азотосодержащих соединений.
 Спасибо за внимание
Спасибо за внимание


