Л 1 Введение, сырье.ppt
- Количество слайдов: 93

ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ 5 курс 8 лекций 2 лабораторные работы 4 семинара рефераты экзамен Елисеев Сергей Юрьевич Канд. хим. наук, доцент кафедры химии БГПУ

Литература l Основная l Алтухов К. В. , Мухленов И. П. , Тумаркина Е. С. Химическая технология. – М. : Просвещение, 1985. – 304 с. l Аранская О. С. Сборник задач и упражнений по химической технологии и биотехнологии. 2 -е изд. - Мн. : - Университетское, 1989. – 311 с. l Аранская В. С. Самастойная работа студэнтаў пры вывученні хімічнай тэхналогіі і біятэхналогіі. - Віцебск. : В-ва ВДУ ім П. М. Машэрава, 1995. - 47 с. l Аранская О. С. , Слабин В. К. Лабораторный практикум по химической технологии с основами биотехнологии. - Витебск. : Из-во ВГУ им П. М. Машерова. 2000. - 43 с. l Ключников Н. Г. Практические занятия по химической технологии. 4 -е изд, перераб. – М. : Просвещение, 1978. – 223 с. l Мухленов И. П. , Горштейн А. Е, Тумаркина Е. С. , Кузичкин Н. В. Основы химической технологии. 4 -е изд. , перераб. и доп. – М: Высшая школа, 1991. – 462 с. l Соколов Р. С. Химическая технология: Учеб. пособие для студентов ВУЗов: В 2 т. - М. : Гуманитар. изд. центр ВЛАДОС, 2000. – Т. 1. – 368 с. – Т. 2. – 448 с.

Предмет и задачи химической технологии Технология – наука о производствах, методах и аппаратах, посредством которых исходные материалы превращают в предметы потребления или средства производства. Технология: Механическая – изучает процессы, в которых меняется лишь форма или физические свойства перерабатываемого материала. Химическая – изучает процессы, связанные с изменением химического состава, свойств и внутреннего строения перерабатываемого материала.

Химическая технология – естественная и прикладная наука l предмет изучения - химическое производство; l цель изучения создание целесообразного способа производства необходимых человеку продуктов; l методы исследования экспериментальный, моделирование и системный анализ.

Особенности химической промышленности l высокая материалоёмкость производства; l высокое энергопотребление, которое в два раза превосходит энергопотребление промышленности в целом; l низкая доля живого труда и высокая степень автоматизации и механизации производства.

Продукция химической промышленности I класс Продукты неорганического синтеза II класс Полимерные материалы (синтетические каучуки, пластмассы, химические волокна) III класс Лакокрасочные материалы IV класс Синтетические красители и полупродукты V класс Продукты органического синтеза (нефте-, коксо- и лесохимия) VI класс Химические реактивы и чистые вещества VII класс Химико-фармацевтические препараты (Не относят: металлургия, производство силикатных материалов, биотехнологии, переработка растительного и животного сырья. )

Классификация химической технологии l. Неорганическая химическая технология l. Органическая химическая технология В химической технологии рассматривается совокупность физических и химических явлений, из которых и складывается Технологический Процесс. Стадии ТП: подвод компонентов; химическая реакция; отвод из зоны реакции полученных продуктов.

Неорганическая химическая технология l основной неорганический синтез - производство кислот, щелочей, солей и минеральных продуктов; l тонкий неорганический синтез - производство неорганических препаратов, реактивов, редких элементов, материалов электроники, лекарственных веществ и др. ; l ядерно-химическая технология; l металлургия - производство черных и цветных металлов; l силикатные производства - производства вяжущих материалов, керамических изделий, стекла.

Органическая химическая технология l переработка нефти и газа - первичная переработка (первичное разделение, очистка, облагораживание) газообразных, жидких и твердых природных углеводородов (ископаемого топливного сырья); l нефтехимический синтез - производство органических продуктов и полупродуктов на основе переработки газообразных, жидких и твердых углеводородов, а также на основе оксидов углерода и водорода; l основной органический синтез - производство органических продуктов на основе главным образом углеводородного сырья;

Органическая химическая технология l биотехнология - производство кормовых дрожжей, аминокислот, ферментов, антибиотиков и др. на основе биологических процессов; l тонкий органический синтез - производство органических препаратов, реактивов, лекарственных веществ, средств защиты растений и др. ; l высокомолекулярная технология - получение высокомолекулярных соединений (синтетический каучук, пластмассы, химические волокна, пленкообразующие вещества); l технологии переработки растительного и животного сырья.

ХИМИЧЕСКОЕ ПРОИЗВОДСТВО Объект изучения химической технологии: Химическое производство - совокупность процессов и операций, осуществляемых в машинах и аппаратах и предназначенных для переработки сырья путем химических превращений в необходимые продукты.
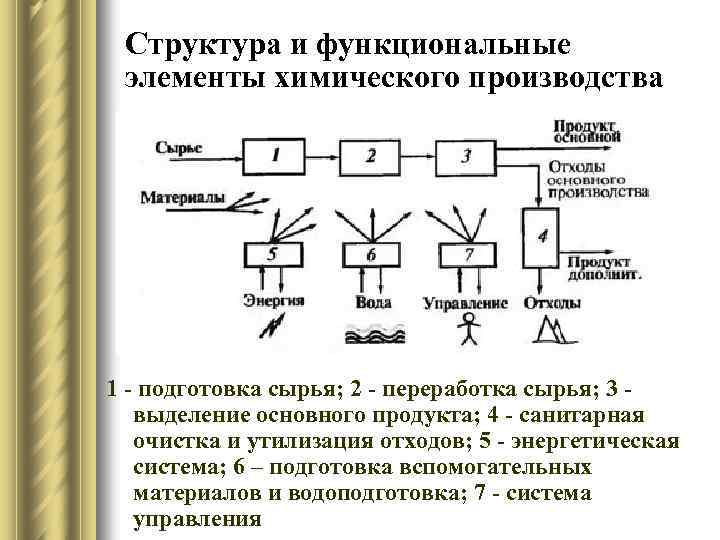
Структура и функциональные элементы химического производства 1 - подготовка сырья; 2 - переработка сырья; 3 выделение основного продукта; 4 - санитарная очистка и утилизация отходов; 5 - энергетическая система; 6 – подготовка вспомогательных материалов и водоподготовка; 7 - система управления

Требования к химическому производству: l получение в производстве необходимого продукта; l экологическая безопасность; l безопасность и надежность эксплуатации; l максимальное использование сырья и энергии; l максимальная производительность труда.

Компоненты химических производств l Переменные (сырье, вспомогательные материалы, продукты – основной и дополнительный, электро- и тепловаяэнергия, отходы производства) l Постоянные (завод – аппаратура, здания и сооружения, обслуживающий персонал)

Состав химических производств l собственно химическое производство; l хранилища сырья, продуктов и других материалов; l транспортировка сырья, продуктов, промежуточных веществ, отходов; l обслуживающий персонал производственного подразделения; l система управления, обеспечения и безопасности

Технологический процесс Последовательное проведение нескольких химических реакций, механических и физико-химических операций. Разделяется на несколько стадий, которые проводятся в различных аппаратах. Стадия: одна реакция и несколько операций (нагревание/охлаждение, смешение, перекачка, фильтрование) Технологическая схема производства сочетание всех стадий, аппаратов и транспортных сетей

Виды процессов и операций 1. Механические и гидромеханические процессы l измельчение; l сортировка; l подача сырья в реакционный аппарат; l удаление из аппарата и транспортировка продуктов реакции в другие аппараты; l фильтрование и промывка. Все они протекают без изменения химического и фазового состава обрабатываемого материала.

Виды процессов и операций 2. Теплообменные процессы l нагрев, l охлаждение, l изменение фазового (агрегатного) состояния

Виды процессов и операций 3. Массообменные процессы (физикохимические) l растворение; l поглощение или конденсация; l извлечение или экстракция; l перегонка и ректификация

Виды процессов и операций энергетические процессы - взаимное преобразование различных видов энергии (тепловой, механической, электрической) в турбинах, генераторах, моторах

Виды процессов и операций процессы управления - получение и передача информации о состоянии потоков и веществ, изменение их состояния. К устройствам управления относятся датчики, сигнальные и информационные системы

Химические процессы – изменение химического состава в химических реакторах. Требования к химическим реакциям l при проведении химических реакций исходные вещества должны достигнуть зоны реакции; l продукты реакции должны быть удалены из зоны реакции;

l Химические реакции протекают в процессах периодических или непрерывных. l Периодический процесс – это когда порция сырья загружается в аппарат, проходит в нем ряд стадий обработки и затем выгружаются все образовавшиеся вещества. Время цикла – продолжительность производственного процесса. l Непрерывный процесс – когда поступление сырья в аппарат и выпуск продукции происходят непрерывно.

Каталитические реакции l повысить производительность процесса; l снизить температуру и давление; l повысить выход продукта.

Непрерывно-действующие реакторы называются проточными, т. к. через них постоянно протекают потоки реагирующих масс. - Полное смешение (турбулентный режим) – концентрация реагентов одинакова во всем объеме аппарата. - Идеальное вытеснение – когда исходная смесь не перемешивается с продуктами реакции. Проточные по температурному режиму: - Изотермические (температура постоянна во всем реакционном объеме); - Адиабатические (нет отвода или подвода тепла) - Программно-регулируемые (политермические)

l Технологические процессы делятся на однородные (гомогенные) и неоднородные (гетерогенные). l Гомогенные системы – все вещества находятся в одной фазе: газовой – Г, жидкой – Ж, твердой – Т. l Гетерогенные системы – включают две или большее количество фаз: Г-Ж, Г-Т, Ж-Т, Т-Т, Ж-Ж, Г-Ж-Т, Г-Т-Т, Ж-Т-Т, Г-Ж-Т-Т. l Фаза, часть системы, отличающаяся по своим физическим или химическим свойствам от других частей системы и отделенная от них поверхностью раздела.

l Технологические схемы Схема с открытой цепью состоит из аппаратов, через которые реагирующие компоненты проходят лишь один раз (проточная схема). Если степень превращения в одном аппарате невелика, в схему включают несколько однотипных аппаратов – батарею реакторов. (Кислотная абсорбция нитрозных газов. ) Циклическая схема предусматривает многократное возвращение в один и тот же аппарат всех реагирующих масс или одной из фаз в гетерогенном процессе, вплоть до достижения заданной степени превращения исходных веществ. (Синтез аммиака, спиртов, моторного топлива. )

l Производительностью аппаратов называется количество выработанного продукта G или переработанного сырья за единицу времени (кг/ч; т/ч) (объем V) l = G/. = V/ l Повышение производительности работы аппарате может быть достигнуто увеличением его размеров или интенсивности работы. l Интенсивностью работы аппарата I называется отношение ( ) производительности аппарата к какой-либо величине его размера (vа): I = /vа = G/ vа. I = V/ vа

Выход продукта отношение фактически полученного продукта к максимально возможному по уравнению реакции = Gф/Gт.

ОСНОВНЫЕ ПРИНЦИПЫ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ l непрерывность процесса; l противоток; l автотермичность; l комплексное использование сырья; l комбинирование и кооперирование производств.

Принцип непрерывности процесса подача сырья и отбор продуктов осуществляется непрерывно или порциями без остановки аппарата или системы l экономия технологического времени; l устойчивость и равномерность протекания процесса, постоянно поддерживается оптимальный режим производства; l возможность автоматизации и механизации производства.

Принцип противотока Противотоком называются противоположно направленные движения взаимодействующих веществ l l l проведение химических реакций; поглощение газов; растворение твёрдых тел; нагревание исходных веществ; охлаждение продуктов реакции.

Принцип комплексного использования сырья превращение отходов в побочные продукты, что позволяет полнее использовать все содержащиеся в сырье вещества. l снижение себестоимости продукции; l предотвращает загрязнение окружающей среды

Принцип кооперативного производства Химическое предприятие поставляет один или несколько готовых продуктов в качестве сырья другому предприятию (энергетической промышленности, машиностроение, транспорт. )

РАЗРАБОТКА ТЕХНОЛОГИЧЕСКОЙ СХЕМЫ ПРОИЗВОДСТВА ЭТАПЫ l Научный (лабораторный) l Опытно-промышленный l Промышленный
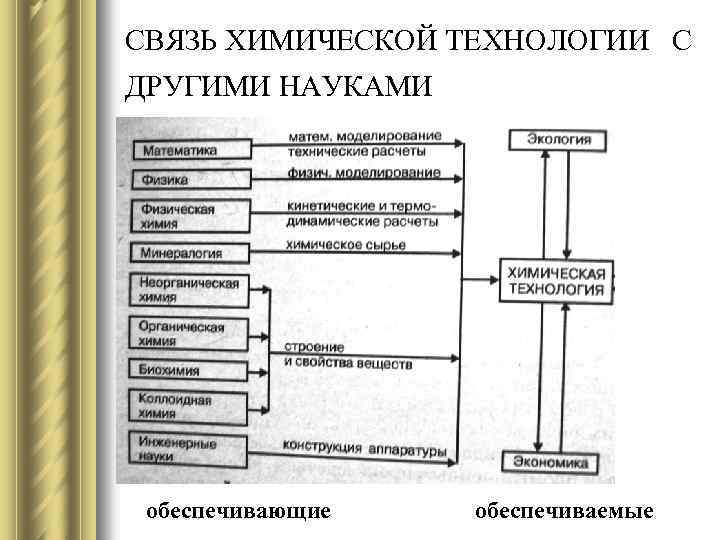
СВЯЗЬ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ С ДРУГИМИ НАУКАМИ обеспечивающие обеспечиваемые

этапы развития химического производства Начальные этапы – на основе опыта l Керамическая посуда l Выплавка и обработка металлов (бронза, железо) l Производство кирпича, извести, стекла, минеральных красок и органических красителей, поваренной соли l Производство фарфора, бумаги и черного пороха

этапы развития химического производства Средние века – химический эксперимент l серной и азотной кислоты, l соли, l поташа - K 2 CO 3 , l сера l селитра (для изготовления пороха)

XVII - XVIII века –промышленное производство l 1789 год - получение синтетической соды Na 2 SO 4 + 2 C = Na 2 S + 2 CO 2 Н = 502 к. Дж/моль, Na 2 S + Ca. CO 3 = Na 2 CO 3 + Ca. S S = 370 Дж/моль град. l NH 3 + H 2 O + CO 2 = NH 4 HCO 3 Na. Cl + NH 4 HCO 3 Na. HCO 3 + NH 4 Cl 2 Na. HCO 3 = Na 2 CO 3 + CO 2 + H 2 O. H 4 Cl + Ca(OH)2 = Ca. Cl 2 + NH 3 + H 2 O l серная кислота по камерному способу для получения сульфата натрия из хлорида натрия: 2 Na. Cl + H 2 SO 4 = Na 2 SO 4 + 2 HCl l Выплавка чугуна, l Топливные производства (кокс, древесный уголь) l Производство удобрений

XIX век l черная металлургия (выплавка стали в кислородных конвертерах и мартеновских печах) l промышленность органического синтеза (органических красителей – индиго и ализарина, лекарственных средств, взрывчатых веществ) l контактный способ производства серной кислоты l электролитический способ производства хлора и едкого натра

XX век l высокомолекулярные вещества (искусственные волокна, бездымный порох, пласмассы) l 1915 год Германия – связывание атмосферного азота l крекинг нефтепродуктов l синтез синтетического каучука Лебедевым в 1932 году

Химическая промышленность в Белоруссии l 1930 – фабрика искусственного волокна (Могилев) l 1956 – завод «Крион» , Минск (кислород, азот, аргон); завод стекловолокна г. Полоцк l 1957 – завод РТИ в Борисове l 1963 -1969 гг – калийный комбинат Солигорск l 1963 – азотнотуковый завод г. Гродно l 1968 – гомельский химический завод

нефтеперерабатывающие предприятия 60 -70 гг. l новополоцкий нефтеперерабатывающим заводом «Нафтан» . проектная мощность завода - 24 млн. тонн нефти в год; l б) мозырский нефтеперерабатывающий завод, проектная мощность - 16 млн. тонн нефти в год.

Химическая промышленность в Белоруссии l l l Заводы полимерных материалов: 1965 год - завод пластмассовых изделий (Борисов); 1965 год светлогорский завод искусственного волокна; химический комбинат «Полимер» г. Полоцк; комбинат синтетического волокна «Химволокно» г. Могилев; 1 -я очередь гродненского завода синтетического волокна. 1975 год - Белорусский шинный комбинат «Белшина» (? ).

Сырьё химической промышленности

Технологическая схема химического производства

Сырьём называются природные или промышленные материалы, которые используются в производстве для получения промышленной продукции. l ШИХТА – смесь, состоящая из нескольких видов твердых материалов. l ПУЛЬПА – полужидкая смесь нескольких материалов l ШЛАМ – вязкая, малотекучая смесь нескольких материалов

l ПРОМЕЖУТОЧНЫЙ ПРОДУКТ (полупродукт, полуфабрикат) – продукт, получаемых в какой-либо промежуточной стадии. l ПОБОЧНЫЕ ПРОДУКТЫ – используемые отходы производства l ОТХОДЫ производства – образующиеся наряду с целевым конечные продукты. l ОТБРОСЫ – неиспользуемые отходы производства.

Классификация сырья l по происхождению (минеральное, растительное, животное, вода, воздух) (Минеральное - рудное, нерудное, горючее); l по химическому составу; l по агрегатному состоянию (тв. , ж. , г. ); l по предназначению.

Классификация сырья l природное; l первичное (извлекаемое из природного источника; l вторичное (промежуточные и побочные продукты); l искусственное (полученное в результате переработки природного сырья)
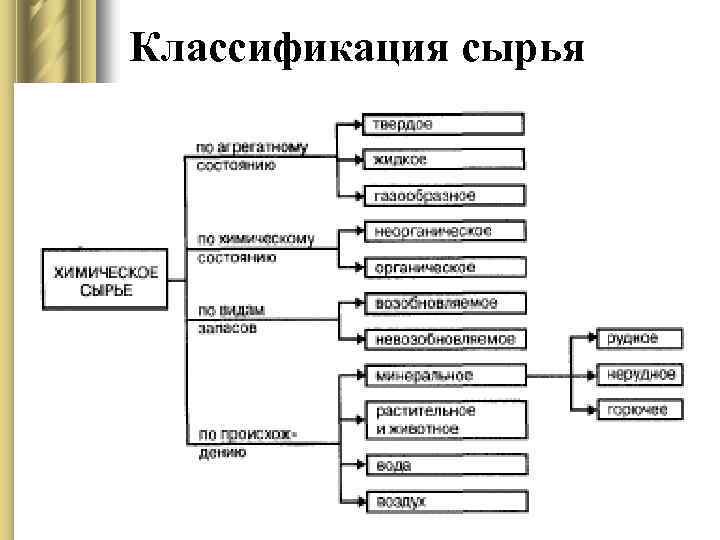
Классификация сырья

Минеральное сырьё добываемые из земных недр минералы l - рудное – для получения металлов; l - нерудное – для производства неметаллов (Cl, S, P…), (удобрений, соды, щелочей, кислот…); l - горючее.

Рудное сырье l оксиды (Mеn. Om) l сульфиды (Mеn. Sm) l Полиметаллические руды – содержат несколько цветных металлов

Нерудное сырье горные породы или минералы, которые используют для: l - производства неметаллов - серы, хлора, фосфора; l - других химических продуктов удобрений, соды, щелочей, кислот.

Классификация нерудных ископаемых l Строительные материалы (гравий, песок, глины, строительные камни). l Индустриальное сырьё - без химической переработки (графит, слюда, асбест). l Химическое минеральное сырьё подвергается химической переработке (сера, селитра, фосфоритная мука, поваренная и калийная соли). l Драгоценное, полудрагоценное и поделочное сырьё: алмазы, изумруды, рубины, малахит, яшма, мрамор.

Горючее минеральное сырьё это ископаемые, которые могут служить в качестве топлива l каменный и бурый угли, l горючие сланцы, l нефть, l природный газ Топливом называют естественные или искусственные горючие органические материалы, служащие источником тепловой энергии и сырьём для химической промышленности.

Сырьё растительного и животного происхождения l Пищевое l техническое (дерево, хлопок, лён, кожа, шерсть, пушнина) Техническое использование пищевого сырья: l картофель и другие продукты - этиловый спирт ; l животные и растительные масла - мыло и косметические средства. l растительные масла – моторные топлива

ТРЕБОВАНИЯ К СЫРЬЮ l малостадийность производственного процесса; l агрегатное состояние, l минимальное рассеяние подводимой энергии; l возможно более низкие параметры процесса; l максимальное содержание целевого продукта в реакционной смеси.

Подготовка сырья l Измельчение l Классификация l Обезвоживание l Сушка l Обогащение

Методы обогащения Механические l рассеивание (грохочение), l гравитационное разделение, l электромагнитная и электростатическая сепарация, Химические Физико-химические: флотация

Пенная флотация Flotation (англ. ) - всплывание основан на различии в смачивании водой мелких частиц различных веществ, входящих в состав сырья

Краевой угол смачивания Смачиваемая (2, острый краевой угол ) и не смачиваемая (1, тупой краевой угол ) жидкостью твердая частица
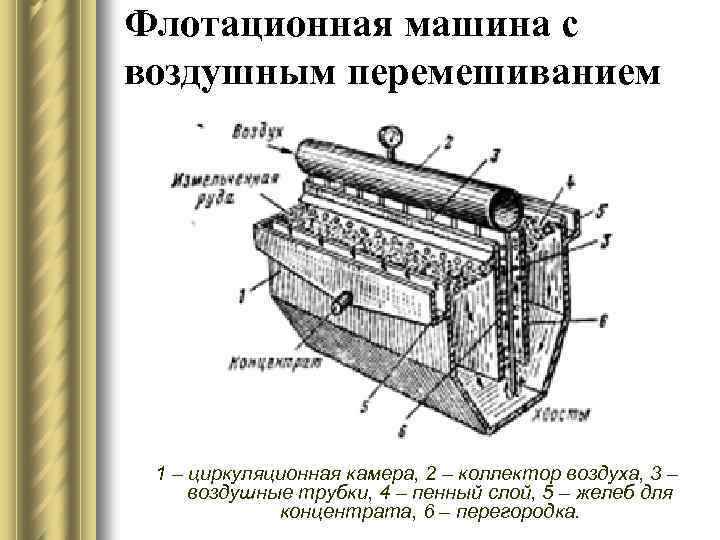
Флотационная машина с воздушным перемешиванием 1 – циркуляционная камера, 2 – коллектор воздуха, 3 – воздушные трубки, 4 – пенный слой, 5 – желеб для концентрата, 6 – перегородка.

Принцип пенной флотации а — механическая флотационная машина: 1 — мешалка; 2 — труба для подачи воздуха; 3 — решетка; 4 — желоб для концентрата; б - флотация не смачиваемых водой гидрофобных частиц в пузырьке воздуха: 1 — пузырек воздуха; 2— частицы; в — адсорбция собирателя на поверхности частицы флотируемого материала: 1 — частица; 2 — молекулы или ионы собирателя (коллектора) ПАВ 1, 3 – воздух, 4 – молекулы или ионы пенообразователя ПАВ 2.

Флотагенты l Собиратель (коллектор, ПАВ 1) – придание частице флотируемости l Регуляторы: – Активаторы (способствуют абсорбции собирателей) – Депрессоры (увеличивают гидрофильность побочных в-в) l Пенообразователи (ПАВ 2)

Флотация l Коллективная l Селективная – последовательная флотация полиметаллических руд в нескольких машинах.

Водные ресурсы и химическая технология l Атмосферные воды l Поверхностные воды l Подземные воды Для промышленного водоснабжения – поверхностные воды
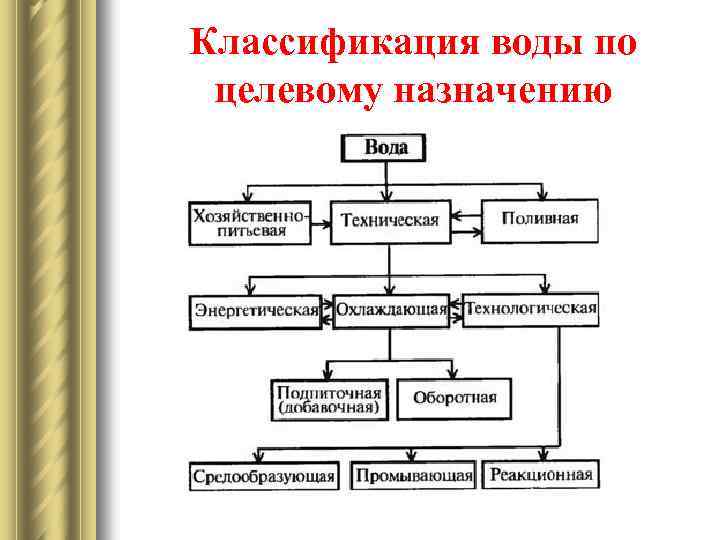
Классификация воды по целевому назначению

Примеси в воде l грубодисперсные взвеси, с размером частиц более 100 Å; l коллоидные частицы, с размером частиц от 1 до 100 Å; l молекулярно-дисперсные частицы (растворенные соли и органические вещества)

Водоподготовка комплексная система операций, обеспечивающая очистку воды путем удаления из нее вредных примесей, находящихся в растворенном, коллоидном и взвешенном состоянии l Промышленная l Питьевая
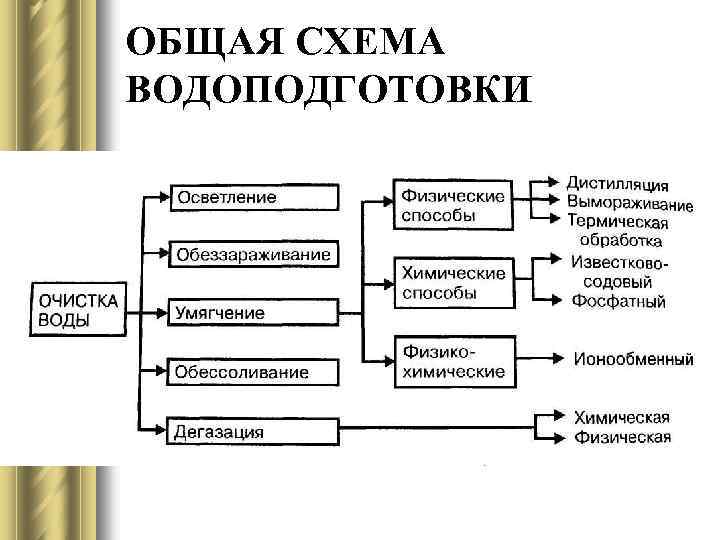
ОБЩАЯ СХЕМА ВОДОПОДГОТОВКИ

Очистка питьевой воды Качество питьевой воды оценивается по следующим показателям: l бактериальная загрязнённость, l вкус, l цвет, l запах, l жёсткость.

Основные показатели качества l общее число бактерий - не более 100 шт. /мл; l кишечной палочки - не более 3 шт. /л; l общее содержание солей не должно превышать 1000 мг/л.

Классификация воды по жесткости (мг-экв/л) l Очень мягкая l Мягкая l Умеренно жёсткая l Жёсткая l Очень жёсткая 0 - 1, 5 - 3 3 -6 6 - 10 > 10

Этапы водоподготовки Осветление: l Отстаивание - грубодисперсные l Коагуляция - растворенные и коллоидные l Фильтрация

Механизм коагуляции Коагуляция - это процесс слипания коллоидных частиц под действием каких-либо внешних факторов, с образованием частиц более крупных размеров. l Al 2(SO 4)3 l Al 3+ + {КЧ}- = осадок l Al 2(SO 4)3 + 3 Ca(HCO 3)2 = 2 Al(OH)3 + 3 Ca. SO 4 + H 2 O

Этапы водоподготовки Умягчение воды Жесткость воды l временная жёсткость (карбонатная жёсткость); l постоянная или некарбонатная жёсткость; l общая жёсткость.

Химические методы удаления жесткости l Известковый (Са(ОН)2) l Натронный (Na. OH) l Содовый (Na 2 CO 3 ) l Фоcфатный (Na 3 PO 4)

Известковый метод Обработка воды гашеной известью Ca(HCO 3)2 + Ca(OH)2 = 2 Ca. CO 3↓ + 2 H 2 O; Mg(HCO 3)2 + Ca(OH)2 = Ca. CO 3↓ + Mg(OН)2↓ + H 2 O; Fe. SO 4 + Ca(OH)2 = Fe(OH)2↓ + Ca. SO 4↓; 4 Fe(OH)2 + O 2 + 2 H 2 O = 4 Fe(OH)3↓; CO 2 + Ca(OH)2 = 2 Ca. CO 3↓ + 2 H 2 O.

Натронный способ Временная и постоянная l Mg(HCO 3)2 + 2 Na. OH = Mg. CO 3↓ + Na 2 CO 3↓ + 2 H 2 O l Ca. Cl 2+2 Na. OH = Ca(OH)2↓ + 2 Na. Cl
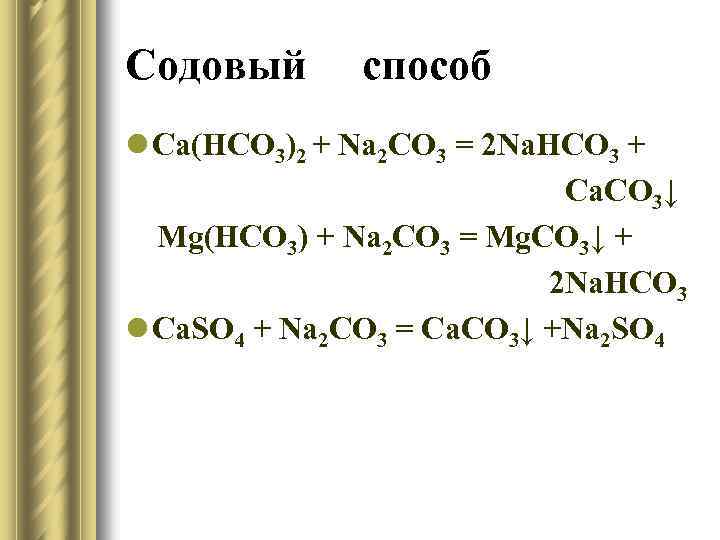
Содовый способ l Ca(HCO 3)2 + Na 2 CO 3 = 2 Na. HCO 3 + Ca. CO 3↓ Мg(HCO 3) + Na 2 CO 3 = Mg. CO 3↓ + 2 Na. HCO 3 l Ca. SO 4 + Na 2 CO 3 = Ca. CO 3↓ +Na 2 SO 4

Фосфатный способ l 3 Ca(HCO 3)2 + 2 Na 3 PO 4 = Ca 3(PO 4)2↓ + 6 Na. HCO 3 l 3 Ca. SO 4 + 2 Na 3 PO 4 = Ca 3(PO 4)2↓ + 3 Na 2 SO 4 l 3 Mg. Cl 2 + 2 Na 3 PO 4 = Mg 3(PO 4)2↓ + 6 Na. Cl

Физико-химические методы умягчения (обессоливания) воды Метод ионного обмена Ионообменные смолы: - Катиониты - Аниониты

Механизм действия ионитов Na+ -катионит l Na 2(Кат) + Ca. SO 4 = Ca(Кат) + Na 2 SO 4 (пост. ) l Na 2(Кат) + Ca(HCO 3)2 = Ca(Кат) + 2 Na. HCO 3 (врем. ) Регенерация l Ca(Кат) + 2 Na. Cl = Na 2(Кат) + Ca. Cl 2 ОН- -анионит l 2(Ан)OH + SO 42 - = (Ан)2 SO 4 + 2 OHРегенерация l (Ан)Сl + Na. OH = (Ан)OH + Na. Cl
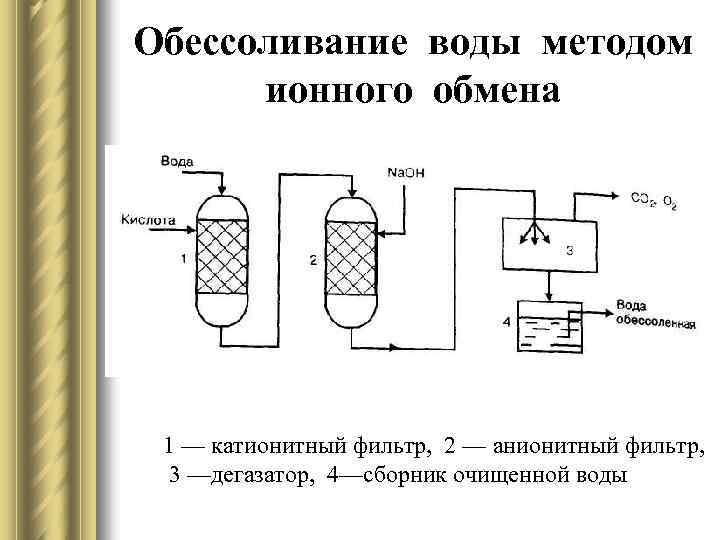
Обессоливание воды методом ионного обмена 1 — катионитный фильтр, 2 — анионитный фильтр, 3 —дегазатор, 4—сборник очищенной воды

Этапы очистки воды деаэрация или дегазация удаление О 2 и СО 2 для предотвращения коррозии (физические и химические) l N 2 H 4 (гидразин) + O 2 = N 2 + 2 H 2 O l 2 Na 2 SO 3 + O 2 = 2 Na 2 SO 4 l Слой железных опилок l СО 2 + Са(ОН)2 = Са. СО 3 + Н 2 О.

Этапы очистки воды Обеззараживание l газообразный хлор l хлорная известь l гипохлорит кальция l озонирование
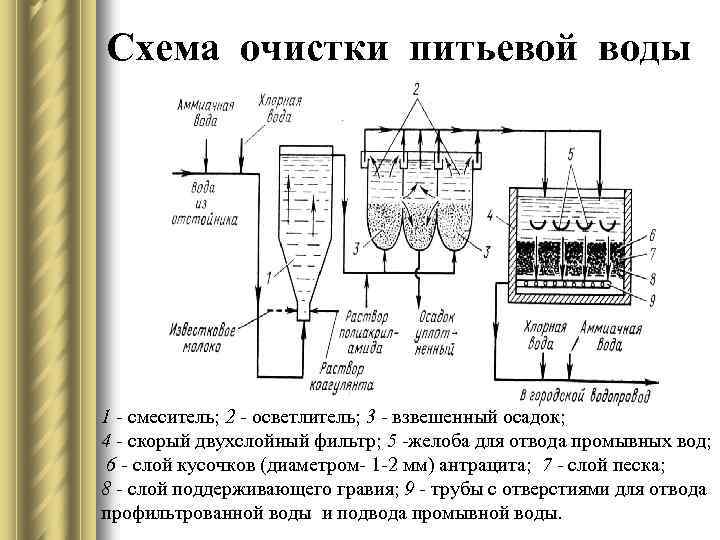
Схема очистки питьевой воды 1 - смеситель; 2 - осветлитель; 3 - взвешенный осадок; 4 - скорый двухслойный фильтр; 5 -желоба для отвода промывных вод; 6 - слой кусочков (диаметром- 1 -2 мм) антрацита; 7 - слой песка; 8 - слой поддерживающего гравия; 9 - трубы с отверстиями для отвода профильтрованной воды и подвода промывной воды.

Водооборотные циклы химических производств l Прямоточные l Оборотные

Прямоточный цикл l подаваемая от первичного источника вода после однократного использования отводится за пределы предприятия

Оборотный цикл отработанная вода подвергается охлаждению, очистке и возвращается для последующего использования в этом же производстве, т. е. замыкается в цикле (обороте).

l Градирня

l Гиперболоидные градирни
Л 1 Введение, сырье.ppt