лекция Физ.химия.pptx
- Количество слайдов: 12
 ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
 Термодинамика – наука о взаимопревращениях различных форм энергии и законах этих превращений. Термодинамика изучает: 1. Переходы энергии из одной формы в другую, от одной части системы к другой; 2. Энергетические эффекты, сопровождающие различные физические и химические процессы и зависимость их от условий протекания данных процессов; 3. Возможность, направление и пределы самопроизвольного протекания процессов в рассматриваемых условиях.
Термодинамика – наука о взаимопревращениях различных форм энергии и законах этих превращений. Термодинамика изучает: 1. Переходы энергии из одной формы в другую, от одной части системы к другой; 2. Энергетические эффекты, сопровождающие различные физические и химические процессы и зависимость их от условий протекания данных процессов; 3. Возможность, направление и пределы самопроизвольного протекания процессов в рассматриваемых условиях.
 ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ Термодинамическая система – тело или группа тел, находящихся во взаимодействии, мысленно или реально обособленные от окружающей среды. Гомогенная система – система, внутри которой нет поверхностей, разделяющих отличающиеся по свойствам части системы (фазы). Гетерогенная система – система, внутри которой присутствуют поверхности, разделяющие отличающиеся по свойствам части системы. Фаза – совокупность гомогенных частей гетерогенной системы, одинаковых по физическим и химическим свойствам, отделённая от других частей системы видимыми поверхностями раздела.
ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ Термодинамическая система – тело или группа тел, находящихся во взаимодействии, мысленно или реально обособленные от окружающей среды. Гомогенная система – система, внутри которой нет поверхностей, разделяющих отличающиеся по свойствам части системы (фазы). Гетерогенная система – система, внутри которой присутствуют поверхности, разделяющие отличающиеся по свойствам части системы. Фаза – совокупность гомогенных частей гетерогенной системы, одинаковых по физическим и химическим свойствам, отделённая от других частей системы видимыми поверхностями раздела.
 ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ Изолированная система – система, которая не обменивается с окружающей средой ни веществом, ни энергией. Закрытая система – система, которая обменивается с окружающей средой энергией, но не обменивается веществом. Открытая система – система, которая обменивается с окружающей средой и веществом, и энергией.
ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ Изолированная система – система, которая не обменивается с окружающей средой ни веществом, ни энергией. Закрытая система – система, которая обменивается с окружающей средой энергией, но не обменивается веществом. Открытая система – система, которая обменивается с окружающей средой и веществом, и энергией.
 Внутренняя энергия системы – сумма кинетической и потенциальной энергии всех частиц, составляющих систему. Первый закон (первое начало термодинамики): энергия неуничтожима и несотворяема, она только может переходить их одной формы в другую или двигателя первого рода не существует!!! ∆U = U 2 – U 1 = Q – A , т. е. Изменение внутренней энергии системы равно количеству сообщенной системе теплоты минус количество работы, совершенной системой против внешних сил.
Внутренняя энергия системы – сумма кинетической и потенциальной энергии всех частиц, составляющих систему. Первый закон (первое начало термодинамики): энергия неуничтожима и несотворяема, она только может переходить их одной формы в другую или двигателя первого рода не существует!!! ∆U = U 2 – U 1 = Q – A , т. е. Изменение внутренней энергии системы равно количеству сообщенной системе теплоты минус количество работы, совершенной системой против внешних сил.
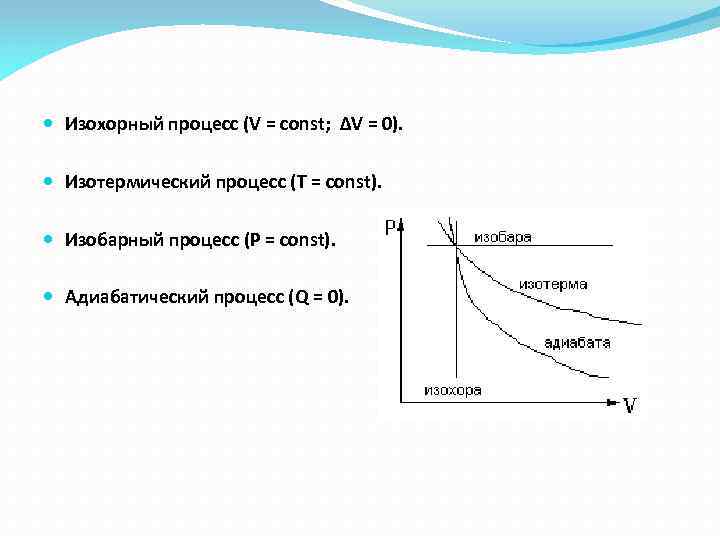 Изохорный процесс (V = const; ΔV = 0). Изотермический процесс (Т = const). Изобарный процесс (Р = const). Адиабатический процесс (Q = 0).
Изохорный процесс (V = const; ΔV = 0). Изотермический процесс (Т = const). Изобарный процесс (Р = const). Адиабатический процесс (Q = 0).
 Тепловой эффект (теплота) химической реакции – количество теплоты, выделившейся либо поглотившейся в ходе реакции. Выделение теплоты (Q > 0) => экзотермическая реакция Поглощение теплоты (Q < 0) => эндотермическая реакция Q = - ΔН (энтальпия) Единица измерения - (к. Дж/моль)
Тепловой эффект (теплота) химической реакции – количество теплоты, выделившейся либо поглотившейся в ходе реакции. Выделение теплоты (Q > 0) => экзотермическая реакция Поглощение теплоты (Q < 0) => эндотермическая реакция Q = - ΔН (энтальпия) Единица измерения - (к. Дж/моль)
 Закон Гесса: Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорноизотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
Закон Гесса: Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорноизотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
 Второе начало термодинамики теплота не может самопроизвольно переходить от менее нагретого к более нагретому (постулат Клаузиуса) Энтропия (ΔS) - мера хаотичности, неупорядоченности системы. Все самопроизвольные процессы в природе идут с увеличением энтропии. d. S=d. Q/T
Второе начало термодинамики теплота не может самопроизвольно переходить от менее нагретого к более нагретому (постулат Клаузиуса) Энтропия (ΔS) - мера хаотичности, неупорядоченности системы. Все самопроизвольные процессы в природе идут с увеличением энтропии. d. S=d. Q/T
 Третье начало термодинамики энтропия индивидуальных веществ при абсолютном нуле по шкале Кельвина равна нулю (постулат Нернста) ΔSреакции = ∑(n. S)прод. - ∑(n. S)реаг. Единицей энтропии ΔSреакции - (Дж/К), а для молярной энтропии вещества - (Дж/(моль·К)).
Третье начало термодинамики энтропия индивидуальных веществ при абсолютном нуле по шкале Кельвина равна нулю (постулат Нернста) ΔSреакции = ∑(n. S)прод. - ∑(n. S)реаг. Единицей энтропии ΔSреакции - (Дж/К), а для молярной энтропии вещества - (Дж/(моль·К)).
 Свободная энергия Гиббса Количественно зависимость между изменениями энтальпии, энтропии и свободной энергии описывается уравнением Гиббса-Гельмгольца: ΔG = ΔH - T · ΔS Единица измерения - (к. Дж)
Свободная энергия Гиббса Количественно зависимость между изменениями энтальпии, энтропии и свободной энергии описывается уравнением Гиббса-Гельмгольца: ΔG = ΔH - T · ΔS Единица измерения - (к. Дж)
 Условия протекания процесса 1. Экзотермические реакции; ΔH < 0. а) Если ΔS > 0, то ΔG < 0 - реакции всегда протекают самопроизвольно. б) Если ΔS < 0, реакция будет идти самопроизвольно при ΔН > TΔS (т. е. при низких температурах). 2. Эндотермические реакции; ΔH > 0. а) Если ΔS > 0, процесс будет самопроизвольным при ΔН < TΔS (т. е. при высоких температурах). б) Если ΔS < 0, то ΔG > 0; самопроизвольное протекание реакций невозможно.
Условия протекания процесса 1. Экзотермические реакции; ΔH < 0. а) Если ΔS > 0, то ΔG < 0 - реакции всегда протекают самопроизвольно. б) Если ΔS < 0, реакция будет идти самопроизвольно при ΔН > TΔS (т. е. при низких температурах). 2. Эндотермические реакции; ΔH > 0. а) Если ΔS > 0, процесс будет самопроизвольным при ΔН < TΔS (т. е. при высоких температурах). б) Если ΔS < 0, то ΔG > 0; самопроизвольное протекание реакций невозможно.


