лекция 14 по теории горения и взрыва ДБЖ-09.ppt
- Количество слайдов: 39
 Химическая термодинамика горения и взрыва Лекция 14 по теории горения и взрыва ДБЖ-09
Химическая термодинамика горения и взрыва Лекция 14 по теории горения и взрыва ДБЖ-09
 При решении большинства технических задач необходимо знать тот тепловой эффект, который сопровождает горение или взрыв. Этот тепловой эффект определяет воздействие взрыва на среду, в которой находится заряд ВВ. Во многих реальных задачах параметры горения и взрыва строго ограничены. Раздел термохимия горения и взрыва – расчетный. Предполагается, что продукты взрыва находятся в равновесии. Основные равновесные реакции, которые протекают в продуктах горения и взрыва ВВ, состоящих из углерода водорода, кислорода и азота:
При решении большинства технических задач необходимо знать тот тепловой эффект, который сопровождает горение или взрыв. Этот тепловой эффект определяет воздействие взрыва на среду, в которой находится заряд ВВ. Во многих реальных задачах параметры горения и взрыва строго ограничены. Раздел термохимия горения и взрыва – расчетный. Предполагается, что продукты взрыва находятся в равновесии. Основные равновесные реакции, которые протекают в продуктах горения и взрыва ВВ, состоящих из углерода водорода, кислорода и азота:
 Равновесие зависит от стехиометрии взрывчатого соединения или смеси. Рассмотрим несколько примеров реакций химического превращения ВВ: нитроглицерин C 3 H 5(ONO 2)3 → 3 CO 2+2, 5 H 2 O+1, 5 N 2+0, 25 O 2 +1400 МДж (333200 ккал); аммиачная селитра NH 4 NO 3 → 2 H 2 O + N 2 + 0, 5 O 2 + 121 МДж (29000 ккал); нитрогликоль C 2 H 4 (ONO 2)2 → 2 CO 2 + 2 H 2 O + N 2 + 990 МДж (236500 ккал); аммонит 6 ЖВ, состоящий из смеси аммиачной селитры (79%) и тротила (21%) C 6 H 2(NO 2)3 CH 3 +10, 7 NH 4 NO 3 → 7 CO 2+23, 9 H 2 O+12, 2 N 2+0, 1 O 2+4520 МДж (1078000 ккал);
Равновесие зависит от стехиометрии взрывчатого соединения или смеси. Рассмотрим несколько примеров реакций химического превращения ВВ: нитроглицерин C 3 H 5(ONO 2)3 → 3 CO 2+2, 5 H 2 O+1, 5 N 2+0, 25 O 2 +1400 МДж (333200 ккал); аммиачная селитра NH 4 NO 3 → 2 H 2 O + N 2 + 0, 5 O 2 + 121 МДж (29000 ккал); нитрогликоль C 2 H 4 (ONO 2)2 → 2 CO 2 + 2 H 2 O + N 2 + 990 МДж (236500 ккал); аммонит 6 ЖВ, состоящий из смеси аммиачной селитры (79%) и тротила (21%) C 6 H 2(NO 2)3 CH 3 +10, 7 NH 4 NO 3 → 7 CO 2+23, 9 H 2 O+12, 2 N 2+0, 1 O 2+4520 МДж (1078000 ккал);
 тротил C 6 H 2(NO 2)3 CH 3→ 3, 5 CO+2, 5 H 2 O+3, 5 C+1, 5 N 2+922 МДж (219500 ккал); азид свинца Pb. N 6 → Pb + 3 N 2 + 448 МДж (107000 ккал). Применяют несколько стехиометрических соотношений. 1. В случае вторичных ВВ наиболее употребительной величиной является кислородный баланс (Кб) – выраженная в массовых процентах разность между количеством кислорода, имеющимся в системе, и тем его количеством, которое необходимо для полного сгорания, т. е. превращения всего углерода в СО 2, водорода в H 2 O, алюминия в Al 2 O 3 и т. д. Если в системе присутствуют галогены – хлор или фтор – предполагают их взаимодействие с водородом с образованием галоидоводородов.
тротил C 6 H 2(NO 2)3 CH 3→ 3, 5 CO+2, 5 H 2 O+3, 5 C+1, 5 N 2+922 МДж (219500 ккал); азид свинца Pb. N 6 → Pb + 3 N 2 + 448 МДж (107000 ккал). Применяют несколько стехиометрических соотношений. 1. В случае вторичных ВВ наиболее употребительной величиной является кислородный баланс (Кб) – выраженная в массовых процентах разность между количеством кислорода, имеющимся в системе, и тем его количеством, которое необходимо для полного сгорания, т. е. превращения всего углерода в СО 2, водорода в H 2 O, алюминия в Al 2 O 3 и т. д. Если в системе присутствуют галогены – хлор или фтор – предполагают их взаимодействие с водородом с образованием галоидоводородов.
 Коэффициент 1, 6/М в этой формуле получается делением молекулярной массы кислорода (0, 016 кг/моль) на молекулярную массу системы М и умножением на 100 для получения результата в процентах. Кислородный баланс смеси – аддитивная функция кислородных балансов компонентов. Аммиачная селитра NH 4 NO 3 : Тротил С 7 H 5 N 3 O 6
Коэффициент 1, 6/М в этой формуле получается делением молекулярной массы кислорода (0, 016 кг/моль) на молекулярную массу системы М и умножением на 100 для получения результата в процентах. Кислородный баланс смеси – аддитивная функция кислородных балансов компонентов. Аммиачная селитра NH 4 NO 3 : Тротил С 7 H 5 N 3 O 6
 Рассчитать состав аммонита с кислородным балансом КБ=0%. Учитывая тот факт, что кислородный баланс аддитивен, уравнение для расчета составляется крайне просто: Аммиачная селитра х, тротил (1 – х). 20 х+( - 74)(1 – х)=0, 20 х-74+74 х=0, Содержание селитры 0. 787 ~ 79% Промышленный аммонит № 6 имеет состав: Тротил 21% Аммиачная селитра 79% ВВ с нулевым кислородным балансом в экологическом аспекте более предпочтительны, чем с отрицательным. У последних в составе газообразных продуктов взрыва присутствуют ядовитые оксиды азота и оксид углерода – угарный газ СО.
Рассчитать состав аммонита с кислородным балансом КБ=0%. Учитывая тот факт, что кислородный баланс аддитивен, уравнение для расчета составляется крайне просто: Аммиачная селитра х, тротил (1 – х). 20 х+( - 74)(1 – х)=0, 20 х-74+74 х=0, Содержание селитры 0. 787 ~ 79% Промышленный аммонит № 6 имеет состав: Тротил 21% Аммиачная селитра 79% ВВ с нулевым кислородным балансом в экологическом аспекте более предпочтительны, чем с отрицательным. У последних в составе газообразных продуктов взрыва присутствуют ядовитые оксиды азота и оксид углерода – угарный газ СО.
 2. Коэффициент избытка окислителя α. α это отношение количества кислорода в системе к количеству кислорода необходимому для полного сгорания, т. е. для образования продуктов полного сгорания Н 2 О и СО 2. Если в системе присутствуют металлы Mg или Al и галлогены, при расчете α учитывают только то количество кислорода, которое осталось после окисления металлов и то количество водорода, которое осталось после образования галлоидоводородной кислоты.
2. Коэффициент избытка окислителя α. α это отношение количества кислорода в системе к количеству кислорода необходимому для полного сгорания, т. е. для образования продуктов полного сгорания Н 2 О и СО 2. Если в системе присутствуют металлы Mg или Al и галлогены, при расчете α учитывают только то количество кислорода, которое осталось после окисления металлов и то количество водорода, которое осталось после образования галлоидоводородной кислоты.
 Системе, «сбалансированной по кислороду» , отвечает =1 (КБ=0) , при избытке кислорода >1 (КБ>0), при недостатке <1 (КБ<0). Недостатком α является то, что это соотношение не аддитивно по отношению к массовым доля. Тротил α=6/(14+2, 5)= 0, 36 Аммиачная селитра α=3/2 =1, 5 Применить α для расчета сбалансированного состава смеси этих веществ нельзя. Применяются также две производные от величины: 3. Кислородный коэффициент A = 100 4. Эквивалентное отношение = 1/
Системе, «сбалансированной по кислороду» , отвечает =1 (КБ=0) , при избытке кислорода >1 (КБ>0), при недостатке <1 (КБ<0). Недостатком α является то, что это соотношение не аддитивно по отношению к массовым доля. Тротил α=6/(14+2, 5)= 0, 36 Аммиачная селитра α=3/2 =1, 5 Применить α для расчета сбалансированного состава смеси этих веществ нельзя. Применяются также две производные от величины: 3. Кислородный коэффициент A = 100 4. Эквивалентное отношение = 1/
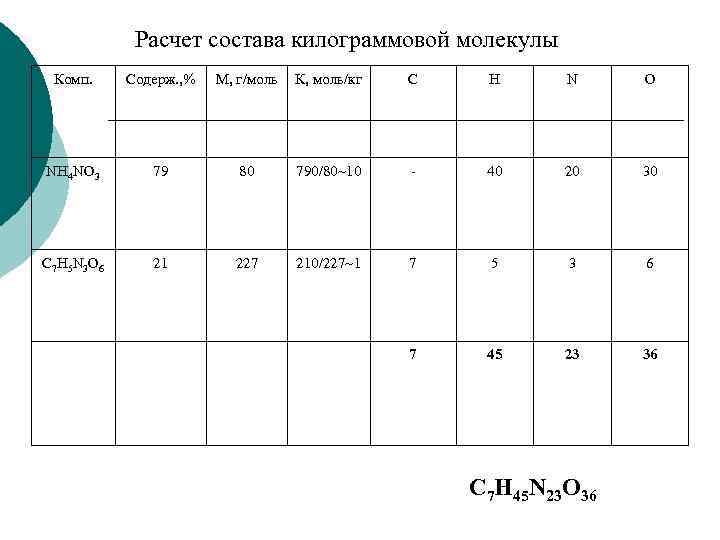 Расчет состава килограммовой молекулы Комп. Содерж. , % M, г/моль К, моль/кг С Н N O NH 4 NO 3 79 80 790/80~10 - 40 20 30 C 7 H 5 N 3 O 6 21 227 210/227~1 7 5 3 6 7 45 23 36 С 7 H 45 N 23 O 36
Расчет состава килограммовой молекулы Комп. Содерж. , % M, г/моль К, моль/кг С Н N O NH 4 NO 3 79 80 790/80~10 - 40 20 30 C 7 H 5 N 3 O 6 21 227 210/227~1 7 5 3 6 7 45 23 36 С 7 H 45 N 23 O 36
 Для расчета теплового эффекта реакции взрывного превращения применяется следствие из закона Гесса: ΔНr=Σnпр ΔН 0 f – Σkисх ΔH 0 f Если реакция протекает в форме взрывного превращения ΔНr<0, т. е. тепло выделяется (термодинамическая система, в ней энтальпия образования парообразной воды ΔН 0 f = - 57, 8 ккал/моль. Следует иметь в виду, что в старых изданиях приводили данные по энтальпиям образования в термохимической системе, где знаки обратные. К примеру это имеет место в таблицах учебника К. К. Андреева и А. Ф. Беляева).
Для расчета теплового эффекта реакции взрывного превращения применяется следствие из закона Гесса: ΔНr=Σnпр ΔН 0 f – Σkисх ΔH 0 f Если реакция протекает в форме взрывного превращения ΔНr<0, т. е. тепло выделяется (термодинамическая система, в ней энтальпия образования парообразной воды ΔН 0 f = - 57, 8 ккал/моль. Следует иметь в виду, что в старых изданиях приводили данные по энтальпиям образования в термохимической системе, где знаки обратные. К примеру это имеет место в таблицах учебника К. К. Андреева и А. Ф. Беляева).
 В теории горения и взрыва принято теплоту взрыва считать положительной величиной, поэтому теплота взрыва при постоянном давлении Qp= - ΔНr. При постоянном давлении горение протекает на воздухе и в камере ракетного двигателя, работающего в стационарном режиме. Для сопловой части РД и процессов, следующих за взрывом заряда ВВ характерно изоэнтропическое расширение газа. В связи с этим теплота взрыва при постоянном объеме Qv больше чем Qp на работу расширения газов: Q v = Q p + n 0 R T 0, где n 0 – число молей газообразных продуктов на единицу массы заряда.
В теории горения и взрыва принято теплоту взрыва считать положительной величиной, поэтому теплота взрыва при постоянном давлении Qp= - ΔНr. При постоянном давлении горение протекает на воздухе и в камере ракетного двигателя, работающего в стационарном режиме. Для сопловой части РД и процессов, следующих за взрывом заряда ВВ характерно изоэнтропическое расширение газа. В связи с этим теплота взрыва при постоянном объеме Qv больше чем Qp на работу расширения газов: Q v = Q p + n 0 R T 0, где n 0 – число молей газообразных продуктов на единицу массы заряда.
 Энтальпия образования Фундаментальная термодинамическая характеристика любого химического соединения, только для элементов она равна нулю. Она отрицательна, например, для тротила ΔНf = - 15 ккал/моль и аммиачной селитры ΔНf = - 87. 37 ккал/моль. Для гексогена и ацетилена – она положительно и составляет, соответственно ΔНгекс f = + 14. 7 ккал/моль и ΔНац f = + 54. 19 ккал/моль Для наиболее часто образующихся продуктов взрыва энтальпии образования (в к. Дж/моль) собраны в таблице. Эта таблица понадобится при решении домашней задачи – первой рейтинговой контрольной точки.
Энтальпия образования Фундаментальная термодинамическая характеристика любого химического соединения, только для элементов она равна нулю. Она отрицательна, например, для тротила ΔНf = - 15 ккал/моль и аммиачной селитры ΔНf = - 87. 37 ккал/моль. Для гексогена и ацетилена – она положительно и составляет, соответственно ΔНгекс f = + 14. 7 ккал/моль и ΔНац f = + 54. 19 ккал/моль Для наиболее часто образующихся продуктов взрыва энтальпии образования (в к. Дж/моль) собраны в таблице. Эта таблица понадобится при решении домашней задачи – первой рейтинговой контрольной точки.

 Получают энтальпии образования главным образом с помощью измерения теплот сгорания в калориметрической бомбе при давлении кислорода Р=30 атм: Сс. Hh. Oo. Nn + O 2 с СО 2 + 0, 5 h Н 2 О + N 2 – ΔНr = Σnпр ΔНf –ΔHисхf Энтальпии образования органических веществ, в том числе, многих ВВ собраны в таблицах в книге Сталл Д. , Вестрам Э. , Зинке Г. Термодинамика органических соединений, М. , Мир, 1971 г. , а также в базе данных NIST (National Institute of Standards and Technology). Сайт легко найти, введя в поисковую систему Интернета аббревиатуру NIST.
Получают энтальпии образования главным образом с помощью измерения теплот сгорания в калориметрической бомбе при давлении кислорода Р=30 атм: Сс. Hh. Oo. Nn + O 2 с СО 2 + 0, 5 h Н 2 О + N 2 – ΔНr = Σnпр ΔНf –ΔHисхf Энтальпии образования органических веществ, в том числе, многих ВВ собраны в таблицах в книге Сталл Д. , Вестрам Э. , Зинке Г. Термодинамика органических соединений, М. , Мир, 1971 г. , а также в базе данных NIST (National Institute of Standards and Technology). Сайт легко найти, введя в поисковую систему Интернета аббревиатуру NIST.

 H 2 Oпар→ H 2 Oжидк-10. 6 кал CO 2 +H 2 CO + H 2 O +~10 кал Hf= - (Qж – 10. 6 nводы) Экспериментальна кривая калориметрического опыта
H 2 Oпар→ H 2 Oжидк-10. 6 кал CO 2 +H 2 CO + H 2 O +~10 кал Hf= - (Qж – 10. 6 nводы) Экспериментальна кривая калориметрического опыта
 Температуру взрыва можно найти двояко, однако принцип нахождения один и тот же. 1. Теплота взрыва расходуется на увеличение внутренней энергии продуктов взрыва (Е). Внутренняя энергия – однозначная функция температуры. Таблицы значений внутренней энергии от температуры имеются в литературе (например в учебнике К. К. Андреева и А. Ф. Беляева. Qv= ΣΔE(T) После нахождения Qv задаются некоторой температурой Tv, при которой суммируют внутреннюю энергию продуктов реакции, не забывая ни об одном из них. Поиск температуры осуществляют несколько раз, добиваясь, чтобы: ΔEТ 1
Температуру взрыва можно найти двояко, однако принцип нахождения один и тот же. 1. Теплота взрыва расходуется на увеличение внутренней энергии продуктов взрыва (Е). Внутренняя энергия – однозначная функция температуры. Таблицы значений внутренней энергии от температуры имеются в литературе (например в учебнике К. К. Андреева и А. Ф. Беляева. Qv= ΣΔE(T) После нахождения Qv задаются некоторой температурой Tv, при которой суммируют внутреннюю энергию продуктов реакции, не забывая ни об одном из них. Поиск температуры осуществляют несколько раз, добиваясь, чтобы: ΔEТ 1
 Остальные параметры горения и взрыва находят пользуясь соотношениями, известными из термодинамики: Средняя теплоемкость в интервале (Tv – T 0): Сv= Qv/(Tv-T 0). Теплоемкость при постоянном давлении: Cp= Cv+n 0 R. Показатель политропы γ= Cp/Cv. Температура взрыва при постоянном давлении TP=Tv/ γ. Теплота взрыва при постоянном давлении, как указывалось ранее : Qp=Qv – n 0 RT 0 или Qp= Cp(Tp – T 0). 2. Второй способ нахождения температуры взрыва несколько проще. В нем использован тот факт, известный их термодинамики, что энтальпия продуктов взрыва (Н) связана с их внутренней энергией соотношением: Н = E + pv, или Н = Е + p v
Остальные параметры горения и взрыва находят пользуясь соотношениями, известными из термодинамики: Средняя теплоемкость в интервале (Tv – T 0): Сv= Qv/(Tv-T 0). Теплоемкость при постоянном давлении: Cp= Cv+n 0 R. Показатель политропы γ= Cp/Cv. Температура взрыва при постоянном давлении TP=Tv/ γ. Теплота взрыва при постоянном давлении, как указывалось ранее : Qp=Qv – n 0 RT 0 или Qp= Cp(Tp – T 0). 2. Второй способ нахождения температуры взрыва несколько проще. В нем использован тот факт, известный их термодинамики, что энтальпия продуктов взрыва (Н) связана с их внутренней энергией соотношением: Н = E + pv, или Н = Е + p v
 Изменение энтальпии продуктов реакции сравнивается с теплотой взрыва при постоянном объеме Qp. Зависимость изменения энтальпии продуктов взрыва имеет вид: В широком диапазоне температур: Ti – (3000 -4000 К) она прямолинейна: Этим и пользуются при расчете:
Изменение энтальпии продуктов реакции сравнивается с теплотой взрыва при постоянном объеме Qp. Зависимость изменения энтальпии продуктов взрыва имеет вид: В широком диапазоне температур: Ti – (3000 -4000 К) она прямолинейна: Этим и пользуются при расчете:
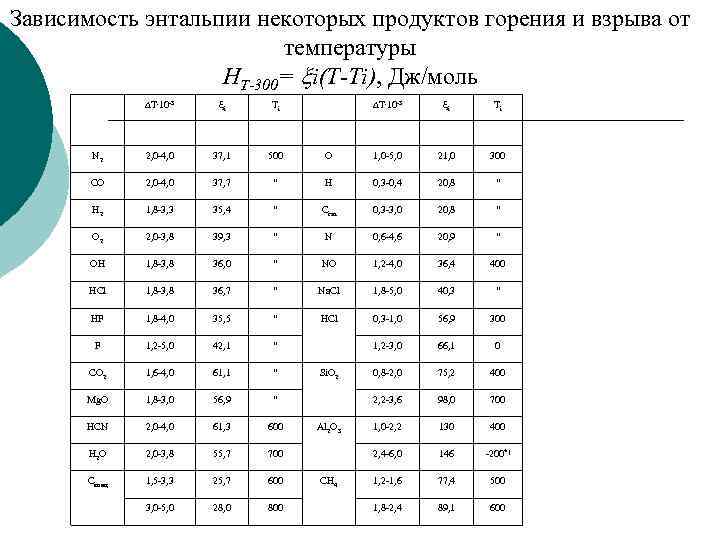 Зависимость энтальпии некоторых продуктов горения и взрыва от температуры HT-300= i(T-Ti), Дж/моль T. 10 -3 i Ti N 2 2, 0 -4, 0 37, 1 500 O 1, 0 -5, 0 21, 0 300 CO 2, 0 -4, 0 37, 7 “ H 0, 3 -0, 4 20, 8 “ H 2 1, 8 -3, 3 35, 4 “ Cгаз 0, 3 -3, 0 20, 8 “ O 2 2, 0 -3, 8 39, 3 “ N 0, 6 -4, 6 20, 9 “ OH 1, 8 -3, 8 36, 0 “ NO 1, 2 -4, 0 36, 4 400 HCl 1, 8 -3, 8 36, 7 “ Na. Cl 1, 8 -5, 0 40, 3 “ HF 1, 8 -4, 0 35, 5 “ HCl 0, 3 -1, 0 56, 9 300 F 1, 2 -5, 0 42, 1 “ 1, 2 -3, 0 66, 1 0 CO 2 1, 6 -4, 0 61, 1 “ 0, 8 -2, 0 75, 2 400 Mg. O 1, 8 -3, 0 56, 9 “ 2, 2 -3, 6 98, 0 700 HCN 2, 0 -4, 0 61, 3 600 1, 0 -2, 2 130 400 H 2 O 2, 0 -3, 8 55, 7 700 2, 4 -6, 0 146 -200*) Cконц 1, 5 -3, 3 25, 7 600 1, 2 -1, 6 77, 4 500 3, 0 -5, 0 28, 0 800 1, 8 -2, 4 89, 1 600 Si. O 2 Al 2 O 3 CH 4
Зависимость энтальпии некоторых продуктов горения и взрыва от температуры HT-300= i(T-Ti), Дж/моль T. 10 -3 i Ti N 2 2, 0 -4, 0 37, 1 500 O 1, 0 -5, 0 21, 0 300 CO 2, 0 -4, 0 37, 7 “ H 0, 3 -0, 4 20, 8 “ H 2 1, 8 -3, 3 35, 4 “ Cгаз 0, 3 -3, 0 20, 8 “ O 2 2, 0 -3, 8 39, 3 “ N 0, 6 -4, 6 20, 9 “ OH 1, 8 -3, 8 36, 0 “ NO 1, 2 -4, 0 36, 4 400 HCl 1, 8 -3, 8 36, 7 “ Na. Cl 1, 8 -5, 0 40, 3 “ HF 1, 8 -4, 0 35, 5 “ HCl 0, 3 -1, 0 56, 9 300 F 1, 2 -5, 0 42, 1 “ 1, 2 -3, 0 66, 1 0 CO 2 1, 6 -4, 0 61, 1 “ 0, 8 -2, 0 75, 2 400 Mg. O 1, 8 -3, 0 56, 9 “ 2, 2 -3, 6 98, 0 700 HCN 2, 0 -4, 0 61, 3 600 1, 0 -2, 2 130 400 H 2 O 2, 0 -3, 8 55, 7 700 2, 4 -6, 0 146 -200*) Cконц 1, 5 -3, 3 25, 7 600 1, 2 -1, 6 77, 4 500 3, 0 -5, 0 28, 0 800 1, 8 -2, 4 89, 1 600 Si. O 2 Al 2 O 3 CH 4
 Расчет состава продуктов взрыва Предположения: 1. Состав продуктов горения отвечает термодинамическому равновесию. 2. Предполагается возможность протекания следующих равновесных реакций. Основные равновесные реакции, которые протекают в продуктах горения и взрыва ВВ, состоящих из углерода водорода, кислорода и азота:
Расчет состава продуктов взрыва Предположения: 1. Состав продуктов горения отвечает термодинамическому равновесию. 2. Предполагается возможность протекания следующих равновесных реакций. Основные равновесные реакции, которые протекают в продуктах горения и взрыва ВВ, состоящих из углерода водорода, кислорода и азота:
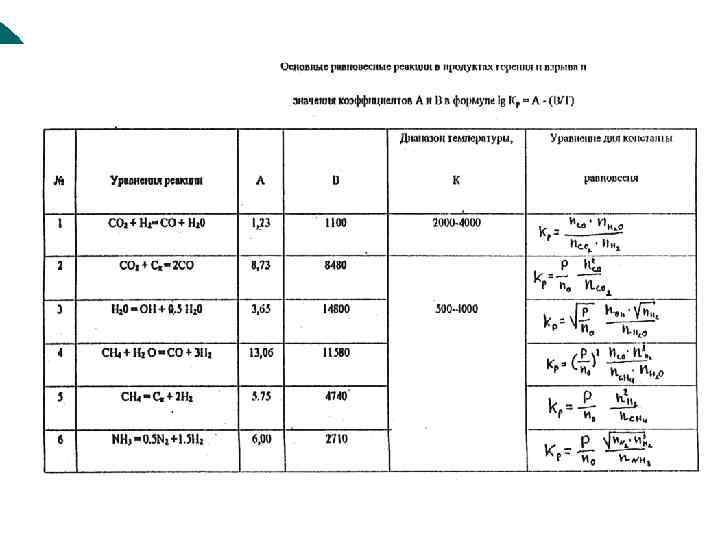
 При приближенных расчетах, когда углерода в системе меньше, чем кислорода, учитывают только равновесие 1. Это наиболее простой случай, если не принимать во внимание вещества с положительным и нулевым кислородным балансом, когда уравнение реакции взрывного разложения пишется просто – в продуктах реакции вода (пар), диоксид углерода и азот. Если углерода больше, чем кислорода, то должно выделиться некоторое количество углерода в чистом виде, и внимание принимаются равновесия 1 и 2. это сильно усложняет итерационный расчет. Сгорание Al и Mg происходит нацело практически при любых условиях, можно считать, что они нацело переходят в Al 2 O 3 и Mg. O. Al горит в смеси с карбонатами и сульфатами: 3 Na 2 SO 4 +8 Al 4 Al 2 O 3 + 3 Na 2 S - Hr
При приближенных расчетах, когда углерода в системе меньше, чем кислорода, учитывают только равновесие 1. Это наиболее простой случай, если не принимать во внимание вещества с положительным и нулевым кислородным балансом, когда уравнение реакции взрывного разложения пишется просто – в продуктах реакции вода (пар), диоксид углерода и азот. Если углерода больше, чем кислорода, то должно выделиться некоторое количество углерода в чистом виде, и внимание принимаются равновесия 1 и 2. это сильно усложняет итерационный расчет. Сгорание Al и Mg происходит нацело практически при любых условиях, можно считать, что они нацело переходят в Al 2 O 3 и Mg. O. Al горит в смеси с карбонатами и сульфатами: 3 Na 2 SO 4 +8 Al 4 Al 2 O 3 + 3 Na 2 S - Hr
 3. Предполагается, что продукты реакции подчиняются законам идеального газа. PV=n. RT. При более точных расчетах и давлении 500 -5000 ат надо пользоваться уравнением Ван дер Вальса P(V-Vk) = RT. В внутренней баллистике вводят обозначения: RTv=fg – сила пороха и 1/V - плотность заряжания. Уравнение Нобля-Абеля: P= fп/(1 -Vk ) При давлении несколько тысяч ат. Пользуются уравнением с вириальными коэффициентами: PV/RT ~1+B 2/V+ K 1 B 22/V 2+K 2 B 23/V 3 + K 3 B 24/V 4
3. Предполагается, что продукты реакции подчиняются законам идеального газа. PV=n. RT. При более точных расчетах и давлении 500 -5000 ат надо пользоваться уравнением Ван дер Вальса P(V-Vk) = RT. В внутренней баллистике вводят обозначения: RTv=fg – сила пороха и 1/V - плотность заряжания. Уравнение Нобля-Абеля: P= fп/(1 -Vk ) При давлении несколько тысяч ат. Пользуются уравнением с вириальными коэффициентами: PV/RT ~1+B 2/V+ K 1 B 22/V 2+K 2 B 23/V 3 + K 3 B 24/V 4
 При расчете параметров детонации: За рубежом применяется ур-ние BKW (Беккера. Кистяковского-Вильсона. Широко распространено уравнение Ми-Грюнайзена: Е=Еу+Ет , Р=Ру+Рт Тепловое давление связано с тепловой энергией уравнением Ми-Грюнайзена: Рт=ГЕт/V Г- коэффициент Грюнайзена порядка единиц, для большинства металлов Г/V~ const.
При расчете параметров детонации: За рубежом применяется ур-ние BKW (Беккера. Кистяковского-Вильсона. Широко распространено уравнение Ми-Грюнайзена: Е=Еу+Ет , Р=Ру+Рт Тепловое давление связано с тепловой энергией уравнением Ми-Грюнайзена: Рт=ГЕт/V Г- коэффициент Грюнайзена порядка единиц, для большинства металлов Г/V~ const.
 Экспериментальные способы измерения теплоты взрыва и состава продуктов взрыва: 1. Калориметрическая бомба. 2. Бомба Бихеля. 3. Бомба Долгова. С помощью бомбы Бихеля установлено: 1. Если КБ>0, то основные продукты взрыва CO 2, H 2 O, N 2, O 2, (NO 2 – мало). 2. Если КБ<0, а углерода меньше чем кислорода в системе, то основные продукты: CO 2, CO, H 2, N 2, (CH 4 и NH 3 – мало). 3. Если КБ<0, а углерода больше чем кислорода в системе, то основные продукты: С, СН 4, NH 3, HCN, (CN)2, CO, H 2, N 2.
Экспериментальные способы измерения теплоты взрыва и состава продуктов взрыва: 1. Калориметрическая бомба. 2. Бомба Бихеля. 3. Бомба Долгова. С помощью бомбы Бихеля установлено: 1. Если КБ>0, то основные продукты взрыва CO 2, H 2 O, N 2, O 2, (NO 2 – мало). 2. Если КБ<0, а углерода меньше чем кислорода в системе, то основные продукты: CO 2, CO, H 2, N 2, (CH 4 и NH 3 – мало). 3. Если КБ<0, а углерода больше чем кислорода в системе, то основные продукты: С, СН 4, NH 3, HCN, (CN)2, CO, H 2, N 2.
 1. При КБ>0 состав продуктов взрыва рассчитывать не требуется, он определяется при написании реакции взрывного превращения: Cc. Hh. Nn. Oo c. CO 2 + 0. 5 h H 2 O + 0. 5 n N 2 + 0. 5[(O)-2 C – 0. 5 H] O 2 2. Если углерода меньше, чем кислорода и КБ <0, то составляется система уравнений, состоящее из трех балансовых элементов в системе и уравнения константы реакции водяного газа (реакция 1 в таблице):
1. При КБ>0 состав продуктов взрыва рассчитывать не требуется, он определяется при написании реакции взрывного превращения: Cc. Hh. Nn. Oo c. CO 2 + 0. 5 h H 2 O + 0. 5 n N 2 + 0. 5[(O)-2 C – 0. 5 H] O 2 2. Если углерода меньше, чем кислорода и КБ <0, то составляется система уравнений, состоящее из трех балансовых элементов в системе и уравнения константы реакции водяного газа (реакция 1 в таблице):
 Принимают обозначения: a = (n. С+0, 5 n Н – n(О)) kp ; b = n. C(n(O) – n. C), Где n. С, n. H, n(O) – содержание в килограммовой молекуле, соответственно углерода, водорода и кислорода. Система уравнений с помощью обычных алгебраических манипуляций сводится к виду: Решение этого простого квадратного уравнения дает содержание СО 2 в продуктах взрыва:
Принимают обозначения: a = (n. С+0, 5 n Н – n(О)) kp ; b = n. C(n(O) – n. C), Где n. С, n. H, n(O) – содержание в килограммовой молекуле, соответственно углерода, водорода и кислорода. Система уравнений с помощью обычных алгебраических манипуляций сводится к виду: Решение этого простого квадратного уравнения дает содержание СО 2 в продуктах взрыва:
 Содержание остальных газообразных продуктов n. CO, n. H 2 O и n. H 2 находится из балансовых уравнений, входящих в систему, содержание азота в газообразных продуктах определяется, как: Где n. N – содержание азота в килограммовой молекуле.
Содержание остальных газообразных продуктов n. CO, n. H 2 O и n. H 2 находится из балансовых уравнений, входящих в систему, содержание азота в газообразных продуктах определяется, как: Где n. N – содержание азота в килограммовой молекуле.
 Для того, чтобы выполнить расчет состава продуктов взрыва, а затем и теплоты взрыва Qp необходимо задаться некоторой ориентировочной температурой взрыва Трор и вычислить константу реакции водяного газа kp по той зависимости, которая приведена для этой реакции (1) в таблице с равновесными реакциями (см выше). После этого вычисляется теплота взрыва Qp, и по приведенной выше для каждого из продуктов взрыва зависимости энтальпии от температуры вычисляется суммарное изменение энтальпии продуктов взрыва: Где ni – содержание каждого продукта взрыва, Нi – изменение его энтальпии.
Для того, чтобы выполнить расчет состава продуктов взрыва, а затем и теплоты взрыва Qp необходимо задаться некоторой ориентировочной температурой взрыва Трор и вычислить константу реакции водяного газа kp по той зависимости, которая приведена для этой реакции (1) в таблице с равновесными реакциями (см выше). После этого вычисляется теплота взрыва Qp, и по приведенной выше для каждого из продуктов взрыва зависимости энтальпии от температуры вычисляется суммарное изменение энтальпии продуктов взрыва: Где ni – содержание каждого продукта взрыва, Нi – изменение его энтальпии.
 Если величины Qp и Σni Hi совпадают, расчет считают законченным и Тр=Тор, если нет, то задаются новой температурой и весь расчет состава продуктов повторяют. Если расчет ведется с помощью ЭВМ, то проведение итераций не представляет особой сложности, просто задают изменение Тор в некотором разумном диапазоне с шагом, например, в 1 градус и ту температуру Тор, при которой различие между Qp и Σni Hi равно нулю считают Тр. Для сокращения итераций (в особенности при ручном счете) можно воспользоваться корреляционными соотношениями для нахождения Тор. Отметим, что эти соотношения не имеют прямого физического смысла, а выведены в результате проведения многочисленных ручных расчетов в то время, когда быстродействующих ЭВМ еще не было.
Если величины Qp и Σni Hi совпадают, расчет считают законченным и Тр=Тор, если нет, то задаются новой температурой и весь расчет состава продуктов повторяют. Если расчет ведется с помощью ЭВМ, то проведение итераций не представляет особой сложности, просто задают изменение Тор в некотором разумном диапазоне с шагом, например, в 1 градус и ту температуру Тор, при которой различие между Qp и Σni Hi равно нулю считают Тр. Для сокращения итераций (в особенности при ручном счете) можно воспользоваться корреляционными соотношениями для нахождения Тор. Отметим, что эти соотношения не имеют прямого физического смысла, а выведены в результате проведения многочисленных ручных расчетов в то время, когда быстродействующих ЭВМ еще не было.
 Top = 500 + 103 A/B A = 255 n(O) – 142 n. C + Hfисх [к. Дж/кг] B = 17, 4 n. C + 20, 3 n(O) +17, 7 n. H + 18, 5 n. N [к. Дж/кг К] Итак, схема расчета: 1. Расчет килограммовой молекулы. 2. Расчет энтальпии образования смеси. 3. Расчет КБ, α и объема газообразных продуктов n 0. 4. n 0= n. C+0. 5 (n. H+n. N) 4. Итерационный расчет состава продуктов взрыва и температуры взрыва. В результате выдаются: Qp, Qv, n 0, КБ, α, Tp, Tv, γ, состав продуктов взрыва и теплоемкости Ср и Сv. Пример расчета для однокомпонентной смеси имеется в файле «из задачника. doc» .
Top = 500 + 103 A/B A = 255 n(O) – 142 n. C + Hfисх [к. Дж/кг] B = 17, 4 n. C + 20, 3 n(O) +17, 7 n. H + 18, 5 n. N [к. Дж/кг К] Итак, схема расчета: 1. Расчет килограммовой молекулы. 2. Расчет энтальпии образования смеси. 3. Расчет КБ, α и объема газообразных продуктов n 0. 4. n 0= n. C+0. 5 (n. H+n. N) 4. Итерационный расчет состава продуктов взрыва и температуры взрыва. В результате выдаются: Qp, Qv, n 0, КБ, α, Tp, Tv, γ, состав продуктов взрыва и теплоемкости Ср и Сv. Пример расчета для однокомпонентной смеси имеется в файле «из задачника. doc» .
 3. Если КБ<0, а углерода больше чем кислорода в системе, то расчет существенно усложняется, т. к. рассчитываемая при итерациях температура должна соответствовать двум уравнениям реакции (1) и (2), иными словами, при этой температуре состав должен быть таким, что оба равновесия соблюдаются. Обычно, приближенных расчетах, не учитывают протекания равновесных реакций диссоциации в продуктах реакции. Они имеют место при температурах более 3000 К и несколько снижают температуру взрыва. Насколько сильно их влияние и насколько учет диссоциации усложняет расчет можно увидеть в рекомендованном в разделе «Литература» Задачнике, в котором пример такого расчета приведен.
3. Если КБ<0, а углерода больше чем кислорода в системе, то расчет существенно усложняется, т. к. рассчитываемая при итерациях температура должна соответствовать двум уравнениям реакции (1) и (2), иными словами, при этой температуре состав должен быть таким, что оба равновесия соблюдаются. Обычно, приближенных расчетах, не учитывают протекания равновесных реакций диссоциации в продуктах реакции. Они имеют место при температурах более 3000 К и несколько снижают температуру взрыва. Насколько сильно их влияние и насколько учет диссоциации усложняет расчет можно увидеть в рекомендованном в разделе «Литература» Задачнике, в котором пример такого расчета приведен.
 Для расчета параметров горения и взрыва имеется несколько компьютерных программ. 1. Программа расчета параметров детонации “SD” (Shock and Detonation). Создана в РХТУ им Д. И. Менделеева проф. Б. Н. Кондриковым и его аспирантом А. И. Суминым. Рассчитывает теплоту взрыва, объем газообразных продуктов взрыва их состав, скорость и давление детонации (по этим параметрам для C, H, O, N нитросоединений результаты расчета прекрасно согласуются с экспериментом), массовую скорость продуктов взрыва, показатель политропы. Может автоматически рассчитывать зависимость параметров детонации от плотности или состава смеси. Уравнение состояния, заложенное в алгоритм расчета, это модифицированное авторами физически обоснованное уравнение Ми-Грюнайзена для сверхвысоких температур и давлений.
Для расчета параметров горения и взрыва имеется несколько компьютерных программ. 1. Программа расчета параметров детонации “SD” (Shock and Detonation). Создана в РХТУ им Д. И. Менделеева проф. Б. Н. Кондриковым и его аспирантом А. И. Суминым. Рассчитывает теплоту взрыва, объем газообразных продуктов взрыва их состав, скорость и давление детонации (по этим параметрам для C, H, O, N нитросоединений результаты расчета прекрасно согласуются с экспериментом), массовую скорость продуктов взрыва, показатель политропы. Может автоматически рассчитывать зависимость параметров детонации от плотности или состава смеси. Уравнение состояния, заложенное в алгоритм расчета, это модифицированное авторами физически обоснованное уравнение Ми-Грюнайзена для сверхвысоких температур и давлений.
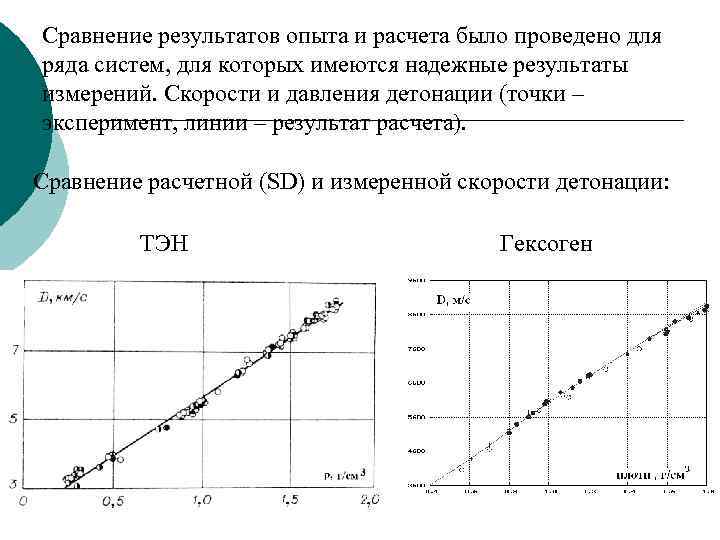 Сравнение результатов опыта и расчета было проведено для ряда систем, для которых имеются надежные результаты измерений. Скорости и давления детонации (точки – эксперимент, линии – результат расчета). Сравнение расчетной (SD) и измеренной скорости детонации: ТЭН Гексоген
Сравнение результатов опыта и расчета было проведено для ряда систем, для которых имеются надежные результаты измерений. Скорости и давления детонации (точки – эксперимент, линии – результат расчета). Сравнение расчетной (SD) и измеренной скорости детонации: ТЭН Гексоген
 Сравнение расчетного (по SD) и измеренного давления детонации Тетрил Тротил
Сравнение расчетного (по SD) и измеренного давления детонации Тетрил Тротил
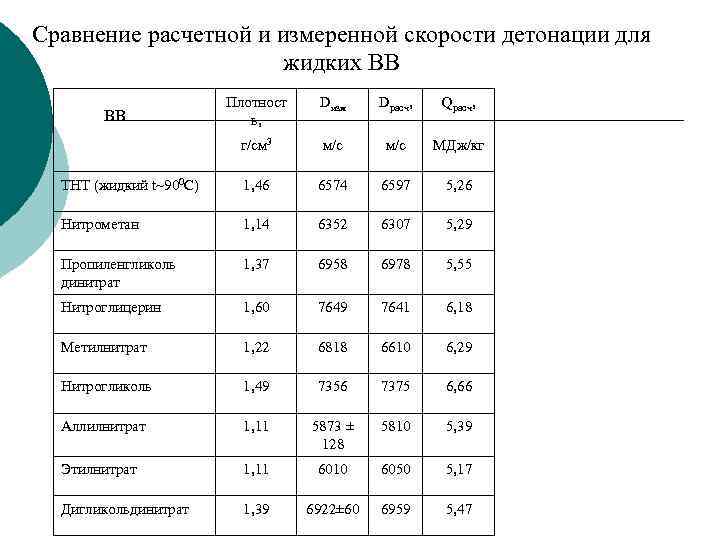 Сравнение расчетной и измеренной скорости детонации для жидких ВВ Плотност ь, Dизм Dрасч, Qрасч, г/см 3 м/с МДж/кг ТНТ (жидкий t~900 C) 1, 46 6574 6597 5, 26 Нитрометан 1, 14 6352 6307 5, 29 Пропиленгликоль динитрат 1, 37 6958 6978 5, 55 Нитроглицерин 1, 60 7649 7641 6, 18 Метилнитрат 1, 22 6818 6610 6, 29 Нитрогликоль 1, 49 7356 7375 6, 66 Аллилнитрат 1, 11 5873 ± 128 5810 5, 39 Этилнитрат 1, 11 6010 6050 5, 17 Дигликольдинитрат 1, 39 6922± 60 6959 5, 47 ВВ
Сравнение расчетной и измеренной скорости детонации для жидких ВВ Плотност ь, Dизм Dрасч, Qрасч, г/см 3 м/с МДж/кг ТНТ (жидкий t~900 C) 1, 46 6574 6597 5, 26 Нитрометан 1, 14 6352 6307 5, 29 Пропиленгликоль динитрат 1, 37 6958 6978 5, 55 Нитроглицерин 1, 60 7649 7641 6, 18 Метилнитрат 1, 22 6818 6610 6, 29 Нитрогликоль 1, 49 7356 7375 6, 66 Аллилнитрат 1, 11 5873 ± 128 5810 5, 39 Этилнитрат 1, 11 6010 6050 5, 17 Дигликольдинитрат 1, 39 6922± 60 6959 5, 47 ВВ
 2. Программа для расчета параметров детонации ВВ, созданная в ИХФ АН РАФ под руководством д. ф. -м. н. В. И. Пепекина. В основе ее также лежит физически обоснованное уравнение состояния при сверхвысоких температурах и давлениях. Результаты расчетов по скорости и давлению детонации для 1 и 2 программ практически совпадают для C, H, O, N нитросоединений. Для обеих программ необходимыми вводимыми параметрами являются химические формулы, энтальпия образования, процентное содержание компонентов и плотность заряда.
2. Программа для расчета параметров детонации ВВ, созданная в ИХФ АН РАФ под руководством д. ф. -м. н. В. И. Пепекина. В основе ее также лежит физически обоснованное уравнение состояния при сверхвысоких температурах и давлениях. Результаты расчетов по скорости и давлению детонации для 1 и 2 программ практически совпадают для C, H, O, N нитросоединений. Для обеих программ необходимыми вводимыми параметрами являются химические формулы, энтальпия образования, процентное содержание компонентов и плотность заряда.
 3. Баллистическая программа “Real”, разработанная в МГТУ им Н. Э. Баумана для работы в операционной системе DOC и модернизированная в РХТУ им Д. И. Менделеева для работы в о. с. Windows. Уравнения состояния для расчета могут быть выбраны (у. с. идеального газа, у. с. С вириальными коэффициентами. В алгоритм заложены многочисленные равновесные уравнения реакций для соединений с очень большим числом элементов. Рассчитывает состав продуктов взрыва, температуру взрыва, импульс, развиваемый порохом, теплоемкость продуктов взрыва. В первоначальном варианте теплота взрыва не рассчитывалась, и ее приходилось считать вручную по составу продуктов взрыва. Программа широко используется специалистами по внутренней баллистике.
3. Баллистическая программа “Real”, разработанная в МГТУ им Н. Э. Баумана для работы в операционной системе DOC и модернизированная в РХТУ им Д. И. Менделеева для работы в о. с. Windows. Уравнения состояния для расчета могут быть выбраны (у. с. идеального газа, у. с. С вириальными коэффициентами. В алгоритм заложены многочисленные равновесные уравнения реакций для соединений с очень большим числом элементов. Рассчитывает состав продуктов взрыва, температуру взрыва, импульс, развиваемый порохом, теплоемкость продуктов взрыва. В первоначальном варианте теплота взрыва не рассчитывалась, и ее приходилось считать вручную по составу продуктов взрыва. Программа широко используется специалистами по внутренней баллистике.


