Химическая связь1.pptx
- Количество слайдов: 10
 Химическая связь в твердых телах. Выполнила: студентка гр: 4301 -51 Лямина К. С. Проверила: Исхакова И. О.
Химическая связь в твердых телах. Выполнила: студентка гр: 4301 -51 Лямина К. С. Проверила: Исхакова И. О.
 Твердые вещества, как правило, имеют кристаллическое строение. Оно характеризуется правильным расположением частиц в строго определенных точках пространства. При мысленном соединении этих точек пересекающимися прямыми линиями образуется пространственный каркас, который называют кристаллической решеткой. Точки, в которых размещены частицы, называются узлами кристаллической решетки. В узлах воображаемой решетки могут находиться ионы, атомы или молекулы. Они совершают колебательные движения. С повышением температуры амплитуда колебаний возрастает, что проявляется в тепловом расширении тел. По своему внутреннему строению твердые тела разделяются на : • кристаллические • аморфные
Твердые вещества, как правило, имеют кристаллическое строение. Оно характеризуется правильным расположением частиц в строго определенных точках пространства. При мысленном соединении этих точек пересекающимися прямыми линиями образуется пространственный каркас, который называют кристаллической решеткой. Точки, в которых размещены частицы, называются узлами кристаллической решетки. В узлах воображаемой решетки могут находиться ионы, атомы или молекулы. Они совершают колебательные движения. С повышением температуры амплитуда колебаний возрастает, что проявляется в тепловом расширении тел. По своему внутреннему строению твердые тела разделяются на : • кристаллические • аморфные
 Кристаллы – вещества, в которых мельчайшие частицы (атомы, ионы или молекулы) «упакованы» в определенном порядке. В результате при росте кристаллов на их поверхности самопроизвольно возникают плоские грани, а сами кристаллы принимают разнообразную геометрическую форму. Аморфные тела – это твердые тела, которые не имеют кристаллической структуры. К ним относятся стекла (искусственные и вулканические), смолы (естественные и искусственные), клеи, сургуч, пластмассы и т. п.
Кристаллы – вещества, в которых мельчайшие частицы (атомы, ионы или молекулы) «упакованы» в определенном порядке. В результате при росте кристаллов на их поверхности самопроизвольно возникают плоские грани, а сами кристаллы принимают разнообразную геометрическую форму. Аморфные тела – это твердые тела, которые не имеют кристаллической структуры. К ним относятся стекла (искусственные и вулканические), смолы (естественные и искусственные), клеи, сургуч, пластмассы и т. п.
 Свойства твердых веществ определяются природой частиц, занимающих узлы кристаллической решетки и типом взаимодействия между ними. В зависимости от строения кристаллические решетки делятся на: q Атомные и молекулярные кристаллы q Ионные кристаллы q Металлические Рассмотрим их подробнее.
Свойства твердых веществ определяются природой частиц, занимающих узлы кристаллической решетки и типом взаимодействия между ними. В зависимости от строения кристаллические решетки делятся на: q Атомные и молекулярные кристаллы q Ионные кристаллы q Металлические Рассмотрим их подробнее.
 ØТвердые аргон и метан образуют атомные и молекулярные кристаллы. Поскольку силы между атомами и молекулами в этих решетках относятся к типу слабых ван дер ваальсовых, такие вещества плавятся при довольно низких температурах. Большая часть веществ, которые при комнатной температуре находятся в жидком и газообразном состоянии, при низких температурах образуют молекулярные кристаллы.
ØТвердые аргон и метан образуют атомные и молекулярные кристаллы. Поскольку силы между атомами и молекулами в этих решетках относятся к типу слабых ван дер ваальсовых, такие вещества плавятся при довольно низких температурах. Большая часть веществ, которые при комнатной температуре находятся в жидком и газообразном состоянии, при низких температурах образуют молекулярные кристаллы.
 Атомная кристаллическая решетка в своих узлах содержит атомы многовалентных элементов, которые связаны друг с другом прочными ковалентными связями. Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в них ковалентные, как полярные, так и неполярные. Связи в молекулах прочные, но между молекулами связи не прочные. Алмаз и графит кристаллы с атомной решеткой, имеющей в узлах атомы углерода с разным расположением этих узлов в пространстве.
Атомная кристаллическая решетка в своих узлах содержит атомы многовалентных элементов, которые связаны друг с другом прочными ковалентными связями. Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в них ковалентные, как полярные, так и неполярные. Связи в молекулах прочные, но между молекулами связи не прочные. Алмаз и графит кристаллы с атомной решеткой, имеющей в узлах атомы углерода с разным расположением этих узлов в пространстве.
 В ковалентных кристаллах решетка построена из атомов, в узлах которой они одинаковые или разные , соединенные ковалентной связью, поэтому эти кристаллы обладают высокими твердостью, температурой плавления и низкими тепло и электропроводностью. Кристаллы с ковалентной связью диэлектрики или полупроводники.
В ковалентных кристаллах решетка построена из атомов, в узлах которой они одинаковые или разные , соединенные ковалентной связью, поэтому эти кристаллы обладают высокими твердостью, температурой плавления и низкими тепло и электропроводностью. Кристаллы с ковалентной связью диэлектрики или полупроводники.
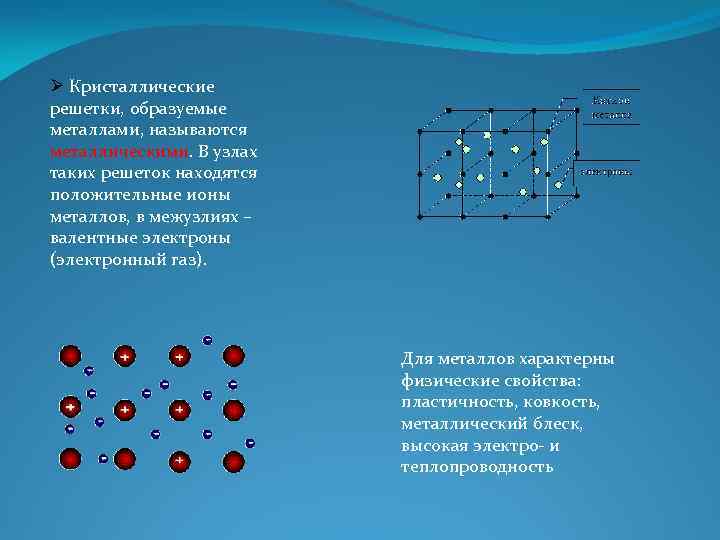 Ø Кристаллические решетки, образуемые металлами, называются металлическими. В узлах таких решеток находятся положительные ионы металлов, в межузлиях – валентные электроны (электронный газ). Для металлов характерны физические свойства: пластичность, ковкость, металлический блеск, высокая электро и теплопроводность
Ø Кристаллические решетки, образуемые металлами, называются металлическими. В узлах таких решеток находятся положительные ионы металлов, в межузлиях – валентные электроны (электронный газ). Для металлов характерны физические свойства: пластичность, ковкость, металлический блеск, высокая электро и теплопроводность
 Тип решетки определяется формой элементарного геометриче ского тела, многократное повторение которого по трем пространственным осям образует решетку данного кристаллического тела. 1 – простая кубическая решетка; 2 –гранецентрированная кубическая решетка; 3 – объемно-центрированная кубическая решетка; 4 – гексагональная решетка
Тип решетки определяется формой элементарного геометриче ского тела, многократное повторение которого по трем пространственным осям образует решетку данного кристаллического тела. 1 – простая кубическая решетка; 2 –гранецентрированная кубическая решетка; 3 – объемно-центрированная кубическая решетка; 4 – гексагональная решетка
 ØТемпературы плавления ионных кристаллов выше, чем атомных и молекулярных, поскольку электростатические силы, действующие между ионами, намного превышают слабые ван дер ваальсовы силы. Ионные соединения более твердые и хрупкие. Такие кристаллы образуются элементами с сильно различающимися электроотрицательностями (например, галогениды щелочных металлов). Ионные кристаллы, содержащие многоатомные ионы, имеют более низкие температуры плавления; так для Na. Cl tпл. = 801 °C, а для Na. NO 3 tпл = 306, 5 °C. Кварц – кристаллическая форма оксида кремния
ØТемпературы плавления ионных кристаллов выше, чем атомных и молекулярных, поскольку электростатические силы, действующие между ионами, намного превышают слабые ван дер ваальсовы силы. Ионные соединения более твердые и хрупкие. Такие кристаллы образуются элементами с сильно различающимися электроотрицательностями (например, галогениды щелочных металлов). Ионные кристаллы, содержащие многоатомные ионы, имеют более низкие температуры плавления; так для Na. Cl tпл. = 801 °C, а для Na. NO 3 tпл = 306, 5 °C. Кварц – кристаллическая форма оксида кремния


