Лекция_02_хим_связь_КБ.ppt
- Количество слайдов: 41
 Химическая связь в органических соединениях Лекция 2
Химическая связь в органических соединениях Лекция 2
 Определение Химическая связь – совокупность взаимодействий между электронами и ядрами, приводящих к соединению атомов в молекулу Уравнение Шредингера Ψ h Е Ер - оператор Лапласа - волновая функция электрона - постоянная Планка - полная энергия системы - потенциальная энергия
Определение Химическая связь – совокупность взаимодействий между электронами и ядрами, приводящих к соединению атомов в молекулу Уравнение Шредингера Ψ h Е Ер - оператор Лапласа - волновая функция электрона - постоянная Планка - полная энергия системы - потенциальная энергия
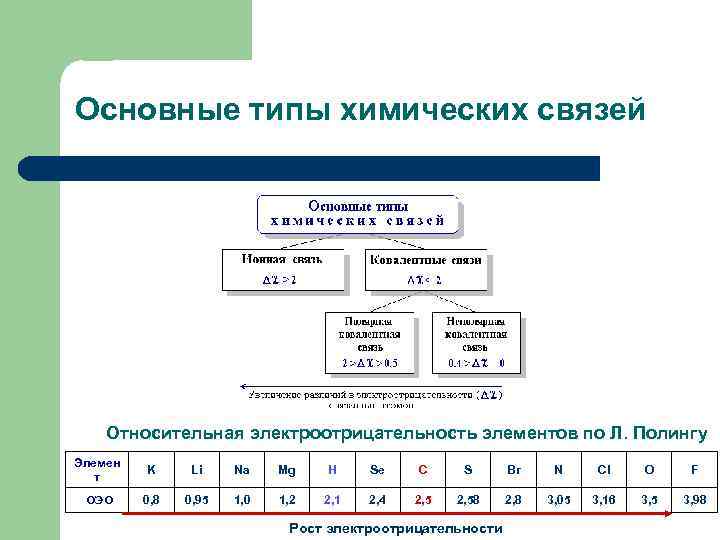 Основные типы химических связей Относительная электроотрицательность элементов по Л. Полингу Элемен т K Li Na Mg H Se C S Br N Cl O F ОЭО 0, 8 0, 95 1, 0 1, 2 2, 1 2, 4 2, 58 2, 8 3, 05 3, 16 3, 5 3, 98 Рост электроотрицательности
Основные типы химических связей Относительная электроотрицательность элементов по Л. Полингу Элемен т K Li Na Mg H Se C S Br N Cl O F ОЭО 0, 8 0, 95 1, 0 1, 2 2, 1 2, 4 2, 58 2, 8 3, 05 3, 16 3, 5 3, 98 Рост электроотрицательности
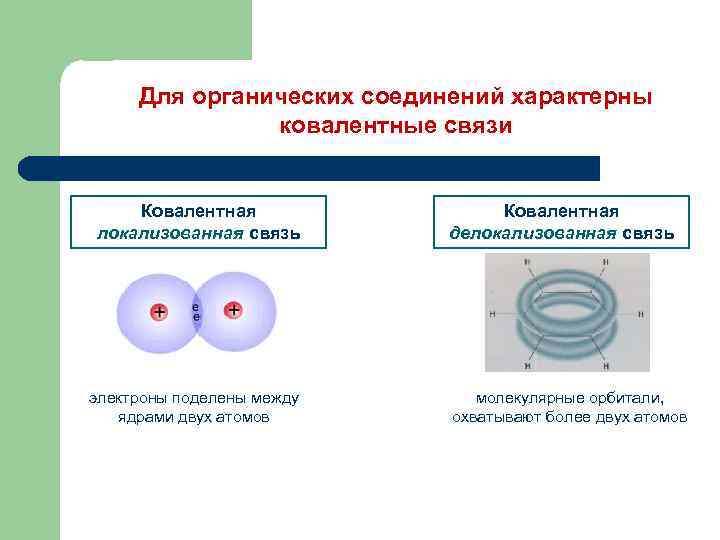 Для органических соединений характерны ковалентные связи Ковалентная локализованная связь электроны поделены между ядрами двух атомов Ковалентная делокализованная связь молекулярные орбитали, охватывают более двух атомов
Для органических соединений характерны ковалентные связи Ковалентная локализованная связь электроны поделены между ядрами двух атомов Ковалентная делокализованная связь молекулярные орбитали, охватывают более двух атомов
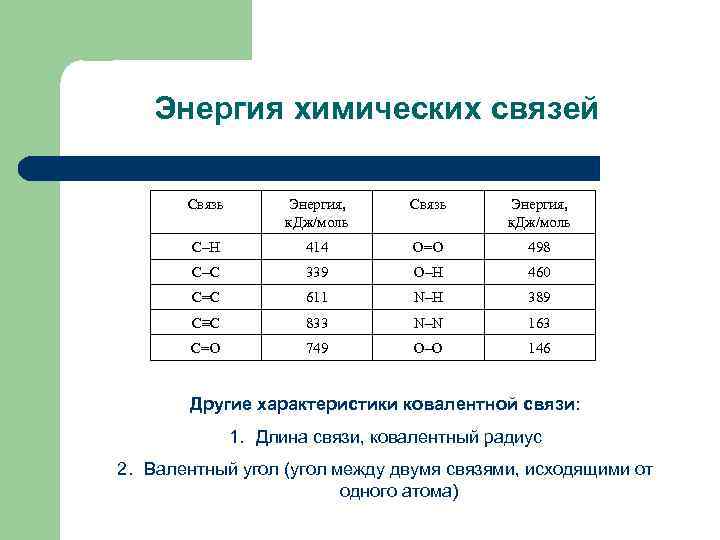 Энергия химических связей Связь Энергия, к. Дж/моль С–Н 414 O=O 498 С–С 339 O–H 460 С=С 611 N–H 389 С≡С 833 N–N 163 C=O 749 O–O 146 Другие характеристики ковалентной связи: 1. Длина связи, ковалентный радиус 2. Валентный угол (угол между двумя связями, исходящими от одного атома)
Энергия химических связей Связь Энергия, к. Дж/моль С–Н 414 O=O 498 С–С 339 O–H 460 С=С 611 N–H 389 С≡С 833 N–N 163 C=O 749 O–O 146 Другие характеристики ковалентной связи: 1. Длина связи, ковалентный радиус 2. Валентный угол (угол между двумя связями, исходящими от одного атома)
 Свойства ковалентной связи 1) Направленность: связь атомов осуществляется в том направлении, в котором обеспечивается максимальное перекрывание орбиталей 2) Насыщаемость: способность атомов образовывать ограниченное число ковалентных связей 3) Полярность: результат неравномерного распределения электронной плотности 4) Дипольный момент связи (μ): векторная величина, характеризующая полярность связи μ [D, Кл·м] 1 D = 3, 4· 10 -30 Кл·м 5) Поляризуемость: смещение электронной плотности под влиянием внешнего поля, среды, реагентов, катализаторов
Свойства ковалентной связи 1) Направленность: связь атомов осуществляется в том направлении, в котором обеспечивается максимальное перекрывание орбиталей 2) Насыщаемость: способность атомов образовывать ограниченное число ковалентных связей 3) Полярность: результат неравномерного распределения электронной плотности 4) Дипольный момент связи (μ): векторная величина, характеризующая полярность связи μ [D, Кл·м] 1 D = 3, 4· 10 -30 Кл·м 5) Поляризуемость: смещение электронной плотности под влиянием внешнего поля, среды, реагентов, катализаторов
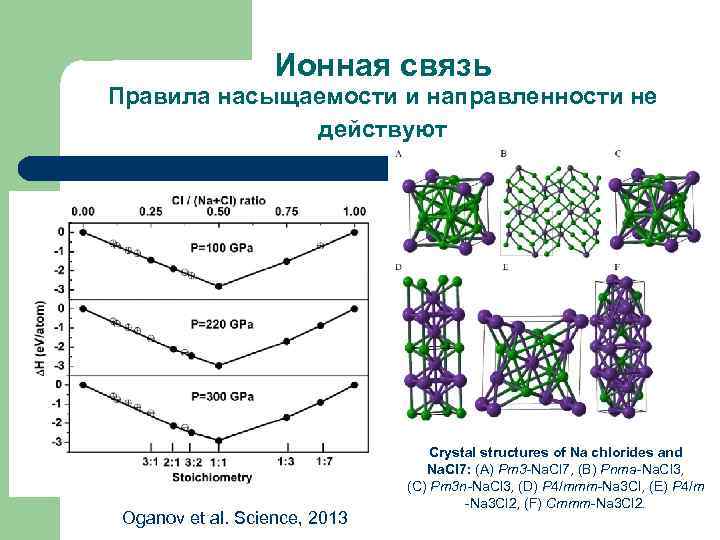 Ионная связь Правила насыщаемости и направленности не действуют Oganov et al. Science, 2013 Crystal structures of Na chlorides and Na. Cl 7: (A) Pm 3 -Na. Cl 7, (B) Pnma-Na. Cl 3, (C) Pm 3 n-Na. Cl 3, (D) P 4/mmm-Na 3 Cl, (E) P 4/m -Na 3 Cl 2, (F) Cmmm-Na 3 Cl 2.
Ионная связь Правила насыщаемости и направленности не действуют Oganov et al. Science, 2013 Crystal structures of Na chlorides and Na. Cl 7: (A) Pm 3 -Na. Cl 7, (B) Pnma-Na. Cl 3, (C) Pm 3 n-Na. Cl 3, (D) P 4/mmm-Na 3 Cl, (E) P 4/m -Na 3 Cl 2, (F) Cmmm-Na 3 Cl 2.
 Гибридизация атомных орбиталей Гибридизация – выравнивание (смешивание) атомных орбиталей (s и р) с образованием новых атомных орбиталей, называемых гибридными орбиталями. Четыре sp 3 -гибридные орбитали атома углерода
Гибридизация атомных орбиталей Гибридизация – выравнивание (смешивание) атомных орбиталей (s и р) с образованием новых атомных орбиталей, называемых гибридными орбиталями. Четыре sp 3 -гибридные орбитали атома углерода
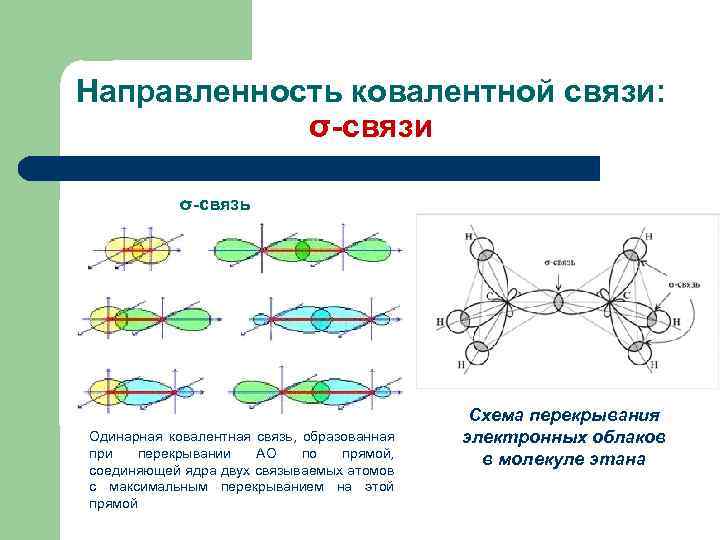 Направленность ковалентной связи: σ-связи σ-связь Одинарная ковалентная связь, образованная при перекрывании АО по прямой, соединяющей ядра двух связываемых атомов с максимальным перекрыванием на этой прямой Схема перекрывания электронных облаков в молекуле этана
Направленность ковалентной связи: σ-связи σ-связь Одинарная ковалентная связь, образованная при перекрывании АО по прямой, соединяющей ядра двух связываемых атомов с максимальным перекрыванием на этой прямой Схема перекрывания электронных облаков в молекуле этана
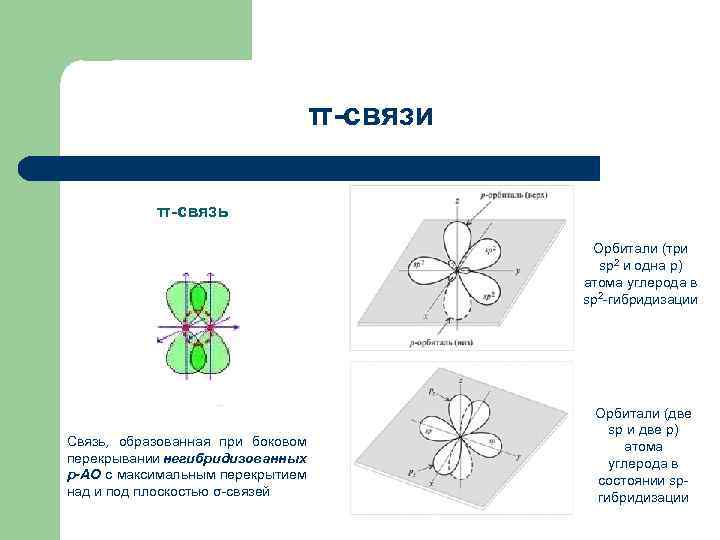 π-связи π-связь Орбитали (три sp 2 и одна р) атома углерода в sp 2 -гибридизации Связь, образованная при боковом перекрывании негибридизованных р-АО с максимальным перекрытием над и под плоскостью σ-связей Орбитали (две sp и две р) атома углерода в состоянии spгибридизации
π-связи π-связь Орбитали (три sp 2 и одна р) атома углерода в sp 2 -гибридизации Связь, образованная при боковом перекрывании негибридизованных р-АО с максимальным перекрытием над и под плоскостью σ-связей Орбитали (две sp и две р) атома углерода в состоянии spгибридизации
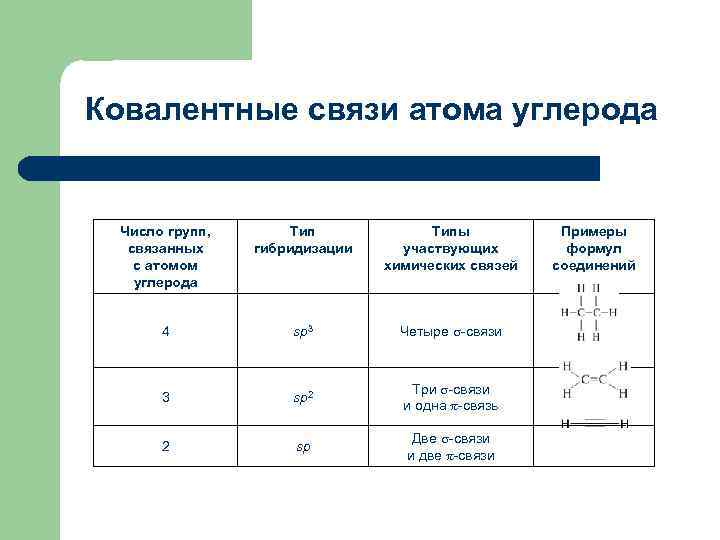 Ковалентные связи атома углерода Число групп, связанных с атомом углерода Тип гибридизации Типы участвующих химических связей Примеры формул соединений 4 sp 3 Четыре -связи 3 sp 2 Три -связи и одна -связь 2 sp Две -связи и две -связи
Ковалентные связи атома углерода Число групп, связанных с атомом углерода Тип гибридизации Типы участвующих химических связей Примеры формул соединений 4 sp 3 Четыре -связи 3 sp 2 Три -связи и одна -связь 2 sp Две -связи и две -связи
 Характерные особенности σ- и πсвязей l l l σ-Связь прочнее π-связи. Это обусловлено более эффективным осевым перекрыванием АО при образовании σ-МО и нахождением σ-электронов между ядрами. По σ-связям возможно внутримолекулярное вращение атомов, т. к. форма σ-МО допускает такое вращение без разрыва связи. Вращение по двойной (σ + π) связи невозможно без разрыва π-связи! Электроны на π-МО, находясь вне межъядерного пространства, обладают большей подвижностью по сравнению с σ-электронами. Поэтому поляризуемость π-связи значительно выше, чем σсвязи.
Характерные особенности σ- и πсвязей l l l σ-Связь прочнее π-связи. Это обусловлено более эффективным осевым перекрыванием АО при образовании σ-МО и нахождением σ-электронов между ядрами. По σ-связям возможно внутримолекулярное вращение атомов, т. к. форма σ-МО допускает такое вращение без разрыва связи. Вращение по двойной (σ + π) связи невозможно без разрыва π-связи! Электроны на π-МО, находясь вне межъядерного пространства, обладают большей подвижностью по сравнению с σ-электронами. Поэтому поляризуемость π-связи значительно выше, чем σсвязи.
 Внутримолекулярное вращение по σсвязям
Внутримолекулярное вращение по σсвязям
 Обменный (спиновый) механизм образования ковалентной связи A· + B· A: B (A-B) Пример: H 3 C· + ·CH 3 H 3 C-CH 3
Обменный (спиновый) механизм образования ковалентной связи A· + B· A: B (A-B) Пример: H 3 C· + ·CH 3 H 3 C-CH 3
 Донорно-акцепторный механизм образования ковалентной связи (координационная связь) D: + A : первичный амин : D A _ _ соль алкиламмония
Донорно-акцепторный механизм образования ковалентной связи (координационная связь) D: + A : первичный амин : D A _ _ соль алкиламмония
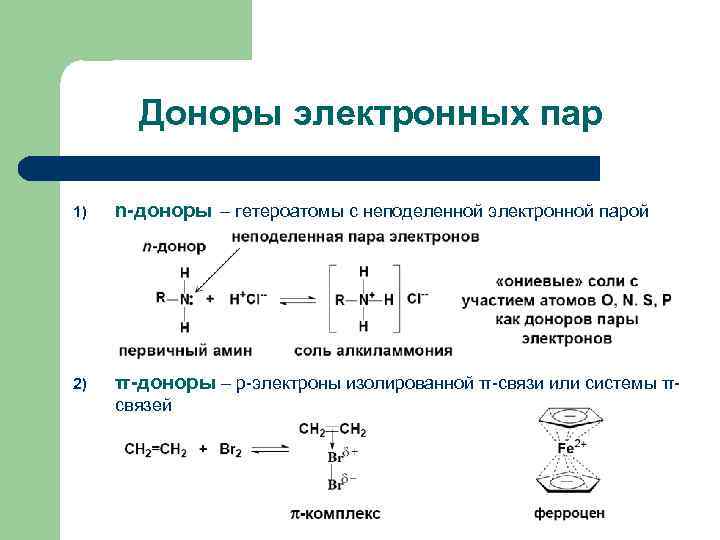 Доноры электронных пар 1) n-доноры – гетероатомы с неподеленной электронной парой 2) π-доноры – р-электроны изолированной π-связи или системы πсвязей
Доноры электронных пар 1) n-доноры – гетероатомы с неподеленной электронной парой 2) π-доноры – р-электроны изолированной π-связи или системы πсвязей
 Методы описания химической связи 1) Метод молекулярных орбиталей (МО) Вариант: МО ЛКАО (молекулярная орбитальлинейная комбинация атомных орбиталей) Р. Малликен (1966) Ψ = С 1ψ1 + С 2ψ2 + … + Сnψn 2) Метод резонансных структур (метод резонанса, РС) К. Ингольд (1922), Л. Полинг (1928)
Методы описания химической связи 1) Метод молекулярных орбиталей (МО) Вариант: МО ЛКАО (молекулярная орбитальлинейная комбинация атомных орбиталей) Р. Малликен (1966) Ψ = С 1ψ1 + С 2ψ2 + … + Сnψn 2) Метод резонансных структур (метод резонанса, РС) К. Ингольд (1922), Л. Полинг (1928)
 Применение методов МО и РС • Описание делокализованных связей • Определение относительной стабильности промежуточных частиц • Прогнозирование реакционной способности органических соединений
Применение методов МО и РС • Описание делокализованных связей • Определение относительной стабильности промежуточных частиц • Прогнозирование реакционной способности органических соединений
 Метод молекулярных орбиталей
Метод молекулярных орбиталей
 Молекулярные орбитали Е |ψ+|2 = | ψA + ψB |2 = ψA 2 + 2ψAψB + ψB 2 _ ψ = ψA - ψB _ |ψ |2 = | ψA - ψB |2 = ψA 2 - 2ψAψB + ψB 2 ψB ψA + ψ = ψA + ψB SAB = ∫ψAψBd. V βAB = C ∫AB(IA + IB) интеграл перекрывания резонансный интеграл
Молекулярные орбитали Е |ψ+|2 = | ψA + ψB |2 = ψA 2 + 2ψAψB + ψB 2 _ ψ = ψA - ψB _ |ψ |2 = | ψA - ψB |2 = ψA 2 - 2ψAψB + ψB 2 ψB ψA + ψ = ψA + ψB SAB = ∫ψAψBd. V βAB = C ∫AB(IA + IB) интеграл перекрывания резонансный интеграл
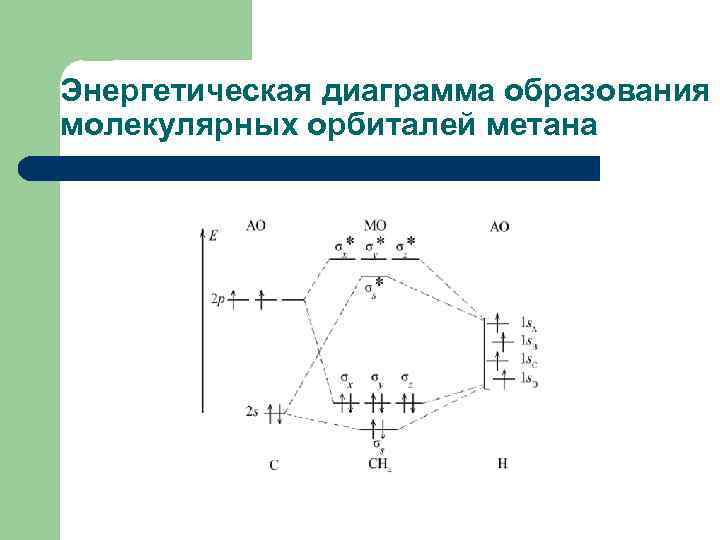 Энергетическая диаграмма образования молекулярных орбиталей метана
Энергетическая диаграмма образования молекулярных орбиталей метана
 Электронные эффекты
Электронные эффекты
 Индуктивный эффект (I-эффект) – передача электронного влияния заместителей по цепи σ-связей Причина: различные электроотрицательности атомов, образующих σ-связь Аδ+→ВδБолее электроотрицательный атом (В) является акцептором по индуктивному эффекту Индуктивный эффект вызывает поляризацию молекул и появление дипольного момента Дипольные моменты связей Связь μ • 1030, Кл • м μ, D C-C 0 0 C=O 10, 88 3, 2 C-H 1, 36 0, 4 C-Cl 7, 82 2, 3 C-N 4, 08 1, 2 N-H 4, 42 1, 3 C≡N 13, 6 4, 0 O-H 5, 1 1, 5 C-O 5, 44 1, 6
Индуктивный эффект (I-эффект) – передача электронного влияния заместителей по цепи σ-связей Причина: различные электроотрицательности атомов, образующих σ-связь Аδ+→ВδБолее электроотрицательный атом (В) является акцептором по индуктивному эффекту Индуктивный эффект вызывает поляризацию молекул и появление дипольного момента Дипольные моменты связей Связь μ • 1030, Кл • м μ, D C-C 0 0 C=O 10, 88 3, 2 C-H 1, 36 0, 4 C-Cl 7, 82 2, 3 C-N 4, 08 1, 2 N-H 4, 42 1, 3 C≡N 13, 6 4, 0 O-H 5, 1 1, 5 C-O 5, 44 1, 6
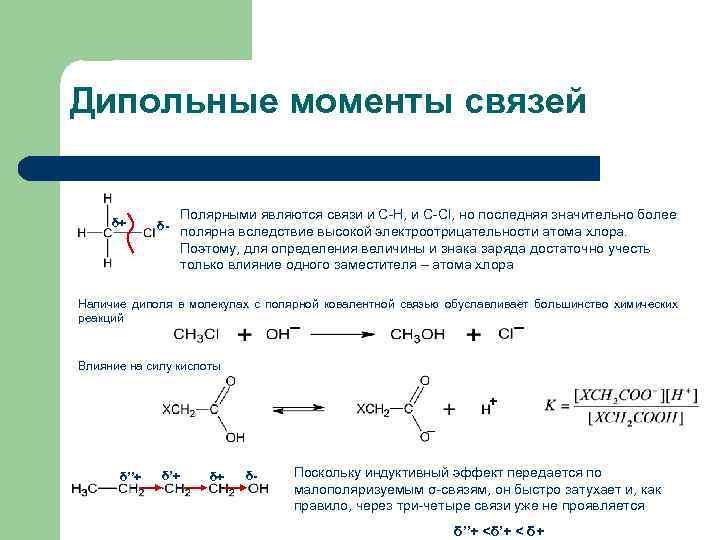 Дипольные моменты связей δ+ δ- Полярными являются связи и С-Н, и С-Сl, но последняя значительно более полярна вследствие высокой электроотрицательности атома хлора. Поэтому, для определения величины и знака заряда достаточно учесть только влияние одного заместителя – атома хлора Наличие диполя в молекулах с полярной ковалентной связью обуславливает большинство химических реакций _ _ Влияние на силу кислоты + _ δ’’+ δ+ δ- Поскольку индуктивный эффект передается по малополяризуемым σ-связям, он быстро затухает и, как правило, через три-четыре связи уже не проявляется δ’’+ <δ’+ < δ+
Дипольные моменты связей δ+ δ- Полярными являются связи и С-Н, и С-Сl, но последняя значительно более полярна вследствие высокой электроотрицательности атома хлора. Поэтому, для определения величины и знака заряда достаточно учесть только влияние одного заместителя – атома хлора Наличие диполя в молекулах с полярной ковалентной связью обуславливает большинство химических реакций _ _ Влияние на силу кислоты + _ δ’’+ δ+ δ- Поскольку индуктивный эффект передается по малополяризуемым σ-связям, он быстро затухает и, как правило, через три-четыре связи уже не проявляется δ’’+ <δ’+ < δ+
 Положительный и отрицательный индуктивный эффект Знак эффекта совпадает с зарядом, приобретаемым заместителем при сдвиге электронов
Положительный и отрицательный индуктивный эффект Знак эффекта совпадает с зарядом, приобретаемым заместителем при сдвиге электронов
 Закономерности проявления индуктивного эффекта Величина I-эффекта растет с увеличением заряда на заместителе + + -NR 2 < -NO 2 < NR 3 < =NR 2 -I растет + + + -SR 2 < -NR 3 ~ -OR 2 -I растет Заместитель обладает тем большим - I-эффектом, чем правее и выше в периодической системе находится элемент, определяющий характер заместителя -NR 2 < -OR ~ -F -I растет -I < -Br < -Cl < -F -I растет
Закономерности проявления индуктивного эффекта Величина I-эффекта растет с увеличением заряда на заместителе + + -NR 2 < -NO 2 < NR 3 < =NR 2 -I растет + + + -SR 2 < -NR 3 ~ -OR 2 -I растет Заместитель обладает тем большим - I-эффектом, чем правее и выше в периодической системе находится элемент, определяющий характер заместителя -NR 2 < -OR ~ -F -I растет -I < -Br < -Cl < -F -I растет
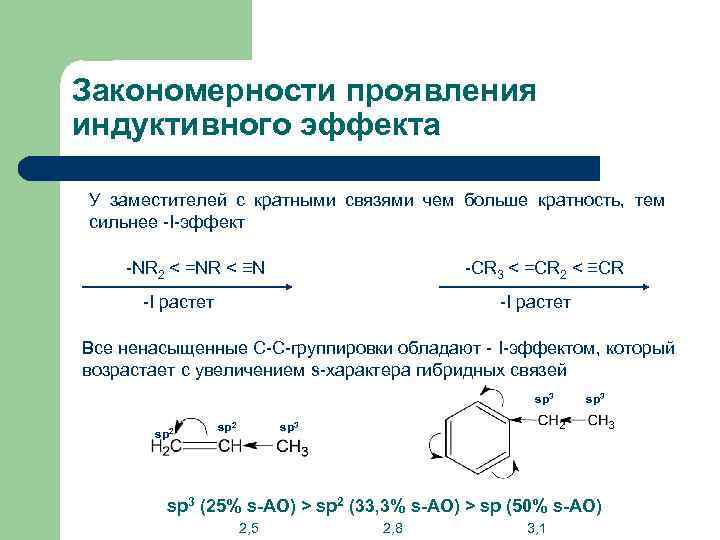 Закономерности проявления индуктивного эффекта У заместителей с кратными связями чем больше кратность, тем сильнее -I-эффект -NR 2 < =NR < ≡N -CR 3 < =CR 2 < ≡CR -I растет Все ненасыщенные С-С-группировки обладают - I-эффектом, который возрастает с увеличением s-характера гибридных связей sp 3 sp 2 sp 3 (25% s-АО) > sp 2 (33, 3% s-АО) > sp (50% s-АО) 2, 5 2, 8 3, 1
Закономерности проявления индуктивного эффекта У заместителей с кратными связями чем больше кратность, тем сильнее -I-эффект -NR 2 < =NR < ≡N -CR 3 < =CR 2 < ≡CR -I растет Все ненасыщенные С-С-группировки обладают - I-эффектом, который возрастает с увеличением s-характера гибридных связей sp 3 sp 2 sp 3 (25% s-АО) > sp 2 (33, 3% s-АО) > sp (50% s-АО) 2, 5 2, 8 3, 1
 Индуктивный эффект алкильных групп Алкильные группы проявляют +I-эффект тем сильнее, чем выше разветвленность -CH 3 < -CH 2 CH 3 < CH(CH 3)2 < C(CH 3)3 +I растет
Индуктивный эффект алкильных групп Алкильные группы проявляют +I-эффект тем сильнее, чем выше разветвленность -CH 3 < -CH 2 CH 3 < CH(CH 3)2 < C(CH 3)3 +I растет
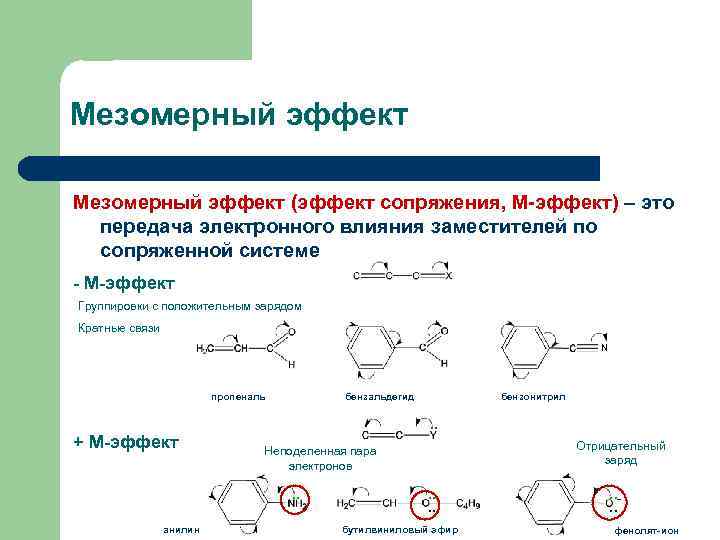 Мезомерный эффект (эффект сопряжения, М-эффект) – это передача электронного влияния заместителей по сопряженной системе - М-эффект Группировки с положительным зарядом Кратные связи N пропеналь + М-эффект бензальдегид . . Отрицательный заряд Неподеленная пара электронов . . анилин бензонитрил . . бутилвиниловый эфир . . фенолят-ион
Мезомерный эффект (эффект сопряжения, М-эффект) – это передача электронного влияния заместителей по сопряженной системе - М-эффект Группировки с положительным зарядом Кратные связи N пропеналь + М-эффект бензальдегид . . Отрицательный заряд Неподеленная пара электронов . . анилин бензонитрил . . бутилвиниловый эфир . . фенолят-ион
 +М-эффект ОН-группы в молекуле фенола
+М-эффект ОН-группы в молекуле фенола
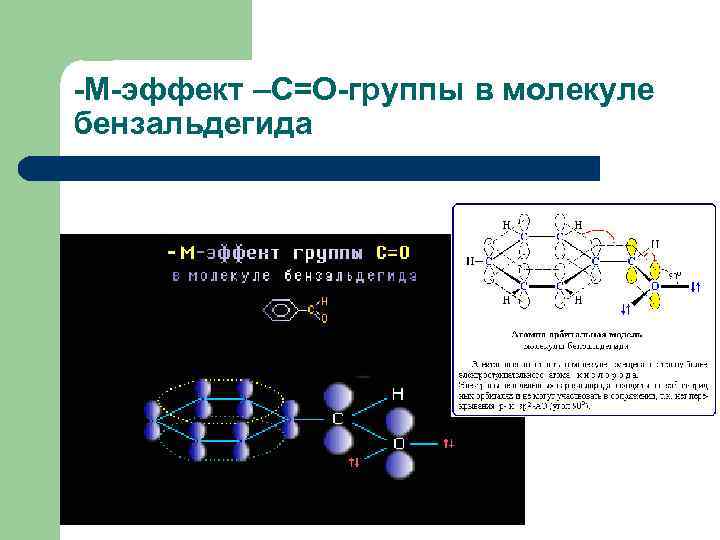 -М-эффект –С=О-группы в молекуле бензальдегида
-М-эффект –С=О-группы в молекуле бензальдегида
 Закономерности проявления мезомерного эффекта Величина -М-эффекта растет с увеличением заряда заместителя + - -HC=NR < -HC=NR 2 -M растет - -O < -SH -M растет + -N≡N > -SO 3 H ~ -NO 2 > -CN > C=O -M убывает -М-эффект тем сильнее, чем имеющихся в заместителе атомов электроотрицательность -CH=CHR < -CH=NR < -C=O -C≡C-R < -C≡N -M растет больше -NR 2 > -OR > -F -M растет
Закономерности проявления мезомерного эффекта Величина -М-эффекта растет с увеличением заряда заместителя + - -HC=NR < -HC=NR 2 -M растет - -O < -SH -M растет + -N≡N > -SO 3 H ~ -NO 2 > -CN > C=O -M убывает -М-эффект тем сильнее, чем имеющихся в заместителе атомов электроотрицательность -CH=CHR < -CH=NR < -C=O -C≡C-R < -C≡N -M растет больше -NR 2 > -OR > -F -M растет
 Характер совместного действия заместителей
Характер совместного действия заместителей
 Резонанс
Резонанс
 Теория резонанса: определения Теория (метод) резонанса – способ описания сопряженных πсистем, демонстрирующий подвижность π-электронов под действием заместителей, обладающих мезомерным эффектом* π-Система – цепочка атомов, каждый их которых имеет р-орбиталь, либо неподеленную пару электронов. Такие системы называются сопряженными * Мезомерный эффект – передача электронного влияния заместителей по сопряженной системе
Теория резонанса: определения Теория (метод) резонанса – способ описания сопряженных πсистем, демонстрирующий подвижность π-электронов под действием заместителей, обладающих мезомерным эффектом* π-Система – цепочка атомов, каждый их которых имеет р-орбиталь, либо неподеленную пару электронов. Такие системы называются сопряженными * Мезомерный эффект – передача электронного влияния заместителей по сопряженной системе
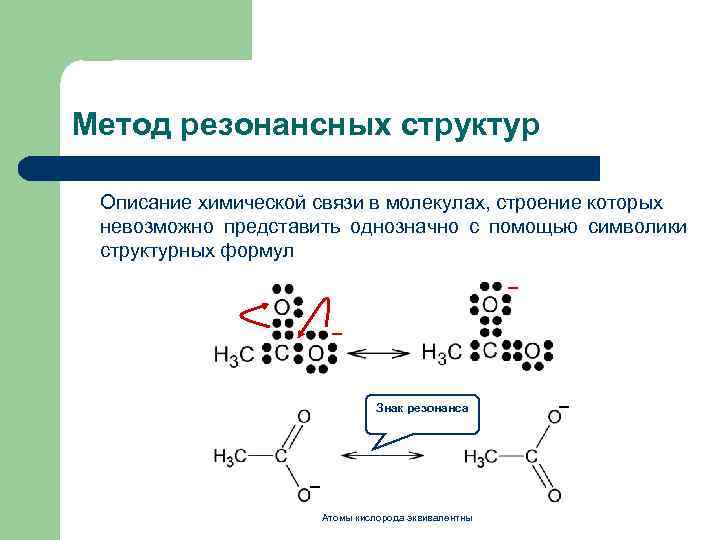 Метод резонансных структур Описание химической связи в молекулах, строение которых невозможно представить однозначно с помощью символики структурных формул _ _ Знак резонанса _ Атомы кислорода эквивалентны _
Метод резонансных структур Описание химической связи в молекулах, строение которых невозможно представить однозначно с помощью символики структурных формул _ _ Знак резонанса _ Атомы кислорода эквивалентны _
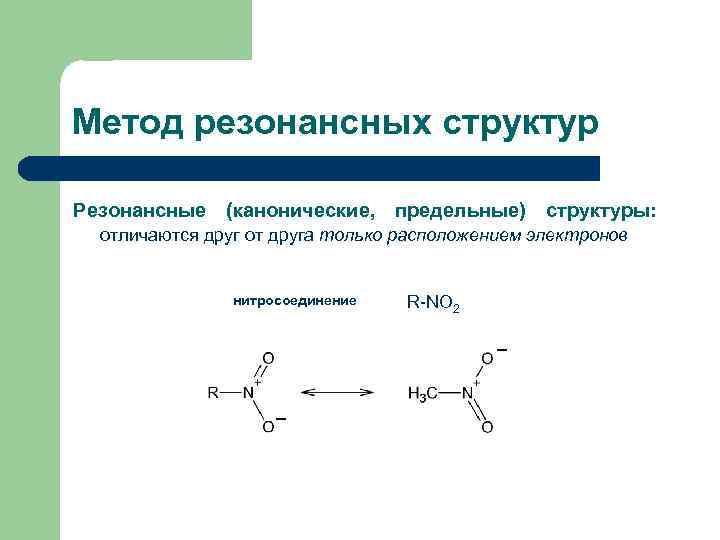 Метод резонансных структур Резонансные (канонические, предельные) структуры: отличаются друг от друга только расположением электронов нитросоединение R-NO 2 _ _
Метод резонансных структур Резонансные (канонические, предельные) структуры: отличаются друг от друга только расположением электронов нитросоединение R-NO 2 _ _
 Положения метода резонанса 1) Резонансные структуры не должны отличаться расположением атомов. 2) Каждая резонансная структура не должна изменять валентность атомов. 3) Все резонансные структуры должны иметь одинаковое число неспаренных электронов.
Положения метода резонанса 1) Резонансные структуры не должны отличаться расположением атомов. 2) Каждая резонансная структура не должна изменять валентность атомов. 3) Все резонансные структуры должны иметь одинаковое число неспаренных электронов.
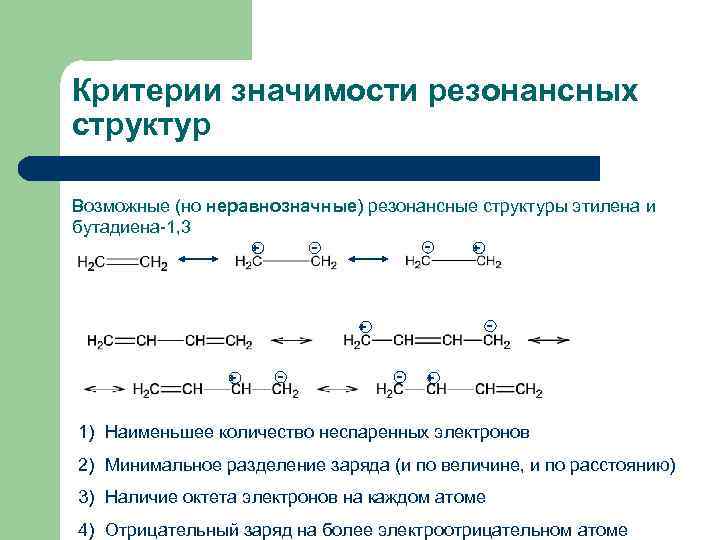 Критерии значимости резонансных структур Возможные (но неравнозначные) резонансные структуры этилена и бутадиена-1, 3 + + - - + 1) Наименьшее количество неспаренных электронов 2) Минимальное разделение заряда (и по величине, и по расстоянию) 3) Наличие октета электронов на каждом атоме 4) Отрицательный заряд на более электроотрицательном атоме
Критерии значимости резонансных структур Возможные (но неравнозначные) резонансные структуры этилена и бутадиена-1, 3 + + - - + 1) Наименьшее количество неспаренных электронов 2) Минимальное разделение заряда (и по величине, и по расстоянию) 3) Наличие октета электронов на каждом атоме 4) Отрицательный заряд на более электроотрицательном атоме
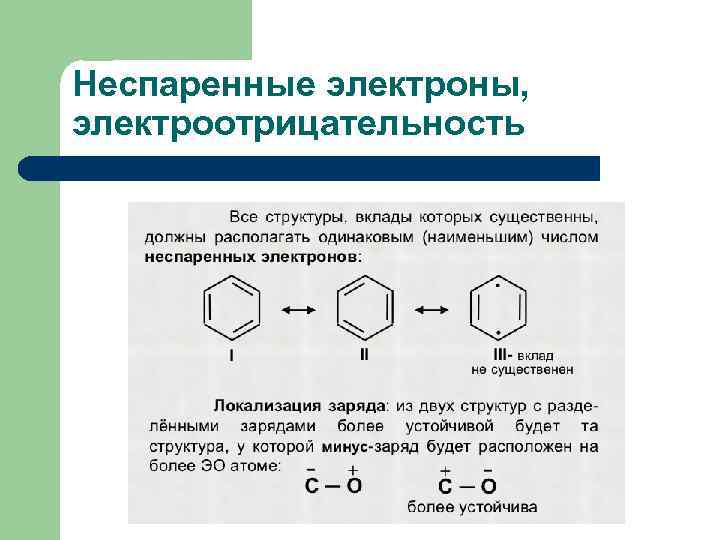 Неспаренные электроны, электроотрицательность
Неспаренные электроны, электроотрицательность
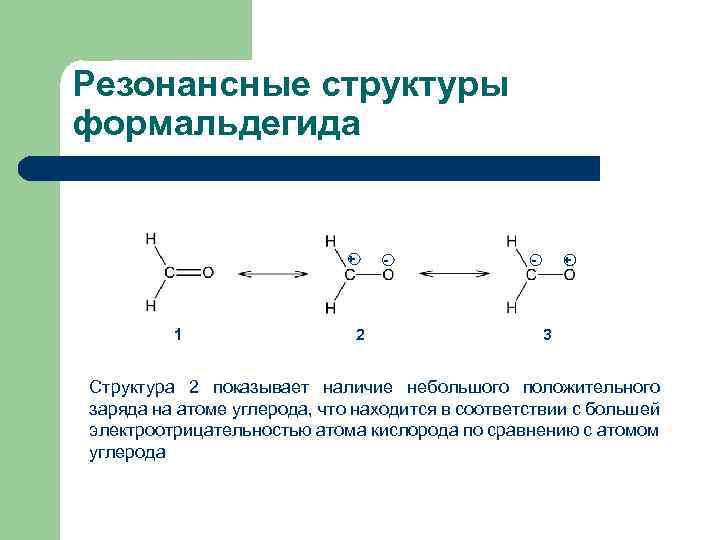 Резонансные структуры формальдегида + 1 - 2 - + 3 Структура 2 показывает наличие небольшого положительного заряда на атоме углерода, что находится в соответствии с большей электроотрицательностью атома кислорода по сравнению с атомом углерода
Резонансные структуры формальдегида + 1 - 2 - + 3 Структура 2 показывает наличие небольшого положительного заряда на атоме углерода, что находится в соответствии с большей электроотрицательностью атома кислорода по сравнению с атомом углерода


