Презентация Химическая связь-ков и ионная (2).ppt
- Количество слайдов: 19
 Химическая связь Шкатова Е. В. ГОУ СОШ № 269
Химическая связь Шкатова Е. В. ГОУ СОШ № 269
 Химическая связь – это совокупность сил, обуславливающих взаимодействие атомов (или других частиц) друг с другом в химическом соединении. Химическая связь – это сила, удерживающая друг возле друга частицы в соединении.
Химическая связь – это совокупность сил, обуславливающих взаимодействие атомов (или других частиц) друг с другом в химическом соединении. Химическая связь – это сила, удерживающая друг возле друга частицы в соединении.
 В образовании химической связи принимают участие валентные электроны (электроны внешнего и иногда предвнешнего энергетического уровня). Ковалентная связь – связь между атомами, возникающая за счёт образования общих электронных пар. При образовании ковалентной связи происходит перекрывание атомных орбиталей.
В образовании химической связи принимают участие валентные электроны (электроны внешнего и иногда предвнешнего энергетического уровня). Ковалентная связь – связь между атомами, возникающая за счёт образования общих электронных пар. При образовании ковалентной связи происходит перекрывание атомных орбиталей.
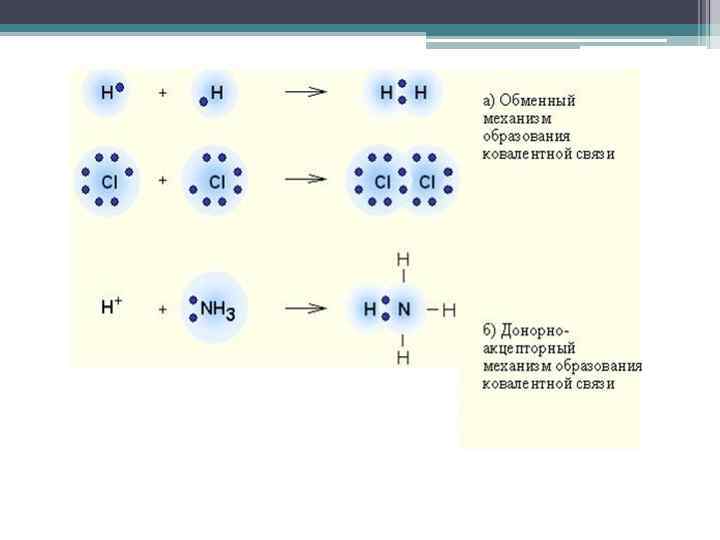
 Существует два механизма образования ковалентной связи: Обменный Общие электронные пары образованы неспаренными электронами исходных атомов. Донорно – акцепторный Общая электронная пара предоставляется одним из атомов (донором), другой атом содержит вакантную (свободную) орбиталь.
Существует два механизма образования ковалентной связи: Обменный Общие электронные пары образованы неспаренными электронами исходных атомов. Донорно – акцепторный Общая электронная пара предоставляется одним из атомов (донором), другой атом содержит вакантную (свободную) орбиталь.
 Существует два вида ковалентной связи: - Ковалентная неполярная -Ковалентная полярная Полярность связи определяется различием в значении электроотрицательности. Электроотрицательность – свойство атомов притягивать электроны, участвующие в образовании химической связи (то есть один из взаимодействующих атомов оттягивает на себя общую электронную пару)
Существует два вида ковалентной связи: - Ковалентная неполярная -Ковалентная полярная Полярность связи определяется различием в значении электроотрицательности. Электроотрицательность – свойство атомов притягивать электроны, участвующие в образовании химической связи (то есть один из взаимодействующих атомов оттягивает на себя общую электронную пару)


 Виды ковалентной связи • Неполярная • Полярная • Связь между атомами одного и того же элемента • Связь, возникающая между атомами элементов, отличающихся значением э/о • Ковалентной неполярной связью образованы молекулы простых веществнеметаллов – кислорода, водорода, хлора, азота и др. • Ковалентной полярной связью образованы молекулы, состоящие из атомов неметаллов – хлороводород, аммиак, оксид углерода и др.
Виды ковалентной связи • Неполярная • Полярная • Связь между атомами одного и того же элемента • Связь, возникающая между атомами элементов, отличающихся значением э/о • Ковалентной неполярной связью образованы молекулы простых веществнеметаллов – кислорода, водорода, хлора, азота и др. • Ковалентной полярной связью образованы молекулы, состоящие из атомов неметаллов – хлороводород, аммиак, оксид углерода и др.
 Характеристики ковалентной связи Длина связи – межъядерное расстояние взаимодействующих атомов (нм). Энергия связи – энергия, выделяющаяся при образовании связи или энергия, которую необходимо затратить на разрыв связи. Кратность связи – число общих электронных пар между соединяющимися атомами. -одинарная связь (молекула водорода) -двойная связь (молекула кислорода) - тройная связь (молекула азота)
Характеристики ковалентной связи Длина связи – межъядерное расстояние взаимодействующих атомов (нм). Энергия связи – энергия, выделяющаяся при образовании связи или энергия, которую необходимо затратить на разрыв связи. Кратность связи – число общих электронных пар между соединяющимися атомами. -одинарная связь (молекула водорода) -двойная связь (молекула кислорода) - тройная связь (молекула азота)
 Свойства ковалентной связи Насыщаемость. При образовании связи в области связывания могут находится только два электрона с противоположными спинами. Насыщаемость кс зависит от валентности атомов элементов, образующих связь. Направленность. Так кс образуется при перекрывании атомных орбиталей, которые направлены в пространстве, то и кс пространственно направлены.
Свойства ковалентной связи Насыщаемость. При образовании связи в области связывания могут находится только два электрона с противоположными спинами. Насыщаемость кс зависит от валентности атомов элементов, образующих связь. Направленность. Так кс образуется при перекрывании атомных орбиталей, которые направлены в пространстве, то и кс пространственно направлены.
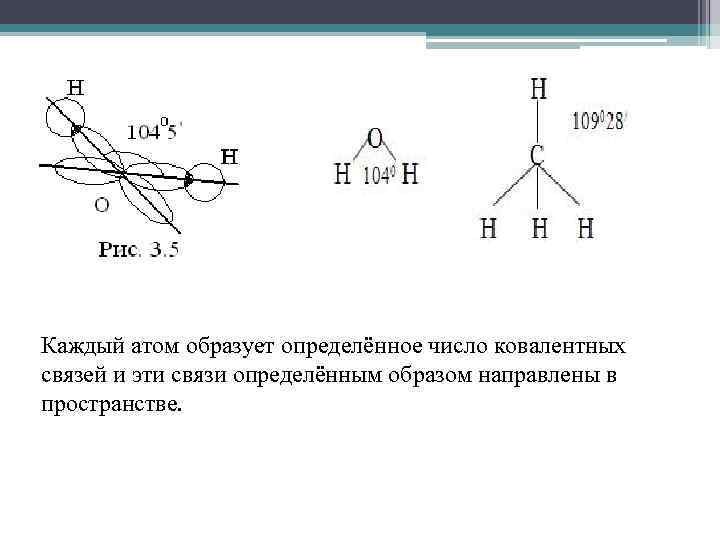 Каждый атом образует определённое число ковалентных связей и эти связи определённым образом направлены в пространстве.
Каждый атом образует определённое число ковалентных связей и эти связи определённым образом направлены в пространстве.
 Ионная связь. В образовании ионной связи участвуют частицы – ионы. Ионы – заряженные частицы, образующиеся в результате отдачи или присоединения электронов атомами или группами атомов. Различают два вида ионов: Катионы «+» Анионы «-»
Ионная связь. В образовании ионной связи участвуют частицы – ионы. Ионы – заряженные частицы, образующиеся в результате отдачи или присоединения электронов атомами или группами атомов. Различают два вида ионов: Катионы «+» Анионы «-»
 Причина образования ионной связи заключается в тенденции атомов к приобретению устойчивой восьмиэлектронной оболочки. Условно можно разделить процесс образования ионной связи (на примере хлорида натрия) на три этапа: - образование катиона натрия (отдаёт 1 электрон и приобретает устойчивую оболочку) - образование аниона хлора (принимает один электрон и приобретает устойчивую оболочку) - образование связи между катионом и анионом Ионная связь – связь, образующаяся между ионами противоположного знака в результате их электростатического взаимодействия.
Причина образования ионной связи заключается в тенденции атомов к приобретению устойчивой восьмиэлектронной оболочки. Условно можно разделить процесс образования ионной связи (на примере хлорида натрия) на три этапа: - образование катиона натрия (отдаёт 1 электрон и приобретает устойчивую оболочку) - образование аниона хлора (принимает один электрон и приобретает устойчивую оболочку) - образование связи между катионом и анионом Ионная связь – связь, образующаяся между ионами противоположного знака в результате их электростатического взаимодействия.
 Ионная связь образуется при взаимодействии атомов, резко отличающихся по значениям электроотрицательности. Как правило в образовании этого типа связи принимают участие атомы типичного металла и типичного неметалла (хлорид натрия, оксиды активных металлов). В молекулах кислот, оснований и солей присутствуют связи ионного типа. Ионная связь – предельный случай ковалентной полярной связи.
Ионная связь образуется при взаимодействии атомов, резко отличающихся по значениям электроотрицательности. Как правило в образовании этого типа связи принимают участие атомы типичного металла и типичного неметалла (хлорид натрия, оксиды активных металлов). В молекулах кислот, оснований и солей присутствуют связи ионного типа. Ионная связь – предельный случай ковалентной полярной связи.

 1. Определите тип химической связи в следующих соединениях: О 2, Н 2 О, Ca. Cl 2, CO 2 2. Ионная связь характерна для каждого из двух веществ: 1) H 2 S, K 2 O 2) NO, HCl 3) Na. F, Ca. O 4) S, CO 2 3. Ковалентная полярная связь характерна для каждого из двух веществ: 1) Na 2 S, NO 2 2) CO, Cl 2 3) O 2, PH 3 4) HF, Si. O 2
1. Определите тип химической связи в следующих соединениях: О 2, Н 2 О, Ca. Cl 2, CO 2 2. Ионная связь характерна для каждого из двух веществ: 1) H 2 S, K 2 O 2) NO, HCl 3) Na. F, Ca. O 4) S, CO 2 3. Ковалентная полярная связь характерна для каждого из двух веществ: 1) Na 2 S, NO 2 2) CO, Cl 2 3) O 2, PH 3 4) HF, Si. O 2
 4. Выберите из списка веществ, в молекулах которых ковалентная неполярная связь: PCl 5, CH 4, H 2, CO 2, S 8, SCl 2, Si. H 4 5. Выберите из списка вещества, в молекулах которых ковалентная полярная связь: O 3, P 2 O 5, P 4, H 2 SO 4, Cs. F, HNO 3, H 2 6. Как меняется полярность связи в ряду HCl-H 2 S-PH 3 7. Как меняется полярность связи в ряду HCl-HBr-HI
4. Выберите из списка веществ, в молекулах которых ковалентная неполярная связь: PCl 5, CH 4, H 2, CO 2, S 8, SCl 2, Si. H 4 5. Выберите из списка вещества, в молекулах которых ковалентная полярная связь: O 3, P 2 O 5, P 4, H 2 SO 4, Cs. F, HNO 3, H 2 6. Как меняется полярность связи в ряду HCl-H 2 S-PH 3 7. Как меняется полярность связи в ряду HCl-HBr-HI
 Урок окончен! Спасибо за внимание!
Урок окончен! Спасибо за внимание!


