Химическая связь Природа и основные количественные
















him.svyazy1_lekciya_4,_5.ppt
- Размер: 373.0 Кб
- Автор:
- Количество слайдов: 22
Описание презентации Химическая связь Природа и основные количественные по слайдам
 Химическая связь Природа и основные количественные характеристики химической связи. Ковалентная связь: метод валентных связей (МВС) и метод молекулярных орбиталей (ММО). Свойства ковалентной связи. Ионная связь и ее свойства. Металлическая связь. Понятие о зонном строении твердого тела. Водородная связь. Межмолекулярные взаимодействия (силы Ван-дер-Ваальса).
Химическая связь Природа и основные количественные характеристики химической связи. Ковалентная связь: метод валентных связей (МВС) и метод молекулярных орбиталей (ММО). Свойства ковалентной связи. Ионная связь и ее свойства. Металлическая связь. Понятие о зонном строении твердого тела. Водородная связь. Межмолекулярные взаимодействия (силы Ван-дер-Ваальса).
 Теории химической связи: метод валентных связей ( МВС ) метод молекулярных орбиталей ( ММО ) теория металлической связи теория кристаллического поля ( ТКП )
Теории химической связи: метод валентных связей ( МВС ) метод молекулярных орбиталей ( ММО ) теория металлической связи теория кристаллического поля ( ТКП )
 Классификация типов химической связи: Ковалентная (полярная и неполярная) Ионная Металлическая Водородная Межмолекулярные взаимодействия (силы Ван-дер-Ваальса)
Классификация типов химической связи: Ковалентная (полярная и неполярная) Ионная Металлическая Водородная Межмолекулярные взаимодействия (силы Ван-дер-Ваальса)
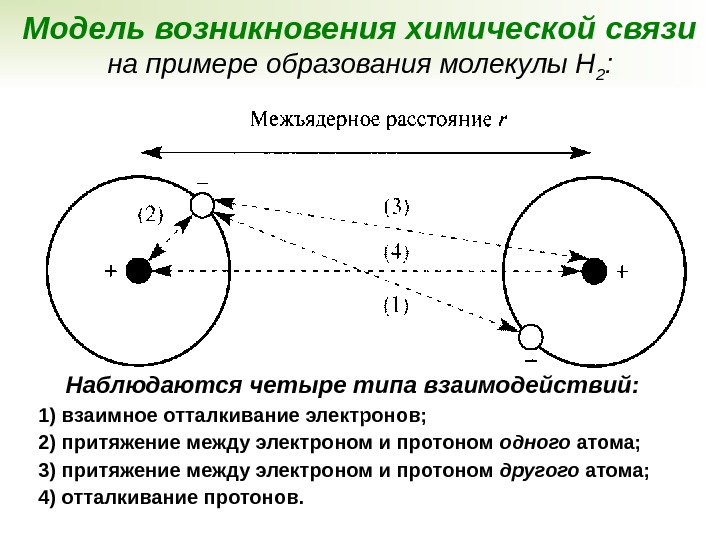
 Модель возникновения химической связи на примере образования молекулы Н 2 : Наблюдаются четыре типа взаимодействий: 1) взаимное отталкивание электронов; 2) притяжение между электроном и протоном одного атома; 3) притяжение между электроном и протоном другого атома; 4) отталкивание протонов.
Модель возникновения химической связи на примере образования молекулы Н 2 : Наблюдаются четыре типа взаимодействий: 1) взаимное отталкивание электронов; 2) притяжение между электроном и протоном одного атома; 3) притяжение между электроном и протоном другого атома; 4) отталкивание протонов.
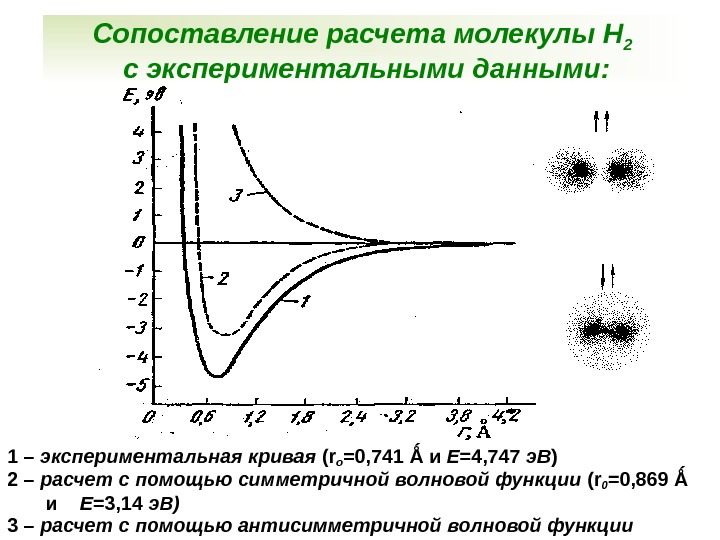
 Сопоставление расчета молекулы Н 2 с экспериментальными данными: 1 – экспериментальная кривая ( r о =0, 741 Ǻ и Е =4, 747 э. В ) 2 – расчет с помощью симметричной волновой функции ( r 0 =0, 869 Ǻ и Е =3, 14 э. В) 3 – расчет с помощью антисимметричной волновой функции
Сопоставление расчета молекулы Н 2 с экспериментальными данными: 1 – экспериментальная кривая ( r о =0, 741 Ǻ и Е =4, 747 э. В ) 2 – расчет с помощью симметричной волновой функции ( r 0 =0, 869 Ǻ и Е =3, 14 э. В) 3 – расчет с помощью антисимметричной волновой функции
 Основные количественные характеристики связи: Энергия связи ( Е ) Длина связи ( d) Валентные углы Кратность связи ( ρ ) Полярность связи
Основные количественные характеристики связи: Энергия связи ( Е ) Длина связи ( d) Валентные углы Кратность связи ( ρ ) Полярность связи
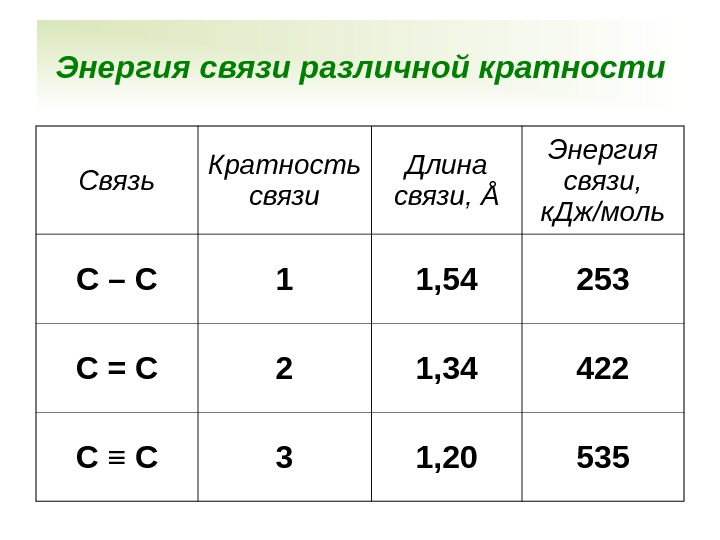
 Энергия связи различной кратности Связь Кратность связи Длина связи, Å Энергия связи, к. Дж/моль С – С 1 1, 54 253 С = С 2 1, 34 422 С ≡ С 3 1,
Энергия связи различной кратности Связь Кратность связи Длина связи, Å Энергия связи, к. Дж/моль С – С 1 1, 54 253 С = С 2 1, 34 422 С ≡ С 3 1,
 Основные положения метода валентных связей: В образовании связи участвуют электроны только внешней ( валентной ) оболочки При образовании молекул электронная структура (кроме внешней электронной оболочки) и химическая индивидуальность каждого атома в основном сохраняется Образование химической связи может происходить за счет спаривания электронов с антипараллельными спинами двух атомов ( обменный механизм ) или пары электронов одного атома и свободной орбитали другого атома ( донорно-акцепторный механизм )
Основные положения метода валентных связей: В образовании связи участвуют электроны только внешней ( валентной ) оболочки При образовании молекул электронная структура (кроме внешней электронной оболочки) и химическая индивидуальность каждого атома в основном сохраняется Образование химической связи может происходить за счет спаривания электронов с антипараллельными спинами двух атомов ( обменный механизм ) или пары электронов одного атома и свободной орбитали другого атома ( донорно-акцепторный механизм )
 • Основное условие образования ковалентной связи − перекрывание электронных облаков взаимодействующих атомов • Согласно МВС ковалентная связь − локализованная, двухцентровая, двухэлектронная связь
• Основное условие образования ковалентной связи − перекрывание электронных облаков взаимодействующих атомов • Согласно МВС ковалентная связь − локализованная, двухцентровая, двухэлектронная связь
 Свойства ковалентной связи: Насыщаемость Направленность
Свойства ковалентной связи: Насыщаемость Направленность
 Насыщаемость Частные определения валентности: ковалентность координационное число (кч) степень окисления
Насыщаемость Частные определения валентности: ковалентность координационное число (кч) степень окисления
 Связь между положением элемента в периодической системе и его максимальной ковалентностью № периода Строение валентного уровня Максимальн. ковалент-нос ть Примеры I 1 s – 1 АО 2 H-F…H-F II 2 s – 1 АО 2 p – 3 АО ∑ = 4 АО 4 NH 4 + , [Be(OH) 4 ] 2 — , [BF 4 ] — , CH 4 III 3 s – 1 АО 3 p – 3 АО 3 d – 5 АО ∑ = 9 АО 9 SF 6 (ковал-ть=6) , Cl. O 4 — (ковал-ть= 7 ), [PCl 6 ] — (ковал-ть=6)
Связь между положением элемента в периодической системе и его максимальной ковалентностью № периода Строение валентного уровня Максимальн. ковалент-нос ть Примеры I 1 s – 1 АО 2 H-F…H-F II 2 s – 1 АО 2 p – 3 АО ∑ = 4 АО 4 NH 4 + , [Be(OH) 4 ] 2 — , [BF 4 ] — , CH 4 III 3 s – 1 АО 3 p – 3 АО 3 d – 5 АО ∑ = 9 АО 9 SF 6 (ковал-ть=6) , Cl. O 4 — (ковал-ть= 7 ), [PCl 6 ] — (ковал-ть=6)
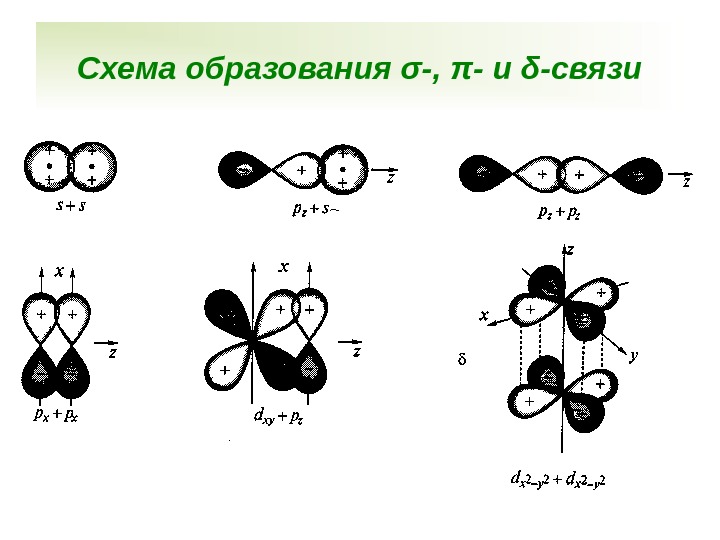
 Направленность Перекрывание АО происходит в направлении максимального перекрывания По способу перекрывания электронных облаков различают σ -, π -, δ -связи
Направленность Перекрывание АО происходит в направлении максимального перекрывания По способу перекрывания электронных облаков различают σ -, π -, δ -связи
 Схема образования σ-, π- и δ-связи
Схема образования σ-, π- и δ-связи
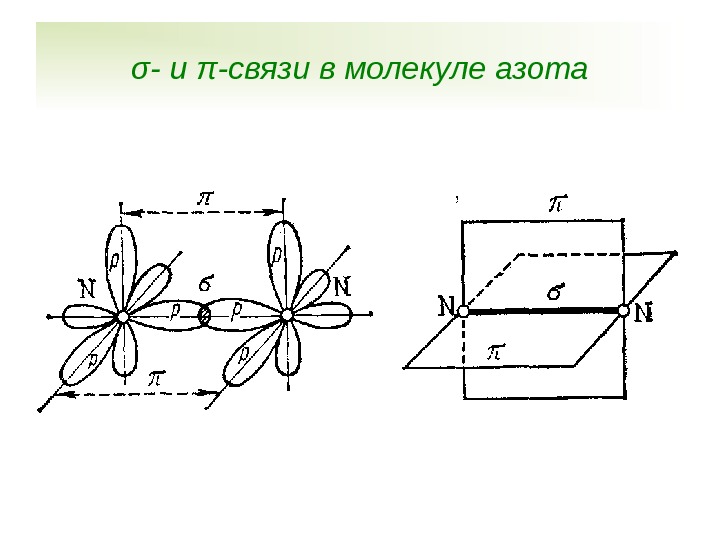
 σ- и π-связи в молекуле азота
σ- и π-связи в молекуле азота
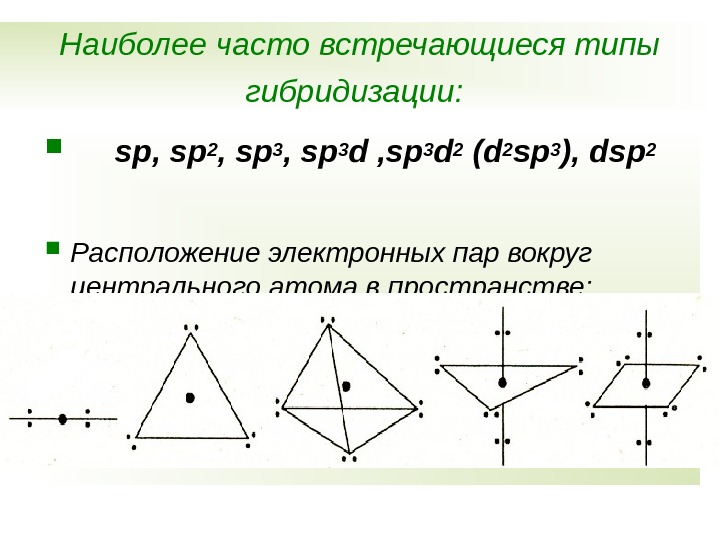
 Наиболее часто встречающиеся типы гибридизации: sp, sp 2 , sp 3 d 2 (d 2 sp 3 ), dsp 2 Расположение электронных пар вокруг центрального атома в пространстве:
Наиболее часто встречающиеся типы гибридизации: sp, sp 2 , sp 3 d 2 (d 2 sp 3 ), dsp 2 Расположение электронных пар вокруг центрального атома в пространстве:
 Схема определения типа гибридизации АО и пространственной структуры молекулы : Определить число σ-связей, образуемых центральным атомом в молекуле Определить число связывающих (поделённых) и несвязывающих (неподелённых) электронных пар (электроны, участвующие в образовании π -связей не учитывать) Определить тип гибридизации центрального атома, учитывая, что число гибридных АО равно числу поделённых и неподелённых электронных пар Определить расположение гибридных АО в пространстве и пространственную форму молекулы
Схема определения типа гибридизации АО и пространственной структуры молекулы : Определить число σ-связей, образуемых центральным атомом в молекуле Определить число связывающих (поделённых) и несвязывающих (неподелённых) электронных пар (электроны, участвующие в образовании π -связей не учитывать) Определить тип гибридизации центрального атома, учитывая, что число гибридных АО равно числу поделённых и неподелённых электронных пар Определить расположение гибридных АО в пространстве и пространственную форму молекулы
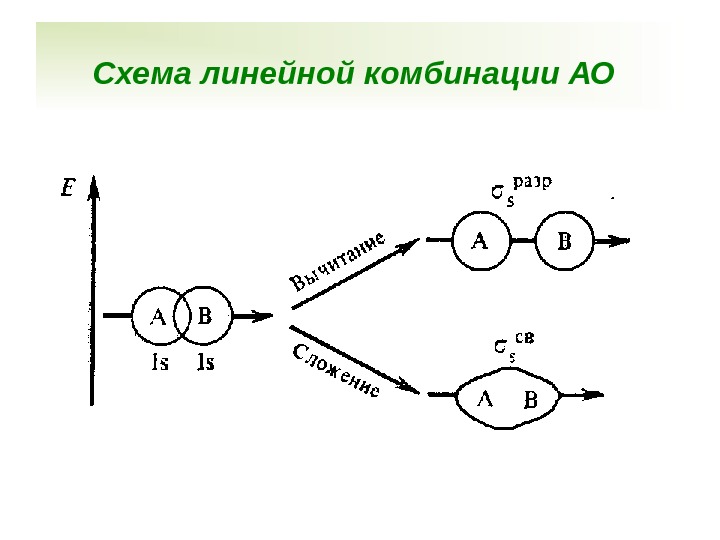
 Метод молекулярных орбиталей (ММО) Основные положения метода МО: Молекула – это единая система ядер и электронов Каждому электрону в молекуле соответствует молекулярная орбиталь (МО) МО представляет собой линейную комбинацию (сложение и вычитание) атомных орбиталей − метод МО ЛКАО При линейной комбинации из N АО образуются N МО.
Метод молекулярных орбиталей (ММО) Основные положения метода МО: Молекула – это единая система ядер и электронов Каждому электрону в молекуле соответствует молекулярная орбиталь (МО) МО представляет собой линейную комбинацию (сложение и вычитание) атомных орбиталей − метод МО ЛКАО При линейной комбинации из N АО образуются N МО.
 Схема линейной комбинации АО
Схема линейной комбинации АО
 Характеристики молекул, образованных атомами элементов I периода ПСЭ Молекулярная ρ Есвязи , к. Дж/моль частица Н 2 + 0, 5 256 Н 2 1 432 Не 2 + 0, 5 250 • ионы Н 2+ и Не 2+ — парамагнитны • молекула Н 2 – диамагнитна
Характеристики молекул, образованных атомами элементов I периода ПСЭ Молекулярная ρ Есвязи , к. Дж/моль частица Н 2 + 0, 5 256 Н 2 1 432 Не 2 + 0, 5 250 • ионы Н 2+ и Не 2+ — парамагнитны • молекула Н 2 – диамагнитна
 Характеристики молекул, образованных атомами элементов II периода ПСЭ Молекула ρ Длина связи, Å Есвязи , к. Дж/моль O 2 2 1, 21 498 N 2 3 1, 1 945 Молекула O 2 – парамагнитна , N 2 – диамагнитна
Характеристики молекул, образованных атомами элементов II периода ПСЭ Молекула ρ Длина связи, Å Есвязи , к. Дж/моль O 2 2 1, 21 498 N 2 3 1, 1 945 Молекула O 2 – парамагнитна , N 2 – диамагнитна
 Сравнение МВС и ММО Оба метода − приближенные и взаимно дополняют друга. ММО позволяет описывать и прогнозировать свойства молекулы, зависящие от состояния в ней отдельных электронов (устойчивость, магнитные свойства). Но ММО не способен передавать насыщаемость ковалентной связи (т. е. состав молекулы), не позволяет объяснить пространственную форму молекул. С помощью метода ВС можно определить геометрические свойства молекулы и её важнейшие параметры (длину связи, валентные углы). Более общим и последовательным методом описания строения молекулы является ММО
Сравнение МВС и ММО Оба метода − приближенные и взаимно дополняют друга. ММО позволяет описывать и прогнозировать свойства молекулы, зависящие от состояния в ней отдельных электронов (устойчивость, магнитные свойства). Но ММО не способен передавать насыщаемость ковалентной связи (т. е. состав молекулы), не позволяет объяснить пространственную форму молекул. С помощью метода ВС можно определить геометрические свойства молекулы и её важнейшие параметры (длину связи, валентные углы). Более общим и последовательным методом описания строения молекулы является ММО

