L_7-8_HS-1.ppt
- Количество слайдов: 92
 ХИМИЧЕСКАЯ СВЯЗЬ
ХИМИЧЕСКАЯ СВЯЗЬ
 Графические формулы • Показывают порядок связи между атомами в молекуле • В бескислородных соединениях атомы элементов чаще всего связаны непосредственно между собой
Графические формулы • Показывают порядок связи между атомами в молекуле • В бескислородных соединениях атомы элементов чаще всего связаны непосредственно между собой
 Например HCl H 2 S H H Cl S H Каждая черточка соответствует единице валентности
Например HCl H 2 S H H Cl S H Каждая черточка соответствует единице валентности
 продолжение • В кислородосодержащих веществах атомы элементов чаще всего соединяются между собой через кислород.
продолжение • В кислородосодержащих веществах атомы элементов чаще всего соединяются между собой через кислород.
 Например Na. OH Na O H
Например Na. OH Na O H
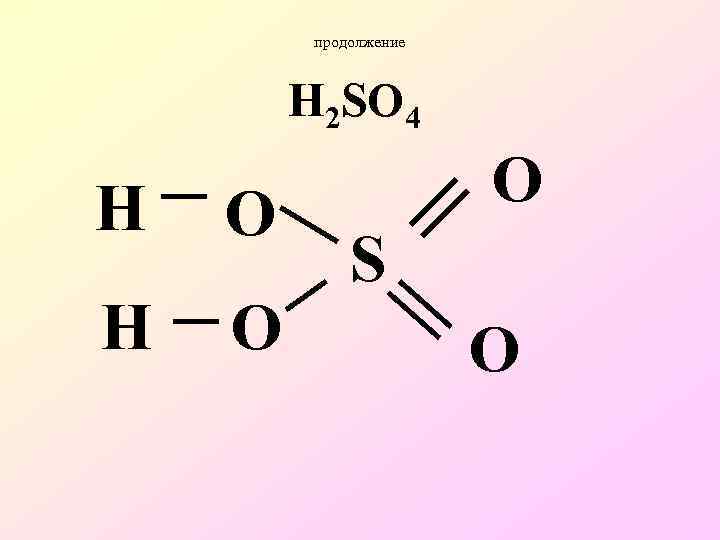 продолжение H 2 SO 4 H O O S O
продолжение H 2 SO 4 H O O S O
 Введение Фундаментальная основа теории химической связи – теория химического строения Александра Михайловича Бутлерова (1861 г). 1828 -1886 Свойства соединений зависят от природы и числа составляющих их частиц и химического строения. Эта теория нашла подтверждение не только для органических, но и для неорганических веществ.
Введение Фундаментальная основа теории химической связи – теория химического строения Александра Михайловича Бутлерова (1861 г). 1828 -1886 Свойства соединений зависят от природы и числа составляющих их частиц и химического строения. Эта теория нашла подтверждение не только для органических, но и для неорганических веществ.
 Определение и характеристики химической связи Химическая связь – это сила, удерживающая вместе два или несколько атомов, ионов, молекул.
Определение и характеристики химической связи Химическая связь – это сила, удерживающая вместе два или несколько атомов, ионов, молекул.
 Природа химической связи – электростатическое взаимодействие между отрицательно заряженными электронами и положительно заряженными ядрами, а также электронов друг с другом.
Природа химической связи – электростатическое взаимодействие между отрицательно заряженными электронами и положительно заряженными ядрами, а также электронов друг с другом.
 Валентность – способность атома образовывать химические связи. Валентные электроны – электроны, принимающие участие в образовании химической связи
Валентность – способность атома образовывать химические связи. Валентные электроны – электроны, принимающие участие в образовании химической связи
 Валентные электроны располагаются на самых высоких по энергии орбиталях атома. Внешняя оболочка атома, содержащая эти орбитали называется валентной оболочкой.
Валентные электроны располагаются на самых высоких по энергии орбиталях атома. Внешняя оболочка атома, содержащая эти орбитали называется валентной оболочкой.
 Основные виды химической связи По механизму образования химической связи и по разности электроотрицательностей между атомами, образующими молекулу : ионная, ковалентная полярная, ковалентная неполярная
Основные виды химической связи По механизму образования химической связи и по разности электроотрицательностей между атомами, образующими молекулу : ионная, ковалентная полярная, ковалентная неполярная
 Ионная связь • ОЭО 2
Ионная связь • ОЭО 2
 Ковалентная связь • Ковалентная полярная (КП) - 0 ОЭО 2 • Ковалентная неполярная (КНП) - ОЭО = 0
Ковалентная связь • Ковалентная полярная (КП) - 0 ОЭО 2 • Ковалентная неполярная (КНП) - ОЭО = 0
 Металлическая связь – связь в металлах Химическая связь между молекулами Водородная Вандерваальсовы взаимодействия
Металлическая связь – связь в металлах Химическая связь между молекулами Водородная Вандерваальсовы взаимодействия
 Характеристики химической связи Энергия связи – энергия, выделяющаяся при образовании связи. Обозначение - Есв. Размерность к. Дж/моль.
Характеристики химической связи Энергия связи – энергия, выделяющаяся при образовании связи. Обозначение - Есв. Размерность к. Дж/моль.
 Длина связи – расстояние между ядрами в соединении. Зависит от размеров электронной оболочки и степени их перекрывания. Обозначение – lсв. Размерность нм
Длина связи – расстояние между ядрами в соединении. Зависит от размеров электронной оболочки и степени их перекрывания. Обозначение – lсв. Размерность нм
 Направленность – перекрывание электронных облаков происходит только в определенном направлении, определяемом расположением орбиталей в пространстве.
Направленность – перекрывание электронных облаков происходит только в определенном направлении, определяемом расположением орбиталей в пространстве.
 Насыщаемость – ограничение количества образуемых связей
Насыщаемость – ограничение количества образуемых связей
 Энергии (Есв) и длины (lсв) некоторых химических связей связь H–F H – Cl H – Br H–I Есв к. Дж/моль 536 432 360 299 lсв нм 0, 092 0, 128 0, 142 0, 162
Энергии (Есв) и длины (lсв) некоторых химических связей связь H–F H – Cl H – Br H–I Есв к. Дж/моль 536 432 360 299 lсв нм 0, 092 0, 128 0, 142 0, 162
 Вывод с увеличением длины связи уменьшается энергия связи и соответственно устойчивость молекул
Вывод с увеличением длины связи уменьшается энергия связи и соответственно устойчивость молекул
 Строение атома и химическая связь По строению атома все элементы можно разделить на 2 группы:
Строение атома и химическая связь По строению атома все элементы можно разделить на 2 группы:
 1. Атомы с завершенным внешним квантовым слоем – инертные газы (Не – дублет электронов, остальные – октет электронов) ИНЕРТНЫ.
1. Атомы с завершенным внешним квантовым слоем – инертные газы (Не – дублет электронов, остальные – октет электронов) ИНЕРТНЫ.
 2. Атомы с незавершенным внешним квантовым слоем - все остальные АКТИВНЫ.
2. Атомы с незавершенным внешним квантовым слоем - все остальные АКТИВНЫ.
 продолжение Любой атом элемента стремится приобрести устойчивую восьмиэлектронную или двухэлектронную конфигурацию
продолжение Любой атом элемента стремится приобрести устойчивую восьмиэлектронную или двухэлектронную конфигурацию
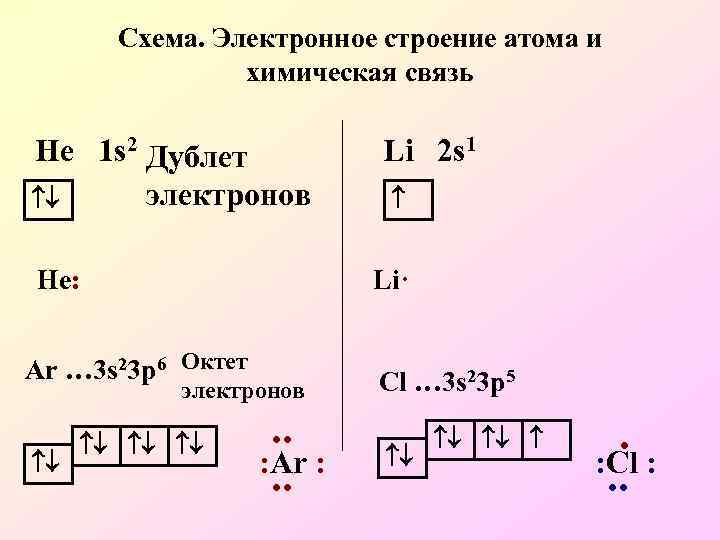 Схема. Электронное строение атома и химическая связь He 1 s 2 Дублет электронов Не: Li· Ar … 3 s 23 p 6 Октет электронов Li 2 s 1 . . : Ar : . . Cl … 3 s 23 p 5 . : Cl : . .
Схема. Электронное строение атома и химическая связь He 1 s 2 Дублет электронов Не: Li· Ar … 3 s 23 p 6 Октет электронов Li 2 s 1 . . : Ar : . . Cl … 3 s 23 p 5 . : Cl : . .
 Теория Льюиса-Косселя 1916 г немецкий ученый Коссель: Атомы при взаимодействии либо отдают, либо принимают электроны. При этом они превращаются либо в катионы, либо в анионы, имеющие устойчивые электронные конфигурации. Взаимное притяжение ионов обусловливает химическую связь. Идеи Косселя легли в основу теории ионной связи.
Теория Льюиса-Косселя 1916 г немецкий ученый Коссель: Атомы при взаимодействии либо отдают, либо принимают электроны. При этом они превращаются либо в катионы, либо в анионы, имеющие устойчивые электронные конфигурации. Взаимное притяжение ионов обусловливает химическую связь. Идеи Косселя легли в основу теории ионной связи.
 Льюис 1916 год американский ученый Г. Льюис: Устойчивые внешние электронные конфигурации у молекул могут возникать в результате обобществления электронов. Связь, образованная за счет общей электронной пары электронов, поставляемых по одному от каждого атома получила название ковалентной.
Льюис 1916 год американский ученый Г. Льюис: Устойчивые внешние электронные конфигурации у молекул могут возникать в результате обобществления электронов. Связь, образованная за счет общей электронной пары электронов, поставляемых по одному от каждого атома получила название ковалентной.
 Правило октета В результате образования химической связи атомы приобретают структуру благородного газа, которые (за исключением гелия) имеют во внешней электронной оболочке октет (восемь электронов). Это правило справедливо, как для инной, так и для ковалентной связи.
Правило октета В результате образования химической связи атомы приобретают структуру благородного газа, которые (за исключением гелия) имеют во внешней электронной оболочке октет (восемь электронов). Это правило справедливо, как для инной, так и для ковалентной связи.
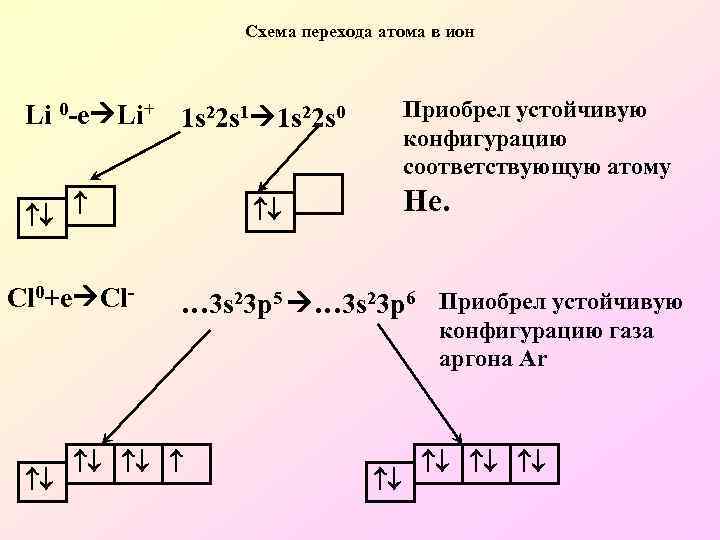 Схема перехода атома в ион Li 0 -e Li+ 1 s 22 s 1 1 s 22 s 0 Приобрел устойчивую конфигурацию соответствующую атому Не. Cl 0+e Cl- … 3 s 23 p 5 … 3 s 23 p 6 Приобрел устойчивую конфигурацию газа аргона Ar
Схема перехода атома в ион Li 0 -e Li+ 1 s 22 s 1 1 s 22 s 0 Приобрел устойчивую конфигурацию соответствующую атому Не. Cl 0+e Cl- … 3 s 23 p 5 … 3 s 23 p 6 Приобрел устойчивую конфигурацию газа аргона Ar
 Образование ионной связи Ионная химическая связь – электростатическое взаимодействие отрицательно и положительно заряженных ионов в химическом соединении.
Образование ионной связи Ионная химическая связь – электростатическое взаимодействие отрицательно и положительно заряженных ионов в химическом соединении.
 Мерой ионности связи • в соединении служит разность между ОЭО атомов элементов, образующих данное соединение.
Мерой ионности связи • в соединении служит разность между ОЭО атомов элементов, образующих данное соединение.
 Например катионы металлов IA и IIА групп и анионами неметаллов VIA VIIA групп периодической системы (Li. F, Cs. Cl, K 2 O и др. ).
Например катионы металлов IA и IIА групп и анионами неметаллов VIA VIIA групп периодической системы (Li. F, Cs. Cl, K 2 O и др. ).
 продолжение Однако чисто ионной связи не существует, т. к. не происходит полного перехода электрона от одного атома к другому. Поэтому чаще говорят о степени или доле ионности.
продолжение Однако чисто ионной связи не существует, т. к. не происходит полного перехода электрона от одного атома к другому. Поэтому чаще говорят о степени или доле ионности.
![Схема образования ионной связи Na • e. . +[: Cl: ]Na . . • Схема образования ионной связи Na • e. . +[: Cl: ]Na . . •](https://present5.com/presentation/90992014_142242829/image-35.jpg) Схема образования ионной связи Na • e. . +[: Cl: ]Na . . • Cl : . . Образуется ионная решетка
Схема образования ионной связи Na • e. . +[: Cl: ]Na . . • Cl : . . Образуется ионная решетка
 продолжение
продолжение
 Как видно из предыдущего рисунка электрическое поле иона имеет сферический характер. Такие заряды могут притягивать к себе неограниченное число зарядов (ионов) противоположного знака. Следовательно для ионной связи не характерна направленность и насыщаемость.
Как видно из предыдущего рисунка электрическое поле иона имеет сферический характер. Такие заряды могут притягивать к себе неограниченное число зарядов (ионов) противоположного знака. Следовательно для ионной связи не характерна направленность и насыщаемость.
 Ковалентная связь Химическая связь, осуществляемая электронными парами, называется ковалентной.
Ковалентная связь Химическая связь, осуществляемая электронными парами, называется ковалентной.
 Метод валентных связей. 1. Ковалентная связь образуется двумя электронами, обладающими противоположно направленными спинами и принадлежащими двум атомам, между которыми осуществляется связь.
Метод валентных связей. 1. Ковалентная связь образуется двумя электронами, обладающими противоположно направленными спинами и принадлежащими двум атомам, между которыми осуществляется связь.
 Два механизма образования ковалентной связи – обычный(обменный) и донорноакцепторный.
Два механизма образования ковалентной связи – обычный(обменный) и донорноакцепторный.
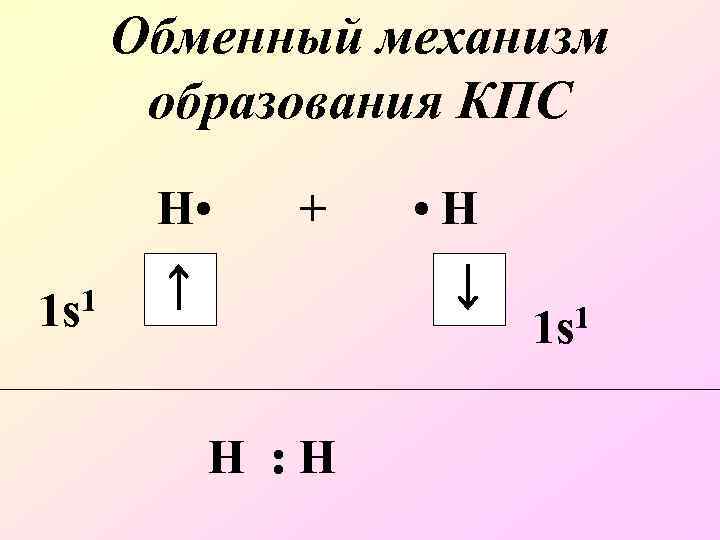 Обменный механизм образования КПС Н • + 1 1 s • Н 1 s 1 Н : Н
Обменный механизм образования КПС Н • + 1 1 s • Н 1 s 1 Н : Н
 Образование ковалентной связи
Образование ковалентной связи
 Пояснения к графику Рассмотрим образование ковалентной связи в молекуле водорода. Между ядром атома водорода одного атома и электронами другого действуют кулоновские силы притяжения (рис. а). В результате атомы водорода сближаются и происходит перекрывание электронных облаков (б). Электронная плотность между ядрами возрастает. В результате ядра сближаются, энергия системы снижается (в). Однако при очень сильном сближении атомов ядра начинают отталкиваться (г). Поэтому существует оптимальное расстояние между ядрами (lсв. ) при котором система имеет минимальную энергию (минимум на кривой). При таком состоянии выделяется энергия(Есв)
Пояснения к графику Рассмотрим образование ковалентной связи в молекуле водорода. Между ядром атома водорода одного атома и электронами другого действуют кулоновские силы притяжения (рис. а). В результате атомы водорода сближаются и происходит перекрывание электронных облаков (б). Электронная плотность между ядрами возрастает. В результате ядра сближаются, энергия системы снижается (в). Однако при очень сильном сближении атомов ядра начинают отталкиваться (г). Поэтому существует оптимальное расстояние между ядрами (lсв. ) при котором система имеет минимальную энергию (минимум на кривой). При таком состоянии выделяется энергия(Есв)
 Характеристики связи Н – Н • lсв=0, 74 нм; • Есв=436 к. Дж/моль
Характеристики связи Н – Н • lсв=0, 74 нм; • Есв=436 к. Дж/моль
 Донорно-акцепторный механизм образования КС N 22 p 3 … 2 s H 1 … 1 s -e H … 1 s 0
Донорно-акцепторный механизм образования КС N 22 p 3 … 2 s H 1 … 1 s -e H … 1 s 0
![продолжение H | H― N: + | H [ H | ] ― H+ продолжение H | H― N: + | H [ H | ] ― H+](https://present5.com/presentation/90992014_142242829/image-46.jpg) продолжение H | H― N: + | H [ H | ] ― H+ H N : H | H +
продолжение H | H― N: + | H [ H | ] ― H+ H N : H | H +
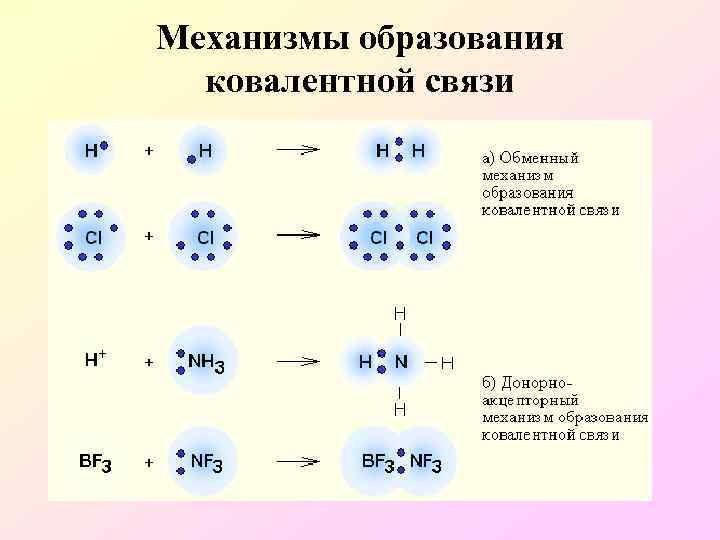 Механизмы образования ковалентной связи
Механизмы образования ковалентной связи
 2. Ковалентная связь тем прочнее, чем в большей степени перекрываются взаимодействующие электронные облака. Ковалентная связь образуется в направлении при котором перекрывание электронных облаков атомов максимально.
2. Ковалентная связь тем прочнее, чем в большей степени перекрываются взаимодействующие электронные облака. Ковалентная связь образуется в направлении при котором перекрывание электронных облаков атомов максимально.
 Свойства ковалентной связи Насыщаемость – вызвана ограничением числа электронов, находящихся на внешних электронных оболочках, которые участвуют в образовании связи.
Свойства ковалентной связи Насыщаемость – вызвана ограничением числа электронов, находящихся на внешних электронных оболочках, которые участвуют в образовании связи.
 продолжение • Т. е. количество связей, которое может образовать атом элемента ограничено числом неспаренных электронов в валентном слое. • Обычно число валентных электронов равно номеру группы. • Исключения: кислород (В=2), фтор (В=1)
продолжение • Т. е. количество связей, которое может образовать атом элемента ограничено числом неспаренных электронов в валентном слое. • Обычно число валентных электронов равно номеру группы. • Исключения: кислород (В=2), фтор (В=1)
 Направленность ковалентной связи Направленность. Атомные орбитали пространственно ориентированы. Следовательно перекрывание электронных облаков происходит по определенным направлениям.
Направленность ковалентной связи Направленность. Атомные орбитали пространственно ориентированы. Следовательно перекрывание электронных облаков происходит по определенным направлениям.
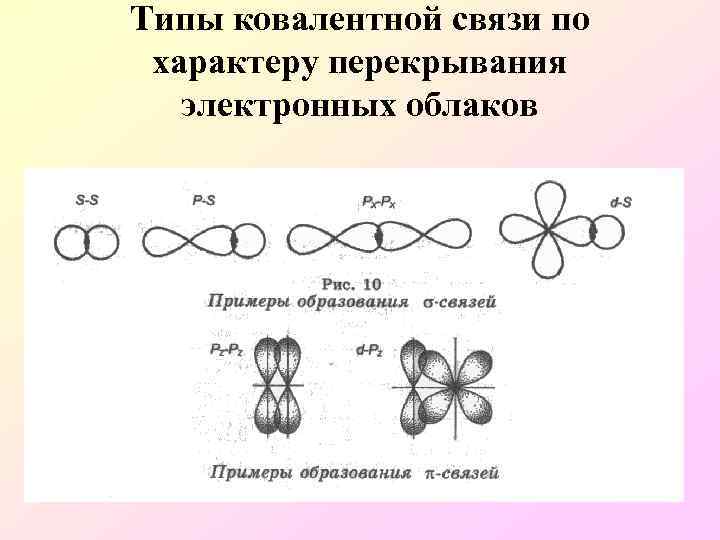 Типы ковалентной связи по характеру перекрывания электронных облаков
Типы ковалентной связи по характеру перекрывания электронных облаков
 Сигма и пи-связи - связь – однократное перекрывание облаков по линии соединяющей центры атомов Сигма связи присутствуют во всех молекулах.
Сигма и пи-связи - связь – однократное перекрывание облаков по линии соединяющей центры атомов Сигма связи присутствуют во всех молекулах.
 продолжение • π - связь – двукратное перекрывание электронных облаков по обе стороны от линии соединяющей центры атомов.
продолжение • π - связь – двукратное перекрывание электронных облаков по обе стороны от линии соединяющей центры атомов.
 продолжение • π связи присутствуют в молекулах, имеющих двойные (молекула кислорода, этилена и др. ) и тройные связи (молекула азота, СО и др. ). Если в молекуле вещества несколько связей, то одна из них сигма, остальные пи.
продолжение • π связи присутствуют в молекулах, имеющих двойные (молекула кислорода, этилена и др. ) и тройные связи (молекула азота, СО и др. ). Если в молекуле вещества несколько связей, то одна из них сигма, остальные пи.
 • Длина одинарной связи>двойной>тройной • Прочность одинарной связи <двойной<тройной
• Длина одинарной связи>двойной>тройной • Прочность одинарной связи <двойной<тройной
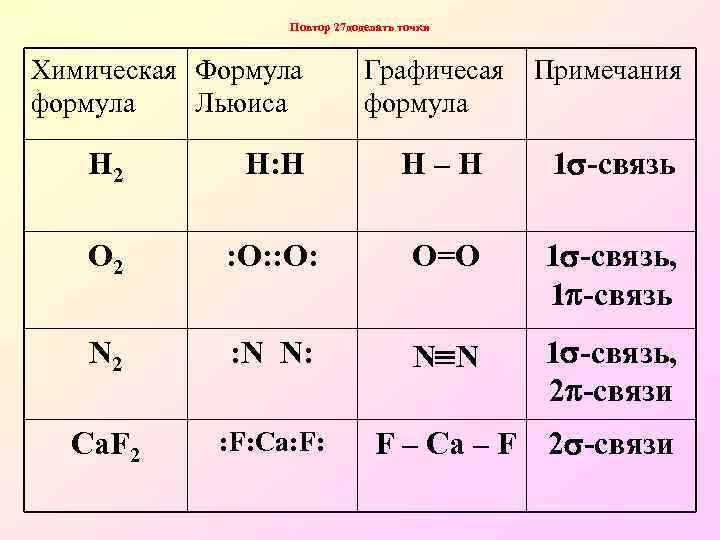 Повтор 27 доделать точки Химическая Формула формула Льюиса Графичесая формула Примечания Н 2 Н: Н Н–Н 1 -связь О 2 : О: О=О 1 -связь, 1 -связь N 2 : N N: N N 1 -связь, 2 -связи Ca. F 2 : F: Са: F: F – Ca – F 2 -связи
Повтор 27 доделать точки Химическая Формула формула Льюиса Графичесая формула Примечания Н 2 Н: Н Н–Н 1 -связь О 2 : О: О=О 1 -связь, 1 -связь N 2 : N N: N N 1 -связь, 2 -связи Ca. F 2 : F: Са: F: F – Ca – F 2 -связи
 Металлическая связь • Металлическая связь – это взаимодействие, удерживающее атомы металлов в кристаллической решетке. • В образовании металлической связи участвуют валентные электроны металла, принадлежащие всему объему металла.
Металлическая связь • Металлическая связь – это взаимодействие, удерживающее атомы металлов в кристаллической решетке. • В образовании металлической связи участвуют валентные электроны металла, принадлежащие всему объему металла.
 продолжение • В металле электроны отрываются от атома и перемещаются по всей массе металла. • При этом атомы металла превращаются в «+» -заряженные ионы, которые снова притягивают к себе электроны. • Одновременно другие атомы металла отдают свои электроны.
продолжение • В металле электроны отрываются от атома и перемещаются по всей массе металла. • При этом атомы металла превращаются в «+» -заряженные ионы, которые снова притягивают к себе электроны. • Одновременно другие атомы металла отдают свои электроны.
 продолжение • Т. о, внутри металла постоянно циркулирует «электронный газ» , который прочно связывает между собой все атомы металла. В металлической связи отсутствует направленность. • Отсюда свойства характерные для металлов: электропроводность, пластичность, ковкость, теплопроводность и т. д.
продолжение • Т. о, внутри металла постоянно циркулирует «электронный газ» , который прочно связывает между собой все атомы металла. В металлической связи отсутствует направленность. • Отсюда свойства характерные для металлов: электропроводность, пластичность, ковкость, теплопроводность и т. д.
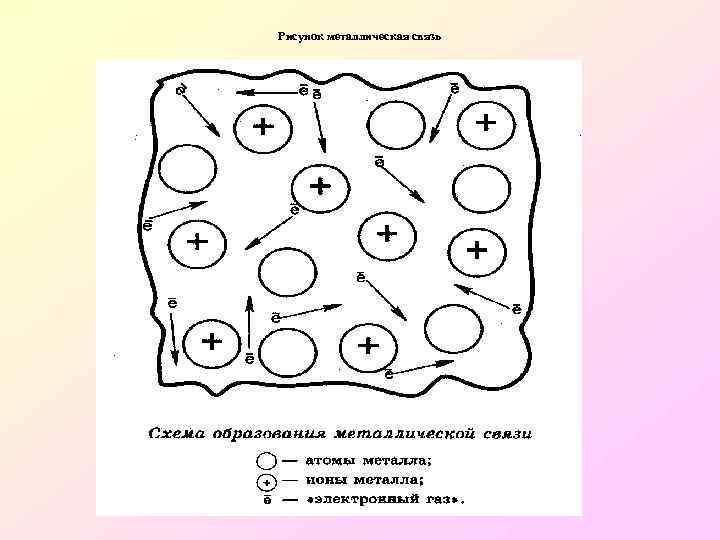 Рисунок металлическая связь
Рисунок металлическая связь
 Примеры. Определите тип химической связи между атомами в молекулах веществ: гидроксида натрия, серной кислоты, гидроксида мышьяка, сульфата натрия. Покажите стрелкой к какому элементу смещена электронная пара Какая связь более полярна? Каковы степени окисления атомов элементов?
Примеры. Определите тип химической связи между атомами в молекулах веществ: гидроксида натрия, серной кислоты, гидроксида мышьяка, сульфата натрия. Покажите стрелкой к какому элементу смещена электронная пара Какая связь более полярна? Каковы степени окисления атомов элементов?
 Алгоритм выполнения 1. Изобразить графическую формулу. 2. 2. Под каждым элементом проставить значение электроотрицательности из таблицы. 3. 3. Стрелкой показать смещение электронной плотности. 4. 4. Рассчитать разность относительных электроотрицательностей и указать тип связи (ионная, КП, КНП) 5. 5. По направлению и количеству смещений электронной плотности определить степени окисления атомов элементов.
Алгоритм выполнения 1. Изобразить графическую формулу. 2. 2. Под каждым элементом проставить значение электроотрицательности из таблицы. 3. 3. Стрелкой показать смещение электронной плотности. 4. 4. Рассчитать разность относительных электроотрицательностей и указать тип связи (ионная, КП, КНП) 5. 5. По направлению и количеству смещений электронной плотности определить степени окисления атомов элементов.
 Пример выполнения Na. OH + -2 + Na O H 0, 93 3, 5 2, 1 ОЭО(O-Na)= 3, 5 – 0, 93=2, 63 ионная ОЭО(О-Н)= 3, 5 -2, 1=1, 4 КП
Пример выполнения Na. OH + -2 + Na O H 0, 93 3, 5 2, 1 ОЭО(O-Na)= 3, 5 – 0, 93=2, 63 ионная ОЭО(О-Н)= 3, 5 -2, 1=1, 4 КП
 Полярность молекул. Дипольный момент. При образовании ковалентной связи общее электронное облако смещается к атому более электроотрицательного элемента.
Полярность молекул. Дипольный момент. При образовании ковалентной связи общее электронное облако смещается к атому более электроотрицательного элемента.
 продолжение • В результате более электроотрицательный атом элемента приобретает избыточный отрицательный заряд, другой атом элемента приобретает такой же по абсолютной величине избыточный положительный заряд.
продолжение • В результате более электроотрицательный атом элемента приобретает избыточный отрицательный заряд, другой атом элемента приобретает такой же по абсолютной величине избыточный положительный заряд.
 Система из 2 -х равных по абсолютной величине и противоположных по знаку зарядов, расположенных на определенном расстоянии друг от друга называется диполем.
Система из 2 -х равных по абсолютной величине и противоположных по знаку зарядов, расположенных на определенном расстоянии друг от друга называется диполем.
 Дипольный момент АВ А+ В- Диполь создает вокруг себя электрическое поле определенной напряженности. Напряженность поля оценивается величиной дипольного момента. + - l = q l q– заряд электрона q = (1, 60*10 -19 Кл) l – длина диполя
Дипольный момент АВ А+ В- Диполь создает вокруг себя электрическое поле определенной напряженности. Напряженность поля оценивается величиной дипольного момента. + - l = q l q– заряд электрона q = (1, 60*10 -19 Кл) l – длина диполя
 Усл об непол и пол мол Полярность молекулы зависит от величины дипольного момента. l=0, молекула неполярна l 0 0, молекула полярна + -
Усл об непол и пол мол Полярность молекулы зависит от величины дипольного момента. l=0, молекула неполярна l 0 0, молекула полярна + -
 Форма некоторых мол Дипольный момент величина векторная. Направление вектора от положительного конца диполя к отрицательному. След. дипольный момент многоатомной молекулы можно рассматривать как геометрическую сумму векторов.
Форма некоторых мол Дипольный момент величина векторная. Направление вектора от положительного конца диполя к отрицательному. След. дипольный момент многоатомной молекулы можно рассматривать как геометрическую сумму векторов.
 Двухатомная молекула АВ. • Полярность связи и полярность молекулы совпадают. 1) А В (АВ)= (св) 0 ; 2) А – А =0
Двухатомная молекула АВ. • Полярность связи и полярность молекулы совпадают. 1) А В (АВ)= (св) 0 ; 2) А – А =0
 Трехатомная молекула АВ 2 В А В =0, неполярная, линейная
Трехатомная молекула АВ 2 В А В =0, неполярная, линейная
 0, полярная, угловая А В В
0, полярная, угловая А В В
 Гибридизация Для объяснения геометрической формы молекул (направленности ковалентной связи) используют представление о гибридизации атомных орбиталей.
Гибридизация Для объяснения геометрической формы молекул (направленности ковалентной связи) используют представление о гибридизации атомных орбиталей.
 Идею о гибридизации атомных орбиталей выдвинул американский ученый Лайнус Карл Полинг 1901 -
Идею о гибридизации атомных орбиталей выдвинул американский ученый Лайнус Карл Полинг 1901 -
 Суть гибридизации Смешение разных (s-, p-, d-) атомных орбиталей центрального атома. При этом орбитали должны иметь близкие значения энергии. Результат гибридизации – образование одинаковых по плотности, объему, энергии гибридных орбиталей.
Суть гибридизации Смешение разных (s-, p-, d-) атомных орбиталей центрального атома. При этом орбитали должны иметь близкие значения энергии. Результат гибридизации – образование одинаковых по плотности, объему, энергии гибридных орбиталей.
 продолжение • Количество исходных атомных и образовавшихся гибридных орбиталей одинаково. В гибридной орбитали электронная плотность смещена в сторону от ядра, что позволяет добиться большего перекрывания с атомной орбиталью другого атома.
продолжение • Количество исходных атомных и образовавшихся гибридных орбиталей одинаково. В гибридной орбитали электронная плотность смещена в сторону от ядра, что позволяет добиться большего перекрывания с атомной орбиталью другого атома.

 Число ГАО В формировании структуры молекулы участвуют орбитали, содержащие валентные электроны, образующие только сигма связи и орбитали, содержащие электронные пары. ГАО = число сигма связей+число электронных пар
Число ГАО В формировании структуры молекулы участвуют орбитали, содержащие валентные электроны, образующие только сигма связи и орбитали, содержащие электронные пары. ГАО = число сигма связей+число электронных пар
 Алгоритм определения типа гибридизации. 1. Изобразить графическую формулу. 2. 2. Определить валентность центрального атома. 3. 3. Распределить электроны по орбиталям для соответствующего валентного состоянии центрального атома.
Алгоритм определения типа гибридизации. 1. Изобразить графическую формулу. 2. 2. Определить валентность центрального атома. 3. 3. Распределить электроны по орбиталям для соответствующего валентного состоянии центрального атома.
 продолжение 4. В графической формуле молекулы обозначить сигма связи и электронные пары 5. Определить какие и сколько орбиталей участвуют в формировании структуры молекулы. Указать тип гибридизации и полярность молекулы.
продолжение 4. В графической формуле молекулы обозначить сигма связи и электронные пары 5. Определить какие и сколько орбиталей участвуют в формировании структуры молекулы. Указать тип гибридизации и полярность молекулы.
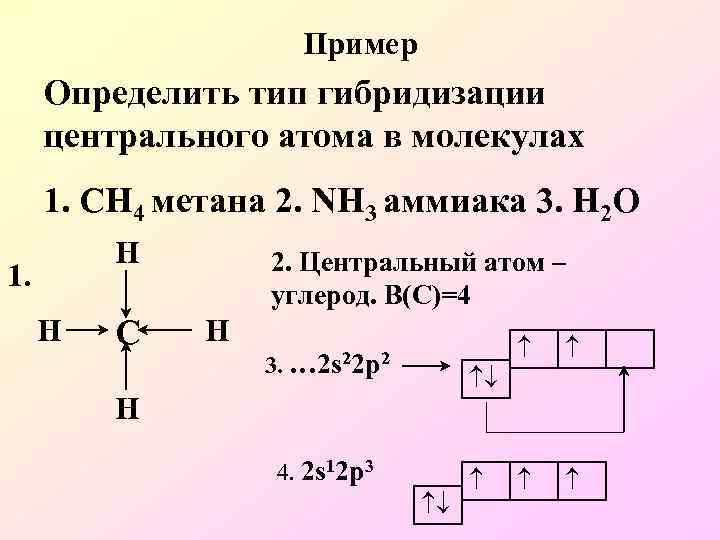 Пример Определить тип гибридизации центрального атома в молекулах 1. СН 4 метана 2. NH 3 аммиака 3. Н 2 О Н 1. Н С 2. Центральный атом – углерод. В(С)=4 Н 3. … 2 s 22 p 2 Н 4. 2 s 12 p 3
Пример Определить тип гибридизации центрального атома в молекулах 1. СН 4 метана 2. NH 3 аммиака 3. Н 2 О Н 1. Н С 2. Центральный атом – углерод. В(С)=4 Н 3. … 2 s 22 p 2 Н 4. 2 s 12 p 3
 5. В формировании структуры молекулы участвуют одна s и три p- электронные орбитали. Все связи в молекуле метана одинарные -связи. Тип гибридизации sp 3. Все электронные облака участвующие в гибридизации одинаковы. Следовательно углы между ними одинаковы и =0. Молекула неполярна. Геометрическая форма тетраэдр. Ответ sp 3 -гибридизация =0, неполярная молекула
5. В формировании структуры молекулы участвуют одна s и три p- электронные орбитали. Все связи в молекуле метана одинарные -связи. Тип гибридизации sp 3. Все электронные облака участвующие в гибридизации одинаковы. Следовательно углы между ними одинаковы и =0. Молекула неполярна. Геометрическая форма тетраэдр. Ответ sp 3 -гибридизация =0, неполярная молекула
 Молекула аммиака Рассуждая аналогично для молекулы аммиака: 1 H H N: H 2. B(N)=3, … 2 s 22 p 3 3. 4. 3 -связи+электронная пара. 5. SР 3 - гибридизация. Электронные облака разного характера. Углы между ними неодинаковы. 0. Молекула полярна.
Молекула аммиака Рассуждая аналогично для молекулы аммиака: 1 H H N: H 2. B(N)=3, … 2 s 22 p 3 3. 4. 3 -связи+электронная пара. 5. SР 3 - гибридизация. Электронные облака разного характера. Углы между ними неодинаковы. 0. Молекула полярна.
 Молекула воды 1. : O: H H 2. Кислород В=2. 3. 2 s 22 p 4 4. В молекуле 2 -связи и две электроные пары. В формировании структуры молекулы участвуют s- и три p-электронные орбитали. Тип гибридизации sp 3. 0 (т. к. Углы между электронными облаками различны). Молекула полярна.
Молекула воды 1. : O: H H 2. Кислород В=2. 3. 2 s 22 p 4 4. В молекуле 2 -связи и две электроные пары. В формировании структуры молекулы участвуют s- и три p-электронные орбитали. Тип гибридизации sp 3. 0 (т. к. Углы между электронными облаками различны). Молекула полярна.
 Взаимодействия между молекулами. Водородная связь – это особый вид взаимодействия между молекулами веществ. Водородная связь возникает между атомом водорода и другим более электроотрицательным атомом за счет сил электростатического притяжения по донорно-акцепторному механизму.
Взаимодействия между молекулами. Водородная связь – это особый вид взаимодействия между молекулами веществ. Водородная связь возникает между атомом водорода и другим более электроотрицательным атомом за счет сил электростатического притяжения по донорно-акцепторному механизму.
 Вандерваальсово взаимодействие (межмолекулярное взаимодействие) 1873 год голландский ученый И. Ван-дер-Ваальс, предположил, что существуют силы, обусловливвающие притяжение между молекулами. Типы взаимодействия: 1) диполь-дипольное (ориентационное) Взаимодействие полярных молекул. 2) Индукционное. Взаимодействие полярных и неполярных молекул. Энергия этого вида взаимодействия слабее, чем ориентационного. 3)Дисперсионное. В неполярных молекулах (инертные газы) возникают флуктуации электронной плотности, в результате возникают мгновенные диполи, которые могут индуцировать соседние молекулы.
Вандерваальсово взаимодействие (межмолекулярное взаимодействие) 1873 год голландский ученый И. Ван-дер-Ваальс, предположил, что существуют силы, обусловливвающие притяжение между молекулами. Типы взаимодействия: 1) диполь-дипольное (ориентационное) Взаимодействие полярных молекул. 2) Индукционное. Взаимодействие полярных и неполярных молекул. Энергия этого вида взаимодействия слабее, чем ориентационного. 3)Дисперсионное. В неполярных молекулах (инертные газы) возникают флуктуации электронной плотности, в результате возникают мгновенные диполи, которые могут индуцировать соседние молекулы.
 иллюстрация
иллюстрация
 Химическая связь и свойства веществ. Многие свойства веществ зависят и от типа связи между атомами в молекулах, так и от взаимодействий между молекулами. Например, чем более полярна связь между атомами в молекуле вещества, тем лучше они растворяются в полярном растворителе воде. Распад веществ на ионы (диссоциация) в водных растворах также зависит от полярности связи. Лучше всего растворяются и диссоциируют вещества с инным типом связи (высокой степенью ионности). Вещества с ионным типом связи имеют упорядоченную структуру и в твердом состоянии имеют высокие температуры плавления.
Химическая связь и свойства веществ. Многие свойства веществ зависят и от типа связи между атомами в молекулах, так и от взаимодействий между молекулами. Например, чем более полярна связь между атомами в молекуле вещества, тем лучше они растворяются в полярном растворителе воде. Распад веществ на ионы (диссоциация) в водных растворах также зависит от полярности связи. Лучше всего растворяются и диссоциируют вещества с инным типом связи (высокой степенью ионности). Вещества с ионным типом связи имеют упорядоченную структуру и в твердом состоянии имеют высокие температуры плавления.
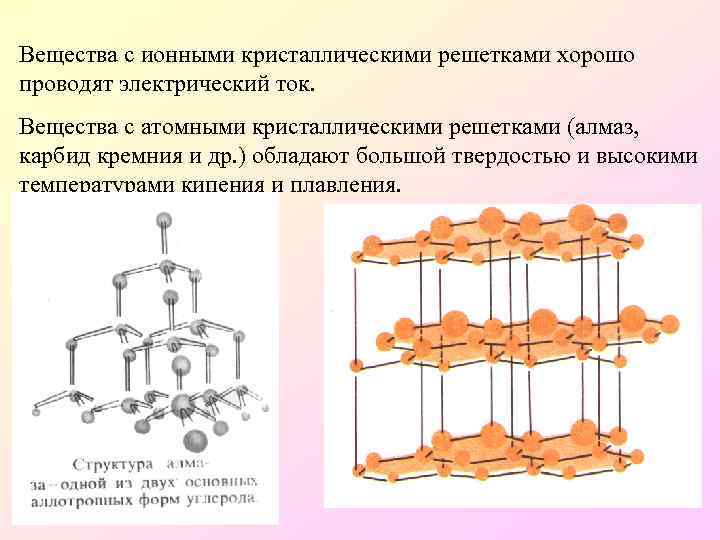 Вещества с ионными кристаллическими решетками хорошо проводят электрический ток. Вещества с атомными кристаллическими решетками (алмаз, карбид кремния и др. ) обладают большой твердостью и высокими температурами кипения и плавления.
Вещества с ионными кристаллическими решетками хорошо проводят электрический ток. Вещества с атомными кристаллическими решетками (алмаз, карбид кремния и др. ) обладают большой твердостью и высокими температурами кипения и плавления.
 Вещества с ковалентной связью, имеющие молекулярную структуру (твердые иод, нафталин; жидкие – бром, вода, этиловый спирт; газы – хлор, аммиак, метан) имеют низкие температуры кипения, плавления. Чем меньше молекулярная масса вещества тем оно легче кипит (летучие вещества). Жидкое или газообразное состояние вещества можно объяснить также силами межмолекулярного взаимодействия (вода и сероводород). Образование водородных связей повышают вязкость, температуры кипения и плавления, диэлектрическую постоянную, теплоты плавления и парообразования.
Вещества с ковалентной связью, имеющие молекулярную структуру (твердые иод, нафталин; жидкие – бром, вода, этиловый спирт; газы – хлор, аммиак, метан) имеют низкие температуры кипения, плавления. Чем меньше молекулярная масса вещества тем оно легче кипит (летучие вещества). Жидкое или газообразное состояние вещества можно объяснить также силами межмолекулярного взаимодействия (вода и сероводород). Образование водородных связей повышают вязкость, температуры кипения и плавления, диэлектрическую постоянную, теплоты плавления и парообразования.
 Проверочная работа 1. Запишите общую электронную формулу элементов подгруппы азота и подгруппы ванадия. 2. 2. Что общего у элементов V группы? 3. а) максимальная степень окисления +5 ; 4. б) число энергетических уровней – 5; 5. в) электронные семейства. 6. 3. Чем отличаются элементы VA и VB групп? 7. а) разные электронные семейства; б) разная максимальная степень окисления
Проверочная работа 1. Запишите общую электронную формулу элементов подгруппы азота и подгруппы ванадия. 2. 2. Что общего у элементов V группы? 3. а) максимальная степень окисления +5 ; 4. б) число энергетических уровней – 5; 5. в) электронные семейства. 6. 3. Чем отличаются элементы VA и VB групп? 7. а) разные электронные семейства; б) разная максимальная степень окисления


